Introduccin a la espectroscopa vibracional Espectro electromagntico Longitud

Introducción a la espectroscopía vibracional Espectro electromagnético Longitud de onda Tipo de radiación Tipos de transición 1020 - 1024 10 -12 - 10 -16 m Rayos gamma Nuclear 1017 - 1020 1 nm - 1 pm Rayos X Electrones internos 1015 - 1017 400 - 1 nm Ultravioleta Electrones externos 4. 3 x 1014 - 7. 5 x 1014 700 - 400 nm Visible Electrones externos 1012 -1014 2. 5 µm - 700 nm Infrarrojo Vibraciones 108 - 1012 1 mm - 2. 5 µm Microondas Rotaciones 100 - 108 - 1 m Radiofrecuencia Inversión de spin Frecuencia (Hz)
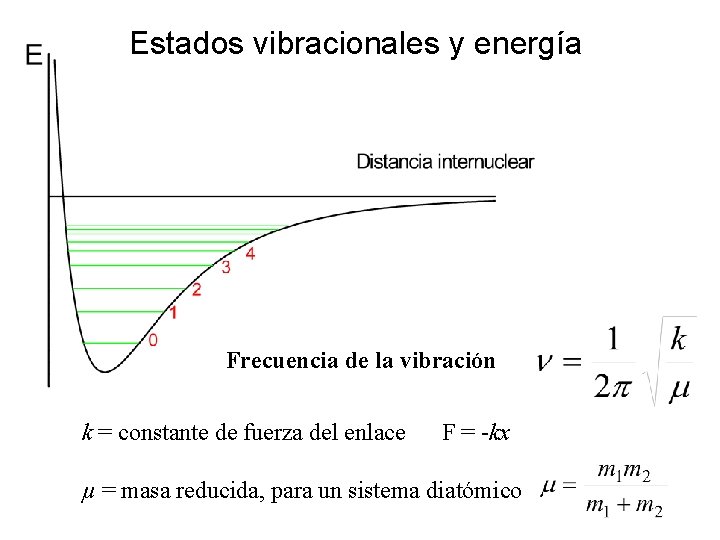
Estados vibracionales y energía Frecuencia de la vibración k = constante de fuerza del enlace F = -kx µ = masa reducida, para un sistema diatómico

Modos normales de vibración (3 N - 5) cm-1 IR RAMAN estiramiento (sim) O C O 1340 - + estiramiento (asim) O C O 2349 + - deformación O C O 667 + -

INFRARROJO Reglas de selección: No todas las vibraciones serán “activas” en IR Sólo aquellas en las que cambie el momento dipolar permanente durante la vibración
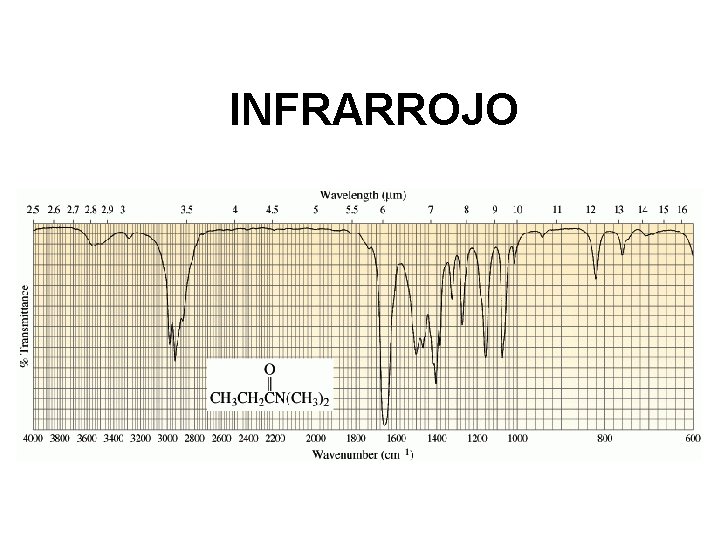
INFRARROJO
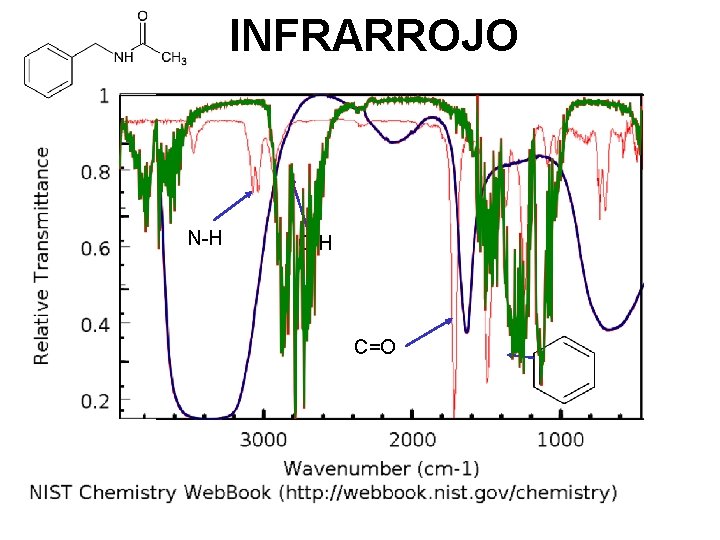
INFRARROJO N-H C=O
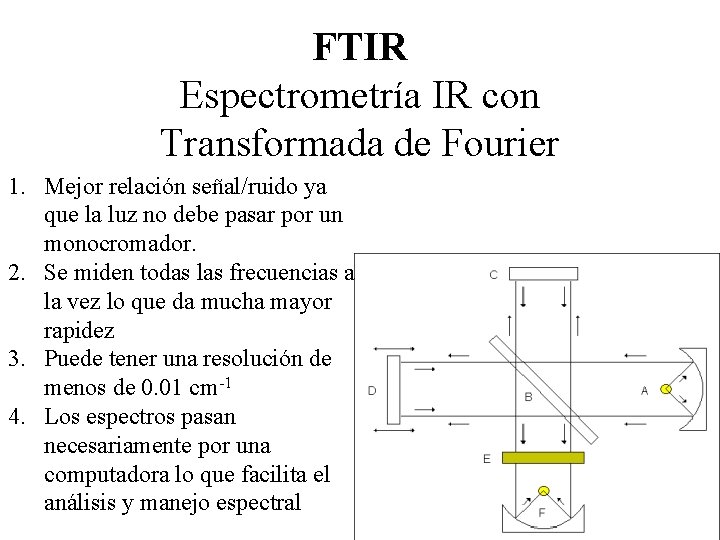
FTIR Espectrometría IR con Transformada de Fourier 1. Mejor relación señal/ruido ya que la luz no debe pasar por un monocromador. 2. Se miden todas las frecuencias a la vez lo que da mucha mayor rapidez 3. Puede tener una resolución de menos de 0. 01 cm-1 4. Los espectros pasan necesariamente por una computadora lo que facilita el análisis y manejo espectral
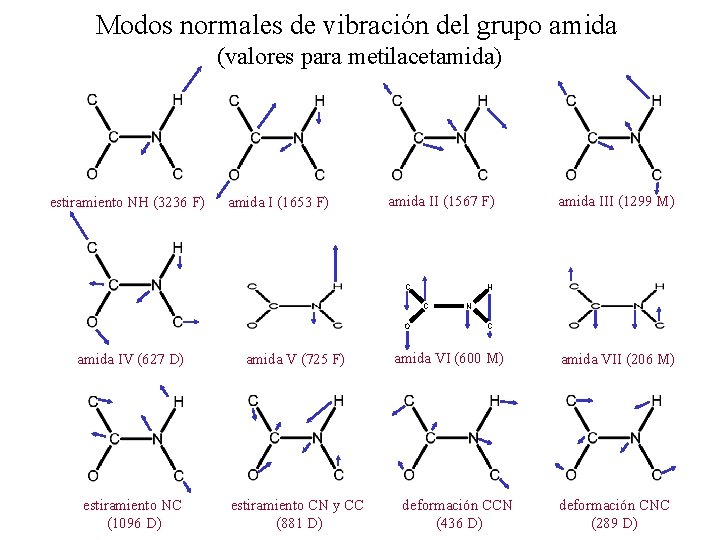
Modos normales de vibración del grupo amida (valores para metilacetamida) estiramiento NH (3236 F) amida I (1653 F) amida II (1567 F) C H C O amida IV (627 D) amida V (725 F) estiramiento NC (1096 D) estiramiento CN y CC (881 D) amida III (1299 M) N C amida VI (600 M) deformación CCN (436 D) amida VII (206 M) deformación CNC (289 D)
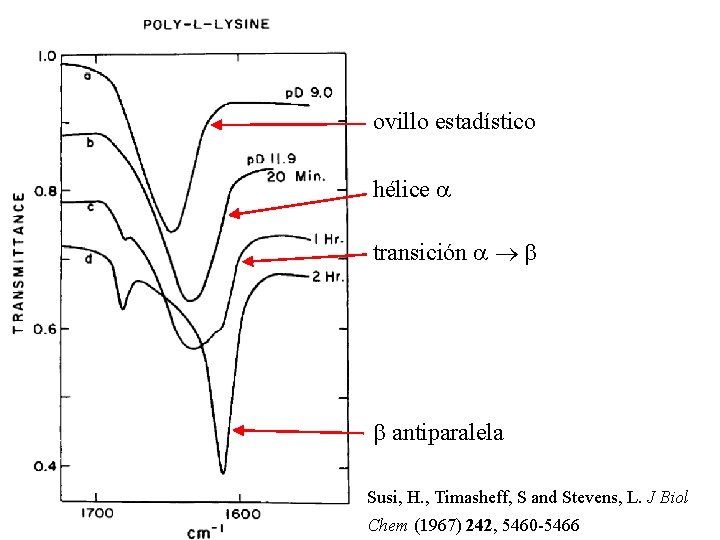
ovillo estadístico hélice a transición a b b antiparalela Susi, H. , Timasheff, S and Stevens, L. J Biol Chem (1967) 242, 5460 -5466
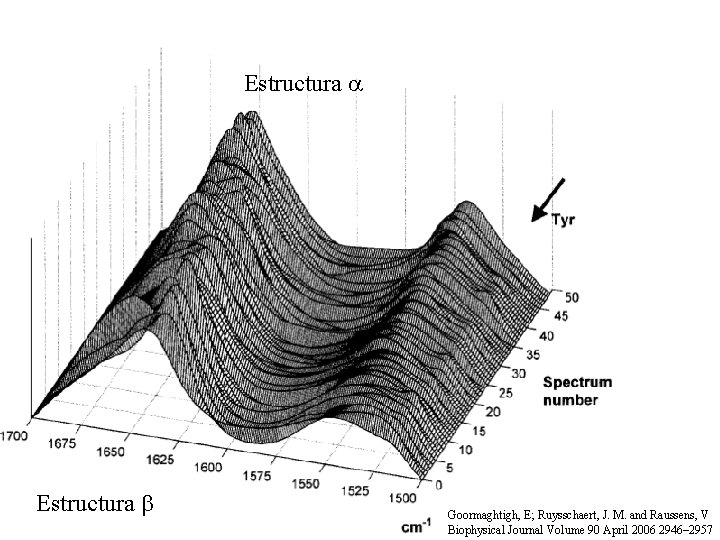
Estructura a Estructura b Goormaghtigh, E; Ruysschaert, J. M. and Raussens, V Biophysical Journal Volume 90 April 2006 2946– 2957
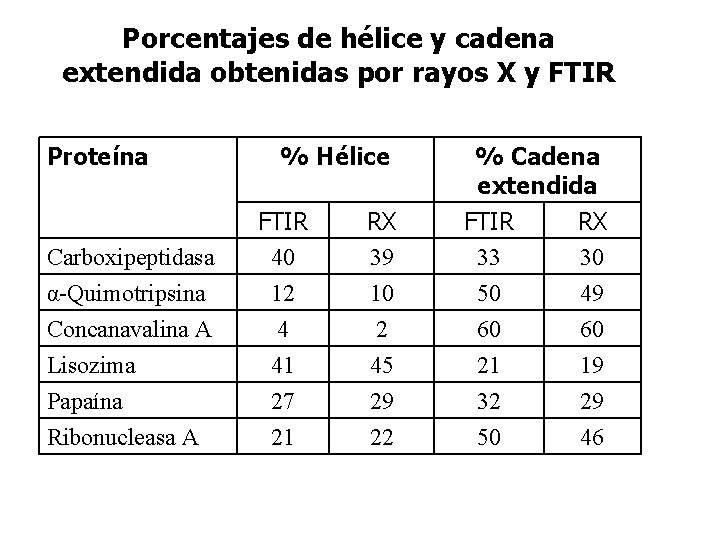
Porcentajes de hélice y cadena extendida obtenidas por rayos X y FTIR Proteína % Hélice % Cadena extendida Carboxipeptidasa FTIR 40 RX 39 FTIR 33 RX 30 α-Quimotripsina Concanavalina A Lisozima Papaína Ribonucleasa A 12 4 41 27 21 10 2 45 29 22 50 60 21 32 50 49 60 19 29 46
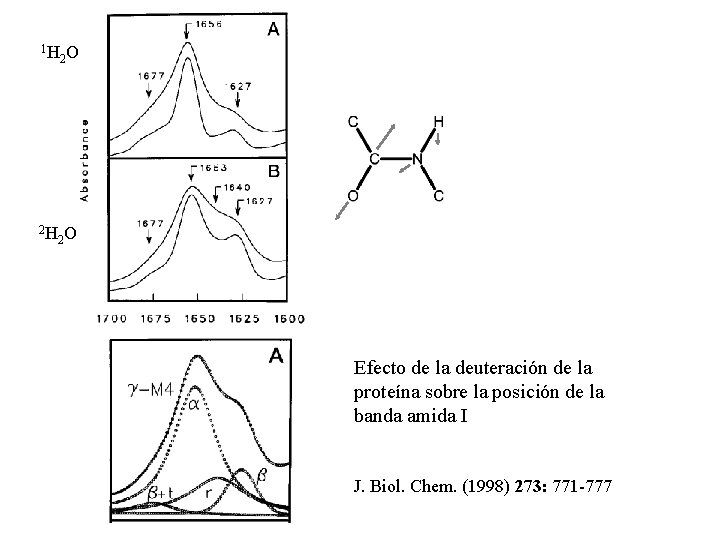
1 H 2 H 2 O 2 O Efecto de la deuteración de la proteína sobre la posición de la banda amida I J. Biol. Chem. (1998) 273: 771 -777

BIAP (A) Asignación tentativa de las diferentes bandas en el espectro FTIR de BIAP y apo. BIAP en 2 H O, p. H 6. 6 2 apo BIAP (B) Asignación tentativa 1682 n. C=O amida I (hoja b) 1660 n. C=O amida I (giro) 1651– 1652 n. C=O amida I (hélice a) 1633 n. C=O amida I (hoja b) 1586– 1577 1586– 1571 n. C=O COO– Asp o Glu 1547 d N-H amida II 1516– 1517 n OH anillo Tyr 1443 1455 d N-2 H amida II y 2 HOH
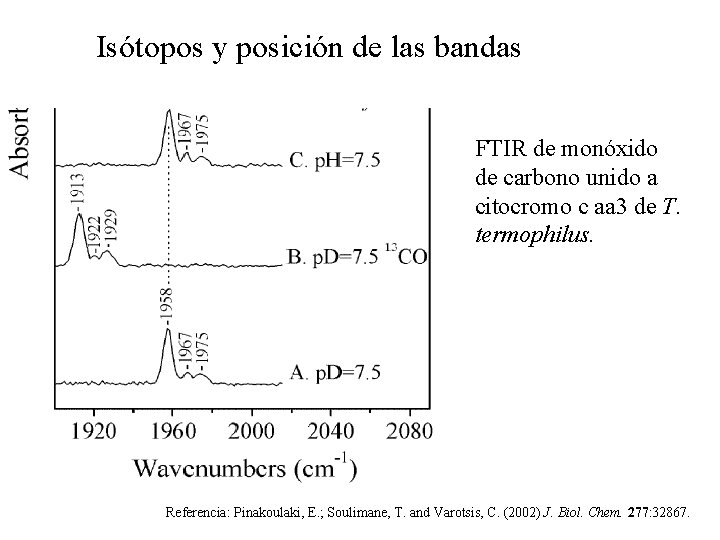
Isótopos y posición de las bandas FTIR de monóxido de carbono unido a citocromo c aa 3 de T. termophilus. Referencia: Pinakoulaki, E. ; Soulimane, T. and Varotsis, C. (2002) J. Biol. Chem. 277: 32867.

Efecto Raman Dispersión inelástica de fotones estados electrónicos virtuales Sir Chandrasekhara Venkata Raman, (������ Tiruchirapalli, Tamil Nadu -7/11/1888 Bangalore, Karnataka - 21/11/1970 Premio Nobel de Física 1930
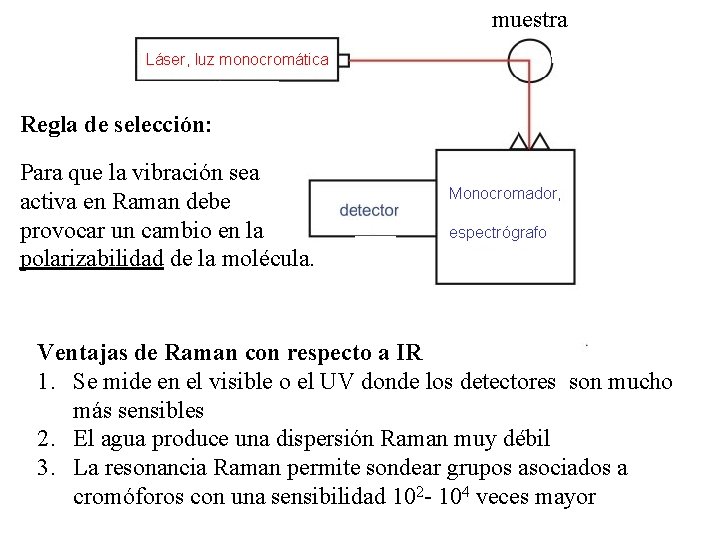
muestra Láser, luz monocromática Regla de selección: Para que la vibración sea activa en Raman debe provocar un cambio en la polarizabilidad de la molécula. Monocromador, espectrógrafo Ventajas de Raman con respecto a IR 1. Se mide en el visible o el UV donde los detectores son mucho más sensibles 2. El agua produce una dispersión Raman muy débil 3. La resonancia Raman permite sondear grupos asociados a cromóforos con una sensibilidad 102 - 104 veces mayor
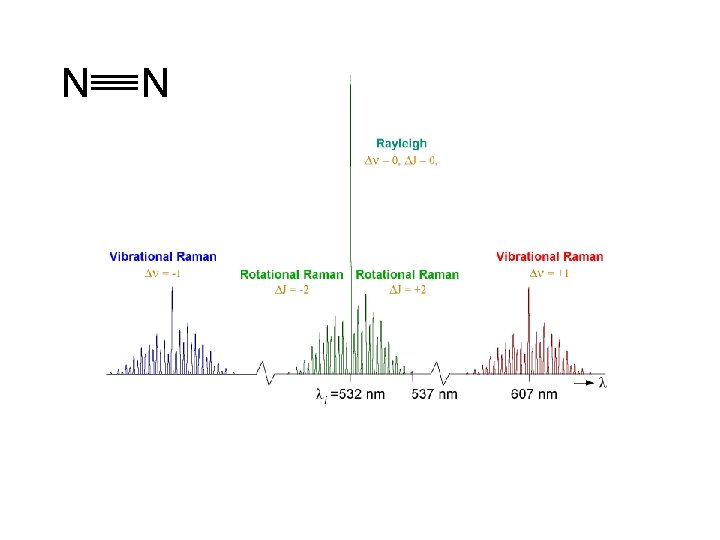
N N
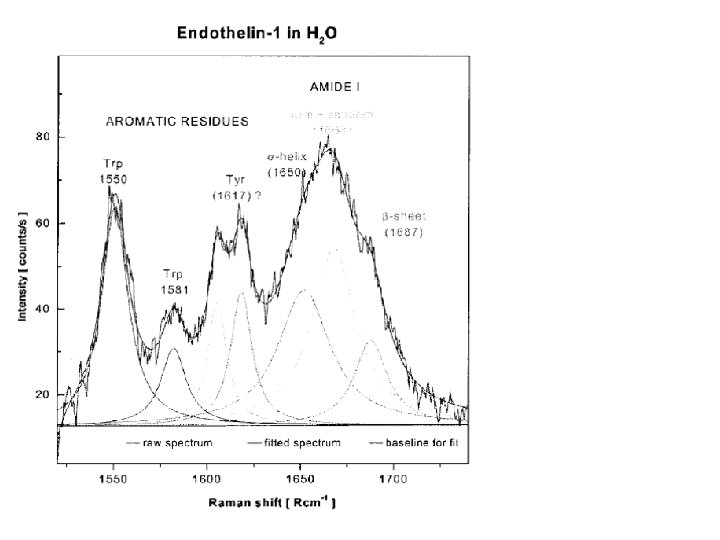
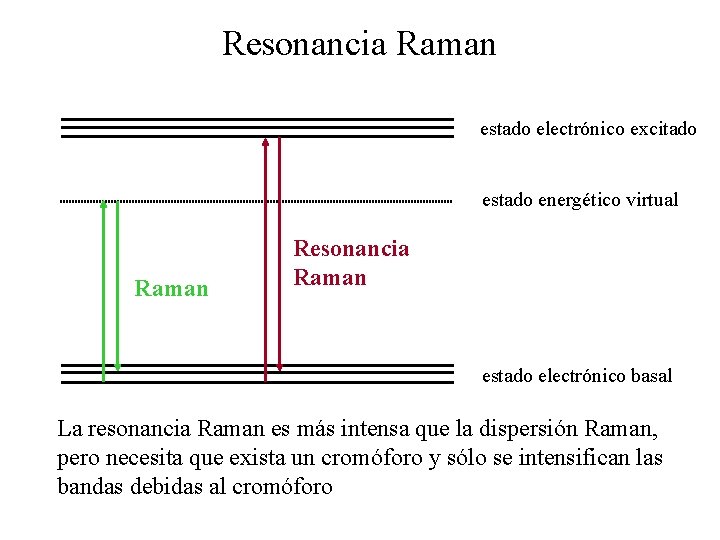
Resonancia Raman estado electrónico excitado estado energético virtual Raman Resonancia Raman estado electrónico basal La resonancia Raman es más intensa que la dispersión Raman, pero necesita que exista un cromóforo y sólo se intensifican las bandas debidas al cromóforo
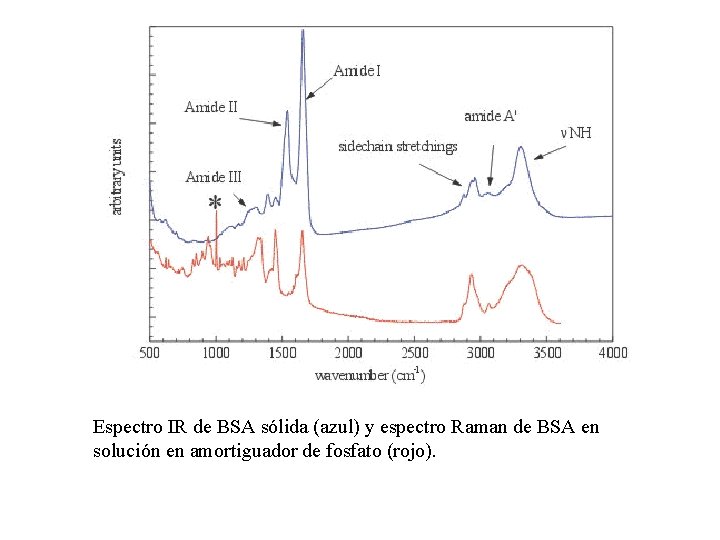
Espectro IR de BSA sólida (azul) y espectro Raman de BSA en solución en amortiguador de fosfato (rojo).
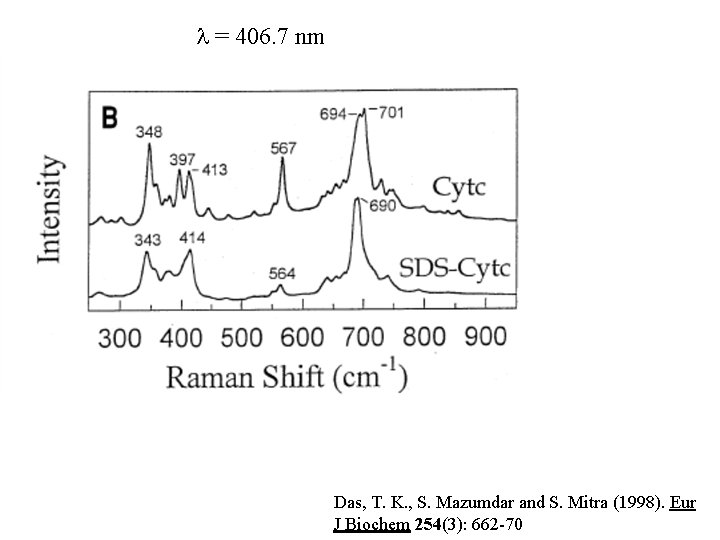
l = 406. 7 nm Das, T. K. , S. Mazumdar and S. Mitra (1998). Eur J Biochem 254(3): 662 -70
- Slides: 21