Intgrations des Inhibiteurs de cycline dpendantes kinases CDK

Intégrations des Inhibiteurs de cycline dépendantes kinases CDK 4/6 dans le traitement de m. BC ER+/HER 2 Pr TAHRI Ali Clinique spécialisée Menara Marrakech

Kinases Dépendantes de Cyclines • Début 1970: identification des gènes impliqués dans la division cellulaire et concept « checkpoint » (Lee Hartwell ) • Fin 1970/début 1980: identification des CDC 2 et rôle dans cycle cellulaire (Paul Nurse) • Début 1980 s: identification des cyclines et de leur variation pendant le cycle cellulaire (Tim Hunt) • 2001 Prix Nobel de Médecine (Hartwell, Nurse et Hunt) 2
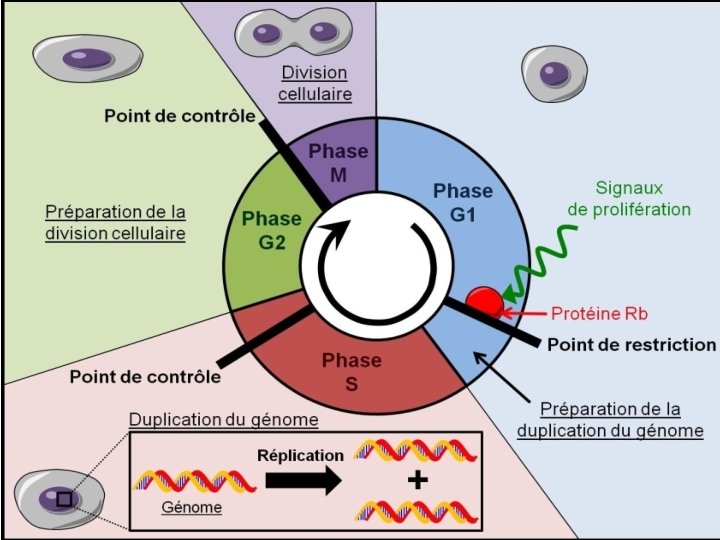

Kinases Dépendantes de Cyclines (CDKs) • Groupe de protéines kinases impliquées dans le contrôle du cycle cellulaire • Activité dépendante de leur association avec les cyclines • Activation de l’activité catalytique / Cyclines • CDK 4 et 6 sont associées à la cycline D • CDK 2 cyclines E et A 4
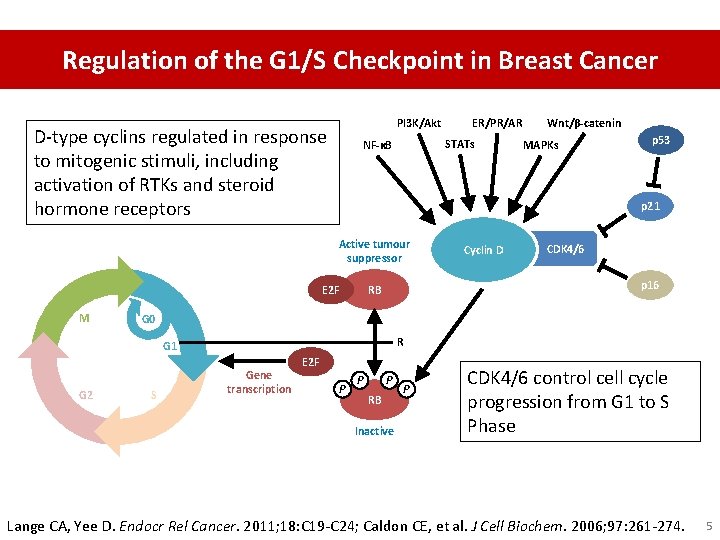
Regulation of the G 1/S Checkpoint in Breast Cancer Pl 3 K/Akt D-type cyclins regulated in response to mitogenic stimuli, including activation of RTKs and steroid hormone receptors STATs NF-κB MAPKs p 53 Cyclin D CDK 4/6 p 16 RB E 2 F G 0 R G 1 G 2 Wnt/β-catenin p 21 Active tumour suppressor M ER/PR/AR S Gene transcription E 2 F P P P RB Inactive P CDK 4/6 control cell cycle progression from G 1 to S Phase Lange CA, Yee D. Endocr Rel Cancer. 2011; 18: C 19 -C 24; Caldon CE, et al. J Cell Biochem. 2006; 97: 261 -274. 5

La voie Cyclin. D-CDK 4/6 -Rb régule la progression du cycle cellulaire et présente fréquemment des anomalies dans les cancers • Une activité augmentée du complexe cycline D-CDK 4/6 survient dans les cancers – – Surexpression/amplification de la cycline D Mutations et amplifications de CDK 4/6 Perte des inhibiteurs de CDK 4/6: p 16 (INK 4 A/CDKN 2 A), KIP Protéine/gène RB est fréquemment maintenue dans les RH+ • Association avec la résistance à l’hormonothérapie dans les cancers luminaux Buckley MF, et al. Oncogene. 1993; 8: 2127 -2133; Dickson C, et al. Cancer Lett. 1995; 90: 43 -50. 6

La voie Cyclin. D-CDK 4/6 -Rb régule la progression du cycle cellulaire et présente fréquemment des anomalies dans les cancers • Une activité augmentée du complexe cycline D-CDK 4/6 survient dans les cancers – – Surexpression/amplification de la cycline D Mutations et amplifications de CDK 4/6 Perte des inhibiteurs de CDK 4/6: p 16 (INK 4 A/CDKN 2 A), KIP Protéine/gène RB est fréquemment maintenue dans les RH+ • Association avec la résistance à l’hormonothérapie dans les cancers luminaux CDK 4/6 représentent une cible dans les cancers du sein luminaux Buckley MF, et al. Oncogene. 1993; 8: 2127 -2133; Dickson C, et al. Cancer Lett. 1995; 90: 43 -50. 7
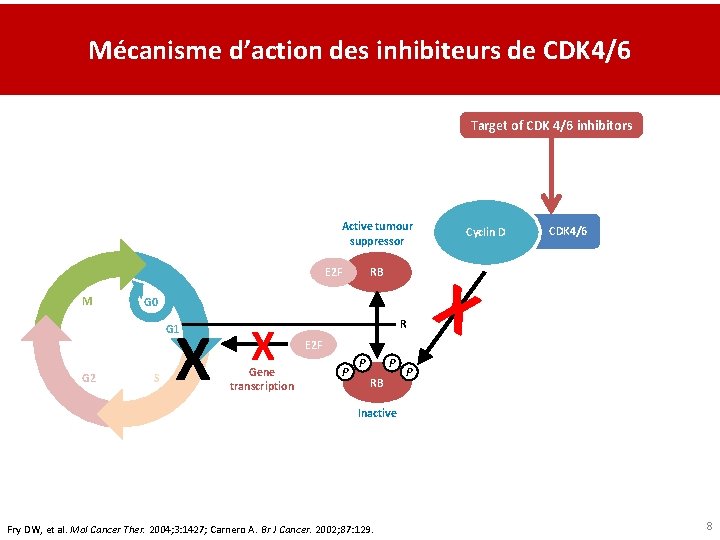
Mécanisme d’action des inhibiteurs de CDK 4/6 Target of CDK 4/6 inhibitors Active tumour suppressor E 2 F M G 0 X G 1 G 2 RB S X Gene transcription R Cyclin D CDK 4/6 X E 2 F P P P RB P Inactive Fry DW, et al. Mol Cancer Ther. 2004; 3: 1427; Carnero A. Br J Cancer. 2002; 87: 129. 8

Palbociclib (PD 0332991) • Inhibiteur oral, hautement sélectif de CDK 4/6 • Bloque la progression du cycle cellulaire de la phase G 1 à la phase S • Activité in vitro dans les lignées cellulaires et tumeurs Rb+ • Faibles concentrations nanomolaires bloquent la phosphorylation Rb, induisant un arrêt en phase G 1 PD-0332991 CDK (cyclin partner) CDK 4 (cyclin D 1) CDK 4 (cyclin D 3) CDK 6 (cyclin D 2) CDK 2 (cyclin A) CDK 1 (cyclin B) CDK 5 (p 25) IC 50 (µM) 0. 011 0. 009 0. 015 >5 >5 >5 . Fry DW, et al. Mol Cancer Ther. 2004; 3: 1427 -1438; Menu E, et al. Cancer Res. 2008; 68: 5519 -5523; Sutherland RL, Musgrove EA. Breast Cancer Res. 2009; 11: 112. 9
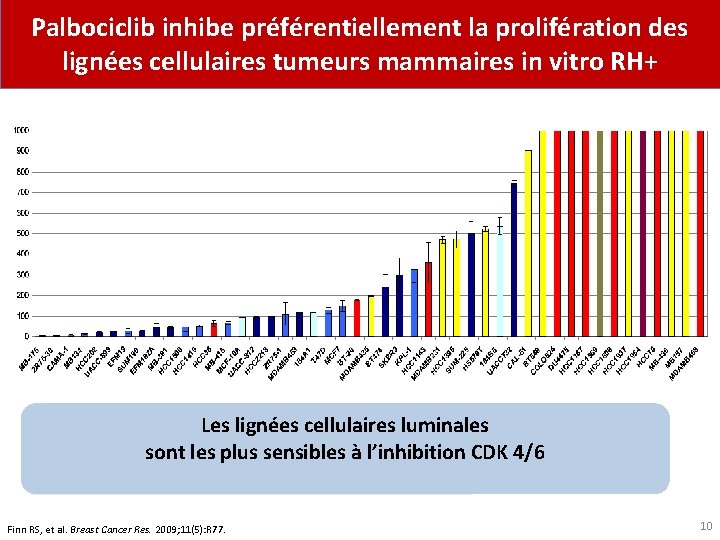
IC 50 n. M Palbociclib inhibe préférentiellement la prolifération des lignées cellulaires tumeurs mammaires in vitro RH+ Les lignées cellulaires luminales sont les plus sensibles à l’inhibition CDK 4/6 Finn RS, et al. Breast Cancer Res. 2009; 11(5): R 77. 10
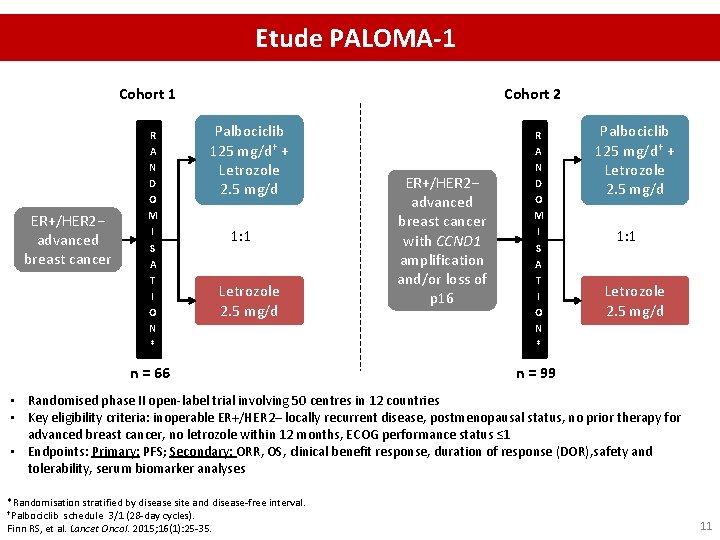
Etude PALOMA-1 Cohort 1 ER+/HER 2− advanced breast cancer R A N D O M I S A T I O N * Cohort 2 Palbociclib 125 mg/d† + Letrozole 2. 5 mg/d 1: 1 Letrozole 2. 5 mg/d n = 66 ER+/HER 2− advanced breast cancer with CCND 1 amplification and/or loss of p 16 R A N D O M I S A T I O N * Palbociclib 125 mg/d† + Letrozole 2. 5 mg/d 1: 1 Letrozole 2. 5 mg/d n = 99 • Randomised phase II open-label trial involving 50 centres in 12 countries • Key eligibility criteria: inoperable ER+/HER 2– locally recurrent disease, postmenopausal status, no prior therapy for advanced breast cancer, no letrozole within 12 months, ECOG performance status ≤ 1 • Endpoints: Primary: PFS; Secondary: ORR, OS, clinical benefit response, duration of response (DOR), safety and tolerability, serum biomarker analyses *Randomisation stratified by disease site and disease-free interval. †Palbociclib schedule 3/1 (28 -day cycles). Finn RS, et al. Lancet Oncol. 2015; 16(1): 25 -35. 11
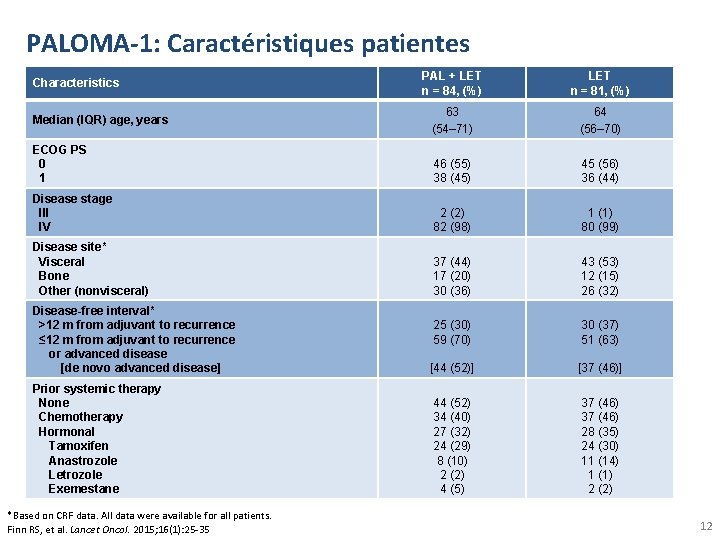
PALOMA-1: Caractéristiques patientes PAL + LET n = 84, (%) LET n = 81, (%) 63 (54– 71) 64 (56– 70) ECOG PS 0 1 46 (55) 38 (45) 45 (56) 36 (44) Disease stage III IV 2 (2) 82 (98) 1 (1) 80 (99) Disease site* Visceral Bone Other (nonvisceral) 37 (44) 17 (20) 30 (36) 43 (53) 12 (15) 26 (32) Characteristics Median (IQR) age, years Disease-free interval* >12 m from adjuvant to recurrence ≤ 12 m from adjuvant to recurrence or advanced disease [de novo advanced disease] 25 (30) 59 (70) 30 (37) 51 (63) [44 (52)] [37 (46)] Prior systemic therapy None Chemotherapy Hormonal Tamoxifen Anastrozole Letrozole Exemestane 44 (52) 34 (40) 27 (32) 24 (29) 8 (10) 2 (2) 4 (5) 37 (46) 28 (35) 24 (30) 11 (14) 1 (1) 2 (2) *Based on CRF data. All data were available for all patients. Finn RS, et al. Lancet Oncol. 2015; 16(1): 25 -35 12
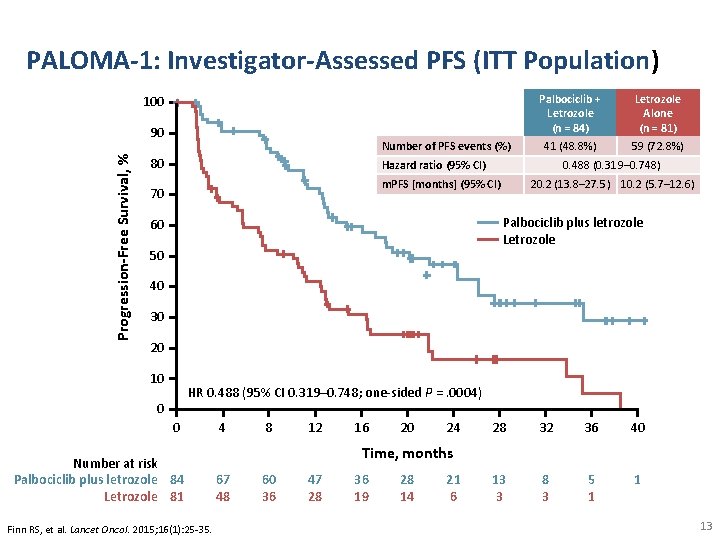
PALOMA-1: Investigator-Assessed PFS (ITT Population) 100 Progression-Free Survival, % 90 Number of PFS events (%) 80 Palbociclib + Letrozole (n = 84) Letrozole Alone (n = 81) 41 (48. 8%) 59 (72. 8%) Hazard ratio (95% CI) 0. 488 (0. 319– 0. 748) m. PFS [months] (95% CI) 70 20. 2 (13. 8– 27. 5) 10. 2 (5. 7– 12. 6) Palbociclib plus letrozole Letrozole 60 50 40 30 20 10 HR 0. 488 (95% CI 0. 319– 0. 748; one-sided P =. 0004) 0 0 Number at risk Palbociclib plus letrozole 84 Letrozole 81 Finn RS, et al. Lancet Oncol. 2015; 16(1): 25 -35. 4 8 12 16 20 24 28 32 36 40 13 3 8 3 5 1 1 Time, months 67 48 60 36 47 28 36 19 28 14 21 6 13

PALOMA-1: Forest Plot for PFS PAL + LET Patients Events 41 All patients (intention-to-treat population) 84 Cohort 1 34 15 26 2 50 Age group (years) <65 years 47 24 17 ≥ 65 years 37 Baseline ECOG performance status 0 46 21 20 1 38 Disease site 21 Visceral 37 5 Bone Only 17 30 15 Other Previous chemotherapy 34 17 Yes No 50 24 Previous antihormonal therapy 27 12 Yes No 57 29 Previous systemic therapy 40 20 Yes No 44 21 Time from end of adjuvant treatment to disease recurrence 59 31 ≤ 12 months (including de-novo presentation) 10 >12 months 25 7 ≤ 12 months (excluding de-novo presentation) 15 LET Hazard ratio (95% CI) Patients Events 81 59 0. 488 (0. 319– 0. 748) 32 49 25 34 0. 299 (0. 156– 0. 572) 0. 508 (0. 303– 0. 853) 0. 14 42 39 35 24 0. 315 (0. 184– 0. 539) 0. 505 (0. 269– 0. 948) 0. 34 45 36 31 28 0. 434 (0. 246– 0. 766) 0. 398 (0. 220– 0. 721) 0. 78 43 12 26 34 7 18 0. 547 (0. 317– 0. 944) 0. 294 (0. 092– 0. 945) 0. 402 (0. 200– 0. 808) 0. 44 37 44 24 35 0. 479 (0. 255– 0. 898) 0. 397 (0. 234– 0. 671) 0. 75 28 53 19 40 0. 460 (0. 222– 0. 956) 0. 397 (0. 244– 0. 646) 0. 88 44 37 28 31 0. 539 (0. 302– 0. 962) 0. 341 (0. 194– 0. 599) 0. 36 51 30 14 39 20 5 0. 418 (0. 259– 0. 674) 0. 399 (0. 185– 0. 858) 0. 765 (0. 232– 2. 523) 0. 95 0. 34 0. 062 0. 125 0. 250 0. 500 Favours palbociclib plus letrozole *Two-sided P value. Finn RS, et al. Lancet Oncol. 2015; 16(1): 25 -35. Interaction P value* 1. 000 2. 000 4. 000 Favours letrozole 14
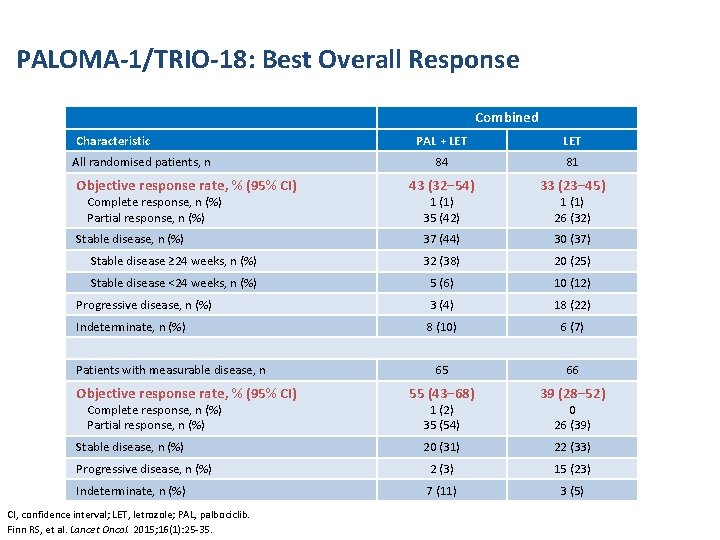
PALOMA-1/TRIO-18: Best Overall Response Combined PAL + LET 84 81 43 (32− 54) 33 (23− 45) 37 (44) 30 (37) Stable disease ≥ 24 weeks, n (%) 32 (38) 20 (25) Stable disease <24 weeks, n (%) 5 (6) 10 (12) Progressive disease, n (%) 3 (4) 18 (22) Indeterminate, n (%) 8 (10) 6 (7) 65 66 55 (43− 68) 39 (28− 52) 20 (31) 22 (33) Progressive disease, n (%) 2 (3) 15 (23) Indeterminate, n (%) 7 (11) 3 (5) Characteristic All randomised patients, n Objective response rate, % (95% CI) Complete response, n (%) Partial response, n (%) Stable disease, n (%) Patients with measurable disease, n Objective response rate, % (95% CI) Complete response, n (%) Partial response, n (%) Stable disease, n (%) CI, confidence interval; LET, letrozole; PAL, palbociclib. Finn RS, et al. Lancet Oncol. 2015; 16(1): 25 -35. 1 (1) 35 (42) 1 (2) 35 (54) 1 (1) 26 (32) 0 26 (39)
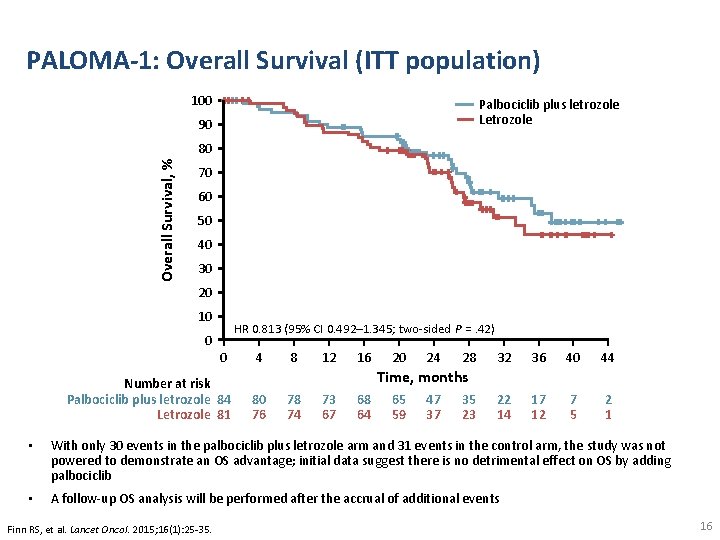
PALOMA-1: Overall Survival (ITT population) 100 Palbociclib plus letrozole Letrozole 90 Overall Survival, % 80 70 60 50 40 30 20 10 0 HR 0. 813 (95% CI 0. 492– 1. 345; two-sided P =. 42) 0 Number at risk Palbociclib plus letrozole 84 Letrozole 81 4 8 12 16 20 24 28 32 36 40 44 22 14 17 12 7 5 2 1 Time, months 80 76 78 74 73 67 68 64 65 59 47 37 35 23 • With only 30 events in the palbociclib plus letrozole arm and 31 events in the control arm, the study was not powered to demonstrate an OS advantage; initial data suggest there is no detrimental effect on OS by adding palbociclib • A follow-up OS analysis will be performed after the accrual of additional events Finn RS, et al. Lancet Oncol. 2015; 16(1): 25 -35. 16
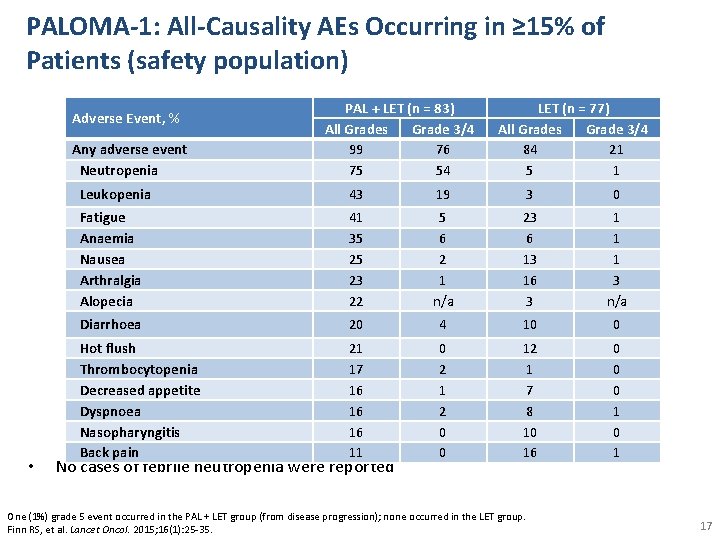
PALOMA-1: All-Causality AEs Occurring in ≥ 15% of Patients (safety population) Adverse Event, % Any adverse event Neutropenia • PAL + LET (n = 83) All Grades Grade 3/4 99 76 75 54 LET (n = 77) All Grades Grade 3/4 84 21 5 1 Leukopenia 43 19 3 0 Fatigue Anaemia Nausea Arthralgia Alopecia 41 35 25 23 22 5 6 2 1 n/a 23 6 13 16 3 1 1 1 3 n/a Diarrhoea 20 4 10 0 Hot flush Thrombocytopenia Decreased appetite Dyspnoea Nasopharyngitis Back pain 21 17 16 16 16 11 0 2 1 2 0 0 12 1 7 8 10 16 0 0 0 1 No cases of febrile neutropenia were reported One (1%) grade 5 event occurred in the PAL + LET group (from disease progression); none occurred in the LET group. Finn RS, et al. Lancet Oncol. 2015; 16(1): 25 -35. 17
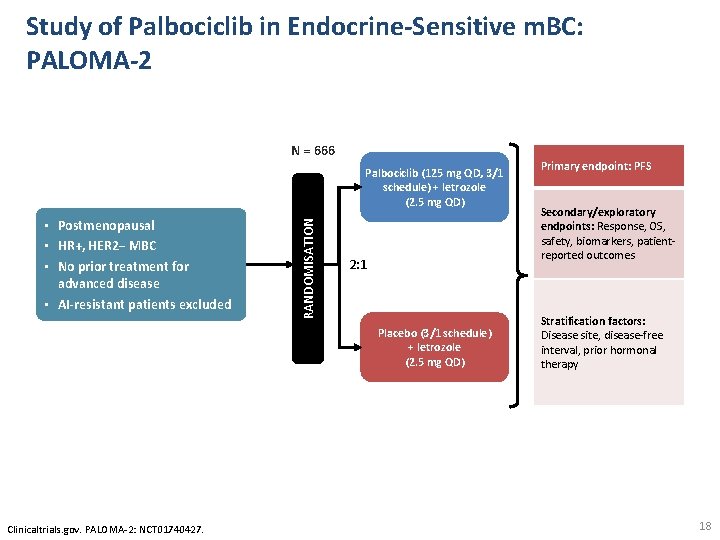
Study of Palbociclib in Endocrine-Sensitive m. BC: PALOMA-2 N = 666 • Postmenopausal • HR+, HER 2− MBC • No prior treatment for advanced disease • AI-resistant patients excluded RANDOMISATION Palbociclib (125 mg QD, 3/1 schedule) + letrozole (2. 5 mg QD) 2: 1 Placebo (3/1 schedule) + letrozole (2. 5 mg QD) Clinicaltrials. gov. PALOMA-2: NCT 01740427. Primary endpoint: PFS Secondary/exploratory endpoints: Response, OS, safety, biomarkers, patientreported outcomes Stratification factors: Disease site, disease-free interval, prior hormonal therapy 18
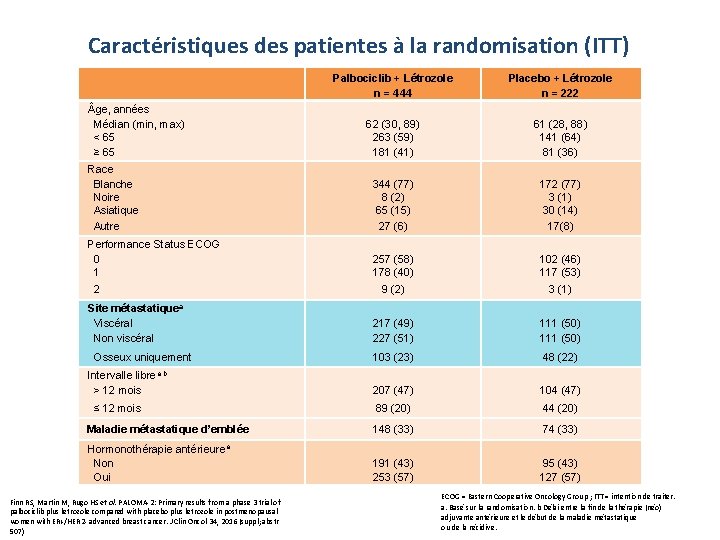
Caractéristiques des patientes à la randomisation (ITT) Palbociclib + Létrozole n = 444 Placebo + Létrozole n = 222 62 (30, 89) 263 (59) 181 (41) 61 (28, 88) 141 (64) 81 (36) Race Blanche Noire Asiatique Autre 344 (77) 8 (2) 65 (15) 27 (6) 172 (77) 3 (1) 30 (14) 17(8) Performance Status ECOG 0 1 257 (58) 178 (40) 102 (46) 117 (53) 9 (2) 3 (1) 217 (49) 227 (51) 111 (50) 103 (23) 48 (22) 207 (47) 104 (47) 89 (20) 44 (20) Maladie métastatique d’emblée 148 (33) 74 (33) Hormonothérapie antérieurea Non Oui 191 (43) 253 (57) 95 (43) 127 (57) ge, années Médian (min, max) < 65 ≥ 65 2 Site métastatiquea Viscéral Non viscéral Osseux uniquement Intervalle librea, b > 12 mois ≤ 12 mois Finn RS, Martin M, Rugo HS et al. PALOMA-2: Primary results from a phase 3 trial of palbociclib plus letrozole compared with placebo plus letrozole in postmenopausal women with ER+/HER 2 - advanced breast cancer. J Clin Oncol 34, 2016 (suppl; abstr 507) PFIZER CONFIDENTIAL ECOG = Eastern Cooperative Oncology Group ; ITT = intention de traiter. a. Basé sur la randomisation. b Délai entre la fin de la thérapie (néo) adjuvante antérieure et le début de la maladie métastatique ou de la récidive.
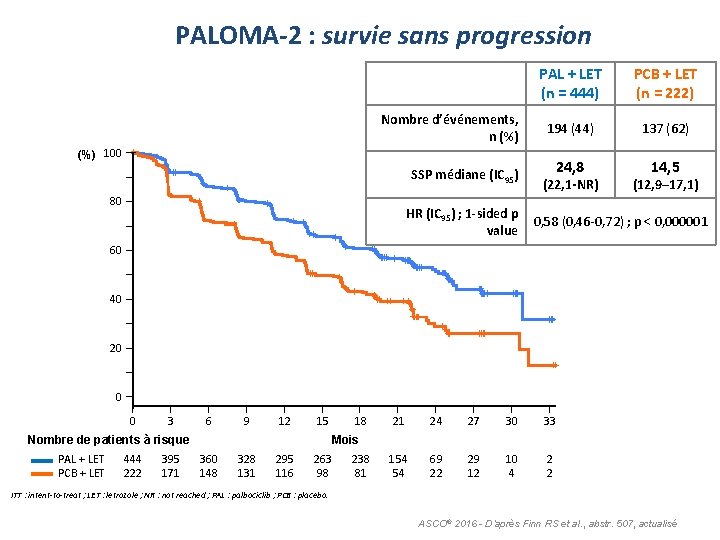
PALOMA-2 : survie sans progression Nombre d’événements, n (%) PAL + LET (n = 444) PCB + LET (n = 222) 194 (44) 137 (62) 24, 8 14, 5 (%) 100 SSP médiane (IC 95) 80 HR (IC 95) ; 1 -sided p value 20 (22, 1 -NR) (12, 9– 17, 1) 0, 58 (0, 46 -0, 72) ; p < 0, 000001 60 40 20 0 0 3 6 9 12 15 Nombre de patients à risque PAL + LET PCB + LET 444 222 395 171 18 21 24 27 30 33 154 54 69 22 29 12 10 4 2 2 Mois 360 148 328 131 295 116 263 98 238 81 ITT : intent-to-treat ; LET : letrozole ; NR : not reached ; PAL : palbociclib ; PCB : placebo. ASCO® 2016 - D’après Finn RS et al. , abstr. 507, actualisé
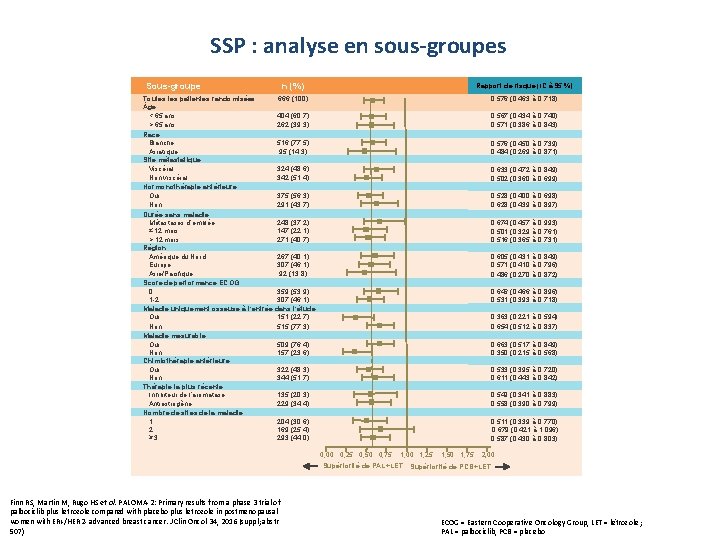
SSP : analyse en sous-groupes Sous-groupe n (%) Rapport de risque (IC à 95 %) 0, 576 (0, 463 à 0, 718) Toutes les patientes randomisées 666 (100) ge < 65 ans 404 (60, 7) > 65 ans 262 (39, 3) Race Blanche 516 (77, 5) Asiatique 95 (14, 3) Site métastatique Viscéral 324 (48, 6) Non viscéral 342 (51, 4) Hormonothérapie antérieure Oui 375 (56, 3) Non 291 (43, 7) Durée sans maladie Métastases d’emblée 248 (37, 2) ≤ 12 mois 147 (22, 1) > 12 mois 271 (40, 7) Région Amérique du Nord 267 (40, 1) Europe 307 (46, 1) Asie/Pacifique 92 (13, 8) Score de performance ECOG 0 359 (53, 9) 1 -2 307 (46, 1) Maladie uniquement osseuse à l’entrée dans l’étude Oui 151 (22, 7) Non 515 (77, 3) Maladie mesurable Oui 509 (76, 4) Non 157 (23, 6) Chimiothérapie antérieure Oui 322 (48, 3) Non 344 (51, 7) Thérapie la plus récente Inhibiteur de l’aromatase 135 (20, 3) Antiestrogène 229 (34, 4) Nombre de sites de la maladie 1 204 (30, 6) 2 169 (25, 4) ≥ 3 293 (44, 0) 0, 567 (0, 434 à 0, 740) 0, 571 (0, 386 à 0, 843) 0, 576 (0, 450 à 0, 739) 0, 484 (0, 269 à 0, 871) 0, 633 (0, 472 à 0, 849) 0, 502 (0, 360 à 0, 699) 0, 528 (0, 400 à 0, 698) 0, 628 (0, 439 à 0, 897) 0, 674 (0, 457 à 0, 993) 0, 501 (0, 329 à 0, 761) 0, 516 (0, 365 à 0, 731) 0, 605 (0, 431 à 0, 849) 0, 571 (0, 410 à 0, 796) 0, 486 (0, 270 à 0, 872) 0, 646 (0, 466 à 0, 896) 0, 531 (0, 393 à 0, 718) 0, 363 (0, 221 à 0, 594) 0, 654 (0, 512 à 0, 837) 0, 663 (0, 517 à 0, 849) 0, 350 (0, 215 à 0, 568) 0, 533 (0, 395 à 0, 720) 0, 611 (0, 443 à 0, 842) 0, 549 (0, 341 à 0, 883) 0, 558 (0, 390 à 0, 799) 0, 511 (0, 339 à 0, 770) 0, 679 (0, 421 à 1, 096) 0, 587 (0, 430 à 0, 803) 0, 00 0, 25 0, 50 0, 75 1, 00 1, 25 Supériorité de PAL+LET Finn RS, Martin M, Rugo HS et al. PALOMA-2: Primary results from a phase 3 trial of palbociclib plus letrozole compared with placebo plus letrozole in postmenopausal women with ER+/HER 2 - advanced breast cancer. J Clin Oncol 34, 2016 (suppl; abstr 507) 1, 50 1, 75 2, 00 Supériorité de PCB+LET PFIZER CONFIDENTIAL ECOG = Eastern Cooperative Oncology Group, LET = létrozole ; PAL = palbociclib, PCB = placebo
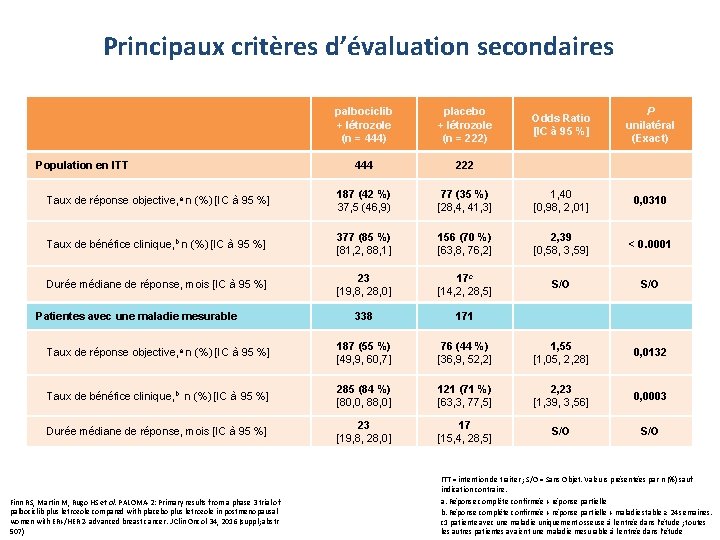
Principaux critères d’évaluation secondaires palbociclib + létrozole (n = 444) placebo + létrozole (n = 222) Odds Ratio [IC à 95 %] P unilatéral (Exact) 444 222 Taux de réponse objective, a n (%) [IC à 95 %] 187 (42 %) 37, 5 (46, 9) 77 (35 %) [28, 4, 41, 3] 1, 40 [0, 98, 2, 01] 0, 0310 Taux de bénéfice clinique, b n (%) [IC à 95 %] 377 (85 %) [81, 2, 88, 1] 156 (70 %) [63, 8, 76, 2] 2, 39 [0, 58, 3, 59] < 0. 0001 Durée médiane de réponse, mois [IC à 95 %] 23 [19, 8, 28, 0] 17 c [14, 2, 28, 5] S/O 338 171 Taux de réponse objective, a n (%) [IC à 95 %] 187 (55 %) [49, 9, 60, 7] 76 (44 %) [36, 9, 52, 2] 1, 55 [1, 05, 2, 28] 0, 0132 Taux de bénéfice clinique, b n (%) [IC à 95 %] 285 (84 %) [80, 0, 88, 0] 121 (71 %) [63, 3, 77, 5] 2, 23 [1, 39, 3, 56] 0, 0003 Durée médiane de réponse, mois [IC à 95 %] 23 [19, 8, 28, 0] 17 [15, 4, 28, 5] S/O Population en ITT Patientes avec une maladie mesurable Finn RS, Martin M, Rugo HS et al. PALOMA-2: Primary results from a phase 3 trial of palbociclib plus letrozole compared with placebo plus letrozole in postmenopausal women with ER+/HER 2 - advanced breast cancer. J Clin Oncol 34, 2016 (suppl; abstr 507) PFIZER CONFIDENTIAL ITT = intention de traiter ; S/O = Sans Objet. Valeurs présentées par n (%) sauf indication contraire. a. Réponse complète confirmée + réponse partielle b. Réponse complète confirmée + réponse partielle + maladie stable ≥ 24 semaines. c 1 patiente avec une maladie uniquement osseuse à l’entrée dans l’étude ; toutes les autres patientes avaient une maladie mesurable à l’entrée dans l’étude
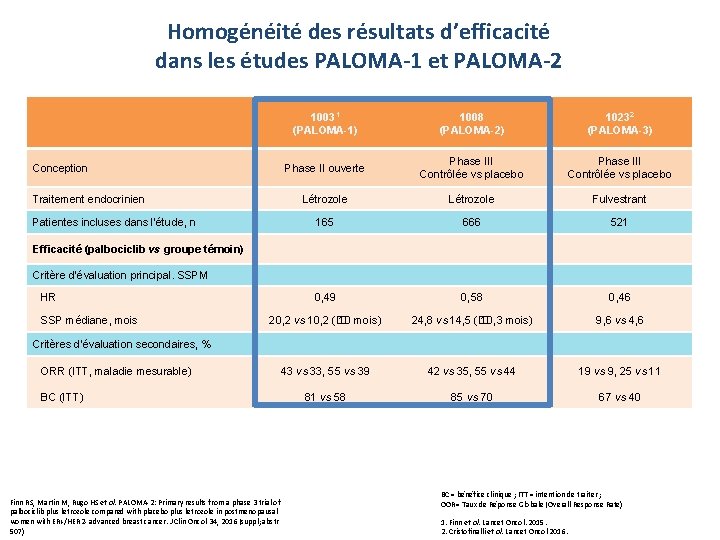
Homogénéité des résultats d’efficacité dans les études PALOMA-1 et PALOMA-2 10031 (PALOMA-1) 1008 (PALOMA-2) 10232 (PALOMA-3) Phase II ouverte Phase III Contrôlée vs placebo Létrozole Fulvestrant 165 666 521 0, 49 0, 58 0, 46 20, 2 vs 10, 2 (� 10 mois) 24, 8 vs 14, 5 (� 10, 3 mois) 9, 6 vs 4, 6 43 vs 33, 55 vs 39 42 vs 35, 55 vs 44 19 vs 9, 25 vs 11 81 vs 58 85 vs 70 67 vs 40 Conception Traitement endocrinien Patientes incluses dans l’étude, n Efficacité (palbociclib vs groupe témoin) Critère d’évaluation principal. SSPM HR SSP médiane, mois Critères d’évaluation secondaires, % ORR (ITT, maladie mesurable) BC (ITT) Finn RS, Martin M, Rugo HS et al. PALOMA-2: Primary results from a phase 3 trial of palbociclib plus letrozole compared with placebo plus letrozole in postmenopausal women with ER+/HER 2 - advanced breast cancer. J Clin Oncol 34, 2016 (suppl; abstr 507) BC = bénéfice clinique ; ITT = intention de traiter ; OOR= Taux de Réponse Globale (Overall Response Rate) PFIZER CONFIDENTIAL 1. Finn et al. Lancet Oncol. 2015. 2. Cristofinalli et al. Lancet Oncol 2016.
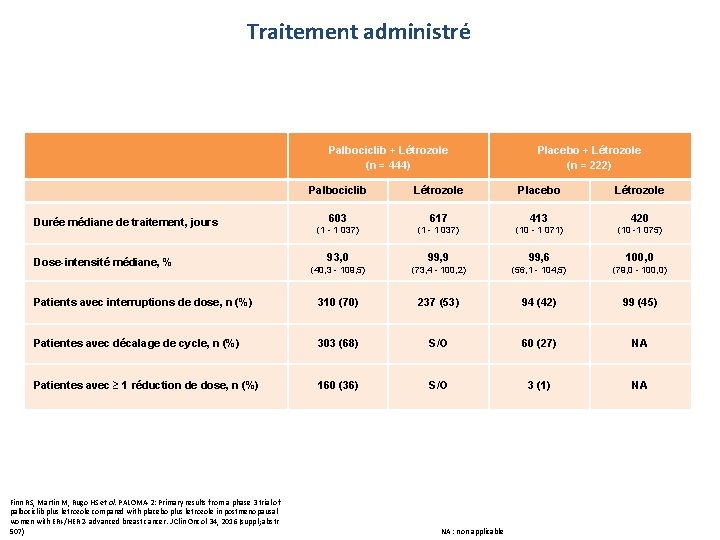
Traitement administré Palbociclib + Létrozole (n = 444) Palbociclib Durée médiane de traitement, jours Létrozole Placebo + Létrozole (n = 222) Placebo Létrozole 603 617 413 420 (1 - 1 037) (10 - 1 071) (10 -1 075) 93, 0 99, 9 99, 6 100, 0 (40, 3 - 109, 5) (73, 4 - 100, 2) (56, 1 - 104, 5) (79, 0 - 100, 0) Patients avec interruptions de dose, n (%) 310 (70) 237 (53) 94 (42) 99 (45) Patientes avec décalage de cycle, n (%) 303 (68) S/O 60 (27) NA Patientes avec ≥ 1 réduction de dose, n (%) 160 (36) S/O 3 (1) NA Dose-intensité médiane, % Finn RS, Martin M, Rugo HS et al. PALOMA-2: Primary results from a phase 3 trial of palbociclib plus letrozole compared with placebo plus letrozole in postmenopausal women with ER+/HER 2 - advanced breast cancer. J Clin Oncol 34, 2016 (suppl; abstr 507) PFIZER CONFIDENTIAL NA : non applicable
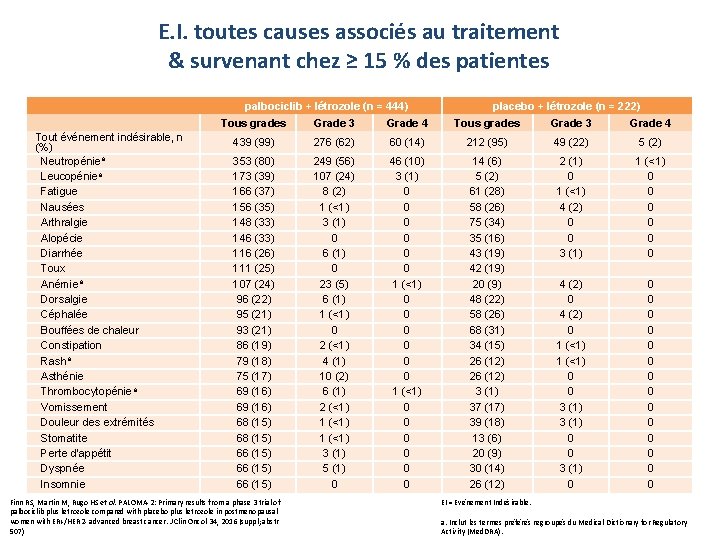
E. I. toutes causes associés au traitement & survenant chez ≥ 15 % des patientes palbociclib + létrozole (n = 444) Tout événement indésirable, n (%) Neutropéniea Leucopéniea Fatigue Nausées Arthralgie Alopécie Diarrhée Toux Anémiea Dorsalgie Céphalée Bouffées de chaleur Constipation Rasha Asthénie Thrombocytopéniea Vomissement Douleur des extrémités Stomatite Perte d’appétit Dyspnée Insomnie placebo + létrozole (n = 222) Tous grades Grade 3 Grade 4 439 (99) 276 (62) 60 (14) 212 (95) 49 (22) 5 (2) 353 (80) 173 (39) 166 (37) 156 (35) 148 (33) 146 (33) 116 (26) 111 (25) 107 (24) 96 (22) 95 (21) 93 (21) 86 (19) 79 (18) 75 (17) 69 (16) 68 (15) 66 (15) 249 (56) 107 (24) 8 (2) 1 (<1) 3 (1) 0 6 (1) 0 23 (5) 6 (1) 1 (<1) 0 2 (<1) 4 (1) 10 (2) 6 (1) 2 (<1) 1 (<1) 3 (1) 5 (1) 0 46 (10) 3 (1) 0 0 0 1 (<1) 0 0 0 14 (6) 5 (2) 61 (28) 58 (26) 75 (34) 35 (16) 43 (19) 42 (19) 20 (9) 48 (22) 58 (26) 68 (31) 34 (15) 26 (12) 3 (1) 37 (17) 39 (18) 13 (6) 20 (9) 30 (14) 26 (12) 2 (1) 0 1 (<1) 4 (2) 0 0 3 (1) 1 (<1) 0 0 0 4 (2) 0 1 (<1) 0 0 3 (1) 0 0 0 0 Finn RS, Martin M, Rugo HS et al. PALOMA-2: Primary results from a phase 3 trial of palbociclib plus letrozole compared with placebo plus letrozole in postmenopausal women with ER+/HER 2 - advanced breast cancer. J Clin Oncol 34, 2016 (suppl; abstr 507) EI = Evénement Indésirable. PFIZER CONFIDENTIAL a. Inclut les termes préférés regroupés du Medical Dictionary for Regulatory Activity (Med. DRA).

Conclusions • L’association du palbociclib et du létrozole a amélioré de manière significative la SSP médiane par rapport à l’association placebo plus létrozole dans le traitement de première ligne des patientes atteintes d’un cancer du sein ER+/HER 2 - au stade avancé Amélioration > 10 mois de la SSP médiane : 24, 8 mois vs 14, 5 mois HR = 0, 58 (IC à 95 % : 0, 46 -0, 72 ; P < 0, 0001) • Le bénéfice du palbociclib a été démontré pour tous les sous-groupes de patientes et confirmé par une revue indépendante en aveugle • Le palbociclib a été bien toléré ; les événements indésirables plus fréquents étant la neutropénie et la leucopénie. Cependant, l’incidence globale de neutropénie fébrile a été faible (1, 8 %) • Ces données confirment les résultats de l’étude ouverte PALOMA-1. Ils représentent à ce jour l’amélioration significative de la SSP la plus longue jamais démontrée en traitement de première ligne Finn RS, Martin M, Rugo HS et al. PALOMA-2: Primary results from a phase 3 trial of palbociclib plus letrozole compared with placebo plus letrozole in postmenopausal women with ER+/HER 2 - advanced breast cancer. J Clin Oncol 34, 2016 (suppl; abstr 507) PFIZER CONFIDENTIAL

PALOMA-3: Study Design n=347 • HR+, HER 2– ABC • Pre-/peri-a or postmenopausalb • Progressed on prior endocrine therapy: – On or within 12 mo adjuvant – On therapy for ABC • ≤ 1 prior chemotherapy regimen for advanced cancer 2: 1 Randomization n=521 c Palbociclib (125 mg QD; 3 wks on/1 wk off) + Fulvestrantd (500 mg IM q 4 w) Stratification: • Visceral metastases • Sensitivity to prior hormonal therapy • Pre-/peri- vs post-menopausal n=174 Placebo (3 wks on/1 wk off) + Fulvestrantd (500 mg IM q 4 w) a. All received goserelin. have progressed on prior endocrine therapy (pre-/perimenopausal) or aromatase inhibitor therapy (postmenopausal). c. Patients randomized. d. Administered on Days 1 and 15 of Cycle 1, then every 28 d. b. Must Phase 3, double-blind study involving 144 centers in 17 countries (NCT 01942135) Turner NC, et al. N Engl J Med 2015; 373: 209 -219 Turner NC, et al. ASCO 2015 (Abstract LBA 502)
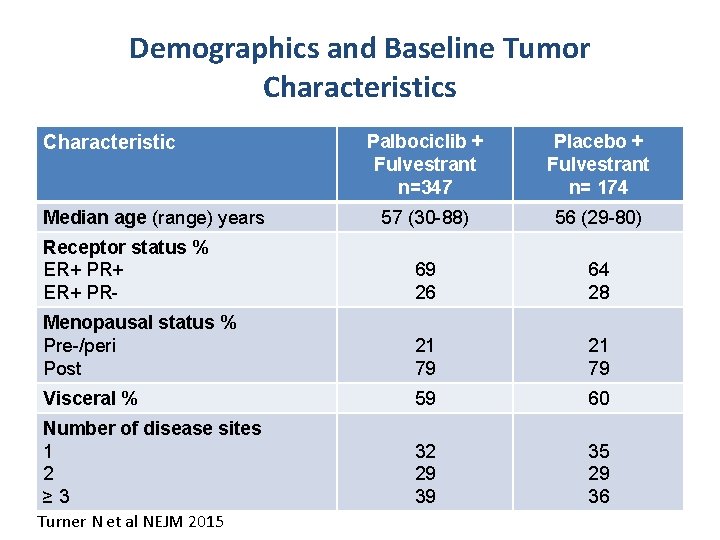
Demographics and Baseline Tumor Characteristics Palbociclib + Fulvestrant n=347 Placebo + Fulvestrant n= 174 57 (30 -88) 56 (29 -80) Receptor status % ER+ PR+ ER+ PR- 69 26 64 28 Menopausal status % Pre-/peri Post 21 79 Visceral % 59 60 Number of disease sites 1 2 ≥ 3 32 29 39 35 29 36 Characteristic Median age (range) years Turner N et al NEJM 2015
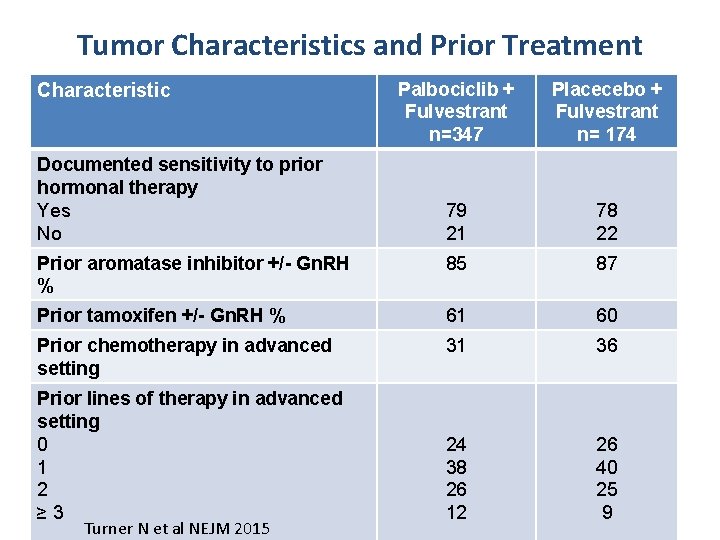
Tumor Characteristics and Prior Treatment Palbociclib + Fulvestrant n=347 Placecebo + Fulvestrant n= 174 79 21 78 22 Prior aromatase inhibitor +/- Gn. RH % 85 87 Prior tamoxifen +/- Gn. RH % 61 60 Prior chemotherapy in advanced setting 31 36 24 38 26 12 26 40 25 9 Characteristic Documented sensitivity to prior hormonal therapy Yes No Prior lines of therapy in advanced setting 0 1 2 ≥ 3 Turner N et al NEJM 2015
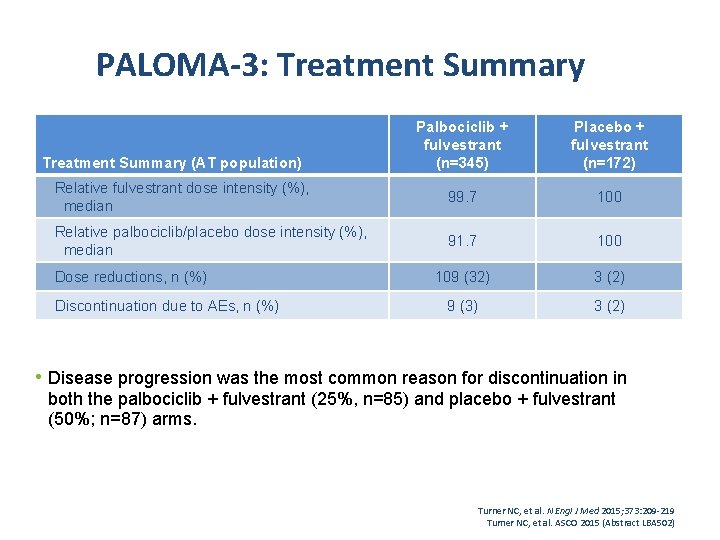
PALOMA-3: Treatment Summary Palbociclib + fulvestrant (n=345) Placebo + fulvestrant (n=172) Relative fulvestrant dose intensity (%), median 99. 7 100 Relative palbociclib/placebo dose intensity (%), median 91. 7 100 109 (32) 3 (2) 9 (3) 3 (2) Treatment Summary (AT population) Dose reductions, n (%) Discontinuation due to AEs, n (%) • Disease progression was the most common reason for discontinuation in both the palbociclib + fulvestrant (25%, n=85) and placebo + fulvestrant (50%; n=87) arms. Turner NC, et al. N Engl J Med 2015; 373: 209 -219 Turner NC, et al. ASCO 2015 (Abstract LBA 502)
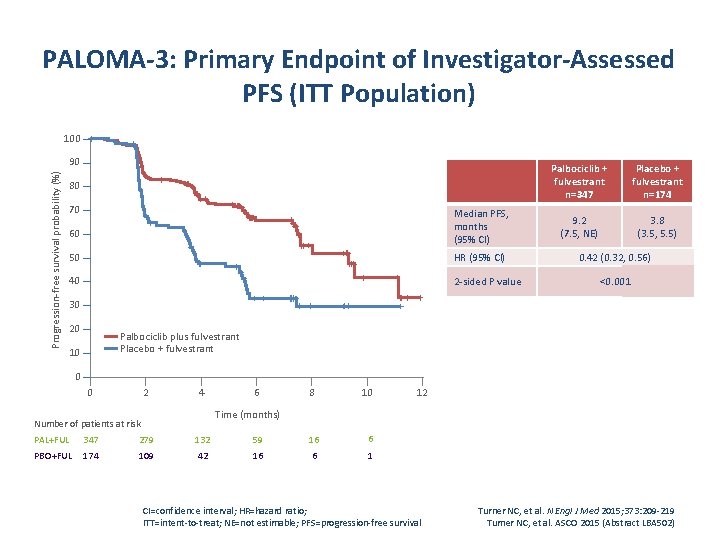
PALOMA-3: Primary Endpoint of Investigator-Assessed PFS (ITT Population) 100 Progression-free survival probability (%) 90 80 70 Median PFS, months (95% CI) 60 50 HR (95% CI) 40 2 -sided P value Palbociclib + fulvestrant n=347 Placebo + fulvestrant n=174 9. 2 (7. 5, NE) 3. 8 (3. 5, 5. 5) 0. 42 (0. 32, 0. 56) <0. 001 30 20 Palbociclib plus fulvestrant Placebo + fulvestrant 10 0 0 2 4 6 8 10 12 Time (months) Number of patients at risk PAL+FUL 347 279 132 59 16 6 PBO+FUL 174 109 42 16 6 1 CI=confidence interval; HR=hazard ratio; ITT=intent-to-treat; NE=not estimable; PFS=progression-free survival Turner NC, et al. N Engl J Med 2015; 373: 209 -219 Turner NC, et al. ASCO 2015 (Abstract LBA 502)
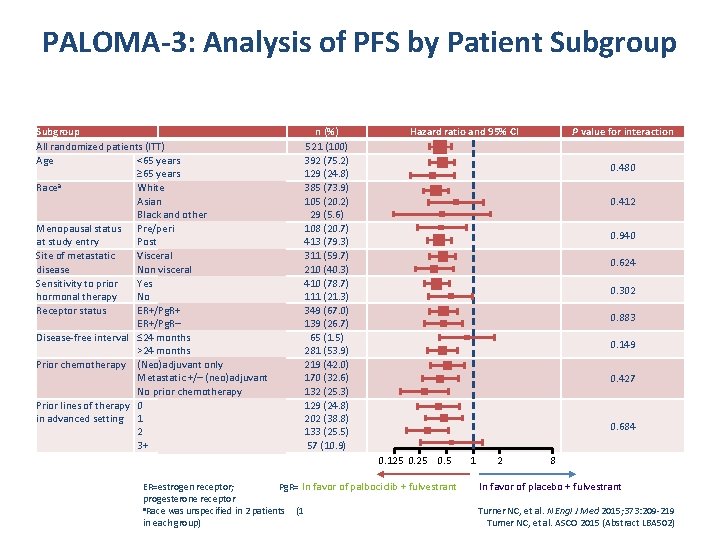
PALOMA-3: Analysis of PFS by Patient Subgroup All randomized patients (ITT) Age <65 years ≥ 65 years Racea White Asian Black and other Menopausal status Pre/peri at study entry Post Site of metastatic Visceral disease Non visceral Sensitivity to prior Yes hormonal therapy No Receptor status ER+/Pg. R+ ER+/Pg. R– Disease-free interval ≤ 24 months >24 months Prior chemotherapy (Neo)adjuvant only Metastatic +/– (neo)adjuvant No prior chemotherapy Prior lines of therapy 0 in advanced setting 1 2 3+ n (%) 521 (100) 392 (75. 2) 129 (24. 8) 385 (73. 9) 105 (20. 2) 29 (5. 6) 108 (20. 7) 413 (79. 3) 311 (59. 7) 210 (40. 3) 410 (78. 7) 111 (21. 3) 349 (67. 0) 139 (26. 7) 65 (1. 5) 281 (53. 9) 219 (42. 0) 170 (32. 6) 132 (25. 3) 129 (24. 8) 202 (38. 8) 133 (25. 5) 57 (10. 9) Hazard ratio and 95% CI P value for interaction 0. 480 0. 412 0. 940 0. 624 0. 302 0. 883 0. 149 0. 427 0. 684 0. 125 0. 5 ER=estrogen receptor; Pg. R= In favor of palbociclib + fulvestrant progesterone receptor a. Race was unspecified in 2 patients (1 in each group) 1 2 8 In favor of placebo + fulvestrant Turner NC, et al. N Engl J Med 2015; 373: 209 -219 Turner NC, et al. ASCO 2015 (Abstract LBA 502)
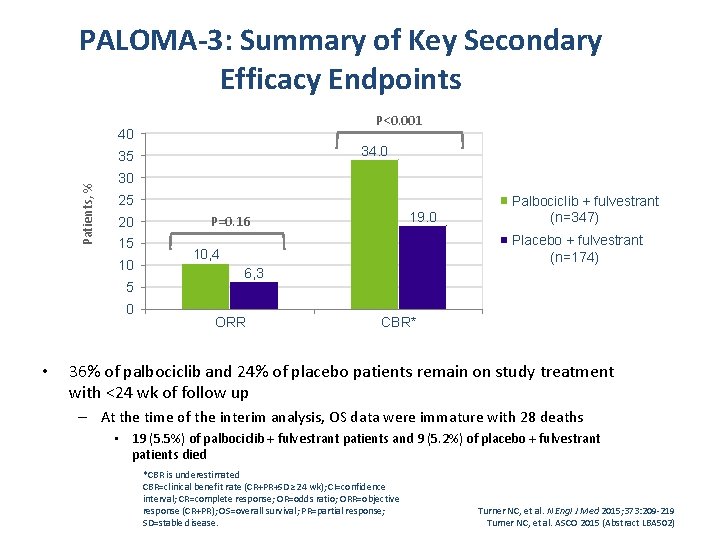
PALOMA-3: Summary of Key Secondary Efficacy Endpoints P<0. 001 40 34. 0 Patients, % 35 30 25 20 15 10 5 0 • 19. 0 P=0. 16 Palbociclib + fulvestrant (n=347) Placebo + fulvestrant (n=174) 10, 4 6, 3 ORR CBR* 36% of palbociclib and 24% of placebo patients remain on study treatment with <24 wk of follow up – At the time of the interim analysis, OS data were immature with 28 deaths • 19 (5. 5%) of palbociclib + fulvestrant patients and 9 (5. 2%) of placebo + fulvestrant patients died *CBR is underestimated CBR=clinical benefit rate (CR+PR+SD ≥ 24 wk); CI=confidence interval; CR=complete response; OR=odds ratio; ORR=objective response (CR+PR); OS=overall survival; PR=partial response; SD=stable disease. Turner NC, et al. N Engl J Med 2015; 373: 209 -219 Turner NC, et al. ASCO 2015 (Abstract LBA 502)
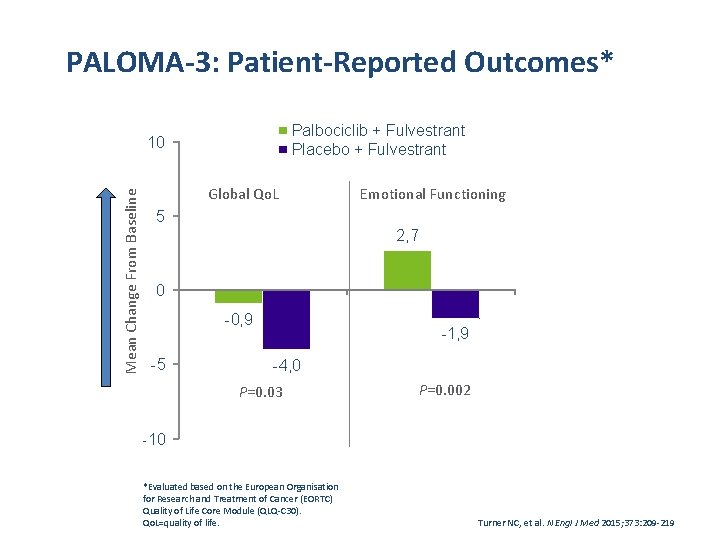
PALOMA-3: Patient-Reported Outcomes* Palbociclib + Fulvestrant Placebo + Fulvestrant Mean Change From Baseline 10 Global Qo. L Emotional Functioning 5 2, 7 0 -0, 9 -5 -1, 9 -4, 0 P=0. 03 P=0. 002 -10 *Evaluated based on the European Organisation for Research and Treatment of Cancer (EORTC) Quality of Life Core Module (QLQ-C 30). Qo. L=quality of life. Turner NC, et al. N Engl J Med 2015; 373: 209 -219
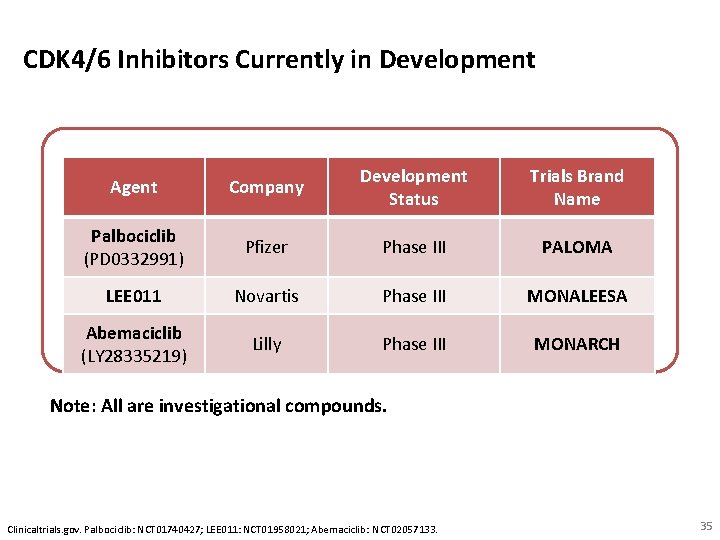
CDK 4/6 Inhibitors Currently in Development Agent Company Development Status Trials Brand Name Palbociclib (PD 0332991) Pfizer Phase III PALOMA LEE 011 Novartis Phase III MONALEESA Abemaciclib (LY 28335219) Lilly Phase III MONARCH Note: All are investigational compounds. Clinicaltrials. gov. Palbociclib: NCT 01740427; LEE 011: NCT 01958021; Abemaciclib: NCT 02057133. 35
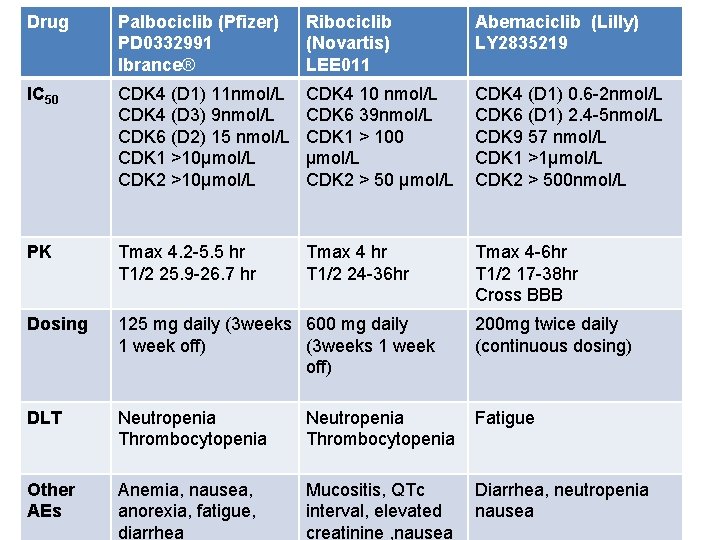
Drug Palbociclib (Pfizer) Ribociclib Key characteristics of PD 0332991 (Novartis) Ibrance® LEE 011 IC 50 CDK 4 (D 1) 11 nmol/L CDK 4 (D 3) 9 nmol/L CDK 6 (D 2) 15 nmol/L CDK 1 >10µmol/L CDK 2 >10µmol/L CDK 4 10 nmol/L CDK 6 39 nmol/L CDK 1 > 100 µmol/L CDK 2 > 50 µmol/L CDK 4 (D 1) 0. 6 -2 nmol/L CDK 6 (D 1) 2. 4 -5 nmol/L CDK 9 57 nmol/L CDK 1 >1µmol/L CDK 2 > 500 nmol/L PK Tmax 4. 2 -5. 5 hr T 1/2 25. 9 -26. 7 hr Tmax 4 hr T 1/2 24 -36 hr Tmax 4 -6 hr T 1/2 17 -38 hr Cross BBB Dosing 125 mg daily (3 weeks 600 mg daily 1 week off) (3 weeks 1 week off) 200 mg twice daily (continuous dosing) DLT Neutropenia Thrombocytopenia Fatigue Other AEs Anemia, nausea, anorexia, fatigue, diarrhea Mucositis, QTc interval, elevated creatinine , nausea Diarrhea, neutropenia nausea CDK Abemaciclib (Lilly) inhibitors LY 2835219
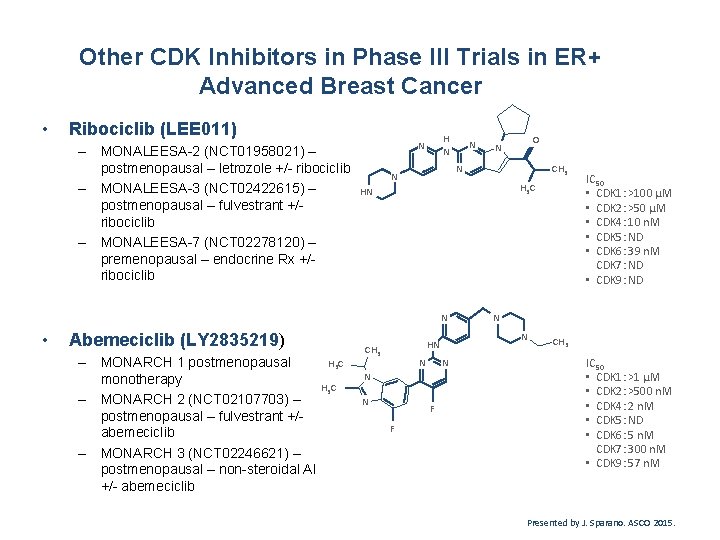
Other CDK Inhibitors in Phase III Trials in ER+ Advanced Breast Cancer • Ribociclib (LEE 011) – MONALEESA-2 (NCT 01958021) – postmenopausal – letrozole +/- ribociclib – MONALEESA-3 (NCT 02422615) – postmenopausal – fulvestrant +/ribociclib – MONALEESA-7 (NCT 02278120) – premenopausal – endocrine Rx +/ribociclib H N N Abemeciclib (LY 2835219) H 3 C – MONARCH 1 postmenopausal monotherapy H 3 C – MONARCH 2 (NCT 02107703) – postmenopausal – fulvestrant +/abemeciclib – MONARCH 3 (NCT 02246621) – postmenopausal – non-steroidal AI +/- abemeciclib CH 3 H 3 C HN N N F F IC 50 • CDK 1: >100 µM • CDK 2: >50 µM • CDK 4: 10 n. M • CDK 5: ND • CDK 6: 39 n. M CDK 7: ND • CDK 9: ND N N HN CH 3 O N N • N CH 3 IC 50 • CDK 1: >1 µM • CDK 2: >500 n. M • CDK 4: 2 n. M • CDK 5: ND • CDK 6: 5 n. M CDK 7: 300 n. M • CDK 9: 57 n. M Presented by J. Sparano. ASCO 2015.

Conclusions (1) • La voie Cycline D 1 -CDK 4/6 -Rb est critique pour la prolifération cellulaire

Conclusions (1) • La voie Cycline D 1 -CDK 4/6 -Rb est critique pour la prolifération cellulaire • Dysrégulation est fréquement observée dans les cancers du sein RH+ et associée à une hormonorésistance

Conclusions (1) • La voie Cycline D 1 -CDK 4/6 -Rb est critique pour la prolifération cellulaire • Dysrégulation est fréquement observée dans les cancers du sein RH+ et associée à une hormonorésistance • Plusieurs Inhibiteurs CDK 4/6 en développement: palbociclib, ribociclib et abemaciclib

Conclusions (1) • La voie Cycline D 1 -CDK 4/6 -Rb est critique pour la prolifération cellulaire • Dysrégulation est fréquement observée dans les cancers du sein RH+ et associée à une hormonorésistance • Plusieurs Inhibiteurs CDK 4/6 en développement: palbociclib, ribociclib et abemaciclib • Inhibiteurs CDK 4/6 et hormonothérapie : mode d’action complémentaire

Conclusions (2) • Palbociclib, inhibiteur CDK 4/6 a démontré une activité préclinique (dans les lignées cellulaires et les xénogreffes) en association avec tamoxifene et letrozole

Conclusions (2) • Palbociclib, inhibiteur CDK 4/6 a démontré une activité préclinique (dans les lignées cellulaires et les xénogreffes) en association avec tamoxifene et letrozole • En première ligne M+, l’association palbociclib letrozole (PALOMA-1) a démontré un doublement de la SSP observée dans tous les sous-groupes (20. 2 mois vs 10. 2 mois) • Confirmation des résultats avec Phase III PALOMA 2

Conclusions (2) • Palbociclib, inhibiteur CDK 4/6 a démontré une activité préclinique (dans les lignées cellulaires et les xénogreffes) en association avec tamoxifene et letrozole • En première ligne M+, l’association palbociclib letrozole (PALOMA-1) a démontré un doublement de la SSP observée dans tous les sous-groupes (20. 2 mois vs 10. 2 mois) • Etude de confirmation Phase III PALOMA 2 • L’activité du palbociclib a été confirmée dans une population résistante à l’hormonothérapie (PALOMA 3) – Le profil de tolérance était acceptable avec des effets secondaires transitoires et réversibles

Palbociclib + IA Une des option préférée en 1ère ligne chez les patientes ( pré et post ménopause)


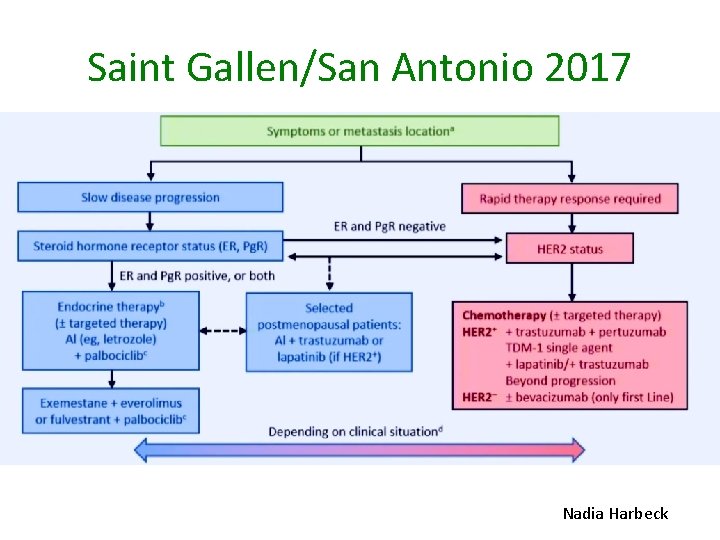
Saint Gallen/San Antonio 2017 Nadia Harbeck
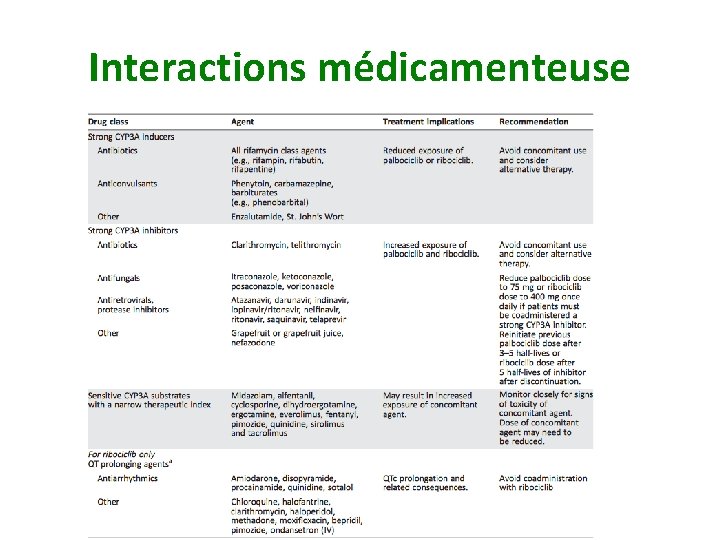
Interactions médicamenteuse

Modifications posologiques: Toxicités hématologiques Bilan: Biologie mensuelle + NFS au J 15 les 2 premiers mois.
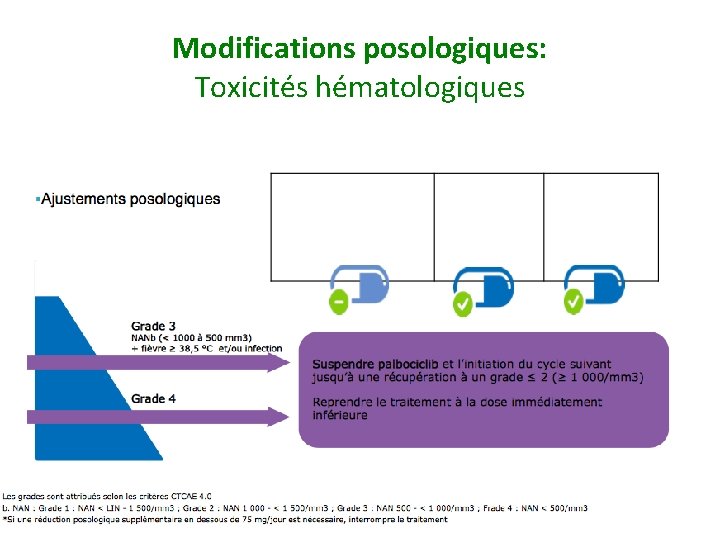
Modifications posologiques: Toxicités hématologiques

Conclusion • Palbociclib : nouvelle arme thérapeutique • Action Complémentaire avec l’hormonothérapie • Efficacité: dédoublement de la SSP observée dans tous les sous-groupes • Tolérance: effets secondaires transitoires et réversibles
- Slides: 52