Interstitialis tdbetegsgek ILD Diffz parenchyms tdbetegsgek DPLD Edit

Interstitialis tüdőbetegségek (ILD) Diffúz parenchymás tüdőbetegségek (DPLD) Edit Csada, MD 2016. 10. 07. 1

n a tüdő kötőszövetes vázának eltérő típusú és fokú, nem fertőzéses eredetű diffúz gyulladása n az alveolocapillaris egység pusztulásával járó kórképek, következményes fibrózissal és pulmonalis hypertoniával n prevalencia: 7 -20/100 000 2
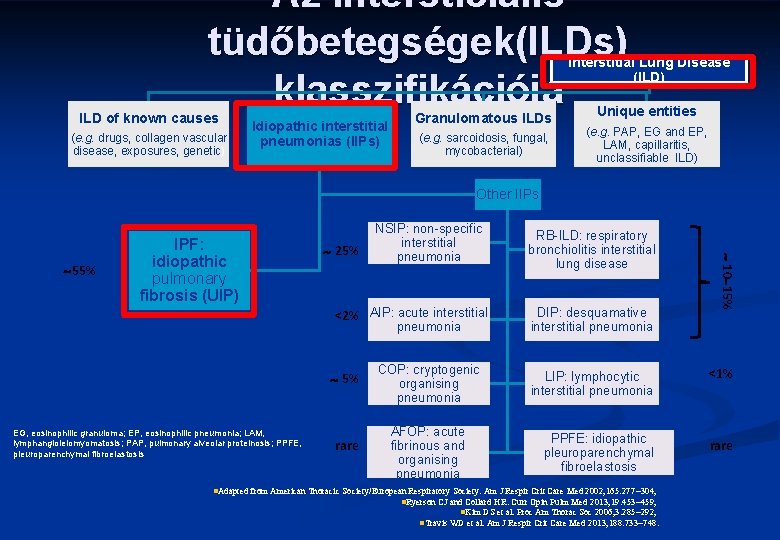
Az interstíciális tüdőbetegségek(ILDs) klasszifikációja Interstitial Lung Disease (ILD) ILD of known causes (e. g. drugs, collagen vascular disease, exposures, genetic) Idiopathic interstitial pneumonias (IIPs) Granulomatous ILDs (e. g. sarcoidosis, fungal, mycobacterial) Unique entities (e. g. PAP, EG and EP, LAM, capillaritis, unclassifiable ILD) Other IIPs 25% <2% AIP: acute interstitial pneumonia 5% EG, eosinophilic granuloma; EP, eosinophilic pneumonia; LAM, lymphangioleiomyomatosis; PAP, pulmonary alveolar proteinosis; PPFE, pleuroparenchymal fibroelastosis rare COP: cryptogenic organising pneumonia AFOP: acute fibrinous and organising pneumonia RB-ILD: respiratory bronchiolitis interstitial lung disease DIP: desquamative interstitial pneumonia 10 15% 55% IPF: idiopathic pulmonary fibrosis (UIP) NSIP: non-specific interstitial pneumonia LIP: lymphocytic interstitial pneumonia <1% PPFE: idiopathic pleuroparenchymal fibroelastosis rare n. Adapted from American Thoracic Society/European Respiratory Society. Am J Respir Crit Care Med 2002; 165: 277 304; n. Ryerson CJ and Collard HR. Curr Opin Pulm Med 2013; 19: 453 459; n. Kim DS et al. Proc Am Thorac Soc 2006; 3: 285 292; n. Travis WD et al. Am J Respir Crit Care Med 2013; 188: 733 748.

Kórlefolyás szerint I. n Akut DPLD allergia (gyógyszer) Ø toxin (gáz) Ø vasculitis/haemorrh (Goodpasture, idiopátiás haemosiderosis) Ø ARDS (trauma, septicaemia) Ø ismeretlen (COP, BOOP) Ø 4

Kórlefolyás szerint II. n Epizodikus DPLD eosinophil pneumonia Ø vasculitis, haemorrhagia Ø Churg-Strauss sy Ø Hypersensitiv pneumonitis Ø COP Ø 5

Kórlefolyás szerint III. n Krónikus DPLD (pulmonális expozícióval) szervetlen porok (silicosis, asbestosis) Ø szerves porok (baktérium, gomba, állati fehérjék) Ø gyógyszerek Ø 6

Kórlefolyás szerint IV. n Krónikus DPLD (szisztémás megbetegedéssel) sarcoidosis Ø kötőszöveti betegségek Ø malignoma (lymphoma, lymphangitis cc) Ø vasculitis (Wegener) Ø öröklött betegségek Ø egyéb (csv. transzplantáció, gyull. bélbet. , amyloidosis) Ø 7

Kórlefolyás szerint V. n Krónikus DPLD (szisztémás megbetegedés és expozíció nélkül) IIP Ø alveolaris proteinosis Ø krónikus aspiráció Ø LAM Ø Langerhans-sejtes histiocytosis Ø venoocclusiv betegség Ø idiopátiás pulmonális haemosiderosis Ø bronchioloalveolaris cc. Ø 8

Morphologiai változások n n n Kapillárisok pusztulása Az alveolaris epithel sejtek változása Fibrosis Pathogenesis n n A gyulladásos sejtek szaporodnak arányuk megváltozik aktiválódnak Mediátor anyagok szabadulnak fel n toxikus szabadgyökök, proteázok Fibrosis O 2 transzport károsodik 9

BAL sejtösszetétele 90% n 7% n 1% n alveoláris macrophag lymphocyta polymorph leucocyta 10

• Neutrofil alveolitis : cryptogen fibrotizáló alveolitis • Lymfocytás alveolitis : sarcoidosis, hypersensitiv pneumonitis, beryllosis • Eosinophil alveolitis • Kevertsejtes alveolitis : amiodaron fibrosis (eosinophil+lymphocyta) 11

Klinikai jellemzők I n Tünetek Terheléses nehézlégzés n Fáradékonyság n Improduktív köhögés n n Fizikális jellemzők krepitáció n Néha sípolás, hörgi légzés n Dobverőujj n 12

Klinikai jellemzők II n Laboratórium Gyorsult süllyedés n Hypoxaemia n n Mellkas rtg, HRCT Reticuláris n Noduláris n Reticulonoduláris n Tejüvegszerű homály n Lépesméz tüdő n 13

Klinikai jellemzők III n n n Légzésfunkció n VC, TLC csökkenés n FEV 1/FVC: normális, vagy emelkedett n diffuziós kapacitás (DLCO) csökkent n Oxyergospirometria (CPX) Scintigraphia (Tc 99, Xe 133) n Foltos kiesések BAL 14
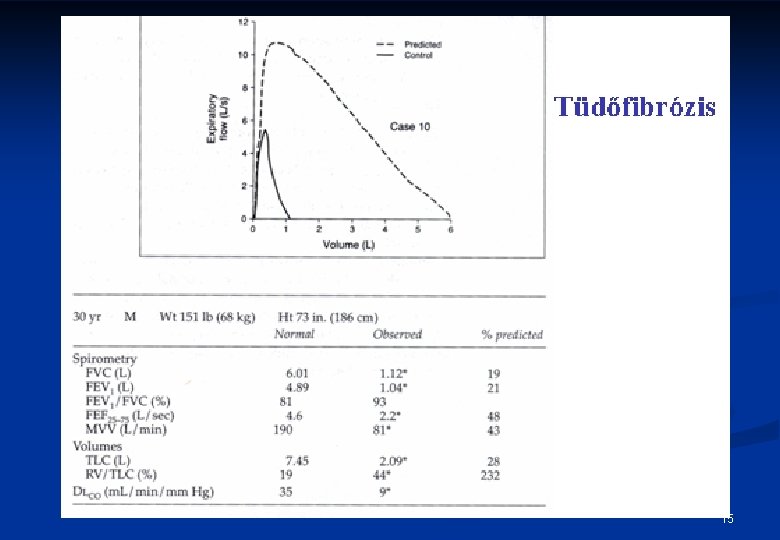
15
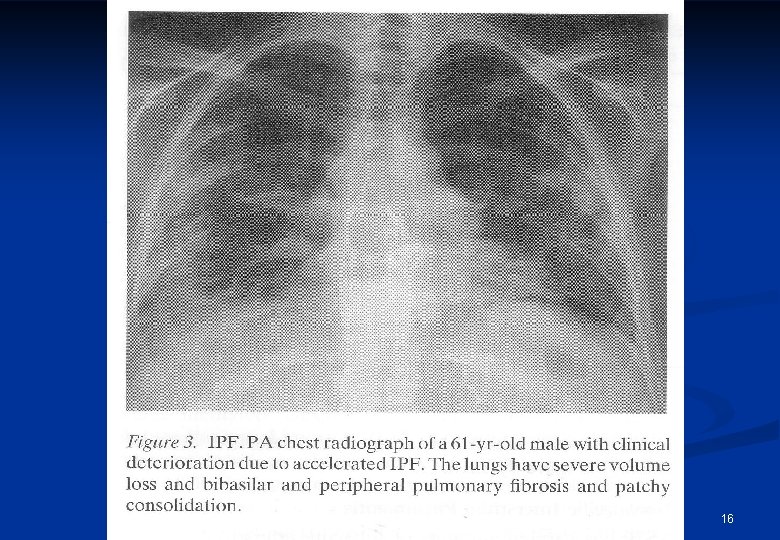
16
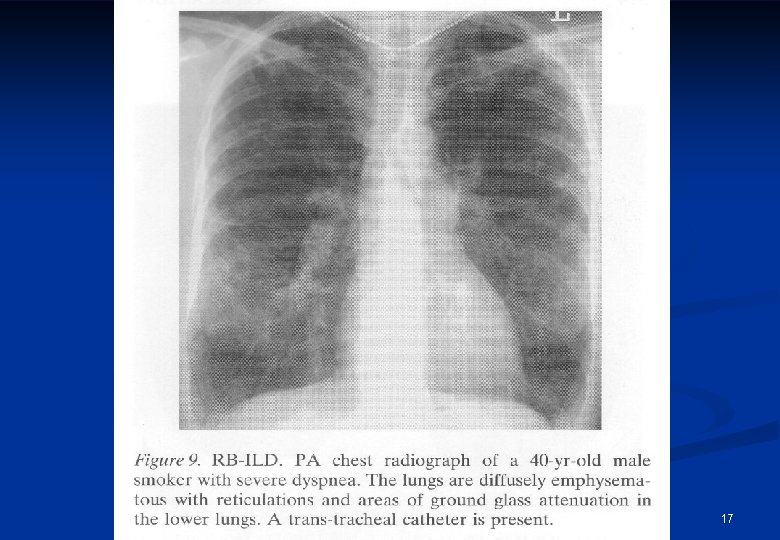
17
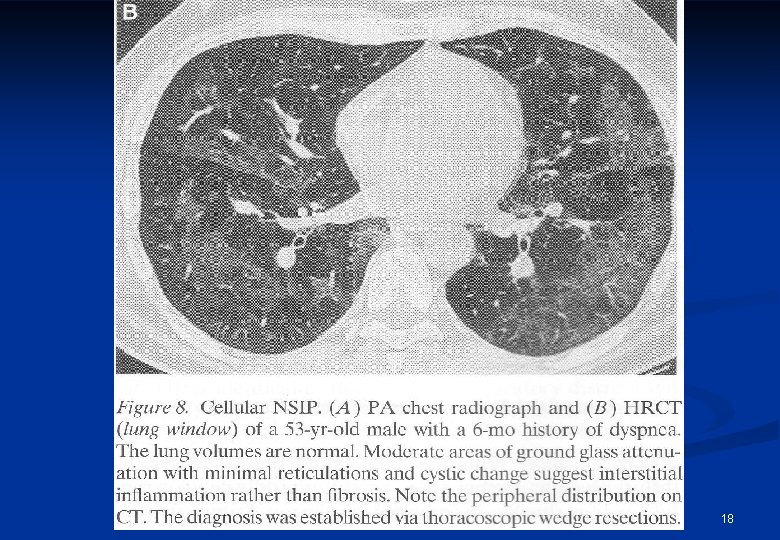
18
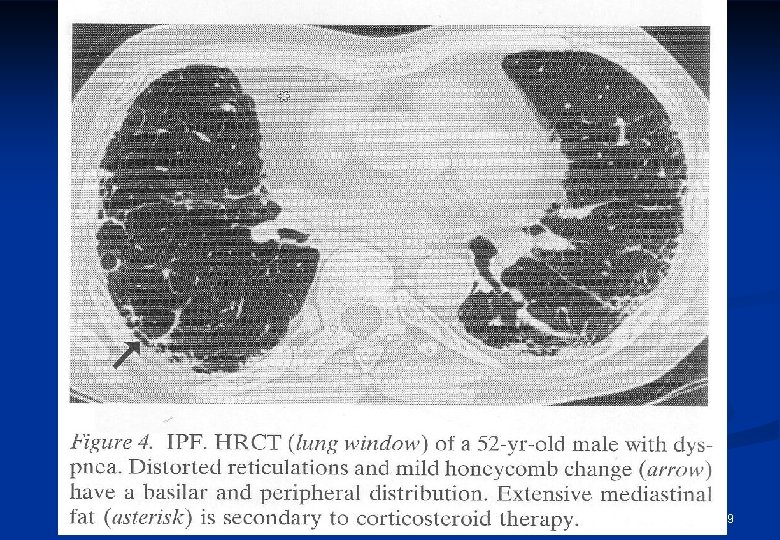
19
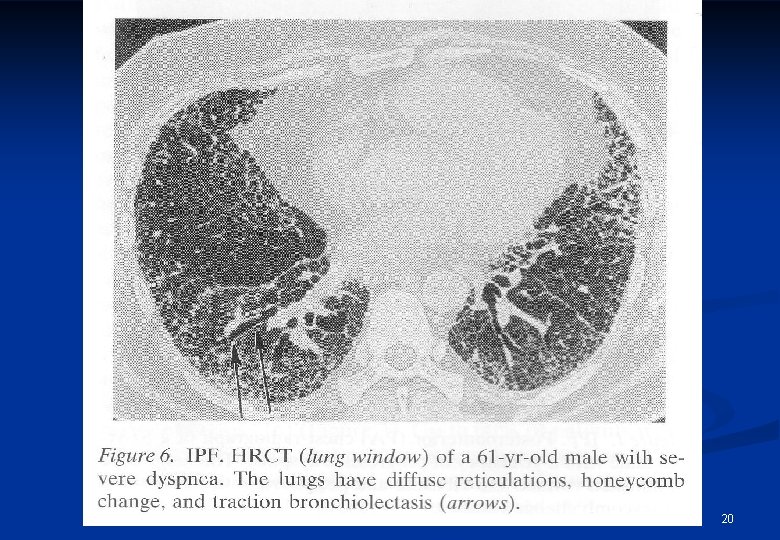
20

Diagnózis Klinikai jellemzők n Transbronchialis biopsia n VATS, nyitott tüdőbiopsia n 21

Terápia n n n Ismert etiologia n Megszüntetni az expozíciót Ismeretelen etiologia n A gyulladásos folyamat gátlása n Oralis corticosteroid (1 mg/kg 0, 25 mg/kg) n CPA (cyclophosphamide) n Imuran (azathioprine) Késői stádium n O 2 n Szupportáció n Transzplantáció 22

Idiopathiás tüdőfibrosis (IPF) n Demográfiai adatok: n Kb 80, 000 -130, 000 beteget érint az EU-ban az IPF Prevalenciája férfiaknál kicsit magasabb(20. 2/100, 000), mint nőknél (13. 2/100, 000)1 Több forrás alapján becsült prevalenciája : 16 22 / 100, 000, 2, 3, 4 Incidenciája: 4. 6 -7. 4 / 100, 000 / év 8 -10 Az IPF incidenciája és prevalenciája életkorral nő 1, 6 n n n Általában 40 80 éves kor között diagnosztizálják 1. Meltzer EB and Noble PW. Orphanet J Rare Dis 2008; 3: 8 22; 2. Coultas DB et al. Am J Respir 7 Crit Care Med 1994; 150: 967 997; Ap revalencia csúcsa 65– 79 év 2002; 57: 338 között van 3. Hodgson U et al. Thorax 342; 4. Hansell A eta l. Thorax 1999; 54: 413 2002; 57: 338 1999; 54: 413 419; n n n 5. Eurostat News Release. Available at http: //ec. europa. eu/eurostat. Accessed on 4 August 2013; 6. Ley B and Collard HR. Clin Epidemiol 2013; 5: 483 492; 7. Valeyre D. Eur Respir Rev 2011; 20: 108 113 n 8. Gribbin J et al. Thorax 2006; 61: 980 985; 9. Navaratnam V et al. Thorax 2011; 66: 462 467; n 10. Ley B and Collard HR. Clin Epidemiol 2013; 5: 483 492; .
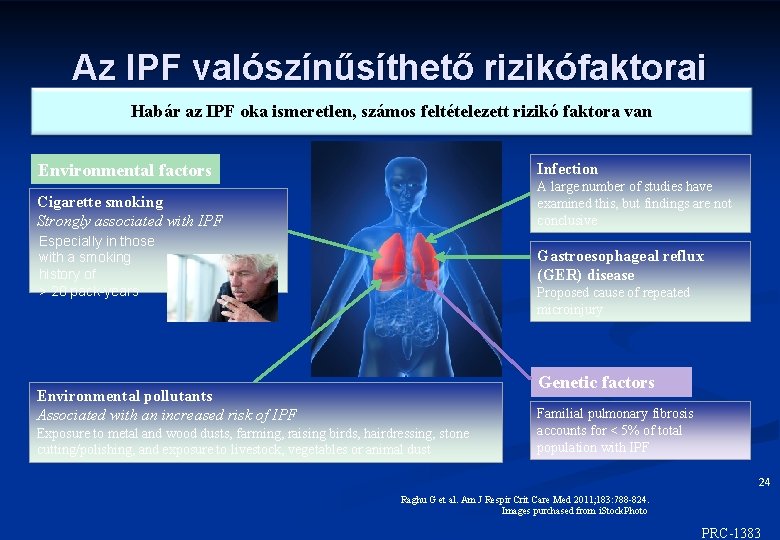
Az IPF valószínűsíthető rizikófaktorai Habár az IPF oka ismeretlen, számos feltételezett rizikó faktora van Infection Environmental factors A large number of studies have examined this, but findings are not conclusive Cigarette smoking Strongly associated with IPF Especially in those with a smoking history of > 20 pack-years Gastroesophageal reflux (GER) disease Proposed cause of repeated microinjury Genetic factors Environmental pollutants Associated with an increased risk of IPF Exposure to metal and wood dusts, farming, raising birds, hairdressing, stone cutting/polishing, and exposure to livestock, vegetables or animal dust Familial pulmonary fibrosis accounts for < 5% of total population with IPF 24 Raghu G et al. Am J Respir Crit Care Med 2011; 183: 788 -824. Images purchased from i. Stock. Photo ©Inter. Mune, Inc. , 2012 PRC-1383
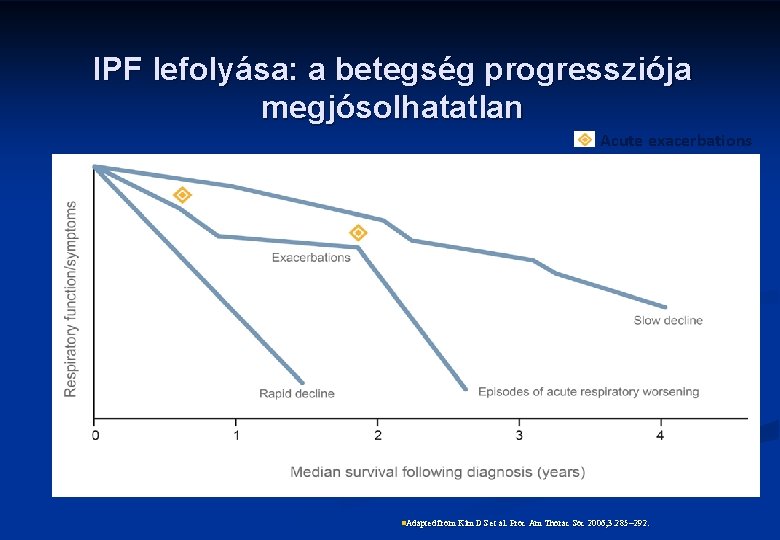
IPF lefolyása: a betegség progressziója megjósolhatatlan Acute exacerbations n. Adapted from Kim DS et al. Proc Am Thorac Soc 2006; 3: 285 292.

Patogenezis n Az IPF patomechanizmusa nem teljesen ismert, de három fázisa feltételezhető: 1. Kezdeti epitheliális sérülés 2. Abnormális repair válasz 3. A tüdő szöveti károsodása 26 du Bois RM. Nat Rev Drug Discov 2010; 9: 129 -140. ©Inter. Mune, Inc. , 2012 PRC-1383
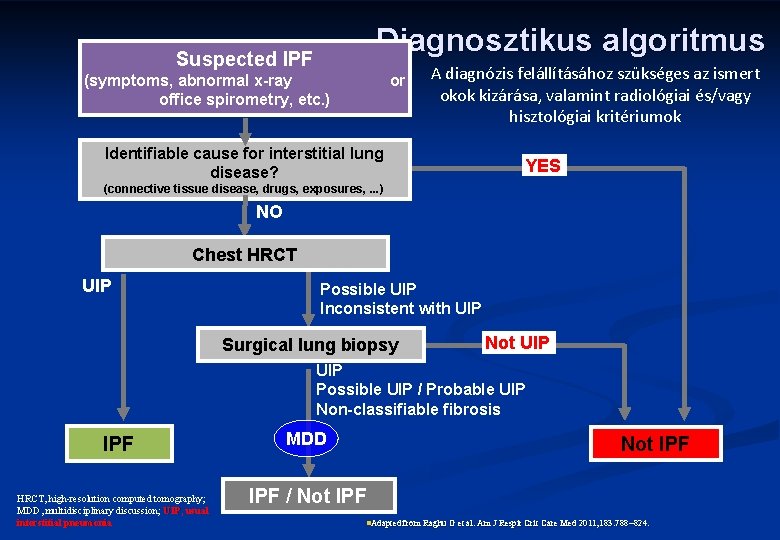
Diagnosztikus algoritmus Suspected IPF (symptoms, abnormal x-ray office spirometry, etc. ) or A diagnózis felállításához szükséges az ismert okok kizárása, valamint radiológiai és/vagy hisztológiai kritériumok Identifiable cause for interstitial lung disease? YES (connective tissue disease, drugs, exposures, . . . ) NO Chest HRCT UIP Possible UIP Inconsistent with UIP Surgical lung biopsy Not UIP Possible UIP / Probable UIP Non-classifiable fibrosis IPF HRCT, high-resolution computed tomography; MDD, multidisciplinary discussion; UIP, usual interstitial pneumonia MDD Not IPF / Not IPF n. Adapted from Raghu G et al. Am J Respir Crit Care Med 2011; 183: 788 824.

Klinikai megjelenése } } Kor >45 éves felismeréskor Száraz köhögés Lassan progrediáló dyspnoe Száraz, kétoldali, belégzéskor jelentkező “Velcro -like” hallgatózási lelet } Abnormális légzésfunkciós eredmények – alapvetően restriktív, károsodott gáz-csere } Dobverő-ujjak (25 -50%-os előfordulással) } További klinikai jellemzői a betegség későbbi fázisában jelenzkeznek • Pl. cyanosis, cor pulmonale and perifériás oedema Az IPF egy súlyos, restriktív tüdő betegség, mely korlátozza a beteg rutin napi fizikai aktivitását n 1. American Thoracic Society/European Respiratory Society. Am J Respir Crit Care Med 2002; 165: 277 304. n. NICE clinical guideline 163, June 2013. Available at n 2. Raghu G et al. Am J Respir Crit Care Med 2011; 183: 788 824; http: //www. nice. org. uk/guidance/cg 163. Accessed on 15 August 2014; n. Panos RJ et al. Am J Med 1990; 88: 396– 404; Image purchased from Science Photo Library.
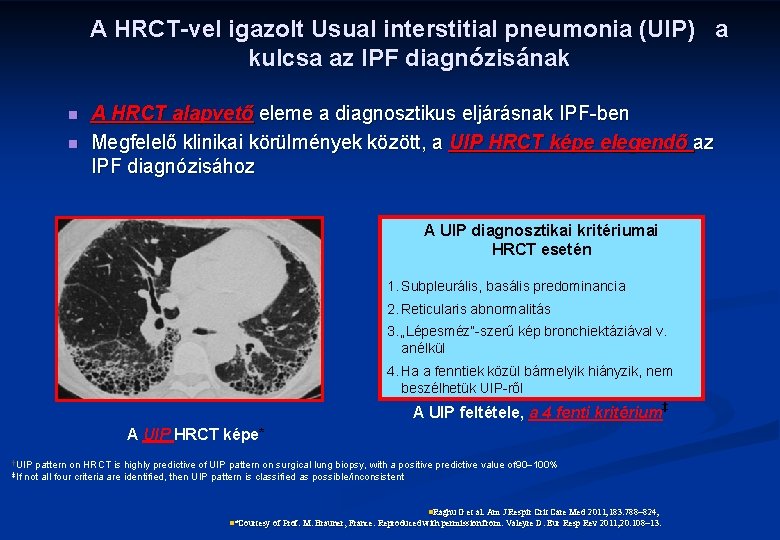
A HRCT-vel igazolt Usual interstitial pneumonia (UIP) a kulcsa az IPF diagnózisának n n A HRCT alapvető eleme a diagnosztikus eljárásnak IPF-ben Megfelelő klinikai körülmények között, a UIP HRCT képe elegendő az IPF diagnózisához A UIP diagnosztikai kritériumai HRCT esetén 1. Subpleurális, basális predominancia 2. Reticularis abnormalitás 3. „Lépesméz”-szerű kép bronchiektáziával v. anélkül 4. Ha a fenntiek közül bármelyik hiányzik, nem beszélhetük UIP-ről A UIP feltétele, a 4 fenti kritérium‡ A UIP HRCT képe* †UIP ‡If pattern on HRCT is highly predictive of UIP pattern on surgical lung biopsy, with a positive predictive value of 90 100% not all four criteria are identified, then UIP pattern is classified as possible/inconsistent n. Raghu G et al. Am J Respir Crit Care Med 2011; 183: 788 824; n*Courtesy of Prof. M. Brauner, France. Reproduced with permission from: Valeyre D. Eur Resp Rev 2011; 20: 108 13.

n n n Radiológiai megjelenés: HRCT alapvető szerepű a diagnosztikus algoritmusban bazális, subpleurális retikuláris rajzolat lépesméztüdő (3 -10 mm-es, esetleg 2 cm nagyságú subpleurális képletek) tractios bronchiectasiával vagy anélkül. tejüveg rajzolat előfordulhat, de a retikuláris rajzolat kiterjedésénél kisebb. n HRCT pozitív prediktív értéke 90 -100% !!! n Lépesméztüdő hiányában szövettani verifikáció szükséges (nem zárja ki a UIP lehetőségét).

A gyógyszeres terápia változóban : n n Korábban, az IPF-t gyulladásos betegségnek tartották, ezért kezelésében is gyulladásgátlókat alkalmaztak 1, 2 Az IPF patomechanizmusának megértésével változott a fókusza a gyógyszeres terápiának is n n A gyulladásos komponensnek ma már csak alárendelt szerepet tulajdonítunk 1, 2 A fibrózis és az epitheliális sérülés dominál a betegségben 1, 2 A fibrózis-ellenes szerek alkalmasak az IPF kezelésére Pirfenidon, Nintedanib n 1. Selman M et al. Ann Intern Med 2001; 134: 136 151; ©Inter. Mune, Inc. , 2012 2. Günther A et al. Eur Respir Rev 2012; 21: 152 160.

IPF - Nem-gyógyszeres terápiája n Oxigén terápia n n Ajánlott : IPF-betegeknek klinikailag szignifikáns nyugalmi hypoxaemia 1 esetén Tüdőtranszplantáció n Csak kevés IPF-beteg számára elérhető 1, 2 1. ATS/ERS/JRS/ALAT. Am J Respir Crit Care Med 2011; 183: 788 -824 2. Meltzer EB, Noble PW. Orphanet J Rare Dis. 2008; 3: 8
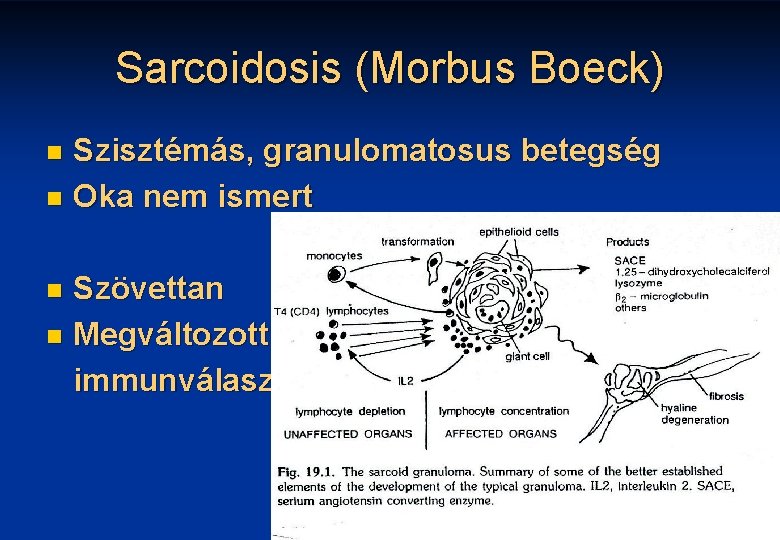
Sarcoidosis (Morbus Boeck) Szisztémás, granulomatosus betegség n Oka nem ismert n Szövettan n Megváltozott immunválasz n 33
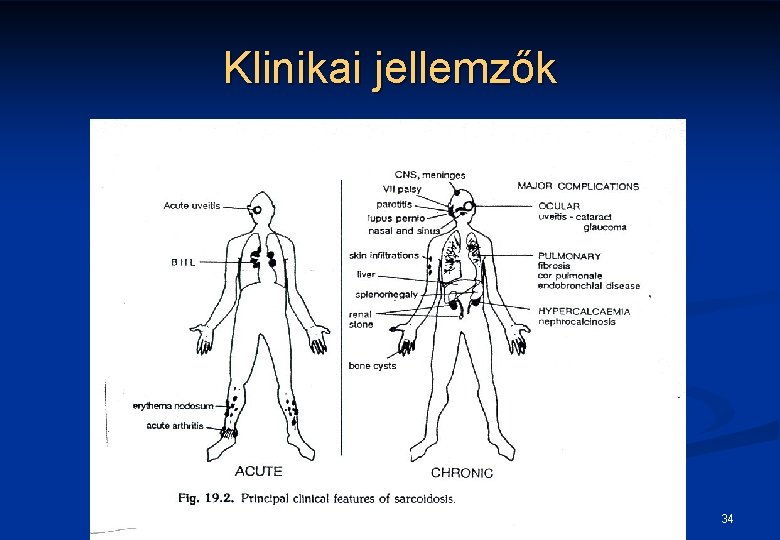
Klinikai jellemzők 34

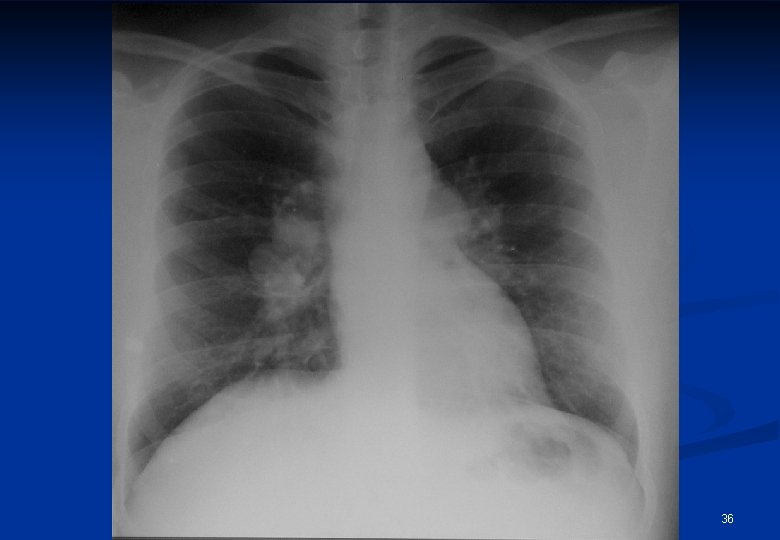
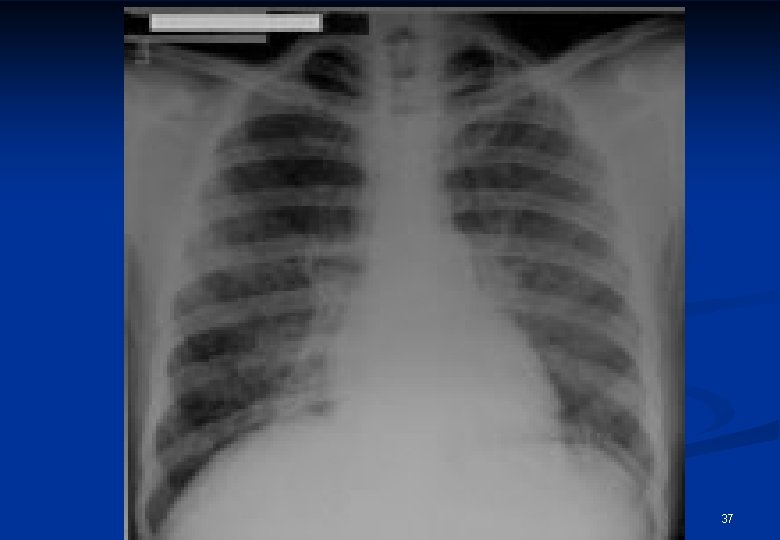
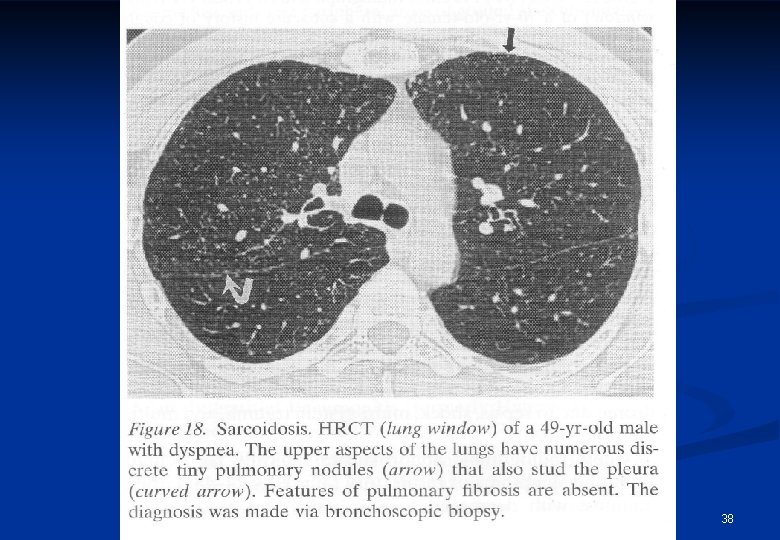
Radiologiai jellemzők Stádium/forma I n Stádium/forma II n n Stádium/forma III BHL sy dissemináció BHL-el, vagy nélküle tüdőfibrosis 35
36
37
38

Diagnózis n n n n BHL erythema nodosummal (Löfgren-sy) Tuberculin test: negativ Légzésfunkció Se ACE (angiotensin convertáló enzym) ↑ Transbronchialis biopsia, perbronchialis biopsia (TBNA) BAL→ly Gallium scan Mediastinoscopia 39

Terápia I stádium: nem szükséges kezelés (spontán remissio lehet) n Steroid kezelés indikációja n Progresszív betegség n Súlyos uveitis n Hypercalcaemia n Neurologiai manifesztáció n 40

Histiocytosis X (Langerhans) n n n Mononucleáris phagocyta rendszer betegsége, a mononucleáris phagocyták felhalmozódása különböző szervekben Gyermekkori manifesztáció n Letterer-Siwe betegség n Hand-Schüller-Christian betegség Felnőttkori manifesztáció n Histiocytosis X n Eosinophil granuloma 41

Klinikai jellemzők 20 -40 éves életkor (dohányos!) n Improduktív köhögés n Dyspnoe n Mellkasi fájdalom n Ptx – 10% n 42

Klinikai jellemzők n Mellkas rtg n n n Légzésfunkció n n n mononuclearis phagocyták ↑ Histologia n n Vegyes restrictiv-obstructiv vent. zavar Csökkent diffusiós capacitás BAL n n Reticulonoduláris elváltozások Kis cysticus elváltozások X testek (Birbeck) a cytoplasmában Terápia: Corticosteroid adható. 43
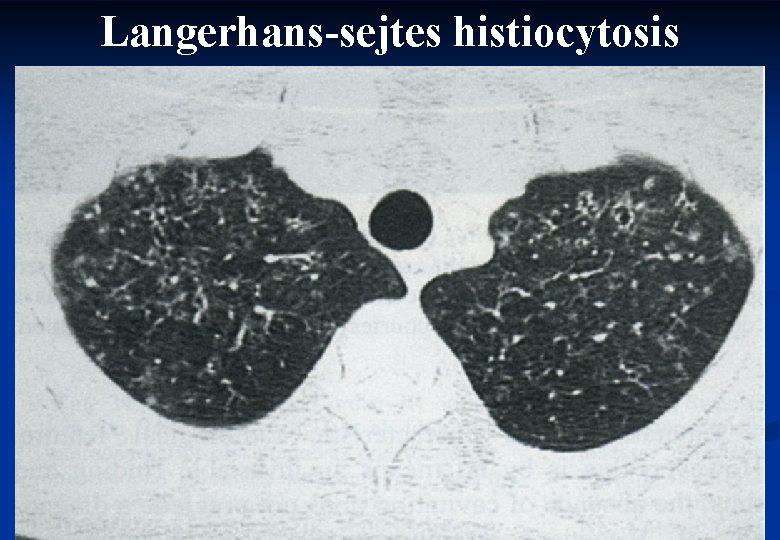
Langerhans-sejtes histiocytosis 44
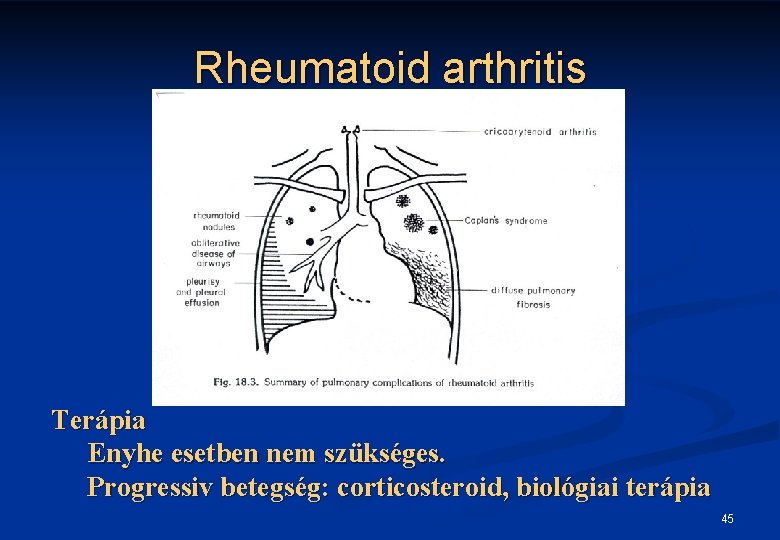
Rheumatoid arthritis Terápia Enyhe esetben nem szükséges. Progressiv betegség: corticosteroid, biológiai terápia 45

Egyéb immunologiai betegségek SLE n Sjögren sy n Scleroderma n Bechterew n Dematomyositis, polymiositis n Periarteritis nodosa n Neurofibromatosis n 46
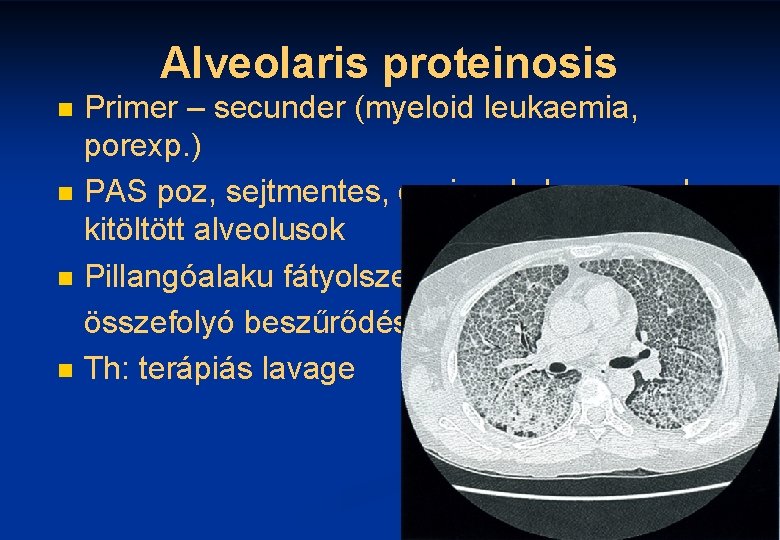
Alveolaris proteinosis n n Primer – secunder (myeloid leukaemia, porexp. ) PAS poz, sejtmentes, eosinophyl anyaggal kitöltött alveolusok Pillangóalaku fátyolszerü, összefolyó beszűrődés Th: terápiás lavage 47

Eosinophil pneumonia Eosinophil infiltratum és vérképben eosinophilia. n Ismert és ismeretlen kiváltó ok n 48

Eosinophil pneumonia n n n Ismert etiologia n Allergiás bronchopulmonaris aspergillosis (ABPA) n Parasitás infestatio (ascaris, toxocara, etc) n Drug reakció (nitrofurantoin, sulphonamide) Idiopathiás (ismeretlen etiologia) n Löffler’s sy n Benignus, acut eosinophil pneumonia (AEP) vándorló infiltratumokkal, minimális kliniai manifesztációval. n Chr. eosinophil pneumonia (CEP) n Tünetek: köhögés, verejtékezés, láz, anorexia, fogyás, hidegrázás n Mellkas rtg: Perifériás infiltrátumok n Churg-Strauss alleriás granulomatosis n Hypereosinophil sy (HES) Terápia: corticosteroid 49

PNEUMOCONIOSISOK Kiváltó okok: inert, anorganikus porbelégzés fémpor szabad szilikát szénpor 50

HYPERSENSITIV PNEUMONITIS Extrinsic allergiás alveolitis A tüdőparenchyma immunologiailag indukált gyulladása, mely az alveolus falat és a terminális légutakat érinti, organikus porok, vagy más ágensek ismételt belégzése után. Kórképek: Farmertüdő (1932) – thermophylus actinomycetes Madártenyésztők betegsége Molnár tüdő Bagassosis Byssinosis Kávémunkások betegsége Légkondicionáló betegség Paprikahasítók betegsége (1932, Kováts Ferenc) 51

Köszönöm a figyelmet! 52
- Slides: 52