Insulinetherapie bij diabetes mellitus type 2 Welke behandeldoelen

Insulinetherapie bij diabetes mellitus type 2 Welke behandeldoelen moeten we nastreven en welke therapeutische interventies passen daarbij?
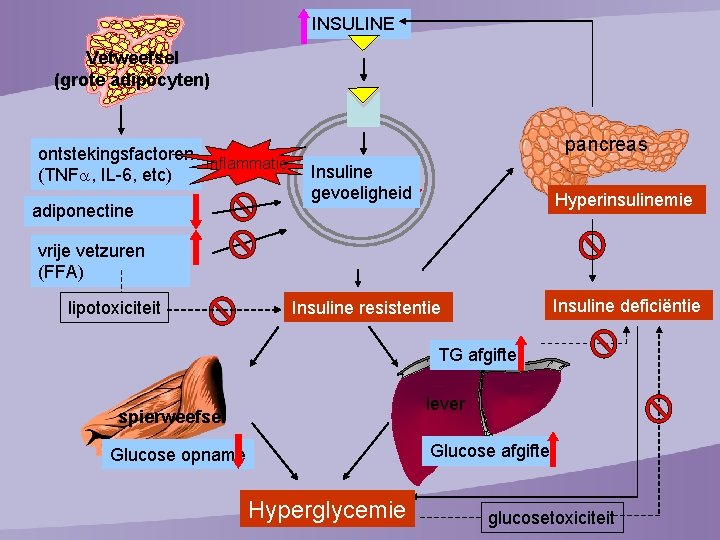
INSULINE Vetweefsel (grote adipocyten) ontstekingsfactoren inflammatie (TNF , IL-6, etc) adiponectine pancreas Insuline effect gevoeligheid Hyperinsulinemie Insuline resistentie Insuline deficiëntie vrije vetzuren (FFA) lipotoxiciteit TG afgifte lever spierweefsel Glucose afgifte Glucose opname Hyperglycemie glucosetoxiciteit
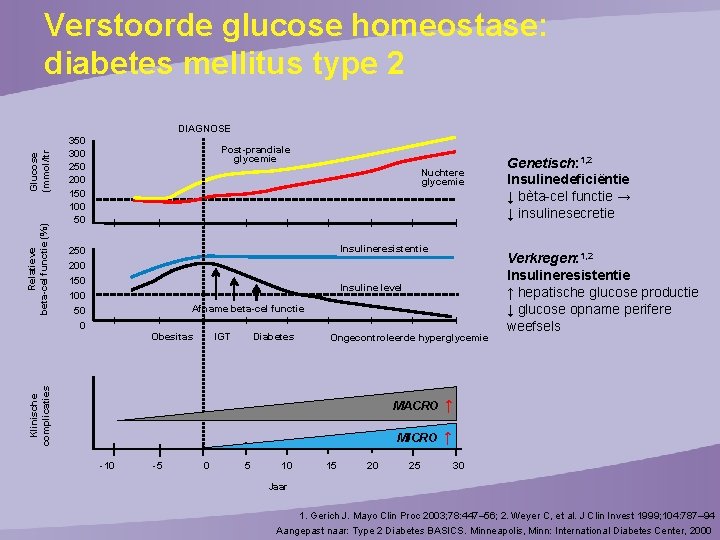
Verstoorde glucose homeostase: diabetes mellitus type 2 Relatieve beta-cel functie (%) Glucose (mmol/ltr DIAGNOSE 350 300 250 200 150 100 50 Post-prandiale glycemie Nuchtere glycemie Insulineresistentie 250 200 150 100 Insuline level Afname beta-cel functie 50 0 IGT Diabetes Ongecontroleerde hyperglycemie Klinische complicaties Obesitas -10 -5 0 5 10 15 20 MACRO ↑ MICRO ↑ 25 Genetisch: 1, 2 Insulinedeficiëntie ↓ bèta-cel functie → ↓ insulinesecretie Verkregen: 1, 2 Insulineresistentie ↑ hepatische glucose productie ↓ glucose opname perifere weefsels 30 Jaar 1. Gerich J. Mayo Clin Proc 2003; 78: 447– 56; 2. Weyer C, et al. J Clin Invest 1999; 104: 787– 94 Aangepast naar: Type 2 Diabetes BASICS. Minneapolis, Minn: International Diabetes Center, 2000

Intensieve behandeling: UKPDS Risicoreductie diabetes gerelateerde complicaties p=0, 0099 25% Microvasculair Retinopathie 21% p=0, 015 Albuminurie 33% Myocardinfarct 16% Diabetes gerelateerde eindpunten p=0, 052 12% 0 5 10 15 p=0, 000054 p=0, 029 20 25 30 35 Risicoreductie (%) UK Prospective Diabetes Study (UKPDS) Group. Lancet. 1998; 352: 837 -853.
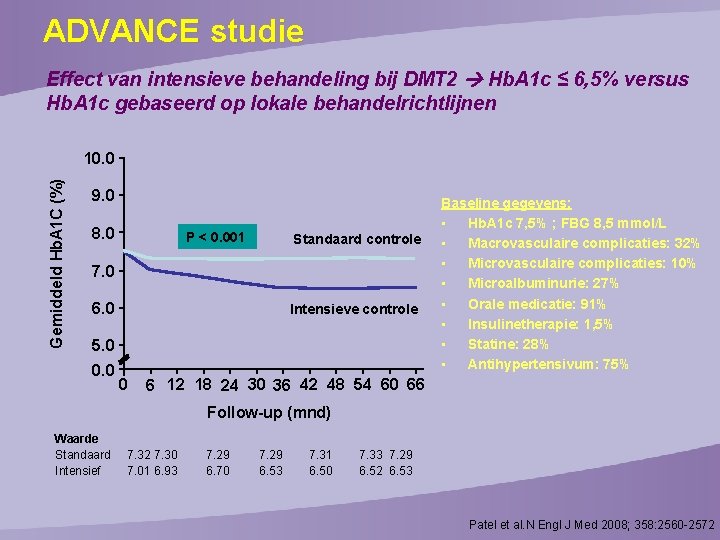
ADVANCE studie Effect van intensieve behandeling bij DMT 2 Hb. A 1 c ≤ 6, 5% versus Hb. A 1 c gebaseerd op lokale behandelrichtlijnen Gemiddeld Hb. A 1 C (%) 10. 0 9. 0 8. 0 P < 0. 001 Standaard controle 7. 0 6. 0 Intensieve controle 5. 0 0 Baseline gegevens: • Hb. A 1 c 7, 5% ; FBG 8, 5 mmol/L • Macrovasculaire complicaties: 32% • Microvasculaire complicaties: 10% • Microalbuminurie: 27% • Orale medicatie: 91% • Insulinetherapie: 1, 5% • Statine: 28% • Antihypertensivum: 75% 6 12 18 24 30 36 42 48 54 60 66 Follow-up (mnd) Waarde Standaard Intensief 7. 32 7. 30 7. 01 6. 93 7. 29 6. 70 7. 29 6. 53 7. 31 6. 50 7. 33 7. 29 6. 52 6. 53 Patel et al. N Engl J Med 2008; 358: 2560 -2572
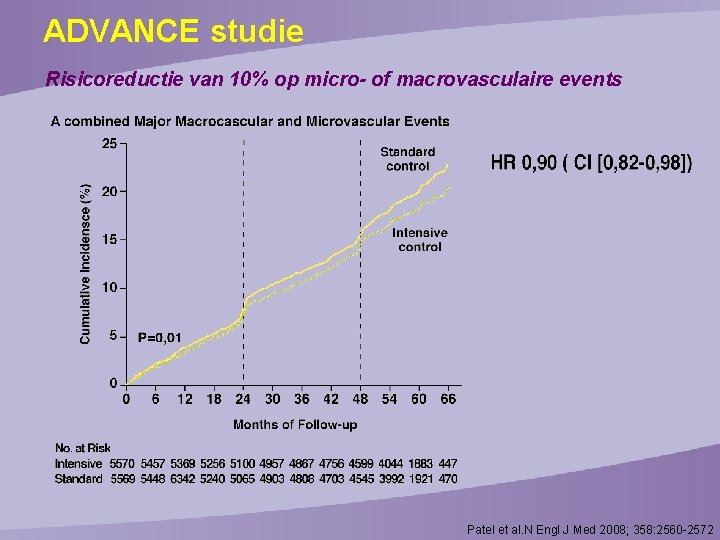
ADVANCE studie Risicoreductie van 10% op micro- of macrovasculaire events Patel et al. N Engl J Med 2008; 358: 2560 -2572
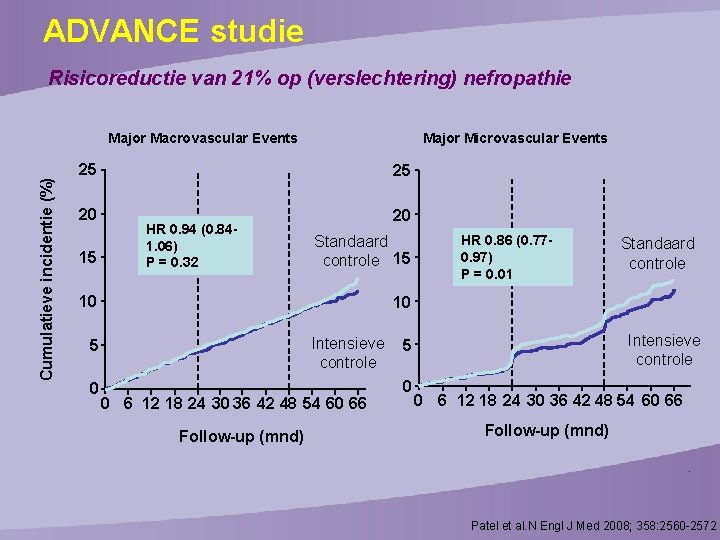
ADVANCE studie Risicoreductie van 21% op (verslechtering) nefropathie Cumulatieve incidentie (%) Major Macrovascular Events Major Microvascular Events 25 20 15 25 HR 0. 94 (0. 841. 06) P = 0. 32 20 Standaard controle 15 10 Standaard controle 10 Intensieve controle 5 0 HR 0. 86 (0. 770. 97) P = 0. 01 0 0 6 12 18 24 30 36 42 48 54 60 66 Follow-up (mnd) Intensieve controle 5 0 6 12 18 24 30 36 42 48 54 60 66 Follow-up (mnd). Patel et al. N Engl J Med 2008; 358: 2560 -2572

ADVANCE studie Risicoreductie met name bij patiënten zonder complicaties • Macrovasculaire events in voorgeschiedenis: – NEE relatieve risicoreductie 14% (CI [4 - 23]) – JA relatieve risicoreductie 4% (CI [-10 - 16]) • Microvasculaire events in voorgeschiedenis: – NEE relatieve risicoreductie 11% (CI [2 - 19]) – JA relatieve risicoreductie 4% (CI [-16 - 21]) Patel et al. N Engl J Med 2008; 358: 2560 -2572
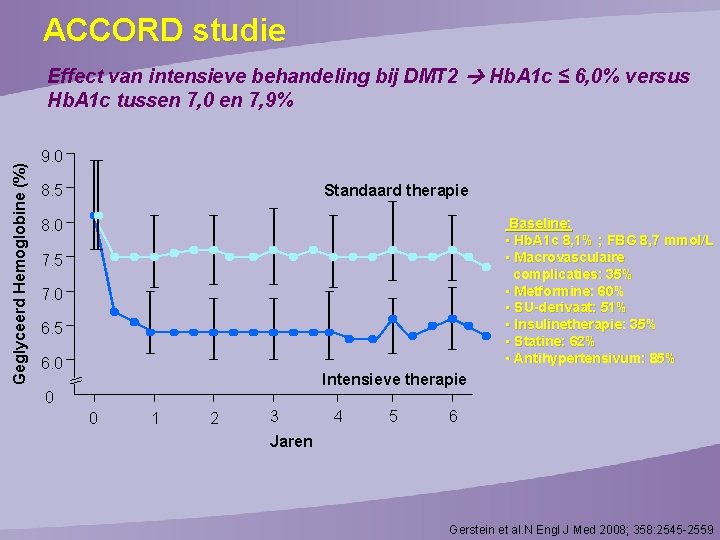
ACCORD studie Geglyceerd Hemoglobine (%) Effect van intensieve behandeling bij DMT 2 Hb. A 1 c ≤ 6, 0% versus Hb. A 1 c tussen 7, 0 en 7, 9% 9. 0 8. 5 Standaard therapie Basel i n e: • Hb A 1 c 8, 1% ; F BG 8, 7 mmo l / L • Ma c r o v a s c u l a i r e c o m p l i c a ti e s : 3 5 % • Me tfo r m i n e : 6 0 % • S U -d e r i v a a t: 5 1 % • I n s u l i n e th e r a p i e : 3 5 % • S ta ti n e : 6 2 % • A n ti h y p e r te n s i v u m : 8 5 % 8. 0 7. 5 7. 0 6. 5 6. 0 Intensieve therapie 0 0 1 2 3 4 5 6 Jaren Gerstein et al. N Engl J Med 2008; 358: 2545 -2559
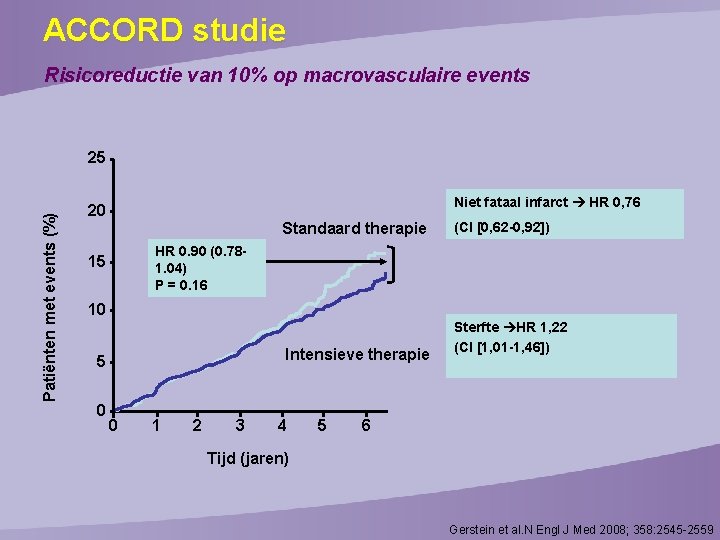
ACCORD studie Risicoreductie van 10% op macrovasculaire events Patiënten met events (%) 25 Niet fataal infarct HR 0, 76 20 Standaard therapie (CI [0, 62 -0, 92]) HR 0. 90 (0. 781. 04) P = 0. 16 15 10 Intensieve therapie 5 0 0 1 2 3 4 5 Sterfte HR 1, 22 (CI [1, 01 -1, 46]) 6 Tijd (jaren) Gerstein et al. N Engl J Med 2008; 358: 2545 -2559
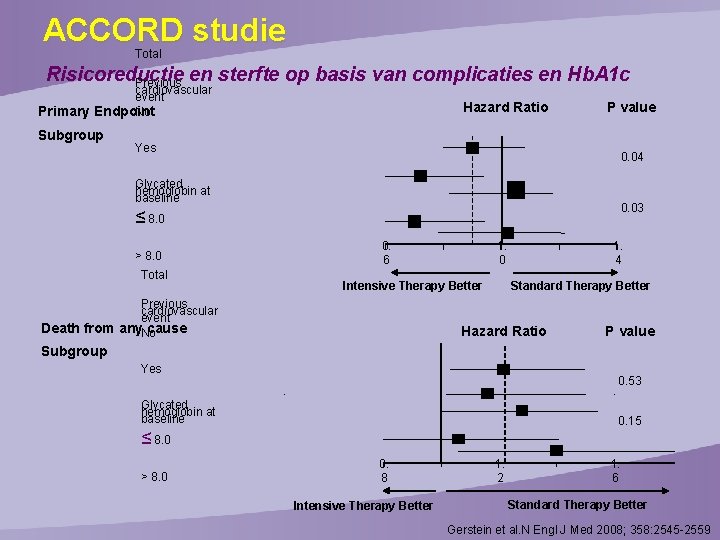
ACCORD studie Total Risicoreductie Previous en sterfte op basis van complicaties en Hb. A 1 c cardiovascular event No Primary Endpoint Subgroup Hazard Ratio P value Yes 0. 04 Glycated hemoglobin at baseline 0. 03 ≤ 8. 0 > 8. 0 Total 1. 0 0. 6 Intensive Therapy Better Previous cardiovascular event Death from any. No cause 1. 4 Standard Therapy Better Hazard Ratio P value Subgroup Yes 0. 53 Glycated hemoglobin at baseline 0. 15 ≤ 8. 0 > 8. 0 0. 8 Intensive Therapy Better 1. 2 1. 6 Standard Therapy Better Gerstein et al. N Engl J Med 2008; 358: 2545 -2559
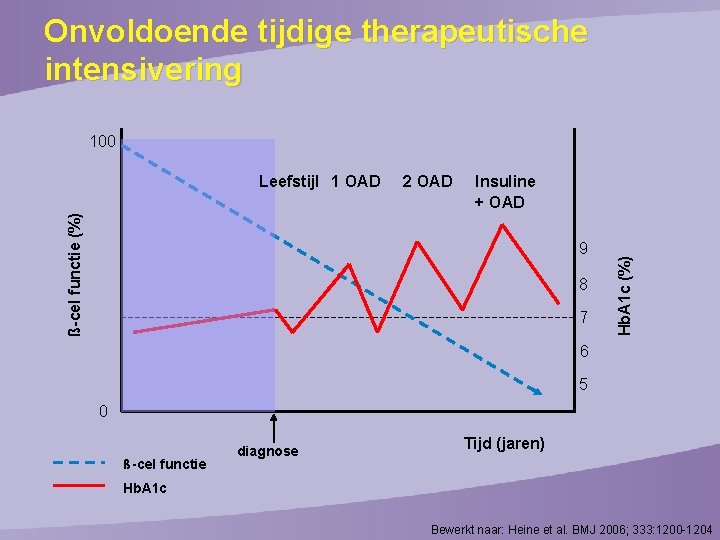
Onvoldoende tijdige therapeutische intensivering 100 Insuline + OAD 9 8 7 Hb. A 1 c (%) 2 OAD ß-cel functie (%) Leefstijl 1 OAD 6 5 0 ß-cel functie diagnose Tijd (jaren) Hb. A 1 c Bewerkt naar: Heine et al. BMJ 2006; 333: 1200 -1204
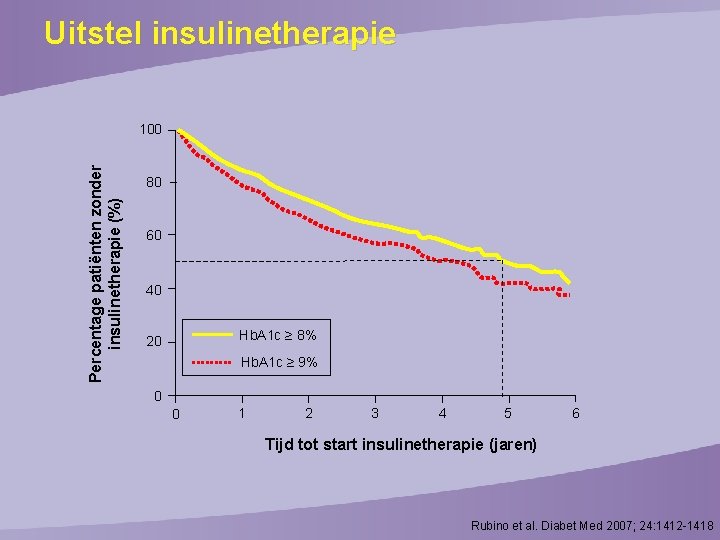
Uitstel insulinetherapie Percentage patiënten zonder insulinetherapie (%) 100 80 60 40 Hb. A 1 c ≥ 8% 20 Hb. A 1 c ≥ 9% 0 0 1 2 3 4 5 6 Tijd tot start insulinetherapie (jaren) Rubino et al. Diabet Med 2007; 24: 1412 -1418

Psychologische insulineresistentie • • Angst voor hypoglycemieën Angst voor meerdaags injecteren en controleren Angst voor injecteren hoge doseringen insuline Angst voor gewichtstoename Welk insulineregime geeft de beste glycemische controle verlaging Hb. A 1 c met zo min mogelijk bijwerkingen Korytkowski M. Int J Obes Metab Disord 2002; 26: S 18 -S 24 Peyrot M. et al. Diabetes Care 2005; 28: 2673 -2679
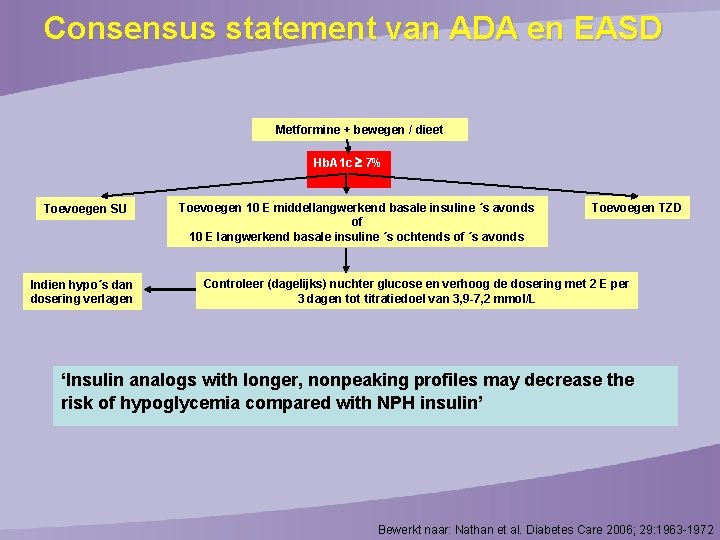
Consensus statement van ADA en EASD Metformine + bewegen / dieet Hb. A 1 c 7% Toevoegen SU Indien hypo´s dan dosering verlagen Toevoegen 10 E middellangwerkend basale insuline ´s avonds of 10 E langwerkend basale insuline ´s ochtends of ´s avonds Toevoegen TZD Controleer (dagelijks) nuchter glucose en verhoog de dosering met 2 E per 3 dagen tot titratiedoel van 3, 9 -7, 2 mmol/L ‘Insulin analogs with longer, nonpeaking profiles may decrease the risk of hypoglycemia compared with NPH insulin’ Bewerkt naar: Nathan et al. Diabetes Care 2006; 29: 1963 -1972
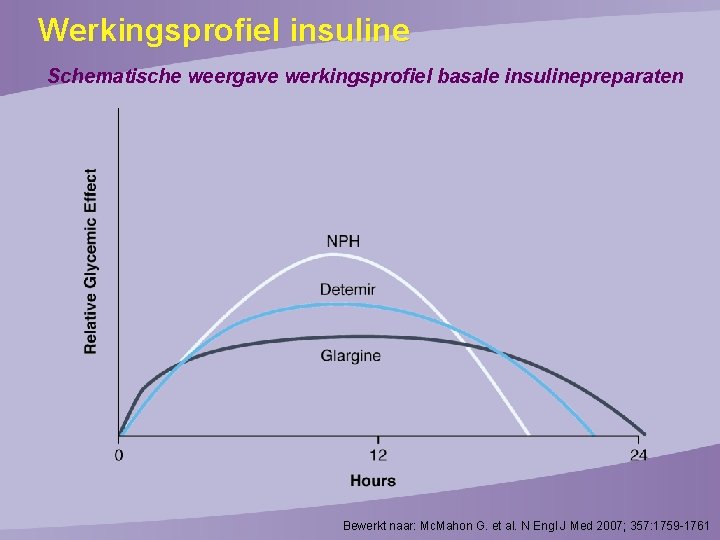
Werkingsprofiel insuline Schematische weergave werkingsprofiel basale insulinepreparaten Bewerkt naar: Mc. Mahon G. et al. N Engl J Med 2007; 357: 1759 -1761
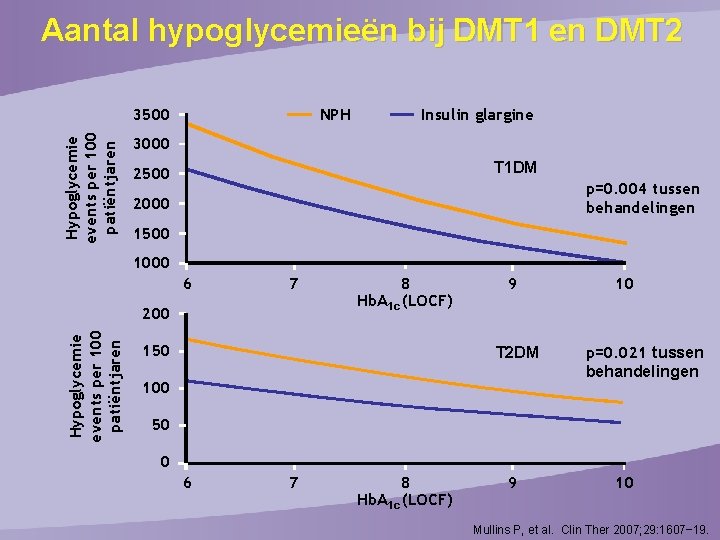
Aantal hypoglycemieën bij DMT 1 en DMT 2 Hypoglycemie events per 100 patiëntjaren 3500 NPH Insulin glargine 3000 T 1 DM 2500 p=0. 004 tussen behandelingen 2000 1500 1000 6 7 Hypoglycemie events per 100 patiëntjaren 200 8 Hb. A 1 c (LOCF) 150 9 T 2 DM 100 10 p=0. 021 tussen behandelingen 50 0 6 7 8 Hb. A 1 c (LOCF) 9 10 Mullins P, et al. Clin Ther 2007; 29: 1607− 19.

Psychologische insulineresistentie • • Angst voor hypoglycemieën Angst voor meerdaags injecteren en controleren Angst voor injecteren hoge doseringen insuline Angst voor gewichtstoename Korytkowski M. Int J Obes Metab Disord 2002; 26: S 18 -S 24 Peyrot M. et al. Diabetes Care 2005; 28: 2673 -2679
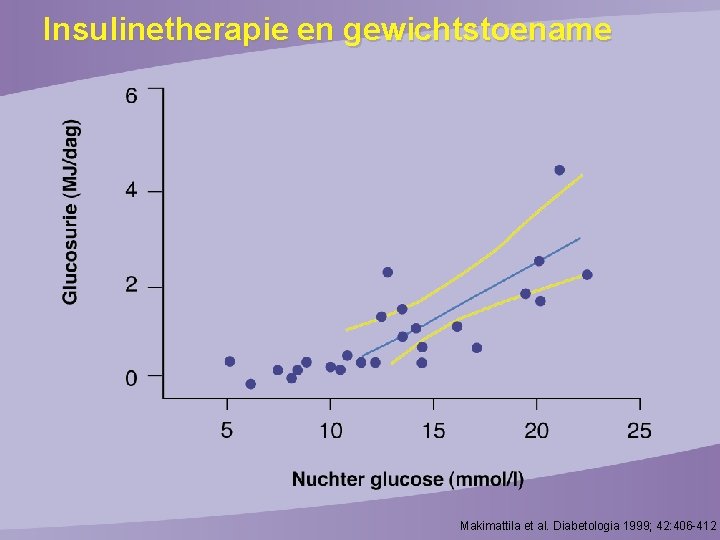
Insulinetherapie en gewichtstoename Makimattila et al. Diabetologia 1999; 42: 406 -412
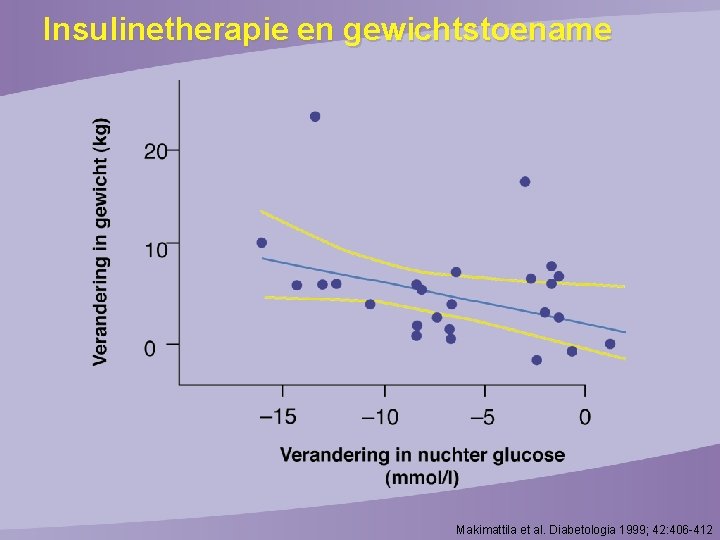
Insulinetherapie en gewichtstoename Makimattila et al. Diabetologia 1999; 42: 406 -412
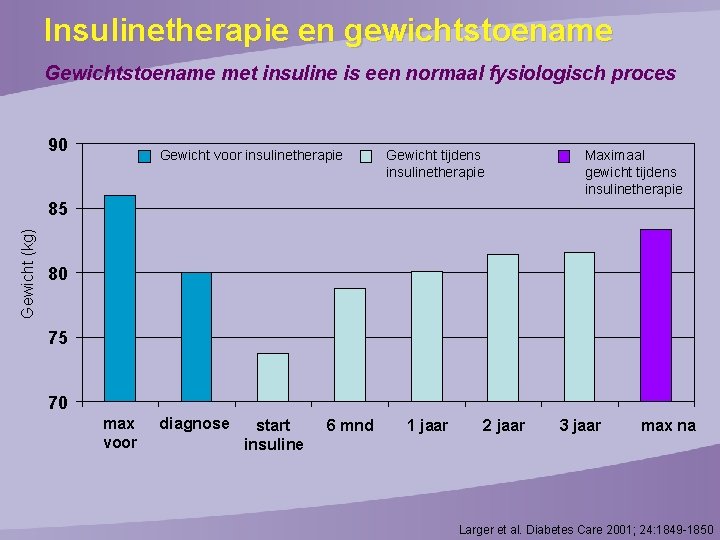
Insulinetherapie en gewichtstoename Gewichtstoename met insuline is een normaal fysiologisch proces 90 Gewicht voor insulinetherapie Gewicht tijdens insulinetherapie Maximaal gewicht tijdens insulinetherapie Gewicht (kg) 85 80 75 70 max voor diagnose start insuline 6 mnd 1 jaar 2 jaar 3 jaar max na Larger et al. Diabetes Care 2001; 24: 1849 -1850

A randomised, 52 week, treat-to-target trial comparing insuline detemir with insuline glargine when administered as add-on to glucose-lowering drugs in insuline-naive people with type 2 diabetes Rosenstock J. et al. Diabetologia 2008; 51: 408 -416
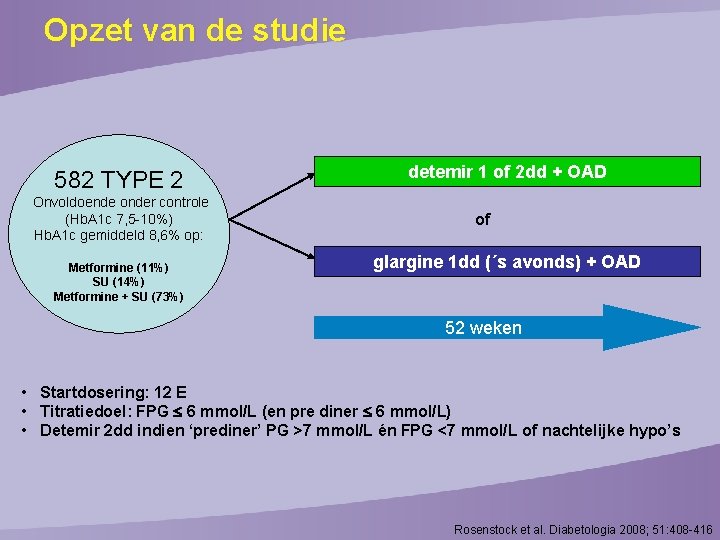
Opzet van de studie 582 TYPE 2 Onvoldoende onder controle (Hb. A 1 c 7, 5 -10%) Hb. A 1 c gemiddeld 8, 6% op: Metformine (11%) SU (14%) Metformine + SU (73%) detemir 1 of 2 dd + OAD of glargine 1 dd (´s avonds) + OAD 52 weken • Startdosering: 12 E • Titratiedoel: FPG 6 mmol/L (en pre diner 6 mmol/L) • Detemir 2 dd indien ‘prediner’ PG >7 mmol/L én FPG <7 mmol/L of nachtelijke hypo’s Rosenstock et al. Diabetologia 2008; 51: 408 -416
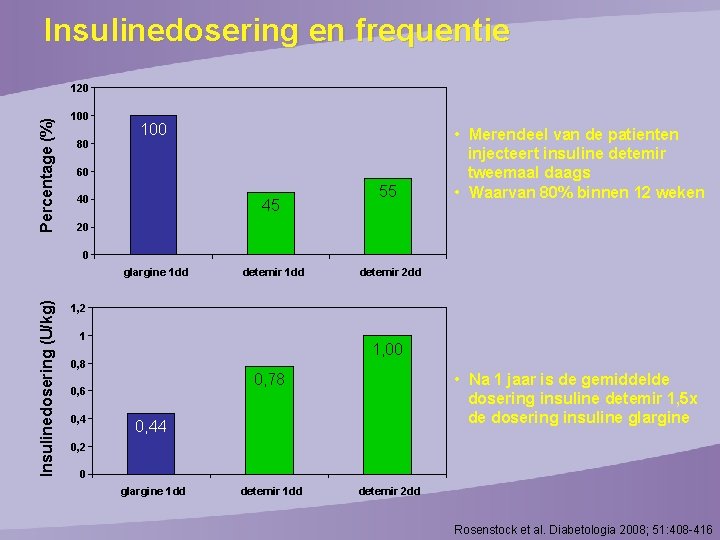
Insulinedosering en frequentie Percentage (%) 120 100 80 100 60 40 45 55 • Merendeel van de patienten injecteert insuline detemir tweemaal daags • Waarvan 80% binnen 12 weken 20 0 Insulinedosering (U/kg) glargine 1 dd detemir 2 dd 1, 2 1 1, 00 0, 8 0, 4 • Na 1 jaar is de gemiddelde dosering insuline detemir 1, 5 x de dosering insuline glargine 0, 78 0, 6 0, 44 0, 2 0 glargine 1 dd detemir 2 dd Rosenstock et al. Diabetologia 2008; 51: 408 -416
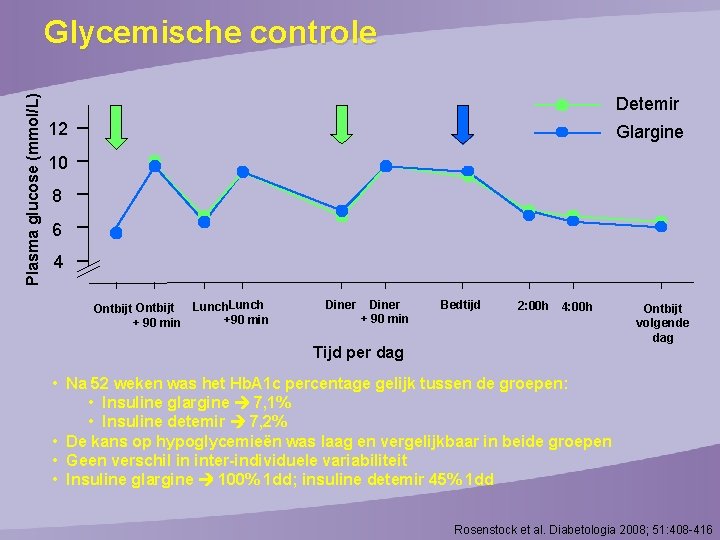
Plasma glucose (mmol/L) Glycemische controle Detemir 12 Glargine 10 8 6 4 Ontbijt Lunch +90 min + 90 min Diner + 90 min Bedtijd 2: 00 h 4: 00 h Tijd per dag Ontbijt volgende dag • Na 52 weken was het Hb. A 1 c percentage gelijk tussen de groepen: • Insuline glargine 7, 1% • Insuline detemir 7, 2% • De kans op hypoglycemieën was laag en vergelijkbaar in beide groepen • Geen verschil in inter-individuele variabiliteit • Insuline glargine 100% 1 dd; insuline detemir 45% 1 dd Rosenstock et al. Diabetologia 2008; 51: 408 -416
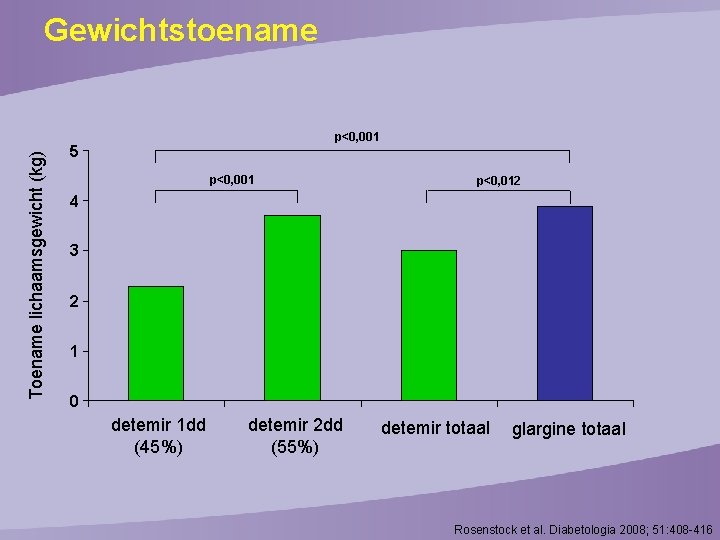
Toename lichaamsgewicht (kg) Gewichtstoename p<0, 001 5 p<0, 001 p<0, 012 4 3 2 1 0 detemir 1 dd (45%) detemir 2 dd (55%) detemir totaal glargine totaal Rosenstock et al. Diabetologia 2008; 51: 408 -416
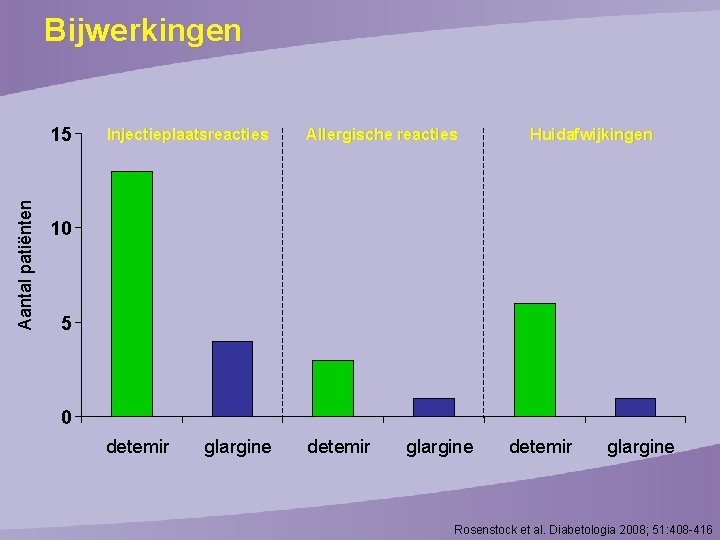
Bijwerkingen Aantal patiënten 15 I n j e c ti e p l a a ts r e a c ti e s A l l e r g i s c h e r e a c ti e s detemir H u i d a fw i j k i n g e n 10 5 0 glargine detemir glargine Rosenstock et al. Diabetologia 2008; 51: 408 -416
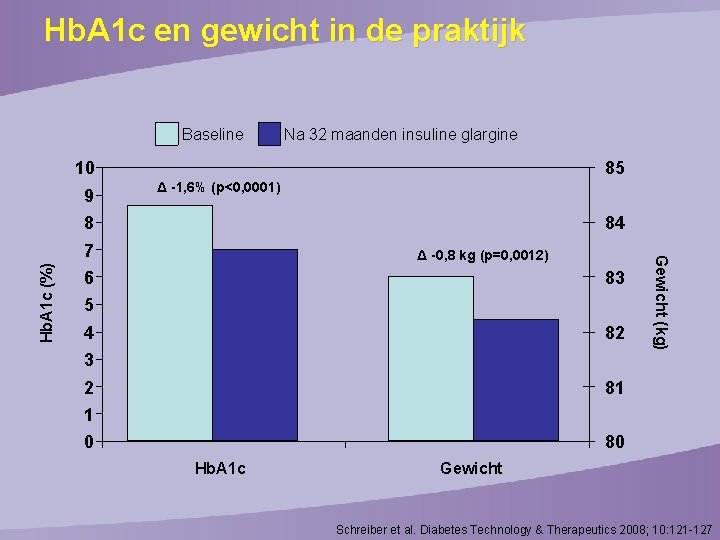
Hb. A 1 c en gewicht in de praktijk Baseline Na 32 maanden insuline glargine 10 9 85 Δ -1, 6% (p<0, 0001) 84 7 6 Δ -0, 8 kg (p=0, 0012) 83 5 4 3 82 2 1 81 0 80 Hb. A 1 c Gewicht (kg) Hb. A 1 c (%) 8 Gewicht Schreiber et al. Diabetes Technology & Therapeutics 2008; 10: 121 -127

Conclusies • Tijdig intensiveren van therapie is nodig om (het verslechteren van) micro- en macrovasculaire complicaties te helpen voorkomen • Bij patiënten met een verhoogd risico is het huidige behandeldoel (Hb. A 1 c < 7%) voldoende • Toevoegen van basale insuline met een lange werking, zonder pieken, wordt aanbevolen in de ADA/EASD behandelrichtlijnen • Gewichtstoename na start insulinetherapie is een normaal fysiologisch proces • Er bestaan geen grote verschillen in gewichtstoename tussen de basale insulineanalogen insuline glargine en insuline detemir • Insuline glargine en insuline detemir verschillen wel ten aanzien van benodigde insulinedosering en doseringsfrequentie
- Slides: 29