Inquinamento atmosferico Il termine inquinamento indica un degrado








































- Slides: 48

Inquinamento atmosferico Il termine “inquinamento” indica un degrado dell’ambiente per immissione di • sostanze (rifiuti, sottoprodotti di attività produttive ecc. ); • effetti (calore, rumore, vibrazioni ecc. ) che ne alterino le caratteristiche fisico-chimiche o biologiche. Le sostanze inquinanti possono essere solide, liquide, gassose o emettere radiazionizzanti.

Polveri (particolato) Il particolato (PM: Particulate Matter) è l’insieme di tutte le particelle microscopiche, solide o liquide, sospese nell'aria, esclusa l'acqua pura. Se ne misura la quantità in microgrammi per ogni metro cubo d’aria (µg/m 3). Può formarsi sia in seguito ad eventi naturali, come eruzioni vulcaniche o incendi boschivi, sia come conseguenza di attività umane (origine antropica). Le attività umane contribuiscono alla formazione del particolato sia in modo diretto (ad esempio, con le polveri prodotte durante uno scavo) sia in modo indiretto: in questo caso il particolato si forma per mezzo di reazioni chimiche coinvolgono altri inquinanti, come i composti organici volatili COV (idrocarburi a basso peso molecolare, alcoli, ecc. ), gli ossidi di azoto NOx e l’anidride solforosa SO 2. Si parlerà nel primo caso di particolato primario e nel secondo di particolato secondario.

Sorgenti del particolato naturale particolato primario • • • eruzioni vulcaniche tempeste di sabbia incendi boschivi emissione di spore pollini antropico • combustioni (per autotrazione, riscaldamento, produzione di energia) • usura (ad esempio da attrito tra asfalto e pneumatici) • processi industriali (cementifici, fonderie ecc. ) • movimentazione di terra (attività agricole, scavi, ecc. ) particolato secondario da reazione di ossidazione di varie sostanze: • H 2 S e SO 2 (attività vulcanica, incendi) • ossidi di azoto (dai terreni) • terpeni (dai vegetali) da ossidazione di idrocarburi, ossidi di zolfo, ossidi di azoto prodotti nelle attività umane

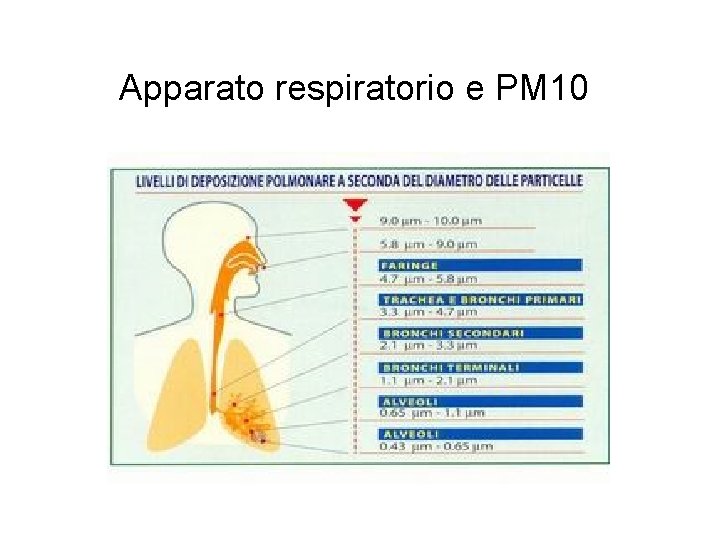
La sigla PM 10 indica le particelle con Ømedio ≤ 10 µm (a titolo di confronto: il diametro medio di un capello umano è circa 50 µm). Quelle più grandi si depositano al suolo in tempi relativamente brevi (dell’ordine dei giorni). La sigla PM 2, 5 indica le particelle con un Ømedio ≤ 2, 5 µm: costituiscono il maggiore pericolo per la salute perché possono rimanere in sospensione nell’atmosfera anche per settimane. E’ evidente che le particelle costituenti il PM 2, 5 fanno parte anche della frazione PM 10 Effetti del particolato sulla salute In relazione agli effetti sulla salute il PM 2, 5 è più importante del PM 10 perché particelle più piccole possono arrivare fino agli alveoli polmonari con l’aria inspirata. Per questo se un elevato valore del PM 10 corrisponde alla presenza di poche particelle del tipo PM 2, 5 e molte di dimensioni maggiori la situazione è più accettabile rispetto ad un PM 10 di valore inferiore con poche particelle grossolane e molte PM 2, 5.

Apparato respiratorio e PM 10

La nocività è in parte dovuta all'azione diretta sulla mucosa dell'albero respiratorio e sugli alveoli, in parte è indiretta e conseguente a gas assorbiti (SO 2) e/o particelle adsorbite sulla superficie del particolato (essenzialmente metalli pesanti tossici, come il piombo, e idrocarburi policiclici aromatici). L'aumento della concentrazione atmosferica di polveri determina un aumento della morbosità (quindi dei ricoveri ospedalieri) e della mortalità prevalentemente per disturbi dell'apparato respiratorio. Dal 1 febbraio 2010 la Commissione Europea ha fissato i seguenti limiti: • • • valore massimo per la media annuale: 20 µg/m 3 valore massimo giornaliero: 50 µg/m 3 numero massimo di sforamenti in un anno: 7 Gli Stati membri hanno di regola due anni di tempo per adeguare le loro normative alle direttive.

Ozono - O 3 Forma allotropica dell’ossigeno, gassoso (p. e. – 112 °C), è instabile (può esplodere allo stato liquido) e molto più reattivo dell’ossigeno O 2. I suoi effetti sono molto diversi a seconda della sua “collocazione” nell’atmosfera: • al suolo: è irritante (occhi, apparato respiratorio); partecipa alla formazione dello smog (da smoke e fog); • nella stratosfera: assorbe le radiazioni UV di alta energia (200 -300 nm di lunghezza d’onda). E’ quindi evidente che la sua presenza in stratosfera è indispensabile per la vita sul pianeta, mentre al suolo è dannoso per la salute. Si produce per mezzo di scariche elettriche (15 -25 k. V a 50 -500 Hz) su ossigeno o aria. La resa non è molto elevata. L’ozono puro, ottenuto raffreddando la miscela di gas a – 120 °C, viene stabilizzato adsorbendolo su gel di silice. O 2 + energia ———› O 2٠ (attivato) ———› 2 O O + O 2 ———› O 3

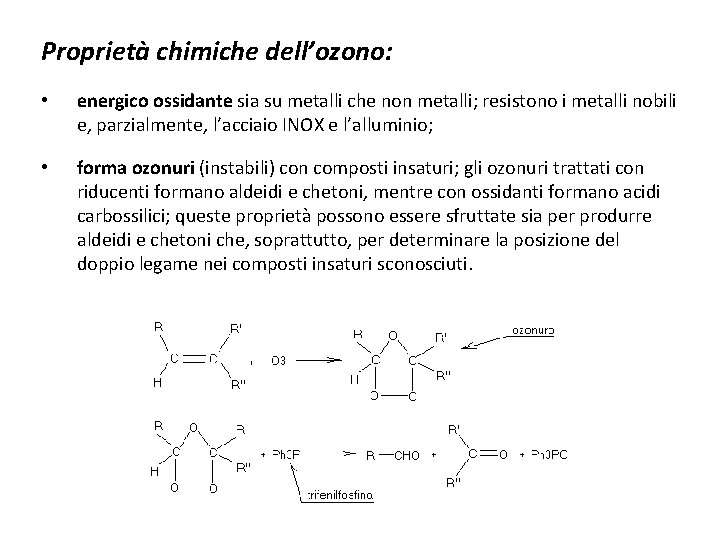
Proprietà chimiche dell’ozono: • energico ossidante sia su metalli che non metalli; resistono i metalli nobili e, parzialmente, l’acciaio INOX e l’alluminio; • forma ozonuri (instabili) con composti insaturi; gli ozonuri trattati con riducenti formano aldeidi e chetoni, mentre con ossidanti formano acidi carbossilici; queste proprietà possono essere sfruttate sia per produrre aldeidi e chetoni che, soprattutto, per determinare la posizione del doppio legame nei composti insaturi sconosciuti.

L’ozono nell’atmosfera • Nella stratosfera (tra i 15 e i 60 km di quota) si forma per azione della luce UV di alta energia (l < 180 nm) su O 2. La quantità complessiva in condizioni normali rimane pressoché costante perché assorbe UV trasformandosi in O 2 e O atomico, che si ricombinano formando ancora ozono. O 3 + hn <=====> O 2 + O La concentrazione dell’ozono nell’atmosfera si misura in cm*km-1: spessore a c. n. dello strato di ozono, puro, contenuto in uno strato di atmosfera alto 1 km. La concentrazione è massima a circa 15 km di quota (2 x 10 -2 cmxkm-1). Il continuo assorbimento di luce UV produce un riscaldamento della stratosfera, la cui temperatura raggiunge un massimo a circa 50 km di quota. • Nella troposfera (quota minore di 15 km) è un pericoloso inquinante. Si forma per azione della luce UV su NOx (ossidi di azoto) e COV.

Distruzione dello strato di ozono nella stratosfera Avviene per mezzo di diversi cicli di reazioni la cui rilevanza dipende dalla quota: a) ciclo degli ossidrili (quota maggiore di 50 km): H + O 2 ———› HO 2 + O ———› OH + O 2 OH + O 3 ———› HO 2 + O 2 b) ciclo dei composti del cloro (da CFC) (quota compresa tra 30 e 50 km): Cl + O 3 ———› Cl. O + O 2 Cl. O + O ———› Cl + O 2 c) ciclo degli NOx (quota compresa tra 20 e 30 km): NO + O 3 ———› NO 2 + O 2 NO 2 + O ———› NO + O 2 NO 2 + NO ———› 2 NO + O I cicli b e c sono ritenuti più importanti. In generale, comunque, avvengono reazioni radicaliche molto complesse su cui influiscono diversi fattori.

Valori limite di esposizione all’ozono AMBIENTE ESTERNO In Italia sono in vigore : • 110 µg/m 3 concentrazione media su 8 ore per la protezione della salute umana • 180 µg/m 3 concentrazione oraria di "attenzione“ • 200 µg/m 3 concentrazione oraria da non raggiungere più di una volta al mese • 360 µg/m 3 concentrazione oraria di " allarme" AMBIENTE DI LAVORO (ACGIH-USA : Associazione degli Igienisti Industriali Americani) • 200 µg/m 3 TLV-Ceiling concentrazione da non superarsi neppure per brevissimi periodi, 15' o di meno • 100 µg/m 3 TLV-TWA concentrazione media sulle 8 ore lavorative (valore proposto) • 400 µg/m 3 TLV- STEL concentrazione consentita per non più di 15' in 8 ore lavorative (valore proposto)

• TLV – Threshold Limit Value (valore limite di soglia): livello fissato in base alle conoscenze scientifiche, incluse quelle relative alle migliori tecnologie disponibili, al fine di evitare, prevenire o ridurre gli effetti nocivi per la salute umana o per l’ambiente nel suo complesso, che deve essere raggiunto entro un limite prestabilito e che non deve essere successivamente superato. • TLV-C (ceiling): concentrazione che non deve essere superata durante qualsiasi momento dell'esposizione lavorativa. • TLV-TWA (time-weightened average): concentrazione limite, calcolata come media ponderata nel tempo (8 ore/giorno; 40 ore settimanali), al di sotto della quale tutti i lavoratori possono essere esposti, giorno dopo giorno senza effetti avversi per la salute per tutta la vita lavorativa. • TLV- STEL (short-term exposure limit): è il valore massimo consentito per esposizioni brevi (non oltre 15 minuti) ed occasionali (non oltre quattro esposizioni nelle 24 ore, intervallate almeno ad un'ora di distanza l'una dall'altra).

Effetti dell’ozono sulla salute • esplica un’azione irritante sulle mucose, in particolare delle vie respiratorie: – Si concentra prevalentemente nei tessuti della parte terminale dell'albero respiratorio tra bronchioli e alveoli, ove esercita una forte azione ossidante, aumentando la frequenza degli attacchi asmatici e dei disturbi respiratori, soprattutto nei soggetti più sensibili (bambini, anziani, soggetti affetti da malattie croniche dell’apparato respiratorio); – passa nel sangue solo in minima quantità; • potenzia gli effetti nocivi di altri inquinanti atmosferici, in particolare idrocarburi, polveri, piombo e biossido di azoto; • svolge un ruolo importante nello smog fotochimico. Cosa si può fare per difendersi? • • stare all’aperto d’estate possibilmente solo nelle ore del primo mattino o del tardo pomeriggio, specialmente se si pratica intensa attività fisica. seguire una dieta ricca di vitamina C (agrumi, frutta in genere, pomodori, peperoni, verdure fresche, patate), vitamina E (germogli di grano, oli di soia e di mais crudi, olio di fegato di merluzzo) e selenio (pesce e crusca).

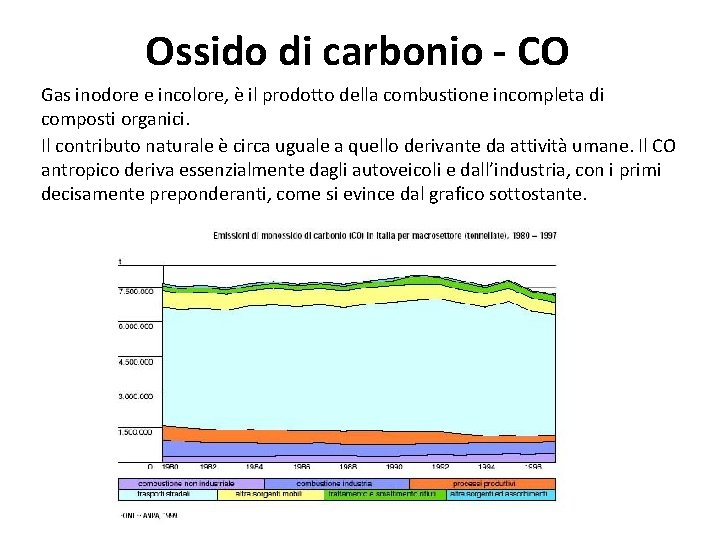
Ossido di carbonio - CO Gas inodore e incolore, è il prodotto della combustione incompleta di composti organici. Il contributo naturale è circa uguale a quello derivante da attività umane. Il CO antropico deriva essenzialmente dagli autoveicoli e dall’industria, con i primi decisamente preponderanti, come si evince dal grafico sottostante.

La produzione di CO è più elevata nei motori a benzina, in particolare con il motore al minimo. Nei motori Diesel la combustione è più efficiente (minori emissioni di CO), ma è più grande la formazione di particolato. Per ridurre la quantità di CO rilasciato nell’atmosfera dalle auto oggi si usano le marmitte catalitiche, che portano a compimento l’ossidazione dell’ossido di carbonio ad anidride carbonica ed eliminano anche gli ossidi di azoto (→ N 2) e gli idrocarburi incombusti (→ CO 2 + H 2 O). Le fonti industriali di CO sono gli impianti siderurgici (riduzione del materiale ferroso con coke, riduzione del contenuto in carbonio) e petrolchimici. L’emissione industriale di CO per incompleta combustione è in generale ridotta. Nell’industria le combustioni sono utilizzate per produrre energia, quindi si tende ad ottimizzarle per evitare un costo inutile. Comunque una cattiva manutenzione degli impianti può determinare emissioni di questo inquinante. La concentrazione di CO varia da circa 120 ppb (ppb = parti per miliardo) in atmosfera non inquinata a 1 10 ppm (ppm = parti per milione) in aree fortemente urbanizzate.

Effetti dell’ossido di carbonio sulla salute L’ossido di carbonio si lega all’emoglobina molto più fortemente dell’ossigeno formando carbossiemoglobina. Per questo motivo l’ossido di carbonio: → provoca la morte in circa 90 minuti concentrazioni di 1000 ppm → a 100 ppm di esposizione per diverse ore provoca vertigini, cefalea e senso di spossatezza, che possono essere seguiti da collasso → provoca danni (anche permanenti) per esposizione prolungata a concentrazioni di 50 ppm → in seguito ad esposizione prolungata a basse concentrazioni provoca intossicazione che si manifesta con disturbi nervosi e respiratori. La percentuale di carbossiemoglobina nel sangue può variare dal 6% in fumatori moderati, sino al 10% in accaniti fumatori di sigarette che siano esposti anche ad una concentrazione esterna di CO di circa 40 ppm per 1 ora, condizioni che in un non fumatore determinano un aumento di carbossiemoglobina da 1, 6 al 2, 6%.

Interventi in caso di intossicazione da CO Il CO ha un’affinità per l’emoglobina circa 200 volte maggiore dell’ossigeno. Per questo motivo è necessario sottoporre l’intossicato ad elevate concentrazioni di ossigeno per decomporre la carbossiemoglobina a favore della formazione dell’ossiemoglobina. Valori limite di esposizione all’ossido di carbonio Dal 30 settembre 2010 è entrato in vigore il Decreto Legislativo n. 155 del 13 agosto 2010 che va ad abrogare norme precedenti in ottemperanza della Direttiva Europea 2008/50/CE. Per quanto riguarda l’ambiente il valore limite è fissato a 10 mg/m 3 (d’aria). Per i lavoratori esposti al CO il TLV-TWA è di 25 ppm, pari a 29 mg/m 3 (limite indicato dall’ACGIH).

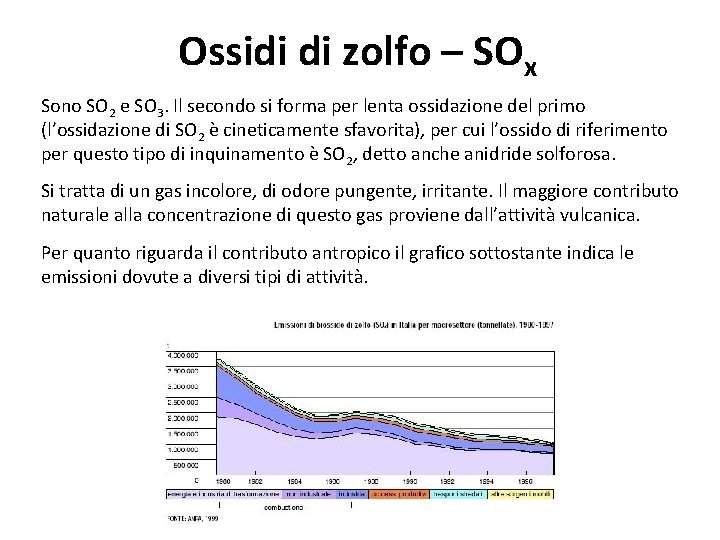
Ossidi di zolfo – SOx Sono SO 2 e SO 3. Il secondo si forma per lenta ossidazione del primo (l’ossidazione di SO 2 è cineticamente sfavorita), per cui l’ossido di riferimento per questo tipo di inquinamento è SO 2, detto anche anidride solforosa. Si tratta di un gas incolore, di odore pungente, irritante. Il maggiore contributo naturale alla concentrazione di questo gas proviene dall’attività vulcanica. Per quanto riguarda il contributo antropico il grafico sottostante indica le emissioni dovute a diversi tipi di attività.

Il grosso delle emissioni degli ossidi di zolfo proviene dalle combustioni industriali dato che tutti i combustibili contengono zolfo. Il biossido di zolfo in Italia deriva approssimativamente per il 5% dal riscaldamento domestico, per il 40% dai processi industriali (comprese le combustioni) e per il 50% dalla produzione di energia elettrica ad opera delle centrali termoelettriche; tutte assieme le altre sorgenti contribuiscono per il 5% circa. A fronte di una concentrazione in zone non inquinate di meno di 0, 5 mg/m 3 di SO 2, nelle città si raggiungono facilmente i 50 mg/m 3 per arrivare nelle grandi città industriali a 300 mg/m 3 (OMS, 1998). Oggi la situazione è migliorata sia per l’uso di combustibili per autotrazione a basso tenore di zolfo sia per una sempre più estesa metanizzazione degli impianti di riscaldamento. Normalmente la presenza di questo inquinante negli ambienti chiusi è molto ridotta. Non a caso la principale contromisura in caso di inquinamento grave (o comunque superiore alla soglia limite fissata per legge) è restare chiusi in casa, precauzione particolarmente necessaria per i bambini, per le persone anziane e/o affette da patologie dell’apparato respiratorio.

Effetti degli SOx sulla salute La pericolosità degli ossidi di zolfo deriva essenzialmente dalla loro elevata reattività e solubilità in acqua e dalle loro proprietà irritanti. Sia il diossido che il triossido formano con acqua i corrispondenti acidi (solforoso e solforico). Gli effetti dell’esposizione prolungata a dosaggi relativamente bassi di SO 2 dipendono dalle concentrazioni : → 0, 06 mg/m 3 (valore medio annuale) provocano un aumento delle malattie delle prime vie respiratorie → da 0, 3 mg/m 3 si osserva un aumento statistico dei ricoveri ospedalieri L’esposizione a concentrazioni più massicce (si tenga presente che quando si percepisce l’odore della SO 2 la concentrazione è già tale da richiedere l’uso di una maschera antigas) ha effetti pesanti: → 3 mg/m 3 provocano broncospasmo in soggetti predisposti, tachicardia e aumento del ritmo respiratorio anche per brevi esposizioni → concentrazioni maggiori di 5 g/m 3 sono mortali.

Effetti sull’ambiente La SO 2 produce danni rilevanti sia per la sua tossicità che per l’acidificazione delle acque e del suolo. La figura mostra la distruzione della clorofilla dovuta all’esposizione alla SO 2. L’azione della SO 2 sulle piante è potenziata da umidità e temperatura elevate, luce intensa e dalla presenza di altri inquinanti, come l’ozono. L’acidificazione del suolo comporta perdita di sali e un generale impoverimento che coinvolge anche i batteri capaci di fissare l’azoto atmosferico, indispensabili per la sopravvivenza delle piante. Anche la vita acquatica è fortemente danneggiata. Le acque acidificate uccidono svariate specie acquatiche superiori sia direttamente sia eliminando organismi vegetali e animali facenti parte della catena alimentare.

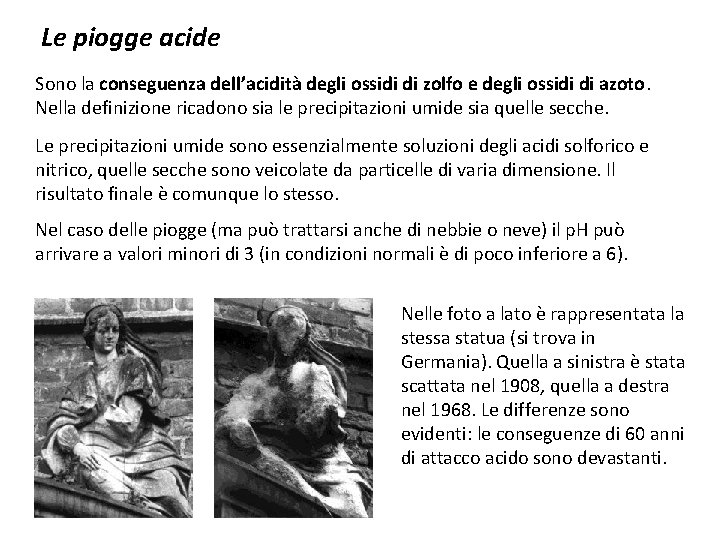
Le piogge acide Sono la conseguenza dell’acidità degli ossidi di zolfo e degli ossidi di azoto. Nella definizione ricadono sia le precipitazioni umide sia quelle secche. Le precipitazioni umide sono essenzialmente soluzioni degli acidi solforico e nitrico, quelle secche sono veicolate da particelle di varia dimensione. Il risultato finale è comunque lo stesso. Nel caso delle piogge (ma può trattarsi anche di nebbie o neve) il p. H può arrivare a valori minori di 3 (in condizioni normali è di poco inferiore a 6). Nelle foto a lato è rappresentata la stessa statua (si trova in Germania). Quella a sinistra è stata scattata nel 1908, quella a destra nel 1968. Le differenze sono evidenti: le conseguenze di 60 anni di attacco acido sono devastanti.

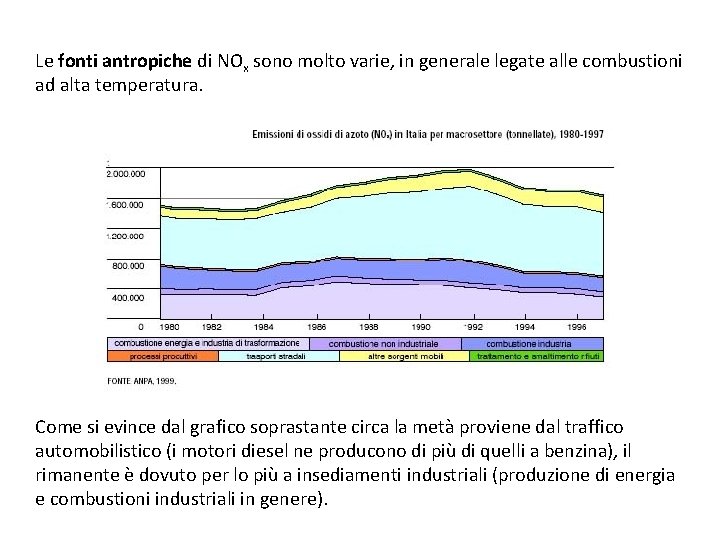
Ossidi di azoto - NOx La formula NOx indica la media pesata di NO e NO 2, gli ossidi di azoto di gran lunga più importanti in relazione alla qualità dell’aria. NO (ossido di azoto) è un gas incolore, inodore e insapore. Poco tossico, si trasforma in NO 2 per azione di O 2 e O 3. NO 2 (diossido di azoto o ipoazotide), molto più tossico di NO, è un gas rossastro, di odore pungente, irritante, corrosivo, ossidante. Gli NOx partecipano con SO 2 alla formazione delle piogge acide e svolgono un ruolo fondamentale nella formazione dello smog fotochimico. I contributi naturali e antropici alla formazione di NOx sono all’incirca uguali. La principale fonte naturale sono le decomposizioni anaerobiche di sostanze organiche (riduzione di nitrati a nitriti, trasformazione dei nitriti in acido nitroso che, instabile, dismuta in NO e NO 2).

Le fonti antropiche di NOx sono molto varie, in generale legate alle combustioni ad alta temperatura. Come si evince dal grafico soprastante circa la metà proviene dal traffico automobilistico (i motori diesel ne producono di più di quelli a benzina), il rimanente è dovuto per lo più a insediamenti industriali (produzione di energia e combustioni industriali in genere).

La concentrazione naturale di NO è in genere compresa tra 0, 2 e 10 mg/m 3. In aria inquinata si possono superare i 900 mg/m 3. Per NO 2 la concentrazione naturale è compresa tra 1 e 9 mg/m 3, mentre in città non si supera in genere i 40 mg/m 3. Dato che per formazioni non continuative degli NOx (ad esempio, in una cucina per effetto dell’uso dei fornelli a gas) la loro concentrazione diminuisce abbastanza rapidamente, i maggiori problemi si hanno quando la produzione di questi inquinanti è protratta nel tempo. In questo caso i danni per la salute derivano sia dall’azione tossica diretta del diossido di azoto sia dalla serie di reazioni che portano alla formazione dello smog fotochimico. Per quanto riguarda gli ambienti di lavoro la maggiore esposizione agli NOx si verifica durante le saldature ad arco elettrico e in molti impianti chimici (ad esempio, nell’industria galvanica) in cui si utilizza l’acido nitrico. I limiti di sicurezza per NO 2 sono 5, 6 mg/m 3 (TLV-TWA) e 9, 4 mg/m 3 (TLV-STEL), mentre per NO è raccomandato un TLV-TWA di 31 mg/m 3.

Effetti degli NOx sulla salute NO 2 esplica un’azione irritante che contribuisce all’insorgenza di vari tipi di affezioni polmonari. Anche a basse concentrazioni l’esposizione prolungata deprime le difese polmonari. L’OMS indica come limite orario 200 mg/m 3 e come limite per la media annuale 40 mg/m 3. NO non manifesta un’azione tossica importante, ma svolge un ruolo in diversi ambiti: Ø è accertato il ruolo di NO nell’attivazione di un enzima coinvolto nel rilassamento della muscolatura liscia; Ø prodotto dall’endotelio vascolare permette di mantenere un’attività vasodilatatrice importante per la regolazione del flusso ematico e della pressione arteriosa; Ø ha effetto anche sulla contrattilità del muscolo cardiaco e come neurotrasmettitore; Ø studi recenti descrivono il coinvolgimento di NO nella patogenesi di molte malattie, come cirrosi epatica, infarto del miocardio e morbo di Parkinson.

Composti organici volatili - COV Sono composti ad alta tensione di vapore. Si tratta di idrocarburi, chetoni, aldeidi, alcoli, acidi, esteri, terpeni. Questi ultimi, abbondanti nel regno vegetale, costituiscono molte essenze di uso comune in profumeria. Il contributo naturale e quello antropico alla presenza di COV in atmosfera sono quasi uguali. Nell’atmosfera entrano nel meccanismo di formazione dello smog fotochimico. Tra gli idrocarburi ricordiamo il benzene. Effetti sull’ambiente Sono coinvolti nel meccanismo di formazione dello smog fotochimico. Effetti sulla salute I COV aromatici sono cancerogeni. Tra essi il benzene è il più diffuso: entra in innumerevoli produzioni industriali e costituisce circa l’ 1 % della benzina verde.

Idrocarburi policiclici aromatici Questi composti, spesso indicati con la sigla IPA, sono idrocarburi caratterizzati da anelli aromatici condensati. In prevalenza sono di origine antropica dato che si formano in seguito a combustione incompleta di idrocarburi. Chimicamente sono piuttosto stabili. In atmosfera condensano e vengono adsorbiti su particelle carboniose (nerofumo). Per questo sono veicolati dalle polveri sottili. Effetti sulla salute Quelli più pericolosi per la salute sono costituiti da quattro o più anelli condensati. Tra questi molto noto è il benzo[a]pirene, uno dei primi inquinanti classificati come cancerogeni e l’unico monitorato per legge in Italia (ma gli IPA classificati come cancerogeni sono ben sette). In associazione con CO e altri inquinanti provocano il blocco della catena respiratoria. Benzo[a]pirene

Diossine Sono una serie di composti organici clorurati a struttura triciclica, il più noto dei quali è il 2, 3, 7, 8 -tetraclorodibenzo-p-diossina, noto semplicemente come diossina, di formula C 12 H 4 Cl 4 O 2. Questi composti possono formarsi nel processo di preparazione del triclorofenolo, intermedio nella produzione di erbicidi e antibatterici, quando la temperatura sale a livelli troppo alti. Le diossine possono prodursi anche in seguito all’incenerimento di materie plastiche clorurate, come il PVC, o non clorurate se in presenza di cloro. Effetti sulla salute Le diossine sono cancerogene e probabilmente mutagene. Provocano danni al cuore, ai reni, al fegato, allo stomaco e agli organi e tessuti linfatici e la dermatite nota come cloracne.

Radon - Rn Il radon, gas nobile incolore, è radioattivo e a sua volta prodotto del decadimento di tre nuclidi capostipiti che danno luogo a tre diverse famiglie radioattive: 232 Th, 235 U e 238 U. Nella tabella a lato e' riportata la sequenza del decadimento del nuclide più abbondante in natura, 238 U, responsabile della produzione dell'isotopo 222 Rn, anch’esso quindi più abbondante degli altri isotopi naturali del radon, anche in virtù della sua emivita di 3, 82 giorni: 220 Rn e 219 Rn (prodotti rispettivamente da 232 Th e 235 U) hanno emivite inferiori al minuto. Dato che l’uranio è presente quasi ovunque nella crosta terrestre, il gas radon è largamente diffuso sia nel terreno che nei materiali da costruzione. Isotopo Radiazione Emivita Uranio 238 alfa 4. 5 x 109 anni Torio 234 Beta 24. 1 giorni Protoattinio 234 Beta 1. 2 minuti Uranio 234 alfa 2. 5 x 105 anni Torio 230 alfa 7. 5 x 104 anni Radio 226 alfa 1600 anni Radon 222 alfa 3. 8 giorni Polonio 218 alfa 3 minuti Piombo 214 beta 27 minuti Bismuto 214 alfa e beta 20 minuti Polonio 214 alfa 1. 5 x 10 -4 secondi Piombo 210 beta 25 anni Bismuto 210 beta 5 giorni Polonio 210 alfa 136 giorni Piombo 206 Stabile

Nella cartina in figura è rappresentata la situazione italiana relativamente alla concentrazione del radon. Come si vede i problemi maggiori si riscontrano in Lombardia, Lazio, Campania e Friuli. Lazio e Campania sono particolarmente colpiti dal problema radon per il frequente utilizzo in edilizia di materiali di origine vulcanica, principalmente il tufo: il radon, prodotto per decadimento radioattivo dentro i muri delle case o proveniente dal sottosuolo, tende a concentrarsi all’interno dei locali e può così essere inalato più facilmente. Per questo un’efficace contromisura è arieggiare frequentemente i locali.

Il radon si forma dentro le rocce, in particolare quelle vulcaniche, e raggiunge l’aria aperta passando attraverso fenditure delle rocce stesse. La concentrazione è ovviamente massima nel sottosuolo. Non a caso tra i minatori l’incidenza del cancro polmonare è cinque volte maggiore rispetto al resto della popolazione. La concentrazione del radon nell’atmosfera si misura in Becquerel su metro cubo (Bq/m 3): 1 Bq = 1 disintegrazione/s. Può essere espressa anche in Curie su metro cubo (Ci/m 3). [Il Becquerel ha sostituito il Curie: 1 Bq = 2, 7 x 10 -11 Ci] In ambienti chiusi la concentrazione media è di circa 80 bq/m 3, molto superiore a quella che si riscontra all’aperto, ma si possono superare valori anche dieci volte più grandi. Come già detto le massime concentrazioni si hanno in edifici costruiti con materiali di origine vulcanica, come il tufo. A parità di altre condizioni la concentrazione del radon diminuisce all’aumentare della distanza dal suolo, anche in virtù della sua elevata densità (oltre otto volte maggiore di quella dell’aria).

Effetti del radon sulla salute Gli effetti sulla salute dipendono dalla sua radioattività. Un atomo 222 Rn può decadere all’interno del polmone emettendo una particella a, che penetrando in una cellula può danneggiare il DNA. Anche gli atomi che si producono nel decadimento radioattivo del radon possono a loro volta emettere particelle a. Se i danni al patrimonio genetico non vengono riparati può insorgere un tumore a carico del polmone. Per i fumatori il rischio è maggiore perché è stato provato che esiste una sinergia tra il radon e gli inquinanti contenuti nel fumo. Salvo casi estremi che richiedono interventi di specialisti, per proteggersi è sufficiente cambiare spesso l’aria dei locali chiusi. In Italia non esiste una legislazione specifica relativa al radon negli edifici residenziali. L’Euratom (Comunità europea dell’energia atomica – 1957) nel 1990 ha proposto come limite oltre il quale intervenire una concentrazione di 400 Bq/m 3 per gli edifici esistenti e di 200 Bq/m 3 per quelli in progettazione.

In Italia si è in ritardo anche per gli ambienti di lavoro. Dal 2001 l’Euratom ha fissato in 500 Bq/m 3 il limite oltre il quale intervenire. Per gli ambienti di lavoro il TLV per la dose assorbita equivalente è di 20 m. Sv (media annuale calcolata su 5 anni) e di 50 m. Sv (in un solo anno). Alcune grandezze e unità di misura relative alle radiazionizzanti Dose assorbita: energia assorbita dall’unità di massa; la sua unità di misura è il Gray (Gy) 1 Gy = 1 J/kg • Dose assorbita equivalente: come la dose assorbita, ma con riferimento agli effetti biologici della radiazione. Infatti ogni tipo di radiazione ha un effetto diverso. Ad esempio, i raggi a hanno effetti molto maggiori rispetto ai raggi g. La sua unità di misura è il Sievert (Sv) 1 Sv = 1 J/kg (stesse dimensioni SI del Gy). • Becquerel (Bq): 1 disintegrazione (decadimento) per ogni secondo. • Curie (Ci): è pari a 3, 7 x 1010 Bq; corrisponde approssimativamente all’attività di 1 g dell’isotopo 226 del radio. •

Ecco alcuni esempi di dose equivalente assorbita (si tengano presenti i TLV citati in precedenza, 20 e 50 m. Sv): Ø 10 Sv – morte nell’arco di tempo di giorni o settimane Ø 4 Sv – rischio di morte (50 %) Ø 2 ÷ 5 Sv – nausea, perdita dei capelli, emorragie Ø 1 Sv – alterazioni dell’emoglobina; rischio (5 %) di insorgenza di un cancro nell’arco della vita Ø 100 m. Sv – rischio (5 ‰) di insorgenza di un cancro nell’arco della vita Ø 10 ÷ 40 m. Sv – dose assorbita equivalente in una radioterapia Ø 10 ÷ 20 m. Sv – idem in una scintigrafia o una PET Ø 2 ÷ 15 m. Sv – idem in una TAC Ø ~ 2 m. Sv/anno – idem a causa della radioattività naturale Ø < 1 m. Sv – idem in una radiografia.

Amianto E’ il nome comune di un gruppo di minerali fibrosi (amosite, crocidolite, tremolite ed altri). In virtù dello loro grande lavorabilità, unita alla resistenza al calore e agli agenti chimici, in passato questi minerali sono stati ampiamente utilizzati in un gran numero di prodotti sia da soli che in associazione con altri materiali. Purtroppo proprio la struttura fibrosa dell’amianto, alla base della sua versatilità, si è rivelata un grave problema. Infatti i materiali a base di amianto sono diventati una fonte di fibre microscopiche estremamente pericolose soprattutto per inalazione. Le principali patologie legate all’inalazione delle fibre di amianto sono l’asbestosi, il mesotelioma e il tumore del polmone.

Le dimensioni delle fibre di amianto sono messe bene in evidenza dalla foto a lato in cui sono confrontate con un capello. Le fibre di amianto sono presenti anche nell’aria non inquinata. In questo caso la loro concentrazione risulta inferiore a 100 fibre/m 3. Questo dato può anche triplicare nelle città (si pensi, ad esempio, che i ferodi dei freni e delle frizioni delle auto erano ottenuti impastando l’amianto con resine sintetiche). Le concentrazioni di fibre di amianto aumentano anche di un ordine di grandezza (2000 fibre/m 3) nelle zone minerarie e possono arrivare a valori elevatissimi (migliaia di fibre per litro) nei luoghi dove viene lavorato. In Italia è emblematico il caso di Bagnoli, sede di una fabbrica della Eternit: si sono verificati innumerevoli casi di mesotelioma (tumore della pleura) e di tumore al polmone da amianto sia tra i lavoratori sia tra i cittadini, in particolare tra i familiari dei lavoratori. E’ ancora in corso il processo ai dirigenti e ai proprietari della società.

Effetti dell’amianto sulla salute Le fibre di amianto possono entrare nel nostro organismo per ingestione e per inalazione. Gli effetti delle fibre ingerite non sono ancora del tutto certi, anche se si è riscontrata una maggiore incidenza di alcuni tumori dell’apparato digerente in popolazioni che usano acqua inquinata da fibre di amianto. I danni dovuti alle fibre inalate sono invece ben conosciuti fino dagli anni ‘ 60 del ‘ 900. Le fibre più pericolose sono quelle che arrivano più in profondità, fino agli alveoli polmonari. Le più piccole possono insediarsi anche nella pleura, la membrana che riveste i polmoni, o entrare nel circolo sanguigno. I problemi più seri si hanno proprio a carico della pleura e dei polmoni, con l’insorgenza di malattie molto gravi come l’asbestosi, il mesotelioma e il tumore del polmone. La malattia si manifesta dopo un tempo piuttosto lungo, dai quindici (asbestosi) fino ai trent’anni (mesotelioma). Dal 1992 l’uso, la produzione e la commercializzazione dell’amianto sono vietati. Per gli ambienti di lavoro il TLV-TWA è fissato a 10 fibre/L.

Altri inquinanti • • • Solfuro di idrogeno, H 2 S, dovuto ai processi di desolforazione dei petroli in genere (delle benzine in particolare) e del gas naturale. Tiofene e mercaptani emessi da raffinerie e cokerie, facilmente individuabili a causa del loro sgradevole odore di uovo marcio. Acidi inorganici e organici (solforico, cloridrico, fluoridrico, bromidrico, acetico, fumarico, tannico, ecc. ) liberati nelle combustioni o in cicli industriali diversi. Prodotti radioattivi artificiali dovuti, oltre che alle esplosioni atomiche, a lavorazione di sostanze radioattive per l'utilizzazione pacifica dell'energia nucleare, all'impiego di nuclidi radioattivi nella ricerca scientifica, nell'industria, in campo medico e in agricoltura. Cloro, acido cloridrico e microinquinanti organoclorurati (vedere anche la voce “diossine”) liberati dalla decomposizione dovuta ad incenerimento di materie plastiche clorurate.

Lo smog fotochimico E’ il risultato di una serie di reazioni, determinate dalla luce UV e facilitate da temperatura elevata, che coinvolgono NOx e COV. Consiste in un aumento notevole della concentrazione di ozono al suolo, accompagnato da un gran numero di altre sostanze. Le aree mediterranee ne sono colpite dato che presentano tutte le caratteristiche suddette, specialmente d’estate e nelle zone ad alta densità di traffico. Nella foto a sinistra lo smog fotochimico sulla città di Seattle (USA) è reso visibile dal colore rossastro caratteristico del diossido di azoto.

Fasi di sviluppo dello smog fotochimico In seguito al traffico automobilistico aumenta la concentrazione di COV e ossidi di azoto. La luce solare provoca la fotolisi di NO 2: NO 2 + UV ———› NO + O. si formano ozono e radicali ossidrile: O 2 + O. ———› O 3 O. + H 2 O ———› 2 OH. si producono radicali perossido da COV e radicali ossidrile: RH + OH. ———› R. + H 2 O R. + O 2 ———› RO 2. i radicali perossido reagiscono con NO ossidandolo: RO 2. + NO ———› RO + NO 2

Come si è detto l’ozono è il principale componente dello smog fotochimico, ma non l’unico. Ad esempio, due altri inquinanti si formano in seguito a reazioni che interrompono il ciclo precedentemente descritto: - si può produrre acido nitrico da NO 2 e radicali ossidrile NO 2 + OH. ———› HNO 3 - o perossiacetil nitrato (PAN) da NO 2 e radicali perossiacetile che si formano per ossidazione fotochimica di COV NO 2 + CH 3 -CO-O-O. ———› CH 3 -CO-O-O-NO 2 Il PAN, oltre ad avere effetti irritanti sugli occhi, è fitotossico (blocca la fotosintesi). In associazione con l’ozono, che aumenta la respirazione e quindi il fabbisogno di nutrienti, provoca il rapido deperimento delle piante.

L’inquinamento e il clima Tra il clima e la concentrazione degli inquinanti al suolo esiste un legame molto stretto. Se è vero che le condizioni climatiche possono influenzare la persistenza degli inquinanti, è anche vero che molte sostanze inquinanti svolgono un ruolo importante nella determinazione del clima. Su grande scala sono molto importanti i venti di alta quota e le turbolenze derivanti dagli spostamenti di grandi masse d’aria da aree anticicloniche (alta pressione) ad aree cicloniche (bassa pressione). A livello locale l’intensità del vento a bassa quota, le condizioni di alta pressione invernale conseguenti possibili inversioni termiche, sono determinanti per il livello degli inquinanti. Ad esempio, l’inversione termica favorisce l’accumulo degli inquinanti (foto a destra), mentre il Smog da inversione termica vicina al suolo vento forte facilita la loro dispersione.

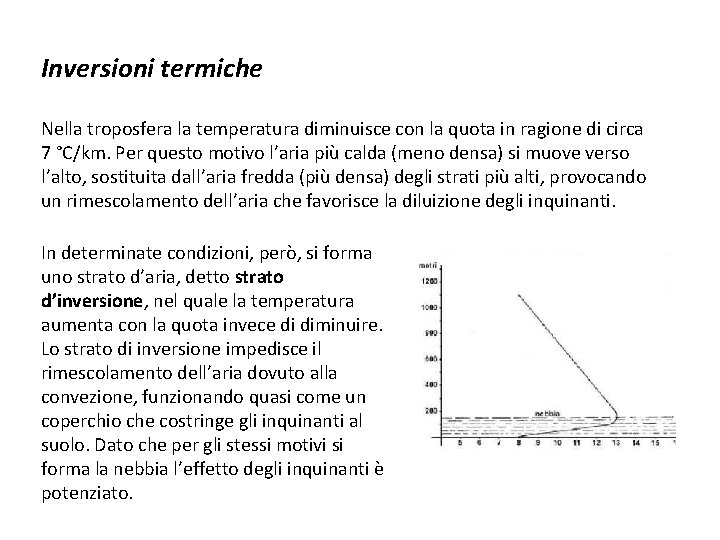
Inversioni termiche Nella troposfera la temperatura diminuisce con la quota in ragione di circa 7 °C/km. Per questo motivo l’aria più calda (meno densa) si muove verso l’alto, sostituita dall’aria fredda (più densa) degli strati più alti, provocando un rimescolamento dell’aria che favorisce la diluizione degli inquinanti. In determinate condizioni, però, si forma uno strato d’aria, detto strato d’inversione, nel quale la temperatura aumenta con la quota invece di diminuire. Lo strato di inversione impedisce il rimescolamento dell’aria dovuto alla convezione, funzionando quasi come un coperchio che costringe gli inquinanti al suolo. Dato che per gli stessi motivi si forma la nebbia l’effetto degli inquinanti è potenziato.

Meccanismi di formazione dello strato di inversione - inversione radiativa: si ha quando, in condizioni di pressione alta nella stagione fredda, di notte il suolo e l’aria ad esso adiacente si raffreddano molto velocemente per irraggiamento IR. Si forma così uno strato di inversione a bassa quota che viene distrutto dal riscaldamento solare solo a mattino inoltrato. E’ per questo motivo che le nebbie sono particolarmente fitte dalle ore serali al primo mattino; - inversione per spostamento orizzontale: tipica delle zone costiere, è dovuta allo spostamento di masse d’aria più calda e umida dal mare verso terra, dove la temperatura è più bassa. Si forma uno strato d’inversione a quota più elevata rispetto al caso precedente (qualche centinaio di metri). Se il riscaldamento mattutino non è abbastanza intenso da rompere lo strato d’inversione, si possono verificare eventi di smog fotochimico persistenti e addirittura crescenti per alcuni giorni.

Effetti dell’inquinamento sul clima Le attività umane influenzano il clima essenzialmente in due modi: con l’effetto serra e con il rilascio di grandi quantità di calore di scarto. L’effetto serra è il risultato di uno squilibrio tra la quantità di energia che giunge alla Terra dal sole e quella che la Terra stessa disperde nello spazio per irraggiamento IR. E’ dovuto ai cosiddetti gas serra. I gas serra, assorbendo la radiazione infrarossa, fanno diminuire la frazione di energia che viene dispersa verso lo spazio provocando il riscaldamento dell’atmosfera. Le varie sostanze hanno una diversa capacità di assorbimento della radiazione IR. Ad esempio, l’ozono assorbe l’IR circa duemila volte di più della CO 2, ma quest’ultima a causa della sua abbondanza è la maggiore responsabile dell’effetto serra.

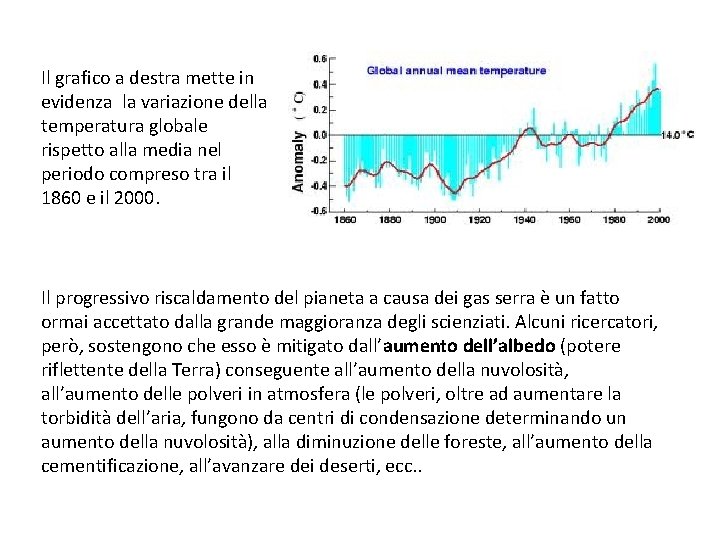
Il grafico a destra mette in evidenza la variazione della temperatura globale rispetto alla media nel periodo compreso tra il 1860 e il 2000. Il progressivo riscaldamento del pianeta a causa dei gas serra è un fatto ormai accettato dalla grande maggioranza degli scienziati. Alcuni ricercatori, però, sostengono che esso è mitigato dall’aumento dell’albedo (potere riflettente della Terra) conseguente all’aumento della nuvolosità, all’aumento delle polveri in atmosfera (le polveri, oltre ad aumentare la torbidità dell’aria, fungono da centri di condensazione determinando un aumento della nuvolosità), alla diminuzione delle foreste, all’aumento della cementificazione, all’avanzare dei deserti, ecc. .

Anche riguardo agli effetti del calore di scarto rilasciato in atmosfera (e nelle acque superficiali) i pareri sono discordi. Molti sostengono che si è già superato il livello di emissioni che il pianeta può smaltire per irradiazione nello spazio e che quindi si contribuisca in tal modo ad aumentare la temperatura media globale, altri pensano invece che il calore di scarto emesso dagli impianti industriali può essere compensato dall’aumento dell’albedo. In ogni caso, non fosse altro che per un sano principio di cautela, è necessario invertire la tendenza all’aumento delle emissioni di gas serra e del rilascio di calore di scarto nell’ambiente e fare fronte al progressivo esaurimento delle risorse naturali e al deterioramento dell’ambiente che già ora è evidente.