INOVATIVN VZDLVAC PROGRAMY PRO FARMACEUTICK PRACOVNKY Trombofiln stavy

INOVATIVNÍ VZDĚLÁVACÍ PROGRAMY PRO FARMACEUTICKÉ PRACOVNÍKY Trombofilní stavy Přehled patofyziologie trombofilních stavů a možností jejich ovlivnění Tento studijní materiál vznikl jako výstup z projektu č. CZ. 1. 07/3. 2. 04/04. 0035

Osnova lekce: Virchowova trias Trombofilní stavy – trombofílie (vrozené, získané, smíšené) – patofyziologie, medikamenty a zajímavosti: • 1. Zpomalení krevního proudu – Elastická komprese • 2. Porušení endotelu – Endoteliální dysfunkce • 3. Zvýšená srážlivost krve – A. Agregace trombocytů – primární hemostáza • Adheze trombocytů • Aktivace trombocytů • Degranulace trombocytů • Agregace trombocytů – B. Zvýšená srážlivost krve - hyperkoagulace (novější pojetí schématu) – sekundární hemostáza • Vyšší aktivita koagulačních faktorů – TF, II, V, VIII, IX, X, XII, XIII, … • Nižší aktivita antikoagulačních faktorů – AT, PC, PS, APC, trombomodulinu, … – C. Snížená fibrinolýza • Vyšší tvorba fibrinu – PAI, … • Nižší fibrinolytická aktivita – Plasminogen, t-PA, …

Úvod • Trombotické cévní komplikace vedoucí příčinou nemocnosti a úmrtnosti • Každoročně 1 úmrtí na plicní embolii, 2– 4 úmrtí na mozkovou příhodu a asi 5 úmrtí na infarkt myokardu na 1000 obyvatel [1] • Trombóza rozhodující příčinou: – – – – Infarktu myokardu (IM) Mozkové mrtvice (TIA, AP, CMP) Kritické končetinové ischémie (ICHDK) Plicní a systémové embolie [1] Plicní hypertenze Trombózy žil a posttrombotického syndrom Intrauterinní růstové retardace, potratů aj. Mikroangiopatických poruch

Antiagregancia, antitrombotika, antikoagulancia a fibrinolytika • Narůstají počty nemocných, kteří jsou indikováni k: – – – Profylaxi tromboembolické nemoci Prevenci embolizace v tepenném řečišti Jsou antikoagulancii léčeni pro vzniklé TE komplikace • Toho času je v ČR léčeno antikoagulancii asi 2 % populace – dlouhodobé podávání v ambulantním režimu • ACCP Guidelines (American College of Chest Physicians) – – – Devátá v časopisu CHEST mnoho změn vzhledem k registraci nových antitrombotik • http: //journal. publications. chestnet. org/issue. aspx? journalid=99&issueid=23443&direction=P • 3 nová antikoagulancia již v indikaci: – Profylaxe TE po ortopedických výkonech • Zkouší se v: – – – Prevenci ischemických příhod U fibrilací síní u umělých chlopní v profylaxi flebotrombóz mimo ortopedické stavy v léčbě akutní žilní trombózy a její sekundární prevenci Orientace v rozsáhlé problematice = patofyziologie strukturovaně před očima

1. Zpomalení krevního proudu • Rozšíření řečiště (x okolní svaloviny): – Varixy (DK, jícnové, hemeroidy aj. ), venektazie, cévní malformace, immobilizace – ležící pacient, ochrnutí – Fibrilace síní • Stáza před překážkou (zúžení): – Trombózy, flebedém, ateroskleroza, st. p. IM, CMP – Ateroskleróza – Nádory – Dlouhé sezení, sádrová fixace, chybně nasazená kompresivní pomůcka, těhotenství, obezita aj. – Plicní hypertenze, portální hypertenze • Pokles krevního tlaku (celkově): – Operace, dehydratace, letadlem (3 h+ cca 4 týdny před / po OP), selhávání srdce, ležící pacient, průjmy, pocení, popáleniny, krvácení, vazodilatace (zánět, šok, hypertermie aj. ), exsudace do střeva, aj. Vysoká viskozita krve – Leukémie a nádory obecně vč. nadprodukce protilátek, autoimunity, polycytemia vera, lymfomy, paraproteinémie, aj. – Dehydratace, metabolické X, talasemie, srpk. anemie apod. – Hyperkoagulační stavy obecně (zvýšená aktivace, nadprodukce, x degradace) • • Zúžení řečiště /aktivace ok. svaloviny: • Kompresivní punčochy a podkolenky, lymfoven, kompresivní bandáž • Odstranění povrchových varikozních žil (vena safena magna) – flebektomie, stripping aj. • Aktivace žilně svalové pumpy RHB • Defibrilace, terapie srdečního selhávání aj. • Odstranění překážky – dle příčiny: • Operace/jiné zmenšení nádoru, stenty, trombektomie, trombolýza, mobilizace, redukce hmotnosti, terapie příčiny… • Udržení krevního tlaku a průtoku: • Hydratace vč. i. v. , transfúze, kardiotonika, antiarytmika, kardiostimulátory aj. • Časná mobilizace + RHB vždy • Kostní fixace, endoprotézy aj. ortopedické rekonstrukce hřeby a dlahy • Snížení viskozity krve • Hydratace, plasmaferézy, leukaferézy aj. • Hypolipidemika, kompenzace DM aj. • Rheologika: Pentoxifylin, Naftidrofurylem, Alprostadil, … • Antiagregancia, Venotonika: • Rostlinné: escin, rutosidy, diosmin, vitis viniferae seminis extractum, rusci extractum + hesperidini methylchalconum • Semisyntetické: tribenosid, troxerutin • Syntetické: calcii dobesilas
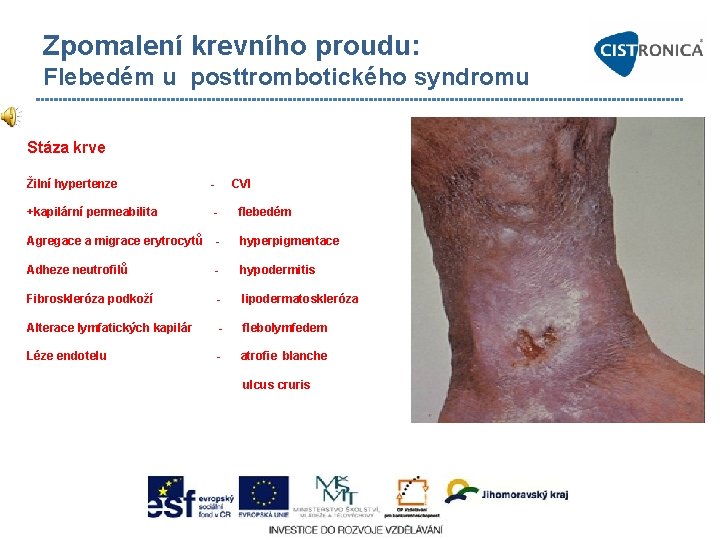
Zpomalení krevního proudu: Flebedém u posttrombotického syndromu Stáza krve Žilní hypertenze - CVI +kapilární permeabilita - flebedém Agregace a migrace erytrocytů - hyperpigmentace Adheze neutrofilů - hypodermitis Fibroskleróza podkoží - lipodermatoskleróza Alterace lymfatických kapilár - flebolymfedem Léze endotelu - atrofie blanche ulcus cruris
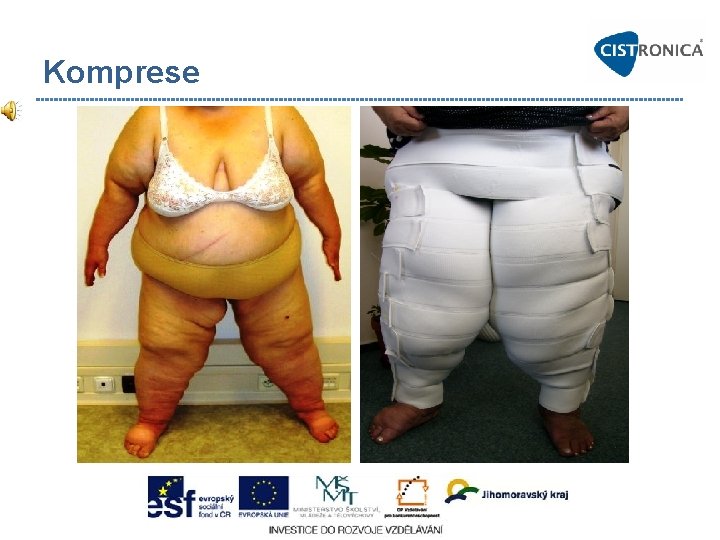
Komprese

2. Endotel Povrch endotelu cca 500 1000 m 2, hmotnost cca 1, 5– 3 kg • Výměna metabolitů – semipermeabilita • Regulace průsvitu cévy – Produkce vazodilatačních působků • • • NO inhibuje expresi adhezivních molekul, adhezi a agregaci trombocytů a apoptózu endotelií Prostacyklin – PGI 2 Endothelium – derived hyperpolarizing factor – Produkce vazokonstirkčních působků (důsledkem i proliferace myocytů) • Endotelin 1 (expresi stimulují: např. trombin, oxidovaný LDL, angiotenzin II aj. ), TXA 2 – Regulace hladin angiotenzinu II, bradykyninu expresí ACE • Adheze trombocytů, leukocytů a prostup – Vazoadhezivní molekuly endotelu: E selektin, ICAM 1, VCAM 1, PECAM 1 – Nesmáčivý povrch – porušením aktivace primární destičkové fáze hemokoagulace a sekundární hemostázy se vznikem nerozpustného fibrinu – Regulace koagulace a antikoagulace (vazba antitrombinu III, produkce trombomodulinu) a fibrinolýzy (syntéza t PA, PAI 1) • Reparace (hyperplázií intimy a hypertrofií cévní stěny) – TGF beta, FGF, destičkový růstový faktor, interleukin 1, endotelin 1 X NO • • Angiogeneze Pro/proti zánětlivá odpověď
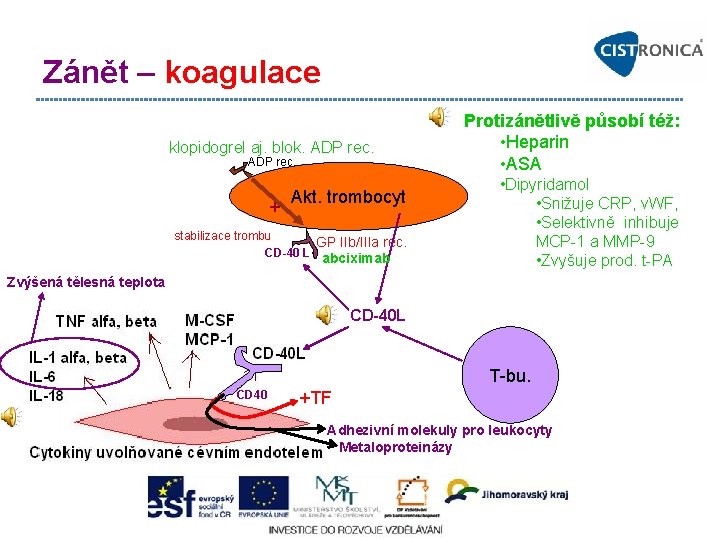
Zánět – koagulace klopidogrel aj. blok. ADP rec. + Akt. trombocyt stabilizace trombu GP IIb/IIIa rec. CD-40 L abciximab Protizánětlivě působí též: • Heparin • ASA • Dipyridamol • Snižuje CRP, v. WF, • Selektivně inhibuje MCP 1 a MMP 9 • Zvyšuje prod. t PA Zvýšená tělesná teplota CD-40 L T bu. CD 40 +TF Adhezivní molekuly pro leukocyty Metaloproteinázy
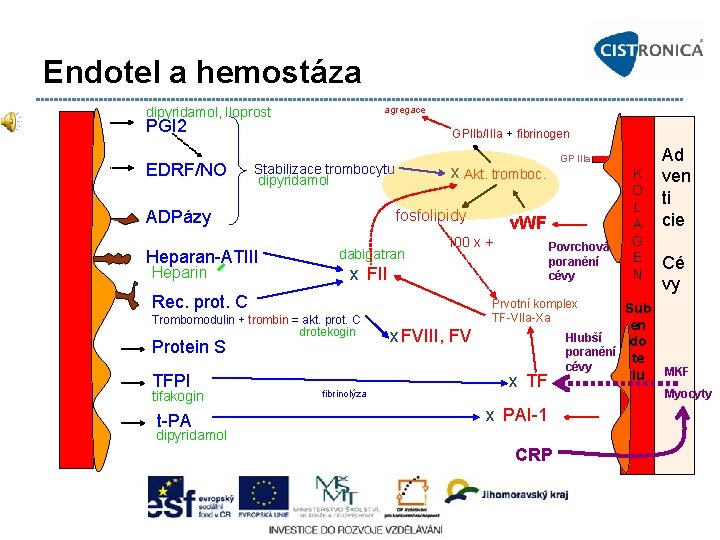
Endotel a hemostáza agregace dipyridamol, Iloprost PGI 2 EDRF/NO GPIIb/IIIa + fibrinogen Stabilizace trombocytu dipyridamol Heparan ATIII Heparin x Akt. tromboc. fosfolipidy ADPázy dabigatran 100 x + Rec. prot. C Protein S TFPI tifakogin t PA v. WF Povrchová poranění cévy x FII Trombomodulin + trombin = akt. prot. C drotekogin fibrinolýza GP IIIa K O L A G E N Ad ven ti cie Cé vy Prvotní komplex TF VIIa Xa x FVIII, FV x TF x PAI 1 dipyridamol CRP Sub en Hlubší do poranění te cévy lu MKF Myocyty

Prozánětlivé stavy jako riziko TE • • • • Operace, trauma, císařský řez, porod, šestinedělí Popáleniny, Obezita, Flebitida Malignita nádorové onemocnění Myeloproliferativní onemocnění Reakce na bakteriální LPS: Centrální žilní katétr in situ Do 30 -90 min (zánětlivá fáze do 2 h) Autoimunní onemocnění • Mononukleáry – m. RNA pro TF – vylití TF – zvýšení Xa Behcetův syndrom • Vyšší TNFalfa, IL 6 Pomalejší fáze s tvorbou II (koagulační fáze 6. -10. h) Akutní zánětlivé onemocnění • Vzestup IIa, fragmenty protrombinu 1 a 2 Infekce obecně • Vzestup TAT (trombin-AT) komplexů – peak 4 6 h po Fibrinolýza Nespecifické střevní záněty • Časný vzestup t. PA Cronova choroba • Následně vzestup PAI 1 • Riziko progrese do DIC při sepsi (generalizace) Ulcerózní kolitida Degenerace buněk (nad 10 h) Selhání plic • Vylití elastáz – poškození okolních buněk – vzestup rozpustného fibrinu, TF Věk nad 60 let • X mikrokapilár se vzestupem laktátu v cirkulaci Aj. • Toto potenciuje hepatotoxicitu Aflatoxinu B 1

Endoteliální dysfunkce Funkční poškození endotelu: • • 1. Zvýšená propustnost cévní stěny (NOS) (a depozice) 2. Nedostatečná vazomotorická odpověď na endoteldependentní podněty (sklon k vazospazmu) (prostanoidy, tromboxany, endotelin) 3. Zvýšená produkce prozánětlivých (IL 1, IL 6, hs. CRP, MMP, SAA) a cytoadhezivních (ICAM 1, VCAM, E selektin) signálů 4. Oslabení antikoagulačních a fibrinolytických mechanismů (TF, t. PA, PAI 1, v. WF) Tendence k trombóze – Nízké hladiny Mg – vedou k zánětu a endoteliální dysfunkci, vyššímu CRP, zvýšené produkci cytokinů, Nucl. Kappa B a k dysf. trombocytů až k trombóze PMID: 22907037 • Inhibitory protonové pumpy – známo, že vedou k hypo Mg od r. 2006. 2011 U. S. FDA varuje že dlouhodobé užívání může indukovat hypo Mg PMID: 22892510 • 5. Nedostatečná inhibice subendoteliální proliferace (FGF beta, TGF beta, VEGF) – Ginsenosid Rg 3 (ginseng) – může indukovat proliferaci hladké svaloviny a vaskulární remodelaci

Porušení endotelu • • Cizí povrchy Vhodné podmínky pro funkci a – Katetry, defibrilátory, umělé chlopně, stenty aj. regeneraci endotelu Mechanicky zevně – Trauma vč. operací, angioplastika = prevence trombóz a trombembolií, CMP, IM, Mechanicky turbulentním prouděním / vířením terapie aterosklerózy, – Okolí insuficientích chlopní žil, ouška v síních srdce, diabetu, hypertenze, hypertenze – bifurkace a zužení tepen, aneurysmata, cévní malformace, zaškrcení, menší fixace cévy k okolí dyslipidémií, …. . Prozánětlivé stavy = nezbytné pro udržení dobré – Infekce Chlamydophila pneumonia, stafylokok, funkce všech ostatních helicobacter p. aj, autoimunitny vč. arteritidy, orgánů revmtaická onemocnění, imunokomplexy, vyšší CRP, flebitidy = antiageing medicína Metabolicky (X regenerace, +oxidační stres) 1. Symptomy v praxi: – Dyslipidemie (hypercholesterolémie, oxidované či glykované LDL), hyperglykémie, hyperinzulinémie, • Esenciální hypertenze, erektilní hypoxie, stárnutí, cytostatika, kouření, … dysfunkce, postmenopauzální návaly, – Hyperhomocysteinémie (vč. X MTHFR, X migrény, angína pectoris, Raynaudův cystathionbetasyntázy, B 12, B 6, K. list. , +Met. ve sy. aj. stravě), Termické a radiační poškození (ionizující záření) Podávání B vit. vedlo k poklesu homocysteinu a D dimerů. – Omrzliny, Popáleniny PMID: 12195694 [Pub. Med] Genetické vlivy aj.

3. Zvýšená krevní srážlivost • Primární hemostáza – – A. Adheze trombocytů B. Aktivace trombocytů C. Degranulace trombocytů D. Agregace trombocytů • Sekundární hemostáza Antiagregancia Antikoagulancia – E. Vnitřní a vnější aktivace koagulace a inhibice – F. Produkce trombinu – G. Tvorba nerozpustného fibrinu + fibrinolýza Fibrinolytika / trombolytika
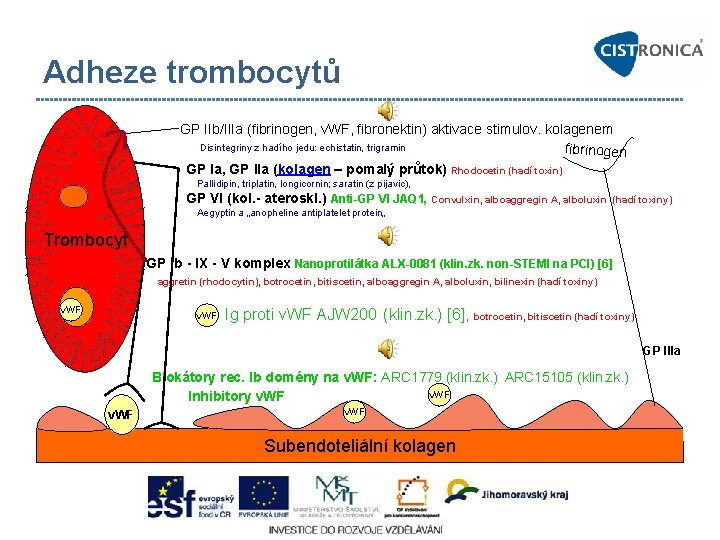
Adheze trombocytů GP IIb/IIIa (fibrinogen, v. WF, fibronektin) aktivace stimulov. kolagenem Disintegriny z hadího jedu: echistatin, trigramin fibrinogen GP Ia, GP IIa (kolagen – pomalý průtok) Rhodocetin (hadí toxin) Pallidipin, triplatin, longicornin; saratin (z pijavic), GP VI (kol. - ateroskl. ) Anti-GP VI JAQ 1, Convulxin, alboaggregin A, alboluxin (hadí toxiny) Aegyptin a „anopheline antiplatelet protein„ Trombocyt GP Ib - IX - V komplex Nanoprotilátka ALX-0081 (klin. zk. non-STEMI na PCI) [6] aggretin (rhodocytin), botrocetin, bitiscetin, alboaggregin A, alboluxin, bilinexin (hadí toxiny) v. WF Ig proti v. WF AJW 200 (klin. zk. ) [6], botrocetin, bitiscetin (hadí toxiny) GP IIIa Blokátory rec. Ib domény na v. WF: ARC 1779 (klin. zk. ) ARC 15105 (klin. zk. ) v. WF Inhibitory v. WF Subendoteliální kolagen
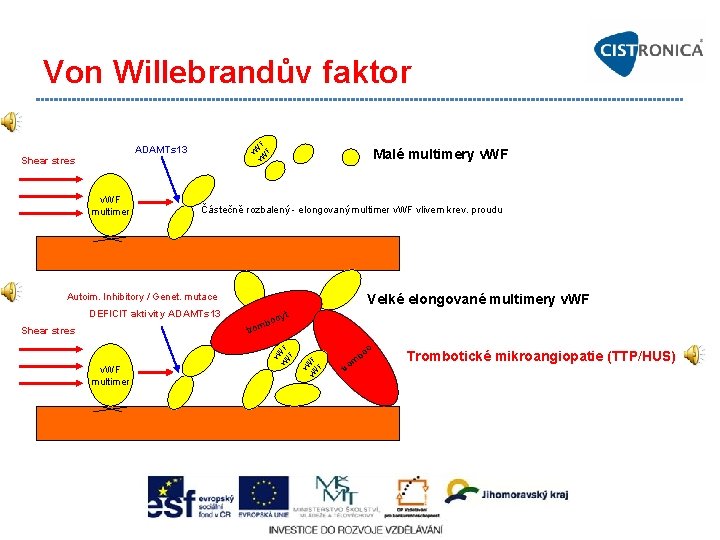
Von Willebrandův faktor F v. W ADAMTs 13 Shear stres v. WF multimer Malé multimery v. WF Částečně rozbalený elongovaný multimer v. WF vlivem krev. proudu Autoim. Inhibitory / Genet. mutace Velké elongované multimery v. WF DEFICIT aktivity ADAMTs 13 c v v. W WF F v. WF multimer v v. W WF F b trom Shear stres t ocy bo m tro Trombotické mikroangiopatie (TTP/HUS)

Aktivace trombocytů Hypokalcémie – snížená agregace trombc. , Suppl. Ca 2+ zmírňuje fci a agregaci destiček při +Na+ Nízké Ca 2+ stim. ADP indukovanou vazbu trombc. na fibrinogen. Vysoké Ca 2+ snižuje ADP indukovanou vazbu trombc. na fibrinogen ale stim. vazbu trombc. na fibrinogen, Aktivací povrchových receptorů • GP receptorů IIb/IIIa (+ agregace) – aktivace tr. vede k další aktivaci GP IIb/IIIa • PAF rec. jeden z nejmocnějších stimulátorů destiček – PAF z: aktivovaných neutrofilních granulocytů, bazofilů a makrofágů, endotelu a destiček • Aktivace rec. pro ADP – (Uvolněním ADP) – Rec. P 2 Y 12 Aktivuje destičky inhibicí adenylátcyklázy, potencuje pozdní fáze agregace – Rec. P 2 Y 1 Mobilizuje ionizované kalcium ze zásobních vezikul, exprese GP IIb/IIIa • Štětka drsná (Dipsacus asper) – zvyšuje Ca 2+ v trombocytech – prokoagulační ef. Vzestup intracelulární koncentrace kalcia: • Viskózní metamorfóza destiček: Centralizace organel, tvar z diskoidního na měňavkovitý (adhezivita+) • Aktivace fosfolipázy A 2 – produkce k. arachidonové z fosfolipidů membrán trombocytů – COX: TXA 2 – silně proagregační a Prostacyklin PGI 2 – ASA: Inhibice COX trombocytů ireverzibilní, v endotelu resyntetéza • Akt. fosfolipázy C, Akt. Adenylátcyklázy Deficience neutrálnách glykolipidů • Glykosilceramidy: Galactosylceramid, Lactosylceramid aj. Fosfolipidy, Glykolipidy membrány ovlivňují prokoagulační / antikoagulační vlastnosti komplexů vč. proteinu C, regulace produkce trombinu, zánětu aj. Saturované tuky ve stravě asociovány s: • Více protrombotických fospholipidů • 20: 3 (n 9) proagregační reakce na rec. IIa • Pokles trombocytárního cholesterolu PMID: 3707672 [ Pub. Med] VASP (vasodilator-stimulated Změna orientace membránových fosfolipidů (PL) (PF 3 platelet factor 3) - mechanismus flip-flop phosphoprotein): regulace aktivace • Koagulačně aktivní fosfolipidy vnitřního listu buněčné membrány (fosfatidylserin), jsou exprimovány navenek trombc. – ovliv. Aktinová filamenta • Zevní fosfolipidy se obrátí dovnitř buňky • Míra a místa fosforylace k • Urychlují reakci mezi koagulačními faktory a lokalizují je na místa, kde je třeba vytvořit koagulum posouzení efektu antidestičkové – Vazba s aktivovanými serpinovými enzymy (protrombinázovým komplexem aj. koag. f. ) via Ca 2+ [5] medikace • +Ca 2+ v tromboc. , deplece ATP, ROS, kaspázová aktivace = activace scramblázy, inhibice flippázy) – Apyrázy – hydrolýza ATP – inhibice agregace – sliny moskytů, brouků, písečných much, blech, klíšťat aj. Poruchy vazby koagulačních faktorů nebo inhibitorů na fosfolipidovou membránu • X karboxylace faktorů protrombinového komplexu a systému PC/PS (x metabolismu vitamínu K ) Pomalé blokátory Ca kanálů: – Ztráta vazebého místa pro Ca, které je normálně váže na PL • Verapamil, diltiazem, nifedipin • Antifosfolipidový syndrom (APS) - Inhibice těchto pochodů anti. PL protilátkami • Inh. Trombc. Adheze – Ig proti negativně nabitým destičkovým PL • Méně uvolnění ADP, TXA 2 – Tromboembolické komplikace, trombocytopenie • Blokují vstup Ca 2+ do trombc. – Inhibitory koagulace beta 2 GPI (apolipoprotein H) a anexin V (VAP, PAP). Nitráty • Asociovány s PL, role v etiopatogenezi antifosfolipidového syndromu (zvláště beta 2 GPI) • Akcelerace syntézy c. GMP a c. AMP
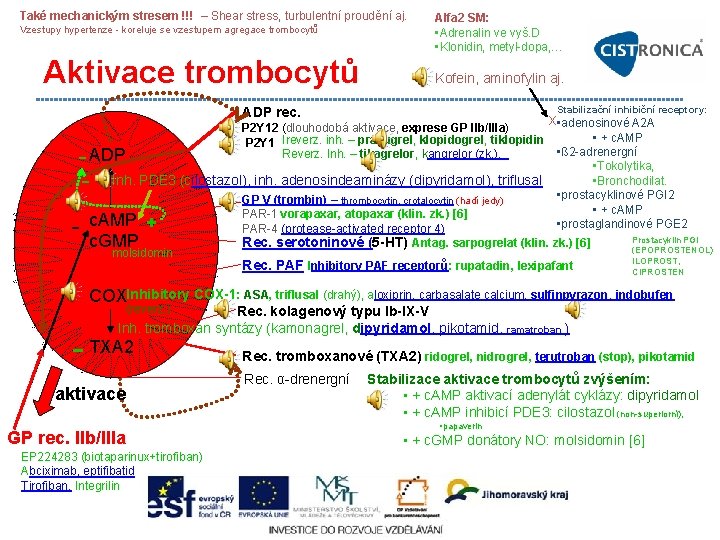
Také mechanickým stresem !!! – Shear stress, turbulentní proudění aj. Vzestupy hypertenze koreluje se vzestupem agregace trombocytů Aktivace trombocytů Alfa 2 SM: • Adrenalin ve vyš. D • Klonidin, metyl dopa, … Kofein, aminofylin aj. Stabilizační inhibiční receptory: ADP rec. ADP P 2 Y 12 (dlouhodobá aktivace, exprese GP IIb/IIIa) P 2 Y 1 Ireverz. inh. – prasugrel, klopidogrel, tiklopidin Reverz. Inh. – tikagrelor, kangrelor (zk. ), Inh. PDE 3 (cilostazol), inh. adenosindeaminázy (dipyridamol), triflusal c. AMP + c. GMP molsidomin x • adenosinové A 2 A • + c. AMP • ß 2 adrenergní • Tokolytika, • Bronchodilat. • prostacyklinové PGI 2 • + c. AMP • prostaglandinové PGE 2 GP V (trombin) – thrombocytin, crotalocytin (hadí jedy) PAR 1 vorapaxar, atopaxar (klin. zk. ) [6] PAR 4 (protease activated receptor 4) Rec. serotoninové (5 -HT) Antag. sarpogrelat (klin. zk. ) [6] Rec. PAF Inhibitory PAF receptorů: rupatadin, lexipafant Prostacyklin PGI (EPOPROSTENOL) ILOPROST, CIPROSTEN COXInhibitory COX-1: ASA, triflusal (drahý), aloxiprin, carbasalate calcium, sulfinpyrazon, indobufen (reverz. ) Rec. kolagenový typu Ib-IX-V Inh. tromboxan syntázy (kamonagrel, dipyridamol, pikotamid, ramatroban ) TXA 2 aktivace GP rec. IIb/IIIa EP 224283 (biotaparinux+tirofiban) Abciximab, eptifibatid Tirofiban, Integrilin Rec. tromboxanové (TXA 2) ridogrel, nidrogrel, terutroban (stop), pikotamid Rec. α drenergní Stabilizace aktivace trombocytů zvýšením: • + c. AMP aktivací adenylát cyklázy: dipyridamol • + c. AMP inhibicí PDE 3: cilostazol (non superiorní), • papaverin • + c. GMP donátory NO: molsidomin [6]

ASA Primární prevence a indikace k užívání ASA: • U mužů ve věku 45– 79 let, pokud potenciální prospěch z redukce rizika IM převažuje potenciální riziko gastrointestinálního (GI) krvácení • U žen ve věku 55– 79 let, pokud potenciální prospěch z redukce rizika ischemické CMP převažuje potenciální riziko GI krvácení ASA a žaludek: ASA se z běžné lékové formy uvolní právě už v žaludku, kde v jeho kyselém p. H přechází nedisociovaná (lipofilní) ASA volně skrz membránu do buněk žaludeční sliznice. • V neutrálním intracelulárním p. H se ASA disociuje, stává se rozpustnou ve vodě a snižuje se její schopnost prostupovat membránami. • ASA se tak uvnitř buněk hromadí (tzv. „ion‑trapping“) a vede k intracelulární acidóze a odumření buněk – event. až k rozvoji žaludečního vředu. Aspirin Protect: 100 mg ASA v enterosolventním obalu (ec. ASA) • Metakrylátový kopolymer rezistentní vůči žaludeční kyselině, uvolňuje ASA až při p. H > 6, tj. ve střední nebo distální části tenkého střeva Salicyláty v potravinách: denní příjem v západní stravě 10 -200 mg v přírodní formě, cca 3 mg acetylsalicylátu • V rostlinách: zvyšují odolnost proti hmyzu, houbám a bakteriím, + růst, zrání a přežívání rostlin, X klíčení semen. Výskyt: +nezralé ovoce, +slupky, koncentrovanější sušením (hrozinky, rybíz, datle aj. ), především bobulovité, ananas, třešně a meruňka, ale i pomeranč, avokádo, broskev, jahody, … zelenina (0 - 6 mg / 100 g) – okurka, zelené olivy, endivie, slupky brambor, kečup, ředkev, jedlé kaštany • Hlavně bylinky a koření: kari, čili, tymián, anýz, rozmarýn, šalvěj, čekanka, dále také mandle, kokos, pistacie, vlašské ořechy aj. , sirup z kukuřice, majoránka, máta, křen, oregano, sezamová semínka, kurkuma, hořtice, jablečný ocet, káva aj. (viz nízko salicylátová dieta u intolerance ASA – astma+nosní polypy, ADHD aj. ) (Swain et al. )

Rezistence k ASA - rizikový faktor Arteriální trombózy Vznik rezistence (klinická, hematologická, genetická) k ASA cca 30% pac. řada podnětů (problém i samotné definice): KLINICKÁ: • Nízké dávky (obézní pacienti) • Nepravidelné užívání / non compliance • X vstřebávání při současném podání inhibitoru protonové pumpy (IPP) [6] → 2 x vyšší KV mortalita a morbidita [6] – Slabé kyseliny hydrofilní povahy, vstřebávány pouze nedisociované, tj. při p. H nižším než 3, 5 Interakce s ibuprofenem – interakce s acetylací ASA • Nemožnost inhibice COX acetylací při ter. např. ibuprofenem, indometacinem [6] (Ostatní salicyláty neobsahují acetylovou skupinu – blokáda COX 1 je u nich reverzibilní !) • Akcentace agregace destiček zevními faktory (stres, kouření aj. ) • Cévní uzávěry z jiných než aterotrombotických příčin (embolizace, vegetace, nádorové bu. , cizí hmoty) • Arteritidy (obecně záněty vyšší tvorba tromboxanu A 2 monocyty, makrofágy, endotelem neblok. ASA = 2 x více IM (HOPE)) • Hypercholesterolémie – Zvýšený počet destičkových agregátů [17], Zvýšení syntézy tromboxanu A 2 [17], Zvýšení tvorby trombinu [17], Pokles antitrombotického efektu ASA [17] – Pokles cholesterolu je jedním z faktorů snížení ASA rezistence [17] (Význam výživy na snížení inzulinorezistence aj. ) • Hyperkoagulační stav po akutním IM, při nestabilní angíně pektoris, aortokoronáním by passu (Nižší senzitivita na antitrombotika od 7 dnů do 3 měsíců) [17] BUNĚČNÁ: • Regenerovaná, neinhibovaná COX 1 v jaderdných buňkách • Zvýšená exprese COX 2 m. RNA • Vyšší hladiny noradrenalinu • Tvorba izoprostanoidů 8 iso PGF 2 alfa vlivem neenzymatické peroxidace • Vyšší trombocytární obrat v kostní dřeni (reakce na krevní ztráty – např. po koronárním bypassu, u diabetiků) • Zvýšená senzitivita destiček na kolagen, stimulaci erytrocyty, trombinem aj. [17] GENETICKÁ: • Polymorfismus COX 1 (X acetylace serinu v oblasti katalytického místa COX 1), COX 2, tromboxan A 2 syntázy • Polymorfismus GPIa/IIa, Ib/V/IX a IIb/IIIa receptorů • Polymorfismus kolagenového receptoru • Polymorfismus receptoru pro von Willebrandův faktor • Polymorfismus f. XIII Val 34 Leu (inhibice aktivace f. XIII při terapii ASA) [17] ASA ze 100 mg až na 325 mg /d

Aktivace trombocytů a klopidogrel Selektivně ireverzibilně inhibuje vazbu ADP na jeho destičkový receptor GPIIb/IIIa a jeho aktivaci Klopidogrel duálně s ASA (akutní + subakutní KV až 1 rok) / alternativa při rezistenci či intoleranci ASA • Rezistence často i na oba léky současně [6] (až 50% pac. Rezist. K ASA je rez i ke klopidogrelu). Rezistence ke klopidogrelu (cca 30%): „Loading D“ z 300 mg na 600 mg/d • Nedostatečná bioaktivace • 85 % proléčiva degradováno esterázami Udržovací D ze 75 mg na 150 mg/d • Inhibice konvertujících enzymů: • Oxidáza P 450 izoenzymy: CYP 2 C 19 • Polymorfismus CYP 2 C 19*2 a CYP 2 C 19*3 a (CYP 2 C 19*4, *5, *6, *7 a 8 ) • (cca 30 % popul. ) konverze velmi pomalá • Inhibice jinými medikamenty: • Omeprazol (dostupnost o 40 45% klopidogrelu nižší a efekt na antiagregaci o 21 39% nižší) a esomeprazol (pantoprazol nevadil) • Fluvoxamin, fluoxetin, moklobemid, vorikonazol, flukonazol, tiklopidin, ciprofloxacin, cimetidin, karbamazepin, oxkarbazepin a chloramfenikol Prasugrel (Effient, Efient ) a tikagrelor • CYP 3 A 4 (Brilinta, Brilique, Possia ) x klopidogrel • Inhibice konverze SSRI, antimykotiky, grapefruitovou šťávou (Plavix): • CYP 2 B 6, 1 A 2 a 1 A 1 • Menší výskyt rezistence • Transferáza paroxonáza • Menší nebezpečí interakcí • Pomalý nástup účinku • Rychlejší nástup účinku • Eliminační pumpa – glykoprotein P (P-gp) • Aktivitou rozdíly v dostupnosti více než 2 násobné. Při chronické medikaci vznik rezistence až u 15% pacientů. • Genotyp 3435 T/T P gp vysoká aktivita

Degranulace trombocytů • Denzní granula – obsah potencuje aktivaci, adhezi a agregaci trombocytů, vazokonstrikci – ADP, ATP, Ca 2+ ionty a serotonin, trombin, TXA 2, epinefrin, k. arachidonová [5] • A-granula (potencují hemokoagulaci) – – – – v. WF Inhibitory degranulace = x aktivace a stabilizace trombc. Fibrinogen • Inhibitory produkce a signalizace TXA 2 Fibronectin • ASA aj. • Stabilizace trombocytu Trombospondin • + c. AMP, c. GMP Vitronectin aj. • + syntézy c. AMP stimulací adenylátcyklázy FV • x degradace c. AMP inhibicí fosfodiesterázy (PDE) PAI Destičkový růstový faktor 4 (PGDF 4) • Lysozomy – hydrolytické enzymy
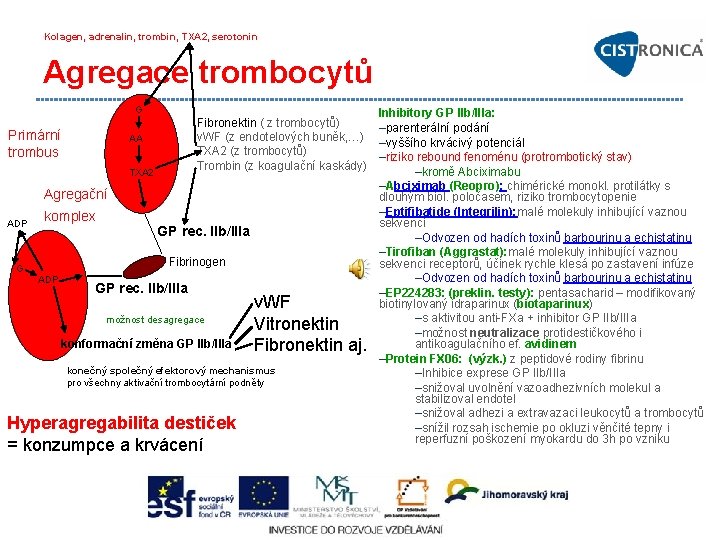
Kolagen, adrenalin, trombin, TXA 2, serotonin Agregace trombocytů G Inhibitory GP IIb/IIIa: Fibronektin ( z trombocytů) –parenterální podání Primární v. WF (z endotelových buněk, …) –vyššího krvácivý potenciál AA TXA 2 (z trombocytů) trombus –riziko rebound fenoménu (protrombotický stav) Trombin (z koagulační kaskády) –kromě Abciximabu TXA 2 –Abciximab (Reopro): chimérické monokl. protilátky s Agregační dlouhým biol. poločasem, riziko trombocytopenie –Eptifibatide (Integrilin): malé molekuly inhibující vaznou komplex ADP sekvenci GP rec. IIb/IIIa –Odvozen od hadích toxinů barbourinu a echistatinu –Tirofiban (Aggrastat): malé molekuly inhibující vaznou Fibrinogen sekvenci receptorů, účinek rychle klesá po zastavení infúze G –Odvozen od hadích toxinů barbourinu a echistatinu ADP GP rec. IIb/IIIa –EP 224283: (preklin. testy): pentasacharid – modifikovaný biotinylovaný idraparinux (biotaparinux) v. WF –s aktivitou anti FXa + inhibitor GP IIb/IIIa možnost desagregace Vitronektin –možnost neutralizace protidestičkového i konformační změna GP IIb/IIIa antikoagulačního ef. avidinem Fibronektin aj. –Protein FX 06: (výzk. ) z peptidové rodiny fibrinu konečný společný efektorový mechanismus –Inhibice exprese GP IIb/IIIa pro všechny aktivační trombocytární podněty –snižoval uvolnění vazoadhezivních molekul a stabilizoval endotel –snižoval adhezi a extravazaci leukocytů a trombocytů Hyperagregabilita destiček –snížil rozsah ischemie po okluzi věnčité tepny i reperfuzní poškození myokardu do 3 h po vzniku = konzumpce a krvácení

Mutace GP IIIa, II, I aj… Fibrinogenový receptorový protein destiček zodp. za agregaci. • GPIIIa eprimován i v endotelu jako součást vitronektinových receptorů zodpovědných za hyperplazii intimy. – Účinnost ASA v antiagregaci je v. s. též úměrná množství exprimovaných GP IIb/IIIa – Mezi pacienty s ICHS rezistence k ASA: • 100 mg ASA/d : 12, 1% - 15. 2% dle užití biochemické metody • 200 mg ASA/d : 7, 6 % v ČR – 10. 3 % v USA , 7, 1 % bělochů , 16, 5 % hispánců , 3, 7% Asiatů HPA-1/Pl A 1/A 2 polymorfizmus destičkového GPIIIa • Destičky jedinců s alelami A 2 více váží fibrinogen a více agregují. (Roos et al. 1999) proti A 1 homozygotům • A 2 alely jsou asociovány s vyšším rizikem IM před 60. rokem věku a komplikacemi po bypassových OP • Rizikový faktor pro koronární trombózu a náhlou srdeční smrt HPA-2 (Thr 145 Met) polymorfizmus destičkového GPIb α • GPIb α V IX complex k adhezi trombocytů na fisury v plátech plaků, mutace mění vazebné místo k trombinu • Nosiči Met alely mají vyšší aktivaci destiček mechanickým stresem (Douglas et al. 2000) C 807 T polymorfizmus destičkového glycoproteinu GPIa • GPIa/IIa receptory pro vazbu ke kolagenu • T alela je asociovaná s vyšším množstvím receptorů (Kritzik et al. 1998) • TT genotyp v. s. zvyšuje riziko IM (Moshfegh et al. 1998) Polymorfizmus GPIa/IIa, Ib/V/IX, a IIb/IIIa receptoru - Mutace GP IIIa - 59 P/L (196 C/T) - Aspirinová rezistence

Trombocyty a trombofilní stavy Trombocytémie – trombocytóza: Funkce trombocytů může být inhibována, např. : • Červené víno • Vitamín E • Rybí olej • Česnek • Hnědá mořská řasa Laminaria japonica • F fucoidan stimuluje endotel k produkci PGI 2 – snižuje agregaci tr. ) PMID: 23374164 • Tymián a rozmarýn • V. s. přímá inhibice trombocytů PMID: 15850964[Pub. Med] • Špenátové saponiny • více mechanismů inhibice agregace PMID: 21631362 • Kurkumin – zvyšuje tvorbu PGI 2, inh. agregaci trombc. • Zázvor – inhibice synt. TX 2 • Arganový olej • Cibule Vařením v páře rychle ztrácí antidestičkovou aktivitu • Esenciální trombocytémie (ET) • Myeloproliferativní nemoci • CML, polycytemia vera, myelofibróza (poč. stadia) • Anagrelid (Tromboreductin, Xagrid) • Silný inh. PD, snižuje velikost a euploidii megakaryocytů v postmitotické fázi zrání • Hydroxyurea • Nádory jater (trombopoetin – prod. játry, vs. stim. IL 6) • Zánětlivá onemocnění: Kawasakiho nemoc, dermatitidy, nespecifické zánětlivé onem. střev, revmatoidní artritida, nefrotický syndrom, pneumonie, sepse, meningitida, infekce močového traktu, septická arthritida • Nedostatek železa, st. p. velkém krvácení • http: //www. nutritionj. com/content/11/1/76 • Zhoubné nádory: sarkom měkých tkání, osteosarcom • Betulin (Betulinic acid) • z břízy bělokoré (Betula pubescens), Jujuba čínská (Ziziphus • Hyposplenismus / st. p. splenektomii / asplenie mauritiana), černohlávek obecný (Prunella vulgaris), • Iatrogenně medikací: eltrombopag, romiplostim masožravé květiny trifid štítnatý a liány Ancistrocladus heyneanus, Diospyros leucomelas, liána Tetracera boiviniana, Syzygium formosanum, kdoulovec čínský (Chaenomeles sinensis), rozmarýn, koniklec obecný (Pulsatilla chinensis). • Mango ginger (Curcuma amada Roxb. ) rhizome • Vitamin C Trombocyty - hlavní role v hyperkoagulaci v arteriálním řečišti: • CMP, infarkty, periferní ischemie atd. Vzácně i v oblasti venózní a mikrocirkulační: • TTP (Trombotická Trombocytopenická Purpura) • HUS (Hemolyticko Uremický Syndrom) Některé látky zlepšující periferní prokrvení též inhibují funkci destiček: • HELLP (Hemolysis, + Liver enzymes, Low Platelet count) • Pentoxifylin, naftidrofuryl, ketanserin (antag. 5 HT rec. ) • HIT II (Heparinem Indukovaná Trombocytopenie) • Nitráty, molsidomin aj. atd.

Další látky inhibující agregaci trombocytů Oligopeptidy z vaječného bílku • Inhibovaly ADP indukovano agregaci trombocytů bez vlivu na koagulaci a redukovaly TXB 2 a syntézu PGE 2 po stimulaci lipopolysaccharidy Polyphenols – inh. Agregace mnoha mechanismy • Inhibice COX, lipoxygenázy (Schubert et al. 1999; Hong et al. 2001) • Inhibice phosphodiesteázy (Dell'Agli et al. 2005) – Vzestup c. AMP či c. GMP snižuje Ca 2+ v trombocytech a jejich aktivaci (Demrow et al. 1995) • Skavenging ROS (Frei & Higdon, 2003). Inhibice peroxidace lipidů (Aviram et al. 2002) • Pokles phospholipázy C (Pignatelli et al. 2000) • Interakce s l arginine–nitric oxide met. cestou – vede k produkci NO endotelem (Andriambeloson et al. 1997) • Infračervené záření / fermentace – mohou uvolnit některé kovalentně vázané fenolické sloučeniny a zvýšit tak jejich aktivitu – Ozáření sezamových semen signifikantně zvyšuje množství volné 4 CA (Lee et al. 2005) Šťáva z grepu (7 ml/kg per d) během 2 týdnů • Pokles tvorby superoxidových aniontů trombocyty a pokles agregace, vzest. NO, snížená aktivita protein kinázy C (Freedman et al. 2001) Grepová semínka a slupky společně • Vysoký antidestičkový efekt (Shanmuganayagam et al. 2002).

Další látky inhibující agregaci trombocytů • Červené víno (Pignatelli et al. 2002) • Resveratrol, phytoalexin – antidestičkové vlivy • V konc. 3, 56 mg/l snižuje agregaci destiček o 50 % u zdr. dobrovolníků (Bertelli et al. 1995) • Inhibuje trombinem indukovanou produkci ADP a ATP sekreci z trombc. (Kaneider et al. 2004) • Quercetin Inhibuje collagenem indukovanou agregaci a adhezi tromb. (Pignatelli et al. 2000; Kikura et al. 2004). • Inhibuje agreg. Tromboc. , uvolnění hydrogen peroxidových radikálů z trombc. Po stimulaci kolagenem, (skoro uplně když s katechinem) Inhibuje trombinem indukovanou produkci ADP a ATP sekreci z trombc. (Kaneider et al. 2004) • Katechin inhibuje agreg. Tromboc. , uvolnění hydrogen peroxidových radikálů z trombc. Po stimulaci kolagenem, • P-Coumarinová kyselina (3 -(4 -hydroxyphenyl)-2 -propenoic acid; 4 CA) • Ve vínu, cereáliích, ovoci a zelenině (ubiquitérní rostlinný přechodný metaoblit při syntéze mnoha fenolů (Clifford, 2000) • Jablka, bobulovité ovoce (69– 1700 mg/kg) kukuřičné otruby (2· 9 g/kg) (Stich, 1991; Clifford, 2000; Zhao et al. 2005). • Inhibovala ADP indukovanou agregaci destiček bez vlivu na koagulaci, snižovala produkci TXB 2 a agregaci vyvolanou AA a ADP po 2 tý. Podávání (Clifford, 2000) • Antioxidační a protizánětlivé vlastnosti (Guglielmi et al. 2003; Luceri et al. 2004). • Podání 4 CA (5 mg/kg/d) signifikantně zvyšuje antioxidační kapacitu plazmy po 1 tý. podávání, ještě více po 3 tý. • Silný inhibitor oxidace LDL in vitro (Satué Gracia et al. 1999; Morton et al. 2000). Owen et al. (2000) • Antioxidační aktivita 4 CA proti ROS produkovaným hypoxanthin/xanthin oxidázou • Schopnost redukovat poškození DNA ox. Stresem vlivem železa a kumenových hydroperoxidů • Akutní zánět střevní sliznice po dextran sulfátu sodném nevznikne po předchozím podání 4 CA (50 mg/kg) (blokádu COX 1 a 2) • Denní příjem všech cinnamátů a derivátů hydroxybenzoové kyseliny je asi 1 g/d = cca 15 mg/kg/d muže (Clifford, 2000; Tomàs Barberan & Clifford, 2000) • 4 CA je aktivně transportována z GIT v kolon transportérem Caco 2 cells, vylučována je do moči

Kombinační terapie – duální protidestičková terapie ASA + klopidogrel • Bez manifestního aterosklerotického postižení je kombinační léčba s klopidogrelem nevhodná • St. p. koronární příhodě významné snížení výskytu KV příhod recidiv infarktu myokardu / post IM u mladých • Max. efekt v akutní a subakutní fázi, racionálně až 1 rok – ale nákladná terapie – Výběr jen nejrizikovějších pacientů stran KV (např. OA častějších recidiv příhod či při prokázané rezistenci na jinou protides tičkovou léčbu). • Dlouhodobý efekt po koronární angioplastice a po výkonu na více tepnách přínosem • 1. 3 měs. terapie po CMP (zvýš. Riziko krvácení ve studii bylo až později) Inhibitory receptorů GP IIb/IIIa + ASA + heparin • Abciximab, tirofiban či eptifibatid • Příznivý efekt na pokles KV příhod i mortality Aggrenox (2 x denně 25 mg ASA + 200 mg dipyridamol) • „Pro efekt ASA je důležitá vrcholová koncentrace léku, té však 25 mg ASA nedosahuje. Naopak její podání ve dvou denních dávkách může déletrvajícím útlumem prostacyklinu efekt snížit. “ – Neúčinná dávka ASA !!! na antiagregaci, jen zhoršení funce endotelu • Konverze k. arachidonové vlivem COX na cyklické endoperoxidy (CEP) PG H 2 není zablokována plně – PGI 2 (prostacyklinu) a PGE 2 (zdravý endotel) – snížení produkce – Tromboxansyntetázou na PXA 2 poté TXA 2, TS (akt. trombocyty) – nedostatečná inhibice • „Jediným významným byl snížený výskyt iktů a tranzitorních atak. Metaanalýza doložila významný pokles cerebrovaskulárních příhod řádově o desetinu, nikoli však ischemických komplikací v jiné lokalizaci. “ [6] • „Kombinace ASA s dipyridamolem je stejně účinná v sekundární prevenci mozkových příhod jako monoterapie klopidogrelem, je však zatížena mírně vyšší incidencí významných krvácivých příhod. “ [6]

Kombinační terapie Antikoagulancia + protidestičková léčba po akutních koronárních příhodách (IM, akutní koronární syndrom aj. ) • Jsou silnější alternativou prve zmiňované ASA + klopidogrel 1. rok (a dále jen ASA) Warfarin + ASA / clopidogrel (velmi rizikové případy ateroskl. dle někt. odborníků ano, dle jiných ne) • OASIS-p 1, CHAMP či CARS: nízká fixní dávka 3 mg warfarinu / nízké INR= suboptimální D antikoagulancia kombinace byť v kombinaci s ASA, není účinná • Evidence Based Medicine: ASA + warfarin u rizikových nemocných = po koronární příhodě = postup racionální • Proč se kombinace ASA + warfarin nerozšířila: – Dospěje li nemocný k recidivě infarktu myokardu, pak se spíše jedná o přirozený průběh choroby • Nikdo nikomu nic nevyčítá… – Objeví li se krvácení po léku, pak je „na vině" lékař • Nezvážit kombinaci ASA + warfarin u nemocného s vysokým rizikem recidivy aterotrombotické příhody při nízkém riziku krvácení může vést k nepřímému poškození nemocného z pohledu nevyčerpání všech léčebných možností !!! – možnost testování typu metabolismu warfarinu (polymorfismus CYP 2 C 9 a VKORC 1 – cca 8% populace nosí 3 4 zmutované alely ) ještě před zahájením terapie » podání bezpečnější, ale dražší terapie u vybraných pacientů (inh. f. II nebo X) – možnost domácího monitorování INR V budoucnu: • Nová antiagregancia/antitrombotika: antagonisté P 2 Y 12 receptoru: Prasugrel, Cangrelor, AZD 6140 • Nová antikoagulancia místo warfarinu: xabany a gatrany • Vyšetření rezistence k ASA a klopidogrelu bude rutinní metodou k nastavení optimální terapie u každého pacienta podstupujícího PCI

Erytrocyty a koagulace Počet a funkce erytrocytů také vliv na koagulaci a trombotická onemocnění: • Delší čas krvácení může být zkrácen podáním erymasy • Polycythemia vera – často komplikována trombózami • Sekundární polycytemie: • Nádory ledvin s patol. nadprodukcí erytropoetinu • Ischemie ledvin – produkce erytropoetinu v reakci na sníženou dodávku O 2 – Chronické nemoci plic s nízkou saturací krve O 2 » Těžcí kuřáci s CHOPN, nádory plic, …aj. • Změna ery membrán - externalizace phosphatidylserinů (PS) a mikrovezikulů s PS v membránách – Aktivace koagulace, agregace i trombc. , adheze bu. , clearance nezralých ery, vyšší adhezivita ery – PS na ery = místo pro přisednutí prothrombinázových a tenázových komplexů ke generaci IIa – Indukce expozice PS na ery: • Aktivace Protein kinázy C (PKC) • ATP deplece • Vzestup intra erytr. Ca – Via: ARA, PGE 2, LPA – Lysophosphatidová kys. » LPA: fosfolipid uvolněn z akt. trombc. , ovlivňuje: mitogenezi, invazivitu nádorů, retrakci neuritů, vývoj mnoha buněk do mastocytů, hojení, aterogenní a trombogenní molekula, kt. může zhoršovat KV nemoci (hypertrofie hladké svaloviny, agregace trombocytů a proliferace fibroblastů) • Srpkovitá anemie, talasemie aj. defekty stavby ery = trombotické komplikace
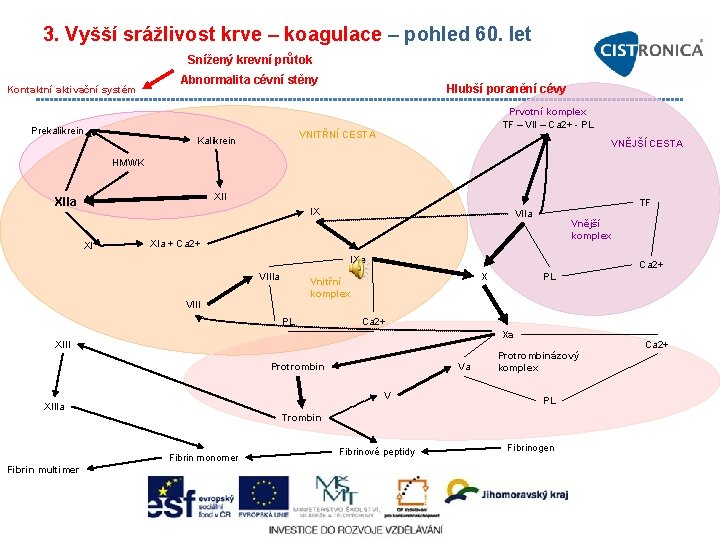
3. Vyšší srážlivost krve – koagulace – pohled 60. let Snížený krevní průtok Kontaktní aktivační systém Prekalikrein Abnormalita cévní stěny Hlubší poranění cévy Prvotní komplex TF – VII – Ca 2+ PL VNITŘNÍ CESTA Kalikrein VNĚJŠÍ CESTA HMWK XIIa TF IX XI VIIa Vnější komplex XIa + Ca 2+ IXa VIIIa Ca 2+ X Vnitřní komplex VIII PL PL Ca 2+ Xa XIII Protrombin Va V XIIIa Ca 2+ Protrombinázový komplex PL Trombin Fibrin monomer Fibrin multimer Fibrinové peptidy Fibrinogen

Fáze koagulační kaskády – buněčný model Iniciační fáze • TF – tkáňový faktor transmem. glykoprotein v mem. vezikulách akt. endotelu a monocytů (stimulace P selektinem, cytokiny, endotoxiny, imunokomplexy) – aktivací uvolnění a vazba na aktivované trombocyty • primární aktivátor koagulace • TF+VII → TF+VIIa → a. IX, a. X (inhib. a. X TFPI a antitrombinem III po uvolnění se a. X z komplexu do plazmy) • Xa → Va (+ z aktivov. destiček) → tvorba malého množství trombinu na buňkách s TF (i na lipoproteinových partikulích) – Nedostačuje pro přeměnu fibrinogenu na fibrin – Významný pro pokračování koagulace a další aktivace destiček Amplifikační fáze • Když už je vytvořen dostatek trombinu, probíhá aktivace trombocytů a kofaktorů asociovaných s trombocyty na povrchu adherovaných destiček po jejich aktivaci vytvořeným trombinem. – Trombin aktivace trombocytů a chemoatrakce + adheze k X endotelu • Degranulace tr. – uvolnění f. V • f. VIII v krvi vázán na v. WF – vazba na trombocyty a aktivace f. VIII – předání na PL trombocytu • XI navázán na PL a aktivován trombinem • Vyvázání faktorů aktivovaných na povrchy aktivovaných trombocytů vytvoření dostatečného množství protrombinázy • Účastní se f. V, VIII a XI po své aktivaci působí jako katalyzátory Propagační fáze • Na povrchu aktivovaných trombocytů a dalších buněk v okolí (i erytrocyty aj. ) • XIa aktivuje volný f. IX na povrchu aktivovaných trombocytů. Vznikne množství koagulačně aktivních komplexů tenáza a poté protrombináza produkující dostatečné množství trombinu pro přeměnu fibrinogenu na fibrin (Pecka, 2004)
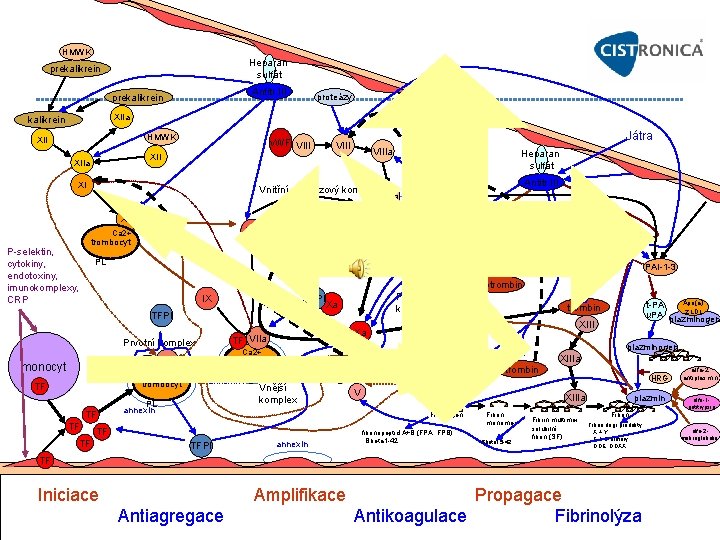
HMWK Heparan sulfát prekalikrein Antitr. III prekalikrein proteázy XIIa kalikrein Trombomodulin HMWK XII v. WF VIIIa XIIa XI Heparan sulfát Antitr. III Vnitřní – tenázový komplex VIIIa annexin IXa XIa IXa Ca 2+ P selektin, cytokiny, endotoxiny, imunokomplexy, CRP Játra trombin X X trombocyt Ca 2+ trombocyt Ca S PL trombin antitrombin komplex, TAT PL TAFI PAI 1 3 protrombin IX TFPI Xa TFPI TF VIIa Prvotní komplex Ca 2+ TF VII monocyt Ca 2+ trombocyt TF TF Xa trombocyt annexin PL PL annexin Protrombinázový komplex protrombin Xa Ca 2+ Va trombocyt annexin PL V Vnější komplex V V TF TFPI annexin XIII plazminogen XIIIa trombin Fibrinogen fibrinopeptid A+B (FPA, FPB) Bbeta 1 42 Apo(a) t PA z LDL u. PA plazminogen trombin HRG XIIIa Fibrin monomer Bbeta 15 42 Fibrin multimer solubilní fibrin (SF) plazmin Fibrin degr. produkty X + Y E + D dimery DDE, DDXX TF Iniciace Antiagregace Amplifikace Propagace Antikoagulace Fibrinolýza alfa 2 antiplasmin alfa 1 antitrypsin alfa 2 makroglobulin

Hyperkoagulační stavy • 1. Vzestup aktivity koagulačních faktorů – TF, F VII, IX, X, II, F VIII, V, XII, XIII • 2. Pokles aktivity inhibitorů koagulace – Sprot. , C prot. , APC, Z prot. , AT, trombomodulin, TFIP, … • 3. Snížení aktivity fibrinolytického potenciálu – Plasminogen, t-PA, … • 4. Vzestup antifibrinolytické aktivity a tvorby fibrinu – Fibrinogen, TAFI (trombinem aktivovaný fibrinolytický inhibitor), PAIs, … • 5. Jiné, vzácnější příčiny – Hyperviskózní syndrom • Paraproteinemie aj. • 6. Kombinace jmenovaných: Estrogeny: • HAK • Vyšší: f. II, VII, IX, X • Těhotenství: • Vyšší: Fibrinogen, VIII, IX, X, trombocytémie • Nižší: prot. S

TF - Tkáňový faktor – f. III - CD 142 (nepřesně tkáňový tromboplastin) Lokalizace: subendotel, trombocyty, leukocyty, monocyty, endotel (po stim. TNF alfa) obvykle není v kontaktu s krví Funkce: Iniciační molekulou v koagulační kaskádě – receptor pro VII. • Důležitým prozánětlivým cytokinem. Signální funkce komplexu TF/VIIa v angiogenezi a apoptóze. Vysoká aktivita TF: Záněty obecně, akutní koronární syndrom (s horší prognózou) Uvolnění TF u septických stavů spouští obávanou intravaskulární koagulaci – DIC !!! Inhibice TF: Grepová šťáva, vit. E – interferuje s aktivací vit. K dep. koagulačních f. a inh. monocytární expressi TF (PMID: 22860586), • Inhibitor tkáňového faktoru (Tissue factor pathway inhibitor – TFPI) (TEPI dříve) – Prot. Akutní fáze. , proteázový inhibitor vázán na HDL-LDL-VLDL částice a LP(a), 10% vázáno na trombocyty (uvolněné po stimulaci f. IIa) a na endotel (2 3 vyšší koncentrace na endotelu než v cirkulaci). Silně uvolňován z endotelu po podání heparinu – Tvoří komplexy s faktory Xa a VIIa (a Ca 2+) – (f. Xa dependentní inhibitor f. VIIa) významně inhibuje tak zevní cestu koagulace – Tvoří komplex s: TF, f. VII a reverz. Inhibuje Xa. – Indukuje reverzibilní vazbu Xa na monocyty (monocytární proteázy mohou opět uvolnit Xa – koagulační potenciál monocytů). • Extrakty ze slupek stolních italských grepů inhibují TF uvolněný monocyty – Vyšší aktivita: u daných hyperlipidémií (snížena terapií simvastatinem), u zánětů (sepse), malignit žaludku, colon, pankreatu aj. , DIC – Deficit TFPI: Konsumpce při DIC (sepse, šok) • Po přerušení terapie i. v. nefrakcionovaným heparinem (ne nízkomolekulárním hep. ) – rebound fenomén – snižování účinku heparinu • Asociován s rizikem trombotických uzávěrů nad poškozenou intimou / prasklými aterosklerotickými pláty • Rekombinantní TFPI – Tifakogin Studie neukázaly přínos podání tifakoginu při septických stavech • Antikoagulační proteiny z nematod Testovány u nestabilní anginy pectoris (ANTHEM/TIMI 32) • Protilátky proti TF • Protilátky proti komplexu TF: FVIIa (NAPc 2) Preklin. výzkum
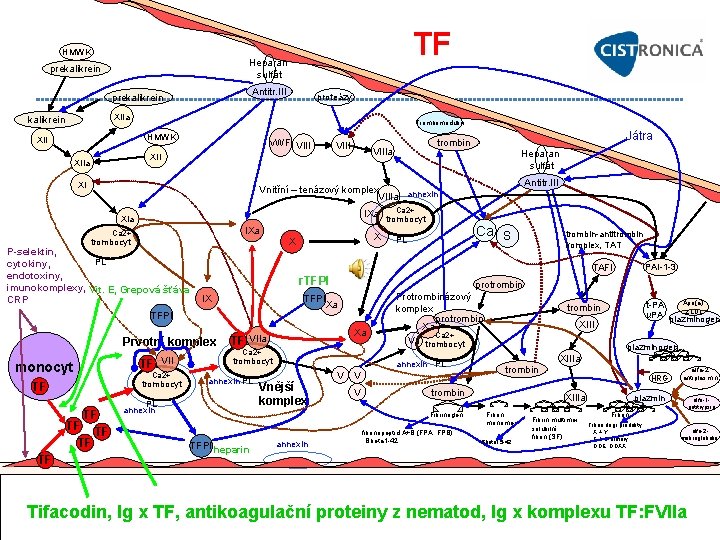
TF HMWK Heparan sulfát prekalikrein Antitr. III prekalikrein proteázy XIIa kalikrein Trombomodulin HMWK XII v. WF VIIIa XIIa XI Heparan sulfát Antitr. III Vnitřní – tenázový komplex VIIIa annexin IXa XIa IXa Ca 2+ P-selektin, PL cytokiny, endotoxiny, imunokomplexy, Vit. E, Grepová šťáva CRP X X trombocyt TF VII Ca 2+ trombocyt TF TF TF Ca S PL r. TFPI IX Prvotní komplex monocyt Ca 2+ trombocyt trombin antitrombin komplex, TAT TAFI TFPI Xa Xa TF VIIa Ca 2+ trombocyt annexin PL PL annexin Protrombinázový komplex protrombin Xa Ca 2+ Va trombocyt annexin PL Vnější komplex V V V TFPI heparin fibrinopeptid A+B (FPA, FPB) Bbeta 1 42 Apo(a) t PA z LDL u. PA plazminogen trombin XIII plazminogen XIIIa trombin Fibrinogen annexin PAI 1 3 protrombin TFPI TF Játra trombin HRG XIIIa Fibrin monomer Bbeta 15 42 Fibrin multimer solubilní fibrin (SF) plazmin Fibrin degr. produkty X + Y E + D dimery DDE, DDXX alfa 2 antiplasmin alfa 1 antitrypsin alfa 2 makroglobulin Tifacodin, Ig x TF, antikoagulační proteiny z nematod, Ig x komplexu TF: FVIIa

X - Stuart-Prowerové faktor Syntéza: játry – vit. K dependentní Funkce: Proteáza trombokináza, serinová endopeptidázya • Štěpí peptidové vazby v protrombinu na dvou místech (vazbu arg thr a pak vazbu arg ile) za vzniku aktivního trombinu – 1 Molekula Xa může aktivovat 1000 molekul trombinu Optimálně Xa s Va = protrombinázaový komplex • Společný uzel „vnitřní“ i „vnější“ cesty koagulační kaskády • Není zapojen do antitrombotického systému směřujícího k aktivaci proteinu C a S Aktivace: Vnější komplex, tenázový komplex, jed z Russelovy zmije (akt. i f. V), trocarin Inaktivace: PLA 2 a naniproin toxiny z jedu hada Naja nigricollis, tick anticoagulant peptide, antistasin; ixolaris a penthalaris z Ixodes scapularis, NAPc 2/3/4 z Ancyclostoma canium and A. ceylanicum, • Z protein dependentní proteázový inhibitor (ZPI) – Serinový proteázový inhibitor (serpin) – Afinita ZPI k Xa cca 1000 x vyšší za přítomnosti proteinu Z • Defekty v proteinu Z vedou ke zvýšené aktivitě faktoru Xa a zvýšenému riziku vzniku trombóz Inhibitory nepřímé – parenterální podání • Antitrombin s kofaktorem heparanem / heparinem (inaktivace Xa, trombinu, XIa, XIIa, tlumí i produkci cytokinů) Inhibitory přímé – xabany - p. o. , inhibice Xa i v protrombinázovém komplexu, není antidotum • Rivaroxaban - BAY 59 -7939 • Apixaban • Betrixaban II. fáze klinic. Zk. • Otamixaban i. v. , rychlý, plazmatický t 1/2 je 2– 3 h, • Razaxaban - Pro krvácivé komplikace zastaven • Edoxaban – III. f. klin. zk. , fixní D, není nutná monitorace, není antidotum • Darexaban – III. f. klin. Zk, fixní D, není nutná monitorace, není antidotum • Inhibitory na bázi aptameru RNA lze okamžitě inaktivovat aplikací oligonukleotidů Komplex aptamer protilátka se zkouší

Hepariny Inaktivace faktoru Xa pomocí heparinů je nepřímá = podmíněná přítomností antitrombinu a jeho přímou interakcí s f. Xa. • Nefunkčnost heparinu při nízké aktivitě antitrombinu !!! (Konzumpce při DIC, jaterní onemocnění, zánětlivé stavy aj. ) Nedostatečný efekt na inhibici faktoru Xa vázaného v protrombinázovém komplexu Neinaktivují trombin vázaný na fibrin po uvolnění z této vazby se koagulační kaskáda opět rozbíhá • Přímé trombinové inhibitory Inaktivace i již vázaného trombinu Inhibitory heparinů: laktoferrin (jeden z x proteinů akutní fáze…), protamin, avidin (deriváty heparinu) Účinnost heparinů vzrůstá se selektivitou k f. Xa: • UFH - Nefrakionovaný heparin – kontin. i. v. , poločas 1 2 h, vylučuje se močí – Cca 1000 x akceleruje vazbu AT II (více) a AT Xa a všechny další serinové proteázy (tím je inaktivuje) (kromě V, VIII) • Po vzniku komplexu TAT se heparin uvolní a váže se na další molekulu AT – Blokuje vazbu trombinu na destičkové GP Ib/IX/V – zpomaluje aktivaci. – Degradace: jaterní heparináza, vazbou na endotel a makrofágy, fibronektin, vitronektin, PDF, v. WF, prot. akutní fáze (!!!) – vyšší i při TEN – Riziko rebound fenoménu po zastavení infúze (uvolnění TF, deplece TFPI, uvolnění II vázaného na fibrin) – Kontrola účinnosti: a. PTT nad 1, 5 2 násobek, aktivita Xa. – Neutralizace: 1 mg protaminu na 1 mg heparinu (100 IU) – HIT – častěji po UHF: HIT I (hyperagrebilita trombocytů 3. 5. den), HIT II (protilátková, 5 21. den – akt. trombocyty+heparin+PDF 4+endotel – tvorba IIa a TEN komplikace ve 20% k amputaci DK, 3% úmrtí – terapie hirudin – ze slin Hirudo medicinalis) • LMWH: Bemiparin, Certoparin, Dalteparin, Enoxaparin, Nadroparin, Parnaparin, Reviparin, Tinzaparin – Menší vazba na plazmatické bílkoviny – předvídatelnější účinek, cca 90% biologická dostupnost při s. c. podání, 2 xd ter. (1 xd profyl. ), renální eliminace, malé riziko trombocytopenie (HIT) – Vyšší inaktivace Xa než nefrakcionovaný heparin – i selektivně inhibuje Xa i bez antitrombinu přímo – Uvolnění TFPI z endotelu (blokuje TF) – cca 10 x zvýšená hladina. Snižuje PAI, zvyšuje fibrinolýzu. – Nedovolí vazbu AT IIa (nedojde k inaktivaci trombinu) – Monitorace: lze měřit anti Xa aktivitu (obézní pac. , renální selh. ) – 0, 2 0, 5 IU prevntiv. , 0, 5 1, 2 IU terap. – Neutralizace: protaminem – stačí 50% D • Syntetické pentasacharidové inhibitory f. Xa (deriváty heparinu): nižší riziko HIT než u LMWH, nemá afinitu k PDF 4, renální eliminace, nepřímá selekt. Inh. Xa – Fondaparinux Ještě větší Xa selektivita než LMWH, poločas 17 h – Idraparinux biotinylovaný pentasacharid, plazmatický t 1/2 je 80 130 h. Vazba biotinu s tetramerem avidinem vede k inaktivaci (Klin. testy EQUINOX, CASSIOPEA) • Heparinoidy: Danaparoid, Dermatan sulfát, Sulodexid

Rivaroxaban - BAY 59 -7939 (Xarelto) • • • Vysoká perorální dostupnost (80 %) Plazmatický t 1/2 7– 11 h, podání 1 2 x d Max. plazmatickou koncentraci 2– 3 h po p. o. podání 1/3 játry: CYP 3 A 4, P-glykoprotein – KI: komedikace se silnými inhibitory: verapamil, azolová antimykotika, amiodaron, klarithromycin, ritonavir aj. 1/3 látky vyloučena nezměněna močí, 1/3 po metabolizaci močí – Delší doba eliminace nad 6– 9 h u starých pacientů a u pokročilé renální insuficience • KI: renální clearance pod 15 ml/ min RECORD 1 4: rivaroxaban 5 20 mg 1 xd 6 8 h postoperačně versus enoxaparin 40 mg 1 xd event. 30 mg 2 xd u operací velkých kloubů – Rivaroxaban: významně účinnější na snížení incidence všech prokázaných flebotrombóz (u výkonů na kolenním kloubu o 49 % a při výkonech na kyčli o 70 %), PE a celkové mortality, proximální trombózy, úmrtí na PE; krvácení stejně MAGELLAN: 10 mg rivaroxabanu denně 31– 39 dní u akutní interní choroby versus 40 mg enoxaparinu denně 6– 14 dnů – rivaroxaban non inferiorní v závěru podávání, ale při vyšším riziku vzniku krvácení EINSTEIN: Rivaroxaban v akutní fázi trombózy 15 mg 2 x d 3 týdny, pak 20 mg 1 x d po 3, 6 nebo 12 měsíců + hodnoc. Rekurence trombóz po roce x enoxaparinu a placebu – non inferiorita rivaroxabanu oproti enoxaparinu v léčbě flebotrombóz a PE EINSTEIN EXT: rivaroxaban x placebo (1, 3 % vs. 7, 1 %), 4 nemocní aktivně léčení významně krváceli, v placebové větvi nikdo ROCKET AF: 20 mg rivaroxabanu d X warfarin u fibrilace síní bez chlopenní vady (CMP / 2 RF v OA) – Ef. Terapie stejná, méně fatálních a intrakraniálních krvácení u rivaroxabanu ODIXa DVT – u flebotrombóz stejná regrese trombu i incidence TEN jako u enoxaparinu s antivitaminem K ACS ATLAS – TIMI 46: léčba akutních IM

Apixaban (Eliquis) • • • • P. o. , plazmatický t 1/2 je 8– 14 h, 1 2 xd Biologická dostupnost je vyšší než 45 % Blokuje volný i vázaný faktor Xa Maximální plazmatické koncentrace po 2 h Částečně metabolizován jaterním CYP 3 A 4 a glykoproteinem P – KI: komedikace s inhibitory: verapamil, azolová antimykotika, amiodaron, klarithromycin, ritonavir Částečně metabolizován v játrech a vylučován stolicí (asi 70 %) Částečně eliminován i ledvinami (25 %) EXPANSE ADVANCE 1 3: apixaban 2, 5 mg 2 xd, 12– 24 h post op v ortopedické profylaxi TEN: – Enoxaparin 30 mg 2 x d: vyšší ef. než apixaban – Enoxaparin 40 mg 1 x d denně: apixaban méně TEN komplikací i úmrtí ADOPT: TEN u interních pacientů: apixaban 2, 5 mg 2 x d 30 dnů X enoxaparin 40 mg 1 xd 6 – 14 dnů – Neprokázala superioritu apixabanu – Spojena s vyšším krvácením BOTTICELLI DVT: léčba flebotrombózy: apixaban 5 10 mg 2 x d, 20 mg 1 xd X nízkomolekulárnímu heparinu a warfarinu – Rekurence flebotrombózy / nárůst trombu u 4, 7 % u léčených apixabanem a 4, 2 % u konvenčně léčených AMPLIFY: ter. flebotrombózy apixaban 10 mg 2 x d 1 týden a následně 5 mg 2 x d X konvenční léčbě heparinem a warfarinem ARISTOTLE: prevence embolizací při fibrilaci síní: 5 mg apixabanu 2 x d X warfarin – Apixaban účinnější v prevenci iktu a systémové embolizace s menším rizikem krvácení AVERROES: apixabanem x ASA při intoler. / KI warfartaminu – Antikoagulační léčba byla účinnější v prevenci iktů a systémových embolizací při srovnatelném riziku krvácení APPRAISE 2: 5 mg apixabanu 2 x d + placebo / ASA + tienopyridin (stop)
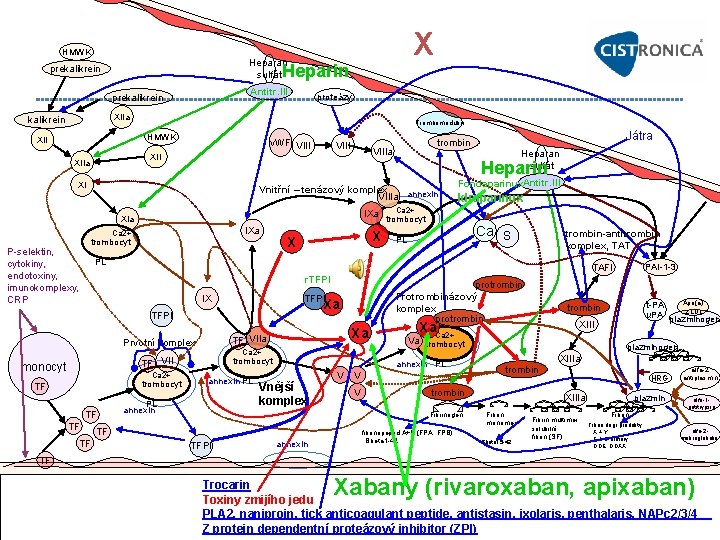
X HMWK Heparan sulfát Heparin prekalikrein Antitr. III prekalikrein proteázy XIIa kalikrein Trombomodulin HMWK XII v. WF VIIIa XIIa Heparan sulfát Heparin XI Vnitřní – tenázový komplex VIIIa annexin IXa XIa IXa Ca 2+ P selektin, cytokiny, endotoxiny, imunokomplexy, CRP Játra trombin trombocyt X X Fondaparinux. Antitr. III Idraparinux Ca 2+ trombocyt Ca S PL trombin-antitrombin komplex, TAT PL TAFI r. TFPI IX TFPI Xa TFPI Ca 2+ TF VII monocyt Ca 2+ trombocyt TF TF Xa TF VIIa Prvotní komplex protrombin Protrombinázový komplex protrombin trombocyt annexin PL PL annexin Vnější komplex V TFPI annexin plazminogen XIIIa trombin Fibrinogen TF XIII Va trombocyt V fibrinopeptid A+B (FPA, FPB) Bbeta 1 42 Apo(a) t PA z LDL u. PA plazminogen trombin Xa. Ca 2+ annexin PL V PAI 1 3 HRG XIIIa Fibrin monomer Bbeta 15 42 Fibrin multimer solubilní fibrin (SF) plazmin Fibrin degr. produkty X + Y E + D dimery DDE, DDXX alfa 2 antiplasmin alfa 1 antitrypsin alfa 2 makroglobulin TF Xabany (rivaroxaban, apixaban) Trocarin Toxiny zmijího jedu PLA 2, naniproin, tick anticoagulant peptide, antistasin, ixolaris, penthalaris, NAPc 2/3/4 Z protein dependentní proteázový inhibitor (ZPI)

II - trombin Protrombin prekurzor proteázy trombinu klíčového pro koagulaci, synt. V játrech, vit. K depend. Trombin: poločas cca 2, 8 + 0, 5 dne Funkce: Konverze fibrinogenu na fibrin. Aktivuje: f. V, XIII, VIII, trombocyty. Vázaný na trombomodulin aktivuje PC na a. PC [4] a TAFI • Aktivace PAR receptorů endotelu, im. buněk a neuronů. Chemotaxe a adheze granulocytů k endotelu, permeabilitu endotelu. • Významný vasokonstriktor a mitogen posthemoragické vazospasmy po subarachnoidálním krvácení může vést až k mozkové ischemii Aktivován: Willebrand factor binding protein (VWFBP) secernován Staphylokokem aureus, staphylocoagulázou, ecarin (z hadího jedu) • Inhibice aktivace II: bothrojaracin, bothroalternin (hadí toxiny) Inhibován: alfa 2 makroglobulin, Diallyl trisulfide (DAT) v česnekovém oleji PMID: 17123684, proteinázovým inhibitorem ze sojových bobů Inhibitory trombinu: Nepřímé • Antitrombin – slabá inhibice, cca 100 x silnější inhibice antitrombin + heparin Protrombinová mutace 20210 G-A - 11 p 11 -11 p 12: Glutamin – Neinaktivuje trombin vázaný na fibrin za arginin v pozici 20210 v promotoru genu pro faktor II [6] zvyšuje – Antidotum: protamin produkci protrombinu následně trombinu (f. II) – Heparinem indukovaná trombocytopenie (HIT) • Protrombin často nad 130 % (Poort, 1996). Vyšší hladina 150 200 % • Odiparcil, β-D-xylosid - Časné fáze klinického hodnocení [6] jen u části nosičů mutace. – Uvolňuje přirozené heparinoidy dermatan sulfát a chondroitin • Objevena r. 1996 u rodin se zvýšeným výskytem HŽT, TEN [4] Přímé • V ČR cca u 1 2% osob kavkazské populace. Heterozygoté [4] 2 3% • Inaktivovace i trombinu již navázaného na fibrin. Není antidotum [5] [6]. Itálie, Řecko, Izrael 4 5% populace heterozygoté [4]. Asie, • Inhibice trombinu vazbou v oblasti aktivního místa trombinu Afrika vzácně [4] – Středověk: po CMP se přikládaly pijavice – hirudin ze slin • 2. nejčastější mutace spojená s vyšším rizikem HŽT dospělých [4]. • Dnes hirudin z Hansenula (Thrombexx, Extrauma) Cca u 5 6% dospělých, kteří prodělali TE [4] 6, 3 % [6] 5 – 7, 3 % [7] – +krvácení než heparin, 0 antidotum – Rekombinantní analoga: Inj. Aplikace: Rizika: • Bivalentní bivalirudin, desirudin (Revasc/Iprivask) • TE [5] i v atypických lokalizacích: Mezenterické žíly, Mozkové splavy, – lepirudin (Refludan) (ex. 2012) V sítnici [4] • Univalentní – argatroban – ter. HŽT při HIT • TE v graviditě: 17 % TE vzniklých v těhotenství [6], – Haemadin, variegin – toxin z Amblyomma variegatum • Riziko pro spontánní aborty není potvrzeno [5]. Uvádí se asociace pro • Dabigatran etexilate (Pradaxa) – p. o. fetální ztráty [5] [6], abrupce placenty [5] [6] , preeklampsie [5] [6], • Ximelagatran (ex) 2006 stažen pro podezření z hepatotoxicity IUGR [5] [6] • Efegatran, Inogatran, napsagatran, melagatran (ex) žádné zprávy

Dabigatran etexilát – inhibitor trombinu (Pradaxa) • • • • T. č. jediný dostupný p. o. inhibitor IIa Přímá a reverzibilní inhibice P. o. podání. Metabolizován na aktivní substanci Rychlý nástupem účinku max. efekt za 1– 2 h Plazmatický poločas je 14– 17 h (1 x 220 mg ev. 2 x 150 mg) Substrátem efluxní pumpy – glykoproteinu P – Zvýšení hladiny dabigatranu o 50– 150 % při současném podávání inhibitorů tohoto transportéru • Verapamil, azolová antimykotika, amiodaron, klarithromycin Eliminace převážně renální – 80 % v nezměněné podobě – Při poklesu clearance kreatininu na 30– 50 ml/min dávku z 220 mg na 150 mg d – při poklesu filtrace pod 30 ml/min kontraindikován RE MODEL, RE NOVATE, RE MOBILIZE, RENOVATE II Profylaxe TEN u ortopedických operací velkých kloubů (220 mg 1 xd = superiorní nad enoxaparinem) RE COVER – méně krvácení než warfarin při TEN RESONATE snížení rizika rekurence TEN REMEDY non inferiorní, se snížením rizika velkého krvácení proti warfarinu RE LY s fibrilací síní v prevenci TEN BISTRO II
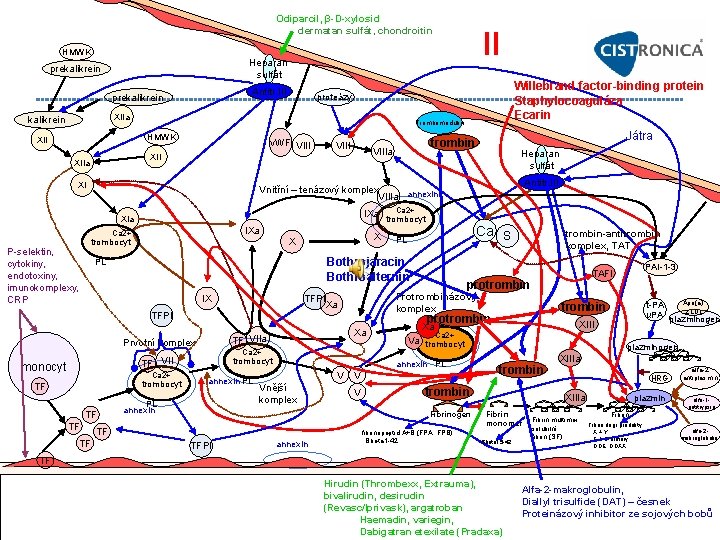
Odiparcil, β-D-xylosid dermatan sulfát, chondroitin II HMWK Heparan sulfát prekalikrein Antitr. III prekalikrein XIIa kalikrein Trombomodulin HMWK XII v. WF VIII XI Heparan sulfát Antitr. III Vnitřní – tenázový komplex VIIIa annexin IXa XIa IXa Ca 2+ P selektin, cytokiny, endotoxiny, imunokomplexy, CRP Játra trombin VIIIa XIIa Willebrand factor-binding protein Staphylocoaguláza Ecarin proteázy X X trombocyt IX TFPI Xa TF TF TF Xa TF VIIa Ca 2+ TF VII trombocyt protrombin trombocyt annexin PL PL annexin Xa Vnější komplex TFPI annexin plazminogen trombin Fibrinogen TF XIII Va trombocyt V V Apo(a) t PA z LDL u. PA plazminogen trombin Ca 2+ annexin PL V PAI 1 3 TAFI protrombin Prvotní komplex Ca 2+ trombin-antitrombin komplex, TAT Protrombinázový komplex TFPI TF Ca S PL Bothrojaracin Bothroalternin PL monocyt Ca 2+ trombocyt fibrinopeptid A+B (FPA, FPB) Bbeta 1 42 XIIIa HRG XIIIa Fibrin monomer Bbeta 15 42 Fibrin multimer solubilní fibrin (SF) plazmin Fibrin degr. produkty X + Y E + D dimery DDE, DDXX alfa 2 antiplasmin alfa 1 antitrypsin alfa 2 makroglobulin TF Hirudin (Thrombexx, Extrauma), bivalirudin, desirudin (Revasc/Iprivask), argatroban Haemadin, variegin, Dabigatran etexilate (Pradaxa) Alfa-2 -makroglobulin, Diallyl trisulfide (DAT) – česnek Proteinázový inhibitor ze sojových bobů

Další koagulační faktory podílející se na trombofilních stavech: Vyšší aktivita f. VII, včetně podání rekombinantního f. VII při zvýšené krvácivosti, u hyperlipidémií, při perzistencí prozánětlivého stavu, u inzulínové rezistence, po požití tučného jídla, u dialyzovaných pacientů a pac. s chronickou renální insuficiencí, různé polymorfizmy genu pro f. VII Vyšší aktivita f. V: ale i krvácivé stavy s deficitem f. V jsou protrombofilní stav, mutace f. V (Leiden) a jiné „APC rezistence“ Vyšší aktivita f. IX: rostě s věkem, zvýšen u někt. Mutací f. IX Vyšší aktivita f. VIII: Jiná než krevní skupina 0 vyšší hladiny FVIII i v. WF, hladina stoupá s věkem [3], vrozeně Vyšší aktivita f. XI: potencionální trombofilní stav Nižší aktivita f. XII: Získané deficience: Systémová zánětlivá odpověď, amyloidóza, nefrotický syndrom, inhibující protilátky (SLE, leukémie aj. ), DIC, ARDS, polycythemia vera, jaterní cirhóza aj. ; Vrozená deficience: Hagemanova choroba (John Hageman zemřel na PE) Vyšší aktivita v. XIII: např. XIII Val 34 Leu polymorfismus

AT - Antitrombin Játry (i iendotelem) produkovaný serpinový glykoprotein. Fyziologická koncentrace AT cca 140 mikrogramů/ml Funkce AT: Relat. silný antitrombotický efekt. Kofaktor pro heparin (bez AT je prakticky neúčinný) / heparan sulfát in vivo • Inhibitor serinových proteáz: f. IIa, XIa, XIIa, VIIa, kallikrein, plasmin, trypsin, podjednotky C 1 komlementu • Rozštěpená a latentní forma AT: silně inhibuje angiogenezi a růst tumorů ve zvířecích modelech Deficit AT: asi u 0. 02 0. 05 % jedicnů [7]. Pokles na 40 -50% může již způsobit trombotickou příhodu, • Rizika: TE: Cca 5 x častější [3], V komb. s p. o. HAK 8 x, Deficit antitrombinu u 1% HŽT • Získané deficience: U novorozenců a kojenců asi do 3 měsíců věku [3], Jaterní onemocněních [3], Nefrotický syndrom [3], Zvýšenou konzumpcí [3], Estrogeny snižují hladiny antitr. III (Dále zvyšují hladiny F VII, XII aj. ), sepse, předčasné narození, velké operace event. kardiopulmonalní bypass • Dědičné deficience: Mnoha bodovými mutacemi, delecemi a insercemi [4] – Většinou autozomálně dominantně [4]: Typ I Kvantitativní deficit [3], Typ II Kvalitativní deficit [3] – Heterozygotní forma deficitu antitrombinu • 1: 250 500 [3], Asi u méně než 0, 5 % lidí [3] prevalence jen 0, 02 % [4] [6] • TE: Nejčastěji v mladém dospělém věku [3], Cca u 3% pacientů s TE [3], Riziko rekurence TE vyšší, Riziko během života je 70 90 % [4] [6], V graviditě cca 60 % [4] [6], Jen zřídka příčinou komplikací v průběhu gravidity včetně opakovaných fetálních ztrát [4] – Homozygotní deficity • S aktivitou antitrombinu pod 10 % většinou neslučitelné se životem [3]. Velmi vzácné, Těžké trombotické příhody v prvních 10 letech života [3] • Zvýšená hladina AT: fucan Ib ze sea cucumber (Isostichopus badionotus) potencuje AT vliv na IIa a na f. Xa • Plazmatický koncentrát AT: Běžně dostupný, Lze použít při vrozeném či získaném deficitu AT [3] Heparin cofactor II (HCII) -"minor antithrombin" • Inhibuje IIa za přítomnosti heparinu nebo dermatan sulfátu (dříve nesprávně chondroitin sulfát B) • Vyšší aktivita HCII: Fucosylovaný chondroitin sulfát f. CS Ib ze „sea cucumber“ (Isostichopus badionotus), sulodexid • Deficience HCII – Mutacemi HCII vyšší hladiny trombinu hypercoagulační stav
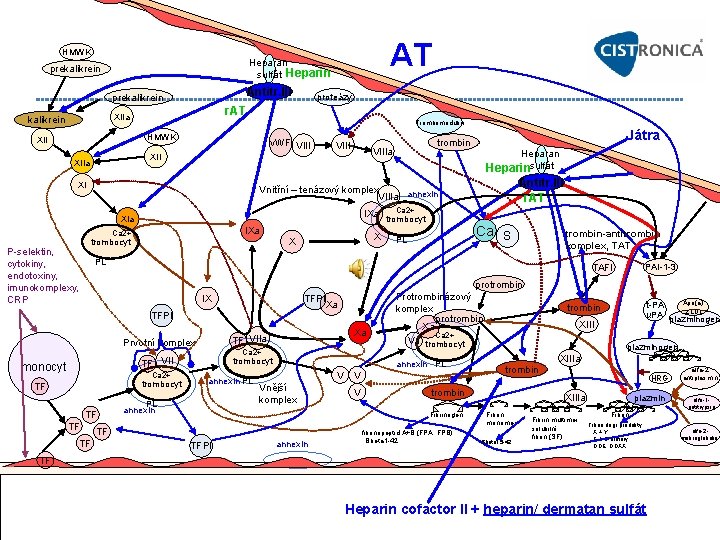
AT HMWK Heparan sulfát Heparin prekalikrein Antitr. III prekalikrein XIIa kalikrein Trombomodulin HMWK XII proteázy r. AT v. WF VIIIa XIIa XI Heparan Heparinsulfát Antitr. III r. AT Vnitřní – tenázový komplex VIIIa annexin IXa XIa IXa Ca 2+ P selektin, cytokiny, endotoxiny, imunokomplexy, CRP Játra trombin X X trombocyt Ca 2+ trombocyt Ca S PL trombin-antitrombin komplex, TAT PL TAFI PAI 1 3 protrombin IX TFPI Xa TFPI TF VIIa Prvotní komplex Ca 2+ TF VII monocyt Ca 2+ trombocyt TF TF Xa trombocyt annexin PL PL annexin Protrombinázový komplex protrombin Xa Ca 2+ Va trombocyt annexin PL V Vnější komplex V V TF TFPI annexin XIII plazminogen XIIIa trombin Fibrinogen fibrinopeptid A+B (FPA, FPB) Bbeta 1 42 Apo(a) t PA z LDL u. PA plazminogen trombin HRG XIIIa Fibrin monomer Bbeta 15 42 Fibrin multimer solubilní fibrin (SF) plazmin Fibrin degr. produkty X + Y E + D dimery DDE, DDXX TF Heparin cofactor II + heparin/ dermatan sulfát alfa 2 antiplasmin alfa 1 antitrypsin alfa 2 makroglobulin
![Protein S Funkce: • Kofaktorem proteinu C, Zvyšuje proteolytickou aktivitu a. PC [3] • Protein S Funkce: • Kofaktorem proteinu C, Zvyšuje proteolytickou aktivitu a. PC [3] •](http://slidetodoc.com/presentation_image_h/797eafd2c9a2f794c574d89b7e470045/image-49.jpg)
Protein S Funkce: • Kofaktorem proteinu C, Zvyšuje proteolytickou aktivitu a. PC [3] • Důležitý pro dostatečně rychlou fagocytózu apoptotických buněk (prevence vzniku autoimunity na intracelulární obsah) PMID: 15032696 [Pub. Med] Deficity proteinu S • TE: Vážné dificience způsobují život ohrožující trombózy, RR TE 2, 4 [3], Cca 3 8% případů všech TE [3] 1 5 % [7] • Pozdní fetální ztráty [2], SVT, ischemické CMP dětí při těžkých stavech [3] • Prevalence deficitu proteinu S: V běžné populaci ne přesně známá [3] 0, 1 2, 1 % [6], Asi vyšší, než v případě deficitu proteinu C [3] • Dědičné: – Kvantitativní (typ I), Kvalitativní (typ II) [3] , Vrozený trombofilní stav poprvé popsal r. 1984 Schwarz et al. [3] [7] – Heterozygoté • TE až v mladším dospělém věku I dříve, Včetně arteriálních TE [3], RR 10 x vyšší [7], RR 5 – 10 x v případě nižších hladin [7] – Homozygoté • Purpura fulminans v novorozeneckém věku [3] • Získané: – U dětí (koncentrace i aktivita nižší než u dospělých [3] ), v těhotenství, při užívání HAK s estrogeny, jaterní onemocnění, aj.

Deficit proteinu C = zvýšená koagulace krve = trombofílie smíšená (vrozená event. získaná) • • Asi u 0. 1 0. 5 % jedinců [2] prevalence 0, 2 0, 3 % [6] Zvyšuje riziko HŽT 9 x [2], 8 10 x [6] 10 x [7]. Vážné dificience způsobují život ohrožující trombózy • Získané deficience proteinu C: – – – • Dědičné – – • Protilátky proti proteinu C V dětském věku (až do dospívání [3]) plazmatické koncentrace proteinu C nižší než u dospělých Při jaterních onemocněních [3] Septických stavech: Typicky těžká meningokoková sepse [3] (neměřitelně nízké aktivity PC [3], trombo hemorhagický stav podobným purpuře fulminans [3] Terapie antagonisty vitamínu K (warfarin) – blok karboxylace glutamových zbytků v Gla části PC [7] • Rychlejší pokles PC (kratší plazm. poločas) než vit. K depend. koagulačních fakturů – Riziko vzniku trombóz v drobných cévkách = kožní nekrózy (obzvláště u jedinců s Leidenskou mutací či jinou APC rezistencí !!!) Poprvé popsáno Griffinem et al. v roce 1981 [7] Kvantitativní (typ I), Kvalitativní (typ II) [3] Knock out genu pro PC je asociován s umrtím myších embryí. Heterozygoté pro deficienci proteinu C: Méně než 0, 5% populace [3], většinou asymptomatický až do dospělosti [3] • TE: do 40 let věku cca 50% nosičů st. p. TE [3], RR cca 6 x vyšší [3] • SVT, ischemické CMP u dětí při vážném stavu (9. 31 OR, 95% CI 4. 81– 18. 02 metaanalýza 6 tis tudií [3] ) Homozygoté pro deficienci proteinu C: • Velmi vzácný, život ohrožující stav [3], Prenatálně úmrtím, Poškozením plodu, Po porodu purpura fulminans novorozenců krvácení, sepse, nekróza, DIC, Rychle progredující hemorhagické nekrózy kůže, podkoží i orgánů při trombotizaci cév [3], Vzácně až trombotickou příhodou ve starším věku [3] V kombinaci s jinými trombof. Stavy: FV Leiden [3], Deficit proteinu S [6], P. o. HAK, RR HŽT 15 x [6] Terapeutické možnosti: Plazmatický koncentrát PC, Rekombinantní aktivovaný PC – Zejména u novorozenců vedl ke zvýšenému riziku krvácení [3] U dětí se v současnosti neužívá [3] – Terap. dávky APC: Mohou zvednout APC z 1 ng/ml až na 500 ng/ml, Kontinuální infúze 4 96 h s nebo před podáním neutrálních glykolipidů

APC Funkce APC: hlavní antikoagulační cesta vedoucí k pokelsu produkce trombinu. Proteolyticky inaktivuje f. Va [3], f. VIIIa [3] • Ok hlaidna APC v krvi 2, 2 ng/ml, vyšší hladiny = zvýšená krvácivost Aktivace PC: Komplexem trombin trombomodulin [3] s kofaktorem proteinem S [3], EPCR • Trombomodulinová hladina je inverzně asociovaná s IM (Salomaa 1999). – Ala 455 Val polymorfismus v genu pro thrombomodulin • Cca 56 65% Ala, 32 36% Ala. Val a 3 8% Val. Ala alela souvisela s více IM (Norlund et al. 1997) – Zkoumané polymorfizmy trombomodulinu jen slabé asociace s IM – v. s. velmi slabé RF pro populaci – Absence trombomodulinu asociována s úmrtím myších embryí • HDL působí antikoagulačně kofaktor pro APC: protein S Zvýšení APC: Omega 3 MK (vč. alpha linolenic acid) • Phosphatidylcholine (PCh): hlavní fospholipid vázaný na lidský rozpustný Endoteliální PC Receptor (s. EPCR). Aktivitou s. PLA(2) V je PCh nahrazen lysophosphatidylcholinem (lyso. PCh) a (PAF) s. EPCR pak hůře váže a aktivuje PC na endotelu. – Enkrypce EPCR indukuje buněčnou APC rezistenci = ztráta cytoprotektivního efektu APC na buňky endotelu Drotekogin • přípravek s aktivovaným proteinem C. degradace f. Va a VIIIa. Indikace při ter. šokových septických stavů APC rezistence: u cca 3 5 % jedinců v populaci • Dědičná: – Cca v 90 95% na podkladě Leidenské mutace [3], Ostatní polymorfismy f. V. Vrozená APC resistance tvoří asi 50 % všech vrozených trombofilí • Získaná APC rezistence: – V těhotenství [3] [6] (Pokles proteinu S), Při podávání orálních kontraceptiv atd. , Deficit endogenního plasmatického Glc. Cer (Snížená antikoagulační účinnost APC), Protilátky proti APC, Snížením hladiny faktoru V [3] (Snížená hladina f. V + heterozyg. f. V Leiden = "pseudohomozygotní APC-R" [3] ), Při vysoké hladině faktoru VIII [4] [6], Při nízké hladině proteinu S [4] [6], Lupus antikoagulans [4] [6] • Rizika: APC R = cca 8 x vyšší riziko HŽT, APC R + p. o. HAK = cca 35 x vyšší riziko HŽT – Zahajovat léčbu akutní žilní trombózy přímo p. o. antikoagulancii bez překrytí heparinem se nedoporučuje – Riziko rychlého poklesu proteinu C a vzniku hyperkoagulačního stavu s rizikem kumarinové kožní nekrózy !!! • Platí i pro jedince s Leidenskou mutací !!! – Vyšší riziko ICHS a IM i při geneticky normálním f. V

Protein Z (PZ) a Z-dependentní proteázový inhibitor (ZPI) Protein Z (PZ) PROZ gen: Vit. K dependentní kofaktor, který urychluje Z dependentní proteázový inhibitor (ZPI) v inhibici f. Xa – na fosfolipidech membrán. V krvi komplexy PZ ZPI: výrazně zpomalují fázi iniciace • Deficit PZ: warfarin, vrozeně – důsledky: insufficience placenty, fetální ztráty, ischemické CMP, velmi rizikové v kombinaci s Leidenskou mutací [9] • Zvýšení PZ: HAK ZPI: serpinová proteáza. Bez nutnosti PZ přímo inhibuje f. XIa a mírně i IXa vnitřní Xázový komplex z IXa, VIIIa, fosfolipidů a Ca 2+. • Deficit ZPI deficit: vrozeně, warfarin (cca o polovinu): vážnější důsl. než deficit PZ – vč. TEN, IM, isch. CMP [9] • Zvýšení ZPI: HAK
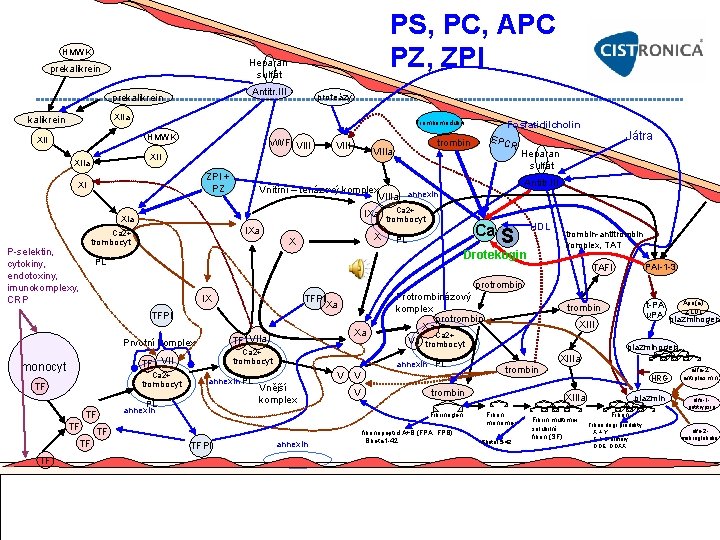
PS, PC, APC PZ, ZPI HMWK Heparan sulfát prekalikrein Antitr. III prekalikrein proteázy XIIa kalikrein Trombomodulin HMWK XII v. WF VIII ZPI + PZ XI IXa P selektin, cytokiny, endotoxiny, imunokomplexy, CRP X X trombocyt Ca 2+ trombocyt Ca PL S HDL Drotekogin PL trombin antitrombin komplex, TAT TAFI PAI 1 3 protrombin IX TFPI Xa TFPI Ca 2+ TF VII monocyt Ca 2+ trombocyt TF TF Xa TF VIIa Prvotní komplex TF Játra Antitr. III Vnitřní – tenázový komplex VIIIa annexin XIa Ca 2+ trombin VIIIa XIIa Fosfatidilcholin EPC R Heparan sulfát trombocyt annexin PL PL annexin Protrombinázový komplex protrombin Xa Ca 2+ Va trombocyt annexin PL V Vnější komplex V V TF TFPI annexin XIII plazminogen XIIIa trombin Fibrinogen fibrinopeptid A+B (FPA, FPB) Bbeta 1 42 Apo(a) t PA z LDL u. PA plazminogen trombin HRG XIIIa Fibrin monomer Bbeta 15 42 Fibrin multimer solubilní fibrin (SF) plazmin Fibrin degr. produkty X + Y E + D dimery DDE, DDXX alfa 2 antiplasmin alfa 1 antitrypsin alfa 2 makroglobulin

Fibrinogen – faktor I Vyšší hladiny fibrinogenu: Asociovány s vyšším rizikem KV nemocí (Kannel et al. 1987) • Mutace gama řetězce: změny hladin gama fibrinogenu asociované s KV nemocemi a HŽT – Bcl. I a Hae. III polymorfizmus – asociován s vyšší hladinou fibrinogenu, závažností KV onemocnění a progresí (Behague et al. 1996) • Inzulínová rezistence, některé margaríny Nižší hladiny fibrinogenu: Alkohol – pravidelně, dlouhodobě malá množství (a vzestup HDLc), l Carnitin supplementace (i pokles CRP) Dysfibrinogenémie • Mutace alfa řetězce: změny štěpení fibrinogenu a funkce FDP (bu. adheze, vazokonstrikce, chemotaxe, mitogeneze): dysfibrinogenémie, hypofibrinogenémie, afibrinogenémie, renální amyloidóza • Wiesbadenská mutace – defekt vedoucí k agregaci monomerů fibrinu. Komplikace krvácivé i trombotické. • Hypalbuminemie Kvalitativní porucha tvorby fibrinového koagula se zvýšenou rezistencí k lýze plasminem • Glykosylace fibrinogenu i fibrinolytických faktorů u diabetiků může vést rovněž k snížené solventnosti fibrinu Tkáňová lepidla: 2 -složkové složení: 1) Fibrinogen, Aprotinin + 2) Thrombin, vápník • Lepení podkožních tkání v plastické, rekonstrukční a popáleninové chirurgii. Kožní štěp se přiloží na ránu okamžitě po aplikaci přípravku – do 60 s než dojde k polymerizaci a přidržet jemným tlakem min. 3 min. Defibrinancia - zvyšují degradaci fibrinogenu • Fibrinolysin (ex. ), Brinase – brinolase z Aspergillus oryzae, Defibrotid derivát deoxyribonukleové kyseliny • Hadí toxiny: ancrod (Arvin®) and batroxobin (Defibrase®) – defibrinogencia, v hadích jedech často metaloproteinázy – větš. působí fibrinolýzu • Proteázy červů: Hementin – anticoagulační proteáza ze slin velké pijavice amazonské (Haementeria ghilianii) – Lumbrokináza fibrinolytický enzym žížaly Lumbricus bimastus • Mikrobiální proteázy – zejména bakterie rodu Bacillus ale i jiné. X rozpad rány při infekci, hemorhagické sepse (bacillus anthracis, vibrio vulnificus aj. ) – Fermentovaná jídla – fibrinolytické enzymy zvýšují fibrinolýzu (riziko interakce s antikoagulancii): • F. sojové boby vařené – natto japonské jídlo Bacillus subtilis nattokináza serinová proteáza – snižuje fibrinogen, f. VIII) • F. sojové boby douchi čínské jídlo Bacillus subtilis fibrinolytický enzym • F. sojové boby tempeh filamentózní houby Rhizopus sp. a Fusarium sp. • F. ryba tunec pruhovaný (Katsuwonus pelamis) – japanské jídlo katsuwokinase (KK) • F. cizrna Bacillus amyloliquefaciens – anticoagulační aktivita vyšší akt. než heparin sodium • F. krevetová pasta – asijské koření a F. mléko (máslové mléko) – indický nápoj • Rostlinné enzymy: P. o. Cayenský Pepř neboli Chilli (Capsicum frutescent) vyšší fibrinolýza u Thajců – Pažitka česneková (Allium tuberosum) fibrinolytické enzymy ATFE I a II urychlují fibrinolýzu – Zelený a černý čaj – fibrinolytický vliv PMID: 15161246 [Pub. Med] – Proteázy z Schizophyllum commune (běžná houba) – fibrinolýza bez aktivace plazminu
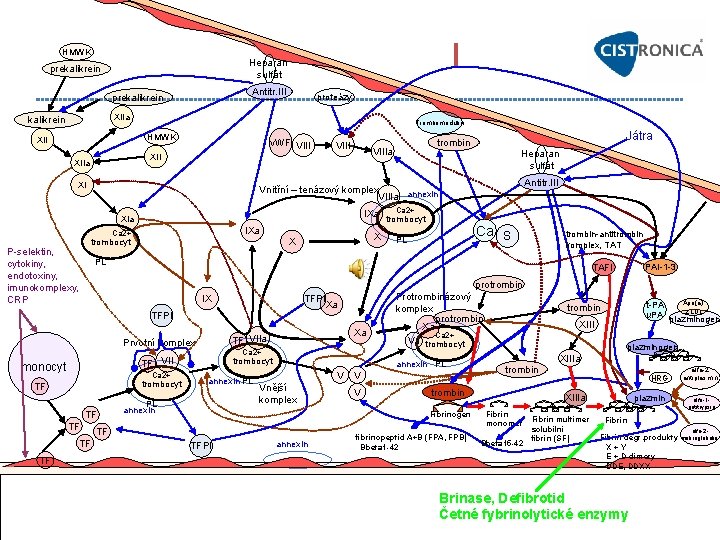
I HMWK Heparan sulfát prekalikrein Antitr. III prekalikrein proteázy XIIa kalikrein Trombomodulin HMWK XII v. WF VIIIa XIIa XI IXa Ca 2+ X X trombocyt Antitr. III Ca 2+ trombocyt Ca S PL trombin antitrombin komplex, TAT PL TAFI PAI 1 3 protrombin IX TFPI Xa TFPI Ca 2+ TF VII monocyt Ca 2+ trombocyt TF TF Xa TF VIIa Prvotní komplex TF Heparan sulfát Vnitřní – tenázový komplex VIIIa annexin XIa P selektin, cytokiny, endotoxiny, imunokomplexy, CRP Játra trombin trombocyt annexin PL PL annexin Protrombinázový komplex protrombin Xa Ca 2+ Va trombocyt annexin PL V Vnější komplex V V TF TFPI annexin XIII plazminogen XIIIa trombin Fibrinogen fibrinopeptid A+B (FPA, FPB) Bbeta 1 -42 Apo(a) t PA z LDL u. PA plazminogen trombin HRG XIIIa Fibrin monomer Bbeta 15 -42 Fibrin multimer solubilní fibrin (SF) plazmin alfa 2 antiplasmin alfa 1 antitrypsin Fibrin degr. produkty X + Y E + D-dimery DDE, DDXX Brinase, Defibrotid Četné fybrinolytické enzymy alfa 2 makroglobulin

Plazminogen a inhibice Syntéza: Játra, Ledviny , Granulocyty Funkce plazminu: Degradace fibrinu. Aktivuje některé mediátory v systému komplementu [7]. Oslabuje stěnu Graafova folikulu (ovulace) [7]. Úloha při fertilizaci, embryogenezi, implantaci a migraci buněk [7] Deficit plazminogenu: Projevy u poklesu pod 40 % (norma 200 mg/l) [7]: Vrozený deficit – oční obtíže, slabá asociace s HŽT Inhibice aktivace plazminogenu na plazmin: • Inhibitor plazminového aktivátoru (PAI 1 -3) Většina zdravých osob v plazmě převaha krevního PAI I nad t. PA [7] – Zásoba PAI v inaktivní formě v trombocytech [7]. Uvolnění velkého mnoţství PAI I = marker trombogeneze [7] – Funkce: Omezení fibrinolytické aktivity na úroveň vznikajícího trombu. t PA a PAI I v plasmě tvoří inaktivní komplex odstraňovány hepatocyty [7], role v signalizaci, bu. adhezi, migraci. – Produkce: Endotel, adipocyty, myocyty hladkého svalstva cév, játra, megakaryocyty [7] – Produkce PAI-I zvýšena: • Vlivem zánětu – snižuje: Xanthoangelols z Angelica keiskei –blokuje vyšší produkci PAI 1 vlivem bakt. LPS, TNF alfa (xanthoangelol, xanthoangelols B, D) • Horečky, obezita, DM, dislipidemie, gravidita, koronární sy. [7], psychický stres, inzulín, jídlo (tučné), nádory, Angiotensin II, nádory prsu s vyšším u. PA a PAI 1 jsou asociovány s vyšší agresivitou a horší prognózou, ACE ID polymorfizmus – vyšší PAI 1 = mírně vyšší riziko IM (nestabilní pláty), + aktivita PAI podporuje stavy s ukládáním fibrinu a progresí do fibrózy – Nižší aktivita PAI-1: • Ovoce, zelenina (+vyšší fibrinolyza, méně KV a TE nemocí) PMID: 2109034, vláknina, pohybová akt. , méně Kj, lykopen, extrakty z černého čaje (převážně teaflaviny – nejsilněji theaflavin 3' galát, teaflavin 3, 3' digalát) • Polymorfismus 4 G/5 G v promotoru genu pro PAI 1 – Alela 5 G: Umožňuje vazbu inhibičních transkripčních faktorů [6]. Nižší transkripce genu [7] • Tiplaxtinin – p. o. inhibitor PAI 1 zk. Na myších • Apo(a) na LDL: Lipoprotein a z podjednotek: Apo. B-100 a Apo (a) - strukturálně podobné plazminogenu – Kompetice LP(a) s plasminogenem o vazbu na: plasminogenové rec. , fibrinogen, fibrin [3], [21] – zhoršení fibrinolýzy !!! • Familiární hypercholesterolémie [3], Defektní apolipoporotein B 100 [3], Hyperlipoproteinemie IIa, b • Terapie statiny může zvýšit hladiny Lp(a) až o 34% a může tak potencionálně zhoršit fibrinolýzu. [21] Inhibice plazminu: Alfa 2 antiplasmin, alfa 1 antitrypsin, alfa 2 makroglobulin • Sojové boby, podzemnice olejná – obsahují inhibitory plasminu • Plazmin vázaný na fibrinogen v trombu chráněn před inaktivací – lokalizace fibrinolýzy Zvýšení odolnosti fibrinu vůči plazminu: • TAFI: Trombomudulin activated fibrinolysis inhibitor – katalyzuje štěpení fibrinových reziduí – činí povrch fibrinu odolnější vůči štěpení plazminem – Aktivován: IIa trombomodulin komplexem

Plazminogen a aktivace Aktivace plazminogenu na plazmin: • XIa, XIIa, kallikrein • t-PA, u-PA (urokináza) – Role v proliferaci bu. , bu. Adhezi, degr. Extracelulární matrix, regulaci RF a matrixových metaloproteináz – Snížení t-PA: Alu repeat I/D polymorfizmus t PA, po požití částečně hydrogenovaného sojového oleje, inzulín – Více t-PA: inzulinová senzitivita, lačnění, pohyb, nižší konzumace sýrů a mléka, sezamový olej (+i synt. t PA a u PA) – Neselektivní PA • Streptokináza: aktivátor plazminogenu ( rychle rozpouští trombus ). (prevence anafyl. současně hydrocortizon v bolusu ) • Urokináza: aktivátor plazminogenu, účinná u velkých plicních embolů, menší riziko krvácení, podání i. v. u IM jako streptokináza – Selektivní - r-t. PA: selektivní aktivace plazminogenu v trombu – Nižší riziko krvácení, vyšší riziko reokluze ( proto se podává s heparinem ) • Altepláza: Retepláza , Tenektepláza (Metalyse) výhodnější • Anistrepláza – anisoylated plasminogen streptokinase activator complex (APSAC): aktivace až po vazbě na fibrin (dlouhý plazmatický poločas ). Podání jako i. v. bolus, účinná u čerstvého IM • Sarupláza – rscu PA: lze kombinovat s t PA, vysoká afinita pro fibrin, dobré vlastnosti, užití k zajištění reperfúze koronárních tepen

Antifibrinolytika Zabraňují vazbě plazminu na fibrin: Indikace: krvácení způsobeného lokální nebo celkovou fibrinolýzou (hyperplazminemie) a krvácení po OP urč. orgánů bohatých na aktivátory plazminogenu: děloha, prostata, plíce, močové ústrojí atd. (plazmin inhibuje i V a VIII) KI: DIC (dif. dg od primární fibrinolýzy – u DIC konzumpce trombocytů, ), TE, PE, trombofílie…(u DIC vždy s heparinem) Kyselina paraaminobenzoová (PABA, vit. B 10) • V někt. potravinách, běžně vzniká činností bakterií E. coli ve střevě (meziproduktem bakteriální syntézy k. listové blokováno sulfonamidy) • PABA jako potravní doplněk v tbl. !!! Kyselina tranexamová • Specificky inhibuje konverzi plasminogenu na plasmin, delší účinek Kyselina e-aminokapronová - EACA (lyzinový analog) • Specificky inhibuje konverzi plasminogenu na plasmin • I. v. pomalu – riziko vzniku trombózy !!! • NÚ: Leukopenie, trombocytopenie, zvýšení BUN (dusíku močoviny v krvi) a selhání ledvin a obecně zvýšená úmrtnost Kyselina p-aminomethylbenzoová (PAMBA ) • Podobná EACA Aprotinin • Inhibitor proteolytických enzymů (plasmin, trypsin, kalikrein), ter. pankreatitid • Krevní konzervy s aprotininem – méně krvácení po OP srdce, ale během 30 dní vyšší úmrtnost na jakékoliv příčiny – 2007 stop Alfa 1 antitrypsin Kamostát
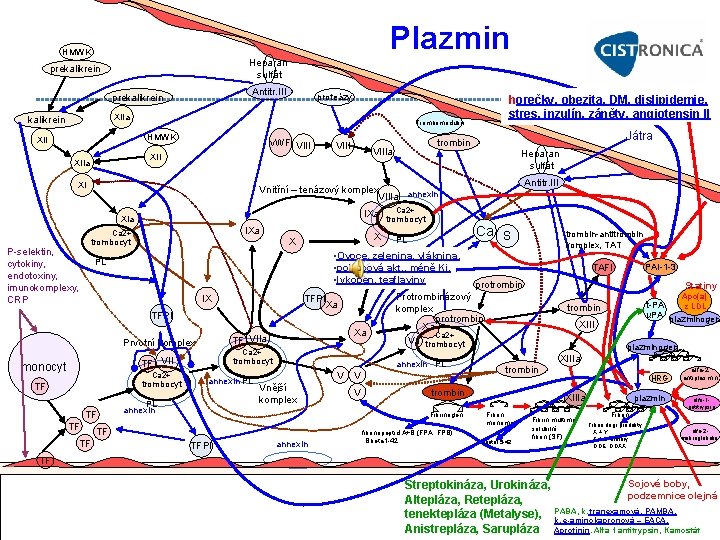
Plazmin HMWK Heparan sulfát prekalikrein Antitr. III prekalikrein proteázy XIIa kalikrein Trombomodulin HMWK XII v. WF VIII XI Heparan sulfát Antitr. III Vnitřní – tenázový komplex VIIIa annexin IXa XIa IXa Ca 2+ P selektin, cytokiny, endotoxiny, imunokomplexy, CRP Játra trombin VIIIa XIIa horečky, obezita, DM, dislipidemie, stres, inzulín, záněty, angiotensin II X X trombocyt IX TFPI Xa TFPI Ca 2+ TF VII Ca 2+ trombocyt TF TF TF Xa TF VIIa Prvotní komplex TF Ca S PL • Ovoce, zelenina, vláknina, • pohybová akt. , méně Kj, • lykopen, teaflaviny PL monocyt Ca 2+ trombocyt annexin PL PL annexin Vnější komplex V V TFPI annexin fibrinopeptid A+B (FPA, FPB) Bbeta 1 42 PAI 1 3 protrombin Statiny Apo(a) z LDL t PA u. PA plazminogen trombin XIII plazminogen XIIIa trombin Fibrinogen TF TAFI Protrombinázový komplex protrombin Xa Ca 2+ Va trombocyt annexin PL V trombin antitrombin komplex, TAT HRG XIIIa Fibrin monomer Bbeta 15 42 Fibrin multimer solubilní fibrin (SF) plazmin Fibrin degr. produkty X + Y E + D dimery DDE, DDXX alfa 2 antiplasmin alfa 1 antitrypsin alfa 2 makroglobulin TF Sojové boby, Streptokináza, Urokináza, podzemnice olejná Altepláza, Retepláza, tenektepláza (Metalyse), PABA, k. tranexamová, PAMBA, k. e-aminokapronová – EACA, Anistrepláza, Sarupláza Aprotinin, Alfa 1 antitrypsin, Kamostát

Warfarin a některé aspekty X vit. K: X připojení zbytků gama-karboxyglutamové kyseliny • X Syntéza neúčinných / parciálně účinných: II, VII, IX, X, proteinu C, S a Z (X vazby pomocí Ca 2+ můstků s fosfolipidy membrány destiček či s TF a mezi sebou) Mutace warfarin metabolizujících enzymů, enzymů metabolizmu vit. K – dědičně zvýšená/snížená citlivost k warfarinu Hypolipidemika bezpečná při warfarinu: Pravastatin majoritně metabolizován renálně. Vzestup INR: Silné inhibitory CYP 3 A 4 (met. R warfarinu): Ketokonazol, Itrakonazol, Cimetidin, Erytromycin, Nefazodon, Fluvoxamin, Sertralin – Amiodaron Inhibitor obou CYP (met. warfarinu R i S): Častá například u pacientů s fibrilacemi síní • Dle databází zdr. pojišťoven 1 z nejčastějších závažných lékových interakcí v ČR • Paracetamol - dávky nad 2, 3 g týdně zvýšení hypoprotrombinemického účinku warfarinu (riziko hematurie nebo krvácení z dásní [2] ) • Fibráty: Snížení syntézy vitamin K dependentních koagulačních faktorů, kompetice o vazbu na plazmatické proteiny [2] • Urychlení degradace jednotlivých koagulačních faktorů – katabolické stavy, konzumpce koag. f. aj. • Antibiotika – pokles produkce vit. K střevní florou • Pesticidy kontaminující potraviny mohou zvyšovat antikoagulační účinky warfarinu. N Engl J Med. 1984 Jul 26; 311(4): 257 8. • Aflatoxin B(1) měl silnější antikoagulační účinky v menších dávkách než 4 hydroxycoumarin. Pokles INR: Induktory jaterních enzymů – vč. Třezalky tečkované Dieta warfarinová: Nejvíce vit. K – játra !!! • "U osob s dlouhodobě výrazně sníženým příjmem vitaminu K potravou dojde při náhodném požití běžné dávky vitaminu K k většímu poklesu INR, než u osob s dlouhodobě jen mírně sníženým příjmem vitaminu K. Denní dávka 150 mµg vitaminu K proti placebu snížila rozdíly mezi nálezy INR u pacientů dříve „nestabilních“ při léčbě warfarinem“ – Stran samotné terapie warfarinem je tedy naopak žádoucí pravidelně nějakou zeleninu s vit. K jíst / suplementovat vit. K !!! • NÚ Warfarinizace s hypovitaminózou vitaminu K: – Vit. K důležitý pro Gla proteiny, skladbu matrix cévní stěny, kostní tkáně aj. = Nárůst kalcifikací medie v tepnách [4] • Normálně by byla inhibována Gla proteiny = Nutnost neustálé obnovy redukované formy vitaminu K = vitamin K hydrochinonon = KH 2 z oxidované formy (vitamin K epoxid, KO) enzymem vitamin K epoxidreduktázou ( VKOR) • Suplementace nízkými D vit. K při warfarinu vedlo ke stabilnějšímu INR a jeho delším periodám v terap. Rozmezí http: //www. amjmed. com/article/S 0002 9343%2804%2900130 5/fulltext – „Treatment with vitamin K for hip fracture patients who receive warfarin shortens preoperative time, reduces the length of hospitalization and probably reduces morbidity and mortality. “ PMID: 23943978 Další antagonisté vit. K: Dikumarol, fenindion, fenprokumon, acenokumarol, ethyl biskumacetát, klorindion, difenandion, tioklomarol, fluindion Kumariny v přírodě přes 600 druhů rostlin: Penicilium nigrans, P. jensi, zapařený jetel (Dicumarol), Dipteryx odorata „kumaru“ ořechy (objev kumarinů), datle, jahody, ostružiny, meruňky, třešně, skořice, levandulový olej, mrkev obecná, vanilovník, koriandr, tabák, fíkovník, smokvoň, citrusové ovoce atd. ; Výroba aromat: Mařinka vonná – svízel vonný (Asperula odorata), komonice lékařská, Slivoň obecná, tomka vonná, tomka severní;
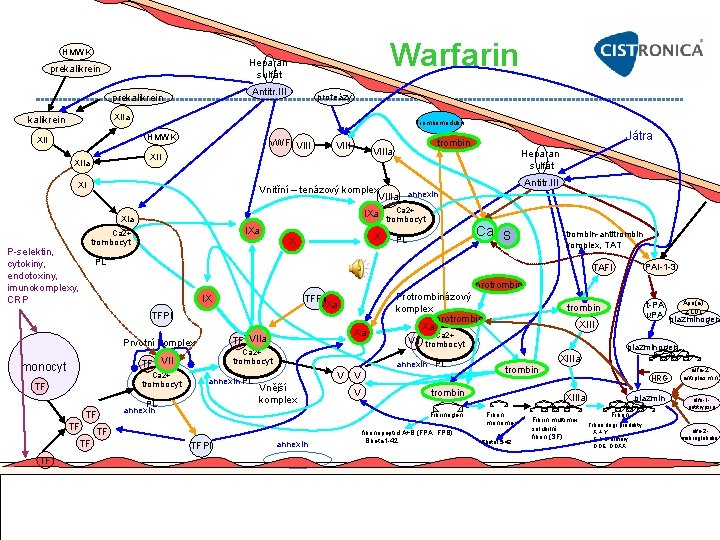
Warfarin HMWK Heparan sulfát prekalikrein Antitr. III prekalikrein proteázy XIIa kalikrein Trombomodulin HMWK XII v. WF VIIIa XIIa XI IXa Ca 2+ X X trombocyt Antitr. III Ca 2+ trombocyt Ca S PL trombin antitrombin komplex, TAT PL TAFI PAI 1 3 protrombin IX TFPI Xa TFPI Ca 2+ TF VII monocyt Ca 2+ trombocyt TF TF Xa TF VIIa Prvotní komplex TF Heparan sulfát Vnitřní – tenázový komplex VIIIa annexin XIa P selektin, cytokiny, endotoxiny, imunokomplexy, CRP Játra trombin trombocyt annexin PL PL annexin Protrombinázový komplex protrombin Xa Ca 2+ Va trombocyt annexin PL V Vnější komplex V V TF TFPI annexin XIII plazminogen XIIIa trombin Fibrinogen fibrinopeptid A+B (FPA, FPB) Bbeta 1 42 Apo(a) t PA z LDL u. PA plazminogen trombin HRG XIIIa Fibrin monomer Bbeta 15 42 Fibrin multimer solubilní fibrin (SF) plazmin Fibrin degr. produkty X + Y E + D dimery DDE, DDXX alfa 2 antiplasmin alfa 1 antitrypsin alfa 2 makroglobulin

Statiny LDL: Intratrombocytární acidóza inhibicí Na+/H+ antiportu mobilizuje Ca 2+ v klidovém stavu a po stimulaci agonistou. • Množství produkce fibrinu po stimulaci ADP přímo úměrně stoupá koncentraci LDL [21] Lp(a) může vlivem statinů stoupnout až o 34% a potenciálně zhoršit fibrinolýzu. [21] Atorvastatin: vzestup fibrinogenu, vyšší při podání 2 xd, vzestup PAI 1 [21] Simvastatin: pokles LDL již po 2 tý. , redukce agregace trombocytů a produkce TX 2 po 4 24 tý. , neprok. snížení trombogeneze v x intimě arterie, bez vlivu na koncentrace fibrinogenu, vzestup PAI 1 [21] Lovastatin: + i – počtu trombocytů a ADP indukované agregace, pokles fibrinogenu, + i – PAI 1 [21] Fluvastatin: bez vlivu na PAI 1 [21] Pravastatin: Snižuje trombocyt dependentní produkci IIa při hypercholesterolemii a Ca 2+ v cytosolu tromboc. a agregaci, PG produkce beze změn, snížená formace trombů na poraněné intimě arterie, pokles fibrinogenu, redukuje PAI 1 – v. s. podporuje fibrinolýzu [21] • JAMA. 1998; 279(20): 1643 1650. doi: 10. 1001/jama. 279. 20. 1643

Další zajímavosti Další antikoagulačně působící potraviny / rostliny / doplňky: • Pivo, borůvky, celer, brusinky, kaštany, lékořice, papaya, granátové jablko, zázvor, výhonky obilí, kůra z vrby, šalvěj červenokořenná, kopretina řimbaba, , kopr, peprmint, mandarinky, med, ocet jablečný, ryzec černohlávek (kominíček), černý jeřáb, semena vinné révy (vitis vinifera), slunečnicovité (Flaveria bidentis ), • Maté (Ilex paraguariensis) obsahuje Triterpen chikusetsusaponin Iva – pokles Xa, IIa, fibrinu (PMID: 23134458) Quercetin a apigenin cibule, kapusta, červené víno a zelený a černý čaj, čokoláda a kakao • Niacin, vit. E (alpha > beta > gamma > delta tokoferol), Bromelain, beta karoten • Ashwagandha (Withania somnifera L. (Solanaceae)) – Ayurvédské bylinné tonikum • „Prokoagulačně působící potraviny“ • Alfa alfa, avokádo, kočičí dráp (Uncaria tomentosa), špenát aj. tmavě zelené listy, kokosový olej nad 50% k. laurová, 18% k. myristová a 8% k. palmitová (zvyšují LDL)

Shrnutí: Trombofilní stavy – trombofílie (vrozené, získané, smíšené) 1. Zpomalení krevního proudu Rozšíření řečiště, stáza krve, pokles krevního tlaku, zvýšená viskozita krve aj. 2. Porušení endotelu Fyzikální, zánětlivé, autoimunitní, metabolické aj. Endoteliální dysfunkce a rozvoj aterosklerózy 3. Zvýšená srážlivost krve • A. Agregace trombocytů – primární hemostáza – Adheze trombocytů – Aktivace trombocytů – Degranulace trombocytů – Agregace trombocytů • B. Zvýšená srážlivost krve - hyperkoagulace (novější pojetí schématu) – sekundární hemostáza – Vyšší aktivita koagulačních faktorů • TF, II, V, VIII, IX, X, XII, – Nižší aktivita antikoagulačních faktorů • AT, PC, PS, APC, trombomodulinu, ZPI, PZ, HCII, … • C. Snížená fibrinolýza – Vyšší tvorba fibrinu • II, XIII, fibrinogen, … – Nižší fibrinolytická aktivita • PAI, t. PA, u. PA, plazmin, inhibitory plazminu a t. PA, …
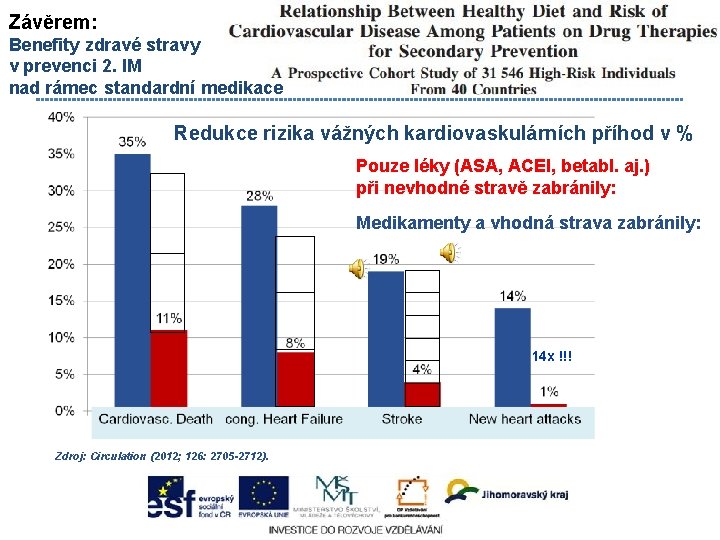
Závěrem: Benefity zdravé stravy v prevenci 2. IM nad rámec standardní medikace Redukce rizika vážných kardiovaskulárních příhod v % Pouze léky (ASA, ACEI, betabl. aj. ) při nevhodné stravě zabránily: Medikamenty a vhodná strava zabránily: 14 x !!! Zdroj: Circulation (2012; 126: 2705 -2712).

Použitá literatura • 1. Faktor V Leiden (G 1691 A; R 506 Q)++, Imalab web 2009 • 2. Effects of newer oral contraceptives on the inhibition of coagulation and fibrinolysis in relation to dosage and type of steroid. ++ Jespersen J, Petersen KR, Skouby SO. Department of Clinical Chemistry, Ribe County Hospital, Esbjerg, Denmark • 3. Zapletal Ondřej, Trombofilní stavy a jejich klinický význam v dětské populaci České republiky, Disertační práce, Masarykova univerzita, Brno 2012, LF, dětská interní klinika, hematologie FN Brno. • 4. Gaillyová Renata MUDr. , Genetické příčiny poruch reprodukce Vyšetření párů s opakovanými fetálními ztrátami, Disertační práce, Lékařská fakulta Masarykovy university v Brně, Ústav preventivního lékařství, Oddělení lékařské genetiky Fakultní nemocnice Brno, 2006 5. Kleprlíková Hana, Incidence tombofilních markerů u klientek léčených pro neplodnost, Diplomová práce, Olomouc 2009 • 6. Farmakoterapie trombembolických stavů, farmakoterapie pro praxi • 7. Endoteliální dysfunkce – první stadium aterosklerózy, MUDr. Michal Vrablík, Ph. D. , Michaela Janotová, MUDr. Eva Motyková, MUDr. Martina Prusíková • 8. Endoteliální dysfunkce, možnosti její detekce a využití v klinické praxi. MUDr. David Karásek Ph. D. , prof. MUDr. Helena Vaverková CSc. , MUDr. Milan Halenka, MUDr. Martin Hutyra Ph. D. • • 9. Protein Z–dependent protease inhibitor deficiency produces a more severe murine phenotype than protein Z deficiency, Jing Zhang, Yizheng Tu, Lan Lu, Nina Lasky, George J. Broze, http: //bloodjournal. hematologylibrary. org/content/111/10/4973. long 10. Thrombosis: Lysophosphatidic Acid Induces Thrombogenic Activity Through Phosphatidylserine Exposure and Procoagulant Microvesicle Generation in Human Erythrocytes, Seung Min Chung, Ok Nam Bae, Kyung Min Lim, Ji Yoon Noh, Moo Yeol Lee, Yi Sook Jung, Jin Ho Chung http: //atvb. ahajournals. org/content/27/2/414. full 11. Krvácivé stavy z destičkových příčin, http: //zdravi. e 15. cz/clanek/priloha lekarske listy/krvacive stavy z destickovych pricin 139840 • 12. Protidestičková léčba – kde jsme a co můžeme očekávat? Prof. MUDr. Jan Bultas, CSc, Doc. MUDr. Debora Karetová, CSc. • 13. Jaký je pokrok v léčbě trombotických stavů? Časopis NEUMM 1/2008 / Co nového můžeme očekávat v léčbě kardiovaskulárních chorob? http: //www. neumm. cz/archiv/351/jaky je pokrok v lecbe trombotickych stavu. html • 14. Kombinace antitrombotik, Prof. MUDr. Jan Bultas, CSc, Doc. MUDr. Debora Karetová, CSc. 2009 Remedia, s. r. o. • 15. Nová éra perorální antikoagulační léčby, doc. MUDr. Debora Karetová, CSc. , II. interní klinika – klinika kardiologie a angiologie 1. LF UK a VFN Praha, Zdraví E 15, Příloha: Lékařské listy, 04/2012 • 16. Hyperkoagulační stavy, http: //zdravi. e 15. cz/clanek/priloha lekarske listy/hyperkoagulacni stavy je li pritomno aspon jedno z pravidel obec 129775 • 17. Rezistence na aspirin – laboratorní odchylka nebo klinický prolblém? MUDr. Debora Karetová, CSc. , doc. MUDr. Jan Bultas, CSc. II. interní klinika 1. LF UK a VFN, Praha http: //www. internimedicina. cz/pdfs/int/2005/01/03. pdf • 18. Rezistence na protidestičkovou léčbu v klinické praxi. Naše první zkušenosti s použitím přístroje multiplate k rychlému měření agregace destiček. Tématický okruh: Varia. Typ: Poster lékařský , 2009 • 19. O'Connell K, Wood J, Wise R, Lozier J, Braun M. Thromboembolic adverse events after use of recombinant human coagulation factor VIIa. JAMA. 2006, roč. 295, čís. 3, s. 293– 8. DOI: 10. 1001/jama. 295. 3. 293. PMID 16418464. • • 20. Factor XII Deficiency Roger S. Riley, M. D. , Ph. D; April, 2005. http: //www. pathology. vcu. edu/clinical/coag/FXII%20 Deficiency. pdf 21. Antiatherothrombotic Properties of Statins. Implications for Cardiovascular Event Reduction FREE, Robert S. Rosenson, MD; Christine C. Tangney, Ph. D, JAMA. 1998; 279(20): 1643 1650. doi: 10. 1001/jama. 279. 20. 1643 22. Toxins in thrombosis and haemostasis: potential beyond imagination, R. M. KINI, http: // onlinelibrary. wiley. com/doi/10. 1111/j. 1538 7836. 2011. 04279. x/full • •

INOVATIVNÍ VZDĚLÁVACÍ PROGRAMY PRO FARMACEUTICKÉ PRACOVNÍKY Děkuji za pozornost MUDr. Dana Maňasková medicinman@medicinman. cz Tento studijní materiál vznikl jako výstup z projektu č. CZ. 1. 07/3. 2. 04/04. 0035
- Slides: 67