INICIACION A LA FORMULACION MAGISTRAL FORMAS FARMACEUTICAS LIQUIDAS

























































- Slides: 60

INICIACION A LA FORMULACION MAGISTRAL FORMAS FARMACEUTICAS LIQUIDAS q SOLUCIONES q SUSPENSIONES 2 Febrero 2011

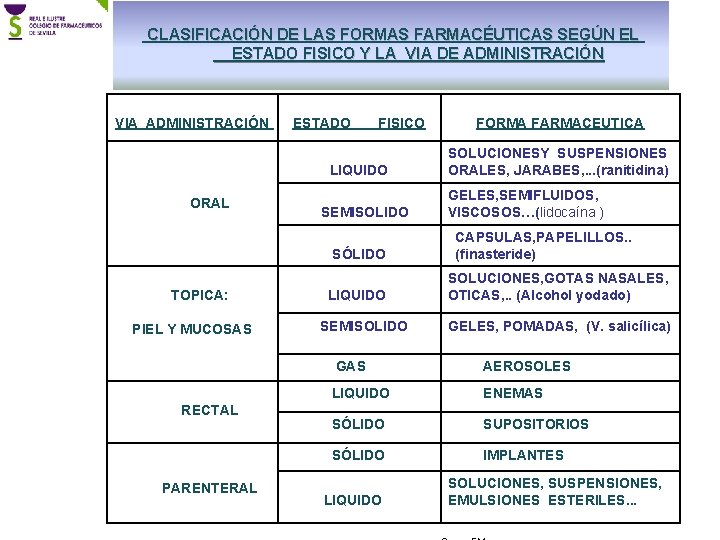
CLASIFICACIÓN DE LAS FORMAS FARMACÉUTICAS SEGÚN EL ESTADO FISICO Y LA VIA DE ADMINISTRACIÓN VIA ADMINISTRACIÓN ESTADO FISICO LIQUIDO ORAL SEMISOLIDO SÓLIDO TOPICA: PIEL Y MUCOSAS RECTAL PARENTERAL LIQUIDO SEMISOLIDO FORMA FARMACEUTICA SOLUCIONESY SUSPENSIONES ORALES, JARABES, . . . (ranitidina) GELES, SEMIFLUIDOS, VISCOSOS…(lidocaína ) CAPSULAS, PAPELILLOS. . (finasteride) SOLUCIONES, GOTAS NASALES, OTICAS, . . (Alcohol yodado) GELES, POMADAS, (V. salicílica) GAS AEROSOLES LIQUIDO ENEMAS SÓLIDO SUPOSITORIOS SÓLIDO IMPLANTES LIQUIDO SOLUCIONES, SUSPENSIONES, EMULSIONES ESTERILES. . .

FORMAS FARMACEUTICAS LIQUIDAS SOLUCIONES : • Son obtenidas por simple mezcla homogénea (una sola fase) donde uno de los componentes se encuentra en menor proporción ( soluto: p. a. ), y dispersado en el seno de otro u otros componentes (disolvente/s : excipiente/s) Curso FM

CLASIFICACION DE LAS SOLUCIONES SEGÚN EL TAMAÑO DEL SOLUTO S. verdadera: - Partículas tamaño inferior a 0. 01 micras - Solución límpida y transparente. - No podemos mediante medios físicos ver las partículas de soluto. . Ej: Minoxidil 2% S. coloidal : - Partículas entre 0, 1 y 0, 01 micras. - Soluciones de aspecto opalescente. - Se pueden ver las partículas por medios físicos. Ej: Gel de carbopol de clindamicina Suspensiones: - Partícula mayor a 0, 1 micras - Su aspecto es opaco - Las partículas se observan a simple vista. - Necesitan una agitación previa a su aplicación. Ej. : Loción de calamina Curso FM

SOLUCIONES VERDADERAS SOLUBILIDAD: Cantidad máxima de un principio activo que puede contener una disolución en unas condiciones determinadas. ( Tª, p. H, …. ) • Este parámetro físico-químico es importante pues va a condicionar su velocidad de disolución, biodisponibilidad, y por tanto eficacia terapéutica del mismo. Curso FM

SOLUCIONES VERDADERAS • CONCENTRACIÓN: De un p. a. en una solución es la cantidad de este p. a. que se encuentra disuelto respecto a la cantidad total de la mezcla. Se expresa en: - % p/p: g de p. a. en 100 g de formula total - % p/v: g de p. a. en 100 ml de fórmula total. - % v/v: ml de p. a. en 100 ml de fórmula total. • Ej. : Solución HA de Eritromicina 4% : hay 4 g de Eritromicina en 100 ml de solución

SOLUCIONES VERDADERAS • Los diferentes p. a. , según su estructura química, van a tener una mayor afinidad a la hora de mezclarse homogéneamente con unos solventes y menor o nula con otros. Se dice que son solubles en los primeros e insolubles en los otros. En general esta afinidad se relaciona con una similitud en sus estructuras químicas, lo similar disuelve a lo similar". Curso FM

SOLUCIONES VERDADERAS Elección del solvente. Será el mas adecuado no solo para solubilizar el p. a. , sino también dependiendo de la zona corporal a aplicar, del tipo de piel y de la patología a tratar. Curso FM

ELABORACION DE SOLUCIONES Las soluciones se preparan por interposición del soluto o solutos en los solventes de forma paulatina , con ayuda mecánica o no, hasta la completa homogeneización. Son formas farmacéuticas que no suelen presentar mayor complicación a menos que se produzca incompatibilidad entre p. a. o que se rebase el coeficiente de solubilidad con lo que se pueden producir precipitaciones. Se dispone de algunos recursos tanto para agilizar el proceso como para evitar precipitaciones. Curso FM

FACTORES QUE AFECTAN A LA SOLUBILIDAD Y VELOCIDAD DE DISOLUCION • a) Naturaleza física del soluto( sólido, líquido, . . ) • b)Tamaño y forma de las partículas del soluto. Una < del tamaño provoca un > en la velocidad de disolución • c) Polimorfismo. Presentación de los p. a. en forma cristalina o amorfa. En general las formas estables son menos solubles, así las formas cristalinas son menos solubles que las amorfas, y las hidratadas menos que las anhidras. • d) Superficie de contacto: La interacción soluto-solvente aumenta cuando hay mayor superficie de contacto y el cuerpo se disuelve con más rapidez ( pulverizando el p. a. ). Curso FM

FACTORES QUE AFECTAN A LA SOLUBILIDAD Y LA VELOCIDAD DE DISOLUCION e) Agitación del soluto y disolvente: Al agitar la solución se van separando las capas de disolución que se forman del soluto y nuevas moléculas del solvente continúan la disolución. • Contribuye a aumentar la rapidez de elaboración y a la homogenización. • Puede ser manual o mecánica. • Tener en cuenta que algunas sustancias (liposomas) no pueden someterse a agitación. Curso FM

FACTORES QUE AFECTAN A LA SOLUBILIDAD Y LA VELOCIDAD DE DISOLUCION f) Naturaleza del disolvente: Es importante elegir un buen disolvente. El agua es el mas empleado, pero en general se considera que el mejor disolvente es aquel con polaridad mas similar a la del soluto. g) Presencia de un ión común : La solubilidad de los fármacos depende de su grado de ionización, si algún motivo, como la presencia de un ión común, hace que disminuya la ionización, afectará a la solubilidad disminuyéndola. Curso FM

FACTORES QUE AFECTAN A LA SOLUBILIDAD Y LA VELOCIDAD DE DISOLUCION h) Temperatura: Al aumentar la temperatura se favorece el movimiento de las moléculas y hace que la energía de las partículas del sólido sea alta y puedan abandonar su superficie disolviéndose. Por regla general la solubilidad aumenta con la Tª a excepción en las reacciones que desprenden calor(exotérmicas), a > Tª < Solubilidad. i) Modificando p. H del medio: Una ligera alcalinización (caso de la furosemida en sol. oral) o acidificación (minoxidil al 10%) facilita la solubilidad de algunos p. Curso FM

FACTORES QUE AFECTAN A LA SOLUBILIDAD Y LA VELOCIDAD DE DISOLUCION i) Uso de Cosolventes: Relativamente frecuente pues: • Modifican la constante dieléctrica de algunos solventes favoreciendo la solubilidad de determinados p. a. . • Confieren mayor extensibilidad e higroscopicidad a las soluciones. • Aumentan la absorción de determinados p. a. • Alcohol, glicerina…. propanol, acetona, Curso FM prpilenglicol,

FACTORES QUE AFECTAN A LA SOLUBILIDAD Y LA VELOCIDAD DE DISOLUCION i) Uso de Cosolventes ( Continuacion) Grupo A: Solventes que además de aumentar la solubilidad de algunos p. a. , contribuyen a la extensibilidad e higroscopicidad : Glicoles, tween, glicerina, siliconas. Son bien tolerados. Grupo B: Solventes orgánicos para p. a. soluble solo en ellos : Acetona, éter, cloroformo. Son irritantes y deslipidizantes. Grupo C : Solventes que aumentan la absorción transdérmica por alterar la estructura queratínica. ( DMSO, . . ) Curso FM

FACTORES QUE AFECTAN A LA SOLUBILIDAD Y LA VELOCIDAD DE DISOLUCION j) Adición de otros p. a. , (Hidrotropía). Hay p. a que en presencia de otra sustancia aumenta considerablemente su solubilidad. (Bórax con Salicílico en agua oxigenada). k) Orden de incorporación de los distintos componentes. La presencia de otros componentes de la fórmula, puede hacer que un determinado p. a. se disuelva ( hidrotropía) o bien al contrario que no se pueda disolver. l) Agentes tensoactivos. Modifican la tensión superficial de algunos solventes. ( Tween, Span, , Brijs. . . ) y favorecen la solubilidad. m) Aceites: aceite de ricino, miristato de isopropilo. . Curso FM

TIPOS SOLUCIONES SEGÚN EL DISOLVENTE Según sea éste pueden ser : q q q acuosas ( en agua) alcohólicas (en alcohol), glicéricas (en glicerina), etéreas (en éter), linimentos (en aceite). Curso FM

SOLUCIONES ACUOSAS El agua es el excipiente básico en muchas formulaciones. Ventajas de las soluciones que forma: • Pueden ser para administración tópica y oral • Elaboración fácil y simple. • El principio activo va totalmente disuelto en el agua. • Con el agua purificada como vehículo tendremos la forma con la que se consigue la absorción mas rápida y completa de los medicamentos. • El sabor y olor generalmente serán agradables por la posible adición de sustancias correctoras • Dosificación en volumen. Curso FM

SOLUCIONES ACUOSAS • Y también Inconvenientes: • La extensibilidad y la humectación en el caso de las soluciones tópicas, son inferiores a otras soluciones con solventes con tensión superficial menor a la del agua. • La solución acuosa es un medio muy reactivo para p. a. que pueden sufrir reacciones de degradación como oxidación, hidrólisis, … pudiendo aparecer interacciones entre los p. a. • Caducidad generalmente corta. Curso FM

FORMAS FARMACEUTICAS LIQUIDAS DISOLVENTES HABITUALES : 1. - AGUA PURIFICADA de calidad Farmacopea Europea. (RFE MON Nº 008) • • Aspecto: Líquido límpido e incoloro. Producción : Agua destinada a la fabricación de medicamentos cuando no es necesario que sean estériles, ni estén exentos de pirógenos, salvo excepción justificada y autorizada. Se prepara por destilación, por intercambio iónico, por ósmosis inversa o por cualquier otro procedimiento adecuado, a partir de agua que cumpla la normativa del agua destinada al consumo humano. Parámetros microbiológicas Máximo 100 microorganismos aerobios viables totales /ml Parámetros fisico-químicos : Conductividad 25ºC = 5, 1 micro. Siemens. cm-1. Curso FM

FORMAS FARMACEUTICAS LIQUIDAS 2. - Agua conservante. FN/2003/EX/001 Solución concentrada de hidroxibenzoatos. . 1 g Agua purificada csp ……. . . 100 ml -Sol. conc. hidroxibenzoatos(FN/2003/EX/025) PHB de metilo(RFE 0409)………. . 8 g PHB de propilo(RFE 0431)………. 2 g Propilenglicol csp……………… 100 g Curso FM

FORMAS FARMACEUTICAS LIQUIDAS Ejemplos Fórmulas ó Preparados Oficinales en Solución Tópica Principio activo. . . x % Solvente. c. s. p 100 ml Sulfato de Zinc 1 g Sulfato de Cobre 1 g Agua purificada csp 1000 ml Salicílico 20% Láctico 20% Colodión elástico csp 30 ml Minoxidil Ac. Retinoico Solución HA Sol. Sulfato Zinc 1/1000 csp 250 c * Sulfato de Cobre 0, 1% csp 250 ml * Permanganato potásico 1/10. 000 csp 200 ml * Hidróxido potásico 4 -5% csp 50 ml * Curso FM 2 - 3 % 0, 025% csp

FORMAS FARMACEUTICAS LIQUIDAS Ejemplos de Formúlas ó Preparados Oficinales en Solución Oral * Sulfato de Zinc 7 H 2 O…. 1, 11 g *Agua purificada ……. 250 ml Solución lugol fuerte Yodo ……………. . 5 g Yoduro potásico. . 10 g Agua purificada csp 100 g *Solución oral pediátrica Enalapriol Enalaprilo maleato…… 1 mg/ml Citrato sódico……… 1 g Acido cítrico………… 0, 35 g Solución conservante… 1 ml Agua purificada… csp 100 ml

SOLUCIONES HIDROALCÓHOLICAS • Las Soluciones HA son parte muy importante de la formulación habitual de la O. de F. . • El etanol, solvente de polaridad media, entre el agua ( polar) y los aceites y parafinas ( apolares) constituye un solvente idóneo para un gran nº de p. a. , como corticoides, estrógenos, , antibióticos, retinoides, …. Curso FM

SOLUCIONES HIDROALCÓHOLICAS El etanol de 96º no se suele utilizar como tal sino diluido con agua en una concentración que dependerá sobre todo de los p. a. y de su concentración, constituyendo soluciones hidro-alcohólicas. Los motivos : El alcohol de 96º reseca el estrato corneo y por ello dificulta la penetración de algunos p. a. No ocurre esto con las soluciones de 70º y de 50º. El etanol de 70º tiene mayor desinfectante que el de 96º. Curso FM poder

SOLUCIONES HIDROALCÓHOLICAS Proporción entre alcohol y agua: la establecerá el farmacéutico de acuerdo con la solubilidad de los p. a. . Cantidad de alcohol: mínima necesaria para la perfecta solubilización de los p. a. Cantidad de agua la sufiente para rebajar la proporción de etanol y así disminuir sus molestias. Añadir algún poliol o silicona para aumentar la extensibilidad de la solución. Curso FM

SOLUCIONES HIDROALCÓHOLICAS en el FN SOLUCION HIDROALCOHOLICA 1. FN/2003/EX/026 Alcohol 96º Agua purificada 50% SOLUCION HIDROALCOHOLICA 2. FN/2003/EX/027 Alcohol 96º Agua purificada 70% 30% Curso FM

CONSIDERACIONES GENERALES PARA ELABORAR UNA SOLUCION 1. Realizar un estudio detallado fisico-químico, galénico y farmacológico, del ó de los p. a. prescritos así como de los excipientes. • (Consultar tabla de solubilidades para los distintos p. a. : ESTUDIO DE PREFORMULACION) Curso FM

ESTUDIO DE PREFORMULACION Propiedades fisico-químicas de los p. a. 1. 2. 3. 4. Características organolépticas Tamaño y forma de partícula Solubilidad. Concentración Curso FM

CONSIDERACIONES GENERALES PARA ELABORAR UNA SOLUCION 2. - El ó los p. a. deben quedar perfectamente disueltos. Si fuera difícil la disolución de éstos, se utilizarán los medios ya vistos que favorecen la solubilidad de los p. a ( Tª, agitación, cosolventes…. ) Curso FM

CONSIDERACIONES GENERALES PARA ELABORAR UNA SOLUCION 3. - En el caso que hubiese mas de un disolvente, incorporar los p. a. disueltos en el más soluble y luego ir añadiendo los demás disolventes, mezclándolos poco a poco con agitación en el orden más idóneo. Curso FM

CONSIDERACIONES GENERALES PARA ELABORAR UNA SOLUCION OBSEVACIONES: A veces será preciso alterar las proporciones del excipiente prescrito por el médico para obtener una solución límpida. La caducidad de las soluciones acuosas generalmente es corta, podremos ampliarla con la adición de sustancias conservantes. Cuando en una prescripción no aparece el excipiente, se sobreentiende que es una solución acuosa. Curso FM

CONSIDERACIONES GENERALES PARA ELABORAR UNA SOLUCION Método general 1. - Pesar o medir todos los componentes de la fórmula ( según PNT correspondiente) 2. - Reunir 3/4 partes del solvente con el principio activo agitando hasta completa disolución. 3. - La velocidad de disolución del principio activo puede aumentarse calentando, siempre que este aumento Curso FM

CONSIDERACIONES GENERALES PARA ELABORAR UNA SOLUCION 4. - Si el principio activo es termolábil, añadirlo en frío. 5. - Si el principio activo es insoluble en el solvente, incorporarlo previamente disuelto en un cosolvente de polaridad adecuado. 6. - Añadir lentamente al solvente, si procede, los conservantes y otros componentes minoritarios, como antioxidantes ( si el p. a es fácilmente oxidable, para asegurar la estabilidad de este componente), correctores de color y/o sabor, etc. , agitando hasta su completa disolución Curso FM

CONSIDERACIONES GENERALES PARA ELABORAR UNA SOLUCION 7. - En caso necesario, filtrar la solución con el filtro adecuado. 8. - Completar, hasta el volumen total especificado en la fórmula, con el resto del solvente. 9. - Homogeneizar y envasar. Curso FM

CONSIDERACIONES GENERALES PARA ELABORAR UNA SOLUCION Acondicionamiento : Envases • Recipiente de material y cierre adecuado y compatible con el contenido • Capacidad adecuada al volumen queremos envasar. • Color topacio, secos y con buen cierre hermético. Se aconseja acompañar la preparación con un dispositivo adecuado que Curso FM

CONSIDERACIONES GENERALES PARA ELABORAR UNA SOLUCION Controles a realizar en el producto acabado. Fórmula magistral: - Evaluación caracteres organolépticos. Formula magistral tipificada y preparados oficinales: - Evaluación caracteres organolépticos Curso FM

SUSTANCIAS AUXILIARES( Aditvos) Edulcorantes: *Fructosa, Sacarosa, Sorbitol, Xilitol(calóricos) *Sacarina, Ciclamato, Aspartamo ( acalóricos) Conservantes: * Parabenes, Dowcil, Phenonip, Kathon (antimicrobianos) * Aceites esenciales: Timol, Eugenol. . * Ac. Benzóico, ac. Sórbico y sus sales Antioxidantes: * Butilhidroxitolueno (0, 01 -0, 05% )Vitamina. E * Metabisulfito sódico( 0, 01 -0, 1%) Vitamina C *Ac. Cítrico, EDTA ( coadyuvantes) Aromatizantes: Dan sabor y olor agradables a las preparaciones orales. Mayoritariamente están los Aceites esenciales (Esencias) Saborizantes: la mayor parte la constituyen los edulcorantes Colorantes: Riboflavina Curso ( E 101) FM

JARABES: (FE Mon. Nº 0672) • Formas Farmacéuticas liquidas de administración oral, límpidas y con elevada viscosidad, que contienen un azúcar disuelto en el agua casi a saturación. Curso FM

JARABES ( RFE Mon Nº 0672) Jarabe Simple. FN/2003/EX/022 Según La RFE el jarabe simple se obtiene mezclando mediante agitación : - Sacarosa 640 g - Agua destilada 360 g Metodologia » Incorporar la sacarosa directamente al agua bajo agitación de forma lenta y gradual y en frio ( para evitar la aparición del azúcar invertido: fructosa y glucosa, y coloraciones amarillentas debido a la caramelización, ésto proporciona un sabor mas dulce al jarabe, por la fructosa, y facilita el desarrollo de hongos y microorganismos. )hasta disolución completa. » Obtención de una disolución homogénea que se filtrará. (Cad. 2 semanas. ) » Puede añadírsele conservantes , se hará en el agua antes de disolver la sacarosa. » En el mercado existe ya preparado(con conservante) Curso FM

JARABES: (RFE Mon. Nº 0672) Características : » Pueden ser soluciones o suspensiones. » El azúcar más común es la sacarosa. » También glucosa, sorbitol, fructosa, edulcorantes de síntesis. » Indicado para vehiculizar los activos hidrosolubles. » Amplia utilización en Pediatría y Geriatría. » El azúcar presente actúa como: conservante, edulcorante y viscosizante. » Olor y sabor agradables por la adición de correctores del sabor, aromas. . , Curso FM

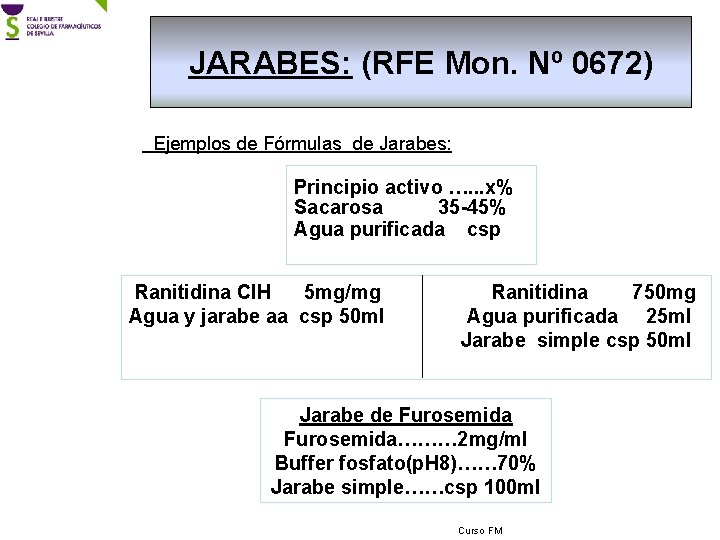
JARABES: (RFE Mon. Nº 0672) Ejemplos de Fórmulas de Jarabes: Principio activo …. . . x% Sacarosa 35 -45% Agua purificada csp Ranitidina Cl. H 5 mg/mg Agua y jarabe aa csp 50 ml Ranitidina 750 mg Agua purificada 25 ml Jarabe simple csp 50 ml Jarabe de Furosemida……… 2 mg/ml Buffer fosfato(p. H 8)…… 70% Jarabe simple……csp 100 ml Curso FM

JARABES: (RFE Mon. Nº 0672) Modus Operandi. 1. -Incorporar el conservante al agua purificada bajo agitación y lentamente hasta su completa disolución. , que será el agua purificada 2. -Incorporación de los p. a. directamente al jarabe elaborado, o bien dependiendo de la solubilidad de los activos, en la cantidad mínima de un disolvente adecuado. 3. -Si se ha utilizado un disolvente, mezclarlo con el jarabe poco apoco y mediante agitación. 4. -Enrasar si hiciera falta, hasta la cantidad total a elaborar. 5. -Homogeneizar y envasar Curso FM

JARABES: (RFE Mon. Nº 0672) Acondicionamiento. -Recipiente de material y cierre adecuado y compatibles con el contenido - Que se llenen hasta su totalidad, para evitar evaporaciones parciales. - color topacio, secos y con buen cierre hermético. Curso FM

JARABES: (RFE Mon. Nº 0672) Controles del producto acabado: Formulas Magistrales : -Evaluación de los caracteres organolépticos: Líquido viscoso, incoloro e inodoro. Densidad a 15 -20 ºC: 1, 315 - 1, 325 g/ml. Fórmulas Magistrales y Preparados oficinales : - Evaluación de los caracteres organolépticos y -Verificación de peso ó volumen. Curso FM

FORMAS FARMACEUTICAS LIQUIDAS ADMINISTRACIÓN POR OTRAS VIAS. Gargarismos: Soluciones acuosas pudiendo contener también polioles y alcoholes y con p. a de acción antiséptica y antiinflamatoria para tratar procesos infecciosos e inflamatorios de la laringe y la nasofaringe. Ej: Solución para gargarismos (FN/ 2003/PO/0077) Glicerina 10 g Bicarbonato sódico 1 g Bórax 1 g Menta piperita 0, 05 g Agua purificada csp 100 ml Colutorios: Soluciones o suspensiones para enjuagues bucales. Pueden ser vehículos acuosos de glicerina/agua, alcohol/agua. Los p. a. usuales: anestésicos tópicos, antifungicos, corticoides. . para diversas infecciones de la mucosa oral. Ej. Acetónido de Triamcinolona 0, 1% en solución acuosa. Curso FM

Gotas óticas: Soluciones ó suspensiones, que se instilan en el conducto auditivo con cuentagotas. Pueden llevar vehículos acuosos, alcoholes diluidos, PEG, glicerina, diversos aceites( oliva, almendras dulces, parafina. . ). Ej. Alcohol boricado, aceite gomenolado, P. A. usuales: anestésicos tópicos, antibióticos, antifungicos, anticerumen, corticoides…para diversas infecciones y eczemas del oído externo. Gotas nasales: Soluciones o suspensiones para administrar por instilación o nebulización en la fosas nasales. Puede llevar excipientes acuosos, oleosos y también con polioles. P. A. usuales: descongestivos, antisépticos, antiinflamtorios. . ELABORACIÓN: La elaboración de estas formas farmacéuticas no supone complejidad alguna, y se seguirá el método general de elaboración de soluciones ó suspensiones, según sea. Curso FM

SUSPENSIONES • Formas Farmacéuticas formadas por sistemas dispersos heterogéneos constituidos por partículas de un solido insoluble finamente divididas(o también puede ser un líquido) dispersadas homogéneamente en el seno de un líquido. Curso FM

CLASIFICACIÓN SEGÚN EL VEHÍCULO: • Acuosas : Vehiculo agua purificada ( vía oral) • Hidroalcóholicas: Hidroalcóholicas agua/alcohol a distintas proporciones. • Hidro-propilenglicol-alcohólicas: Hidro-propilenglicol-alcohólicas agua/propilenglicol/ alcohol a distintas proporciones. • Oleosas: Oleosas Aceite, vaselinas, …etc. (vía tópica, ótica, parenteral…. ) Curso FM

Características: • Para p. a. poco solubles en el vehiculo requerido (agua) o inestables en sol. • Para fármacos amargos, sus derivados insípidos son mejor aceptados en suspensión. • Inestables por su propia naturaleza: tienden a separarse las dos fases (precipita ó sedimenta el polvo; ó se separan los dos líquidos) • Presentan aspecto turbio al agitarlas. • Suele incorporársele viscosizantes. • El agua purificada es el vehiculo mas utilizado. • Pueden prepararse para todas las vías de administración. • La caducidad de las suspensiones acuosas, generalmente, es corta. • AGITAR antes de su aplicación ó ingestión para asegurar la resuspensión, lo más homogénea posible, de los principios activos dispersos.

COMPONENTES DE UNA SUSPENSION • Sustancias que van a contribuir a la estabilidad de una suspensión : 1. Fármaco/s ó p. a. /s Debemos: ---- Reducir el tamaño de partícula del soluto, pulverizándolo (en su caso) al máximo. --- Conseguir que el tamaño de las partículas sea los mas homogéneo posible Curso FM

COMPONENTES DE UNA SUSPENSION 2) Agentes humectantes. • Aumentan la superficie de contacto entre los p. a. insolubles y el liquido dispersante, facilitando que se moje fácilmente el p. a. • Son principalmente: glicerina, propilenglicol, sorbitol liquido, PEG líquidos y tweens. • Se incorporan formando una pasta homogénea con el p. a. una vez finamente pulverizado en el mortero y posterior adición del líquido dispersa Si utilizamos tween en suspensiones para la mucosa oral ( enjuagues) es conveniente añadir algún edulcorante ( sacarina, sorbitol, ) pues da sabor amargo a las preparaciones. • La cantidad a utilizar será la justa para humedecer el ó los p. a. , mas cantidad de la cuenta puede dar lugar a la formación de grumos al final. Curso FM

COMPONENTES DE UNA SUSPENSION 3) Agentes suspensores: Viscosizantes. • Aumentan la viscosidad del disolvente, • Grado de viscosidad óptimo evitando que los p. a sedimenten rápidamente. • La falta de ellos puede dar lugar a poca efectividad en el tratamiento, los p. a sedimentados no pueden hacer su efecto farmacológico. • Los mas empleados: Metilcelulosa, Carboximetilcelulosa, Bentonita, Veegun, Carbopol-940 (para vía tópica) Carbopol-934 P (para vía oral), Goma guar. • Las emulsiones fluidas y los champús pueden actuar como agentes viscosizantes. • Los aceites también pueden actuar como agentes suspensores Curso FM

SUSPENSIONES 1)Ejemplos de Prescripciones de Suspensiones. Orales • Omeprazol Base 2 mg/ml Bicarbonato sodico 8, 4% Sacarina sodica 0, 1% Carboximetilcelulosa Na 0, 5% Esencia vainilla 0, 4% Agua csp • Ac. Ursodeoxicolico 15 mg/ml Glicerina cs Jarabe simple csp 100 ml • Metronidazol 15 mg/ml Jarabe simple csp • Espironolactona 5 mg/ml Alcohol 70º 2% Jarabe simple csp Curso FM

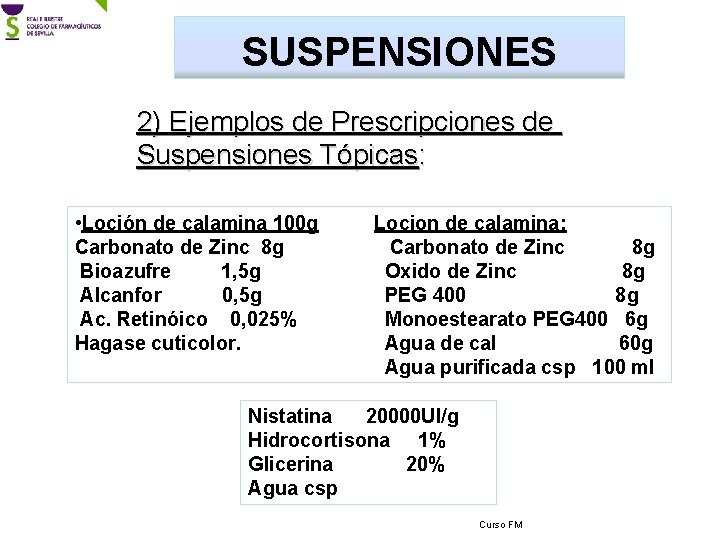
SUSPENSIONES 2) Ejemplos de Prescripciones de Suspensiones Tópicas: • Loción de calamina 100 g Carbonato de Zinc 8 g Bioazufre 1, 5 g Alcanfor 0, 5 g Ac. Retinóico 0, 025% Hagase cuticolor. Locion de calamina: Carbonato de Zinc 8 g Oxido de Zinc 8 g PEG 400 8 g Monoestearato PEG 400 6 g Agua de cal 60 g Agua purificada csp 100 ml Nistatina 20000 UI/g Hidrocortisona 1% Glicerina 20% Agua csp Curso FM

METODO GENERAL ELABORACION SUSPENSIONES • • Medir y/o pesar todos los componentes de la fórmula ( según PNT correspondiente) Incorporación del conservante, antioxidante, . . (en caso de que se utilicen) en el vehiculo adecuado, generalmente agua purificada, hasta total disolución. En mortero se pulverizan finamente el/los p. a. /s y se añade el humectante para mojarlo/s. Seguidamente y con agitación el viscosizante, obteniendo una dispersión homogénea, sin aglomerado. Por último los demás componentes de la fórmula y enrasar hasta el volumen total a preparar. Homogeneizar la suspensión obtenida. Envasar en recipientes de material y sistema de cierre compatibles con el contenido. Curso FM

SUSPENSIONES Acondicionamiento: - Envases de capacidad mayor al del volumen queremos envasar. - Color topacio y con buen cierre hermético Controles al producto acabado 1. -FM • - Verificación de las características organolépticas 2. -FMT y PO • - Verificación de las características organolépticas • - Verificación del peso o/y volumen.

EJEMPLOS DE EXCIPIENTES PARA ELABORAR SUSPENSIONES: Gel fluido de metilcelulosa. (FN/2003/EX/018) metilcelulosa. Metilcelulosa 1000 1% Sol clorhexidina 50 mg agua purificada csp 100 g. MO : Se dispersa, con la ayuda de una varilla, la metilcelulosa en la mezcla de agua purificada y disolución de digluconato de clorhexidina al 20 %, previamente calentada aproximadamente a 80 ºC. Se deja enfriar para que se produzca la gelificación. Curso FM

ASPECTOS A TENER EN CUENTA PARA LA ELECCION DE UN DISOLVENTE • En los procesos inflamatorios resultan útiles las soluciones pues al ser aplicadas sobre la piel se evaporan, absorbiendo el calor de ésta. • Existen solventes que poseen propiedades desengrasantes irritantes y/o antisépticas, como el alcohol. • La mezcla de alcohol y agua se utiliza para aumentar la solubilidad de p. a. y además tiene propiedades conservante y estabilizante, pues disminuye el crecimiento bacteriano y protege a los p. a de la hidrólisis. • Hay diolventes que aumentan la absorción de los p. a, favoreciendo su efectividad, es el caso del propilenglicol, aceite de sésamo… • El solvente puede tener también efecto farmacológico o cualidades cosméticas. • Frecuencia de la aplicación y cantidad aplicada. Curso FM

ASPECTOS A TENER EN CUENTA PARA LA ELECCION DE UN DISOLVENTE • Edad: En general la permeabilidad disminuye con la edad; sin embargo, este fenómeno no sucede con todos los fármacos, así los corticoides penetran con más facilidad en los ancianos que en los adultos jóvenes. La capacidad de absorción está muy aumentada en la piel de los bebés. • Tipo de piel. • Tipo de afección a tratar. • Grado de penetración que se desea: Acción superficial, acción a nivel de la dermis. • Zona de aplicación: Piel, cuero cabelludo, etc • Estado de la piel: La presencia de quemaduras, heridas o erosiones favorece la absorción y las hiperqueratosis la dificultan. • Hidratación.