Inhibitor PERTEMUAN 11 dan 12 Adri Nora S

Inhibitor PERTEMUAN 11 dan 12 Adri Nora S. Si M. Si Bioteknologi/FIKES

Inhibitor Enzim • Agar dapat bekerja dengan baik, maka sistem biologis harus mampu mengatur aktivitas dari enzim. Enzim harus mengetahui kapan waktunya bekerja kapan harus berhenti • Suatu senyawa yang dapat berikatan dapat menghentikan kerja enzim dinamakan dengan inhibitor • Inhibitor berdasarkan kekuatan ikatannya dibagi menjadi dua: 1. Inhibitor ireversibel 2. Inhibitor reversibel

Inhibitor Ireversibel • Beberapa inhibitor dapat berikatan kuat dengan enzim melalui ikatan kovalen atau non-kovalen • Ketika mereka telah berikatan, biasanya inhibitor akan sulit terlepas dari enzim sehingga dianamakan inhbitor ireversibel E+I EI (Ekuilibrium akan bergerak ke kanan) • Beberapa contoh dari inhibitor ireversibel: 1. Penicilin 2. Nerve gas 3. Aspirin

1. Nerve gas: • adalah satu inhibitor yang sangat berbahaya jika berikatan dengan enzim acethylcholinesterase • Enzim ini mengkatalisis pemecahan acethylcholine yang mengatur kontraksi otot. • Jika enzim ini tidak dapat bekerja maka otot akan menjadi lumpuh 2. Penicilin: • adalah satu inhibitor yang berguna ketika terkena infeksi bakteri • Penicilin mampu berikatan dengan transpeptidase sehingga menghalangi bakteri untuk membentuk dinding selnya 3. Aspirin: • Dapat berikatan cyclooxygenase • Cycloooxygenase dapat mengkatalisis pembentukkan senyawa tertentu yang menyebabkan inflamasi

Inhibitor Reversibel • Beberapa inhibitor dapat berikatan lemah dengan enzim • Inhibitor yang dapat berikatan lemah dengan enzim dapat memutuskan ikatannya dengan enzim pada kondisi lingkungan tertentu. Inhibitor ini dinamakan inhibitor reversibel • Inhibitor reversibel dibagi menjadi 3: 1. Inhibitor kompetitif 2. Inhibitor nonkompetitif 3. Inhibitor unkompetitif

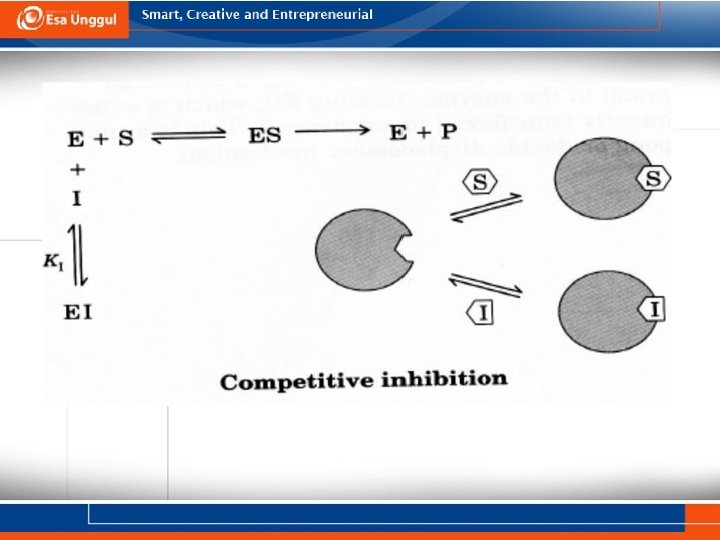
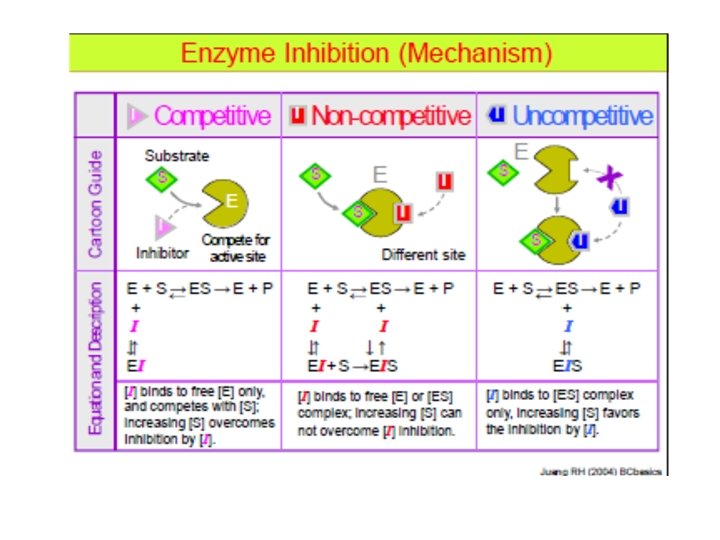
Inhibisi kompetitif • Pada inhibisi ini, inhibitor bentuknya sama dengan substrat dan mampu berikatan secara langsung dengan sisi aktif dari enzim • Ketika inhibitor ini berikatan dengan enzim, maka substrat tidak akan mampu berikatan dengan enzim • Inhibitor ini memiliki afinitas yang lebih besar daripada susbtratnya • Untuk mampu berkompetisi dengan inhibitor, maka konsentrasi substrat dapat dinaikkan sehingga inhibitor dapat terdesak dan terlepas dari enzim • Contoh: methotrexade adalah inhibitor kompetitif pada enzim dihidrofolat reduktase (substrat: dihidrofolat)

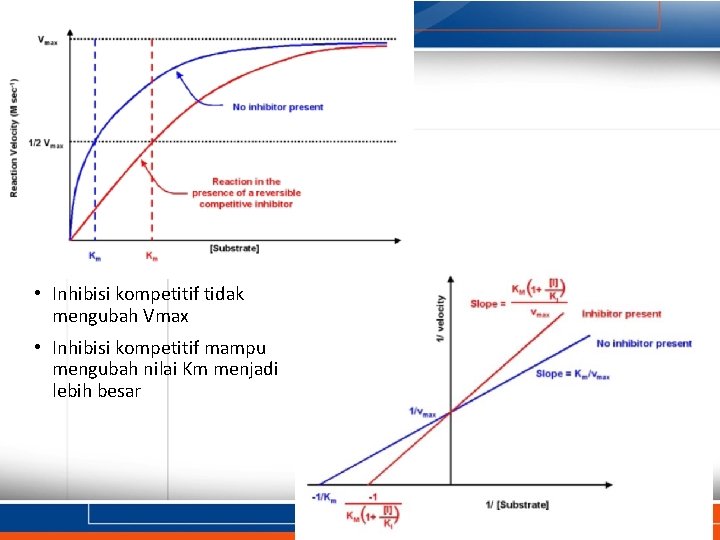
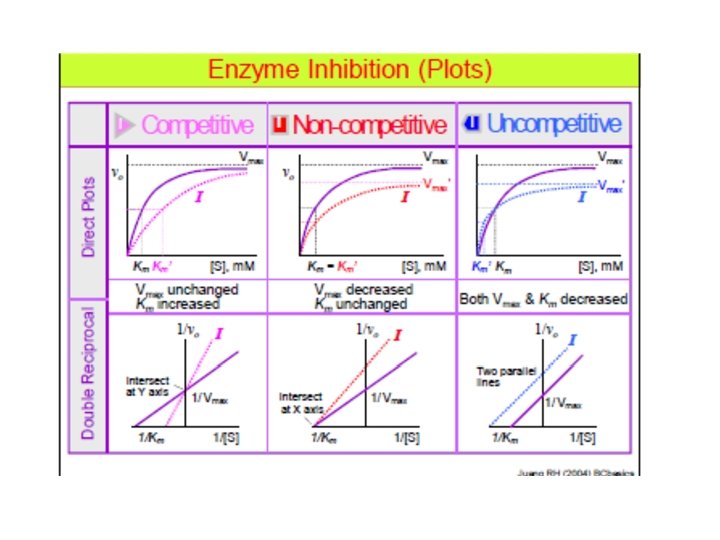
• Inhibisi kompetitif tidak mengubah Vmax • Inhibisi kompetitif mampu mengubah nilai Km menjadi lebih besar

Inhibisi Unkompetitif • Pada inhibisi unkompetitif, inhibitor tidak berkompetisi dengan susbtrat karena bentuknya yang berbeda dengan substrat • Saat substrat telah berikatan dengan enzim, enzim membentuk suatu poket (sisi alosterik) yang sebelumnya tidak ada • Sisi alosterik tersebut akan diisi oleh inhibitor, sehingga kompleks enzim-substrat tidak mampu menghasilkan produk • Penambahan konsentrasi substrat tidak akan menyelesaikan permasalahan inhibisi ini


• Pada inhibisi unkompetitif, nilai V max akan turun karena ketika inhibitor telah menempel pada kompleks ES maka enzim tidak akan berfungsi lebih baik lagi • Nilai Km juga akan turun karena nilai Vmax yang turun sehingga menyebabkan nilai ½ Vmax juga turun • Reaksi ini akan tetap berjalan walaupun konsentrasi substrat hanya sedikit
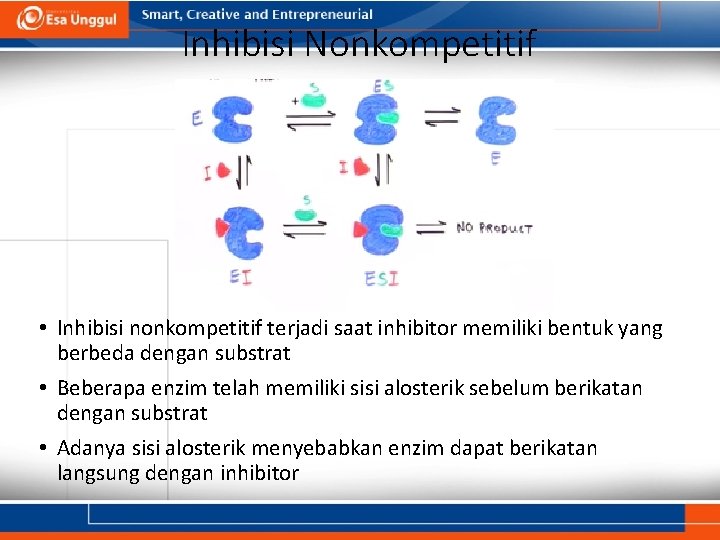
Inhibisi Nonkompetitif • Inhibisi nonkompetitif terjadi saat inhibitor memiliki bentuk yang berbeda dengan substrat • Beberapa enzim telah memiliki sisi alosterik sebelum berikatan dengan substrat • Adanya sisi alosterik menyebabkan enzim dapat berikatan langsung dengan inhibitor
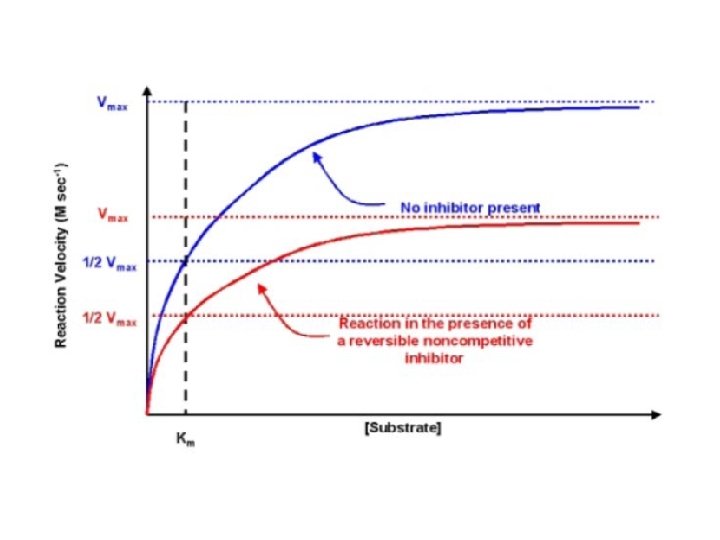
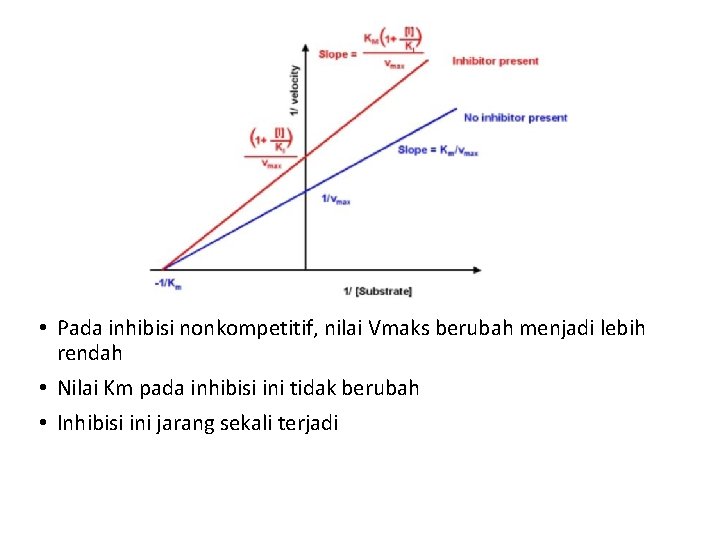
• Pada inhibisi nonkompetitif, nilai Vmaks berubah menjadi lebih rendah • Nilai Km pada inhibisi ini tidak berubah • Inhibisi ini jarang sekali terjadi
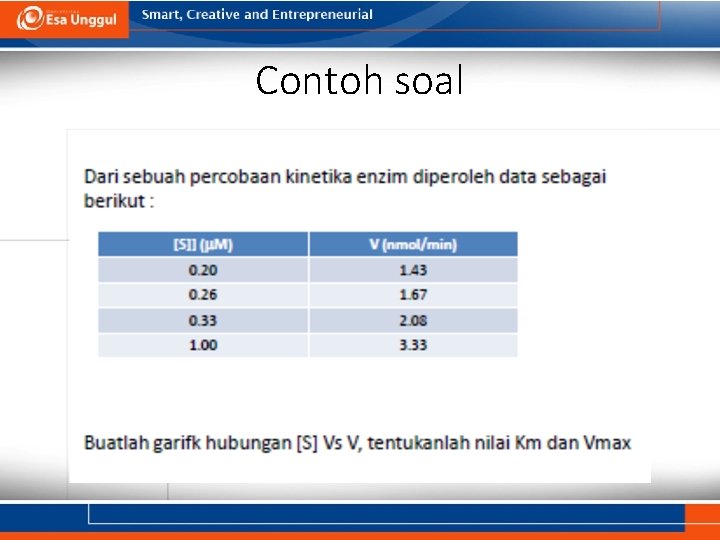
Contoh soal

• Untuk enzim yang mengikuti kinetika michaelis menten, tentukan nilai V max, jika diketahui nilai V adalah 70µmol/s dan nilai [S] = 5 Km! • Tentukan ratio Km/[S], jika kecepatan enzim mengkatalisis reaksi adalah 10% dari Vmaxnya!
- Slides: 19