Inhibicin Enzimtica Mg Ins Arnao Salas Inhibidores n

Inhibición Enzimática Mg Inés Arnao Salas

Inhibidores n n n Agente que reacciona químicamente con un grupo funcional. Participan en la regulación enzimática. Suministran información importante acerca de la estructura y/o grupos funcionales del sitio activo. Permite conocer la especificidad de la enzima por un tipo de reacción o S. Muchos agentes terapéuticos ejercen su acción farmacológica actuando como inhibidores enzimáticos.

Tipos de inhibición enzimática n 1. - Reversible: Competitiva No competitiva Acompetitiva n 2. - Irreversible

Inhibición irreversible n Diisopropilfluorofosfato inactiva los residuos de serín-E. n Iodoacetamida se une a grupos SH o imidazol. n P-Cl mercuribenzoato se une a grupos SH. n La unión E-I es muy fuerte. n Disminuye Vm y no varía Km.
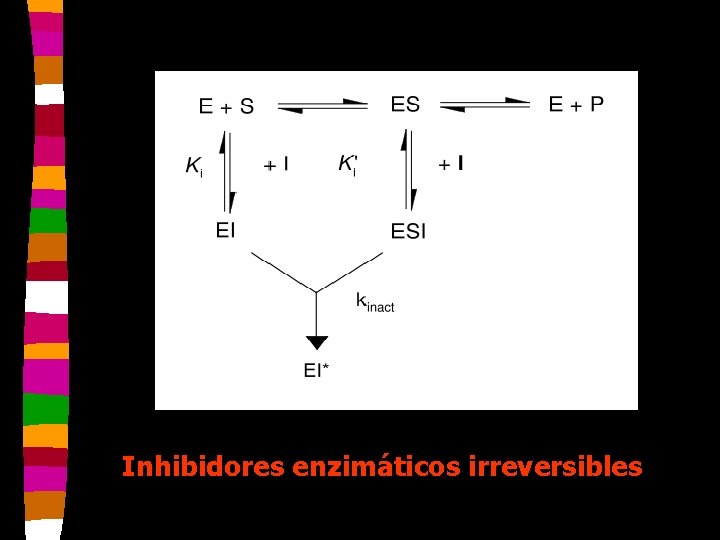
Inhibidores enzimáticos irreversibles
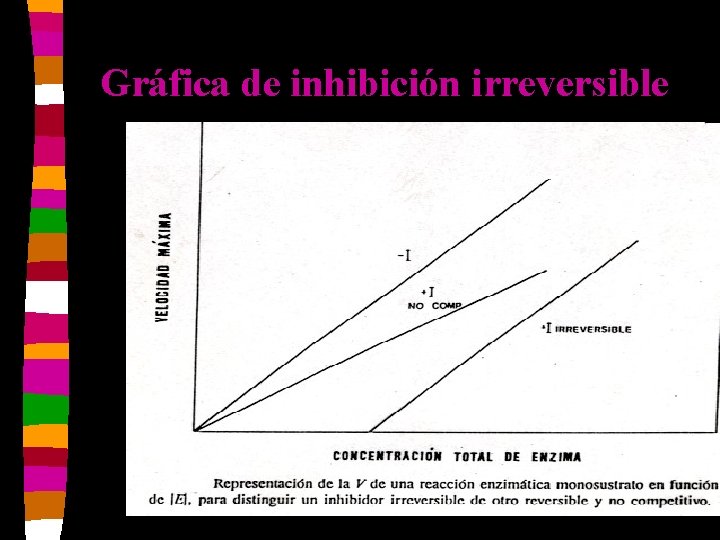
Gráfica de inhibición irreversible
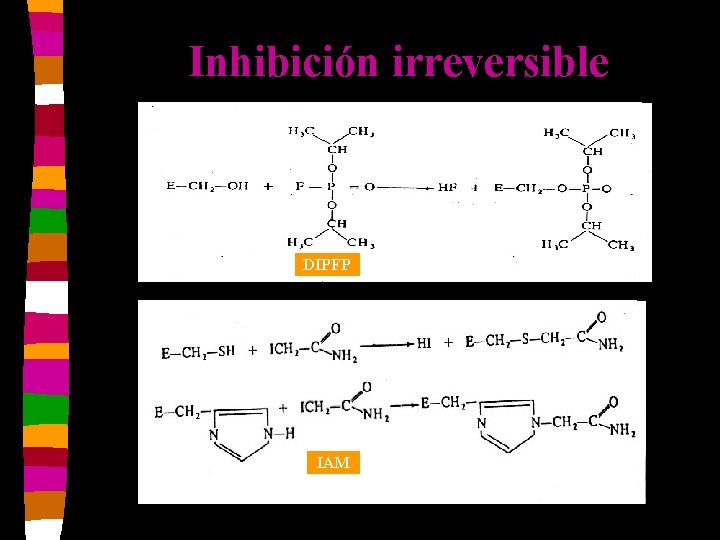
Inhibición irreversible DIPFP IAM

Inhibidores competitivos n n n Tienen una estructura semejante a la del S. Se une al sitio activo de la E. Al aumentar la concentración del S se revierte la inhibición. Se forma un complejo EI. Vm no varía y Km aumenta. El Ki es la concentración del inhibidor que duplica el valor de Km.
![CINETICA ENZIMATICA INHIBICION COMPETITIVA Su comportamiento cinético es el siguiente [E]+[S] + [I] [ CINETICA ENZIMATICA INHIBICION COMPETITIVA Su comportamiento cinético es el siguiente [E]+[S] + [I] [](http://slidetodoc.com/presentation_image_h/84a1e8a4fe1b3147b87701e70fecaf2b/image-9.jpg)
CINETICA ENZIMATICA INHIBICION COMPETITIVA Su comportamiento cinético es el siguiente [E]+[S] + [I] [ EI ] [ES] [E]+[P]
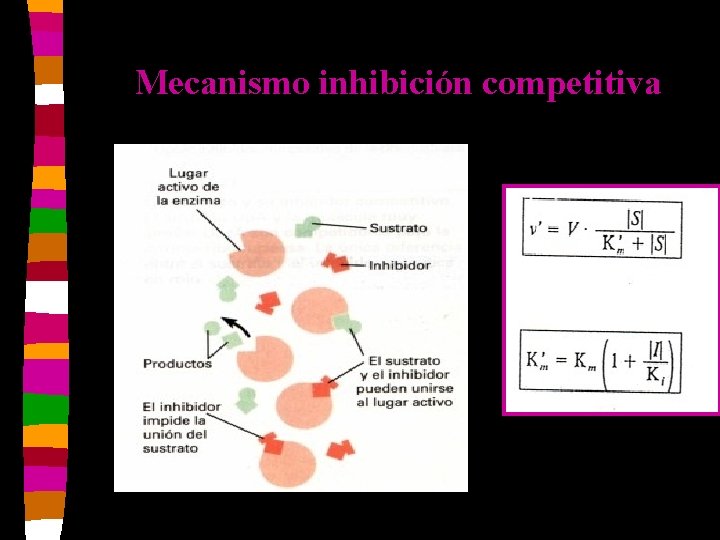
Mecanismo inhibición competitiva
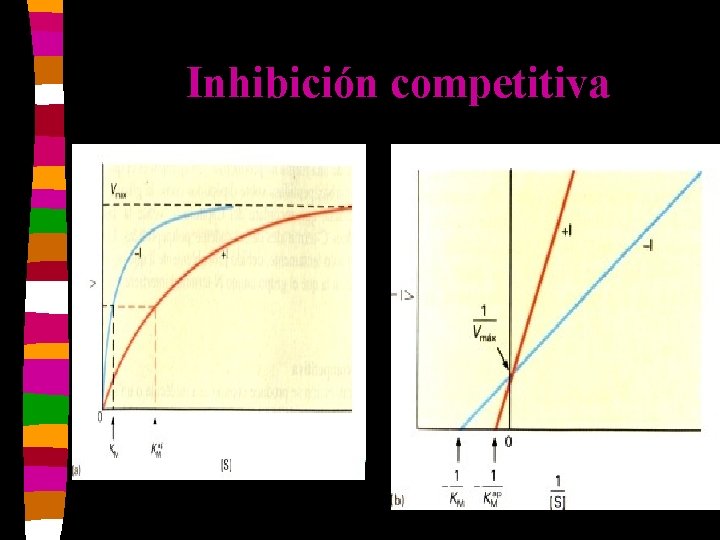
Inhibición competitiva
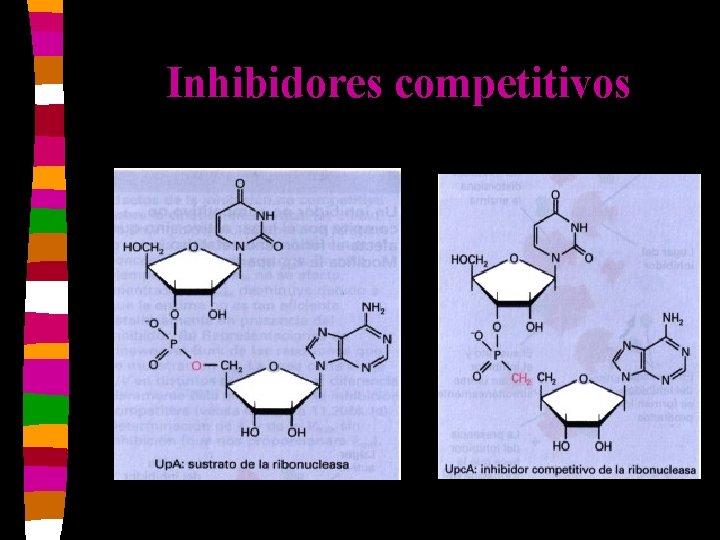
Inhibidores competitivos

Inhibición no competitiva n n n Se une a un sitio diferente al sitio activo. Carece de especificidad por la E. La inhibición no se revierte aumentando la concentración de S. Se forman complejos EI y ESI. El Km no se modifica pero Vm disminuye. El Ki es la concentración del I que reduce a la mitad la Vm.
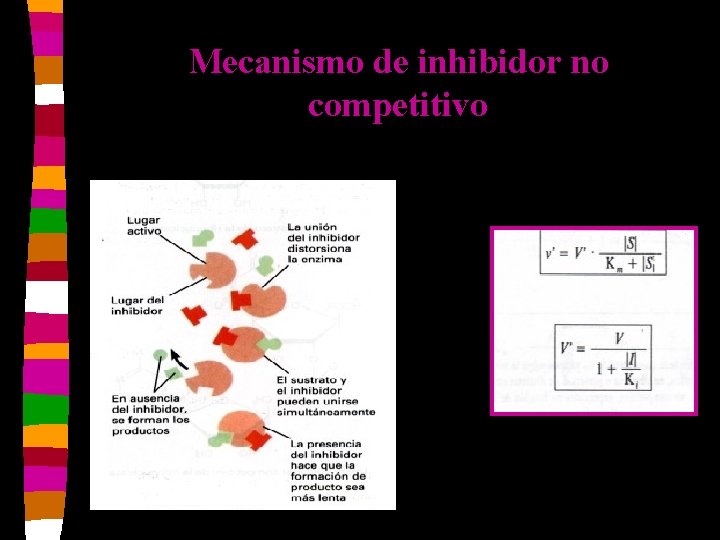
Mecanismo de inhibidor no competitivo
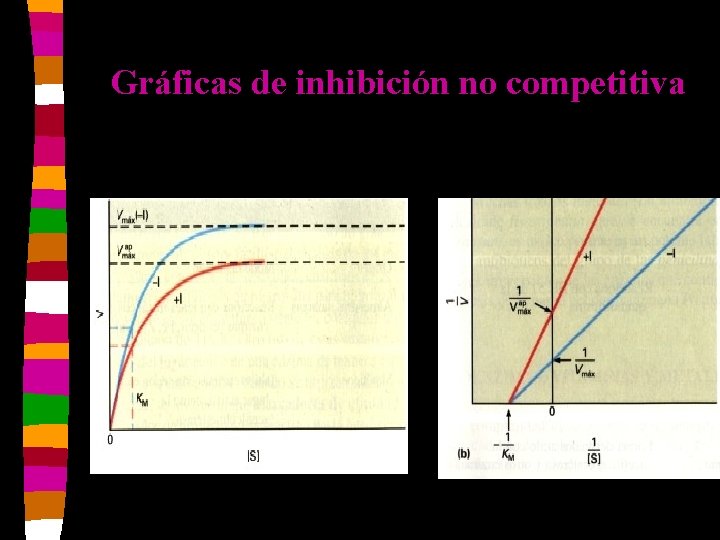
Gráficas de inhibición no competitiva
![CINETICA ENZIMATICA INHIBICION NO COMPETITIVA Su comportamiento cinético es el siguiente [E]+[S] + [I] CINETICA ENZIMATICA INHIBICION NO COMPETITIVA Su comportamiento cinético es el siguiente [E]+[S] + [I]](http://slidetodoc.com/presentation_image_h/84a1e8a4fe1b3147b87701e70fecaf2b/image-16.jpg)
CINETICA ENZIMATICA INHIBICION NO COMPETITIVA Su comportamiento cinético es el siguiente [E]+[S] + [I] [ES] + [I] [ EI ] + [ S ] [ ESI ] [E]+[P]
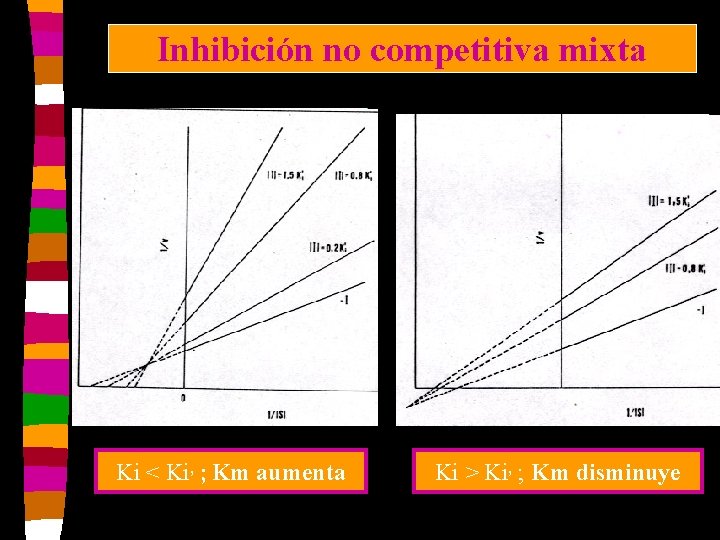
Inhibición no competitiva mixta Ki < Ki, ; Km aumenta Ki > Ki, ; Km disminuye
![CINETICA ENZIMATICA INHIBICION ACOMPETITIVA Su comportamiento cinético es el siguiente [E]+[S] [ ES ] CINETICA ENZIMATICA INHIBICION ACOMPETITIVA Su comportamiento cinético es el siguiente [E]+[S] [ ES ]](http://slidetodoc.com/presentation_image_h/84a1e8a4fe1b3147b87701e70fecaf2b/image-18.jpg)
CINETICA ENZIMATICA INHIBICION ACOMPETITIVA Su comportamiento cinético es el siguiente [E]+[S] [ ES ] + [I] [E]+[P] [ ESI ] Se forma un complejo ESI, el Vm y Km disminuye.
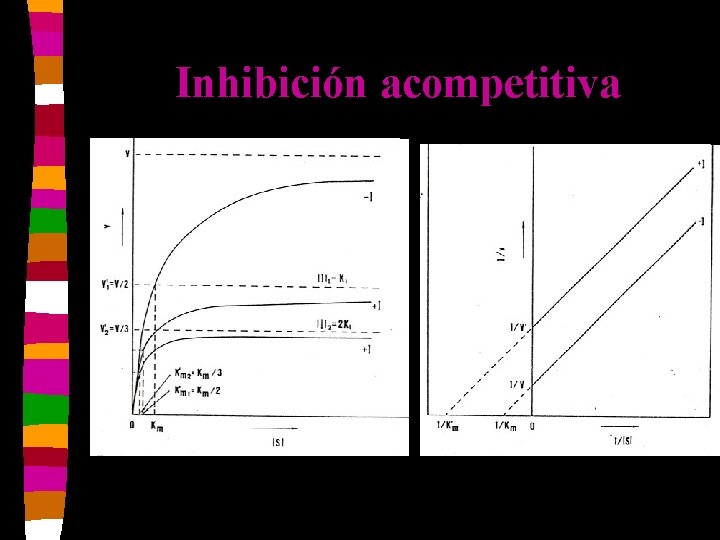
Inhibición acompetitiva

Características principales de los diversos tipos de inhibición enzimática reversible
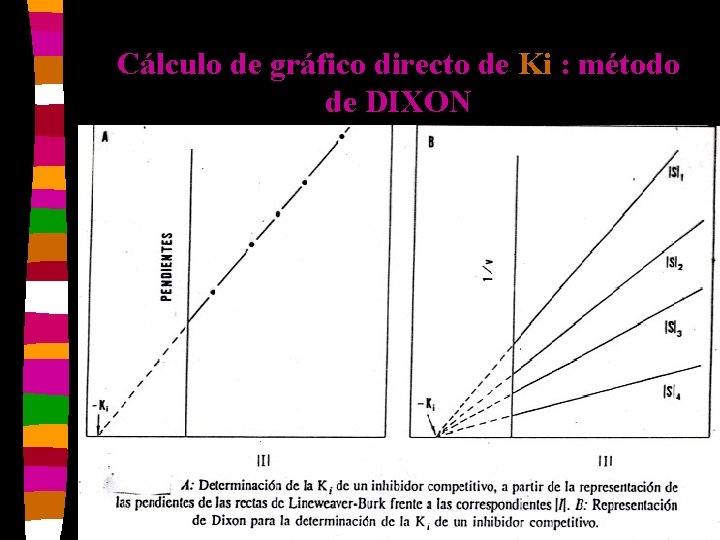
Cálculo de gráfico directo de Ki : método de DIXON
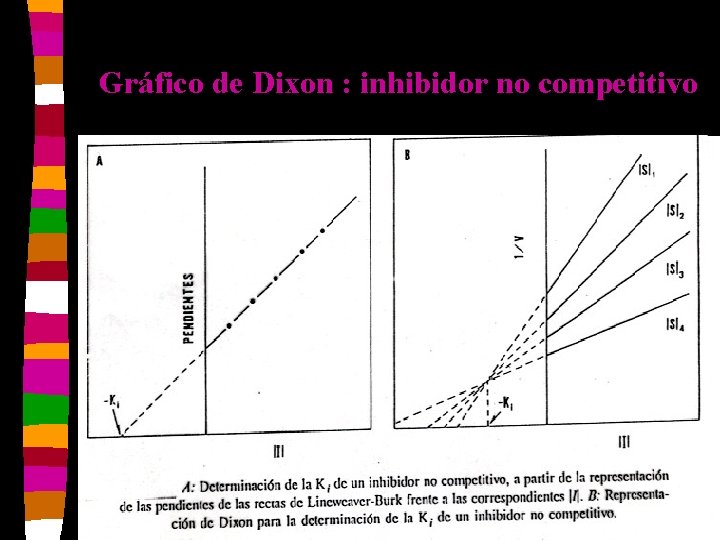
Gráfico de Dixon : inhibidor no competitivo
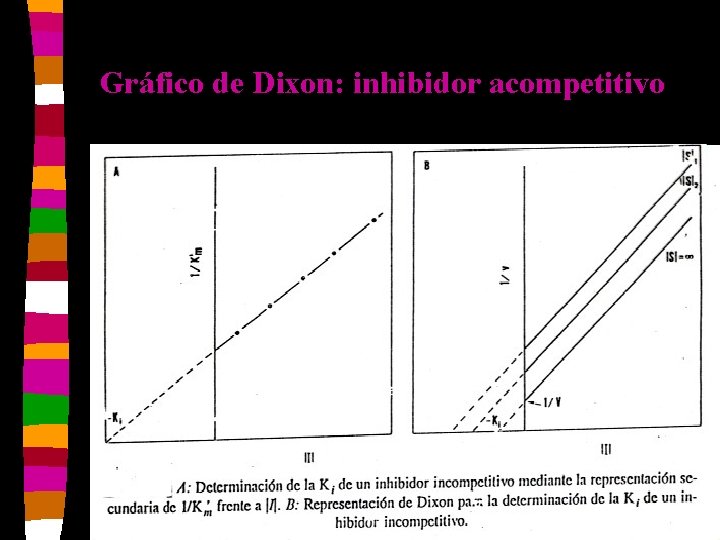
Gráfico de Dixon: inhibidor acompetitivo
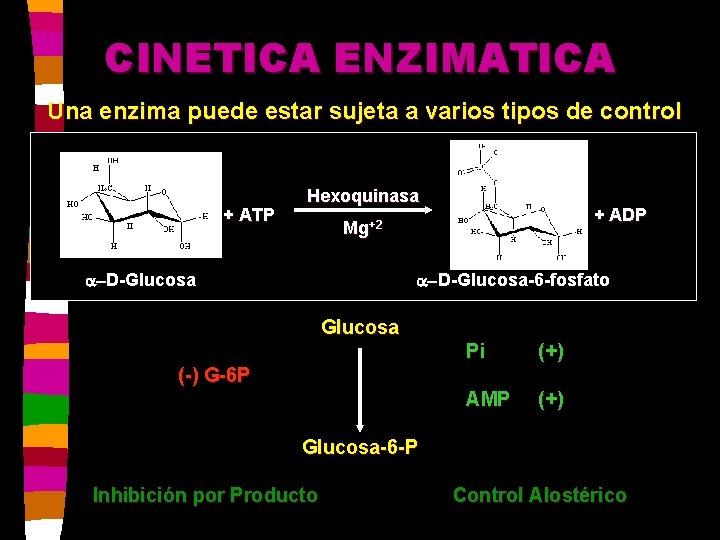
CINETICA ENZIMATICA Una enzima puede estar sujeta a varios tipos de control + ATP Hexoquinasa + ADP Mg+2 a-D-Glucosa-6 -fosfato Glucosa Pi (+) AMP (+) (-) G-6 P Glucosa-6 -P Inhibición por Producto Control Alostérico

CINETICA ENZIMATICA INHIBICION MIXTA COMPETITIVA – NO COMPETITIVA No competitiva L Malato + E-NAD+ OH-Malonato MDH Competitiva E-NADH + H+ + Oxalacetato
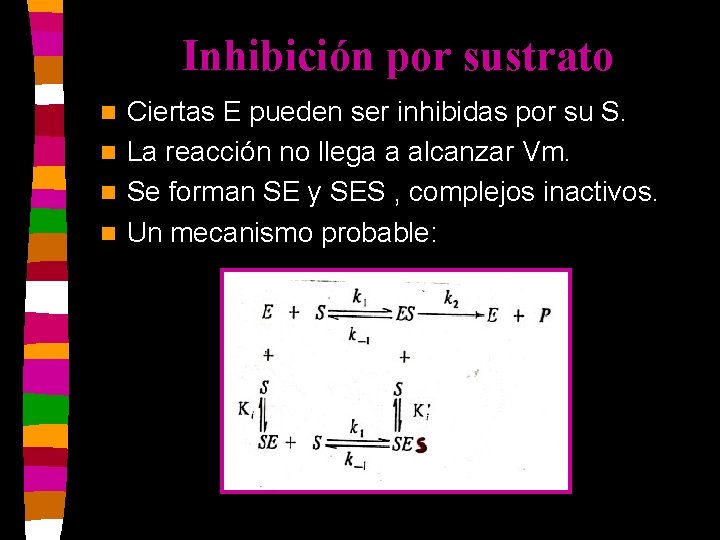
Inhibición por sustrato Ciertas E pueden ser inhibidas por su S. n La reacción no llega a alcanzar Vm. n Se forman SE y SES , complejos inactivos. n Un mecanismo probable: n
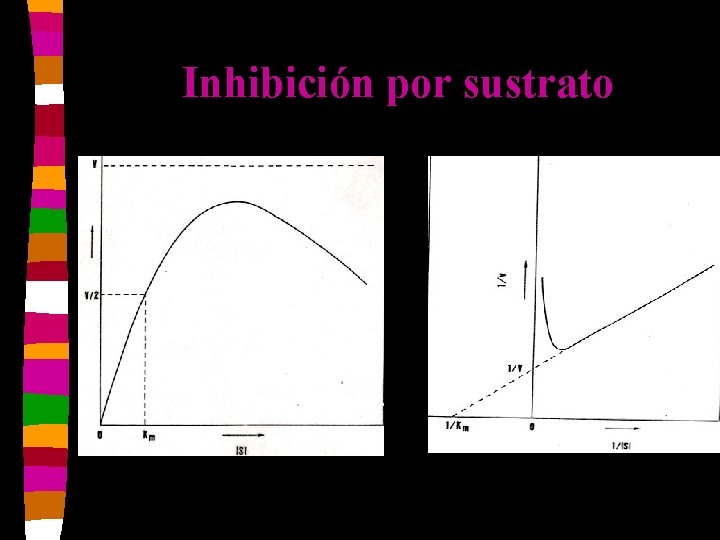
Inhibición por sustrato

Reacciones enzimáticas bisustrato n Isomerasas y liasas catalizan reacciones simples. n. S P 1 + P 2 n También hidrolasas: n A-B + H 2 O A-OH + BH n Muchos de los conceptos cinéticos para las reacciones monosustrato son válidas para reacciones más complejas.

Reacciones bisustrato n A. -Con formación secuencial de complejo ternario. E + S 1 + S 2 ES 1 S 2 EP 1 P 2 E + P 1 + P 2 n A 1. -Mecanismo ordenado S 1 E S 2 ES 1 P 1 ES 1 S 2 EP 1 P 2 EP 2 E
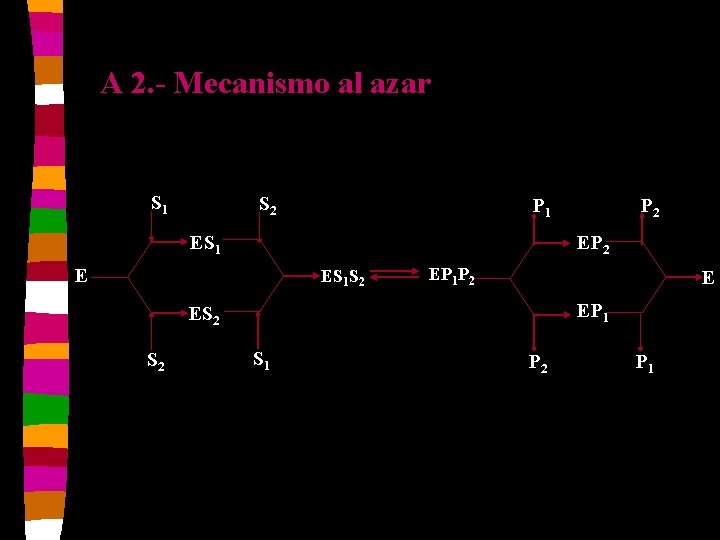
A 2. - Mecanismo al azar S 1 S 2 ES 1 EP 2 E ES 1 S 2 EP 1 P 2 E EP 1 ES 2 P 2 P 1 S 1 P 2 P 1

Reacciones bisustrato n. B 1. - No forma complejo ternario S 1 E S 2 P 1 ES 1 E, P 1 E, S 2 P 2 E, P 1 E Mecanismo de sustitución enzimática o PING PONG
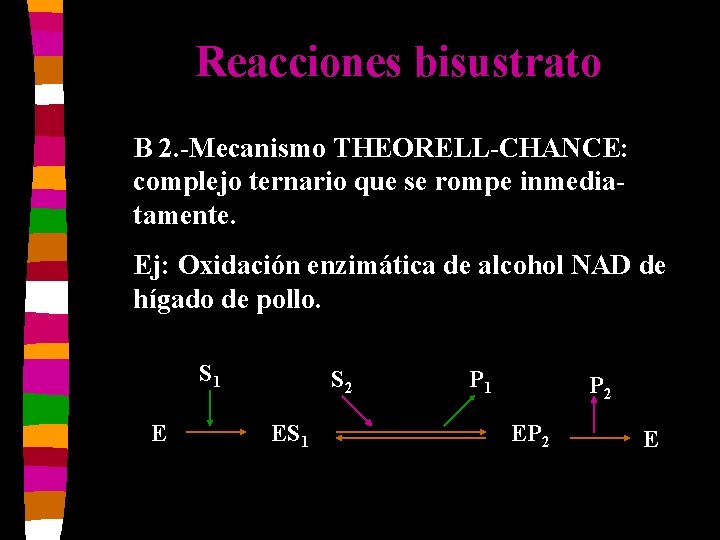
Reacciones bisustrato B 2. -Mecanismo THEORELL-CHANCE: complejo ternario que se rompe inmediatamente. Ej: Oxidación enzimática de alcohol NAD de hígado de pollo. S 1 E S 2 ES 1 P 2 EP 2 E

Inhibición por productos en reacciones bisustrato
- Slides: 33