Inhibice enzym Virov proteiny Petr Kolenko Inhibice enzym

Inhibice enzymů Virové proteiny Petr Kolenko

Inhibice enzymů - fyzikálně-chemická - změnou prostředí (p. H, teplota, apod. ) - ireverzibilní Strukturní reverzibilní inhibice enzymů: - kompetitivní - nekompetitivní - akompetitivní (smíšená)
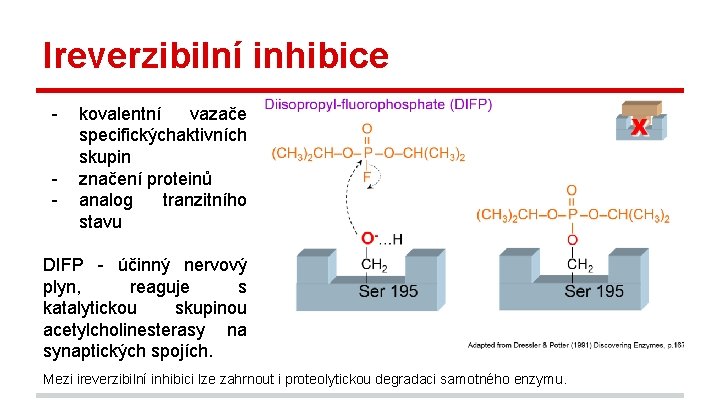
Ireverzibilní inhibice - kovalentní vazače specifickýchaktivních skupin značení proteinů analog tranzitního stavu DIFP - účinný nervový plyn, reaguje s katalytickou skupinou acetylcholinesterasy na synaptických spojích. Mezi ireverzibilní inhibici lze zahrnout i proteolytickou degradaci samotného enzymu.
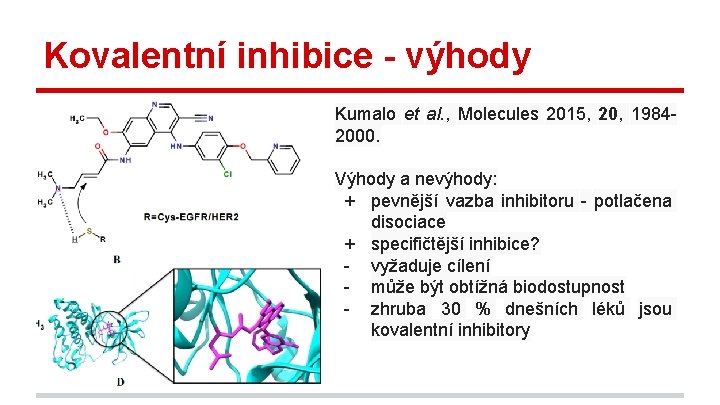
Kovalentní inhibice - výhody Kumalo et al. , Molecules 2015, 20, 19842000. Výhody a nevýhody: + pevnější vazba inhibitoru - potlačena disociace + specifičtější inhibice? - vyžaduje cílení - může být obtížná biodostupnost - zhruba 30 % dnešních léků jsou kovalentní inhibitory

Příklady léčiv - penicilin - sebevražedný inhibitor i analog substrátu kovalentně váže enzym transpeptidasu - bakteriální enzym, který se podílí na tvorbě buněčné stěny penicilin se váže velmi pevně a sám o sobě je velmi reaktivní po vazbě na transpeptidasu je komplex enzym: penicilin neaktivní http: //www. mpbio. com http: //www. antibioticslist. com/penicillin-group. html

Příklady léčiv - aspirin - acetylsalicilat, nesteroidní protizánětlivé léčivo, rovněž se dá používat k léčbě srážlivosti krve kovalentně (ireverzibilně) váže enzym PGH 2 synthasu, který se podílí na tvorbě prostaglandinu kovalentně váže residuum Ser v okolí aktivního místa a tím stericky znemožňuje substrátu dosáhnout aktivního místa http: //cbc. arizona. edu/classes/bioc 460/spring/460 web/le ctures/LEC 12_Enz. Inhib_08 -ppt. pdf health. harvard. edu
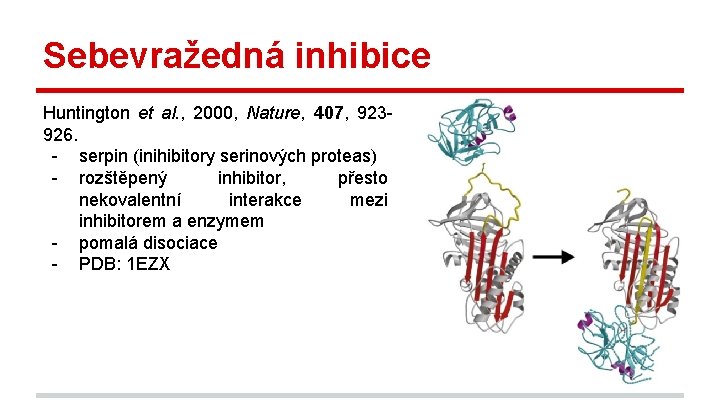
Sebevražedná inhibice Huntington et al. , 2000, Nature, 407, 923926. - serpin (inihibitory serinových proteas) - rozštěpený inhibitor, přesto nekovalentní interakce mezi inhibitorem a enzymem - pomalá disociace - PDB: 1 EZX

Reaktivace Pfl. B pomocí Yfi. D - enzym Pfl. B z E. coli (~ 160 k. Da) aktivován v anaerobním prostředí vytvořením glycylového radikálu na pozici Gly 734 přechodem do aerobního prostředí enzym na tomto místě proteolyticky degraduje, navíc zaniká potřeba zpracovávat sacharidy anaerobními metabolickými procesy opětovným přechodem do anaerobního prostředí bakterie nemusí syntetizovat celý protein znovu, ale pouze “reaktivátor” Yfi. D (~ 16 k. Da) energeticky výhodná reaktivace doposud strukturně neobjasněno - indicie na základě vysoké sekvenční podobnosti C-konců obou proteinů (přes 90 %) krystalová struktura samotného proteinu Yfi. D nepřispěla k objasnění doposud nepublikováno
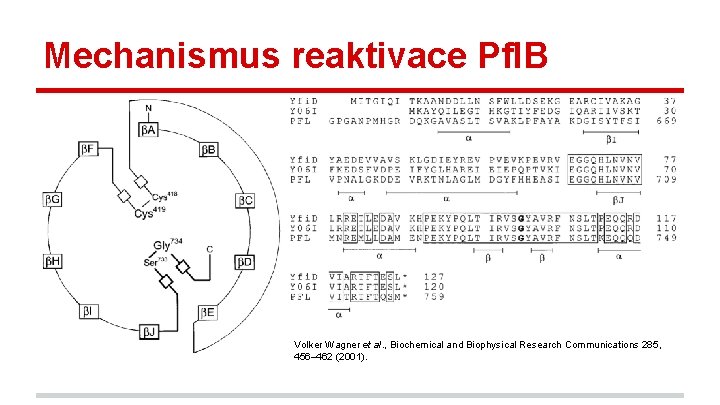
Mechanismus reaktivace Pfl. B Volker Wagner et al. , Biochemical and Biophysical Research Communications 285, 456– 462 (2001).
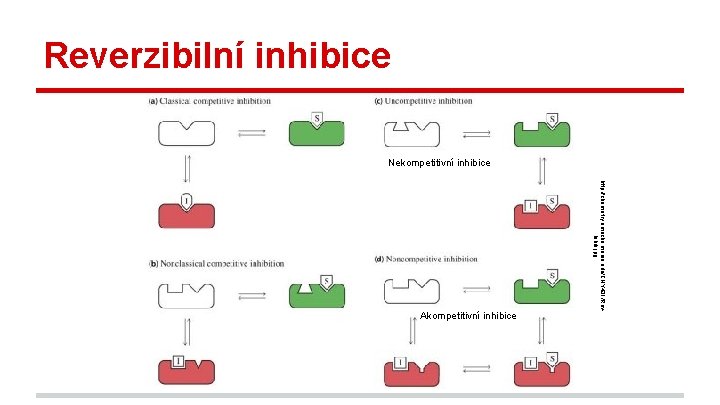
Reverzibilní inhibice Nekompetitivní inhibice http: //chemistry. umeche. maine. edu/CHY 431/Rev. Inhib. jpg Akompetitivní inhibice
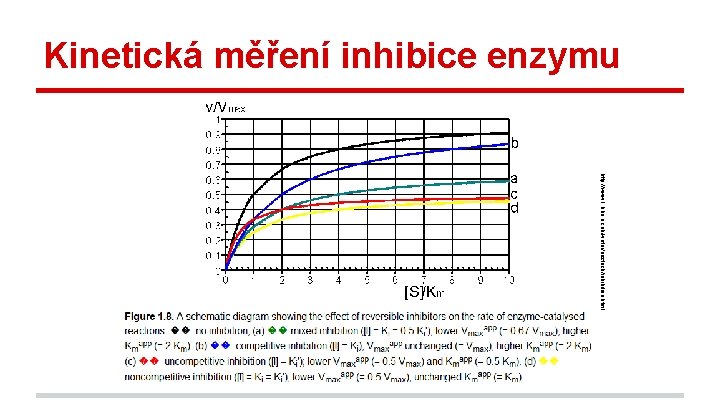
Kinetická měření inhibice enzymu http: //www 1. lsbu. ac. uk/water/enztech/inhibition. html
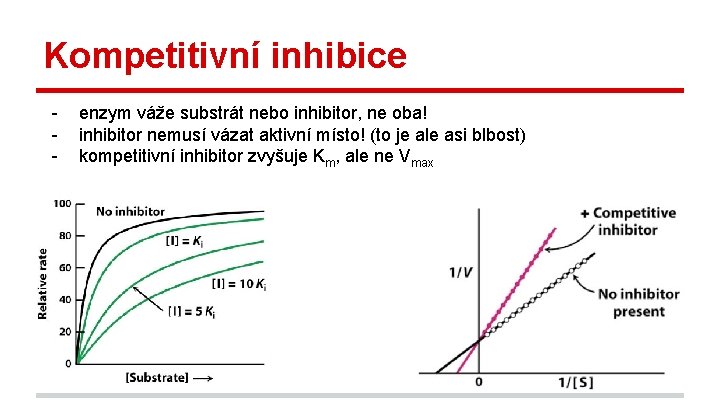
Kompetitivní inhibice - enzym váže substrát nebo inhibitor, ne oba! inhibitor nemusí vázat aktivní místo! (to je ale asi blbost) kompetitivní inhibitor zvyšuje Km, ale ne Vmax
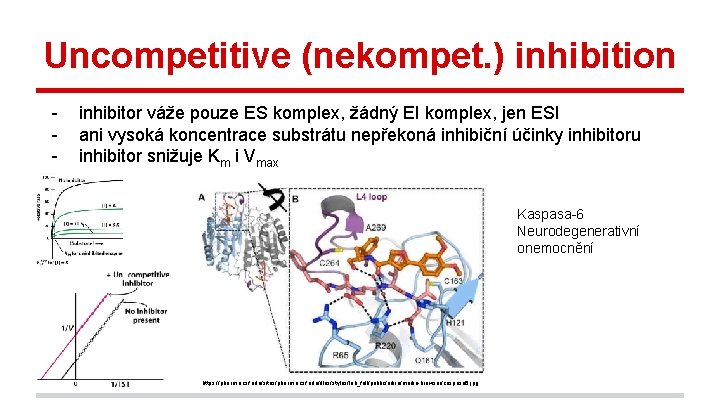
Uncompetitive (nekompet. ) inhibition - inhibitor váže pouze ES komplex, žádný EI komplex, jen ESI ani vysoká koncentrace substrátu nepřekoná inhibiční účinky inhibitoru inhibitor snižuje Km i Vmax Kaspasa-6 Neurodegenerativní onemocnění https: //pharm. ucsf. edu/sites/pharm. ucsf. edu/files/styles/lab_full/public/arkin/media-browser/caspase 6. jpg
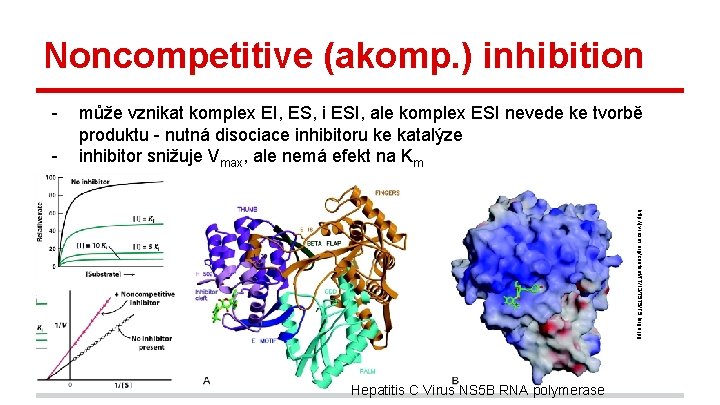
Noncompetitive (akomp. ) inhibition - může vznikat komplex EI, ES, i ESI, ale komplex ESI nevede ke tvorbě produktu - nutná disociace inhibitoru ke katalýze inhibitor snižuje Vmax, ale nemá efekt na Km http: //jvi. asm. org/content/77/13/7575/F 5. large. jpg Hepatitis C Virus NS 5 B RNA polymerase
Inhibice enzymů a strukturní analýza - - drtivá většina všech nových léků má v pozadí strukturní analýzu nejdříve se začíná jednoduchým inhibitorem - posléze rozšiřování, které vede obvykle k lepší inhibici nutnost neustále testovat mezikroky structure-based drug design, fragment -based drug design obvykle potřeba strukturních studií s vysokým rozlišením stanovené molekuly vody mohou napomáhat při analýze
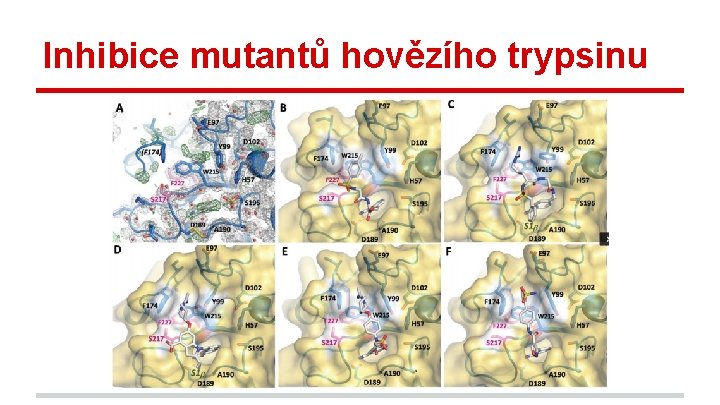
Inhibice mutantů hovězího trypsinu

Viry - - latinsky virus - jed malé nebuněčné organismy žádné virové onemocnění nelze léčit antibiotiky!!! virová částice složena především z bílkovin a nukleových kyselin, jsou výjimečně obaleny membránou původem z napadené buňky k růstu, dělení a životu využívají výhradně hostitelské buňky rozmanitá genetická informace může být ve formě DNA, RNA, ss. DNA, v jedné molekule, i ve více segmentech

Složení známých lidských virů - - stejně jako jiné organismy i viry podléhají evoluci a neustále se zdokonalují včetně mutací viry mohou napadat různé spektrum živých forem (přenosné vs. nepřenosné) genetický materiál obsahuje ve srovnání i s nejjednodušími bakteriemi obvykle podstatně redukované množství proteinů A. Liljas et al. , Textbook of Structural Biology, World Scientific Publishing, 2009

Mechanismus vniku do hostitele - různé způsoby, potřeba překonat buněčnou membránu, genom viru může putovat dále k buněčnému jádru, nebo přetrvávat v cytoplasmě po vniku jsou potlačeny životní mechanismy hostitelských buněk, využití směřováno k produkci nových virových částic Mechanismy: 1. přímá fúze s membránou (např. virus HIV) - díky tzv. fúzním proteinům 2. využití receptorové endocytosy - virus se naváže na receptor hostitelské buňky, dojde k vytvoření endocytolytického nosiče (vezikula) obsahujícího celou virovou částici uvnitř buňky
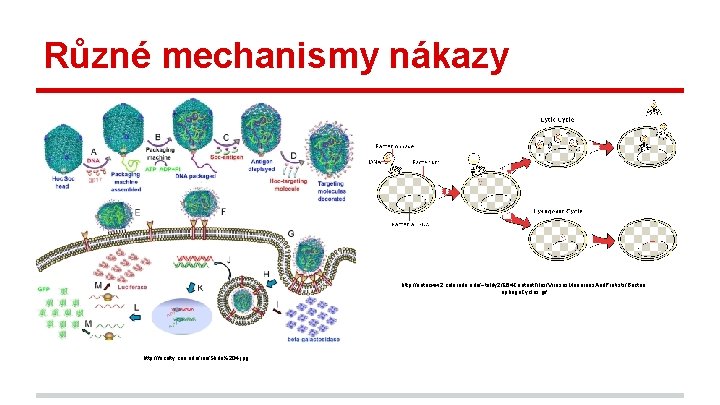
Různé mechanismy nákazy http: //autocww 2. colorado. edu/~toldy 2/E 64 Content. Files/Viruses. Monerans. And. Protists/Bacteri ophage. Cycles. gif http: //faculty. cua. edu/rao/Slide%204. jpg
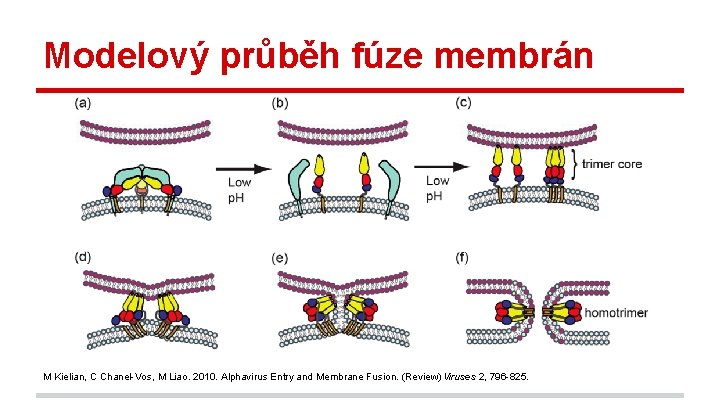
Modelový průběh fúze membrán M Kielian, C Chanel-Vos, M Liao. 2010. Alphavirus Entry and Membrane Fusion. (Review) Viruses 2, 796 -825.
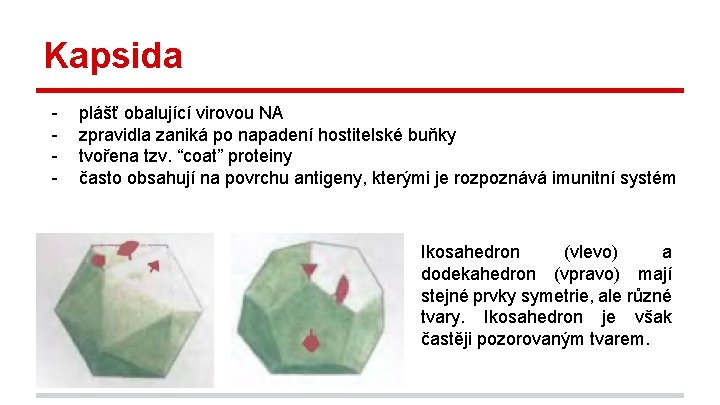
Kapsida - plášť obalující virovou NA zpravidla zaniká po napadení hostitelské buňky tvořena tzv. “coat” proteiny často obsahují na povrchu antigeny, kterými je rozpoznává imunitní systém Ikosahedron (vlevo) a dodekahedron (vpravo) mají stejné prvky symetrie, ale různé tvary. Ikosahedron je však častěji pozorovaným tvarem.
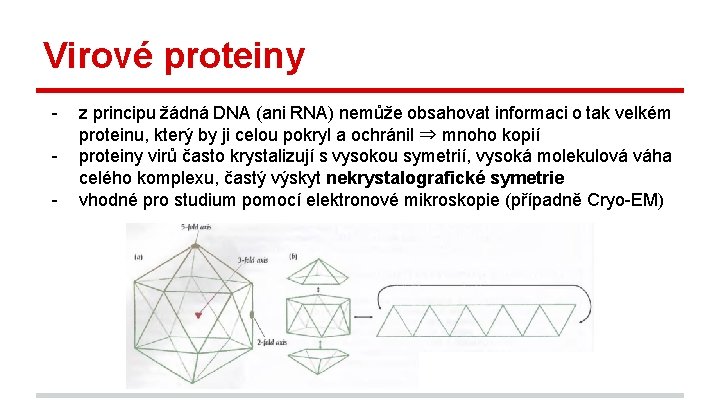
Virové proteiny - z principu žádná DNA (ani RNA) nemůže obsahovat informaci o tak velkém proteinu, který by ji celou pokryl a ochránil ⇒ mnoho kopií proteiny virů často krystalizují s vysokou symetrií, vysoká molekulová váha celého komplexu, častý výskyt nekrystalografické symetrie vhodné pro studium pomocí elektronové mikroskopie (případně Cryo-EM)
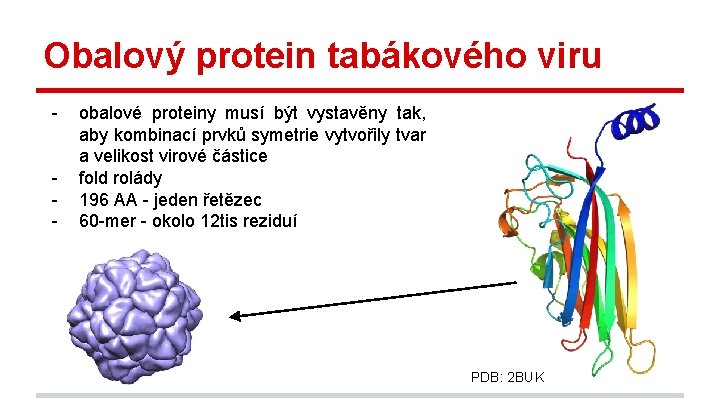
Obalový protein tabákového viru - obalové proteiny musí být vystavěny tak, aby kombinací prvků symetrie vytvořily tvar a velikost virové částice fold rolády 196 AA - jeden řetězec 60 -mer - okolo 12 tis reziduí PDB: 2 BUK

“Core” protein alfaviru - obalené RNA viry, které způsobují encefalitidu, horečku, artritidu a vyrážky u savců. dvě proteinové obálky (vnější glykoproteinovou a vnitřní “core”), které jsou odděleny lipidovou dvojvrstvou C-terminální část core-proteinu strukturně podobná chymotrypsinu pouze jeden řetězec, žádné disulfidy protein obsahuje katalytickou triádu Asp-His-Ser aktivace dlouhého prekursoru po odštěpení core-proteinu dochází k vazbě C-konce do aktivního místa a tím pádem k inhibici - prevence degradace dalších funkčních komponent viru samotného
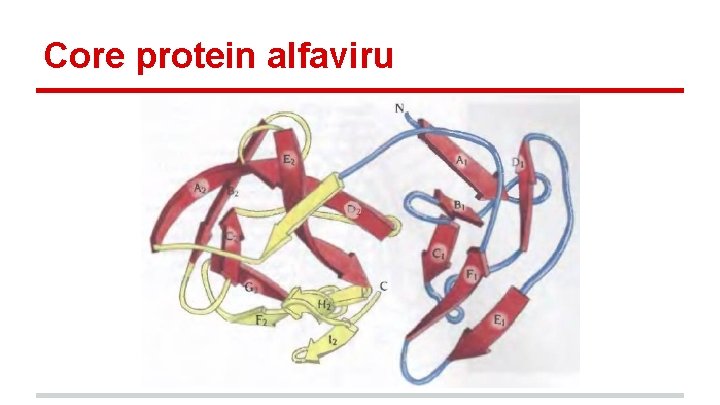
Core protein alfaviru

Fúzní peptidy a jejich “nositelé” - fúzní peptidy pomáhají virům ke kontaktu s membránou cílové buňky části obalových proteinů obvykle nejsou exponovány, ale uchovány uvnitř obalu, nebo kompenzovány dalšími interakcemi E 1 protein from the Semliki Forest virus, PDB: 1 I 9 W doi: 10. 3390/v 2040796 hemagglutinin, PDB: 1 RU 7

Vazba nukleových kyselin - obecně velmi důležitá pro přenos a ochranu NA do hostitelské buňky Fág MS 2: - 180 kopií obalového proteinu - 3500 basí ss. RNA - obalový protein funguje jako translační represor - váže smyčku asi 19 -ti nukleotidů obsahujících iniciační kodon replikovaného genu - tato vazba rovněž iniciační krok při uspořádávání částice - tzv. enkapsidační signál

Návrhy léčiv Cíl: zastavit virus, minimalizovat škody na hostitelském organismu! Výhody: - genetický materiál viru omezený - většina kódovaných proteinů velmi odlišná od proteinů hostitelských buněk Kroky viru vedoucí k nákaze vhodné pro návrhy léků: 1. interakce s hostitelskou buňkou 2. přenos a využití virového genu či enzymů do hostitelské buňky 3. formování a uvolnění celých nových virových částic z nakažené buňky
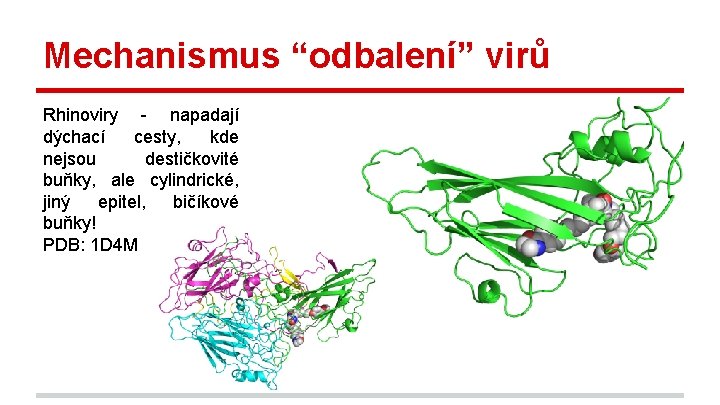
Mechanismus “odbalení” virů Rhinoviry - napadají dýchací cesty, kde nejsou destičkovité buňky, ale cylindrické, jiný epitel, bičíkové buňky! PDB: 1 D 4 M

Problémy při návrhu antivirotik - vakcíny obvykle působí dobře jen u probíhajících virů, ne v jeho počátcích rychlá mutace vede ke zrušení účinků léčiv (např. proti chřipce se vakcína musí měnit každý rok, nebo neschopnost úplně vyléčit virus HIV) stejně jako ostatní organismy i viry podléhají evoluci dlouhá cesta od zkumavky k testování na lidech - opět vyvstává etická otázka! (částečně i rasová a vliv prostředí apod. ) Problémy ve výzkumu léčiv: - tisíce až miliony kandidátů - finančně nákladná záležitost - obvykle nízká rozpustnost, či biodostupnost, fyzikální vlastnosti - testování na různých zvířecích modelech (mnoho kritérií) - vlastní imunitní systém může bojovat proti “cizímu” léku
- Slides: 31