Infecciones asociadas Duodenoscopios Recomendaciones M Ximena Pozo C




























- Slides: 32

Infecciones asociadas Duodenoscopios Recomendaciones M. Ximena Pozo C. Hospital Dipreca 2016

Referencias • En el 2013, Centro para el Control y la Prevención de Enfermedades (CDC) alertó a la FDA (Food and Drug Administration) por una posible asociación de bacterias y duodenoscopios, resistentes a múltiples fármacos • Ese año , 44 pacientes en Illinois fueron identificados con infecciones CRE (Enterobacteria resistente al Carbapenem), muchas relacionadas entre si. Un brote de CRE en el Virginia Mason Medical Center en Seattle 2012 hasta 2014 incluyó a 32 pacientes ( 11 murieron ) con infecciones relacionadas • CDC señala que 48 estados han tenido casos confirmados de infección por CRE y estima que esto representa aproximadamente 9. 300 infecciones y 610 muertes cada año en los Estados Unidos, a pesar de que pueden ser más.

Alerta FDA • Entre enero de 2013 y diciembre de 2014, el ente regulador recibió 75 reportes de infecciones por bacterias multirresistentes que, posiblemente, se transmitieron a partir de duodenoscopios deficientes en el reprocesamiento. • La FDA focaliza su atención en la emergencia de cepas de Enterobacterias resistentes a Carbapenem, en especial algunas cepas de Klebsiella sp. y Escherichia Coli. • La FDA sigue de cerca la posible asociación entre duodenoscopios reprocesados y la transmisión de agentes infecciosos

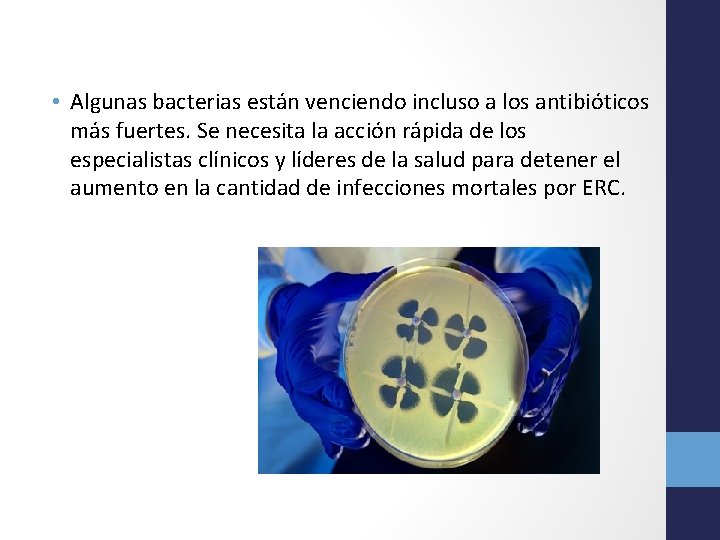
• Algunas bacterias están venciendo incluso a los antibióticos más fuertes. Se necesita la acción rápida de los especialistas clínicos y líderes de la salud para detener el aumento en la cantidad de infecciones mortales por ERC.

CRE, la “bacteria pesadilla” que asedia a los hospitales de EEUU • Al contrario que el resto de bacterias de la familia de las enterobacteriaceas –que comprenden treinta géneros y más de cien especies–, la CRE ha desarrollado una mutación que la hace resistente a los carbapenems, los antibióticos más poderosos que suelen emplearse como última línea defensiva. • La mortalidad que provoca el CRE es inusualmente alta: acaba con casi la mitad de los pacientes infectados.

• El director del CDC, Tom Frieden, ofreció una conferencia para alertar del peligro que puede suponer la bacteria. Su pronóstico fue pesimista: “Tenemos un escaso margen para detener la propagación”. En declaraciones a Discovery News, explicó además las dificultades que tienen para acabar con la “bacteria pesadilla”. Nuestros más poderosos antibióticos no funcionan”, asegura el médico, “y los pacientes son abandonados con infecciones potencialmente intratables”.

• Cualquier persona puede estar infectada con la CRE sin saberlo, pues puede vivir en el intestino sin causar ningún daño. El problema lo tienen las personas con un sistema inmune debilitado pues la bacteria puede entonces entrar en otras partes del cuerpo y provocar neumonía e infecciones de las vías urinarias y el torrente sanguíneo. • La resistencia a los antibióticos, un problema cada vez más grave

• Olympus América Latina tiene conocimiento de múltiples quejas sobre el duodenoscopio OLYMPUS TJF-Q 180 V, asociadas con infecciones en pacientes tras un procedimiento endoscópico en Estados Unidos. Algunas de estas quejas están asociadas con infecciones en pacientes con una entero bacteria resistente a las Carbapemenasas (CRE), que representa un problema de salud pública debido a que las opciones de tratamiento con antibióticos son limitadas. • Aunque el canal del alambre elevador del TJF-Q 180 V es sellado, el área alrededor y debajo de las partes móviles, tales como la uña del elevador, requieren de una limpieza manual meticulosa.


Comité Asesor de la FDA en combinación con el cumplimiento estricto de las instrucciones del Fabricante, deciden: • Cultivo microbiológico • Óxido de Etileno Esterilización • Uso de sistema de procesamiento de líquido esterilizante químico (DAN) • Repetir el proceso DAN • La FDA recomienda a los centros de salud que realizan CPRE evaluar si tienen la experiencia, la formación y los recursos para poner en práctica una o más de las opciones

Problemas Cultivo • Es una buena herramienta; sin embargo, la tasa de falsos positivos y falsos negativos y los límites de detección para la vigilancia microbiana aún no se han establecido para este método. • Si bien el cultivo rutinario de endoscopios no forma parte de las directrices actuales de Estados Unidos , los reciente brotes asociados han llevado a algunos centros a considerar el monitoreo regular para evaluar la adecuación de reprocesamiento. • Un cultivo negativo no excluye por completo la posibilidad de un duodenoscopio contaminado. • Cultivo positivo deben conducir a alguna acción tal como se describe a continuación:

• Acción Correctiva: Cualquier duodenoscopio encontrado contaminado con cualquier organismo de alto interés o inaceptable debe ser reprocesado de nuevo con la repetición después de reprocesamiento de un cultivo nuevo. • El duodenoscopio no debe ser utilizado de nuevo hasta que se ha demostrado estar libre de organismos de alto interés y tiene un nivel aceptable de los organismos bajo preocupación • Costo alto • Tiempo de espera de resultados

Oxido Etileno • Tiempo espera prolongado y costo elevado • Tóxico para el personal y para los pacientes si quedan residuos • Puede afectar las propiedades mecánicas del equipo • Evaluar oferta/demanda (tiempo prolongado) ATP • Los métodos no de cultivo, ensayos de bioluminiscencia han sido utilizado para evaluar el reprocesamiento mediante la detección de material orgánico residual después de limpieza. • Estos métodos carecen de correlación coherente para concentraciones bacterianas. Pueden, sin embargo, dar una idea sobre la calidad de reprocesamiento, si es validado sistemáticamente.

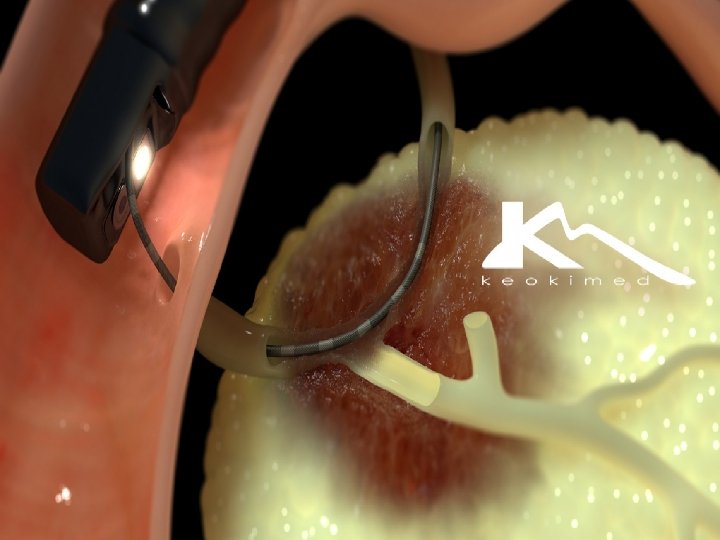
Duodenoscopios • Son tubos de fibra de vidrio delgados y flexibles. Su estructura incluye un canal que permite la irrigación continua de líquidos y medios de contraste, así como también la inserción de otros instrumentos • Poseen canal de aspiración y canal aire/agua • Algunos modelos poseen canal del elevador (más antiguos) • Canal del elevador, contiene un sistema móvil que optimiza el ajuste del ángulo de sus componentes, facilitando el tránsito del dispositivo a través de los conductos biliares. • Aunque el complejo diseño de los duodenoscopios mejora la eficiencia y la efectividad de la CPRE, es también un reto lograr una limpieza y desinfección de alto nivel, ya que algunas partes del visor pueden resultar difíciles de acceder para optimizar su higiene.






Recomendaciones Olympus • Tener en cuenta los cambios fundamentales en el procedimiento de transformación para su Olympus TJFQ 180 V • Durante la inmersión, levantar y bajar el ascensor tres veces. Además , el área alrededor del canal ascensor debe limpiarse con dos pinceles de diferentes tamaños , uno que los hospitales ya utilizan y otro que Olympus enviaría mayo 2015 • Personal altamente capacitado

Recomendaciones Olympus • Asegúrese de que todo el personal de reprocesamiento tiene total conocimiento y está totalmente capacitado en las instrucciones de reprocesamiento detalladas en el manual de reprocesamiento del TJF-Q 180 V. • Olympus América Latina le solicita reportar todas las quejas/eventos adversos, incluyendo cualquier infección o colonización microbiana persistente asociadas con los endoscopios Olympus

Recomendaciones FDA • Profesionales de la Salud : Informar a los pacientes sobre los beneficios y riesgos asociados con la CPRE. Discuta con sus pacientes lo que deben esperar después de la CPRE y qué síntomas debe impulsar a un seguimiento adicional. • Duodenoscopio debe estar completamente desinfectado entre usos y contar con un programa integral de calidad para su reprocesamiento. • Un duodenoscopio sospechoso de estar asociado a una infección del paciente después de la CPRE, debe quedar fuera de servicio y meticulosamente desinfectarlo hasta que se verifique esta libre de patógenos. • Presentar un informe al fabricante y a la FDA

Personal de Reprocesamiento • Seguir estrictamente las instrucciones de limpieza consignadas en el manual del equipo • Reportar las dificultades de reprocesamiento del duodenoscopio a la sección de la FDA encargada de este trámite. • Implementar un programa de control de calidad para el reprocesamiento de equipos para CPRE, que incluye procedimientos escritos para monitorear el avance de los aprendices de mantenimiento, la frecuencia con que éste debe realizarse y los certificados de pruebas de control de calidad a los que ha sido sometido el equipo. • Consultar la guía basada en la evidencia para reprocesamiento endoscópico, desarrollada por la Academia Americana de Endoscopia Gastrointestinal. El documento puede visualizarse en el siguiente enlace: www. asge. org

• La FDA continúa estructurando su postura al respecto mediante la consulta de literatura médica, la opinión de trabajadores de la salud expertos en el área, las sociedades médicas y los Centros para el Control y la Prevención de las Enfermedades de Estados Unidos (CDC). • Los médicos que utilizan duodenoscopios deben mantenerse al día con la información generada por la FDA y los CDC. Deben estar familiarizados con las directrices publicadas que describen las indicaciones apropiadas y selección de pacientes para CPRE.

Ultimas Novedades • 5 de octubre de, el año 2015 • La Administración de Alimentos y Medicamentos de EE. UU. ordenó hoy a los tres fabricantes de duodenoscopios comercializados en los EE. UU. para llevar a cabo estudios de vigilancia posterior a la comercialización para comprender mejor cómo los dispositivos se vuelven a procesar en los entornos del mundo real.

• « Los tres fabricantes - Olympus America, Inc. , Fujifilm Medical Systems, EE. UU. , Inc. , y Hoya Corp. (División de Cuidado de Vida Pentax), tendrán 30 días para presentar los planes de vigilancia posterior a la comercialización, a la FDA. Estas propuestas deben detallar sus planes para llevar a cabo estudios para evaluar, entre otras cosas, qué tan bien el personal de atención de la salud están siguiendo las instrucciones para limpiar y desinfectar duodenoscopios entre los pacientes y para comprender mejor la tasa de contaminación de duodenoscopios de uso clínico. Estos estudios se basan en la comprensión actual de la FDA de los factores que pueden contribuir a los brotes de infección siguiendo los procedimientos de la colangiopancreatografía retrógrada endoscópica (CPRE), así como la información necesaria para ayudar a llenar las lagunas en el conocimiento» .

• En enero de 2016, la Agencia notificó a Olympus que las instrucciones de reprocesamiento actualizados para los modelos duodenoscopio the 160 F / FV eran adecuadas. • Además, la FDA tiene las siguientes recomendaciones para las instalaciones y el personal que utilizan y reprocesar Olympus 160 modelos duodenoscopio F / VF • Implementar la limpieza manual actualizada y procedimientos de desinfección de alto nivel para 160 modelos duodenoscopio F / VF de Olympus, de acuerdo con las instrucciones de reprocesamiento actualizados.

• Instrucciones de reprocesamiento PENTAX Valida para la DE-3490 TK vídeo duodenoscopios: Comunicación Seguridad de la FDA • Fecha de publicación: 19 Febrero el año 2016 • PENTAX ha emitido actualizada, instrucciones de reprocesamiento manuales validados para el ED 3490 TK vídeo duodenoscopio para sustituir al que dispone en el etiquetado dispositivo original. La FDA revisó estas instrucciones de reprocesamiento y actualizados los datos de validación y recomienda que las instalaciones que utilizan capacitar al personal PENTAX ED-3490 TK vídeo duodenoscopios en las instrucciones actualizadas y poner en práctica tan pronto como sea posible.

• FUJIFILM Medical Systems, EE. UU. , Inc. Valida revisadas Instrucciones de reprocesamiento para el modelo ED 530 XT duodenoscopios: Comunicación Seguridad de la FDA • Fecha de publicación: 23 de diciembre de, el año 2015 • Fuji emitió el nuevo, validó las instrucciones de reprocesamiento manual para el duodenoscopio ED-530 XT para sustituir a las previstas en el etiquetado dispositivo original. La FDA revisó las instrucciones de reprocesamiento revisados y los datos de validación y determinó que cumplan con las expectativas de la Agencia. Recomendamos que las instalaciones utilizando ED-530 XT capacitar al personal duodenoscopio de Fuji sobre las nuevas instrucciones y ponerlas en práctica tan pronto como sea posible.

Conclusiones • La base esta en la limpieza del equipo • El reprocesamiento de los Duodenoscopios debe estar protocolizado, de acuerdo al modelo. • Supervisión y revisión sistemática del procedimiento • Garantizar cumplimiento estricto de instrucciones del fabricante , para su limpieza, desinfección y/o esterilización. • Capacitación contínua a lo menos dos veces al año • Protocolo de seguimiento a los paciente sometidos a Colangiopancreatografia Retrograda (CPRE) • Registros claros, para trazabilidad de brotes • Protocolizar toma de cultivo según cada establecimiento Se sigue avanzando en mejoras para evitar IAAS por la FDA, CDC, Industria y organizaciones profesionales


Bibliografía • Supplemental Measures to Enhance Duodenoscope Reprocessing • Olympus Validates New Reprocessing Instructions for Model TJFQ 180 V Duodenoscopes Safety Communication, March 2015 • Pentax Validates New Reprocessing Instructions for Model DE 3490 TK Duodenoscopes Safety Communication , Febrero 2016 • Fujifilm Validates New Reprocessing Instructions for modelo ED -530 XT Duodenoscopes Safety Communication, Diciembre 2015 • HIGH PRIORITY HAZARD REPORTECRI Institute Recommends Culturing Duodenoscopes as a Key Step to Reducing CRE Infections ECRI Institute 2015 | www. ecri. org/cre • CDC Interim Duodenoscope Sampling Algorithm