Infeccin asociada a catter central IACC IACC diagnstico
















































- Slides: 64

Infección asociada a catéter central (IACC)

IACC - diagnóstico • Si se retira catéter: • Punta de catéter y Hemo. C con el mismo organismo • Se mantiene catéter: Catéter Periférico + + IACC, si: + - + Colonización catéter Diagnóstico • • Cuantitativo: Catéter ≥ 3 vs. sangre periférica Crecimiento previo ≥ 2 horas catéter vs. Sangre periférica Bacteremia no relacionada a catéter Rebatet, G. A. , Gabriela, L. J. , Mc. Phee, S. J. , Papadakis, M. A. , María, P. T. , & Rabow, M. W. (2017). Diagnóstico clínico y tratamiento 2017. México: Mc. Graw. Hill. Education. pp. 1287 - 1560

IACC – tratamiento empírico • Vancomicina sola, pero agregar: • Cobertura anti – Pseudomonas, BGN si: • • Choque séptico Neutropenia Colonizado con BGN resistente Línea femoral • Antifúgico (equinocandina) • • • Puede ser fluconazol: no azoles en 3 meses previos, resistencia baja Antibacterianos previos de amplio espectro ≥ 1 sitios colonizados con Candida Cáncer hematológico Línea femoral NPT

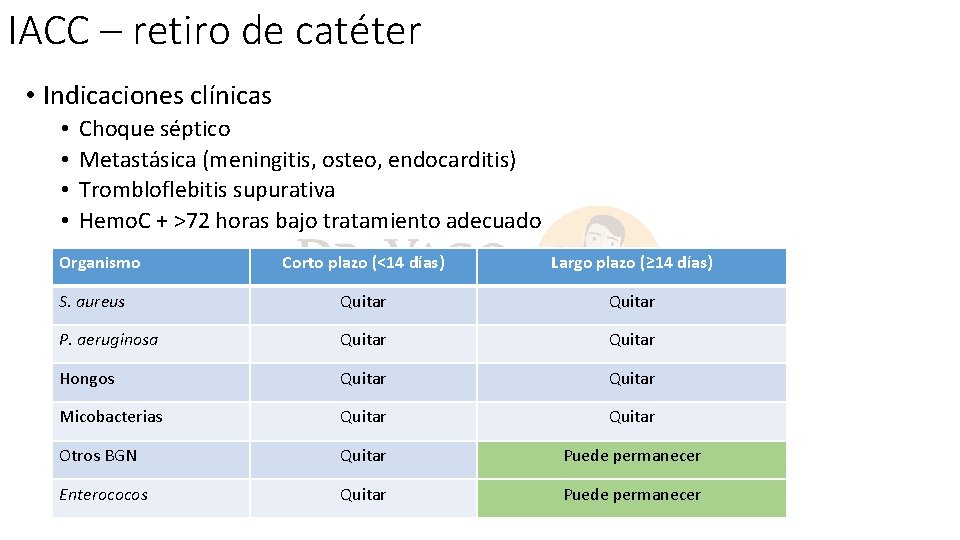
IACC – retiro de catéter • Indicaciones clínicas • • Choque séptico Metastásica (meningitis, osteo, endocarditis) Trombloflebitis supurativa Hemo. C + >72 horas bajo tratamiento adecuado Organismo Corto plazo (<14 días) Largo plazo (≥ 14 días) S. aureus Quitar P. aeruginosa Quitar Hongos Quitar Micobacterias Quitar Otros BGN Quitar Puede permanecer Enterococos Quitar Puede permanecer

IACC – duración del tratamiento. Posterior al primero HC negativo • 7 – 14 días • A excepción si algo de lo posterior • 2 semanas • Hongos • S. aureus, solo si: • No: DM, imunosuprimido, prótesis, metástasis y • ECO TEE negativo, Hemo. C negativo a las 72 hrs posteriores retiro del catéter

IACC – duración del tratamiento. Posterior al primero HC negativo • 4 – 6 semanas • S. aureus • Hemo. C +, >72 hrs posterior al tratamiento • Metastásico • 6 – 8 semanas • Osteomielitis por S. aureus

Bacterias y cáncer de colon

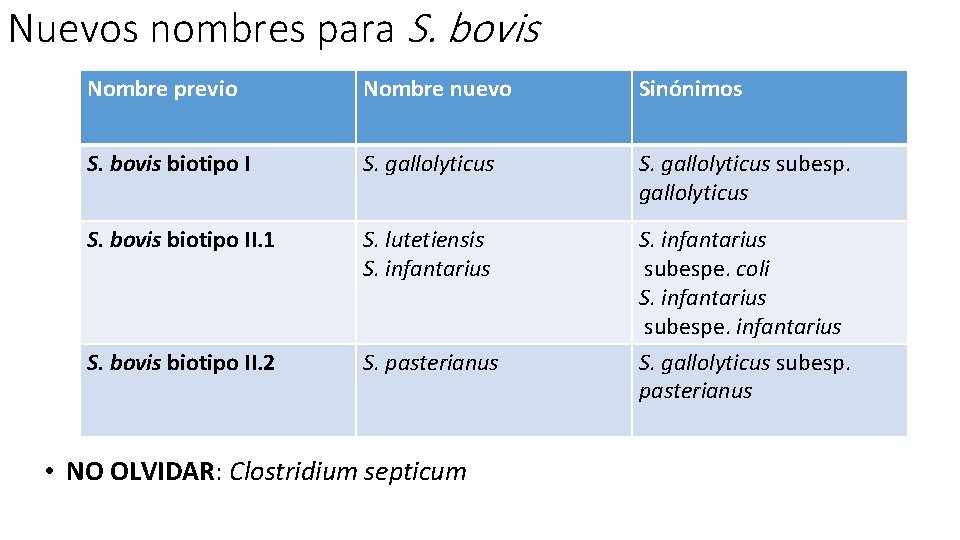
Nuevos nombres para S. bovis Nombre previo Nombre nuevo Sinónimos S. bovis biotipo I S. gallolyticus subesp. gallolyticus S. bovis biotipo II. 1 S. lutetiensis S. infantarius S. bovis biotipo II. 2 S. pasterianus S. infantarius subespe. coli S. infantarius subespe. infantarius S. gallolyticus subesp. pasterianus • NO OLVIDAR: Clostridium septicum

Meningitis por criptococo

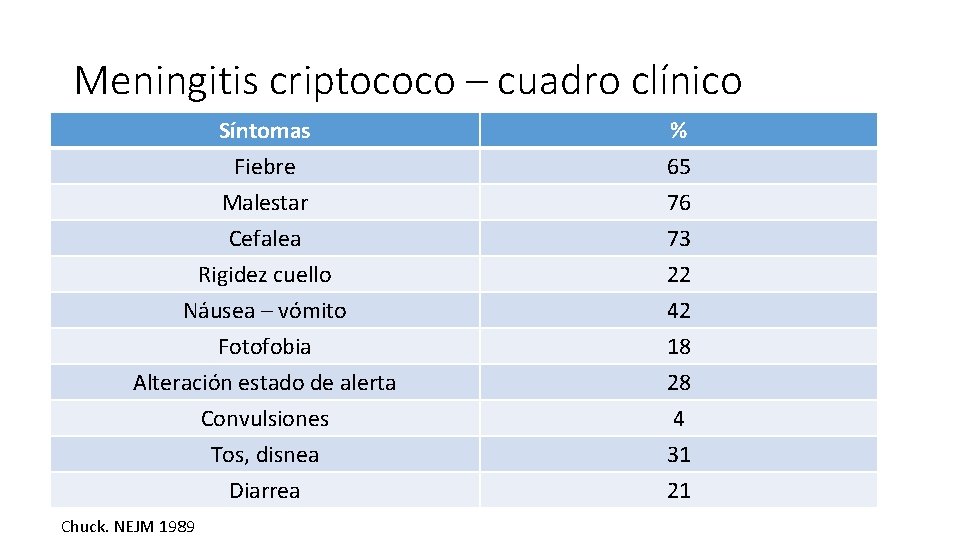
Meningitis criptococo – cuadro clínico Síntomas Fiebre Malestar Cefalea % 65 76 73 Rigidez cuello Náusea – vómito Fotofobia Alteración estado de alerta Convulsiones Tos, disnea Diarrea 22 42 18 28 4 31 21 Chuck. NEJM 1989

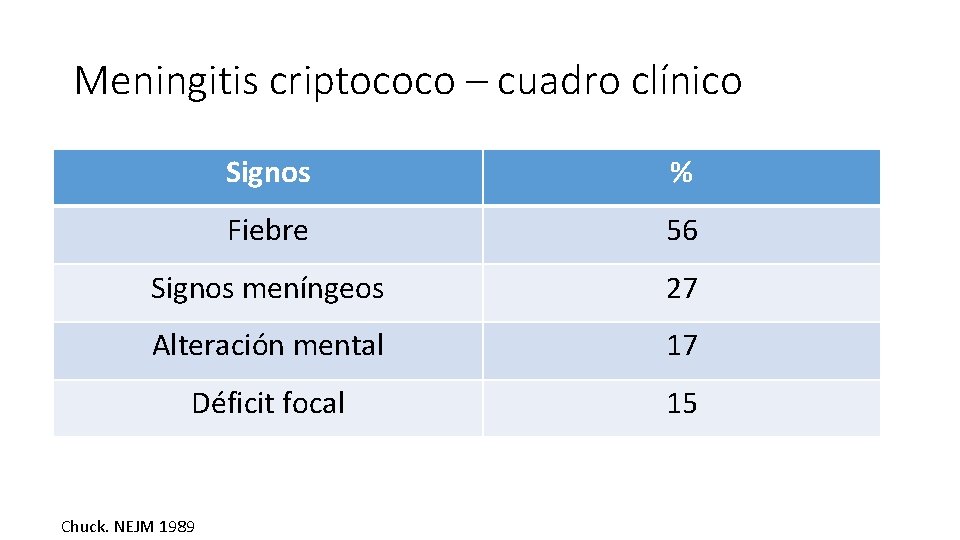
Meningitis criptococo – cuadro clínico Signos % Fiebre 56 Signos meníngeos 27 Alteración mental 17 Déficit focal 15 Chuck. NEJM 1989

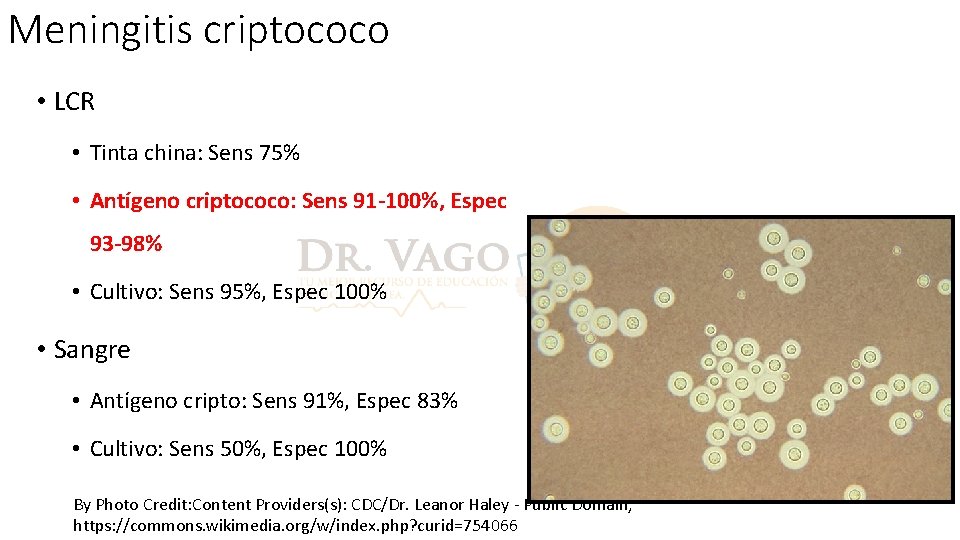
Meningitis criptococo • LCR • Tinta china: Sens 75% • Antígeno criptococo: Sens 91 -100%, Espec 93 -98% • Cultivo: Sens 95%, Espec 100% • Sangre • Antígeno cripto: Sens 91%, Espec 83% • Cultivo: Sens 50%, Espec 100% By Photo Credit: Content Providers(s): CDC/Dr. Leanor Haley - Public Domain, https: //commons. wikimedia. org/w/index. php? curid=754066

Meningitis criptococo - tratamiento • Inducción (2 semanas) • Anfotericina B liposomal + 5 -fluorocitosina* • Repetir PL para mantener presión de apertura normal • Consolidación (8 semanas) • Fluconazol 400 mg/día • Mantenimiento (>1 año) • Fluconazol 200 mg/día • Suspender cuando CD 4+ >100 *5 FC: Difícil de encontrar en México

Infecciones post – trasplante

Infecciones post – trasplante • Principios generales • • • Tiempo es predictivo Signos y síntomas ausentes La anatomía alterada, altera los signos Más común resistencia antibiótica Patógenos múltiples Pueden estar presentes múltiples patógenos • Diagnóstico • Cultivos, detección antígenos, biopsias • Serología usualmente no es útil

Infecciones post – trasplante <1 mes • Derivadas del recipiente • • Sitio quirúrgico, líneas, neumonía intrahospitalaria, IVU Reactivación Hepatitis B y C Clostridium difficile Strongyloides stercoralis • Derivadas del donador • • Tamizaje: HSC, CMV, VIH, Sífilis Bacterias resistente: MRSA, Enterococo resistente a vancomicina Hongos: Candida resistente Toxoplasmosis

Infecciones post – trasplante: 1 – 6 meses • Oportunistas • Hongos: PCP, endémicos • Virus: HSV, VVZ, CMV, BK, JC • Bacterias: Micobacterias • Parásitos: Toxo, Cryptosporidium, Microsporidium • Profilaxis • Pneumocystis (TMP/SMX) • Virus herpes (Valganciclovir)

Infecciones post – trasplante >6 meses • Adquiridas en la comunidad • Infecciones virales tardías • CMV, VHS • Enfermedad linfoproliferativa post – trasplante (EBV) • BK • Leucoencefalopatía multifocal progresiva (JC) • Hongos • Aspergillus, Mucor, Cryptococcus • Bacterias • Nocardia, Rhodococcus

Neumonía rápidamente progresiva post trasplante • Bacterias • Patógenos usuales • Nocardia, Legionella, Rhodococcus • Hongos • PCP, Aspergillus, Cryptococcus, endémicos • Virus • CMV, VVZ, influenza, VSR

Riesgo de enfermedad CMV de acuerdo a estado del donador Seroestado del receptor + - 50% 20% 75% <5%

Enfermedad CMV en inmunocomprometidos • Pulmonar: neumonía • Ocular: retinitis • GI: esofagitis, enteritis, colitis • Neurológico: encefalitis, meningitis, mielitis, polirradiculopatía

Diagnóstico de enfermedad CMV • DNA y antígenos en sangre • Indican infección, no necesariamente enfermedad • Cultivos • Sangre indica infección, no enfermedad • Tejido, posible falso positivo (por viremia) • Tardan tiempo • Serología • No útil por inmunosupresión • Biopsia tejido • DIAGNÓSTICO: Inclusiones y/o tinciones de IHQ

Exantemáticas

Sarampión - epidemiología • Único reservorio: humanos • Diseminación por aerosoles (horas) • Pre vacuna: • 15 años edad 90% • Índice infección 75% • EUA: 4 millones casos/anuales • Post vacuna: • 1990: 27, 000 casos (epidemia) • Siglo XXI: 63 casos/año

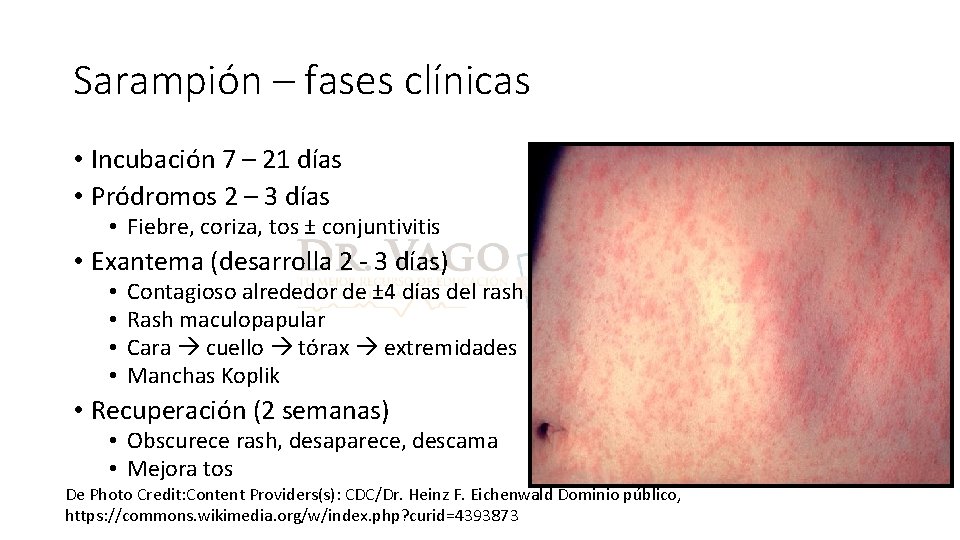
Sarampión – fases clínicas • Incubación 7 – 21 días • Pródromos 2 – 3 días • Fiebre, coriza, tos ± conjuntivitis • Exantema (desarrolla 2 - 3 días) • • Contagioso alrededor de ± 4 días del rash Rash maculopapular Cara cuello tórax extremidades Manchas Koplik • Recuperación (2 semanas) • Obscurece rash, desaparece, descama • Mejora tos De Photo Credit: Content Providers(s): CDC/Dr. Heinz F. Eichenwald Dominio público, https: //commons. wikimedia. org/w/index. php? curid=4393873

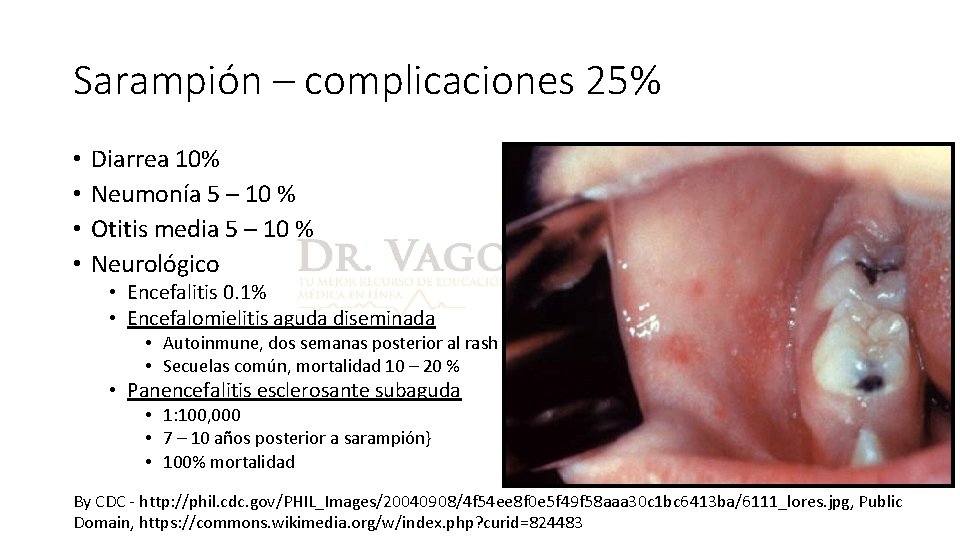
Sarampión – complicaciones 25% • • Diarrea 10% Neumonía 5 – 10 % Otitis media 5 – 10 % Neurológico • Encefalitis 0. 1% • Encefalomielitis aguda diseminada • Autoinmune, dos semanas posterior al rash • Secuelas común, mortalidad 10 – 20 % • Panencefalitis esclerosante subaguda • 1: 100, 000 • 7 – 10 años posterior a sarampión} • 100% mortalidad By CDC - http: //phil. cdc. gov/PHIL_Images/20040908/4 f 54 ee 8 f 0 e 5 f 49 f 58 aaa 30 c 1 bc 6413 ba/6111_lores. jpg, Public Domain, https: //commons. wikimedia. org/w/index. php? curid=824483

Sarampión • Diagnóstico • Clínico • PCR • Serología retrospectiva • Prevención • Vacuna viva atenuada (1968) • Inmunidad de por vida • Tratamiento: soporte

Virus sincitial respiratorio (VSR) • Epidemio • • Pico enero – febrero Transmisión secreciones y fomites Niños <1, adultos >65 Universal a los 3 años de edad, desaparece inmunidad • Clínico • Incubación 4 – 6 días • Bronquitis, broncoespasmo, neumonía • Diagnóstico: antígeno rápido • Tratamiento • Inmunocomprometidos: ribavirina

Faringitis y rash

Faringitis y rash No infeccioso Pénfigo / penfigoide LES Kawasaki Eritema multiforme Necrolisis epidérmica tóxica Infeccioso S. pyogenes VIH Arcanobacterium hemolyticum Mycoplasma pneumoniae EBV Virus Coxsackie Síndrome choque tóxico

Actinomyces y Nocardia

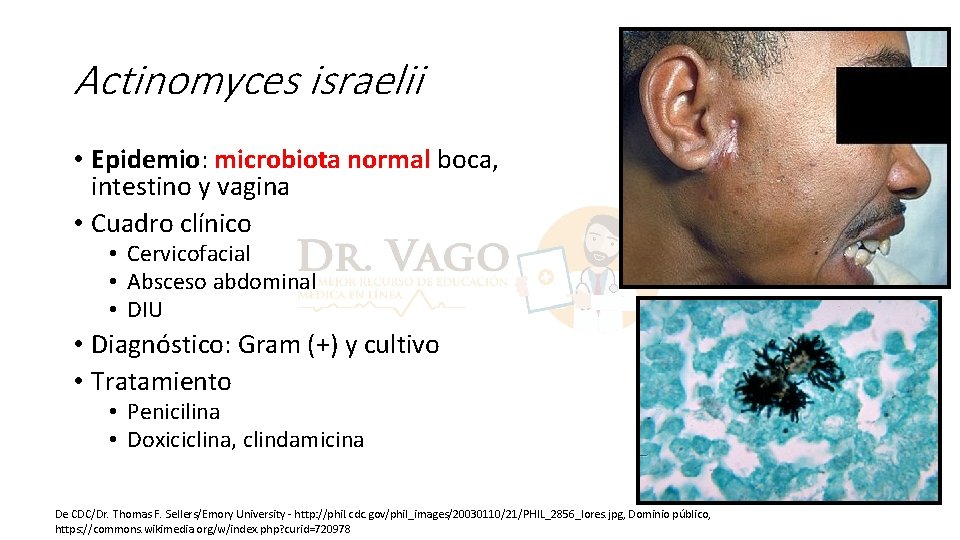
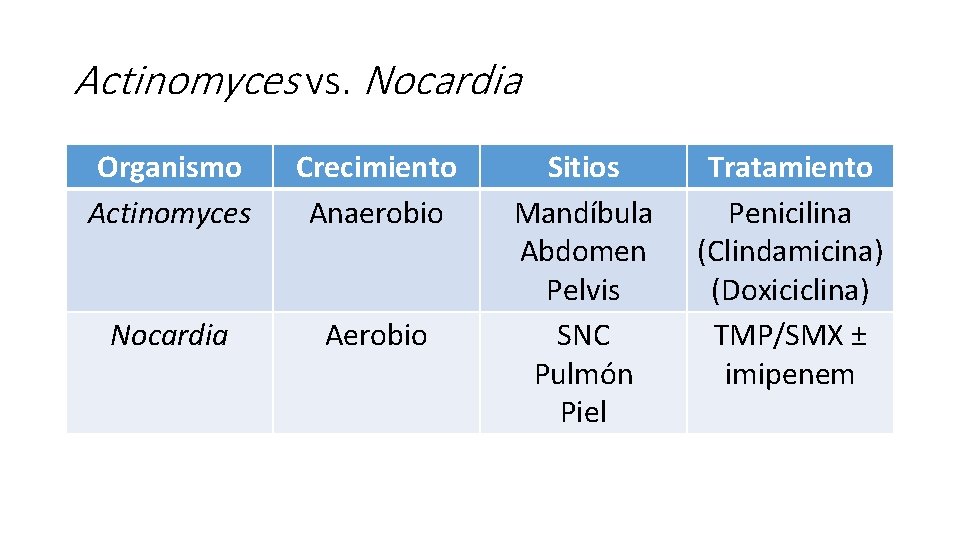
Actinomyces israelii • Epidemio: microbiota normal boca, intestino y vagina • Cuadro clínico • Cervicofacial • Absceso abdominal • DIU • Diagnóstico: Gram (+) y cultivo • Tratamiento • Penicilina • Doxiciclina, clindamicina De CDC/Dr. Thomas F. Sellers/Emory University - http: //phil. cdc. gov/phil_images/20030110/21/PHIL_2856_lores. jpg, Dominio público, https: //commons. wikimedia. org/w/index. php? curid=720978

Nocardia asteroides • Epidemio: • Aerobio, NUNCA microbiota normal • 70% pacientes, compromiso inmunidad celular • Cuadro clínico • SNC • Pulmonar • Cutáneo • Diagnóstico • Gram, cultivo • Tratamiento: TMP/SMX ± imipenem (si grave) By Donated by the pathologist at work. - Work, Attribution, https: //commons. wikimedia. org/w/index. php? curid=11520946

Actinomyces vs. Nocardia Organismo Actinomyces Crecimiento Anaerobio Nocardia Aerobio Sitios Mandíbula Abdomen Pelvis SNC Pulmón Piel Tratamiento Penicilina (Clindamicina) (Doxiciclina) TMP/SMX ± imipenem

Rinosinusitis – indicaciones antibióticos 1. Persistente y no mejoría >10 días • 60% tendrá infección bacteriana 2. Grave por >3 días ó • T >38. 9 C y secreción purulenta • Dolor facial 3. “Doble-enfermedad”, nuevo inicio >3 días • Cefalea • Secreción

Rinosinusitis – microbiología bacteriana Patógeno S. pneumoniae H. influenzae Anaerobios Streptococcus spp. Moraxella catarrhalis S. aureus Otros % casos 41% 35% 7% 7% 4% 3% 4%

Rinosinusitis – riesgo de resistencia • Edad <2 o >65 años • Guarderías • Antibióticos en el mes pasado • Hospitalizado en los últimos 5 días • Comorbilidades (corazón, pulmón) • Inmunocomprometidos

Rinosinusitis - antibióticos • 1ª línea (sin riesgo resistencia) • Amoxicilina / clavulanato • 2ª línea (riesgo de resistencia) • Doxiciclina • FQ • NO USAR • Macrólidos • TMP/SMX • Cefalosporinas

Rinosinusitis - adyuvantes • SS 0. 9% intranasal • Esteroides intranasales • Sospecha de etiología alérgica • No beneficio • Descongestionantes • Antihistamínicos

Rinosinusitis – duración tratamiento • Mejoría posterior a 3 – 5 días • 1ª línea: completar total 5 – 7 días • 2ª línea: completar 7 – 10 días • No mejoría o empeora 3 – 5 días • Ampliar o cambiar cobertura • Sin mejoría 3 – 5 días más • Considerar causas no infecciosas • TC, descartar complicaciones • Cultivos meatales para dirigir tratamiento

Fiebre tifoidea

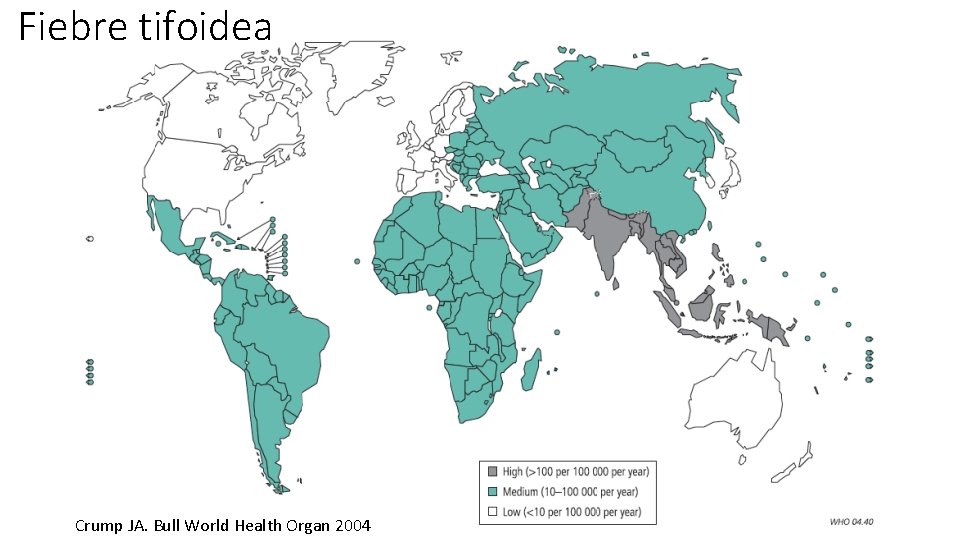
Fiebre tifoidea Crump JA. Bull World Health Organ 2004

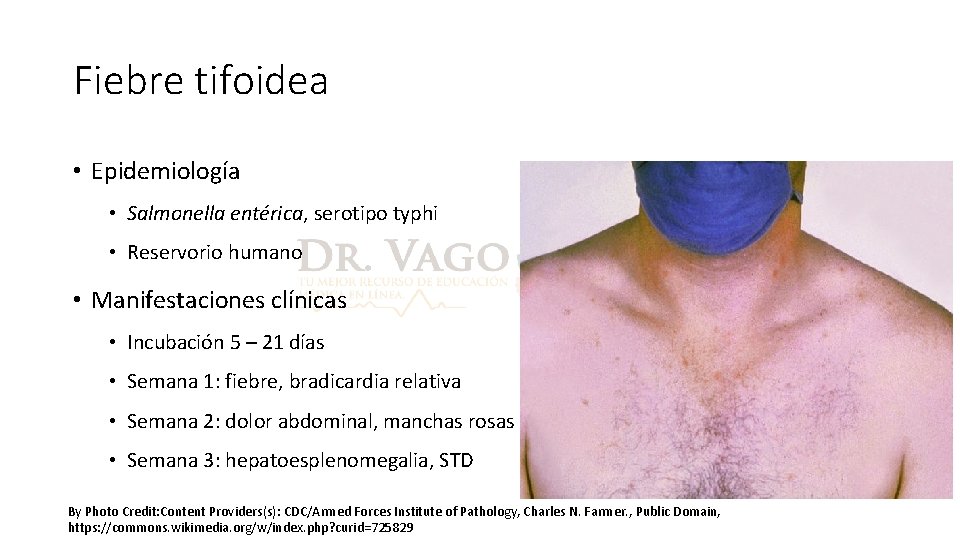
Fiebre tifoidea • Epidemiología • Salmonella entérica, serotipo typhi • Reservorio humano • Manifestaciones clínicas • Incubación 5 – 21 días • Semana 1: fiebre, bradicardia relativa • Semana 2: dolor abdominal, manchas rosas • Semana 3: hepatoesplenomegalia, STD By Photo Credit: Content Providers(s): CDC/Armed Forces Institute of Pathology, Charles N. Farmer. , Public Domain, https: //commons. wikimedia. org/w/index. php? curid=725829

Fiebre tifoidea – laboratorios y cultivos • Laboratorio • Pancitopenia • Elevación de transaminasas • Cultivos • • • Orina 10 – 25% Heces 10 – 25% Manchas rosas 40 – 50% Sangre 40 – 80% AMO 80 – 95%

Fiebre tifoidea - tratamiento • Tratamiento • 1ª línea: FQ • También a portadores (heces/orina (+) >12 meses) • Alternativas: azitromicina, ceftriaxona, cloranfenicol • Prevención (eficacia a 1 año) • Vacuna inactivada: 69% • Vacuna oral: 35%

Dengue

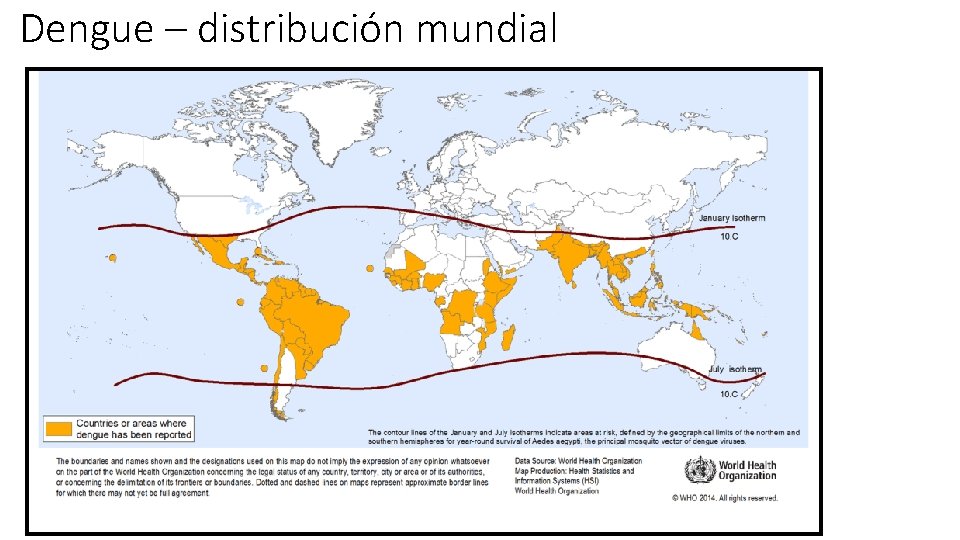
Dengue – distribución mundial

Dengue • Arbovirus más común mundialmente • Mosquito Aedes • 4 serotipos: inmunidad de por vida • Peor pronóstico si infección por otro serotipo • Dengue clásico (incubación 4 – 7 días) • Cefalea intensa, dolor osteomuscular, fiebre • Hemorragia: 10 – 20% • Autolimitado, 7 días

Dengue • Dengue hemorrágico • Síndrome de fuga capilar, sitios múltiples hemorrágicos choque • Diagnóstico • Serología • PCR • Tratamiento • Soporte • Plaquetas <100, 000 y sangrado activo • Prevención vacuna: Dengvaxia

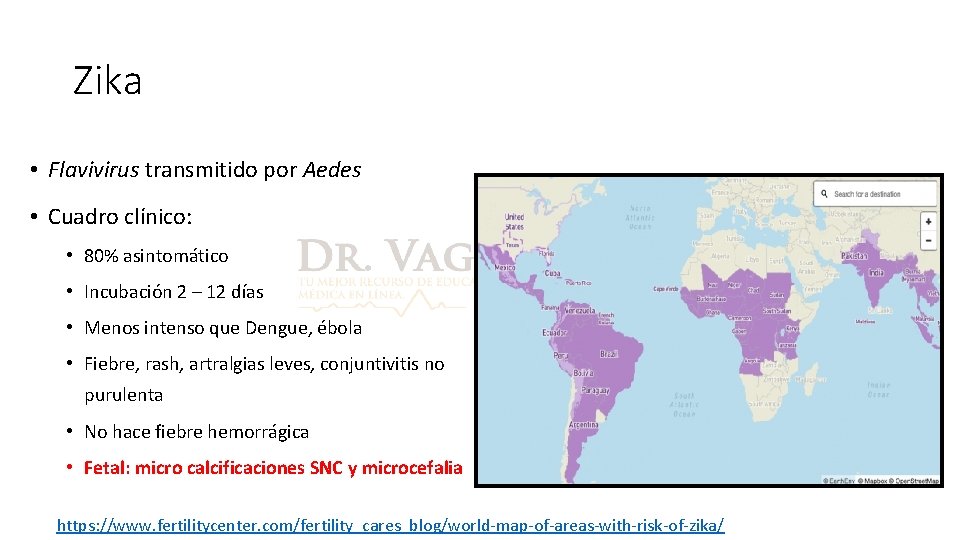
Zika • Flavivirus transmitido por Aedes • Cuadro clínico: • 80% asintomático • Incubación 2 – 12 días • Menos intenso que Dengue, ébola • Fiebre, rash, artralgias leves, conjuntivitis no purulenta • No hace fiebre hemorrágica • Fetal: micro calcificaciones SNC y microcefalia https: //www. fertilitycenter. com/fertility_cares_blog/world-map-of-areas-with-risk-of-zika/

Zika – clínica del viajero (CDC) • Mujeres: evitar embarazo durante el viaje y dos meses posteriores • Hombres: evitar impregnación durante viaje y seis meses posteriores

Influenza epidémica • Epidemio y patogénesis: • Altamente contagiosa, invierno en Norteamérica • Cuadro clínico • Fiebre y tos (en época invierno VPP 80%) • Tratamiento • Inmunoensayo: Sen 60%, Espec 98% • PCR (>90% sens y espec) • ¿A quién hacer estudio dx? • Inmunocompetente en riesgo de enfermedad grave • Inmunocomprometidos • Hospitalizados con enfermedad respiratoria febril

Influenza – tratamiento y prevención • Cuando tratar: • Hospitalizados • IVRI • Riesgo de enfermedad grave • • • Residentes de estancias de cuidados de salud permanentes ≥ 65 años Embarazo EPOC, ICC, ERC Cirrosis DM Drepanocitosis Inmunosuprimidos Dificultad con manejo secreciones Raza negra, pueblos originarios IMC ≥ 40 Rebatet, G. A. , Gabriela, L. J. , Mc. Phee, S. J. , Papadakis, M. A. , María, P. T. , & Rabow, M. W. (2017). Diagnóstico clínico y tratamiento 2017. México: Mc. Graw. Hill. Education. pp. 1287 - 1560

Influenza – tratamiento y prevención • ¿Cómo tratar? DENTRO DE PRIMERAS 48 HORAS • Inhibidor de neuraminidasa • Oseltamivir VO • Zanamivir inhalador • Vacuna contra influenza • >6 meses edad • Inactivada solamente • Vacuna dosis alta • ≥ 65 años • Estatinas Rebatet, G. A. , Gabriela, L. J. , Mc. Phee, S. J. , Papadakis, M. A. , María, P. T. , & Rabow, M. W. (2017). Diagnóstico clínico y tratamiento 2017. México: Mc. Graw. Hill. Education. pp. 1287 - 1560

VIH

VIH – tratamiento • ¿A quién tratar? TODOS • Pruebas de resistencia genotípica inicial: TODOS • ¿Qué iniciar? • 2 NRTIs* + inhibidor integrasa • Emtricitabina + tenofovir + inhibidor de integrasa (cualquiera) • Abacavir + lamivudina + dolutegravir (examen HLA B*5701) • 2 NRTIs + inhibidor de proteasa potenciado • Emtricitabina + tenofovir + darunavir/ritonavir *NRTIs: Inhibidores de la transcriptasa inversa análogos nucleósidos

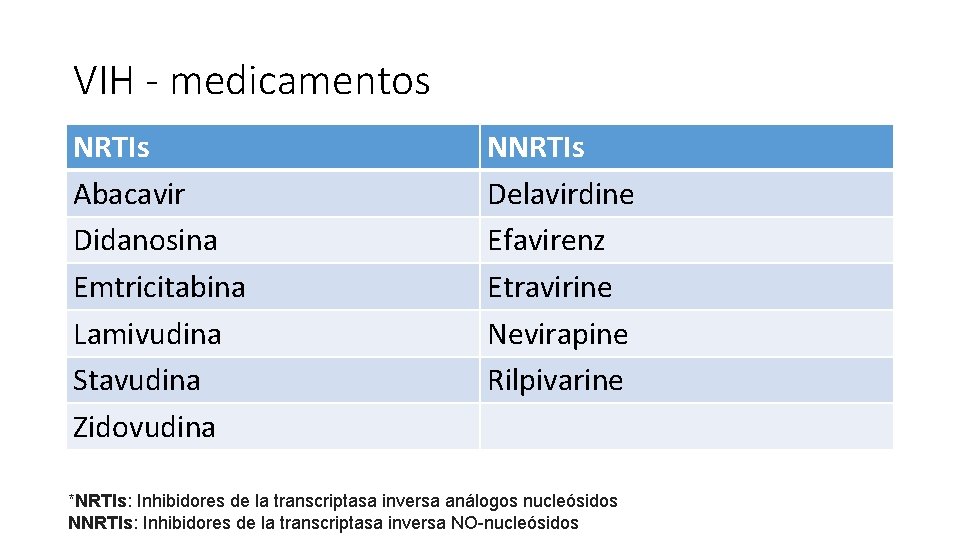
VIH - medicamentos NRTIs Abacavir Didanosina Emtricitabina Lamivudina Stavudina Zidovudina NNRTIs Delavirdine Efavirenz Etravirine Nevirapine Rilpivarine *NRTIs: Inhibidores de la transcriptasa inversa análogos nucleósidos NNRTIs: Inhibidores de la transcriptasa inversa NO-nucleósidos

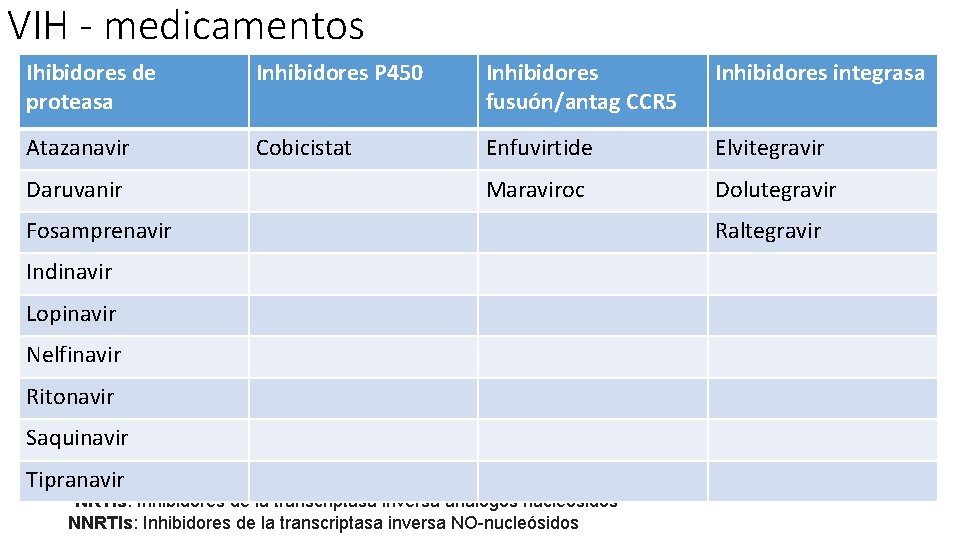
VIH - medicamentos Ihibidores de proteasa Inhibidores P 450 Inhibidores fusuón/antag CCR 5 Inhibidores integrasa Atazanavir Cobicistat Enfuvirtide Elvitegravir Maraviroc Dolutegravir Daruvanir Fosamprenavir Indinavir Lopinavir Nelfinavir Ritonavir Saquinavir Tipranavir *NRTIs: Inhibidores de la transcriptasa inversa análogos nucleósidos NNRTIs: Inhibidores de la transcriptasa inversa NO-nucleósidos Raltegravir

Combinaciones antiretrovirales dosis-fija • Abacavir – lamivudina – zidovudina • Efavirenz – tenofovir – emtricitabine • Elvitegravir – cobicistat – tenofovir – emtricitabine • Tenofovir – emtricitabine • Rilpivirine – emtricitabine – tenofovir • Zidovudina – lamivudina • Dolutegravir – abacavir - lamivudina

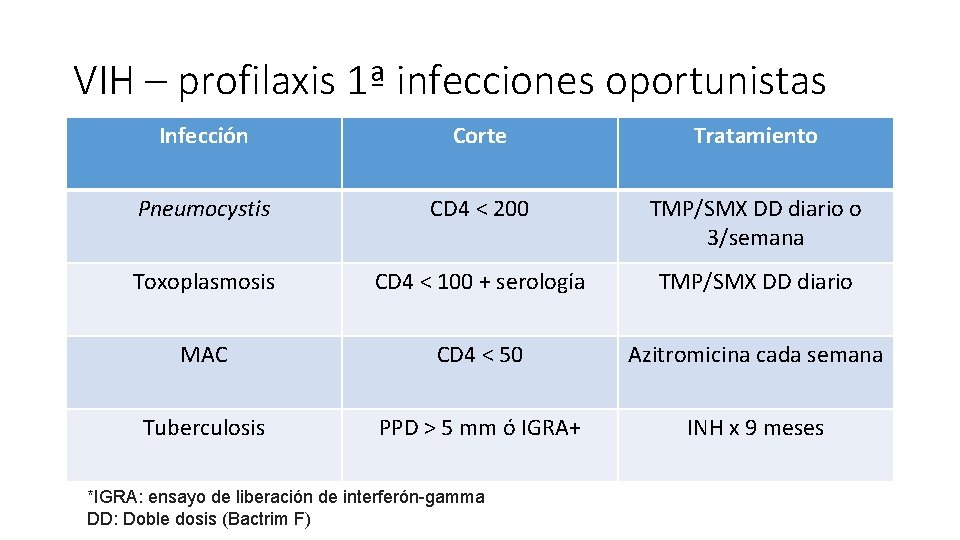
VIH – profilaxis 1ª infecciones oportunistas Infección Corte Tratamiento Pneumocystis CD 4 < 200 TMP/SMX DD diario o 3/semana Toxoplasmosis CD 4 < 100 + serología TMP/SMX DD diario MAC CD 4 < 50 Azitromicina cada semana Tuberculosis PPD > 5 mm ó IGRA+ INH x 9 meses *IGRA: ensayo de liberación de interferón-gamma DD: Doble dosis (Bactrim F)

VIH – profilaxis preexposición • Disminuye riesgo de transmisión • 45% hombres que tienen sexo con hombres • 62% heterosexuales alto riesgo (Botswana) • 67% en parejas heterosexuales discordantes • Consecuencia • FDA aprobó combinación tenofovir-emtricitabine, profilaxis preexposición en VIH(-) en adultos en RIESGO • Pareja infectada, ITS recién, múltiples parejas, no condón, trabajadores sexuales • ≤ 90 días de medicamento, verificar estado VIH antes de volver a surtir

VIH – profilaxis PREexposición • Disminuye riesgo de transmisión • 45% hombres que tienen sexo con hombres • 62% heterosexuales alto riesgo (Botswana) • 67% en parejas heterosexuales discordantes • Consecuencia • FDA aprobó combinación tenofovir-emtricitabine, profilaxis preexposición en VIH(-) en adultos en RIESGO • Pareja infectada, ITS recién, múltiples parejas, no condón, trabajadores sexuales, drogas IV y comparten agujas • ≤ 90 días de medicamento, verificar estado VIH antes de volver a surtir • Ofrecer consejería médica

VIH – profilaxis POSTexposición • Ofrecer, si ambas preguntas con afirmativas (<72 horas): 1. ¿Líquido sanguinolento? 2. ¿Se comprometió la integridad de la piel? • Otras exposiciones de importancia: secreciones semen, vagina/ano, leche materna • Exposiciones no significativas: orina, piel intacta • ¿Qué ofrecer? 1. Si fuente VIH+ conocido: basado en resistencia 2. Tres medicamentos por 4 semanas: emtricitabina + tenofovir + raltegravir • Examen VIH a 0, 6 y 16 semanas • Examen sífilis, gonorrea, Chalmydia, embarazo

Síndrome retroviral agudo