Indeks BATTERYE 1 Indeks Battery Ondersoek Ooreenkomste tussen

Indeks BATTERYE 1
Indeks Battery Ondersoek Ooreenkomste tussen Elektrolitiese en Galvaniese Sel Beskrywing en Illustrasie van Galvaniese Sel Wetenskaplike Verslag Galvaniese sel - Geskiedenis Galvaniese sel – Komponente en Reaksies Galvaniese sel - Werking Galvaniese sel – Reduksie Potensiaal Tabel Verskille tussen Elektrolitiese en Galvaniese Sel Litium-kadmium en Sink-koolstof Battery Indeks Gebruikte Battery Tipe Battery – Gelykstroom of Wisselstroom Battery – Mediese Toepassing 2

Indeks BATTERY ONDERSOEK: q Kies ten minste vier verskillende batterye by die plaaslike winkel. q Ontwerp 'n eenvoudige eksperiment wat jy kan uitvoer om vas te stel watter produk die meeste koste effektief is. q Ontwerp 'n geskrewe verslag wat ooreenstem met die vereistes van 'n goeie wetenskaplike verslag. 3

Indeks Battery A Battery B Battery C Battery D ü Skakel vier verskillende battery aan ’n vier identiese elektriese toestelle bv. ‘n flits. ü Skakel die toestel (flits) aan en neem die tyd wat die neem totdat elk van die flitse nie meer lig-energie uitstraal nie (nie meer brand nie). ü Voltooi die volgende tabel vir elk van die batterye. 4

Indeks Wetenskaplike Verslag: Ondersoekende vraag: Is battery wat die duurste is die mees koste effektief? Hipotese: Battery wat die duurste is, is die mees koste effektief. 5
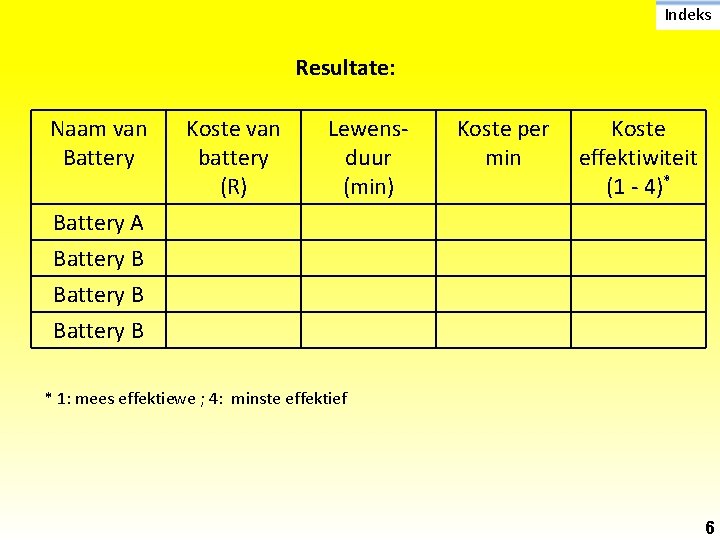
Indeks Resultate: Naam van Battery Koste van battery (R) Lewensduur (min) Koste per min Koste effektiwiteit (1 - 4)* Battery A Battery B * 1: mees effektiewe ; 4: minste effektief 6

Indeks Interpretasie en Bespreking van Resultate: Beskryf die resulate in terme van § Orde van koste effektiweit – watter een is meeste en minste effektief § - Verskillende vervaardigers gebruik verskillende materiale. - Al die chemiese reaksie nie dieselfde effektiwiteit nie. - Batterye se elektrisiteit geleidingsvermoë verskil. Chemiese stowwe in die battery nie van dieselfde kwalitiet nie. - Redes vir verskil in koste effektiwiteit Batterye nie goed metaal houer geseël nie. Verskillende konsentrasie van chemiese stowwe in die battery. 7

Indeks Gevolgtrekking: Antwoord die hipotese. Bv. Duurder batterye se koste effektiwiteit is meer (minder) as goedkoop battery. 8

Indeks GALVANIESE SEL GESKIEDENIS 9

Indeks q Luigi Galvani was die eerste persoon wat dit waargeneem het dat elektrisiteit opgewek kan word wanneer verskillende metale (elektrodes) kontak maak met ’n oplossing waardeur elektrisisteit gelei kan word. (Galvaniese sel) q Alessandro Volta het hierdie inligting gebruik en die eerste elektrochemiese sel ontwikkel wat bestaan het uit metaalelektrodes en oplossings waardeur elektrisiteit gelei kan word. Volta het ook die battery vervaardig wat bestaan het uit verskeie elektrochemiese selle wat aan mekaar geskakel is. (Volt – eenheid van potensiaalverskil) 10

Indeks GALVANIESE SEL KOMPONENTE EN CHEMIESE REAKSIES 11

Indeks § Galvaniese selle is ook bekend as Voltaise selle (Na aanleiding van die bydrae van Alessandro Volta tot die ontwikkeling vanb die galvaniese sel § ’n Galvaniese sel bestaan uit i. twee metaalgeleiers bekend as elektrodes. ii. soutoplossing waardeur elektrisiteit gelei kan word. iii. twee halfselle, elk met ’n elektrode en oplossing wat elektrisiteit kan gelei. § ’n Chemiese proses bekend as oksidasie vind plaas in die een halfsel en hierdie reaksie stel elektrone vry. § ’n Chemiese proses bekend as reduksie vind plaas in die een halfsel en hierdie reaksie neem elektrone op. § Die vloei van elektrone vanf die oksidasie reaksie na die reduksie reaksie vind plaas wanneer die twee halfselle (oksidasie en reduksie halfselle) met ’n eksterne elektriese geleier aan mekaar verbind word. 12

Indeks KATODE: ü Die elektrode (metaal) waar reduksie plaasvind is bekend as die katode. ü In galvaniese selle besit die katode altyd ’n positiewe elektriese lading. ANODE: ü Die elektrode (metaal) waar oksidasie plaasvind is bekend as die anode. ü In galvaniese selle besit die anode altyd ’n negatiewe elektriese lading. 13

Indeks RIGTING VAN ELEKTRON (ELEKTRIESE STROOM) VLOEI: Die elektrone wat tydens oksidasie by die anode vrygestel word beweeg deur die eksterne elektriese geleier na die katode waar die oksideermiddel ‘n chemise proses bekend as reduksie ondergaan deur die elektrone op te neem. 14

Indeks SPONTANITEIT: Die chemiese reaksies wat in ’n galvaniese sel plaasvind is bekend as altyde spontane chemiese reaksies en benodig geen eksterne energie om te plaas te vind nie. . VLOEI VAN IONE: Tydens die werking vandie galvaniese sel beweeg positiewe metaalione (katione) wat tydens oksidasie gevorm word vanaf die halfsel waar oksidasie plaasvind (ANODE) na die halfsel waar reduksie plaasvind (KATODE). Die beweging van die metaalione vind plaas deur ’n gedeelte van die galvaniese sel bekend as ’n soutbrug. 15

Indeks GALVANIESE SEL WERKING 16

Indeks Wanneer twee halfselle bestaande uit ’n metaal elektrode en soutoplossing wat elektrisiteit kan gelei aan mekaar verbind word sal ü die een halfsel elektrone verskaf. Die stof wat elektone verskaf ondergaan oksidasie en is die reduseermiddel. Die vermoë van die stof in hierdie halfsel om oksidasie te ondergaan is baie groter as die vermoë van die stof in die ander halfsel om oksidasie te ondergaan. ü die een halfsel elektrone opneem. Die stof wat elektone opneem ondergaan reduksie en is die oksideermiddel. Die vermoë van die stof in hierdie halfsel om reduksie te ondergaan is baie groter as die vermoë van die stof in die ander halfsel om reduksie te ondergaan. ü Die relatiewe vermoë van stowwe om reduksie te ondergaan word opgesom in die reduksie potensiaal tabel. 17

Indeks GALVANIESE SEL REDUKSIE POTENSIAAL TABEL 18

Indeks E 0 (VOLTS) HALF-REACTIONS Li+ + e - Li K+ + e - -3. 05 K -2. 92 Ba 2+ + 2 e- Ba -2. 90 Ca 2+ + 2 e- Ca -2. 76 Na+ + e- Na -2. 71 Mg 2+ + 2 e- Mg -2. 37 Al 3+ + 3 e- Al -1. 66 Mn 2+ + 2 e- -1. 18 Mn 2 H 2 O + 2 e- H 2(g) + 2 OH - Zn 2+ + 2 e- -0. 76 Zn Cr 2+ + 2 e- Cr -0. 74 Fe 2+ + 2 e- Fe -0. 44 Cr 3+ + e- Cr 2+ -0. 41 Cd 2+ + 2 e- Cd -0. 40 CO 2+ + 2 e- CO -0. 28 Ni 2+ + 2 e- -0. 25 Ni Sn 2+ + 2 e- -0. 14 Sn Pb 2+ + 2 e- -0. 13 Pb Fe 3+ + 3 e- -0. 04 Fe 2 H+ + 2 e- 0. 00 H 2(g) S + 2 H+ + 2 e. Sn 4+ + 2 e- Sn 2+ Cu 2+ + e- +0. 16 Cu+ SO 2(g) + 2 H 2 O Cu 2+ + 2 e- I 2 + 4 OH- +0. 40 S + 2 H 2 O +0. 45 - Cu 1+ + e 2 e- +0. 52 Cu 2 I- +0. 54 O 2(g) + 2 H + + 2 e- H 2 O 2 Fe 3+ + e- Fe 2+ Ag+ + e- NO 2(g) + H 2 O +0. 80 NO 3 - + 4 H+ + 3 e- NO(g) + 2 H 2 O Mn. O 2 + 4 H+ + 2 e- Mn 2+ + 2 H 2 O Cr 2 O 72 - + 14 H+ + 6 e- 2 Cr 3+ + 7 H 2 O Cl 2(g) + 2 e - F 2(g) + 2 e - Mn 2+ + 4 H 2 O Co 2+ 2 F- te ondergaan word bepaal deur die Volt-waarde van die reaksie. Indien twee reaksies met mekaar vergelyk word sal die reaksie met die hoogste Volt-waarde reduksie ondergaan en die ander reaksie sal oksidasie ondergaan. +0. 96 +1. 23 +1. 28 +1. 33 +1. 36 2 Cl- Mn. O 4 - + 8 H+ + 5 e- Die vermoë van die reaksie om reduksie +1. 06 2 Br- O 2(g) + 4 H + + 4 e- Co 3+ + e- +0. 78 Hg(l) Ag Br 2(l) + 2 e - +0. 68 +0. 77 NO 3 - + 2 H+ + e. Hg 2+ + 2 e- +0. 17 +0. 34 Cu SO 2 + 4 H+ + 4 e- tabel voorgestel. +0. 15 SO 42 - + 4 H+ + 2 e. O 2 + 2 H 2 O + 4 e +0. 14 H 2 S(g) ’n Aantal reduksie reaksies se potensiaal word op die -0. 83 +1. 51 +1. 82 +2. 87 19

Indeks VERSKILLE TUSSEN ELEKTROLITIESE EN GALVANIESE SELLE 20

Indeks GALVANIESE SEL ELEKTROLITIESE SEL q Chemiese energie word omgeskakel na elektriese energie. Ø Elektriese energie word omgeskakel na chemiese energie. q Redoksreaksie is spontaan – Geen elektriese sel in die stroombaan. Ø Redoksreaksie is nie-spontaan – Elektriese sel is deel van stroombaan. q Anode is negatief. q Katode is positief. q Twee verskillende elektrodes is in verskillende oplossings. q Soutbrug verbind die twee halfselle. Ø Katode is negatief. Ø Anode is positief. Ø Twee identiese elektrodes is in dieselfde oplossing. Ø Geen soutbrug is nodig nie. 21

Indeks OOREENKOMSTE TUSSEN ELEKTROLITIESE EN GALVANIESE SELLE 22

Indeks • Redoksreaksie vind in beide selle plaas • Oksidasie vind by anode plaas • Reduksie vind by katode plaas • Anione beweeg na anode • Katione beweeg na katode • In eksterne stroom vloei die elektrone vanaf die anode na katode. 23

Indeks BESKRYWING EN ILLUSTRASIE VAN GALVANIESE SEL 24

Indeks Ø ’n Galvaniese sel is ’n battery waar chemiese energie na elektriese energie omgeskakel word. Ø Twee chemiese prosesse vind plaas in ’n galvaniese sel: ü Oksidasie - vrystelling van elektrone deur ’n chemiese stof. ü Reduksie – opneem van elektrone deur ’n chemiese stof. 25
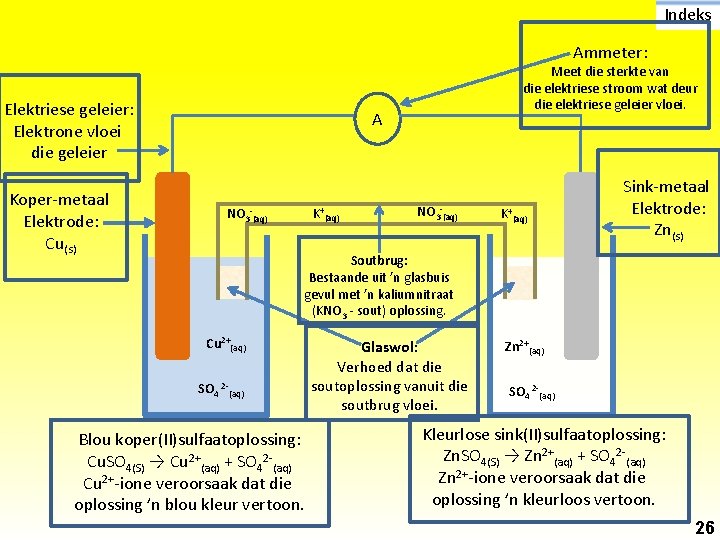
Indeks Ammeter: Elektriese geleier: Elektrone vloei die geleier Koper-metaal Elektrode: Cu(s) Meet die sterkte van die elektriese stroom wat deur die elektriese geleier vloei. A K+(aq) NO 3 -(aq) K+(aq) Sink-metaal Elektrode: Zn(s) Soutbrug: Bestaande uit ’n glasbuis gevul met ’n kaliumnitraat (KNO 3 - sout) oplossing. Cu 2+(aq) SO 4 2 -(aq) Blou koper(II)sulfaatoplossing: Cu. SO 4(S) → Cu 2+(aq) + SO 42 -(aq) Cu 2+-ione veroorsaak dat die oplossing ’n blou kleur vertoon. Glaswol: Verhoed dat die soutoplossing vanuit die soutbrug vloei. Zn 2+(aq) SO 4 2 -(aq) Kleurlose sink(II)sulfaatoplossing: Zn. SO 4(S) → Zn 2+(aq) + SO 42 -(aq) Zn 2+-ione veroorsaak dat die oplossing ’n kleurloos vertoon. 26
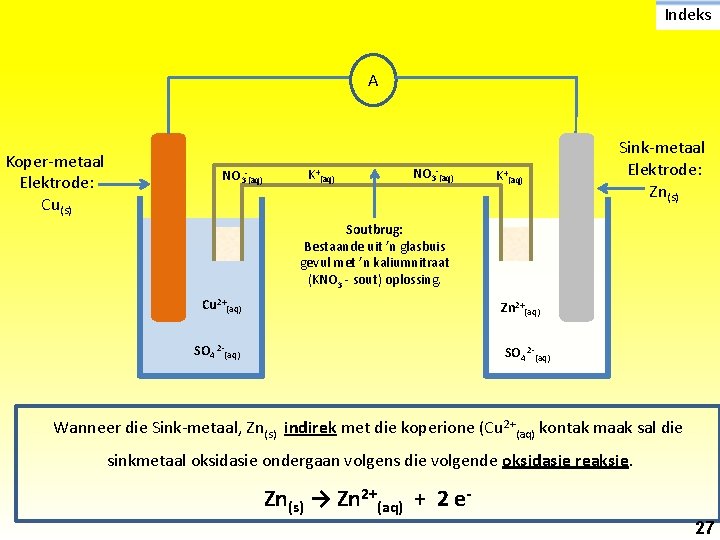
Indeks A Koper-metaal Elektrode: Cu(s) NO 3 -(aq) K+(aq) Sink-metaal Elektrode: Zn(s) Soutbrug: Bestaande uit ’n glasbuis gevul met ’n kaliumnitraat (KNO 3 - sout) oplossing. Cu 2+(aq) Zn 2+(aq) SO 4 2 -(aq) Wanneer die Sink-metaal, Zn(s) indirek met die koperione (Cu 2+(aq) kontak maak sal die sinkmetaal oksidasie ondergaan volgens die volgende oksidasie reaksie. Zn(s) → Zn 2+(aq) + 2 e 27
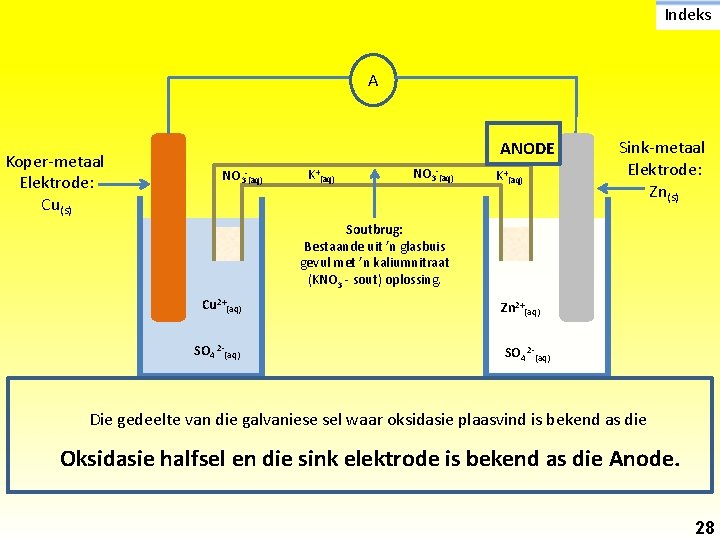
Indeks A Koper-metaal Elektrode: Cu(s) ANODE NO 3 -(aq) K+(aq) Sink-metaal Elektrode: Zn(s) Soutbrug: Bestaande uit ’n glasbuis gevul met ’n kaliumnitraat (KNO 3 - sout) oplossing. Cu 2+(aq) SO 4 2 -(aq) Zn 2+(aq) SO 4 2 -(aq) Die gedeelte van die galvaniese sel waar oksidasie plaasvind is bekend as die Oksidasie halfsel en die sink elektrode is bekend as die Anode. 28
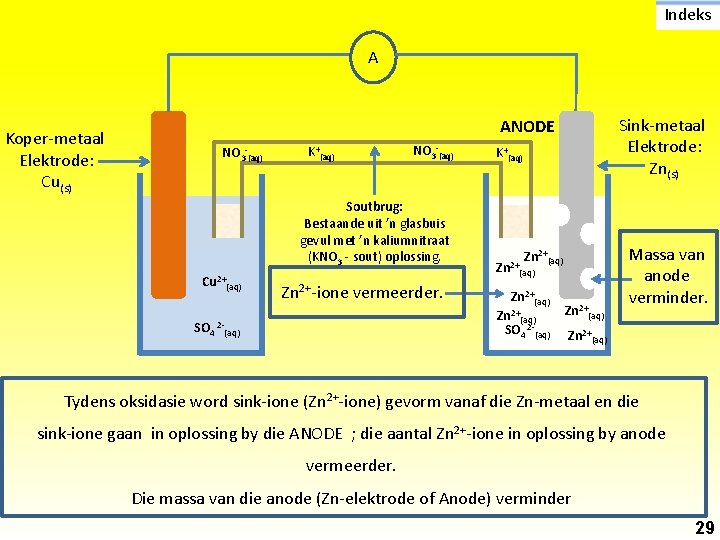
Indeks A Koper-metaal Elektrode: Cu(s) Sink-metaal Elektrode: Zn(s) ANODE NO 3 -(aq) K+(aq) NO 3 -(aq) Soutbrug: Bestaande uit ’n glasbuis gevul met ’n kaliumnitraat (KNO 3 - sout) oplossing. Cu 2+(aq) Zn 2+-ione vermeerder. SO 4 2 -(aq) K+(aq) Zn 2+(aq) SO 4 2 -(aq) Zn 2+(aq) Massa van anode verminder. Zn 2+(aq) Tydens oksidasie word sink-ione (Zn 2+-ione) gevorm vanaf die Zn-metaal en die sink-ione gaan in oplossing by die ANODE ; die aantal Zn 2+-ione in oplossing by anode vermeerder. Die massa van die anode (Zn-elektrode of Anode) verminder 29
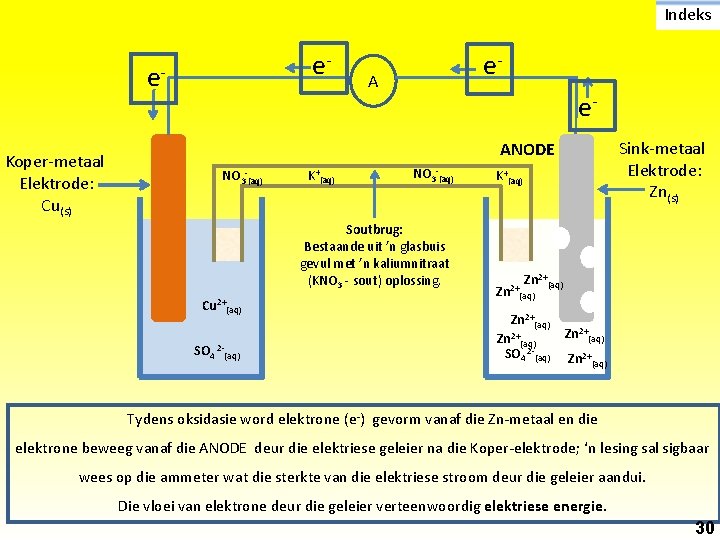
Indeks e- e. Koper-metaal Elektrode: Cu(s) e- A e. Sink-metaal Elektrode: Zn(s) ANODE NO 3 -(aq) K+(aq) NO 3 -(aq) Soutbrug: Bestaande uit ’n glasbuis gevul met ’n kaliumnitraat (KNO 3 - sout) oplossing. Cu 2+(aq) SO 4 2 -(aq) K+(aq) Zn 2+(aq) SO 4 2 -(aq) Zn 2+(aq) Tydens oksidasie word elektrone (e-) gevorm vanaf die Zn-metaal en die elektrone beweeg vanaf die ANODE deur die elektriese geleier na die Koper-elektrode; ‘n lesing sal sigbaar wees op die ammeter wat die sterkte van die elektriese stroom deur die geleier aandui. Die vloei van elektrone deur die geleier verteenwoordig elektriese energie. 30
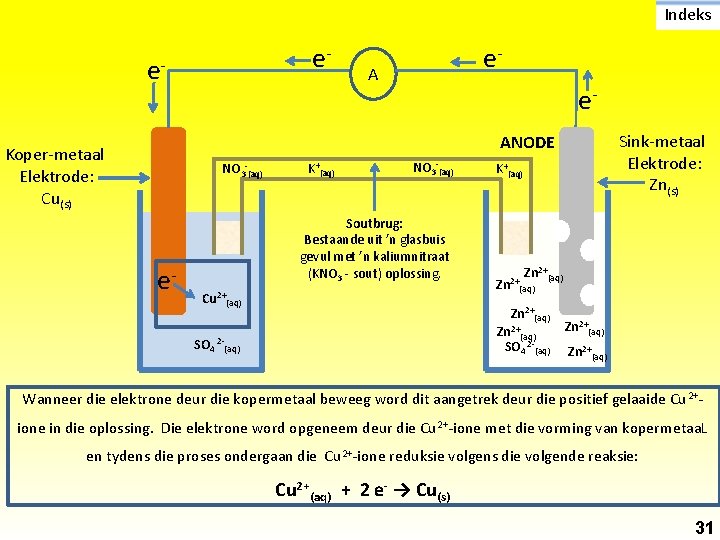
Indeks e- e- e- A e. Sink-metaal Elektrode: Zn(s) ANODE Koper-metaal Elektrode: Cu(s) NO 3 -(aq) e- K+(aq) NO 3 -(aq) Soutbrug: Bestaande uit ’n glasbuis gevul met ’n kaliumnitraat (KNO 3 - sout) oplossing. Cu 2+(aq) K+(aq) Zn 2+(aq) SO 4 2 -(aq) Zn 2+(aq) Wanneer die elektrone deur die kopermetaal beweeg word dit aangetrek deur die positief gelaaide Cu 2+ione in die oplossing. Die elektrone word opgeneem deur die Cu 2+-ione met die vorming van kopermetaa. L en tydens die proses ondergaan die Cu 2+-ione reduksie volgens die volgende reaksie: Cu 2+(aq) + 2 e- → Cu(s) 31
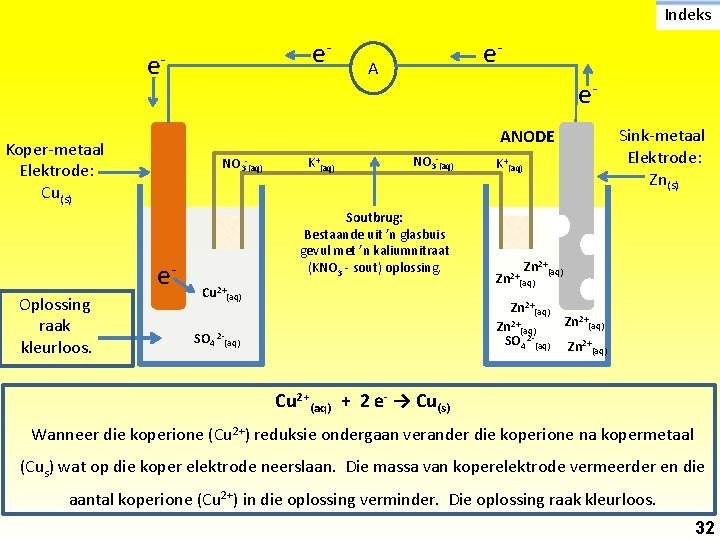
Indeks e- e- A e. Sink-metaal Elektrode: Zn(s) ANODE Koper-metaal Elektrode: Cu(s) NO 3 -(aq) e. Oplossing raak kleurloos. e- K+(aq) NO 3 -(aq) Soutbrug: Bestaande uit ’n glasbuis gevul met ’n kaliumnitraat (KNO 3 - sout) oplossing. Cu 2+(aq) K+(aq) Zn 2+(aq) SO 4 2 -(aq) Zn 2+(aq) Cu 2+(aq) + 2 e- → Cu(s) Wanneer die koperione (Cu 2+) reduksie ondergaan verander die koperione na kopermetaal (Cus) wat op die koper elektrode neerslaan. Die massa van koperelektrode vermeerder en die aantal koperione (Cu 2+) in die oplossing verminder. Die oplossing raak kleurloos. 32
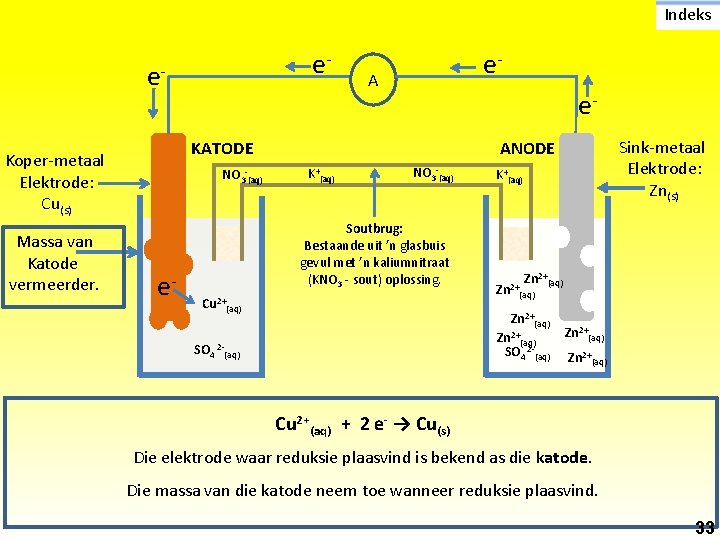
Indeks e- e- A e- KATODE Koper-metaal Elektrode: Cu(s) Massa van Katode vermeerder. e- NO 3 -(aq) e- Sink-metaal Elektrode: Zn(s) ANODE K+(aq) NO 3 -(aq) Soutbrug: Bestaande uit ’n glasbuis gevul met ’n kaliumnitraat (KNO 3 - sout) oplossing. Cu 2+(aq) K+(aq) Zn 2+(aq) SO 4 2 -(aq) Zn 2+(aq) Cu 2+(aq) + 2 e- → Cu(s) Die elektrode waar reduksie plaasvind is bekend as die katode. Die massa van die katode neem toe wanneer reduksie plaasvind. 33
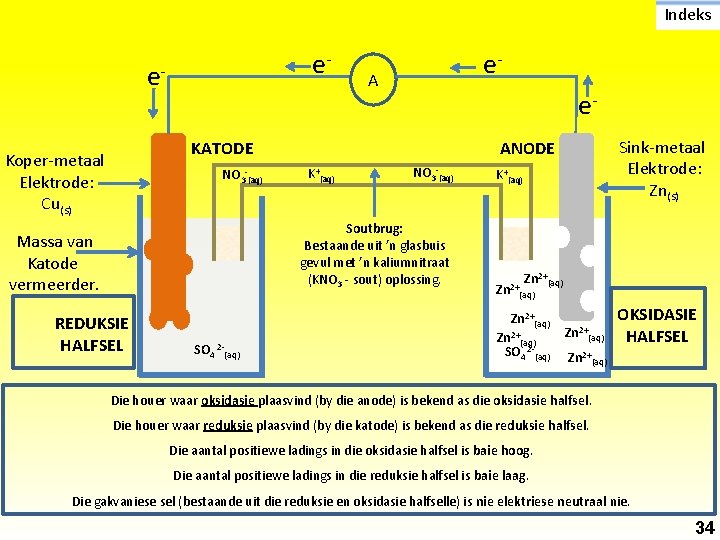
Indeks e- e- e- A e- KATODE Koper-metaal Elektrode: Cu(s) NO 3 -(aq) K+(aq) NO 3 -(aq) Soutbrug: Bestaande uit ’n glasbuis gevul met ’n kaliumnitraat (KNO 3 - sout) oplossing. Massa van Katode vermeerder. REDUKSIE HALFSEL SO 4 2 -(aq) Sink-metaal Elektrode: Zn(s) ANODE K+(aq) Zn 2+(aq) SO 4 2 -(aq) Zn 2+(aq) OKSIDASIE HALFSEL Zn 2+(aq) Die houer waar oksidasie plaasvind (by die anode) is bekend as die oksidasie halfsel. Die houer waar reduksie plaasvind (by die katode) is bekend as die reduksie halfsel. Die aantal positiewe ladings in die oksidasie halfsel is baie hoog. Die aantal positiewe ladings in die reduksie halfsel is baie laag. Die gakvaniese sel (bestaande uit die reduksie en oksidasie halfselle) is nie elektriese neutraal nie. 34
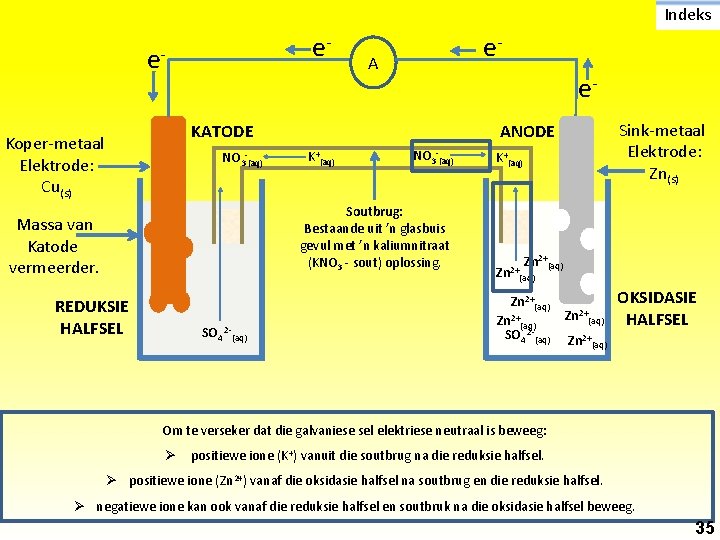
Indeks e- e- e- A e- KATODE Koper-metaal Elektrode: Cu(s) NO 3 -(aq) K+(aq) NO 3 -(aq) Soutbrug: Bestaande uit ’n glasbuis gevul met ’n kaliumnitraat (KNO 3 - sout) oplossing. Massa van Katode vermeerder. REDUKSIE HALFSEL SO 4 2 -(aq) Sink-metaal Elektrode: Zn(s) ANODE K+(aq) Zn 2+(aq) SO 4 2 -(aq) Zn 2+(aq) OKSIDASIE HALFSEL Zn 2+(aq) Om te verseker dat die galvaniese sel elektriese neutraal is beweeg: Ø positiewe ione (K+) vanuit die soutbrug na die reduksie halfsel. Ø positiewe ione (Zn 2+) vanaf die oksidasie halfsel na soutbrug en die reduksie halfsel. Ø negatiewe ione kan ook vanaf die reduksie halfsel en soutbruk na die oksidasie halfsel beweeg. 35
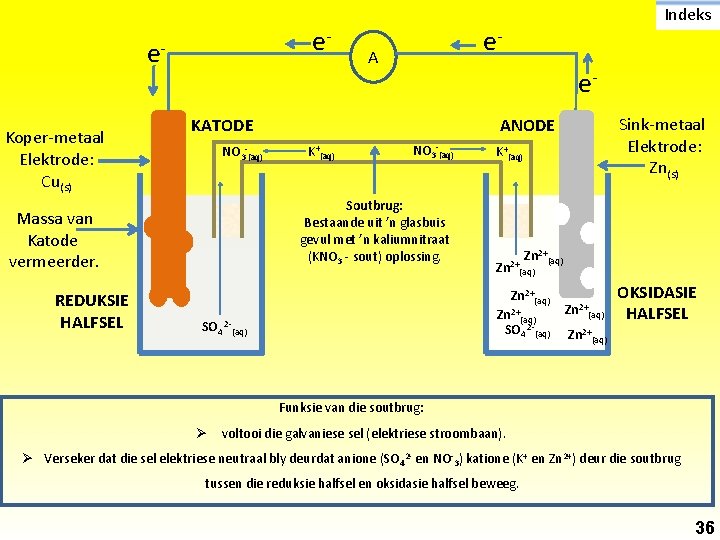
e- e. Koper-metaal Elektrode: Cu(s) A e. Sink-metaal Elektrode: Zn(s) ANODE K+(aq) NO 3 -(aq) Soutbrug: Bestaande uit ’n glasbuis gevul met ’n kaliumnitraat (KNO 3 - sout) oplossing. Massa van Katode vermeerder. REDUKSIE HALFSEL e- KATODE NO 3 -(aq) Indeks K+(aq) Zn 2+(aq) SO 4 2 -(aq) Zn 2+(aq) OKSIDASIE HALFSEL Zn 2+(aq) Funksie van die soutbrug: Ø voltooi die galvaniese sel (elektriese stroombaan). Ø Verseker dat die sel elektriese neutraal bly deurdat anione (SO 42 - en NO-3) katione (K+ en Zn 2+) deur die soutbrug tussen die reduksie halfsel en oksidasie halfsel beweeg. 36
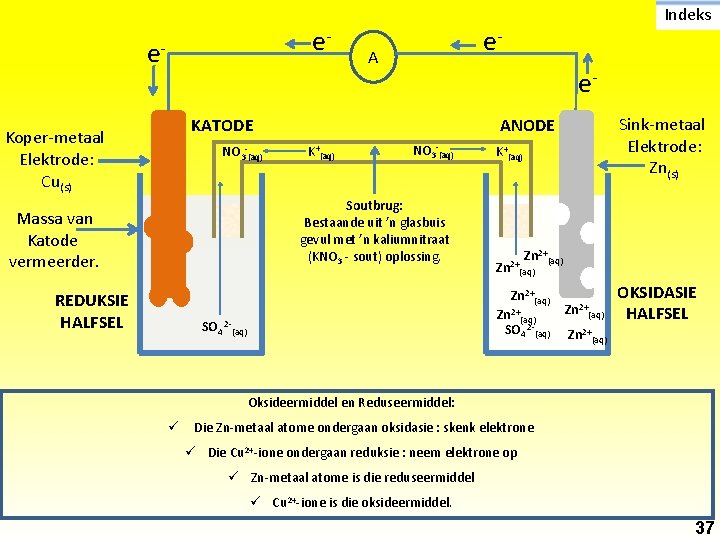
e- e. Koper-metaal Elektrode: Cu(s) A e. Sink-metaal Elektrode: Zn(s) ANODE K+(aq) NO 3 -(aq) Soutbrug: Bestaande uit ’n glasbuis gevul met ’n kaliumnitraat (KNO 3 - sout) oplossing. Massa van Katode vermeerder. REDUKSIE HALFSEL e- KATODE NO 3 -(aq) Indeks K+(aq) Zn 2+(aq) SO 4 2 -(aq) Zn 2+(aq) OKSIDASIE HALFSEL Zn 2+(aq) Oksideermiddel en Reduseermiddel: ü Die Zn-metaal atome ondergaan oksidasie : skenk elektrone ü Die Cu 2+-ione ondergaan reduksie : neem elektrone op ü Zn-metaal atome is die reduseermiddel ü Cu 2+-ione is die oksideermiddel. 37
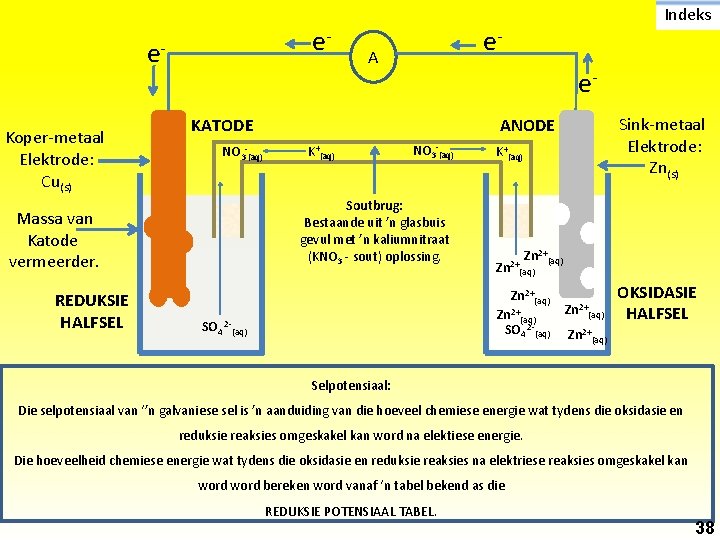
e- e. Koper-metaal Elektrode: Cu(s) A e. Sink-metaal Elektrode: Zn(s) ANODE K+(aq) NO 3 -(aq) Soutbrug: Bestaande uit ’n glasbuis gevul met ’n kaliumnitraat (KNO 3 - sout) oplossing. Massa van Katode vermeerder. REDUKSIE HALFSEL e- KATODE NO 3 -(aq) Indeks K+(aq) Zn 2+(aq) SO 4 2 -(aq) Zn 2+(aq) OKSIDASIE HALFSEL Zn 2+(aq) Selpotensiaal: Die selpotensiaal van ‘’n galvaniese sel is ’n aanduiding van die hoeveel chemiese energie wat tydens die oksidasie en reduksie reaksies omgeskakel kan word na elektiese energie. Die hoeveelheid chemiese energie wat tydens die oksidasie en reduksie reaksies na elektriese reaksies omgeskakel kan word bereken word vanaf ‘n tabel bekend as die REDUKSIE POTENSIAAL TABEL. 38

Indeks REDUKSIE POTENSIAAL TABEL: E 0 (VOLTS) HALF-REACTIONS Li+ + e - Li K+ + e - -3. 05 K -2. 92 Ba 2+ + 2 e- Oksidasie Halfreaksie: Zn(s) → Zn 2+ (aq) + 2 e- E 0 = - 0, 76 V Ba Ca -2. 76 Na+ + e- Na -2. 71 Mg 2+ + 2 e- Mg -2. 37 Al 3+ + 3 e- Al -1. 66 Mn 2+ + 2 e 2 H 2 O + 2 e- H 2(g) + 2 OH - Zn 2+ + 2 e. Cr 2+ + 2 e- Cr -0. 74 Fe 2+ + 2 e- Fe -0. 44 Cr 3+ + e- Cr 2+ -0. 41 Cd 2+ + 2 e- Cd -0. 40 CO 2+ + 2 e- CO -0. 28 + 2 → Cu(s) -0. 13 Pb -0. 04 Fe 2 H+ + 2 e- (aq) -0. 14 Sn Fe 3+ + 3 e- e- -0. 25 Ni Pb 2+ + 2 e- Cu 2+ 0. 00 H 2(g) S + 2 H+ + 2 e- Sn 2+ Cu 2+ + e- +0. 15 +0. 16 Cu+ SO 42 - + 4 H+ + 2 e- SO 2(g) + 2 H 2 O Cu 2+ + 2 e. O 2 + 2 H 2 O + 4 e 4 OH- +0. 40 S + 2 H 2 O +0. 45 - Cu 1+ + e- Cu I 2 + 2 e- 2 I- +0. 52 +0. 54 O 2(g) + 2 H + + 2 e- H 2 O 2 Fe 3+ + e- Fe 2+ Ag+ + e- NO 2(g) + H 2 O Ag +0. 80 NO 3 - + 4 H+ + 3 e- NO(g) + 2 H 2 O Mn. O 2 + 4 H+ + 2 e- Mn 2+ + 2 H 2 O Cr 2 O 72 - + 14 H+ + 6 e- 2 Cr 3+ + 7 H 2 O Cl 2(g) + 2 e - Mn 2+ + 4 H 2 O Co 2+ 2 F- +1. 23 +1. 28 +1. 33 +1. 36 2 Cl- Mn. O 4 - + 8 H+ + 5 e- +0. 96 +1. 06 2 Br- O 2(g) + 4 H + + 4 e- F 2(g) + 2 e - +0. 78 Hg(l) Br 2(l) + 2 e - +0. 68 +0. 77 NO 3 - + 2 H+ + e. Hg 2+ + 2 e- +0. 17 +0. 34 Cu SO 2 + 4 H+ + 4 e- Co 3+ + e- +0. 14 H 2 S(g) Sn 4+ + 2 e- Berekening van die sel potensiaal (E 0): E 0 = E 0(oksidasie halfreaksie) - E 0(reduksie halfreaksie) = (+ 0, 34 V) – (-0, 76 V) = + 0, 34 V + 0, 76 V = + 1, 10 V Die positiewe waarde dui aan dat die oksidasie en Reduksie reaksies spontaan sal plaasvind. Die waarde van 1, 10 V dui aan dat die sel 1, 1 Joule energie Vir 1 Coulomb elektriese lading (elektrone) verskaf wanneer dit vanaf die anode deur die elektriese geleier na die katode sal vloei. Indien die ammeter met ’n gloeilamp vrvang word sal die lampie brand. -0. 83 -0. 76 Zn Sn 2+ + 2 e- E 0 = + 0, 34 V -1. 18 Mn Ni 2+ + 2 e- Oksidasie Halfreaksie: -2. 90 Ca 2+ + 2 e- +1. 51 +1. 82 +2. 87 39

Indeks Faktore wat die grootte van die selpotensiaal bepaal. Drie faktore beinvloed die selpotensiaal of optimale werking van ’n galvaniese sel: * Tipe verbinding wat gebruik word om die galvaniese sel saam te stel. * Konsentrasie van die elektroliete in elk van die halfselle. * Temperatuur van die galvaniese sel. Standaard toestande vir ’n galvaniese sel is: Temperatuur: Konsentrasie van Elektroliet: 298 K 1, 0 mol·dm-3 SELNOTASIE: Oksidasie halfsel // Reduksie halfsel Zn(s) / Zn 2+(aq) (1 mol·dm-3) // Cu 2+(aq) (1 mol·dm-3) / Cu(s) 40

Indeks LITIUM-KADMIUMBATTERY SINK-KOOLSTOFBATTERY. 41

Indeks Litium-kadmiumbatterye is duurder as sink-koolstofbattery omdat, Ø Litium en kadmium baie duur chemiese stowwe is. Ø Litium en kadmium baie suiwer is om te verhoed dat dit oorverhit of elektriese lading verloor wanneer deel is van batterye. Ø Langer en vinniger werk as ander tipe batterye. 42

Indeks GEBRUIKTE BATTERYE 43

Indeks Batterye bevat een of meer van die volgende metale: kadmium, lood, sink, mangaan, nikkel, silwer, kwik en litium. Wanneer gebruikte battery weg gegooi word kan giftige stowwe vanuit die batterye vrygestel word wat ’n negatiewe invloed op grondwater en die gesondheid van mense het. Tydens verbranding kan Kwik en Kadmium as gasse vrygestel word en die lug besoedel. Hierdie twee metale is baie giftig. Die volgende probeleme kan veroorsaak word deur batterye wat klaar gebruik is (“pap batterye”): • Indien batterye verbrand word kan die oorblyfsels, riviere en waterbronne besoedel. • Vrystelling van swaar metale (lood en kwik) wat gevaarlik is. • Omgewing kan blootgestel word aan lood en suur. • Stel chemiese stowwe vry wat oë en vel kan irriteer. 44

Indeks Die chemiese stowwe (metale) wat in batterye voorkom kan herwin word vir hergebruik. Herwinning van die metale verminder die ontginning van natuurlike bronne. Dit is ook belangrik dat metale afkomstig van batterye nie in waterbronne beland en besoedeling veroorsaak nie. 45

Indeks TIPE BATTERYE 46

Indeks Primêre batterye: q Kan nie herlaai word nie q Sink-koolstof batterye, alkaliese batterye en litium batterye. q Sink-koolstof battery word vir algemene doeleindes gebruik en ontlaai vinnig. q Sink-chloried batterye se lewensduur is langer en verskaf meer energie as sinkkoolstof batterye. q Alkaliese batterye se lewensduur is tien keer langer as sink batterye maar die koste is 3 – 5 maal meer as sink batterye. q Batterye vir die gebruik in gehoortoestelle, kameras, horlosies, sakrekenaar - baie klein met ronde voorkoms. q Litium batterye se lewensduur is twee keer die van alkaliese batterye en is baie duur. 47

Indeks Sekondêre batterye: Ø Kan herlaai word Ø Mees algemene batterye is nikkel-cadmium (Ni-Cd), geseëlde lood-suur(Pb), nikkel-metaal hidried (Ni- MH), en litium ioon (Li- Ioon). Ø Nikkel-Kadmium is die mees algemene herlaaibare battery. Een van hierdie batterye kan 150 alkaliese batterye vervang. Ø Geseëlde lood-suur battery word gebruik in kameras en sellulêre telefone. Ø Nikkel Metaal Hidried batterye word gebruik in rekenaars, cellulêre telefone. Hierdie batterye besit lae energie vrystelling en hoë energie kapasiteit. Ø Lithium Ioon batterye so koste is hoog maar is baie lig in massa en hoog in energie digtheid. Word gebruik in sellulêre telefoen en skootrekenaars. 48

Indeks BATTERY GELYKSTROOM OF WISSELSTROOM. 49

Indeks Batterye lewer gelykstroom omdat, q Die batterye se pole nie voordurend verander nie. q Energie word verskaf deur ’n voorwaartse chemiese reaksie. q Geen motor roteer deur ’n magneetveld nie. 50

Indeks MEDIESE TOEPASSING VAN BATTERYE HARTPASAANGEêRS EN GEHOORAPPERATE. 51

Indeks ü Ongeveer 600, 000 hartpasaangeërs word jaarliks ingeplant en die apperaat lewer ’n elektriese puls wat veroorsaak dat die hart teen die regte spoed klop. ü Herlaaibare batterye (nikkel-kadmium batterye) was die eerste tipe battery wat gebruik is in pasaangeërs. ü Biologiese batterye waar energie van die menslike liggaam gebruik is, is ook gebruik sonder enige sukses. ü Kernkrag batterye is ook gebruik maar weens die gevaar daarvan word dit nie meer gebruik nie. 52

Indeks Litium-jodium batterye word huidiglik in hartpasaangeërs gebruik omdat die batterye, Ø ’n goeie energiebron is. Ø se tempo van energie vrystelling laag is. Ø se leeftyd baie lank is. Ø se massa baie min is, 12 tot 15 g. Ø in verskillende vorms beskikbaar is. 53

Indeks In gehoorapperate word sink-lug batterye gebruik wat nie herlaaibaar is nie en na gebruik word dit weggegooi. 54

Indeks einde 55
- Slides: 55