In una reazione chimica come faccio a contare




























- Slides: 30

In una reazione chimica come faccio a contare gli atomi che reagiscono? C + O 2 CO 2 Non li posso contare e quindi posso ricorrrere a misurare la loro massa. Ciò vuol dire che occorre trovare una correlazione tra massa misurata di un elemento o composto ed un certo numero di particelle noto. Questo mi permette anche di avere masse misurabili su una bilancia.

La mole Le grandezze fondamentali e le unita' di misura nel Sistema Internazionale (SI) Grandezza fondamentale lunghezza Unita’ Simbolo metro m massa kilogrammo Kg tempo secondo s corrente elettrica ampere A temperatura kelvin K intensita’ luminosa candela cd quantita’ di sostanza mole mol

La mole descrive una quantità di sostanza correlandola ad un numero di particelle La mole è la quantità di sostanza che contiene un numero N di particelle quanti atomi sono contenuti in esattamente 12 g di 12 C. Il numero di particelle contenute in una mole si chiama numero o costante di Avogadro (NAo N)

La mole N = 6, 0221367(36) × 1023 Poiché N è un numero per mole, esso ha unità di misura mol-1 ed è chiamata costante di Avogadro. NA = 6, 0221367(36) × 1023 mol-1

La mole Una mole di 23 Na è la quantità di sostanza che contiene NA atomi di 23 Na

Esempi Una mole di CO 2 contiene NA molecole di CO 2 Una mole di Na. Cl contiene NA ioni Na+ e NA ioni di Cl. Una mole di Na 2 SO 4 contiene 2 NA ioni Na+ ed NA ioni di SO 42 - Una mole di Si. O 2 contiene NA atomi di Si ed 2 NA atomi di O


Massa Molare: massa in grammi di una mole di materia di una qualsiasi sostanza elementare o composta • la massa molare (M) di una qualsiasi sostanza elementare o composta è la quantità di materia in grammi che contiene un numero di atomi pari a quelli contenuti in 12 grammi di 12 C. Questo numero di atomi è un numero naturale, intero, chiamato numero di Avogadro (NA), e vale circa 6, 022 x 1023. La massa in g di una mole di 12 C è per definizione della mole uguale a 12 g.

Mole e massa molare Una mole di sostanze diverse ha massa diversa !

Mole e massa molare Moli di sostanze diverse hanno massa diversa ! NA= 6, 0221367(36) × 1023 =12 C Massa di una mole =12 g NA= 6, 0221367(36) × 1023 =16 O Massa di una mole =15, 9949 g In una reazione o in una formula chimica contano le moli, non i grammi! C + O 2 CO 2 12 g di C = 1 mole di C 12 g di O 2 è meno di una mole di O 2

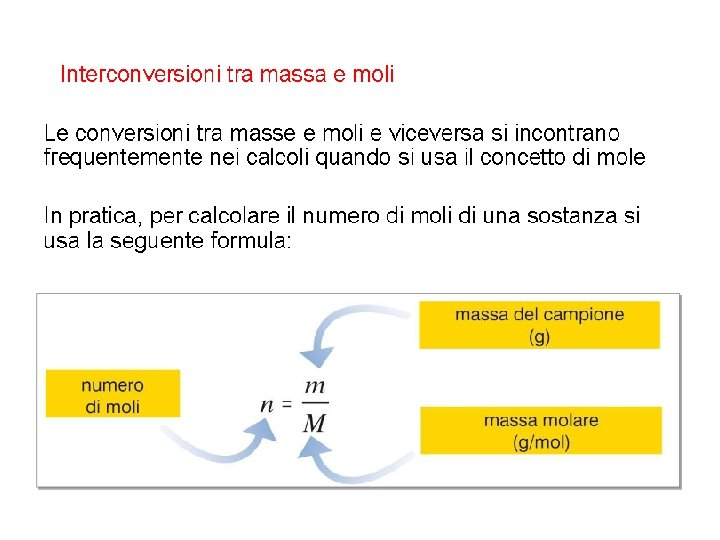
Massa molare = massa di una mole di atomi Rapporto fra massa (in grammi) e quantità di sostanza (in moli), quindi ha come unità di misura g mol-1.

Definendo la mole come la quantità di sostanza che contiene un numero di unità elementari uguale al numero di atomi contenuti in 12 g di 12 C, risulta che la massa molare ha lo stesso valore numerico del peso atomico di un singolo atomo di 12 C, esattamente 12 u. m. a. o Da Il risultato è che per tutti gli elementi il valore numerico della massa in grammi di una mole di atomi (massa molare) e il peso atomico espresso in unità di massa atomica (o Da) sono UGUALI!!!


uma


PA

Reazioni chimiche e mole In una reazione o in una formula chimica contano le moli, non i grammi! Es: C + O 2 CO 2 12 g di C reagiscono con 32 g di O 2 per dare 44 g di CO 2 Ma che corrispondono 1 mole di C, 1 mole di O 2 e una mole di CO 2 quindi allo stesso numero di particelle.

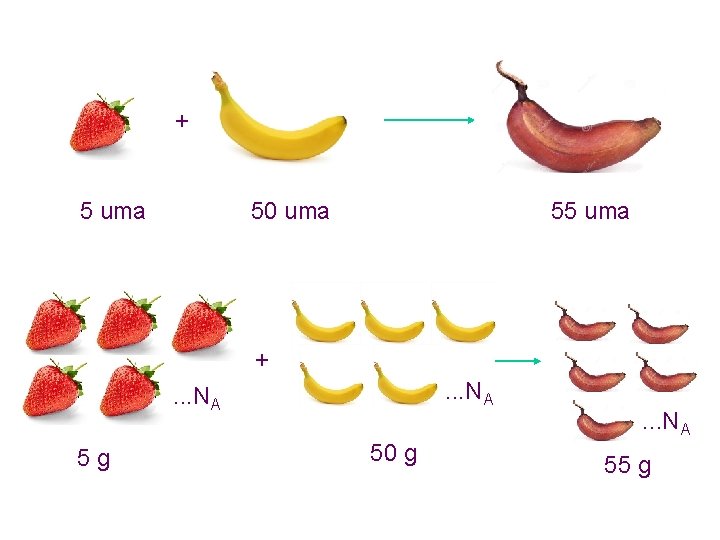
+ 5 uma 50 uma 55 uma +. . . NA 5 g 50 g . . . NA 55 g


Stechiometria: quella parte della chimica che riguarda le quantità delle specie che partecipano a reazioni n. moli= grammi/ massa molare mol =g/g*mol-1 grammi di sostanza= massa molare x n. moli Massa molare= grammi/ n. moli Per i gas: volume molare= volume/ n. moli= volume/ volume molare g=g*mol-1*mol g *mol-1 =g/mol mol =dm 3/dm 3 mol-1


Esercizi Ho un campione di zolfo che pesa 4. 07 g. (a) Quante moli di zolfo sono presenti? (b) Qual è il numero totale di atomi di zolfo nel campione? (a) n. moli= grammi/ massa molare mol =g/g*mol-1 n. moli= 4. 07 g/ 32. 07 g mol-1 = 0. 127 mol (b) n. atomi= moli x NA atomi =mol x mol-1 n. atomi= 0. 127 mol x 6. 022 x 1023 mol-1 = 7. 64 x 1022 atomi

Esercizi Ho questo composto C 2 HBr. Cl. F 3. (a) Quanti atomi di C sono presenti per mole del composto? 1 mole di C 2 HBr. Cl. F 3 contiene 2 moli C Quindi: n. atomi di C = 1 mol x 2 x 6. 022 x 1023 mol-1 = 1. 202 x 1024

Esercizi Determinare le moli di Cu. SO 4 5 H 2 O che sono contenute in 15 g? n. moli= grammi del composto/ massa molare del composto = massa atomica di Cu (63, 55) + massa atomica di S (32, 07) + 4 x massa atomica di O (15, 9994) + 10 x massa atomica di H (1, 008) + 5 x massa atomica di O (15, 9994) = 249, 7 g mol-1 n. moli= 15 g/ 249, 7 g mol-1 = 6, 008 x 10 -2 mol

Esercizi Calcolare quanti grammi dell’elemento idrogeno e dell’elemento ossigeno sono contenuti in 1, 00 g di H 2 O? n. moli= grammi del composto/ massa molare del composto = massa atomica di O (15, 9994) + 2 x massa atomica di H (1, 008) = 18, 02 g mol-1 n. moli di H 2 O= 1 g/ 18, 02 g mol-1 = 0, 0555 mol n. moli di ossigeno = n. moli di H 2 O n. moli di idrogeno = 2 x n. moli di H 2 O grammi di sostanza= massa molare x n. moli grammi di ossigeno = 0, 0555 mol x 15, 9994 g mol-1 = 0, 888 g grammi di idrogeno = 0, 0555 mol x 2 x 1, 008 g mol-1 = 0, 112 g

Esercizi Calcolare la massa di ciascun elemento e di H 2 O che è contenuta in 1, 00 g di Ni. SO 4 7 H 2 O. n. moli= grammi del composto/ massa molare del composto = massa atomica di Ni (58, 69) + massa atomica di S (32, 07) + 4 x massa atomica di O (15, 9994) + 7 x massa molecolare di H 2 O (18) = 280, 9 g mol-1 n. moli di composto = 1 g / 280. 9 g mol-1 = 0, 00356 mol grammi di sostanza= massa molare x n. moli La massa di ciascun elemento e dell’acqua è: 0, 00356 mol x 58, 7 g mol-1 = 0, 209 g di Ni 0, 00356 mol x 32, 1 g mol-1 = 0, 114 g di S 0, 00356 mol x 11 x 15, 9994 g mol-1 = 0, 627 g di O 0, 00356 mol x 14 x 1, 008 g mol-1 = 0, 0503 g di H 0, 00356 mol x 7 x 18, 0 g mol-1 = 0, 449 g di H 2 O

L'analisi elementare • La formula che arriviamo a scrivere per un composto è detta formula minima (stechiometrica o elementare), ossia le proporzioni minime tra gli elementi di un composto: si ricava dall’analisi elementare della sostanza. Per tutte le sostanze è possibile scrivere una formula minima. • L’ analisi elementare di un composto è la determinazione delle percentuali in massa degli elementi presenti nel composto. Da queste percentuali è possibile risalire alla formula minima; per trovare la vera formula molecolare occorre altro dato sperimentale (spesso si deve determinare la massa molare della sostanza).

Esercizi: Composizione % dei composti chimici La percentuale in peso è data dal rapporto fra la massa di ciascun elemento e la massa della sostanza dove l’elemento è contenuto, moltiplicato x 100. % peso dell’elemento contenuto nella sostanza = (massa in g dell’elemento /massa in g della sostanza ) x 100 Es. : Calcolare la % in peso degli elementi del composto C 5 H 5 N. Peso molecolare del composto = 5 x 12, 01 (C) + 5 x 1, 008 (H) + 14, 01 (N) = 79, 10 g mol-1 1 mole di composto contiene 5 moli di C, 5 moli di H e 1 mole di H, quindi: % C = ((5 x 12, 01 g mol-1) / 79, 10 g mol-1 ) x 100 = 75, 9 % % H = ((5 x 1, 008 g mol-1) / 79, 10 g mol-1 ) x 100 = 6, 38 % % N = 14, 01 g mol-1 / 79, 10 g mol-1 ) x 100 = 17, 7 %

Esercizi: Calcolo delle formule minime e molecolari di un composto Se si conosce la % in peso di tutti gli elementi in un composto si può trovare la formula minima del composto. Se si conosce il peso molecolare del composto si può ricavare a anche la formula molecolare. Es. : un composto è costituito da C, H e Cl con percentuali in peso uguali a 49, 0%, 2, 74%, 48, 1%, rispettivamente. Calcolare la formula minima. Consideriamo di avere 100 g del composto: Moli di C = 49, 0 g / 12, 01 g mol-1 = 4, 08 mol Moli di H = 2, 74 g / 1, 008 g mol-1) = 2, 72 mol Moli di Cl = 48, 1 g / 35, 45 g mol-1 ) = 1, 36 mol Dividendo questi numeri per il numero più piccolo (1, 36 mol) si calcola il rapporto tra le moli di C, H e Cl è uguale a 3: 2: 1. quindi la fomula minima è C 3 H 2 Cl. Quella molecolare sarà un multiplo alla n di quella minima (C 3 H 2 Cl)n.

Esercizi: Calcolo delle formule minime e molecolari di un composto Un composto puro è è costituito da 5, 9% di H, 94, 0% di O. Il peso molecolare determinato sperimentalmente è 34, 1. Calcolare la formula molecolare del composto. Consideriamo di avere 100 g del composto: Moli di H = 5, 9 g / 1, 008 g mol-1 = 5, 90 mol Moli di O = 94, 0 g / 15, 994 g mol-1 = 5, 87 mol Il numero di atomi di H rispetto all’O è 5, 9/5, 87 = 1 Quindi la formula minima è HO. Quella molecolare sarà un multiplo alla n di quella minima (HO)n. n = 34, 1 g mol-1 /17, 0 g mol-1 = 2, 0 Quindi la formula molecolare è H 2 O 2