In approssimazione BornOppenheimer per una molecola a N

In approssimazione Born-Oppenheimer per una molecola a N elettroni: L’hamiltoniano elettrostatico per una molecola biatomica AB ha la forma:

r. Ai = distanza tra il nucleo A e l’elettrone i-esimo r. Bi = distanza tra il nucleo B e l’elettrone i-esimo RAB = distanza tra il nucleo A (ZA) e il nucleo B (ZB) Termine cinetico elettronico Attrazione nucleo-elettrone Repulsione nucleo-nucleo
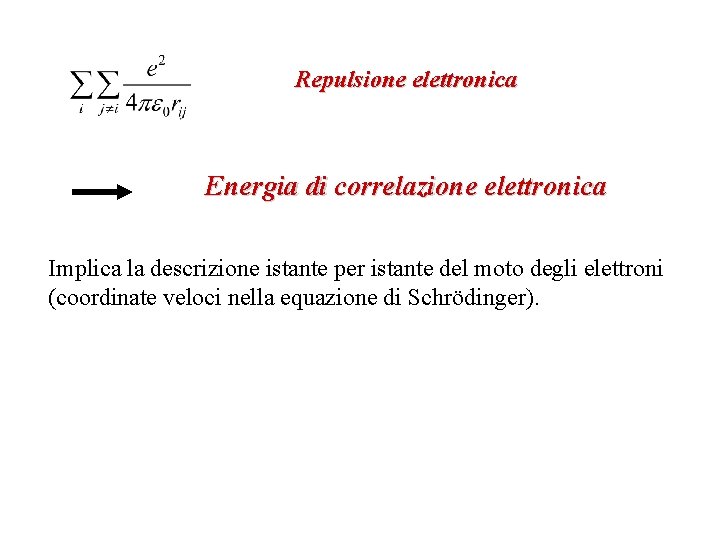
Repulsione elettronica Energia di correlazione elettronica Implica la descrizione istante per istante del moto degli elettroni (coordinate veloci nella equazione di Schrödinger).

Spin-Orbitale: Spin-Orbitale orbitale a singolo elettrone prodotto di un orbitale spaziale per la corrispondente funzione di spin. Orbitale spaziale Funzione di spin Orbitale molecolare a N elettroni come prodotto antisimmetrizzato di N/2 spin-orbitali. Antisimmetrizzato = gli elettroni devono essere descritti da funzioni antisimmetriche (Principio di esclusione di Pauli)

Come ottenere un prodotto antisimmetrizzato?

Es. Determinante di Slater per due elettroni = Prodotto di orbitali a singolo elettrone Antisimmetria di spin

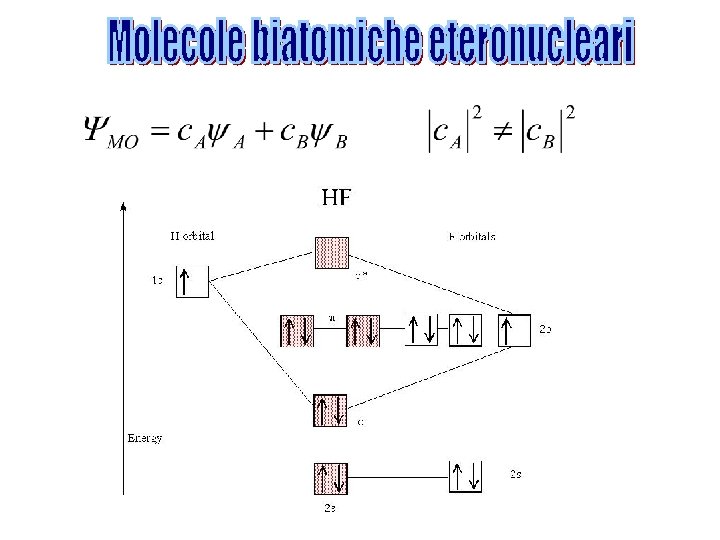
L’orbitale molecolare è costruito come una combinazione lineare di orbitali atomici: Densità di carica nell’elemento di volume d I coefficienti cj sono determinati attraverso il metodo variazionale.

● Una funzione LCAO formata dalla combinazione di n orbitali atomici porta ad un insieme di n equazioni lineari omogenee. ● dalla risoluzione di queste equazioni si ottengono n valori possibili per l’energia. Il valore più basso rappresenta l’energia dello stato fondamentale, quella via più grandi rappresentano l’energia degli stati eccitati. ●ad ogni valore dell’energia corrisponde un set di coefficienti che rappresentano i pesi associati agli orbitali atomici nella combinazione linerae che genera l’orbitale molecolare.

Per la molecola di idrogeno la configurazione elettronica fondamentale è: Antisimmetrica: stato di singoletto di spin

Vi sono altre configurazioni possibili: Antisimmetrica: stato di tripletto di spin

Nel caso di sistemi a più elettroni, gli orbitali atomici che effettivamente concorrono alla formazione di un orbitale molecolare devono rispettare alcune regole generali: 1) devono possedere una corretta simmetria 2) devono avere energie confrontabili 3) devono avere dimensioni confrontabili Orbitali atomici di tipo s possono generare solo orbitali di tipo , orbitali di tipo p danno luogo ad orbitali molecolari di tipo e di tipo .
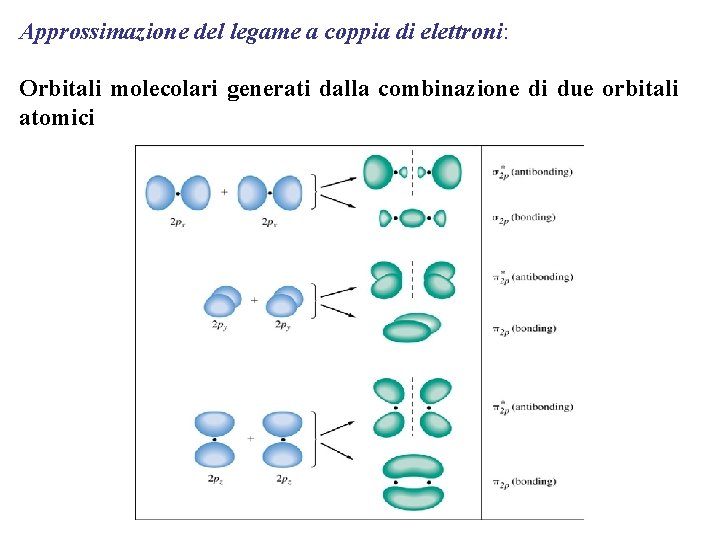
Approssimazione del legame a coppia di elettroni: Orbitali molecolari generati dalla combinazione di due orbitali atomici
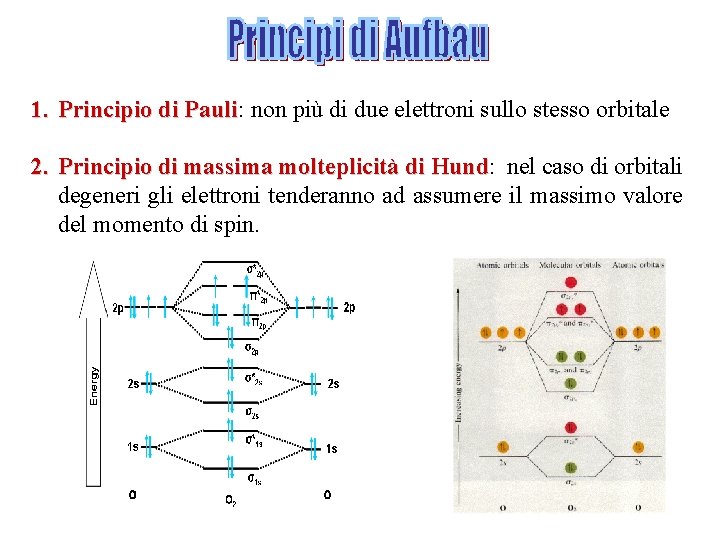
1. Principio di Pauli: Pauli non più di due elettroni sullo stesso orbitale 2. Principio di massima molteplicità di Hund: Hund nel caso di orbitali degeneri gli elettroni tenderanno ad assumere il massimo valore del momento di spin.
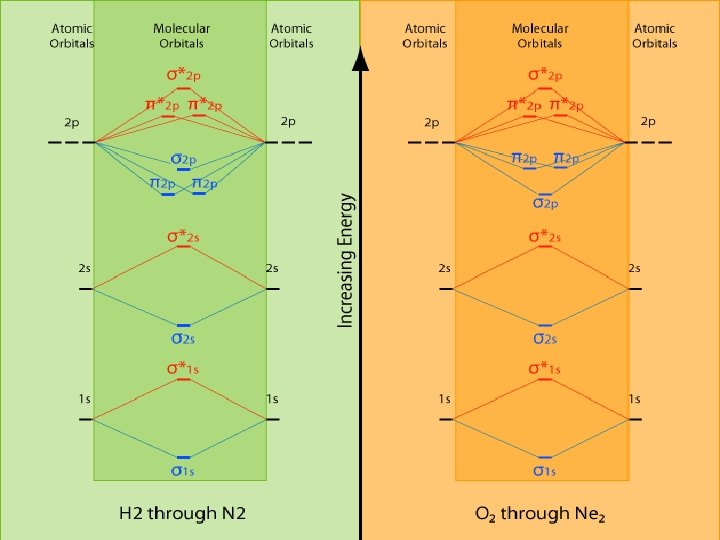

N 2(14 elettroni): (KK*) 1 g 2 u 21 u 43 g 2 Orbitali di kernel O 2(16 elettroni): (KK*) 1 g 2 u 21 u 43 g 2 2 g 2 Il principio di Hund giustifica le proprietà paramagnetiche dell’ossigeno molecolare
- Slides: 16