IMUNOLOGIA TUMORILOR Sef lucrari dr Claudia Burz Obiectivele

IMUNOLOGIA TUMORILOR Sef lucrari dr. Claudia Burz

Obiectivele cursului Definirea tumorilor Modificări genetice responsabile de apariția tumorilor Tumori maligne/tumori benigne Factori etiopatogenetici implicați în apariția tumorilor Răspunsul imun antitumoral Antigene tumorale Celule implicate în apărarea antitumorală Mecanisme de scăpare ale tumorilor
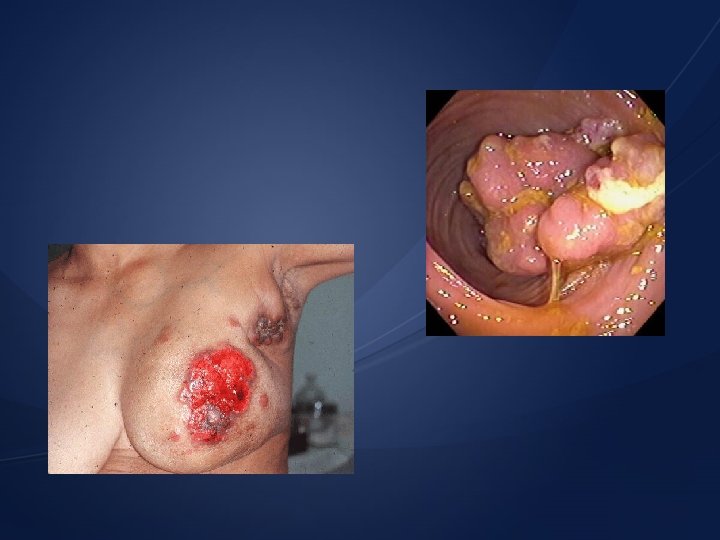

Cancerul este o boala genetica Cancerul este o boala multifactoriala aparuta in urma dereglarii expresiei unor gene implicate in functionarea normala a celulei. Mutatiile genelor care controleaza diviziunea/proliferarea si moartea celulara pot rupe echilibrul natural ce asigura homeostazia tisulara. Cancerul reprezinta o acumulare de alterari genetice

INTRODUCERE Cancerizarea sau transformarea celulelor se datoreaza unor mutatii multiple, la nivelul genomului, care provoaca: - o proliferare continua necontrolata - alterarea functiilor normale celulelor - abolirea apoptozei Celulele maligne sunt “nemuritoare”, se pot cultiva in vitro sub forma de linii standardizate

Genele cancerului Oncogene proto-oncogena, al carui rol normal in celula consta in promovarea diviziunii celulare si care, in urma unor modificari cantitative sau calitative, este susceptibila deveni o “gene transformanta” actiune dominanta
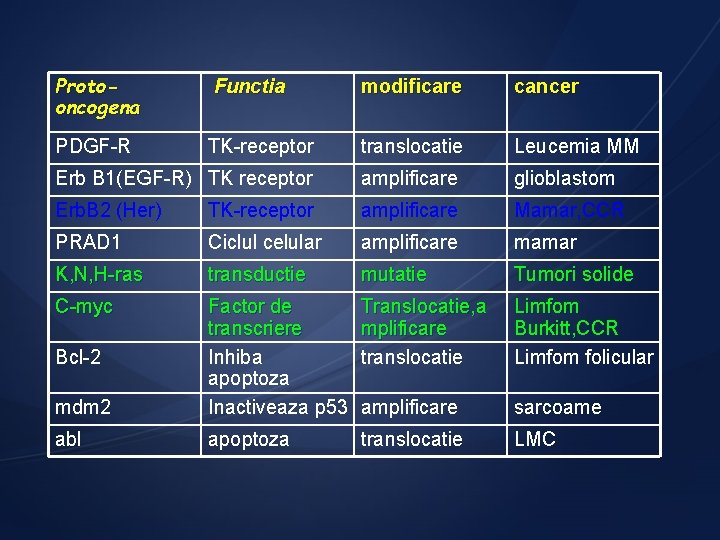
Protooncogena Functia modificare cancer PDGF-R TK-receptor translocatie Leucemia MM Erb B 1(EGF-R) TK receptor amplificare glioblastom Erb. B 2 (Her) TK-receptor amplificare Mamar, CCR PRAD 1 Ciclul celular amplificare mamar K, N, H-ras transductie mutatie Tumori solide C-myc Translocatie, a mplificare translocatie Limfom Burkitt, CCR Limfom folicular mdm 2 Factor de transcriere Inhiba apoptoza Inactiveaza p 53 amplificare sarcoame abl apoptoza translocatie LMC Bcl-2
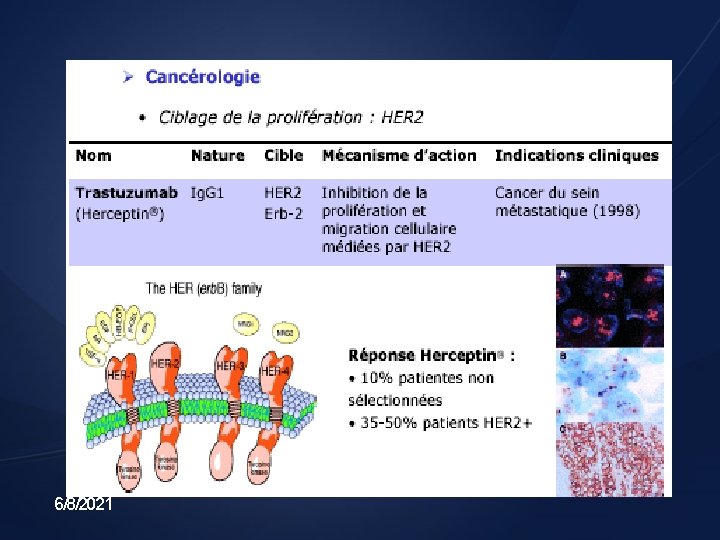
6/8/2021

Genele cancerului Genele supresoare Pierderea functiei prin alterarea ambelor alele pierderea heterozigotiei Intervin in: a) reglarea ciclului celular : gena Rb 1, p 53 p 16 b) reglarea transductiei semnalului : gena NF 1 (17 q), gena APC, DPC 4, SMAD 2, receptorul TGF-beta tip II c) controlul relatiei celula-celula : gena E caderina(16 q) caderina d) controlul apoptozei : p 53 e) neclasificate: BRCA 1 (17 q), BRCA 2 (13 q), VHL
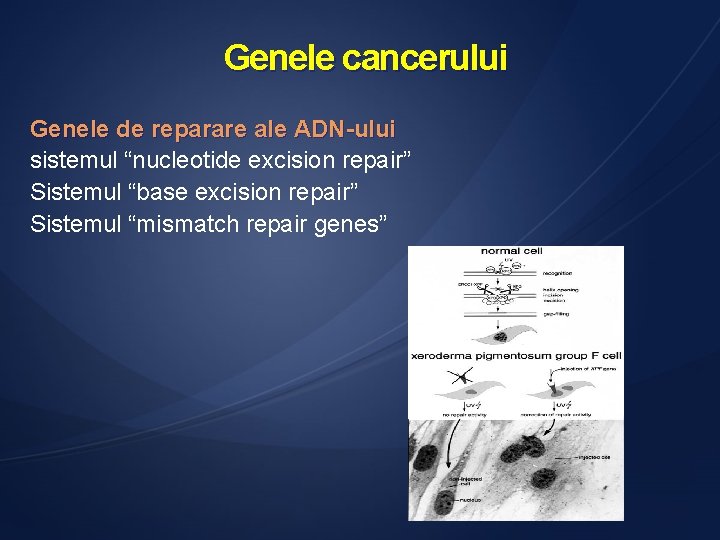
Genele cancerului Genele de reparare ale ADN-ului sistemul “nucleotide excision repair” Sistemul “base excision repair” Sistemul “mismatch repair genes”
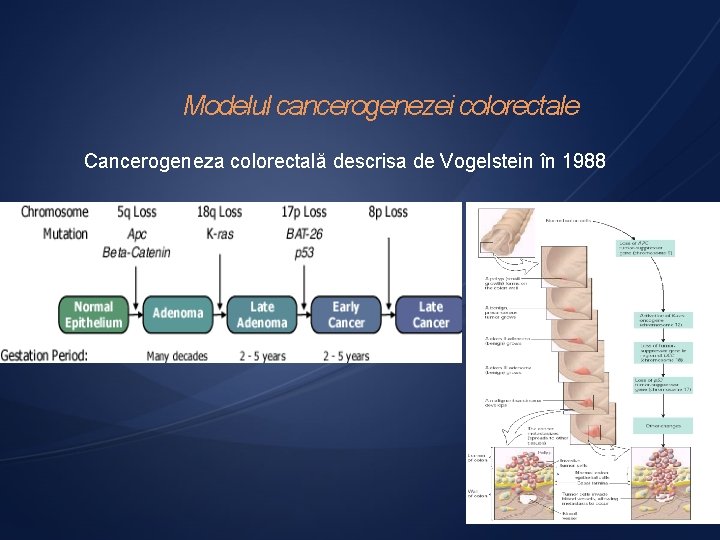
Modelul cancerogenezei colorectale Cancerogeneza colorectală descrisa de Vogelstein în 1988

GENERALITATI Cancerele se pot dezvolta din aproape orice tesut din organism: Carcinoame- tesut epitelial Sarcoame- tesut mezenchimal: muscular, adipos Limfoame- tumori solide ale tesutului limfoid Leucemii- proliferari maligne ale limfocitelor sau a altor celule hematopoetice Celulele transformate -fenotipic diferite fata de cele normale- ar trebiu sa fie considerate de organism ca straine si in consecinta sa induca un raspuns imun antitumoral
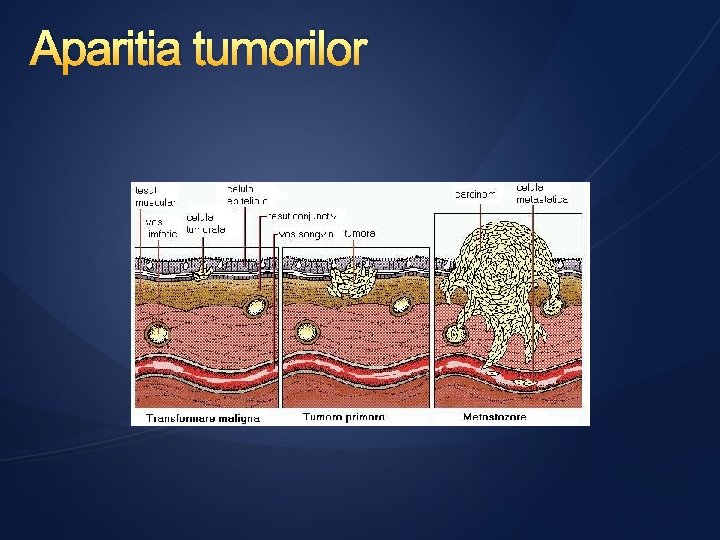
Aparitia tumorilor

Caracteristici ale tumorilor benigne şi maligne Tumori benigne sunt bine delimitate; există un plan de delimitare între ţesutul normal şi cel tumoral au formă regulată; consistenţă moale, elastică; nu invadează ţesuturile vecine şi nu metastazează; nu recidivează după efectuarea corectă a exciziei chirurgicale; au caracter expansiv-compresiv; sunt bine diferenţiate apar ca celule mature mitoze rare adeziunea celulară se păstrează Tumori maligne sunt imprecis delimitate; nu există un plan de delimitare între ţesuturile normale şi cele tumorale; au suprafaţa neregulată, prezintă zone de necroză în centrul tumorii; au consistenţă dură; invadează şi metastazează în situsuri de proliferare departe de ţesutul de origine diferenţiere scăzută sau inexistentă celule cu dimensiuni mari celule tinere cu mitoze atipice conţin puţine structuri specializate nucleoli proeminenţi raport supraunitar (nucleu/citoplasmă) nuclei - hipercromie, hipercromazie pierderea inhibiţiei de creştere dependentă de densitatea celulară

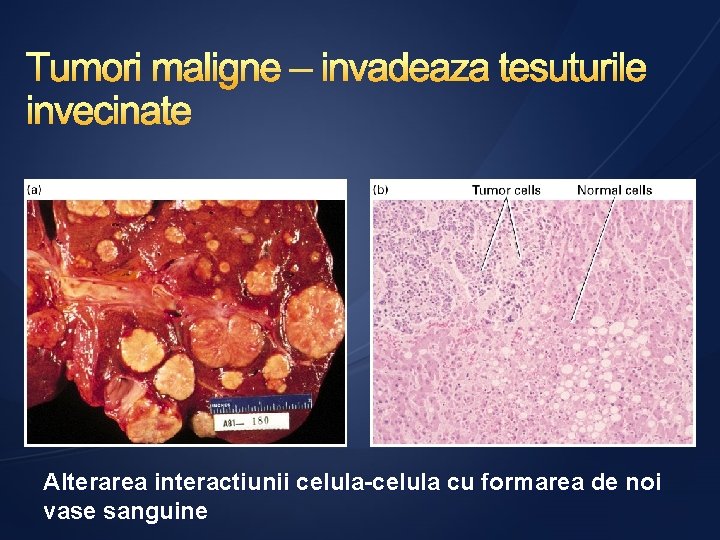
Alterarea interactiunii celula-celula cu formarea de noi vase sanguine

Factori etiopatogenetici Toxice (fumat, alcool, abuzul de cafea. . ) Radiatii Dieta hiperlipidica, Leziuni preneoplazice : esofag Barrett, polipi adenomatoşi gastrici sau intestinali, infecţia cu Helicobacter pylori, gastrita atrofică, metaplazia intestinală a stomacului, Boli inflamatorii (rectocolita hemoragică, boala Crohn. . ) Infectii virale Factori genetici –sindroame familiare de cancer colorectal cu sau fără polipoză colorectală (polipoză adenomatoasă familiară, sdr. Lynch. . )

Factori etiopatogenetici VIRUSURILE ADN Exista mai multe familii de virusuri ADN implicate in dezvoltarea tumorilor experimentale si/sau umane: papova(virusurile papiloma, polioma si virusul simian SV 40), adeno-la rozatoare- si herpes ADN-ul viral este integrat si mentinut indefinit in genomul celulei gazda pe care o transforma , infectia virala este non-productiva In nucleul, citoplasma sau pe membrana celulelor transformate se gasesc mai multe antigene proteice codificate viral

Factori etiopatogenetici VIRUSURILE ARN Pot induce tumori fie rapid – virusurile acut transformante, fie in timp mai indelungat – virusuri transformante lent. RETROVIRUSURILE ACUT TRANSFORMANTE Produc rapid transformarea celulelor normale in celule neoplazice Poseda anumite elemente genetice responsabile de aceasta actiune, denumite oncogene virale (v-onc) Transformarea maligna a celulei se produce prin transcrierea v-onc intr-un ARNm si apoi traducerea intr-o proteina-oncoproteina-.

Factori etiopatogenetici RETROVIRUSURILE TRANSFORMANTE LENTE Nu poseda v-onc insa dupa un timp mai lung provoaca transformarea celulelor, prin activarea protooncogenelor la oncogene Are loc prin insertia genomului viral in vecinatatea unor protooncogene si punerea acestora sub control de catre genele virale, cu functie de promotori sau amplificatori Integrarea virusului produce si dereglarea transcrierii si a altor gene celulare active in perioada embrionara dar reprimate la adult: antigene onco-fetale

virus Tumora indusa v. Epstein-Barr Momonucleoza infectioasa Displazii epiteliale v. Hepatitic B Limfom Burkit, carcinom rinofaringian Cancere anogenitale, ORL hepatocarcinoame v. Hepatitic C hepatocarcinoame Hepatite cr. , ciroze Retrovirusuri (HTLV-1, 2) HIV Leucemii, limfoame Parapareza spastica Sarcom Kaposi SIDA CMV Limfoame non. Hodgkin Deficite imunitare Papilomavirus alte afectiuni Hepatite cr. , ciroze
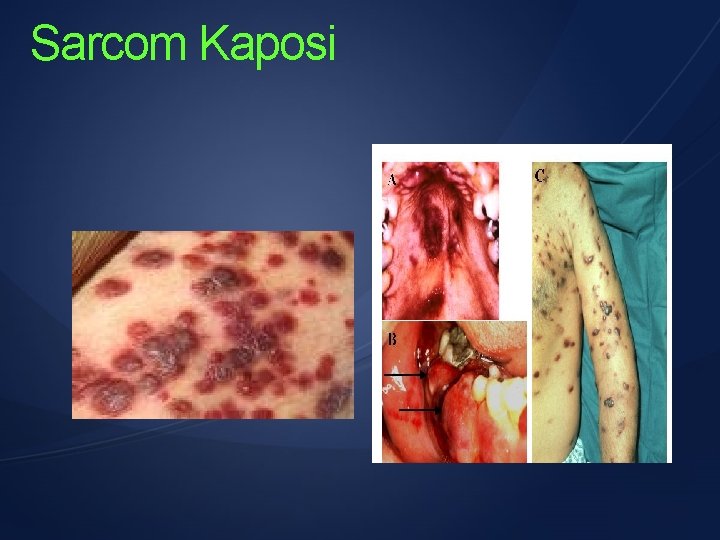
Sarcom Kaposi
Limfom Burkitt
Limfom Non- Hodgkin
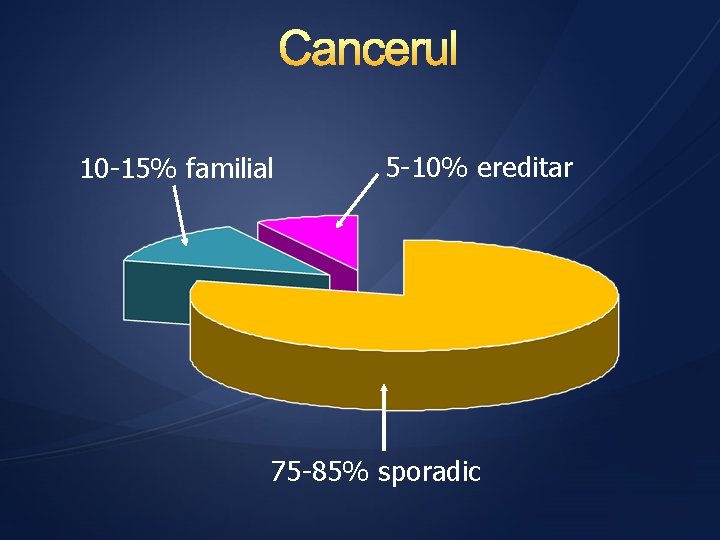
10 -15% familial 5 -10% ereditar 75 -85% sporadic

Factori etiopatogenetici Riscul de apariţie al cancerului colorectal 6% Populaţia generală Antecedente personale de CRC 15%- 20% Boli inflamatorii cronice ale intestinului HNPCC 15%– 40% 70%– 80% >95% FAP 0 20 40 Risc (%) 60 80 100

ANTIGENE TUMORALE → Existenta antigenelor tumorale a putut fi demonstrata experimental prin trnsplantarea unor tumori induse chimic sau viral de la un animal la altul din aceeasi specie Induse chimic Induse viral Induse chimic sau de UV -au fost evidentiate doua tipuri de antigene § Antigene de transplantare specifice tumorilor- TSTA, § Antigene asociate tumorilor- TAA, care nu sunt exprimate exclusiv de catre celulele canceroase

ANTIGENE TUMORALE Induse chimic sau de UV Antigene de transplantare specifice tumorilor (Tumor Specific Antigens TSA): sunt exprimate numai de celulele tumorale MAGE-1, tyrosinase (melanoma), Antigene oncofetale i) carcinoembrionar (Carcinoembryonic antigen CEA in cancerul de colon) ii) Alpha fetoproteina (AFP) (hepatocarcinom) Antigene asociate tumorilor- (Tumor Associated Antigens (TAA): sunt exprimate atât pe celulele tumorale cât şi pe cele normale DAR sunt supraexprimate la nivelul celulele tumorale

MARKERI TUMORALI Definesc antigene sau anticorpi generati ca raspuns ai prezentei acestora utili pentru diagnostic, aprecierea prognosticului, monitorizarea evolutiei monitorizarea raspunsului la tratament

MARKERI TUMORALI După locul unde se testează pot fi clasificaţi Markeri solubili - detectaţi prin metode imunologice sensibile RIA sau ELISA: → produşi normali (hormoni, enzime, proteine, factori de creştere) substanţe oncofetale, carcinoembrionare (CEA, AFP) → paraproteine, imunglobuline monoclonale (mieloame, limfoame) → proteine sintetizate de oncogene sau mutante ale antioncogenelor → componente ale membranelor celulare glicozilate anormal Markeri celulari – constituenti prezenţi în cantităţi mari pe membranele celulelor canceroase şi sunt utilizaţi în diagnosticul citologic şi/sau histologic.

SUPRAVEGHEREA IMUNOLOGICA Teorie aparută în 1960 Una din funcţiile importante ale imunităţii este capacitatea de aparare contra celulelor care poseda pe suprafaţa lor structuri străine, indiferent dacă aceste structuri “self alterate” sunt consecinţa unei infecţii intracelulare, a imbătrânirii sau a alterării proteinelor ca urmare a unor mutatii genetice Conform acestei teorii imunitatea celulară mediată de limfocitele T, joacă un rol esenţial în controlul dezvoltării tumorilor, deoarece disting “selful” de “non-self” Sistemul imun asigură astfel o strictă supraveghere, eliminând orice celula potenţial canceroasă, prevenind progresia la o tumora clinic manifesta
Celulele tumorale prezintă: � Dimensiuni crescute � Ritm rapid de proliferare � Exprimă pe suprafaţa lor antigene specifice (TSA) � Exprimă pe suprafaţa lor în densitate crescută antigene asociate tumorilor (TAA)
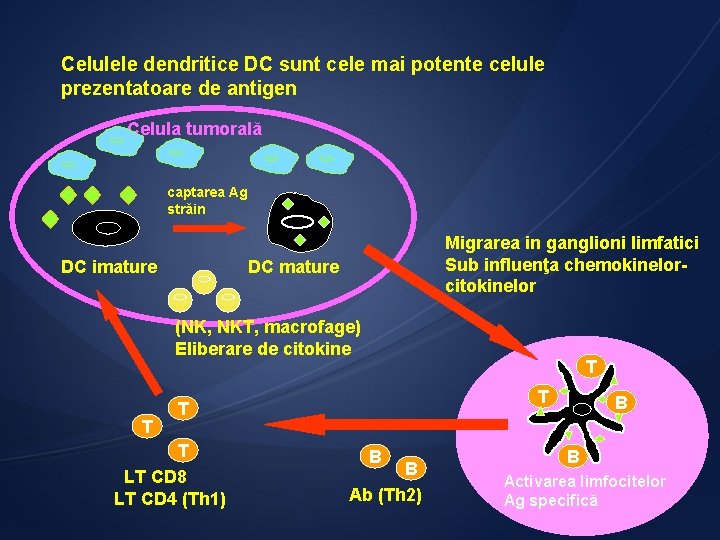
Celulele dendritice DC sunt cele mai potente celule prezentatoare de antigen Celula tumorală captarea Ag străin DC imature Migrarea in ganglioni limfatici Sub influenţa chemokinelorcitokinelor DC mature (NK, NKT, macrofage) Eliberare de citokine T T T LT CD 8 LT CD 4 (Th 1) B B Ab (Th 2) B B Activarea limfocitelor Ag specifică

1. LIMFOCITELE T LT helper – pentru a se induce reactia antitumorala este esentiala activarea acestora → activarea se produce in urma prezentarii antigenelor tumorale cuplate cu MCH cls II de pe celulele prezentatoare de antigen LT citotoxice – recunosc antigenele atunci cand sunt prezentate cuplate cu MCH cls I Prezenta LT tumoral specifice a fost demonstrata in diferite tipuri de cancere se gasesc in infiltratul limfocitar intratumoral si in ganglionii limfatici sateliti LT imunologic active pot sa intre in interiorul tumorilor si au capacitatea de a impiedica cresterea si metastazarea acestora
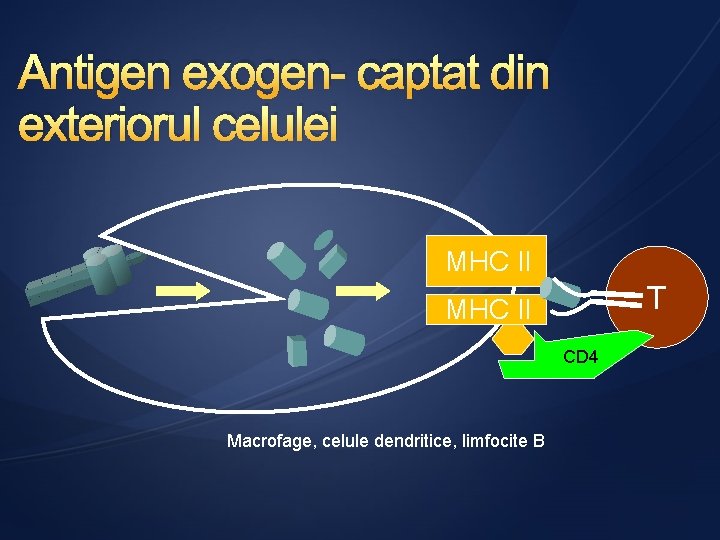
Antigen exogen- captat din exteriorul celulei MHC II T MHC II CD 4 Macrofage, celule dendritice, limfocite B
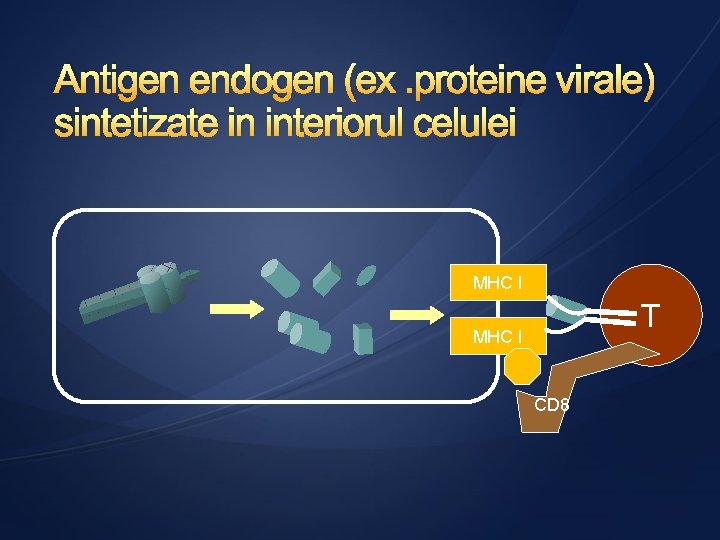
Antigen endogen (ex. proteine virale) sintetizate in interiorul celulei MHC I T MHC I CD 8

2. CELULELE NK Sunt capabile sa lizeze in vitro o mare varietate de tipuri tumorle din liniile de cultura Nu au receptori specifici pentru antigen, dar poseda mai multe grade de selectivitate sunt eficiente fata de celulele tumorale care nu exprima MCH cls I →sunt citotoxice fata de celulele tumorale sau infectate viral

3. CELULELE LAK (lymphokine activated lymphocytes) Sunt LT cu o capacitete crescuta (in prezenta IL-12 are loc o exprimare crescuta a CAM ) de a liza alte celule inclusiv tumorale, care sunt de regula rezistente la actiunea NK 4. MONOCITELE/MACROFAGELE Experimental s-a constatat ca stimularea macrofagelor– activitate citotoxica Pe de alta parte macrofagele pot sa stimuleze cresterea tumorilor prin stimularea vascularizarii, a stromei, a celulelor tumorale Echilibru intre efectele benefice si nocive

5. ANTICORPI ANTI-TUMORALI Pe baza reactivitatii lor pot fi clasificati in 3 grupe: 1. Reactioneaza doar cu propria tumora (anticorpi fata de antigene unice) 2. Reactioneaza cu tumori inrudite 3. Reactioneaza cu antigene proprii distribuite larg atat pe celule normale cat si maligne ►Nu s-a putut demonstra ca acesti anticorpi au un rol protector, de regula nu sunt tumoral specifici ►Marea majoritate a celulelor cancerose sunt rezistente la activitatea citolitica a complementului – isi repara rapid leziunile membranare provocate de acesta ►Pot masca antigenele de pe suprafata tumorilor ”factori blocanti”, sustragandu-le astfel activitatii citotoxice a limfocitelor T efectoare “facilitare imunologica”
ARGUMENTE PRIVIND EXISTENŢA UNUI RăSPUNS IMUN ANTITUMORAL Prezenţa unor infiltrate celulare mononucleare în jurul unor tipuri de tumori, formate din limfocite (LT), celule NK şi macrofage care apar în absenţa unor stimuli binecunoscuţi ai inflamaţiei (infecţie, necroza) Regresia spontană a unor leziuni sugerează posibiliatea edificării unui răspuns antitumoral eficient,

1. Mecanisme dependente de organismul gazda (imunodeficienţe) Pro – incidenta leucemiilor si limfoamelor este de 10. 000 ori mare la persoanele cu deficite imune secundare sau congenitale Contra – absenta incidentei crescute a tipurilor obisnuite de tumori (mamare, pulmonare, gastro-itestinale), la cei cu imunodepresie

MECANISMELE DE SCAPARE DE REACTIILE IMUNE ANTITUMORALE Mecanisme dependente de tumora – tumorile evita recunoasterea si distrugerea de catre sistemul imun= mecanisme de scapare 1)Antigenitatea scazuta sau absenta a tumorilor : mutatiilor sau deletii ale genelor ce codifica antigenele tumorale interiorizarii moleculelor (modularii) – produsa de anticorpii antitumorali desprinderea lor de pe suprafata celulelor – anticorpi blocanti si/sau complexe imune blocante ‘mascarea’antigenelor Tumori dezvoltate in zone privilegiate – gonade, SNC unde nu au acces efectorii imunitatii

MECANISMELE DE SCAPARE DE REACTIILE IMUNE ANTI-TUMORALE 2)Alterarea exprimarii moleculelor MHC si CAM →s -a constatat ca tumorile cu potential ridicat de metastazare nu exprima una din alelele MHC cls I avand drept consecinta, absenta distrugerii lor de catre LTc (sau exprima aberant MHC cls II), aceeasi evolutie o au si tumorile formate din celule lipsite de molecule de adeziune (CAM).

3) Producerea de factori supresori Citokine supresoare produse de catre celulele tumorale: TGF-β (factor de crestere transformant β)- un inhibitor puternic al LTc si a macrofagelor Macrofagele au frecvent o activitate imunosupresoare nespecifica prin prostaglandine PGE 2 Pe masura ce tumora se dezvolta apar si LT CD 4 tolerante, care suprima functia celulelor efectoare
- Slides: 45