Impre Iones en la solucin acuosa Pb NO
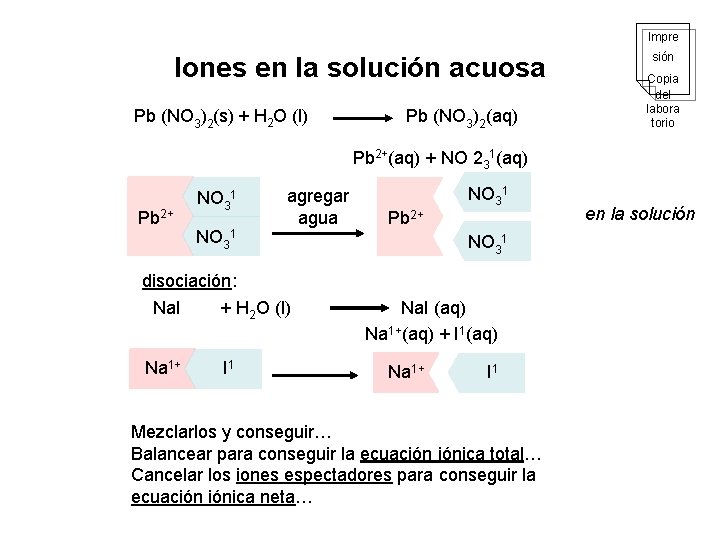
Impre Iones en la solución acuosa Pb (NO 3)2(s) + H 2 O (l) Pb (NO 3)2(aq) sión Copia del labora torio Pb 2+(aq) + NO 231(aq) Pb 2+ NO 31 agregar agua disociación: Na. I + H 2 O (l) Na 1+ I 1 Pb 2+ NO 31 Na. I (aq) Na 1+(aq) + I 1(aq) Na 1+ I 1 Mezclarlos y conseguir… Balancear para conseguir la ecuación iónica total… Cancelar los iones espectadores para conseguir la ecuación iónica neta… en la solución
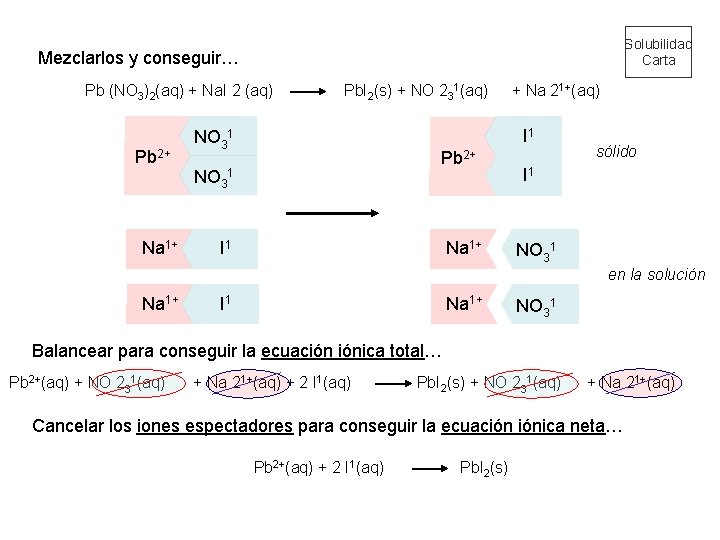
Solubilidad Carta Mezclarlos y conseguir… Pb (NO 3)2(aq) + Na. I 2 (aq) Pb 2+ Na 1+ Pb. I 2(s) + NO 231(aq) + Na 21+(aq) I 1 NO 31 Pb 2+ NO 31 I 1 Na 1+ sólido I 1 NO 31 en la solución Na 1+ I 1 Na 1+ NO 31 Balancear para conseguir la ecuación iónica total… Pb 2+(aq) + NO 231(aq) + Na 21+(aq) + 2 I 1(aq) Pb. I 2(s) + NO 231(aq) + Na 21+(aq) Cancelar los iones espectadores para conseguir la ecuación iónica neta… Pb 2+(aq) + 2 I 1(aq) Pb. I 2(s)
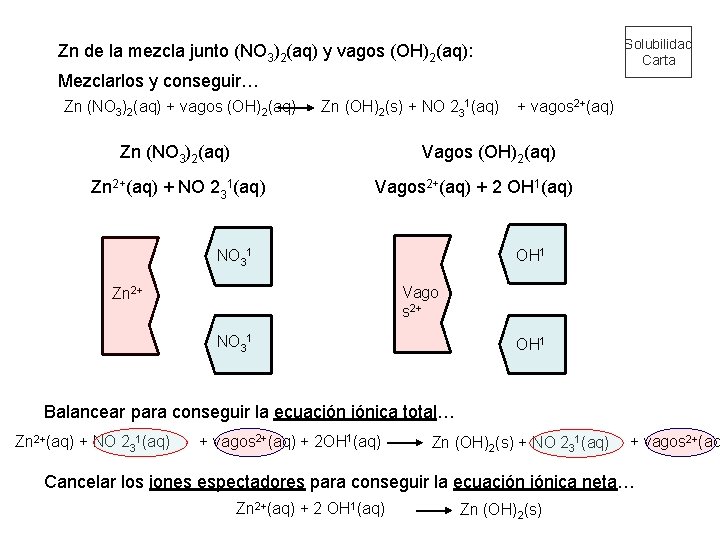
Solubilidad Carta Zn de la mezcla junto (NO 3)2(aq) y vagos (OH)2(aq): Mezclarlos y conseguir… Zn (NO 3)2(aq) + vagos (OH)2(aq) Zn (OH)2(s) + NO 231(aq) Zn (NO 3)2(aq) + vagos 2+(aq) Vagos (OH)2(aq) Zn 2+(aq) + NO 231(aq) Vagos 2+(aq) + 2 OH 1(aq) OH 1 NO 31 Vago s 2+ Zn 2+ NO 31 OH 1 Balancear para conseguir la ecuación iónica total… Zn 2+(aq) + NO 231(aq) + vagos 2+(aq) + 2 OH 1(aq) Zn (OH)2(s) + NO 231(aq) + vagos 2+(aq Cancelar los iones espectadores para conseguir la ecuación iónica neta… Zn 2+(aq) + 2 OH 1(aq) Zn (OH)2(s)

Pre-laboratorio: Na 1+(aq) Cl 1(aq) AG 1+(aq) NO 31(aq) 1. ¿Qué iones están presentes en las soluciones siguientes? _________ Ag. NO del Na. Cl (aq)3_________ del (del aq) 2. Cuando estas soluciones se mezclan juntas, se ve un precipitado. Cuáles son los AG 1+(aq) Cl 1(aq) Na 1+(aq) NO 31(aq) nuevos ¿combinaciones de iones que habrían podido formar el precipitado? _________ y _________ 3. ¿Usando la tabla de la solubilidad, que la nueva combinación formará un precipitado? AG 1+(aq) Cl 1(aq) Ag. Cl _________ 4. ¿Seguirá habiendo qué nueva combinación en la solución? Na 1+(aq) NO 31(aq) _________ 5. Escribir la ecuación total de la reacción para esta reacción. Estar seguro de indicar el correcto fase (condición de la reacción) para cada reactivo y cada producto. 6. Escribir la ecuación iónica neta para esta reacción. Una vez más incluir las fases Na 1+(aq) + NO 31(aq) + Cl 1 condiciones). (aq) + AG 1+(aq) + NO 31(aq) Ag. Cl (reacción 7. Explicar porqué usted no contaba con ninguna reacción entre las soluciones de la KOH (aq) y Na. OH (aq). AG 1+(aq) + Cl 1(aq) Ag. Cl Cuando los cationes cambian lugares terminan con un hidróxido (no se forma ninguna nueva combinación)
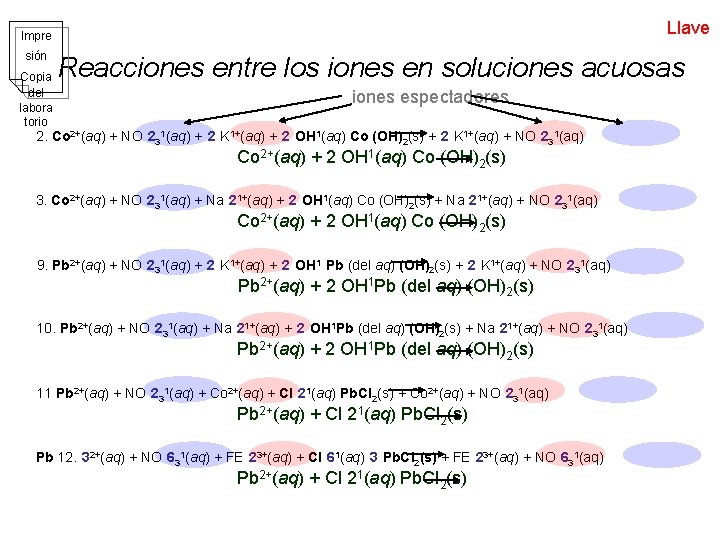
Llave Impre sión Copia del labora torio Reacciones entre los iones en soluciones acuosas iones espectadores 2. Co 2+(aq) + NO 231(aq) + 2 K 1+(aq) + 2 OH 1(aq) Co (OH)2(s) + 2 K 1+(aq) + NO 231(aq) Co 2+(aq) + 2 OH 1(aq) Co (OH)2(s) 3. Co 2+(aq) + NO 231(aq) + Na 21+(aq) + 2 OH 1(aq) Co (OH)2(s) + Na 21+(aq) + NO 231(aq) Co 2+(aq) + 2 OH 1(aq) Co (OH)2(s) 9. Pb 2+(aq) + NO 231(aq) + 2 K 1+(aq) + 2 OH 1 Pb (del aq) (OH)2(s) + 2 K 1+(aq) + NO 231(aq) Pb 2+(aq) + 2 OH 1 Pb (del aq) (OH)2(s) 10. Pb 2+(aq) + NO 231(aq) + Na 21+(aq) + 2 OH 1 Pb (del aq) (OH)2(s) + Na 21+(aq) + NO 231(aq) Pb 2+(aq) + 2 OH 1 Pb (del aq) (OH)2(s) 11 Pb 2+(aq) + NO 231(aq) + Co 2+(aq) + Cl 21(aq) Pb. Cl 2(s) + Co 2+(aq) + NO 231(aq) Pb 2+(aq) + Cl 21(aq) Pb. Cl 2(s) Pb 12. 32+(aq) + NO 631(aq) + FE 23+(aq) + Cl 61(aq) 3 Pb. Cl 2(s) + FE 23+(aq) + NO 631(aq) Pb 2+(aq) + Cl 21(aq) Pb. Cl 2(s)

Llave Reacciones entre los iones en soluciones acuosas 15. Cu 2+(aq) + NO 231(aq) + 2 K 1+(aq) + 2 OH 1 Cu (del aq) (OH)2(s) + 2 K 1+(aq) + NO 231(aq) Cu 2+(aq) + 2 OH 1 Cu (del aq) (OH)2(s) 16. Cu 2+(aq) + NO 231(aq) + Na 21+(aq) + 2 OH 1 Cu (del aq) (OH)2(s) + Na 21+(aq) + NO 231(aq) Cu 2+(aq) + 2 OH 1 Cu (del aq) (OH)2(s) 20. FE 3+(aq) + Cl 31(aq) + 3 K 1+(aq) + 3 OH 1(aq) FE (OH)3(s) + 3 K 1+(aq) + Cl 31(aq) FE 3+(aq) + 3 OH 1(aq) FE (OH)3(s) 21. FE 3+(aq) + Cl 31(aq) + Na 31+(aq) + 3 OH 1(aq) FE (OH)3(s) + Na 31+(aq) + Cl 31(aq) FE 3+(aq) + 3 OH 1(aq) FE (OH)3(s) 24. Co 2+(aq) + Cl 21(aq) + 2 K 1+(aq) + 2 OH 1(aq) Co (OH)2(s) + 2 K 1+(aq) + Cl 21(aq) Co 2+(aq) + 2 OH 1(aq) Co (OH)2(s) 25. Co 2+(aq) + Cl 21(aq) + Na 21+(aq) + 2 OH 1(aq) Co (OH)2(s) + Na 21+(aq) + Cl 21(aq) Co 2+(aq) + 2 OH 1(aq) Co (OH)2(s)
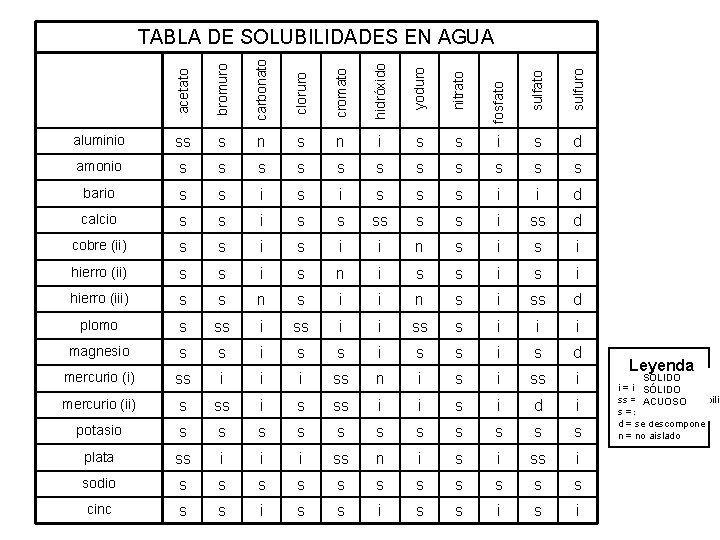
bromuro carbonato cloruro cromato hidróxido yoduro nitrato sulfuro aluminio ss s n i s s i s d amonio s s s bario s s i s s s i i d calcio s s i ss d cobre (ii) s s i i n s i hierro (ii) s s i s n i s s i hierro (iii) s s n s i i n s i ss d plomo s ss i i ss s i i i magnesio s s i s d mercurio (i) ss i i i ss n i ss i mercurio (ii) s ss i i s i d i potasio s s s plata ss i i i ss n i ss i sodio s s s cinc s s i fosfato acetato TABLA DE SOLUBILIDADES EN AGUA Leyenda SÓLIDO i = insoluble SÓLIDO ss = levemente solubilid ACUOSO s = solubilidad d = se descompone n = no aislado
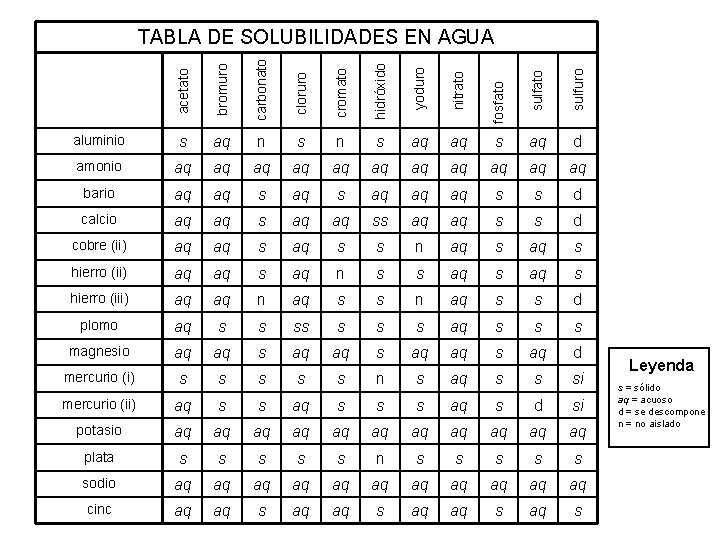
bromuro carbonato cloruro cromato hidróxido yoduro nitrato sulfuro aluminio s aq n s aq aq s aq d amonio aq aq aq bario aq aq s aq aq aq s s d calcio aq aq ss aq aq s s d cobre (ii) aq aq s s n aq s hierro (ii) aq aq s aq n s s aq s hierro (iii) aq aq n aq s s d plomo aq s s s s aq s s s magnesio aq aq s aq d mercurio (i) s s s n s aq s s si mercurio (ii) aq s s s aq s d si potasio aq aq aq plata s s s n s s sodio aq aq aq cinc aq aq s fosfato acetato TABLA DE SOLUBILIDADES EN AGUA Leyenda s = sólido aq = acuoso d = se descompone n = no aislado
- Slides: 8