IMPASSION 031 essai de phase III valuant latzolizumab
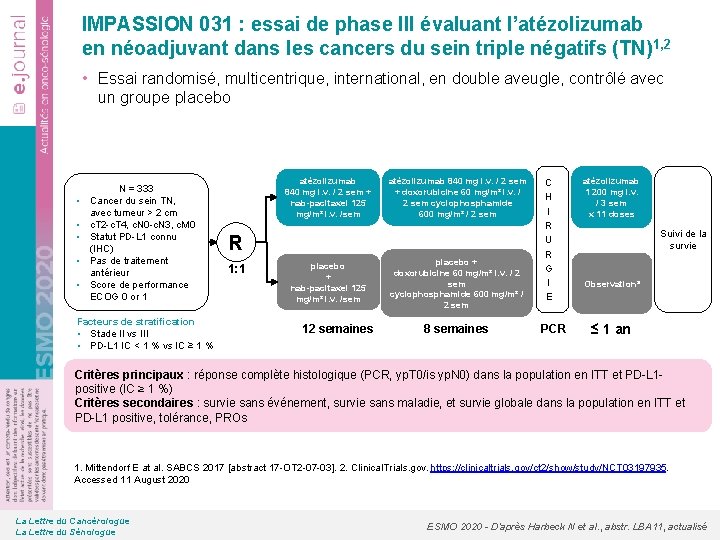
IMPASSION 031 : essai de phase III évaluant l’atézolizumab en néoadjuvant dans les cancers du sein triple négatifs (TN)1, 2 • Essai randomisé, multicentrique, international, en double aveugle, contrôlé avec un groupe placebo • • • N = 333 Cancer du sein TN, avec tumeur > 2 cm c. T 2 -c. T 4, c. N 0 -c. N 3, c. M 0 Statut PD-L 1 connu (IHC) Pas de traitement antérieur Score de performance ECOG 0 or 1 Facteurs de stratification • Stade II vs III • PD-L 1 IC < 1 % vs IC ≥ 1 % atézolizumab 840 mg i. v. / 2 sem + nab-pacitaxel 125 mg/m² i. v. /sem atézolizumab 840 mg i. v. / 2 sem + doxorubicine 60 mg/m² i. v. / 2 sem cyclophosphamide 600 mg/m² / 2 sem R 1: 1 placebo + nab-pacitaxel 125 mg/m² i. v. /sem 12 semaines placebo + doxorubicine 60 mg/m² i. v. / 2 sem cyclophosphamide 600 mg/m² / 2 sem 8 semaines C H I R U R G I E PCR atézolizumab 1 200 mg i. v. / 3 sem x 11 doses Suivi de la survie Observationa ≤ 1 an Critères principaux : réponse complète histologique (PCR, yp. T 0/is yp. N 0) dans la population en ITT et PD-L 1 positive (IC ≥ 1 %) Critères secondaires : survie sans événement, survie sans maladie, et survie globale dans la population en ITT et PD-L 1 positive, tolérance, PROs 1. Mittendorf E at al. SABCS 2017 [abstract 17 -OT 2 -07 -03]. 2. Clinical. Trials. gov. https: //clinicaltrials. gov/ct 2/show/study/NCT 03197935. Accessed 11 August 2020 La Lettre du Cancérologue La Lettre du Sénologue ESMO 2020 - D’après Harbeck N et al. , abstr. LBA 11, actualisé
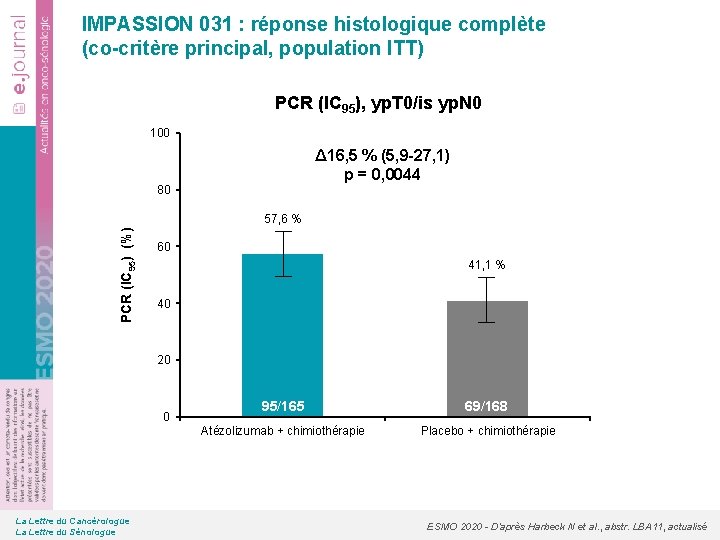
IMPASSION 031 : réponse histologique complète (co-critère principal, population ITT) PCR (IC 95), yp. T 0/is yp. N 0 100 Δ 16, 5 % (5, 9 -27, 1) p = 0, 0044 80 PCR (IC 95) (%) 57, 6 % 60 41, 1 % 40 20 0 La Lettre du Cancérologue La Lettre du Sénologue 95/165 69/168 Atézolizumab + chimiothérapie Placebo + chimiothérapie ESMO 2020 - D’après Harbeck N et al. , abstr. LBA 11, actualisé
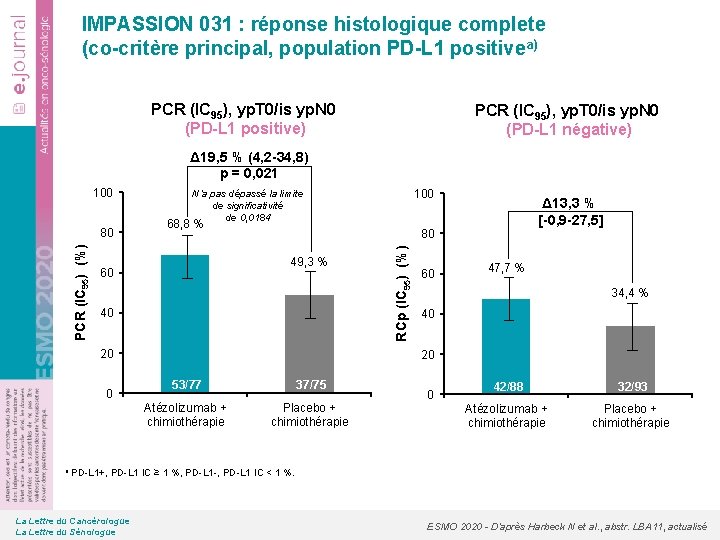
IMPASSION 031 : réponse histologique complete (co-critère principal, population PD-L 1 positivea) PCR (IC 95), yp. T 0/is yp. N 0 (PD-L 1 positive) PCR (IC 95), yp. T 0/is yp. N 0 (PD-L 1 négative) Δ 19, 5 % (4, 2 -34, 8) p = 0, 021 PCR (IC 95) (%) 80 68, 8 % 40 20 a PD-L 1+, Δ 13, 3 % [-0, 9 -27, 5] 80 49, 3 % 60 0 100 N’a pas dépassé la limite de significativité de 0, 0184 RCp (IC 95) (%) 100 60 47, 7 % 34, 4 % 40 20 53/77 37/75 Atézolizumab + chimiothérapie Placebo + chimiothérapie 0 42/88 32/93 Atézolizumab + chimiothérapie Placebo + chimiothérapie PD-L 1 IC ≥ 1 %, PD-L 1 -, PD-L 1 IC < 1 %. La Lettre du Cancérologue La Lettre du Sénologue ESMO 2020 - D’après Harbeck N et al. , abstr. LBA 11, actualisé
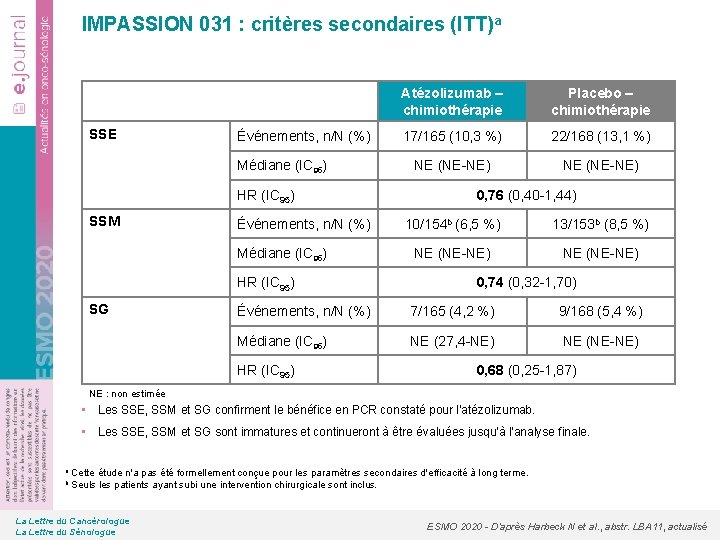
IMPASSION 031 : critères secondaires (ITT)a SSE Événements, n/N (%) Médiane (IC 95) HR (IC 95) SSM Événements, n/N (%) Médiane (IC 95) HR (IC 95) SG Atézolizumab – chimiothérapie Placebo – chimiothérapie 17/165 (10, 3 %) 22/168 (13, 1 %) NE (NE-NE) 0, 76 (0, 40 -1, 44) 10/154 b (6, 5 %) 13/153 b (8, 5 %) NE (NE-NE) 0, 74 (0, 32 -1, 70) Événements, n/N (%) 7/165 (4, 2 %) 9/168 (5, 4 %) Médiane (IC 95) NE (27, 4 -NE) NE (NE-NE) HR (IC 95) 0, 68 (0, 25 -1, 87) NE : non estimée • Les SSE, SSM et SG confirment le bénéfice en PCR constaté pour l'atézolizumab. • Les SSE, SSM et SG sont immatures et continueront à être évaluées jusqu'à l'analyse finale. a Cette b Seuls étude n'a pas été formellement conçue pour les paramètres secondaires d'efficacité à long terme. les patients ayant subi une intervention chirurgicale sont inclus. La Lettre du Cancérologue La Lettre du Sénologue ESMO 2020 - D’après Harbeck N et al. , abstr. LBA 11, actualisé
- Slides: 4