Impact des probiotiques sur les diarrhes associes aux

Impact des probiotiques sur les diarrhées associées aux antibiotiques Présenté par Valérie Dandois et Lina Huynh Voung Résidentes 1 CLSC du Marigot Mai 2019

Aucun conflit d’intérêt à déclarer

Introduction • Incidence de la diarrhée associée aux antibiotiques: 5‐ 39% des adultes • Physiopathologie de la DAA • Surcroissance flore pathogène diarrhée infectieuse • Perturbation métabolisme glucide/acides biliaires diarrhée osmotique • Effet direct sur la motilité intestinale diarrhée motrice • Définition DAA: • Diarrhées qui surviennent avec prise ATB. • Pas d’autres causes possibles • 3 selles ou plus liquides pour > 1‐ 3 jours consécutives

Introduction • Souches de probiotiques approuvées par Santé Canada (niveau de preuve I) • Bio‐K + ™ (L. casei, L. acidophilus, L. rhamnosus) • Culturelle ® (L. rhamnosus GG) • Florastor. Max ® et Florastor ® (Saccharomyces boulardii) • Utilisation de probiotique non recommandée par l’INESSS dans le cas des diarrhées à C. difficile • Mécanismes d’action potentiels des probiotiques • Inhibition de l’adhésion des pathogènes (via compétition des récepteurs et sites d’attache) • Modulation de la réponse inflammatoire et immune (cytokines, Ig. A, MAP kinases) • Production de peptides anti‐microbiens, protéases sériques, mucine

PICO P: population adulte > 18 ans et < 70 ans I: Probiotiques + ATB C: Placebo + ATB O: ‐Incidence des diarrhées associées aux antibiotiques ‐Durée des diarrhées ‐Effets secondaires

Méthodologie
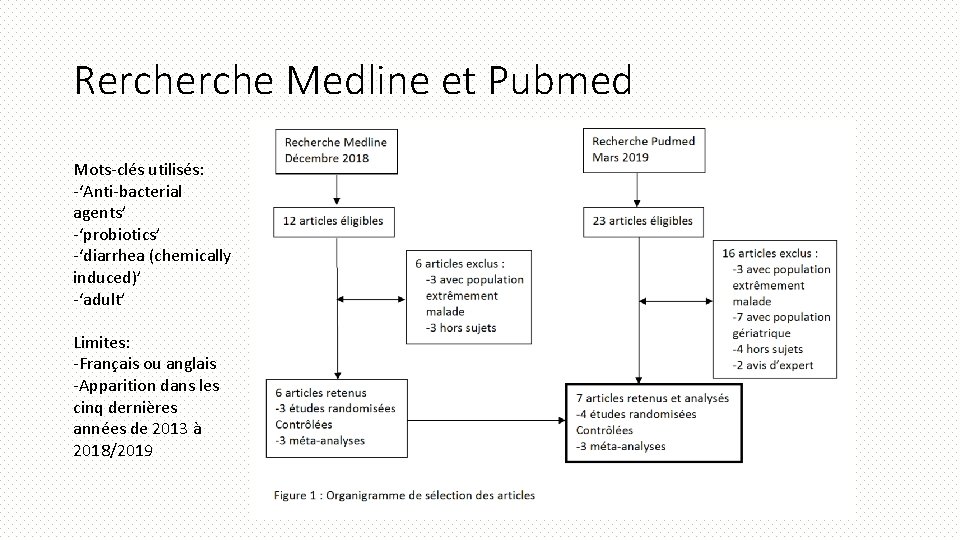
Rerche Medline et Pubmed Mots‐clés utilisés: ‐‘Anti‐bacterial agents’ ‐‘probiotics’ ‐‘diarrhea (chemically induced)’ ‐‘adult’ Limites: ‐Français ou anglais ‐Apparition dans les cinq dernières années de 2013 à 2018/2019
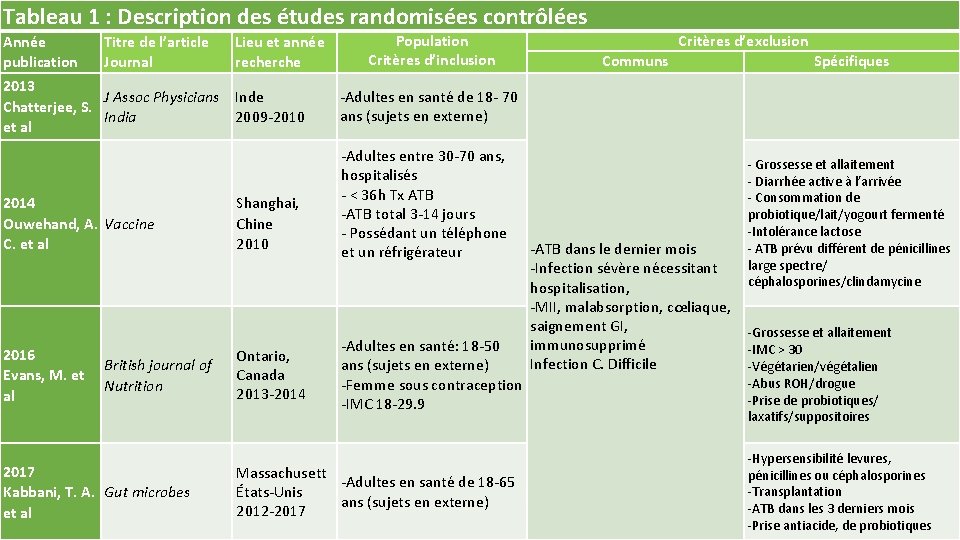
Tableau 1 : Description des études randomisées contrôlées Année publication Titre de l’article Journal Lieu et année recherche 2013 J Assoc Physicians Inde Chatterjee, S. India 2009‐ 2010 et al 2014 Ouwehand, A. Vaccine C. et al Shanghai, Chine 2010 2016 Evans, M. et al Ontario, Canada 2013‐ 2014 British journal of Nutrition 2017 Kabbani, T. A. Gut microbes et al Population Critères d’inclusion Critères d’exclusion Communs Spécifiques ‐Adultes en santé de 18‐ 70 ans (sujets en externe) ‐Adultes entre 30‐ 70 ans, hospitalisés ‐ < 36 h Tx ATB ‐ATB total 3‐ 14 jours ‐ Possédant un téléphone et un réfrigérateur ‐Adultes en santé: 18‐ 50 ans (sujets en externe) ‐Femme sous contraception ‐IMC 18‐ 29. 9 Massachusett ‐Adultes en santé de 18‐ 65 États‐Unis ans (sujets en externe) 2012‐ 2017 ‐ Grossesse et allaitement ‐ Diarrhée active à l’arrivée ‐ Consommation de probiotique/lait/yogourt fermenté ‐Intolérance lactose ‐ ATB prévu différent de pénicillines large spectre/ céphalosporines/clindamycine ‐ATB dans le dernier mois ‐Infection sévère nécessitant hospitalisation, ‐MII, malabsorption, cœliaque, saignement GI, ‐Grossesse et allaitement immunosupprimé ‐IMC > 30 Infection C. Difficile ‐Végétarien/végétalien ‐Abus ROH/drogue ‐Prise de probiotiques/ laxatifs/suppositoires ‐Hypersensibilité levures, pénicillines ou céphalosporines ‐Transplantation ‐ATB dans les 3 derniers mois ‐Prise antiacide, de probiotiques
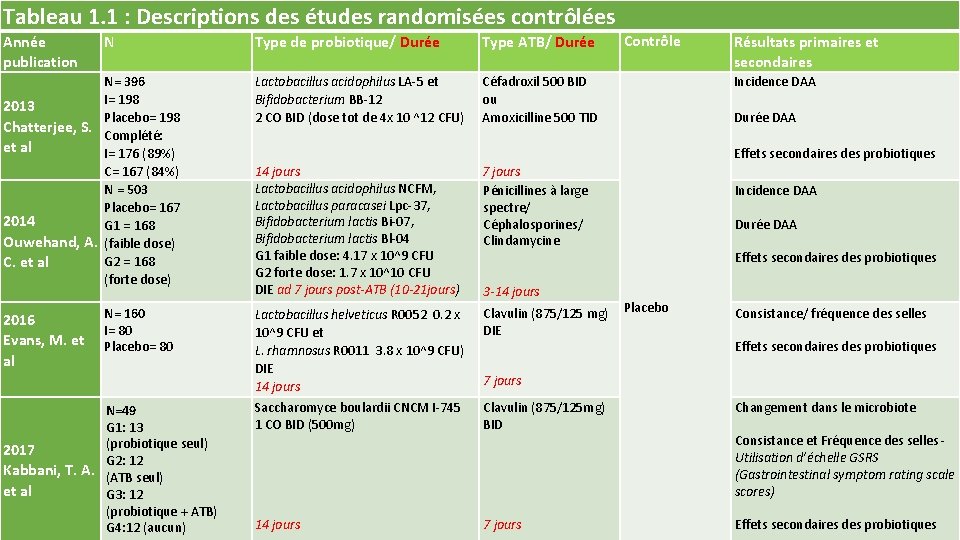
Tableau 1. 1 : Descriptions des études randomisées contrôlées Année publication N N= 396 I= 198 2013 Placebo= 198 Chatterjee, S. Complété: et al I= 176 (89%) C= 167 (84%) N = 503 Placebo= 167 2014 G 1 = 168 Ouwehand, A. (faible dose) G 2 = 168 C. et al (forte dose) 2016 Evans, M. et al N= 160 I= 80 Placebo= 80 N=49 G 1: 13 (probiotique seul) 2017 G 2: 12 Kabbani, T. A. (ATB seul) et al G 3: 12 (probiotique + ATB) G 4: 12 (aucun) Type de probiotique/ Durée Type ATB/ Durée Lactobacillus acidophilus LA‐ 5 et Bifidobacterium BB‐ 12 2 CO BID (dose tot de 4 x 10 ^12 CFU) Céfadroxil 500 BID ou Amoxicilline 500 TID Contrôle Résultats primaires et secondaires Incidence DAA Durée DAA Effets secondaires des probiotiques 14 jours Lactobacillus acidophilus NCFM, Lactobacillus paracasei Lpc‐ 37, Bifidobacterium lactis Bi‐ 07, Bifidobacterium lactis Bl‐ 04 G 1 faible dose: 4. 17 x 10^9 CFU G 2 forte dose: 1. 7 x 10^10 CFU DIE ad 7 jours post-ATB (10 -21 jours) 7 jours Pénicillines à large spectre/ Céphalosporines/ Clindamycine Lactobacillus helveticus R 0052 0. 2 x 10^9 CFU et L. rhamnosus R 0011 3. 8 x 10^9 CFU) DIE 14 jours Clavulin (875/125 mg) Placebo DIE Saccharomyce boulardii CNCM I‐ 745 1 CO BID (500 mg) Clavulin (875/125 mg) BID Changement dans le microbiote 14 jours 7 jours Effets secondaires des probiotiques Incidence DAA Durée DAA Effets secondaires des probiotiques 3 -14 jours Consistance/ fréquence des selles Effets secondaires des probiotiques 7 jours Consistance et Fréquence des selles ‐ Utilisation d’échelle GSRS (Gastrointestinal symptom rating scale scores)
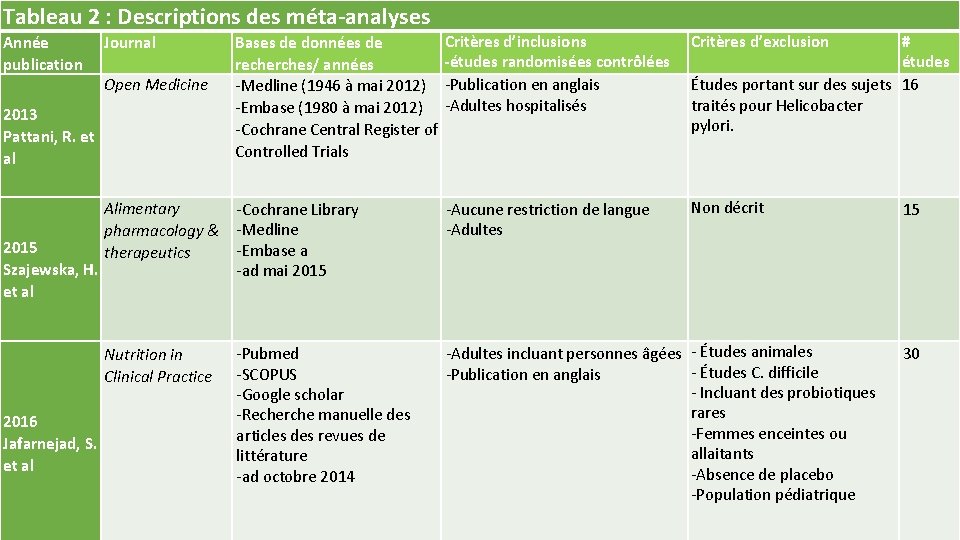
Tableau 2 : Descriptions des méta-analyses Année publication Critères d’inclusions Bases de données de -études randomisées contrôlées recherches/ années ‐Medline (1946 à mai 2012) ‐Publication en anglais ‐Embase (1980 à mai 2012) ‐Adultes hospitalisés ‐Cochrane Central Register of Controlled Trials Critères d’exclusion Alimentary pharmacology & therapeutics ‐Cochrane Library ‐Medline ‐Embase a ‐ad mai 2015 ‐Aucune restriction de langue ‐Adultes Non décrit Nutrition in Clinical Practice ‐Pubmed ‐SCOPUS ‐Google scholar ‐Recherche manuelle des articles des revues de littérature ‐ad octobre 2014 ‐Adultes incluant personnes âgées ‐ Études animales ‐ Études C. difficile ‐Publication en anglais ‐ Incluant des probiotiques rares ‐Femmes enceintes ou allaitants ‐Absence de placebo ‐Population pédiatrique Journal Open Medicine 2013 Pattani, R. et al 2015 Szajewska, H. et al 2016 Jafarnejad, S. et al # études Études portant sur des sujets 16 traités pour Helicobacter pylori. 15 30
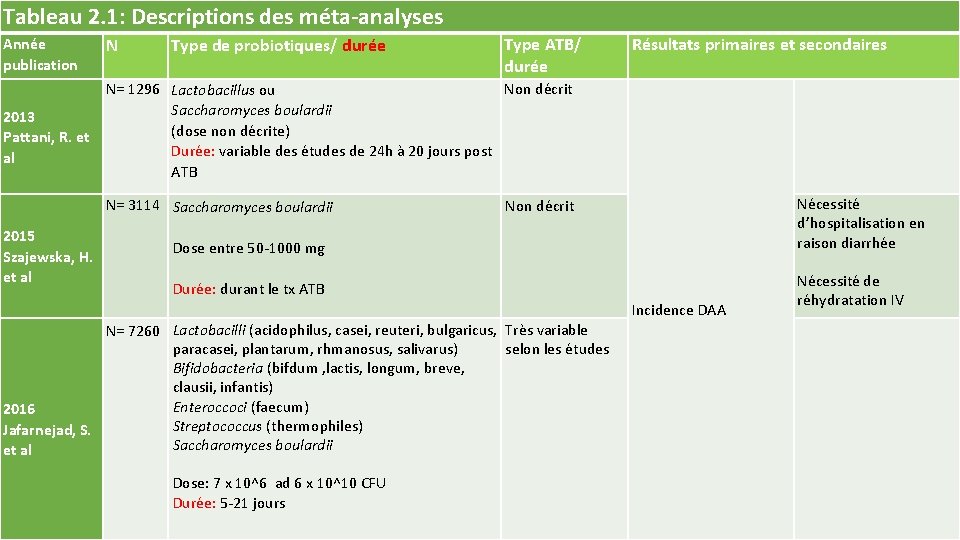
Tableau 2. 1: Descriptions des méta-analyses Année publication N Type de probiotiques/ durée Type ATB/ durée Résultats primaires et secondaires N= 1296 Lactobacillus ou Non décrit Saccharomyces boulardii 2013 (dose non décrite) Pattani, R. et Durée: variable des études de 24 h à 20 jours post al ATB N= 3114 Saccharomyces boulardii 2015 Szajewska, H. et al Nécessité d’hospitalisation en raison diarrhée Non décrit Dose entre 50‐ 1000 mg Durée: durant le tx ATB Incidence DAA N= 7260 Lactobacilli (acidophilus, casei, reuteri, bulgaricus, Très variable paracasei, plantarum, rhmanosus, salivarus) selon les études Bifidobacteria (bifdum , lactis, longum, breve, clausii, infantis) Enteroccoci (faecum) 2016 Streptococcus (thermophiles) Jafarnejad, S. Saccharomyces boulardii et al Dose: 7 x 10^6 ad 6 x 10^10 CFU Durée: 5‐ 21 jours Nécessité de réhydratation IV

Résultats
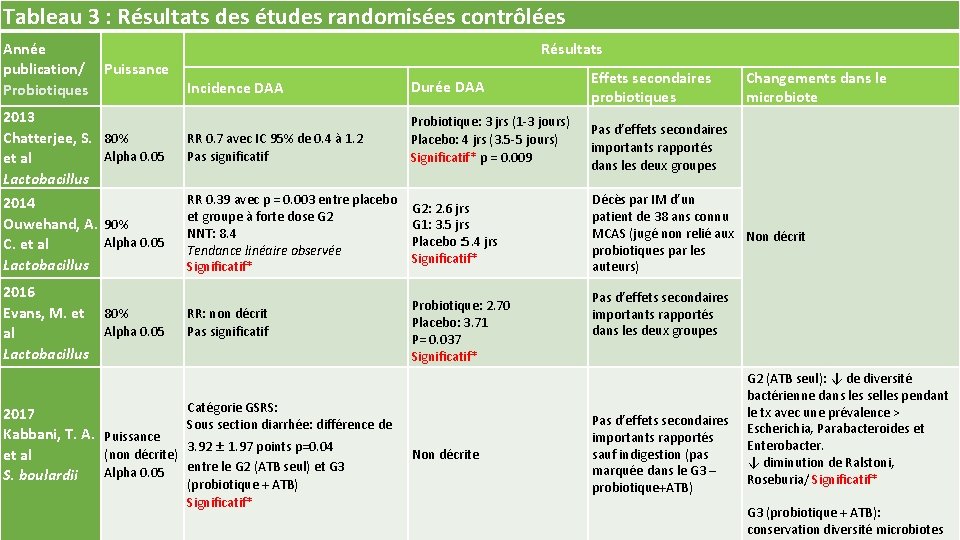
Tableau 3 : Résultats des études randomisées contrôlées Année publication/ Puissance Probiotiques Résultats Incidence DAA Durée DAA 2013 Chatterjee, S. 80% Alpha 0. 05 et al Lactobacillus RR 0. 7 avec IC 95% de 0. 4 à 1. 2 Pas significatif Probiotique: 3 jrs (1‐ 3 jours) Placebo: 4 jrs (3. 5‐ 5 jours) Significatif* p = 0. 009 2014 Ouwehand, A. 90% Alpha 0. 05 C. et al Lactobacillus RR 0. 39 avec p = 0. 003 entre placebo et groupe à forte dose G 2 NNT: 8. 4 Tendance linéaire observée Significatif* 2016 Evans, M. et 80% Alpha 0. 05 al Lactobacillus 2017 Kabbani, T. A. Puissance (non décrite) et al Alpha 0. 05 S. boulardii RR: non décrit Pas significatif G 2: 2. 6 jrs G 1: 3. 5 jrs Placebo : 5. 4 jrs Significatif* Probiotique: 2. 70 Placebo: 3. 71 P= 0. 037 Significatif* Catégorie GSRS: Sous section diarrhée: différence de 3. 92 ± 1. 97 points p=0. 04 entre le G 2 (ATB seul) et G 3 (probiotique + ATB) Significatif* Non décrite Effets secondaires probiotiques Changements dans le microbiote Pas d’effets secondaires importants rapportés dans les deux groupes Décès par IM d’un patient de 38 ans connu MCAS (jugé non relié aux Non décrit probiotiques par les auteurs) Pas d’effets secondaires importants rapportés dans les deux groupes Pas d’effets secondaires importants rapportés sauf indigestion (pas marquée dans le G 3 – probiotique+ATB) G 2 (ATB seul): ↓ de diversité bactérienne dans les selles pendant le tx avec une prévalence > Escherichia, Parabacteroides et Enterobacter. ↓ diminution de Ralstoni, Roseburia/ Significatif* G 3 (probiotique + ATB): conservation diversité microbiotes
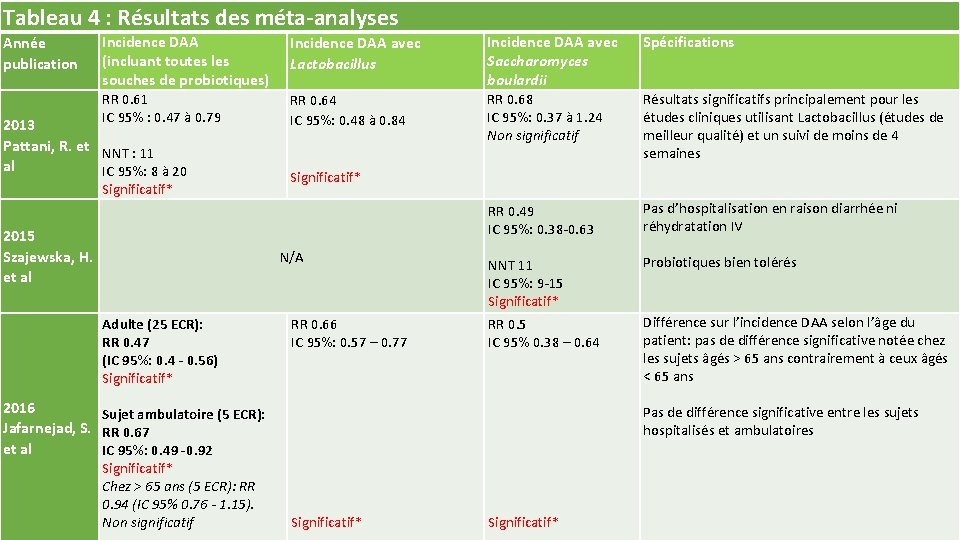
Tableau 4 : Résultats des méta-analyses Année publication Incidence DAA (incluant toutes les souches de probiotiques) Incidence DAA avec Lactobacillus Incidence DAA avec Saccharomyces boulardii Spécifications RR 0. 61 IC 95% : 0. 47 à 0. 79 RR 0. 64 IC 95%: 0. 48 à 0. 84 RR 0. 68 IC 95%: 0. 37 à 1. 24 Non significatif Résultats significatifs principalement pour les études cliniques utilisant Lactobacillus (études de meilleur qualité) et un suivi de moins de 4 semaines RR 0. 49 IC 95%: 0. 38‐ 0. 63 Pas d’hospitalisation en raison diarrhée ni réhydratation IV NNT 11 IC 95%: 9‐ 15 Significatif* Probiotiques bien tolérés RR 0. 5 IC 95% 0. 38 – 0. 64 Différence sur l’incidence DAA selon l’âge du patient: pas de différence significative notée chez les sujets âgés > 65 ans contrairement à ceux âgés < 65 ans 2013 Pattani, R. et NNT : 11 al IC 95%: 8 à 20 Significatif* 2015 Szajewska, H. et al Significatif* N/A Adulte (25 ECR): RR 0. 47 (IC 95%: 0. 4 - 0. 56) Significatif* RR 0. 66 IC 95%: 0. 57 – 0. 77 2016 Sujet ambulatoire (5 ECR): Jafarnejad, S. RR 0. 67 et al IC 95%: 0. 49 -0. 92 Significatif* Chez > 65 ans (5 ECR): RR 0. 94 (IC 95% 0. 76 - 1. 15). Non significatif Pas de différence significative entre les sujets hospitalisés et ambulatoires Significatif*

Discussion

Tableau 5 : Critique des études randomisées contrôlées Année publication 2013 Chatterjee, S. et al Randomisation efficace 2014 Analyse par Ouwehand, A. Étude à l’aveugle intention C. et al thérapeutique 2016 Evans, M. et al Limites Forces Randomisation efficace ‐Représentatif du microbiote canadien 2017 Kabbani, T. A. Évaluation du microbiote et al Biais de sélection: perte au suivi asymétrique ‐Analyse per protocole ‐Peu généralisable: Inde (différences nutritionnelles, génétiques, environnementales) ‐Pas d’analyse selon type ATB ‐Conflit d’intérêt: financée par Zydus Cadila Heathcare Ltd. et Chr. Hansen A/S. ‐Unicentrique et peu généralisable: Chine (différences nutritionnelles, génétiques, environnementales) ‐Randomisation +/‐ efficace par rapport aux maladies sous‐jacentes de base ‐Biais de rappel: suivi téléphonique q 1 smn ‐Pas d’analyse selon le type ATB ‐Unicentrique (population canadienne) ‐Peu généralisable (1 ATB, bcp de critères inclusion/exclusion) ‐Biais d’observation: recueil de données avec échelles subjectives, valeurs utilisées dans l’étude sont une moyenne des valeurs de la smn ‐Biais de rappel (suivi téléphonique q 1 smn) ‐Conflit d’intérêt : financée par Lallemand Health Solutions ‐Biais d’observation: pas à l’aveugle, recueil de données avec échelles subjectives ‐Biais de sélection: peu d’information sur les caractéristiques des patients dans chaque groupe ‐Petit échantillon
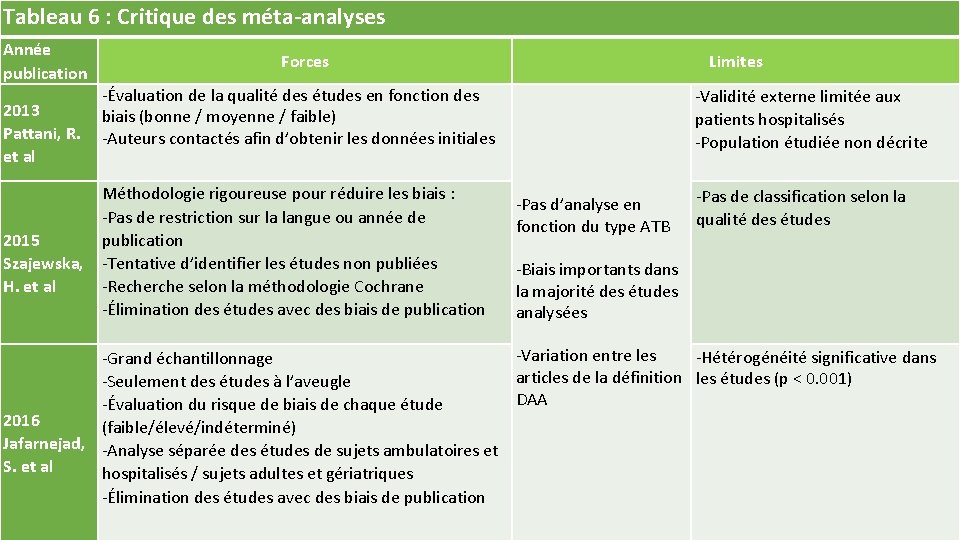
Tableau 6 : Critique des méta-analyses Année publication Forces Limites ‐Évaluation de la qualité des études en fonction des 2013 biais (bonne / moyenne / faible) Pattani, R. ‐Auteurs contactés afin d’obtenir les données initiales et al Méthodologie rigoureuse pour réduire les biais : ‐Pas de restriction sur la langue ou année de publication 2015 Szajewska, ‐Tentative d’identifier les études non publiées ‐Recherche selon la méthodologie Cochrane H. et al ‐Élimination des études avec des biais de publication ‐Validité externe limitée aux patients hospitalisés ‐Population étudiée non décrite ‐Pas d’analyse en fonction du type ATB ‐Pas de classification selon la qualité des études ‐Biais importants dans la majorité des études analysées ‐Variation entre les ‐Hétérogénéité significative dans ‐Grand échantillonnage articles de la définition les études (p < 0. 001) ‐Seulement des études à l’aveugle DAA ‐Évaluation du risque de biais de chaque étude 2016 (faible/élevé/indéterminé) Jafarnejad, ‐Analyse séparée des études de sujets ambulatoires et S. et al hospitalisés / sujets adultes et gériatriques ‐Élimination des études avec des biais de publication

Conclusion

Conclusion • Études: nombreux biais et difficilement généralisables • Tendance démontrée 2/4 études randomisées contrôlées et 3/3 méta‐ analyses: • ↓ incidence des DAA chez les sujets adutes • Souches de Lactobacilli et Saccharomyces boulardii • NNT (nombre de sujet à traiter) 8 -11 • ↓ durée statistiquement significative des DAA variant entre 1 à 2. 9 jours: • Cliniquement significatif ? • Analyse coûts‐bénéfices ? • Bio‐K + ™ 30 CO : 37. 99 $ / Culturelle ® 30 CO: 35. 71$ / Florastor ® 50 CO: 43. 99 $ • (Source: pharmacie Jean‐Coutu) • Utilisation sécuritaire des probiotiques

Conclusion: pistes pour l’avenir • Études comparant l’efficacité des probiotiques selon le type d’ATB • Analyse de la réponse aux probiotiques en fonction des maladies sous‐ jacentes • Impact de l’origine ethnique/culturelle/géographique/alimentaire sur l’efficacité des probiotiques • Études indépendantes (non financées par compagnies pharmaceutiques)

Questions? Merci pour votre écoute!

Références • Levesque A. , Daigle J‐M. et Tardif M. (2017) Efficacité et innocuité des probiotiques en prévention des diarrhées associées à Clostridium difficile [Internet]. Institut national d’excellence en santé et en services sociaux (INESSS). Qc : INESSS; 58 p. Disponible au : https: //www. inesss. qc. ca/fileadmin/doc/INESSS/Rapports/Traitement/INESSS_Rapport_RS_probiotiques. pdf • Skokovic‐Sunjic D. (2019 th edition) Clinical Guide to Probiotic Products available in Canada [Internet]. AEProbio. [cité le 4 mai 2019]. Disponible au : http: //www. probioticchart. ca/PBCAdult. Health. html? utm_source=adult_ind&utm_medium=civ&utm_campa ign=CDN_CHART • Evans, M. , Salewski, R. P. , Christman, M. C. , Girard, S. A. , & Tompkins, T. A. (2016). Effectiveness of Lactobacillus helveticus and Lactobacillus rhamnosus for the management of antibiotic‐associated diarrhoea in healthy adults: a randomised, double‐blind, placebo‐controlled trial. British journal of Nutrition, 116(1), 94 ‐ 103. • Chatterjee, S. , Kar, P. , Das, T. , Ray, S. , Gangulyt, S. , Rajendiran, C. , & Mitra, M. (2013). Randomised placebo‐ controlled double blind multicentric trial on efficacy and safety of Lactobacillus acidophilus LA‐ 5 and Bifidobacterium BB‐ 12 for prevention of antibiotic‐associated diarrhoea. J Assoc Physicians India, 61(10), 708 ‐ 712.

Références • Kabbani, T. A. , Pallav, K. , Dowd, S. E. , Villafuerte‐Galvez, J. , Vanga, R. R. , Castillo, N. E. , . . . & Kelly, C. P. (2017). Prospective randomized controlled study on the effects of Saccharomyces boulardii CNCM I‐ 745 and amoxicillin‐clavulanate or the combination on the gut microbiota of healthy volunteers. Gut microbes, 8(1), 17‐ 32. • Ouwehand, A. C. , Dong. Lian, C. , Weijian, X. , Stewart, M. , Ni, J. , Stewart, T. , & Miller, L. E. (2014). Probiotics reduce symptoms of antibiotic use in a hospital setting: a randomized dose response study. Vaccine, 32(4), 458‐ 463. • Jafarnejad, S. , Shab‐Bidar, S. , Speakman, J. R. , Parastui, K. , Daneshi‐Maskooni, M. , & Djafarian, K. (2016). Probiotics Reduce the Risk of Antibiotic‐Associated Diarrhea in Adults (18– 64 Years) but Not the Elderly (> 65 Years) A Meta‐Analysis. Nutrition in Clinical Practice, 31(4), 502‐ 513. • Szajewska, H. , & Kołodziej, M. (2015). Systematic review with meta‐analysis: Saccharomyces boulardii in the prevention of antibiotic‐associated diarrhoea. Alimentary pharmacology & therapeutics, 42(7), 793‐ 801. • Pattani, R. , Palda, V. A. , Hwang, S. W. , & Shah, P. S. (2013). Probiotics for the prevention of antibiotic‐associated diarrhea and Clostridium difficile infection among hospitalized patients: systematic review and meta‐analysis. Open Medicine, 7(2), e 56.
- Slides: 23