Immunological aspects of pregnancy Isabelle Pellegrin VIROTEAMSeptembre 2017

Immunological aspects of pregnancy Isabelle Pellegrin VIROTEAM-Septembre 2017

Immunology of pregnancy The host–graft model: an outdated concept. Comparison of the immunological state of pregnancy to an immunosuppressed host –graft model (semi-allograft: foreign « non-self » fetus) ü « The successful implantation of the blastocyst and its further development into a growing fetus occur as a result of constant suppression of the maternal immune system » (foreign paternal proteins) ü “the presence of immune cells at the maternal–fetal interface represents an immune response that is directed against the semi-allogeneic fetus”. Concepts in transplant immunology were applied to pregnancy Pregnancy complications: therapeutic approaches used to sustain immunosuppression to promote organ transplantation The immune response at the maternal–fetal interface is instead supports the reception, establishment and growth of the implanting blastocyst
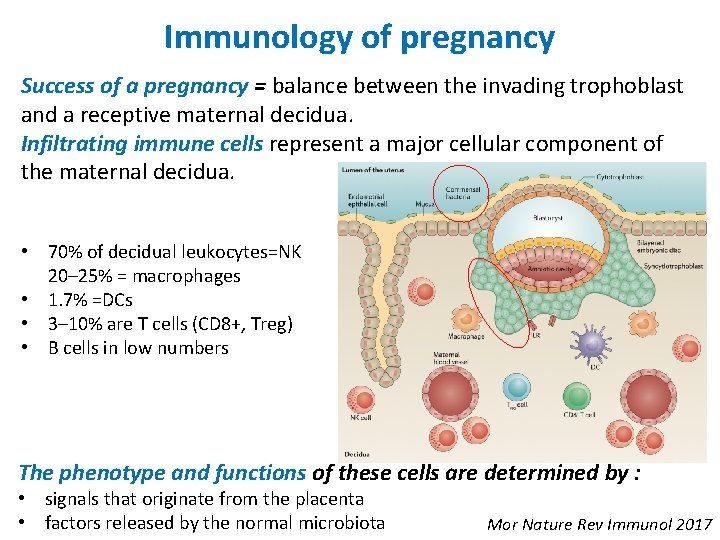
Immunology of pregnancy Success of a pregnancy = balance between the invading trophoblast and a receptive maternal decidua. Infiltrating immune cells represent a major cellular component of the maternal decidua. • 70% of decidual leukocytes=NK 20– 25% = macrophages • 1. 7% =DCs • 3– 10% are T cells (CD 8+, Treg) • B cells in low numbers The phenotype and functions of these cells are determined by : • signals that originate from the placenta • factors released by the normal microbiota Mor Nature Rev Immunol 2017

Immunology of pregnancy Immune cells are not recruited to the decidua as a response to a ‘foreign’ or ‘non-self ’ fetus, but instead are actively and specifically recruited to facilitate proper implantation and promote a successful pregnancy. Specific deletion of decidual NK cells leads to poor endometrial vascularity and impedes trophoblast invasion Hanna Nature Med 2006 Specific deletion of decidual DCs results in improper decidual formation and poor endometrial vascularity Birnberg Am J Reprod Immunol 2007
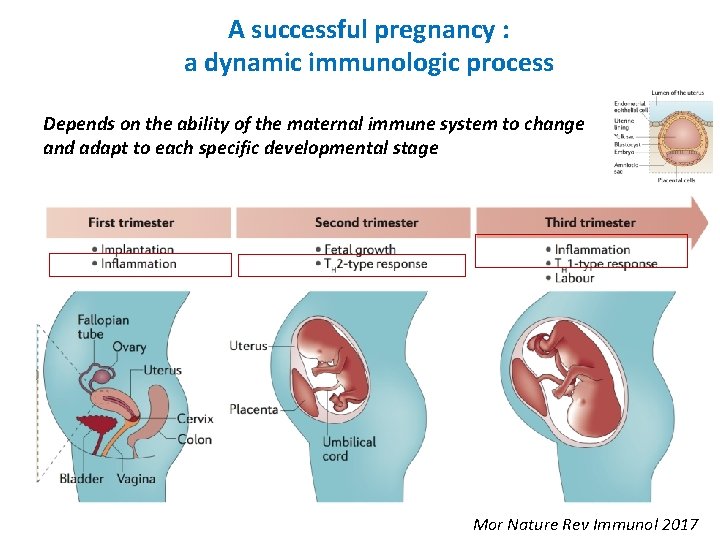
A successful pregnancy : a dynamic immunologic process Depends on the ability of the maternal immune system to change and adapt to each specific developmental stage Mor Nature Rev Immunol 2017
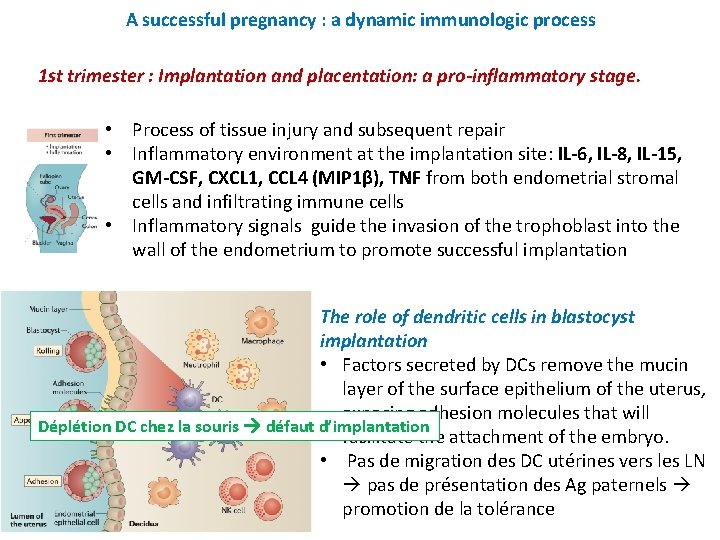
A successful pregnancy : a dynamic immunologic process 1 st trimester : Implantation and placentation: a pro-inflammatory stage. • Process of tissue injury and subsequent repair • Inflammatory environment at the implantation site: IL-6, IL-8, IL-15, GM-CSF, CXCL 1, CCL 4 (MIP 1β), TNF from both endometrial stromal cells and infiltrating immune cells • Inflammatory signals guide the invasion of the trophoblast into the wall of the endometrium to promote successful implantation The role of dendritic cells in blastocyst implantation • Factors secreted by DCs remove the mucin layer of the surface epithelium of the uterus, exposing adhesion molecules that will Déplétion DC chez la souris défaut d’implantation facilitate the attachment of the embryo. • Pas de migration des DC utérines vers les LN pas de présentation des Ag paternels promotion de la tolérance
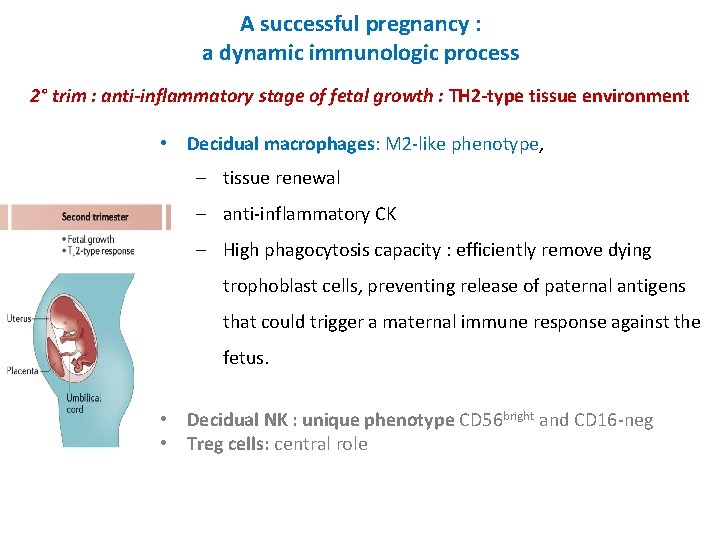
A successful pregnancy : a dynamic immunologic process 2° trim : anti-inflammatory stage of fetal growth : TH 2 -type tissue environment • Decidual macrophages: M 2 -like phenotype, ‒ tissue renewal ‒ anti-inflammatory CK ‒ High phagocytosis capacity : efficiently remove dying trophoblast cells, preventing release of paternal antigens that could trigger a maternal immune response against the fetus. • Decidual NK : unique phenotype CD 56 bright and CD 16 -neg • Treg cells: central role
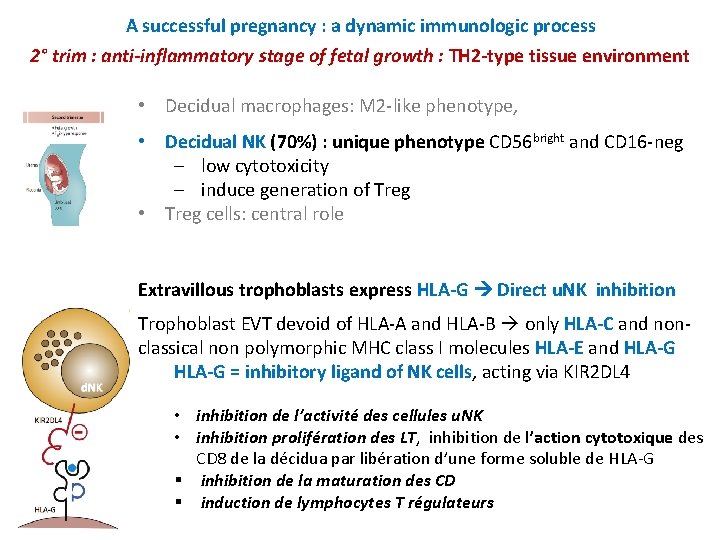
A successful pregnancy : a dynamic immunologic process 2° trim : anti-inflammatory stage of fetal growth : TH 2 -type tissue environment • Decidual macrophages: M 2 -like phenotype, • Decidual NK (70%) : unique phenotype CD 56 bright and CD 16 -neg ‒ low cytotoxicity ‒ induce generation of Treg • Treg cells: central role Extravillous trophoblasts express HLA-G Direct u. NK inhibition Trophoblast EVT devoid of HLA-A and HLA-B only HLA-C and nonclassical non polymorphic MHC class I molecules HLA-E and HLA-G = inhibitory ligand of NK cells, acting via KIR 2 DL 4 • inhibition de l’activité des cellules u. NK • inhibition prolifération des LT, inhibition de l’action cytotoxique des CD 8 de la décidua par libération d’une forme soluble de HLA-G § inhibition de la maturation des CD § induction de lymphocytes T régulateurs
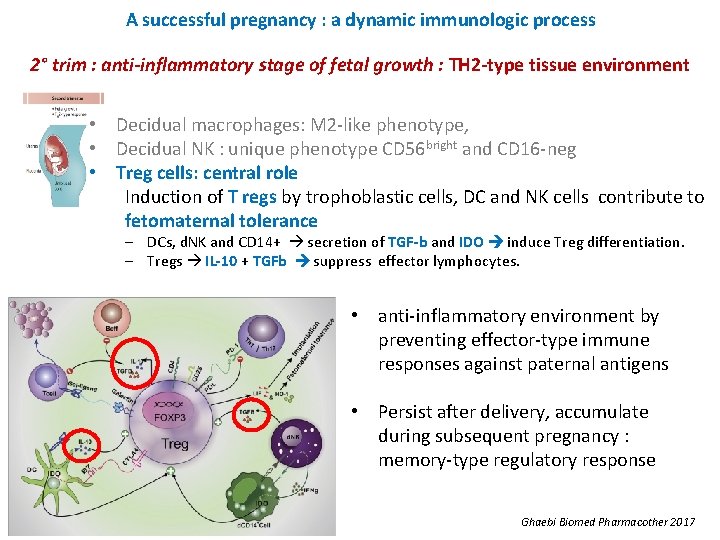
A successful pregnancy : a dynamic immunologic process 2° trim : anti-inflammatory stage of fetal growth : TH 2 -type tissue environment • Decidual macrophages: M 2 -like phenotype, • Decidual NK : unique phenotype CD 56 bright and CD 16 -neg • Treg cells: central role Induction of T regs by trophoblastic cells, DC and NK cells contribute to fetomaternal tolerance ‒ DCs, d. NK and CD 14+ secretion of TGF-b and IDO induce Treg differentiation. ‒ Tregs IL-10 + TGFb suppress effector lymphocytes. • anti-inflammatory environment by preventing effector-type immune responses against paternal antigens • Persist after delivery, accumulate during subsequent pregnancy : memory-type regulatory response Ghaebi Biomed Pharmacother 2017

A successful pregnancy : a dynamic immunologic process 2 nd trim : An anti-inflammatory stage of fetal growth : TH 2 -type tissue environment • Longest period of the pregnancy (W 13 to W 27) • Any ongoing pro-inflammatory signals at this stage can lead to miscarriage and any ensuing pro-inflammatory insult — such as infection — can lead to preterm birth • Treg ‒ Déficit en Fox. P 3 ds tissu endométrial (facteur de transcription Treg) infertilité ‒ Déficit en Treg avortement spontané ‒ Altération Ratio Treg/TH 17 avortement spontané, accouchement prématuré, pré-éclampsie. . .

A successful pregnancy : a dynamic immunologic process 3 rd trimester : A pro-inflammatory switch necessary for labour. . . Once the fetus has completed its development… • The pro-inflammatory nuclear factor-κB (NF-κB) signalling pathway is crucial for initiate labour and delivery • The influx of immune cells into the myometrium is crucial in order to promote the contraction of the uterus, delivery of the baby and separation of the placenta. • Induction : Toll-like receptor 4 (TLR 4) activation by ligands ‒ Surfactant protein A (a protein secreted by the fetal lung) ‒ DAMPs, such as high mobility group box 1 (HMGB 1), present in high levels towards the end of the pregnancy • The normal milieu is created in part by the normal microbiota and can be disrupted by external stimuli such as infections. Immunology during pregnancy is dynamic, and definitely not suppressed.

A successful pregnancy : a dynamic immunologic process A clinically silent viral infection can markedly change the immunemodulated and receptive maternal–fetal interface • need for better detection, treatment, prevention of viral infections. • better pregnancy outcomes • positively affect postnatal development, as viral infections and the ensuing inflammation have been implicated in mental health issues and immune diseases such as allergies and asthma. The recent Zika virus outbreak and its teratogenic effects on brain development may just be the ‘tip of the iceberg’ in terms of our awareness of the potential effects of viral infections during pregnancy on fetal development.

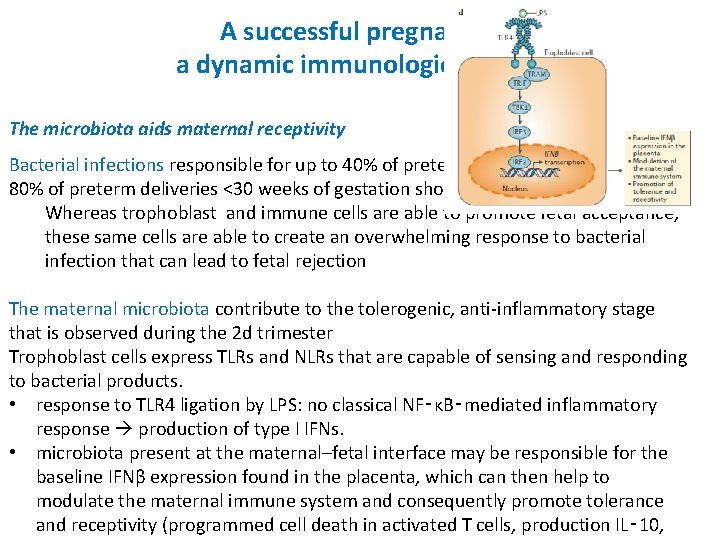
A successful pregnancy : a dynamic immunologic process The microbiota aids maternal receptivity Bacterial infections responsible for up to 40% of preterm birth cases. 80% of preterm deliveries <30 weeks of gestation show evidence of infection. Whereas trophoblast and immune cells are able to promote fetal acceptance, these same cells are able to create an overwhelming response to bacterial infection that can lead to fetal rejection The maternal microbiota contribute to the tolerogenic, anti-inflammatory stage that is observed during the 2 d trimester Trophoblast cells express TLRs and NLRs that are capable of sensing and responding to bacterial products. • response to TLR 4 ligation by LPS: no classical NF‑κB‑mediated inflammatory response production of type I IFNs. • microbiota present at the maternal–fetal interface may be responsible for the baseline IFNβ expression found in the placenta, which can then help to modulate the maternal immune system and consequently promote tolerance and receptivity (programmed cell death in activated T cells, production IL‑ 10,
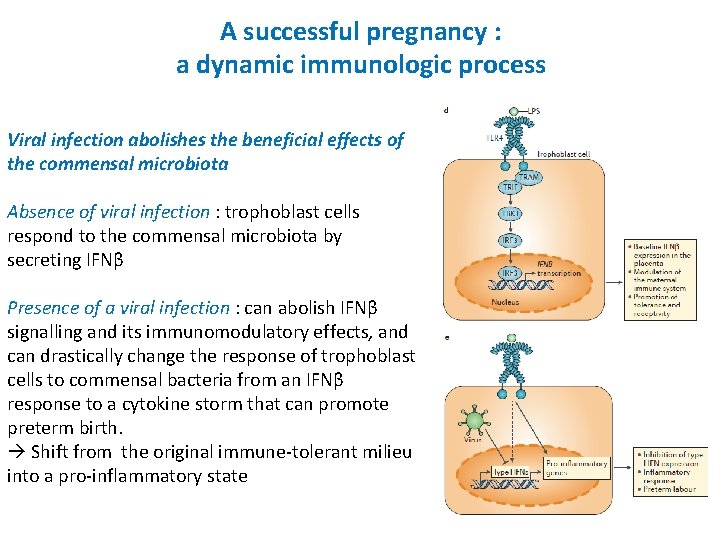
A successful pregnancy : a dynamic immunologic process Viral infection abolishes the beneficial effects of the commensal microbiota Absence of viral infection : trophoblast cells respond to the commensal microbiota by secreting IFNβ Presence of a viral infection : can abolish IFNβ signalling and its immunomodulatory effects, and can drastically change the response of trophoblast cells to commensal bacteria from an IFNβ response to a cytokine storm that can promote preterm birth. Shift from the original immune-tolerant milieu into a pro-inflammatory state
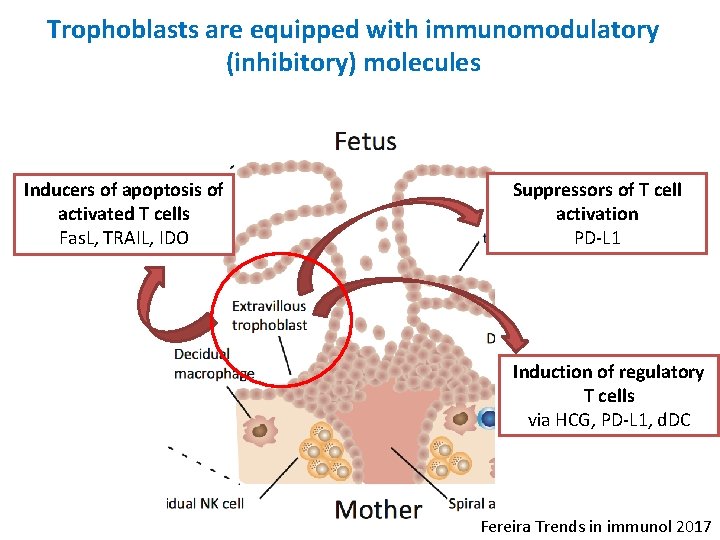
Trophoblasts are equipped with immunomodulatory (inhibitory) molecules Inducers of apoptosis of activated T cells Fas. L, TRAIL, IDO Suppressors of T cell activation PD-L 1 Induction of regulatory T cells via HCG, PD-L 1, d. DC Fereira Trends in immunol 2017
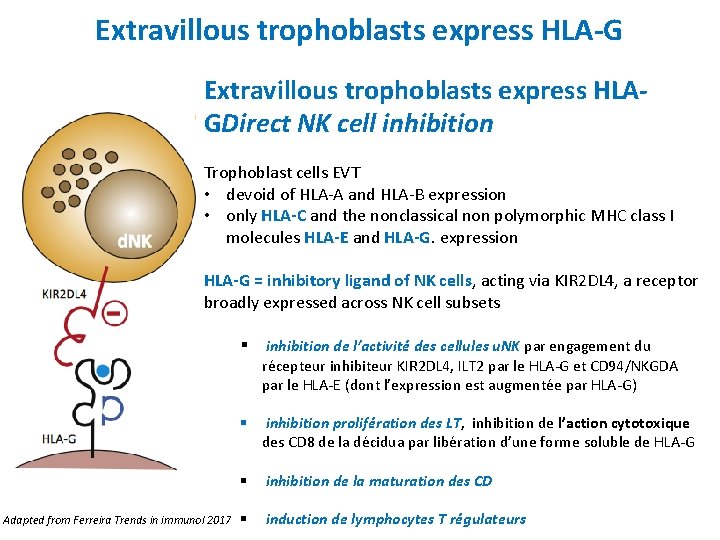
Extravillous trophoblasts express HLA-G Extravillous trophoblasts express HLAGDirect NK cell inhibition Trophoblast cells EVT • devoid of HLA-A and HLA-B expression • only HLA-C and the nonclassical non polymorphic MHC class I molecules HLA-E and HLA-G. expression HLA-G = inhibitory ligand of NK cells, acting via KIR 2 DL 4, a receptor broadly expressed across NK cell subsets § inhibition de l’activité des cellules u. NK par engagement du récepteur inhibiteur KIR 2 DL 4, ILT 2 par le HLA-G et CD 94/NKGDA par le HLA-E (dont l’expression est augmentée par HLA-G) § inhibition prolifération des LT, inhibition de l’action cytotoxique des CD 8 de la décidua par libération d’une forme soluble de HLA-G § inhibition de la maturation des CD Adapted from Ferreira Trends in immunol 2017 § induction de lymphocytes T régulateurs
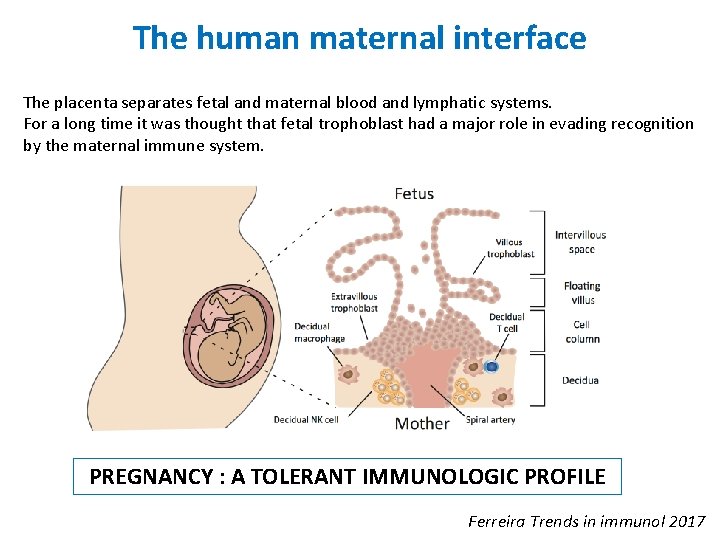
The human maternal interface The placenta separates fetal and maternal blood and lymphatic systems. For a long time it was thought that fetal trophoblast had a major role in evading recognition by the maternal immune system. PREGNANCY : A TOLERANT IMMUNOLOGIC PROFILE Ferreira Trends in immunol 2017

Immunology of pregnancy The role of dendritic cells in blastocyst implantation Factors secreted by DCs remove the mucin layer of the surface epithelium of the uterus, exposing adhesion molecules that will facilitate the attachment of the embryo. Inflammatory signals guide the invasion of the trophoblast into the wall of the endometrium to promote successful implantation • • • Transfer of stored adhesion molecules to the cell surface of epithelial cells at the uterus lumen Expression of new adhesion molecules Removal of the pre-existing layer of mucins present at the luminal surface epithelium of the uterus, as these mucins prevent blastocyst adhesion Mor Nature Rev Immunol 2017
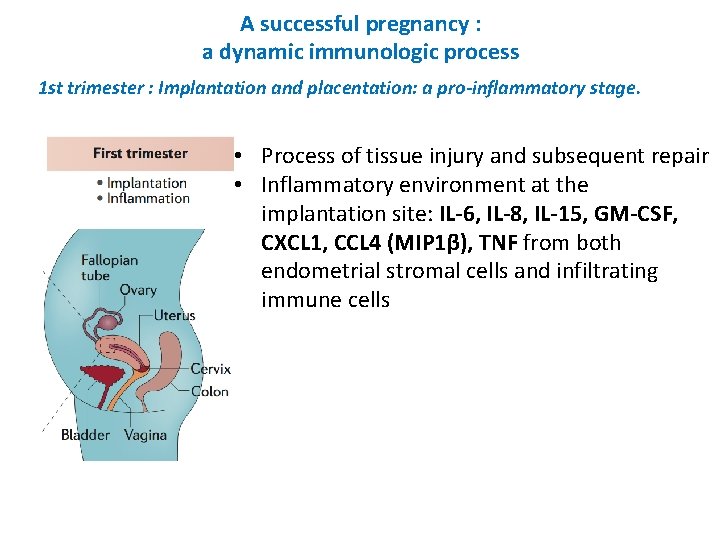
A successful pregnancy : a dynamic immunologic process 1 st trimester : Implantation and placentation: a pro-inflammatory stage. • Process of tissue injury and subsequent repair • Inflammatory environment at the implantation site: IL-6, IL-8, IL-15, GM-CSF, CXCL 1, CCL 4 (MIP 1β), TNF from both endometrial stromal cells and infiltrating immune cells
Chronic Histiocytic Intervillositis : immunological patterns ?
Chronic Histiocytic Intervillositis : immunological patterns - Rare disease - Physiopathology poorly understood - No treatment - Similar to placental histopathological lesions observed during CMV or malaria - Association with underlying autoimmune disorders - High percentage of recurrence
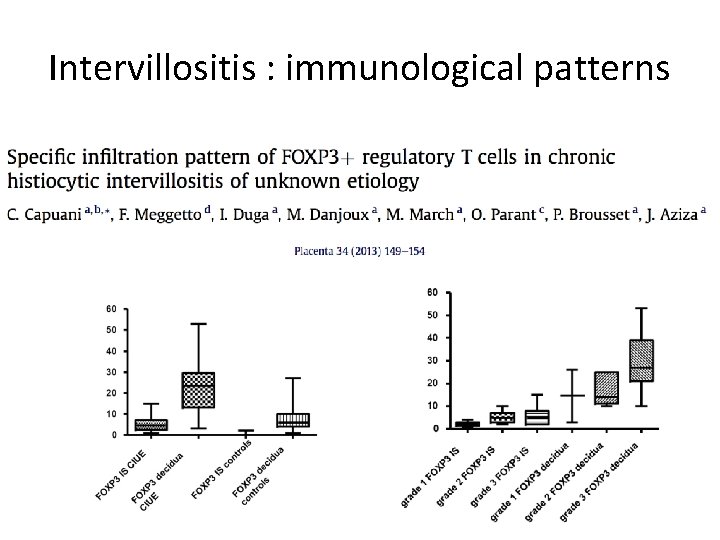
Intervillositis : immunological patterns
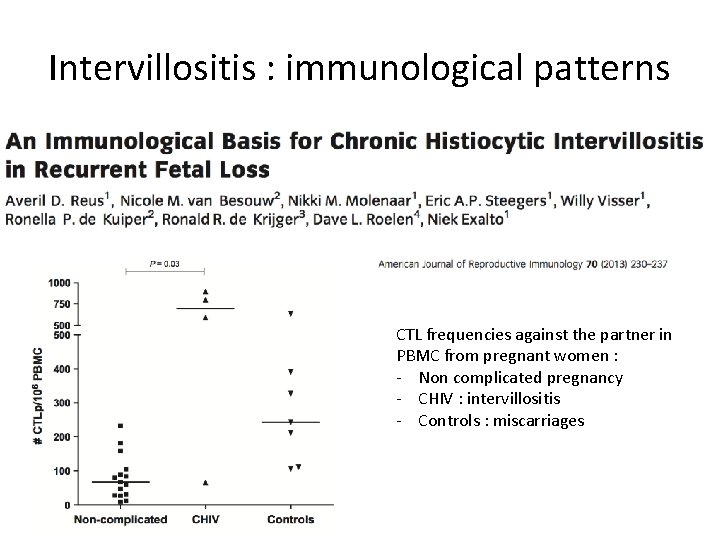
Intervillositis : immunological patterns CTL frequencies against the partner in PBMC from pregnant women : - Non complicated pregnancy - CHIV : intervillositis - Controls : miscarriages

Intervillositis : immunological patterns
Intervillositis : immunological patterns
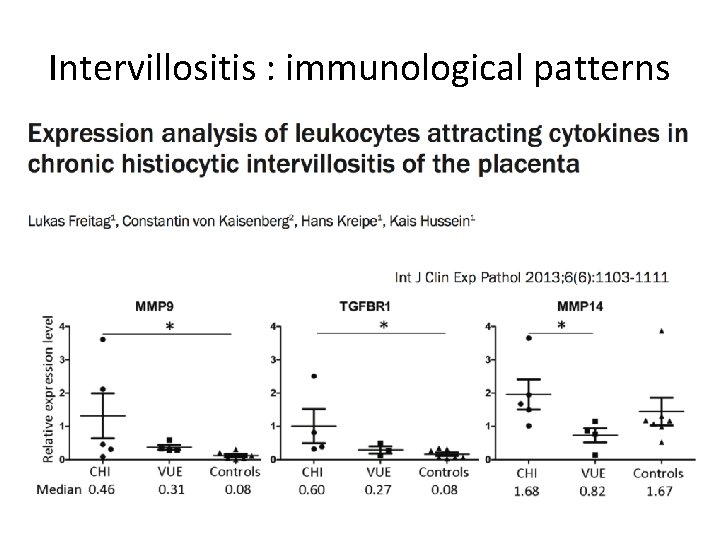
Intervillositis : immunological patterns
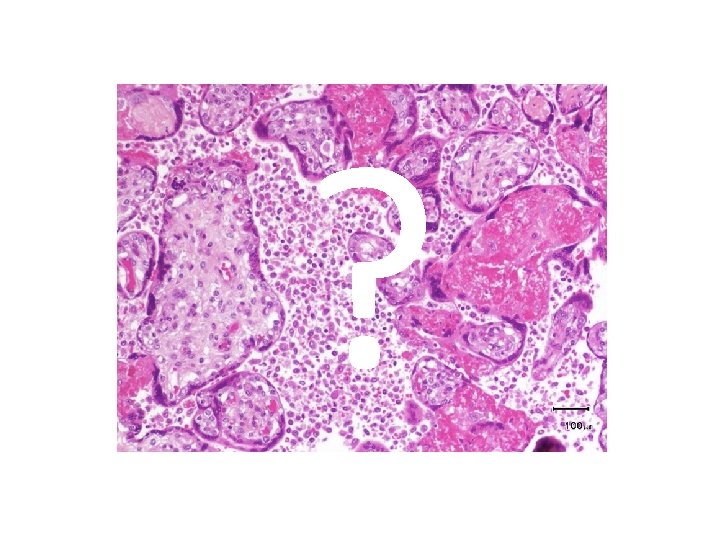

I- IMMUNOLOGIE DE LA GROSSESSE

PARADOXE IMMUNOLOGIQUE DE LA GROSSESSE Embryon : génome pour moitié d’origine paternelle : « greffe semi-allogénique » Comment expliquer la préservation du fœtus? Théorie de Medawar (1953, co-lauréat du prix Nobel médecine en 1960) : 4 grandes hypothèses 1 - utérus = lieu « immunologiquement privilégié » : barrière physique séparant fœtus du système immunitaire (SI) de la mère 2 - fœtus = « immunologiquement neutre » : immaturité antigénique du fœtus n’induisant pas de réponse du SI maternel 3 - absence de réactivité « globale » du SI maternel sorte d’immuno-dépression 4 - la grossesse fait intervenir des mécanismes actifs de régulation le

Que reste-t-il des hypothèses de Medawar? gestation q L’utérus n’est pas un site « immunologiquement privilégié » : - contact du trophoblaste avec le SI de la mère - des cellules fœtales entrent dans la circulation maternelle dès la 4° semaine de q Le SI maternel reconnait les Ag fœtaux : - Ac cytotoxiques dirigés contre les allo. Ag fœtaux (Ac anti-HLA de classe I primipare et 75% multipare) - Présence de lymphocytes T CD 8+ spécifiques d’Ag fœtaux (HLA) 15%, q Le SI maternel est bien réactif : la défense anti-infectieuse de la mère est normale q NECESSITE DE L’INDUCTION D’UNE TOLERANCE MATERNO-FŒTALE : « mécanismes actifs de régulation » selon Medawar

TOLERANCE MATERNO-FŒTALE Mécanismes actifs aux interfaces materno-fœtales : • de protection du fœtus vis-à-vis de la réponse immunitaire de la mère : mettre en place des barrières physiques, réduire l’antigénicité • d’inhibition de l’action de la réponse immunitaire de la mère quand elle a lieu • de tolérance materno-fœtale active nécessitant la reconnaissance immunologique du fœtus Meilleure compréhension de ces mécanismes : • traitement infertilité ou des anomalies d’implantation, de placentation.
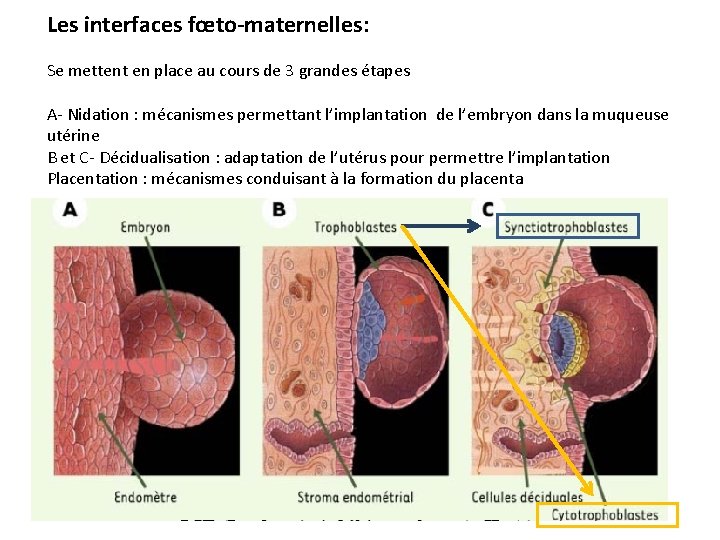
Les interfaces fœto-maternelles: Se mettent en place au cours de 3 grandes étapes A- Nidation : mécanismes permettant l’implantation de l’embryon dans la muqueuse utérine B et C- Décidualisation : adaptation de l’utérus pour permettre l’implantation Placentation : mécanismes conduisant à la formation du placenta
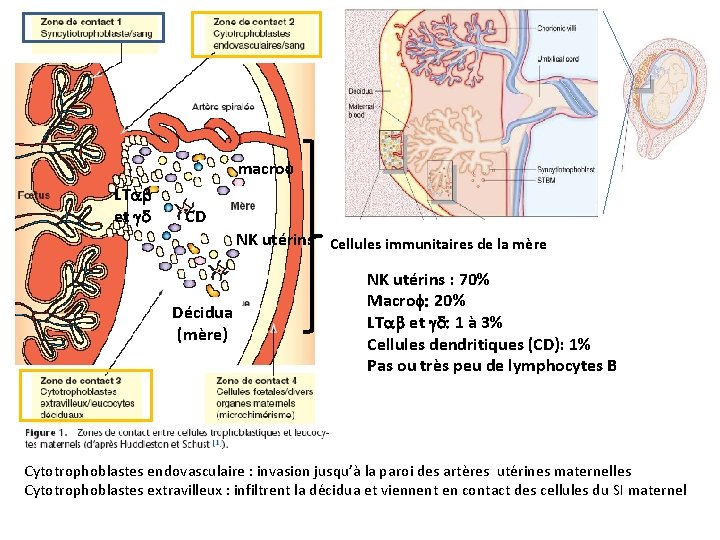
macrof LTab et gd CD NK utérins Cellules immunitaires de la mère Décidua (mère) NK utérins : 70% Macrof: 20% LTab et gd: 1 à 3% Cellules dendritiques (CD): 1% Pas ou très peu de lymphocytes B Cytotrophoblastes endovasculaire : invasion jusqu’à la paroi des artères utérines maternelles Cytotrophoblastes extravilleux : infiltrent la décidua et viennent en contact des cellules du SI maternel

Du côté maternel : importance des cellules utérines NK (u. NK) • 70% des cellules immunitaires maternelles dans la décidua Rôle? Modèle murin déficient en cellules u. NK → placenta hypotrophes et altérations vasculaires ++ • Importance de la sécrétion de cytokines et facteurs de croissances par les u. NK - LIF (Leukemia inhibitory Factor) indispensables à l’implantation - IFN-g : invasion et de la croissance trophoblastique - angiopoïétine : vascularisation (artères spiralées) • A leur surface sont exprimés de nombreux récepteurs inhibiteurs: KIR (Killer cell Inhibitory Receptor) qui les empêchent de s’activer et de lyser leur cible (exple : CD 94/NKG 2 A, KIR 2 DL 4, ILT 2 ) • Les u. NK sécrétent des molécules capables d’interférer avec l’activation d’autres cellules immunitaires (perturbation de la synapse immunologique T-CD) : - galectine-1 - glycodéline A
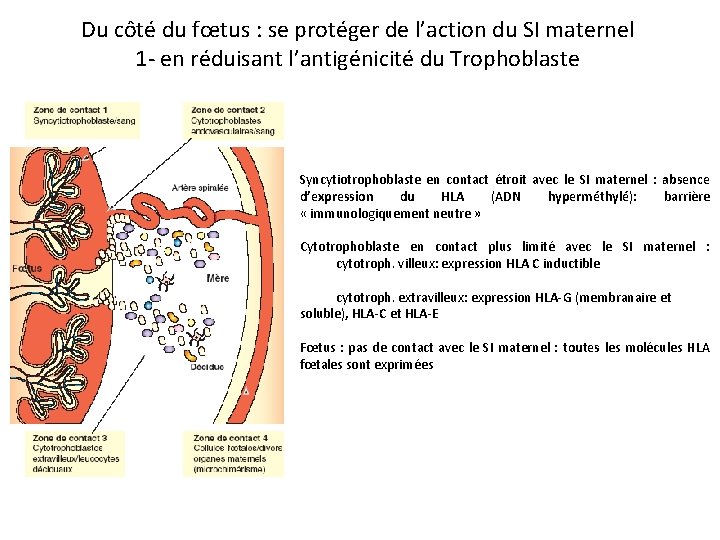
Du côté du fœtus : se protéger de l’action du SI maternel 1 - en réduisant l’antigénicité du Trophoblaste Syncytiotrophoblaste en contact étroit avec le SI maternel : absence d’expression du HLA (ADN hyperméthylé): barrière « immunologiquement neutre » Cytotrophoblaste en contact plus limité avec le SI maternel : cytotroph. villeux: expression HLA C inductible cytotroph. extravilleux: expression HLA-G (membranaire et soluble), HLA-C et HLA-E Fœtus : pas de contact avec le SI maternel : toutes les molécules HLA fœtales sont exprimées
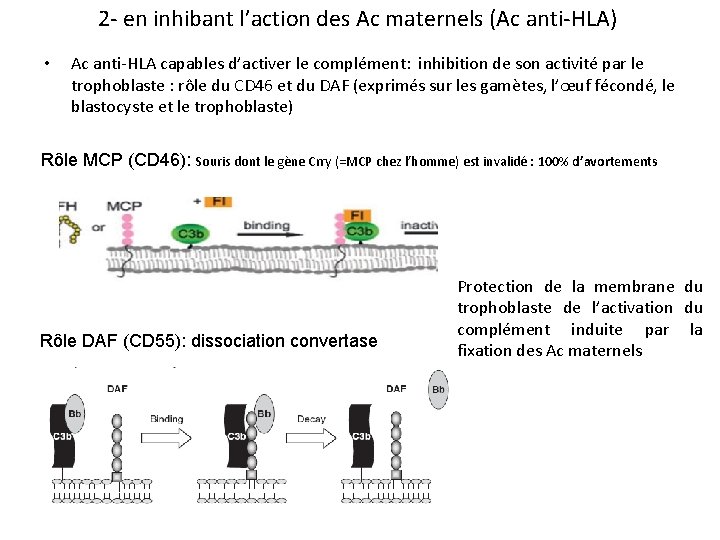
2 - en inhibant l’action des Ac maternels (Ac anti-HLA) • Ac anti-HLA capables d’activer le complément: inhibition de son activité par le trophoblaste : rôle du CD 46 et du DAF (exprimés sur les gamètes, l’œuf fécondé, le blastocyste et le trophoblaste) Rôle MCP (CD 46): Souris dont le gène Crry (=MCP chez l’homme) est invalidé : 100% d’avortements Rôle DAF (CD 55): dissociation convertase Protection de la membrane du trophoblaste de l’activation du complément induite par la fixation des Ac maternels
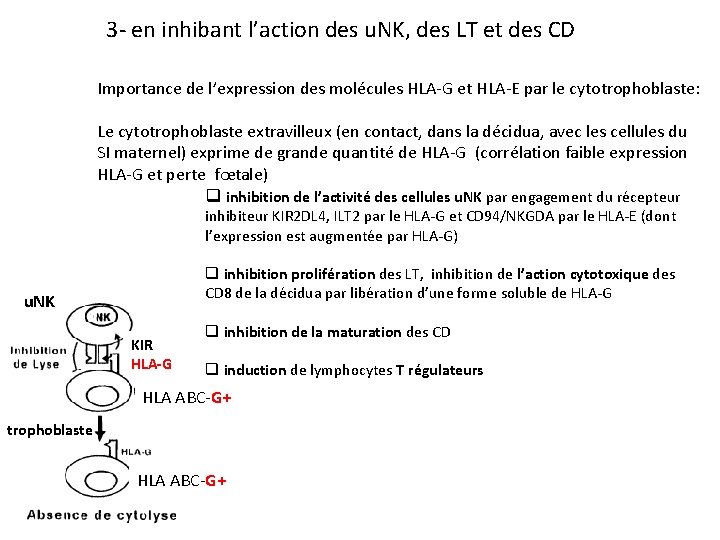
3 - en inhibant l’action des u. NK, des LT et des CD Importance de l’expression des molécules HLA-G et HLA-E par le cytotrophoblaste: Le cytotrophoblaste extravilleux (en contact, dans la décidua, avec les cellules du SI maternel) exprime de grande quantité de HLA-G (corrélation faible expression HLA-G et perte fœtale) q inhibition de l’activité des cellules u. NK par engagement du récepteur inhibiteur KIR 2 DL 4, ILT 2 par le HLA-G et CD 94/NKGDA par le HLA-E (dont l’expression est augmentée par HLA-G) q inhibition prolifération des LT, inhibition de l’action cytotoxique des CD 8 de la décidua par libération d’une forme soluble de HLA-G u. NK KIR HLA-G q inhibition de la maturation des CD q induction de lymphocytes T régulateurs HLA ABC-G+ trophoblaste HLA ABC-G+
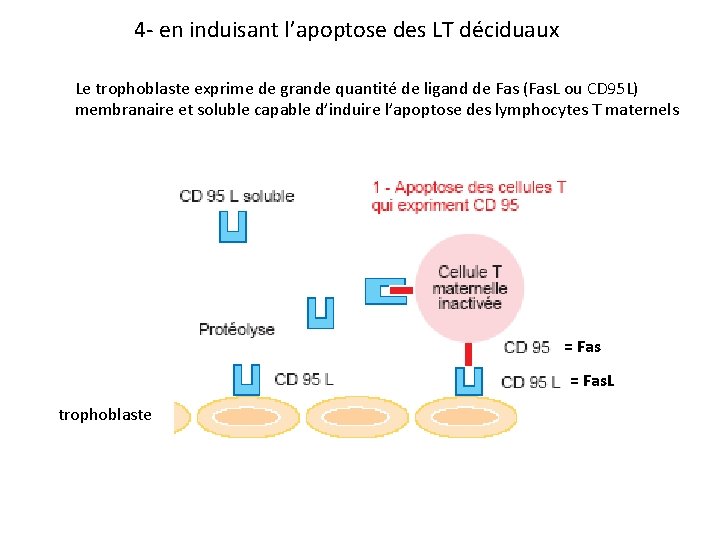
4 - en induisant l’apoptose des LT déciduaux Le trophoblaste exprime de grande quantité de ligand de Fas (Fas. L ou CD 95 L) membranaire et soluble capable d’induire l’apoptose des lymphocytes T maternels = Fas. L trophoblaste
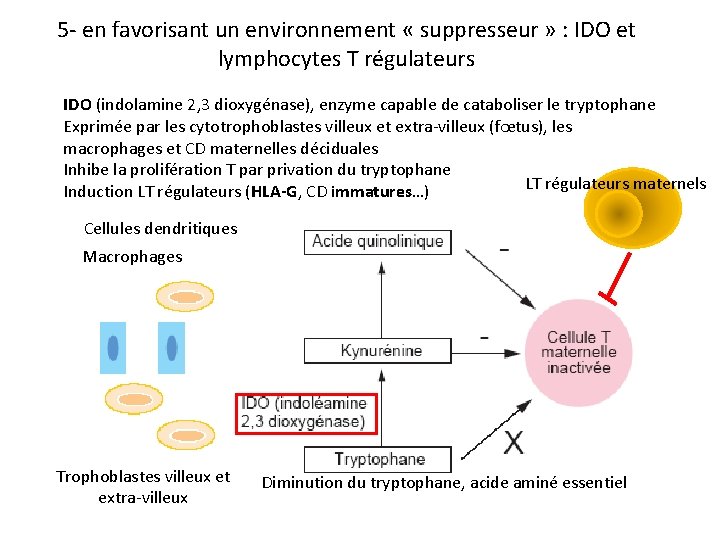
5 - en favorisant un environnement « suppresseur » : IDO et lymphocytes T régulateurs IDO (indolamine 2, 3 dioxygénase), enzyme capable de cataboliser le tryptophane Exprimée par les cytotrophoblastes villeux et extra-villeux (fœtus), les macrophages et CD maternelles déciduales Inhibe la prolifération T par privation du tryptophane LT régulateurs maternels Induction LT régulateurs (HLA-G, CD immatures…) Cellules dendritiques Macrophages Trophoblastes villeux et extra-villeux Diminution du tryptophane, acide aminé essentiel

Pregnancy is not only characterized by a tolerant immunologic profile Early pregnancy is characterized by the presence of both innate and adaptive immune cells : - natural killer (NK) cells (70 %) Macrophages (20 -25 %), Dendritic cells (DCs) (1, 7 %), T cells ( 3 -10 % ) : § CD 8+ T cells § regulatory T (Treg) cells
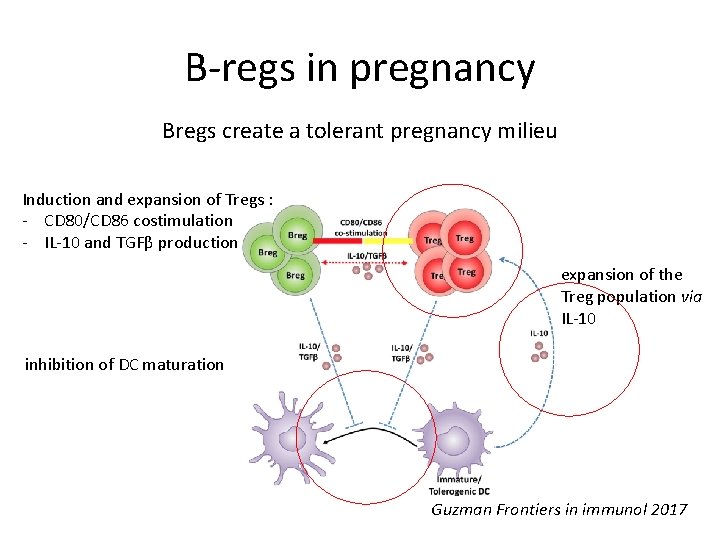
B-regs in pregnancy Bregs create a tolerant pregnancy milieu Induction and expansion of Tregs : - CD 80/CD 86 costimulation - IL-10 and TGFβ production expansion of the Treg population via IL-10 inhibition of DC maturation Guzman Frontiers in immunol 2017
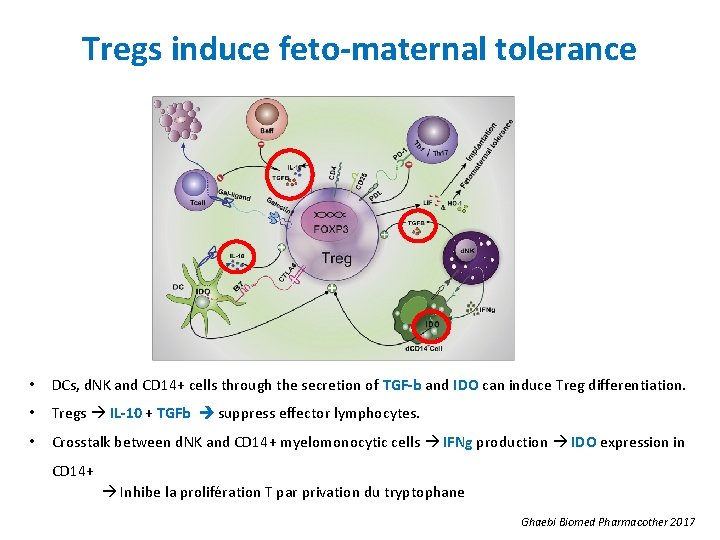
Tregs induce feto-maternal tolerance • DCs, d. NK and CD 14+ cells through the secretion of TGF-b and IDO can induce Treg differentiation. • Tregs IL-10 + TGFb suppress effector lymphocytes. • Crosstalk between d. NK and CD 14+ myelomonocytic cells IFNg production IDO expression in CD 14+ Inhibe la prolifération T par privation du tryptophane Ghaebi Biomed Pharmacother 2017
- Slides: 43