Imagerie du vieillissement crbral O Naggara 1 C

Imagerie du vieillissement cérébral O. Naggara (1), C. Delmaire (2), S. Rodrigo (1), F Charbonneau (1, 2), C Oppenheim (1), JP Pruvo (2), JF Meder (1) 2008 1 Service d’imagerie morphologique et fonctionnelle, CH Sainte-Anne, Paris 2 Service de Neuroradiologie, Hopital Salengro, Lille
Pourquoi étudier le vieillissement cérébral ? • • Un Français sur 5 en 2007 a plus de 60 ans En 2050, un Français sur 3 aura plus de 60 ans 1 million de patients atteints de démence Maladie d’Alzheimer > 60% des démences

Objectifs • Décrire les aspects habituels du vieillissement cérébral en IRM ou « cet aspect est-t’il normal ? » • Définir la place de l’imagerie dans la prise en charge des démences • Décrire l’apport de l’IRM dans l’exploration des troubles cognitifs mineurs • Décrire l’apport des nouvelles méthodes d’IRM

Quel est l’aspect du cerveau du sujet âgé « sain » ? W. Churchill Premier ministre à 81 ans « Baigneuse » P. Picasso, réalisée à 82 ans
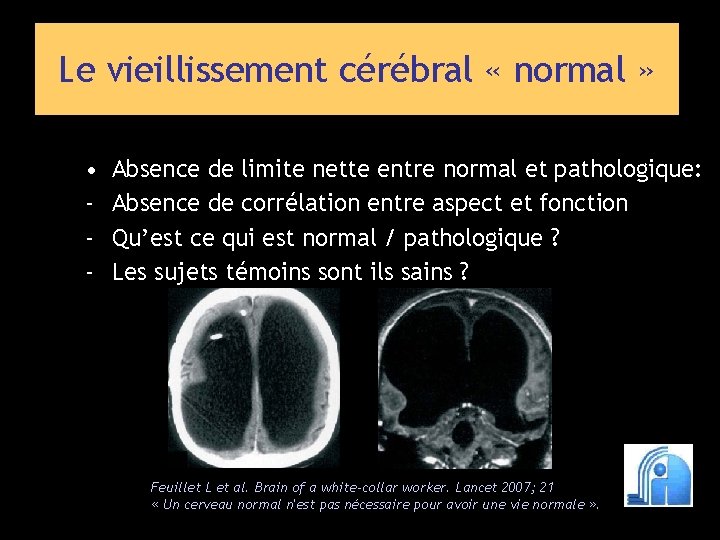
Le vieillissement cérébral « normal » • - Absence de limite nette entre normal et pathologique: Absence de corrélation entre aspect et fonction Qu’est ce qui est normal / pathologique ? Les sujets témoins sont ils sains ? Feuillet L et al. Brain of a white-collar worker. Lancet 2007; 21 « Un cerveau normal n'est pas nécessaire pour avoir une vie normale » .

Le vieillissement cérébral « normal » • Atrophie cérébrale • Dilatation des espaces de Virchow et Robin • Modifications de la substance blanche • Microsaignements intra parenchymateux • Modification de la distribution en fer et de la charge calcique des noyaux gris centraux
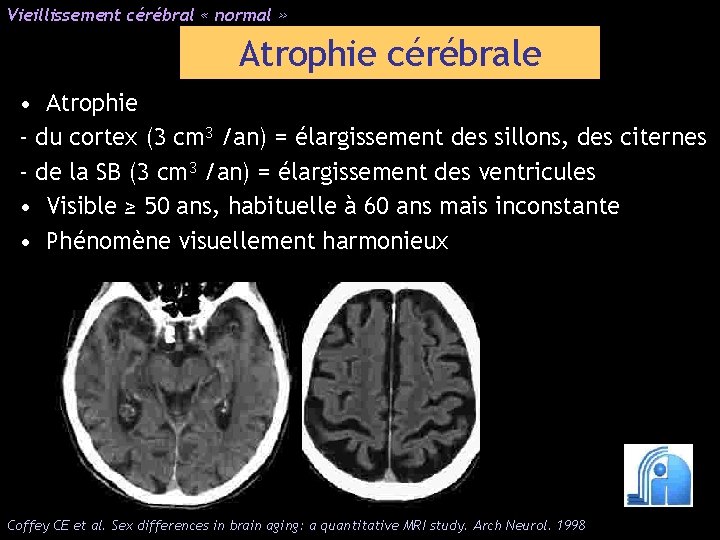
Vieillissement cérébral « normal » Atrophie cérébrale • Atrophie - du cortex (3 cm 3 /an) = élargissement des sillons, des citernes - de la SB (3 cm 3 /an) = élargissement des ventricules • Visible ≥ 50 ans, habituelle à 60 ans mais inconstante • Phénomène visuellement harmonieux Coffey CE et al. Sex differences in brain aging: a quantitative MRI study. Arch Neurol. 1998
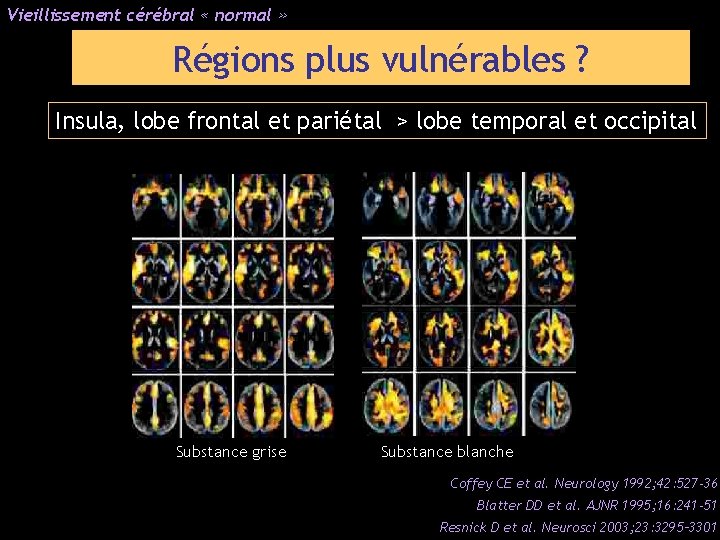
Vieillissement cérébral « normal » Régions plus vulnérables ? Insula, lobe frontal et pariétal > lobe temporal et occipital Substance grise Substance blanche Coffey CE et al. Neurology 1992; 42: 527 -36 Blatter DD et al. AJNR 1995; 16: 241 -51 Resnick D et al. Neurosci 2003; 23: 3295– 3301
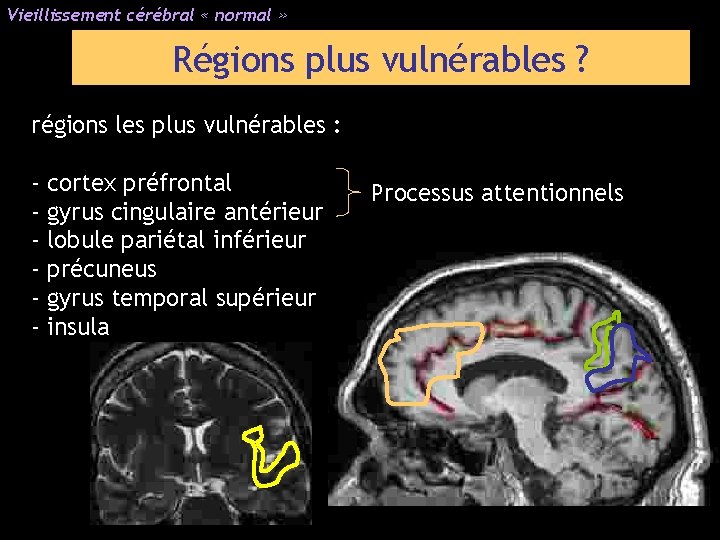
Vieillissement cérébral « normal » Régions plus vulnérables ? régions les plus vulnérables : - cortex préfrontal - gyrus cingulaire antérieur - lobule pariétal inférieur - précuneus - gyrus temporal supérieur - insula Processus attentionnels
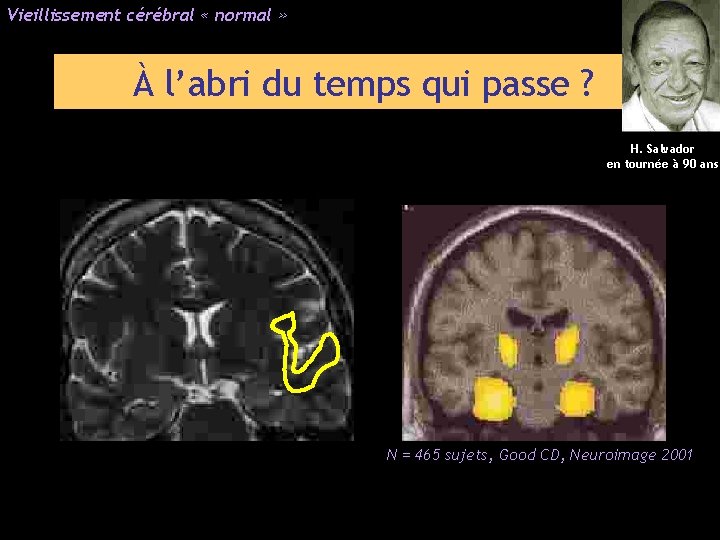
Vieillissement cérébral « normal » À l’abri du temps qui passe ? H. Salvador en tournée à 90 ans N = 465 sujets, Good CD, Neuroimage 2001
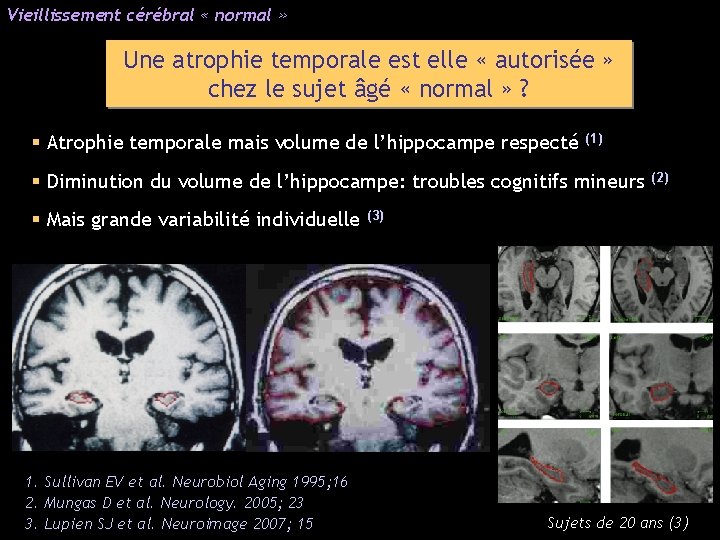
Vieillissement cérébral « normal » Une atrophie temporale est elle « autorisée » chez le sujet âgé « normal » ? § Atrophie temporale mais volume de l’hippocampe respecté (1) § Diminution du volume de l’hippocampe: troubles cognitifs mineurs § Mais grande variabilité individuelle 1. Sullivan EV et al. Neurobiol Aging 1995; 16 2. Mungas D et al. Neurology. 2005; 23 3. Lupien SJ et al. Neuroimage 2007; 15 (2) (3) Sujets de 20 ans (3)

Vieillissement cérébral « normal » Sur l’imagerie, puis je dire: « atrophie normale (ou pathologique) pour l’âge » ? • • • Prudence Atrophie du sujet dément > atrophie sujet sain Grande variabilité individuelle Absence de limite individuelle entre normal et pathologique Pas de lien entre volume et fonction !!! • Homogénéité de l’atrophie entre - SB et SG - les lobes • Peu d’atrophie temporale Coffey CE et al. Relation of education to brain size in normal aging. Implication for the reserve hypothesis. Neurology 1999 Wittelson SF et Al. Intelligence and brain size in 100 postmortem brains: sex, lateralization and age factors. Brain 2006
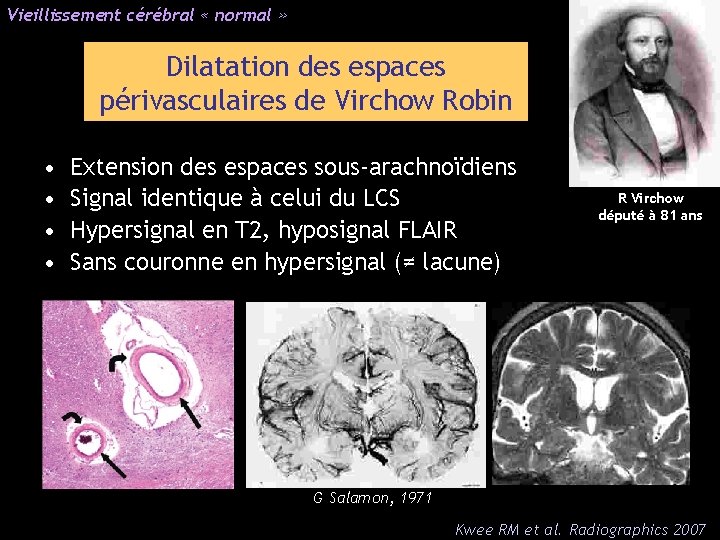
Vieillissement cérébral « normal » Dilatation des espaces périvasculaires de Virchow Robin • • Extension des espaces sous-arachnoïdiens Signal identique à celui du LCS Hypersignal en T 2, hyposignal FLAIR Sans couronne en hypersignal (≠ lacune) R Virchow député à 81 ans G Salamon, 1971 Kwee RM et al. Radiographics 2007
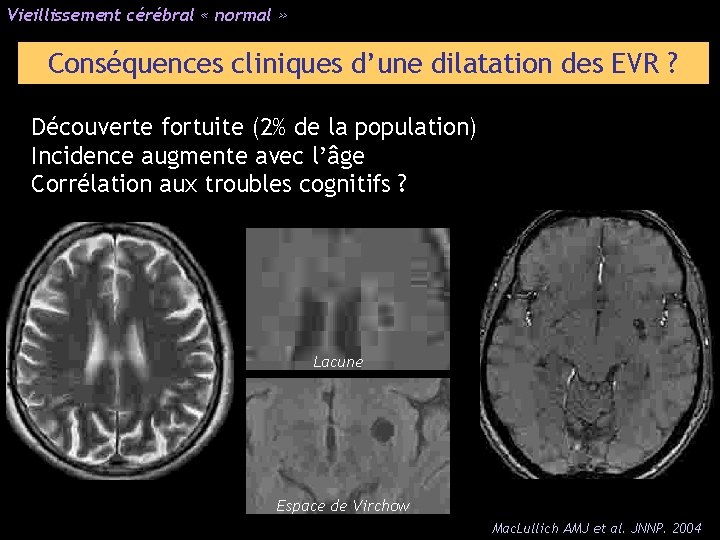
Vieillissement cérébral « normal » Conséquences cliniques d’une dilatation des EVR ? Découverte fortuite (2% de la population) Incidence augmente avec l’âge Corrélation aux troubles cognitifs ? Lacune Espace de Virchow Mac. Lullich AMJ et al. JNNP. 2004

Le vieillissement cérébral « normal » • Atrophie cérébrale • Dilatation des espaces de Virchow et Robin • Modifications de la substance blanche • Microsaignements intra parenchymateux • Modification de la distribution en fer et de la charge calcique des noyaux gris centraux
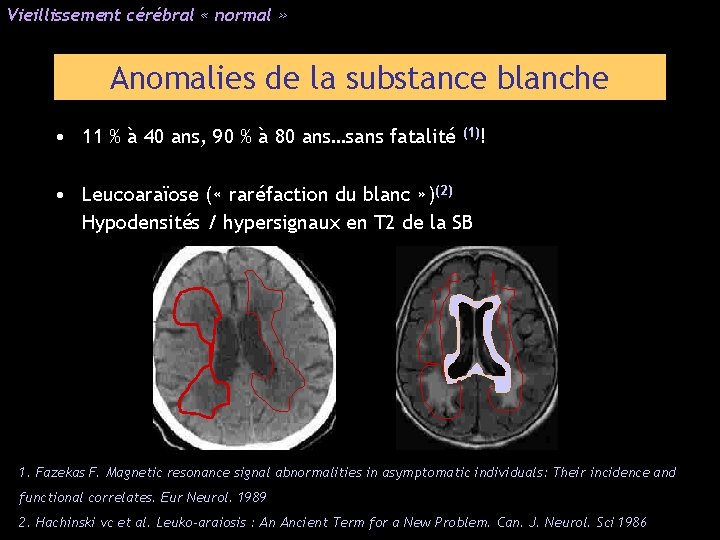
Vieillissement cérébral « normal » Anomalies de la substance blanche • 11 % à 40 ans, 90 % à 80 ans…sans fatalité (1)! • Leucoaraïose ( « raréfaction du blanc » )(2) Hypodensités / hypersignaux en T 2 de la SB 1. Fazekas F. Magnetic resonance signal abnormalities in asymptomatic individuals: Their incidence and functional correlates. Eur Neurol. 1989 2. Hachinski vc et al. Leuko-araiosis : An Ancient Term for a New Problem. Can. J. Neurol. Sci 1986
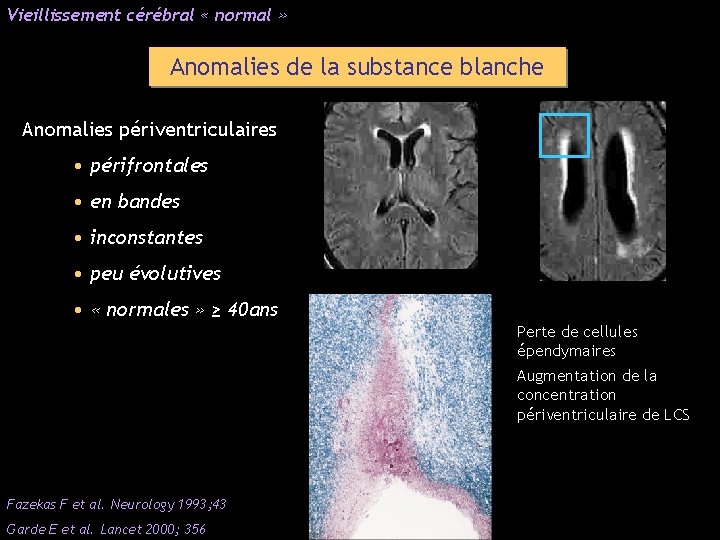
Vieillissement cérébral « normal » Anomalies de la substance blanche Anomalies périventriculaires • périfrontales • en bandes • inconstantes • peu évolutives • « normales » ≥ 40 ans Perte de cellules épendymaires Augmentation de la concentration périventriculaire de LCS Fazekas F et al. Neurology 1993; 43 Garde E et al. Lancet 2000; 356
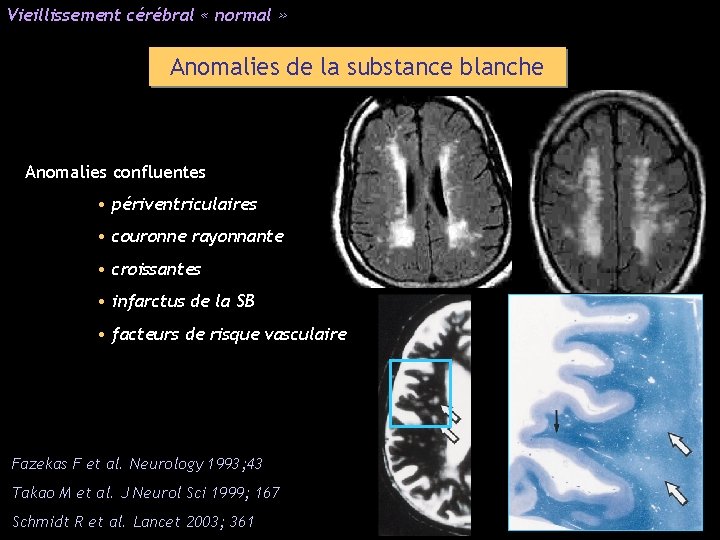
Vieillissement cérébral « normal » Anomalies de la substance blanche Anomalies confluentes • périventriculaires • couronne rayonnante • croissantes • infarctus de la SB • facteurs de risque vasculaire Fazekas F et al. Neurology 1993; 43 Takao M et al. J Neurol Sci 1999; 167 Schmidt R et al. Lancet 2003; 361
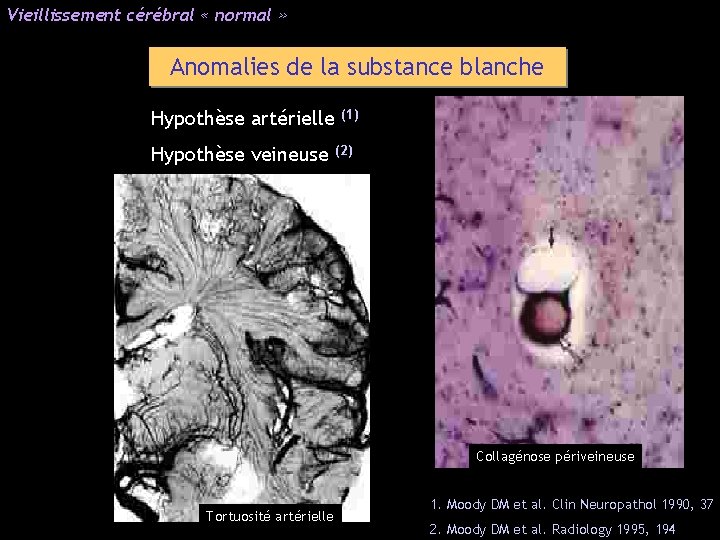
Vieillissement cérébral « normal » Anomalies de la substance blanche Hypothèse artérielle Hypothèse veineuse (1) (2) Collagénose périveineuse Tortuosité artérielle 1. Moody DM et al. Clin Neuropathol 1990, 37 2. Moody DM et al. Radiology 1995, 194
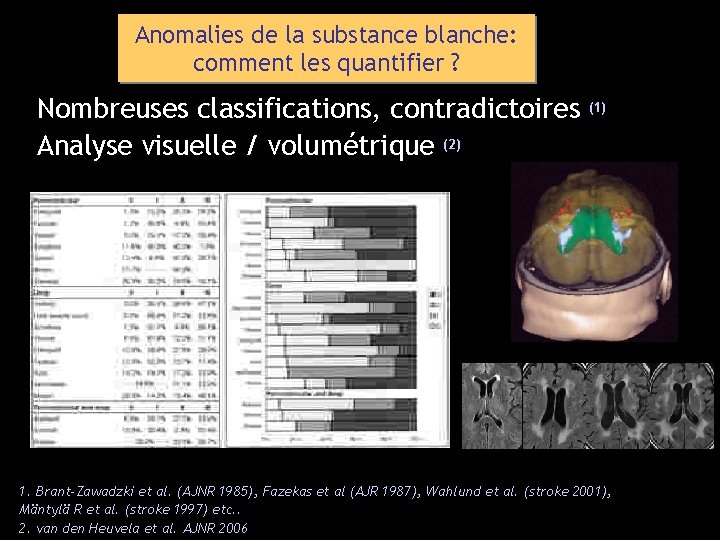
Anomalies de la substance blanche: comment les quantifier ? Nombreuses classifications, contradictoires Analyse visuelle / volumétrique (2) (1) 1. Brant-Zawadzki et al. (AJNR 1985), Fazekas et al (AJR 1987), Wahlund et al. (stroke 2001), Mäntylä R et al. (stroke 1997) etc. . 2. van den Heuvela et al. AJNR 2006
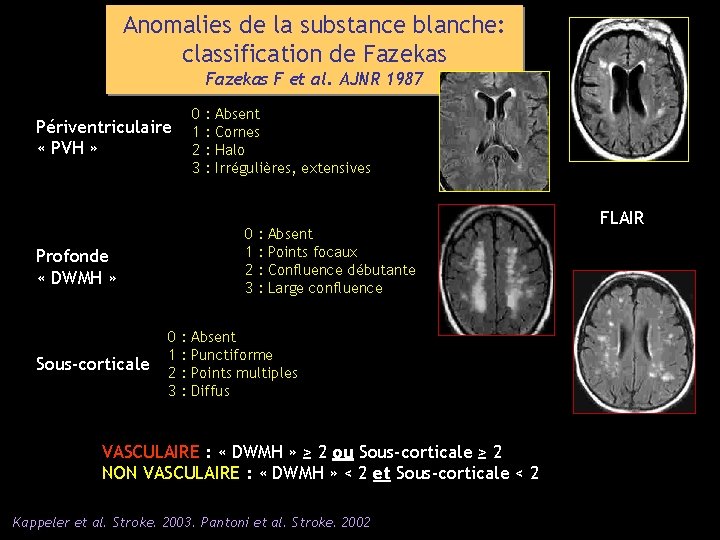
Anomalies de la substance blanche: classification de Fazekas F et al. AJNR 1987 0 1 2 3 Périventriculaire « PVH » Absent Cornes Halo Irrégulières, extensives 0 1 2 3 Profonde « DWMH » Sous-corticale : : 0 1 2 3 : : : : Absent Points focaux Confluence débutante Large confluence Absent Punctiforme Points multiples Diffus VASCULAIRE : « DWMH » ≥ 2 ou Sous-corticale ≥ 2 NON VASCULAIRE : « DWMH » < 2 et Sous-corticale < 2 Kappeler et al. Stroke. 2003. Pantoni et al. Stroke. 2002 FLAIR

Vieillissement cérébral « normal » Implications cliniques • - « habituels, banals… » mais marqueur de risque : de démence vasculaire d’accident ischémique d’hémorragie intracrânienne • Autres – – troubles de la marche, troubles urinaires troubles de l’élocution, cognitifs Syndrome dépressif facteur prédictif de la mortalité Barkhof F et al. Cerebrovasc Dis 2002; 13 Kuller LH et al. Stroke. 2004; 35 reteler MM et al. Neurology 1994; 44 Camicioli R et al. J Am Geriatr Soc 1999; 47 Longstreth WT et al. Stroke 1996; 27 Schmidt R et al. Neurology 1993; 43 Thomas AJ et al. J Affect Disord 2004; 79

Conclusion du compte rendu : « HS de la SB incitant au contrôle des facteurs de risque cardiovasculaires »

Le vieillissement cérébral « normal » • Atrophie cérébrale • Dilatation des espaces de Virchow et Robin • Modifications de la substance blanche • Microsaignements intra parenchymateux • Modification de la distribution en fer et de la charge calcique des noyaux gris centraux
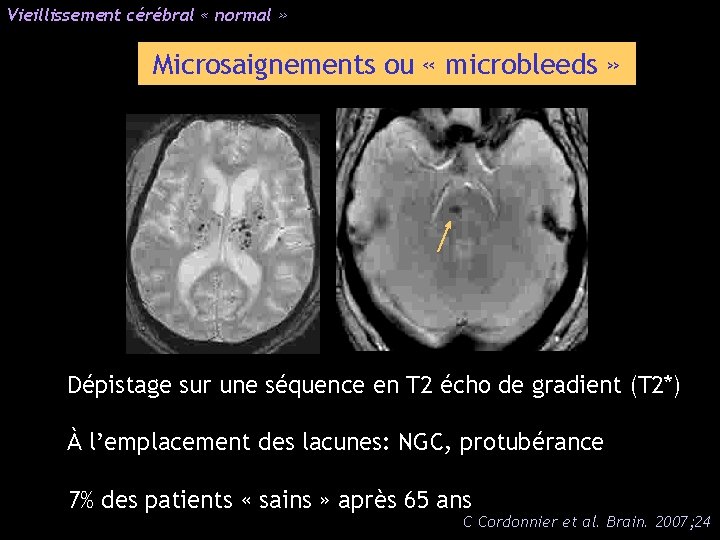
Vieillissement cérébral « normal » Microsaignements ou « microbleeds » Dépistage sur une séquence en T 2 écho de gradient (T 2*) À l’emplacement des lacunes: NGC, protubérance 7% des patients « sains » après 65 ans C Cordonnier et al. Brain. 2007; 24
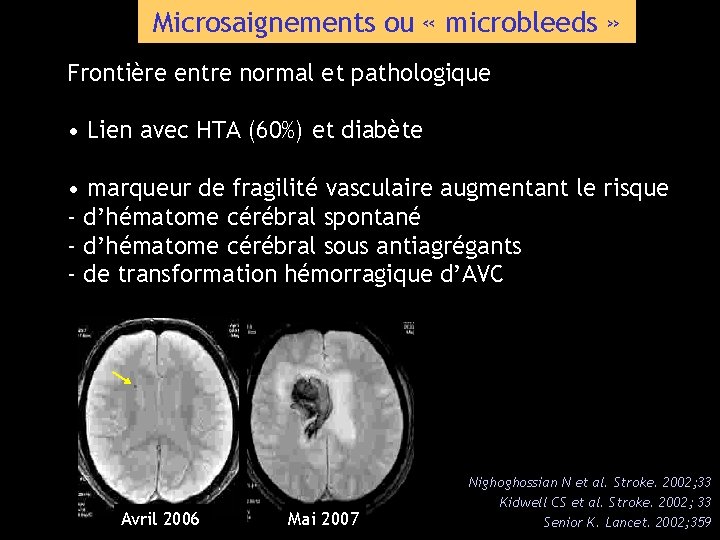
Microsaignements ou « microbleeds » Frontière entre normal et pathologique • Lien avec HTA (60%) et diabète • marqueur de fragilité vasculaire augmentant le risque - d’hématome cérébral spontané - d’hématome cérébral sous antiagrégants - de transformation hémorragique d’AVC Avril 2006 Mai 2007 Nighoghossian N et al. Stroke. 2002; 33 Kidwell CS et al. Stroke. 2002; 33 Senior K. Lancet. 2002; 359

Conclusion du compte rendu : « microsaignements chroniques cérébraux incitant à la réalisation d’un bilan tensionnel»

Le vieillissement cérébral « normal » • Atrophie cérébrale • Dilatation des espaces de Virchow et Robin • Modifications de la substance blanche • Microsaignements intra parenchymateux • Modification de la distribution en fer et de la charge calcique des noyaux gris centraux
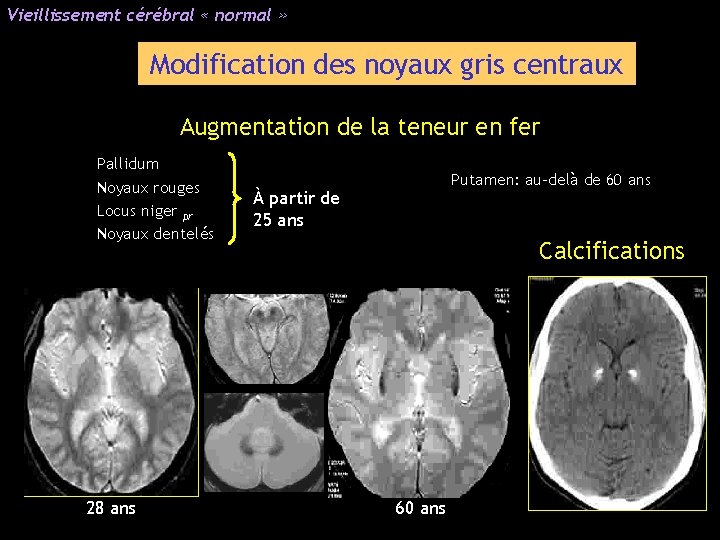
Vieillissement cérébral « normal » Modification des noyaux gris centraux Augmentation de la teneur en fer Pallidum Noyaux rouges Locus niger pr Noyaux dentelés 28 ans Putamen: au-delà de 60 ans À partir de 25 ans Calcifications 60 ans

Quel est l’apport de l’imagerie dans le bilan de troubles cognitifs ?

Faut-il explorer une démence en imagerie ? • 1997 « Coûteux et futile ? » George AE et al. AJNR 1997 • 2007 « Au-delà de l’exclusion » Scheltens F et al. Lancet Neurology - éliminer une cause somatique - apporter des arguments pour une cause vasculaire, dégénérative - identification des patients à risque de développer une DTA

Quelle modalité d’imagerie ? • « Une imagerie cérébrale systématique est recommandée pour toute démence d’apparition récente. Le but de cet examen est de ne pas méconnaître l’existence d’une autre cause de démence (processus expansif intra-crânien, hydrocéphalie à pression normale, lésions d’origine vasculaire …) » • « Cet examen sera au mieux une IRM, à défaut une tomodensitométrie cérébrale en fonction de l’accessibilité à ces techniques… » Recommandantions 2000 HAS Guide des bonnes pratiques radiologiques SFR/SFBM, directive Euratom 97/43
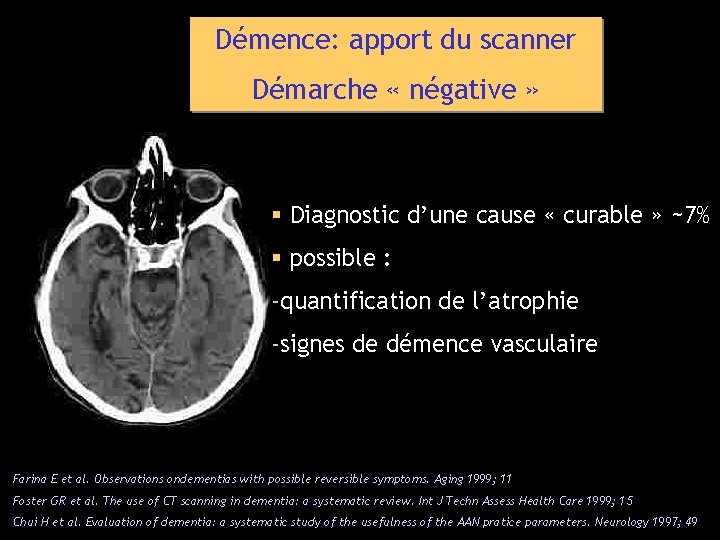
Démence: apport du scanner Démarche « négative » § Diagnostic d’une cause « curable » ~7% § possible : -quantification de l’atrophie -signes de démence vasculaire Farina E et al. Observations ondementias with possible reversible symptoms. Aging 1999; 11 Foster GR et al. The use of CT scanning in dementia: a systematic review. Int J Techn Assess Health Care 1999; 15 Chui H et al. Evaluation of dementia: a systematic study of the usefulness of the AAN pratice parameters. Neurology 1997; 49
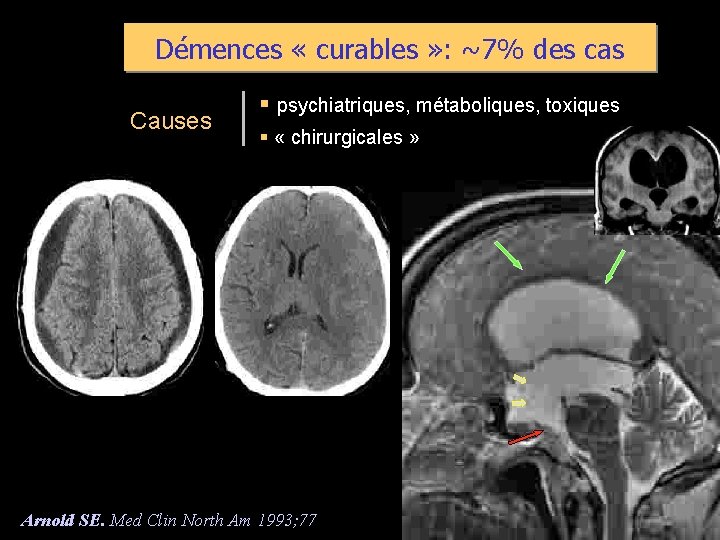
Démences « curables » : ~7% des cas Causes § psychiatriques, métaboliques, toxiques § « chirurgicales » Arnold SE. Med Clin North Am 1993; 77
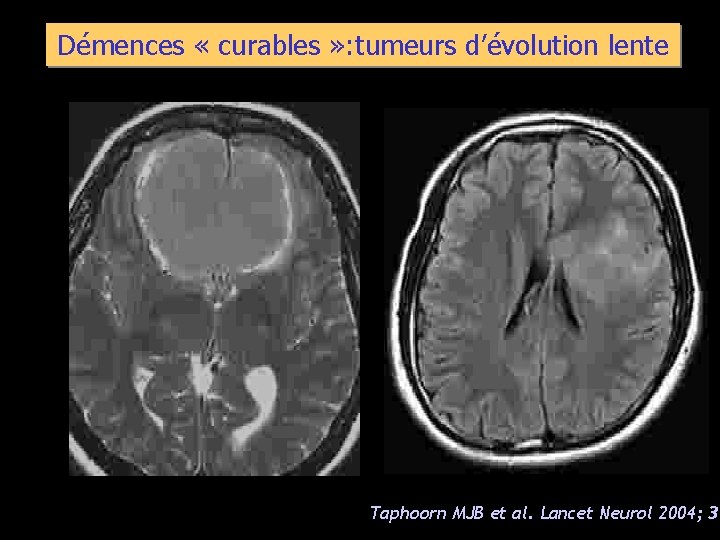
Démences « curables » : tumeurs d’évolution lente Taphoorn MJB et al. Lancet Neurol 2004; 3
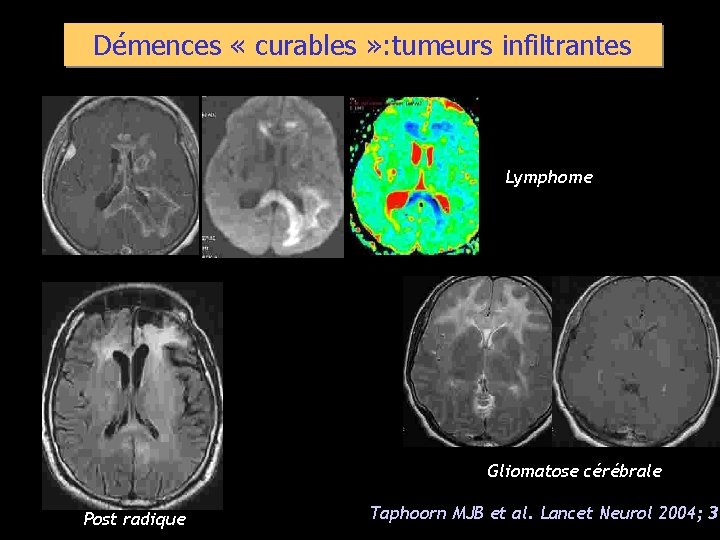
Démences « curables » : tumeurs infiltrantes Lymphome Gliomatose cérébrale Post radique Taphoorn MJB et al. Lancet Neurol 2004; 3

Démence : apport de l’IRM Démarche « positive » En série ü T 1 volumique ü FLAIR ü T 2* ü Diffusion quantification parenchyme hémorragie ischémie En option ü Tenseur Diffusion ü Perfusion ü Activation ü Spectroscopie en évaluation

Démarche « positive » Quels sont les signes en imagerie en faveur d’une démence vasculaire ?

Démences vasculaires 4 échelles diagnostiques existent, discordantes х4– DSM-IV (Diagnostic and Stat Manual of Mental Disorders) х2– ADDTC (Alzheimer Disease Diagnostic and Treatment Centers) х2– ICD-10 (International Classification of Diseases) 1 – NINDS-AIREN (National Institute of Neurological Disorders and Stroke / Association Internationale pour la recherche et l’enseignement en neurosciences) Wetterling et al. Stroke 1996; 27 Lopez et al. Neurology. 2005; 10 W. M. van der Flier et al. Neurology 2005; 65

Démences vasculaires • Importance de l’imagerie dans la définition • Définition – Démence – Maladie cérébro-vasculaire clinique, visible en imagerie – Lien entre les 2 : AVC puis démence dans les 3 mois début brutal déficits cognitifs par pallier Critères du NINDS-AIREN Neurology 1993; 43: 250 -60
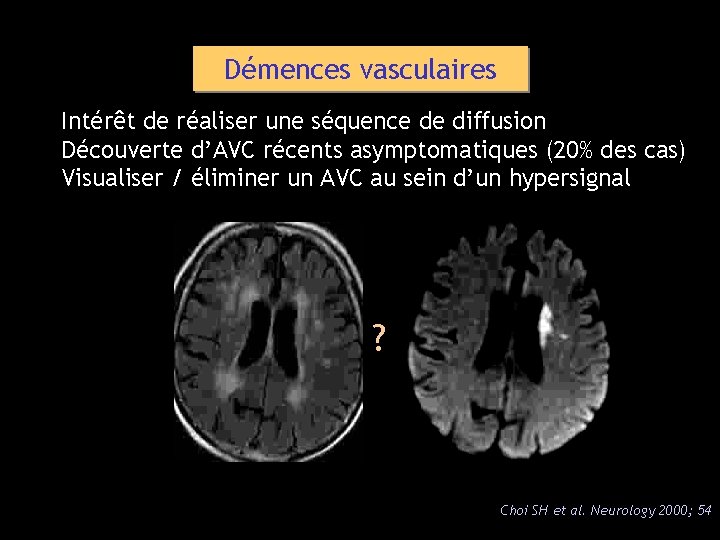
Démences vasculaires Intérêt de réaliser une séquence de diffusion Découverte d’AVC récents asymptomatiques (20% des cas) Visualiser / éliminer un AVC au sein d’un hypersignal ? Choi SH et al. Neurology 2000; 54

Topographie des AVC et démence vasculaire AVC dans le territoire d’artères de gros calibre : - cérébral antérieur bilatéral - cérébral postérieur : thalamique, temporal inféromédian - sylvien : temporopariétal, temporo-occipital, gyrus angulaire - jonctionnel : frontal supérieur, pariéto-occipital, sylvien sup. / profond Microangiopathie: - ≥ 2 lacunes des ganglions de la base ou de la substance blanche frontale - lacunes bithalamiques Guermazi A et al. Neuroradiology 2007; 49
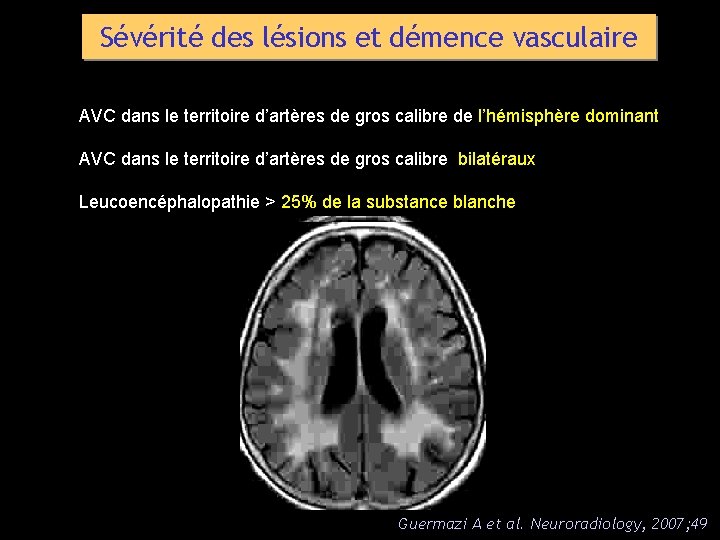
Sévérité des lésions et démence vasculaire AVC dans le territoire d’artères de gros calibre de l’hémisphère dominant AVC dans le territoire d’artères de gros calibre bilatéraux Leucoencéphalopathie > 25% de la substance blanche Guermazi A et al. Neuroradiology, 2007; 49
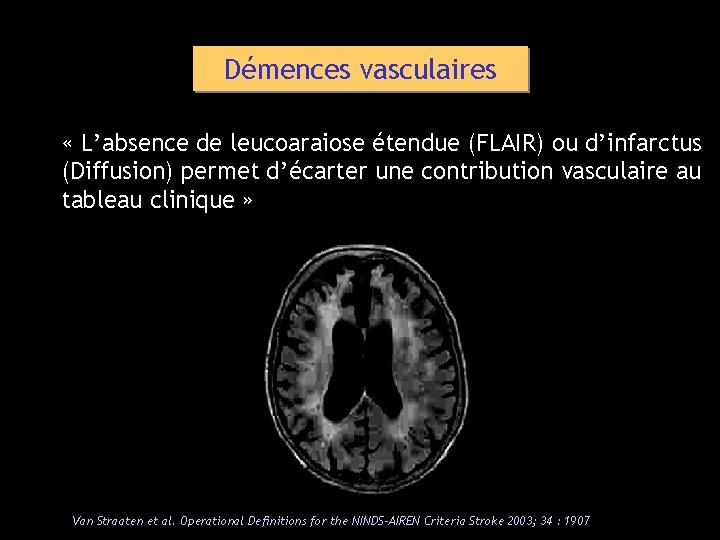
Démences vasculaires « L’absence de leucoaraiose étendue (FLAIR) ou d’infarctus (Diffusion) permet d’écarter une contribution vasculaire au tableau clinique » Van Straaten et al. Operational Definitions for the NINDS-AIREN Criteria Stroke 2003; 34 : 1907

Conclusion du compte rendu : « arguments IRM en faveur d’une origine vasculaire aux troubles cognitifs »
Démarche « positive » Quels sont les signes, en imagerie, évocateurs de démence de type Alzheimer ?

Démence de type Alzheimer: enjeux • 400 000 en 1993, 800 000 en 2003 • Tests neuropsychologiques : sensibles mais tardifs • Traitements : à débuter le plus tôt possible • Comment faire le diagnostic positif précocement ? - (in)formation des professionnels - consultation mémoire - imagerie ?

Plusieurs populations étudiées Démence de type Alzheimer (DTA) – Troubles cognitifs évolués MCI ou Mild Cognitive Impairment – Troubles cognitifs discrets – Risque d’évolution vers une DTA : 10 -30%/an – La cible thérapeutique (1) Sujet sain ≥ 65 ans – Les « témoins » – Risque d’évolution en DTA croissant avec l’âge 1. Petersen RC et al. Arch Neurol. 2001; 58
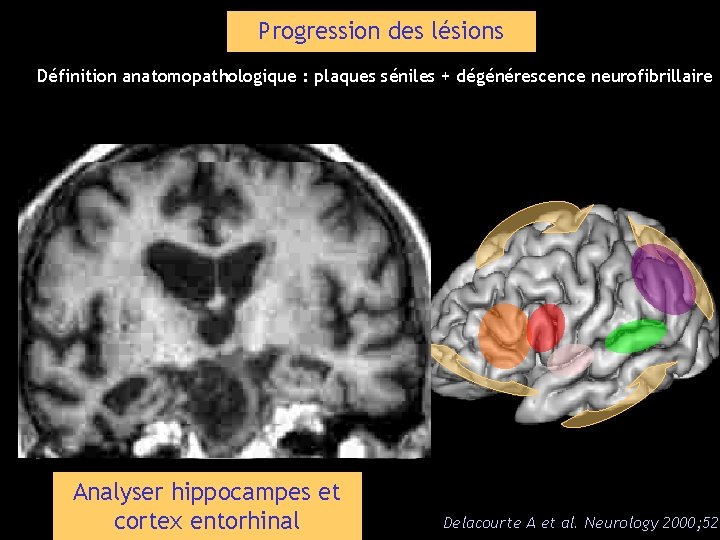
Progression des lésions Définition anatomopathologique : plaques séniles + dégénérescence neurofibrillaire 1 1 1 Analyser hippocampes et cortex entorhinal Delacourte A et al. Neurology 2000; 52

Atrophie cérébrale globale à prédominance temporale médiale Comment l’évaluer ? Analyse visuelle = l’individu – Utilisable en routine – Méthode subjective (difficile dans les formes débutantes) Analyse quantitative = la population – Mesures linéaires – Volumétrie, morphométrie (région d’intérêt) – Développement de logiciels automatisés
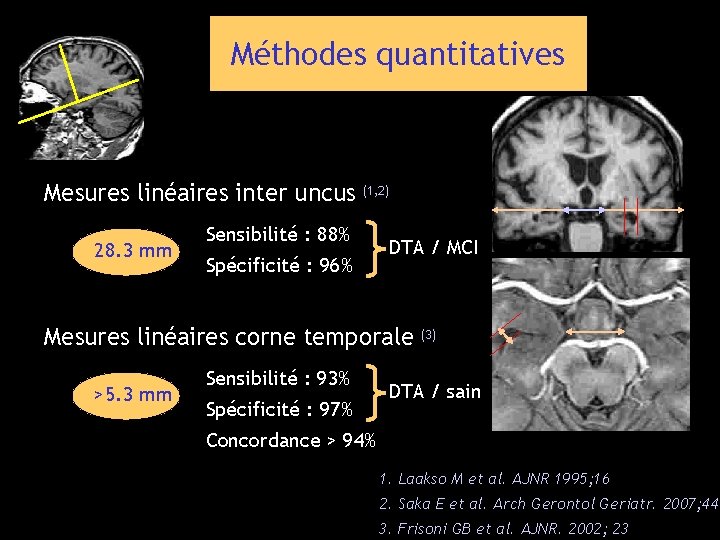
Méthodes quantitatives Mesures linéaires inter uncus (1, 2) 28. 3 mm Sensibilité : 88% Spécificité : 96% DTA / MCI Mesures linéaires corne temporale (3) >5. 3 mm Sensibilité : 93% Spécificité : 97% DTA / sain Concordance > 94% 1. Laakso M et al. AJNR 1995; 16 2. Saka E et al. Arch Gerontol Geriatr. 2007; 44 3. Frisoni GB et al. AJNR. 2002; 23
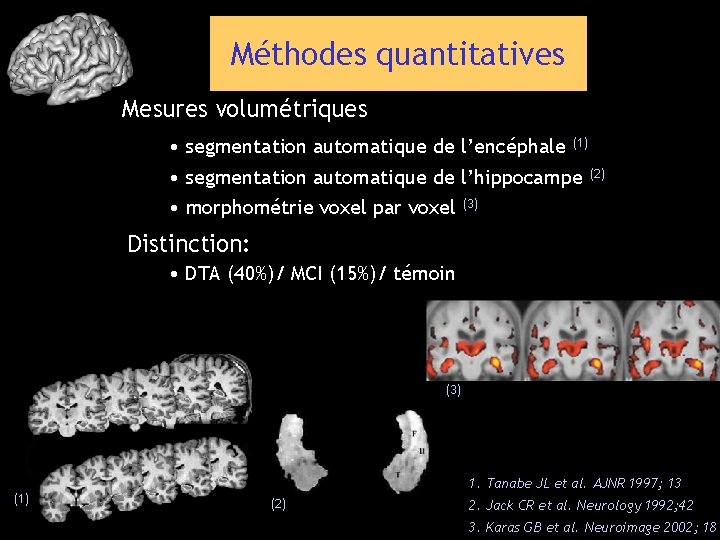
Méthodes quantitatives Mesures volumétriques • segmentation automatique de l’encéphale (1) • segmentation automatique de l’hippocampe • morphométrie voxel par voxel (3) (2) Distinction: • DTA (40%)/ MCI (15%)/ témoin (3) 1. Tanabe JL et al. AJNR 1997; 13 (1) (2) 2. Jack CR et al. Neurology 1992; 42 3. Karas GB et al. Neuroimage 2002; 18
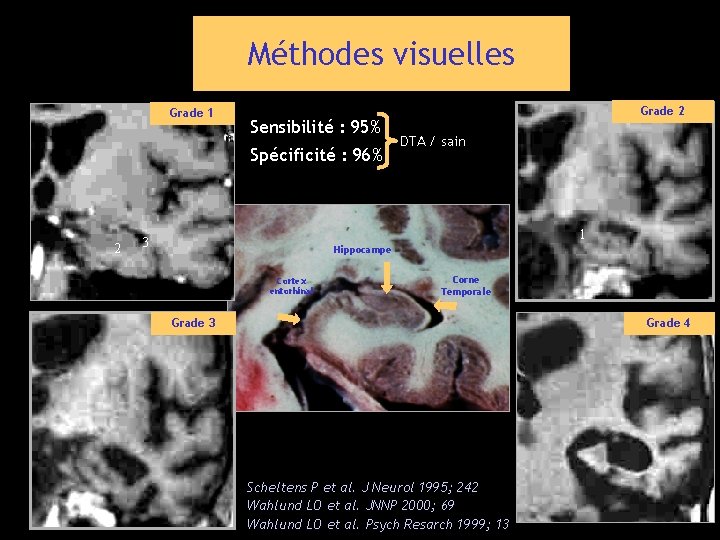
Méthodes visuelles Grade 1 Sensibilité : 95% Spécificité : 96% 2 Grade 2 DTA / sain 1 3 Hippocampe Cortex entorhinal Corne Temporale Grade 3 Grade 4 Scheltens P et al. J Neurol 1995; 242 Wahlund LO et al. JNNP 2000; 69 Wahlund LO et al. Psych Resarch 1999; 13
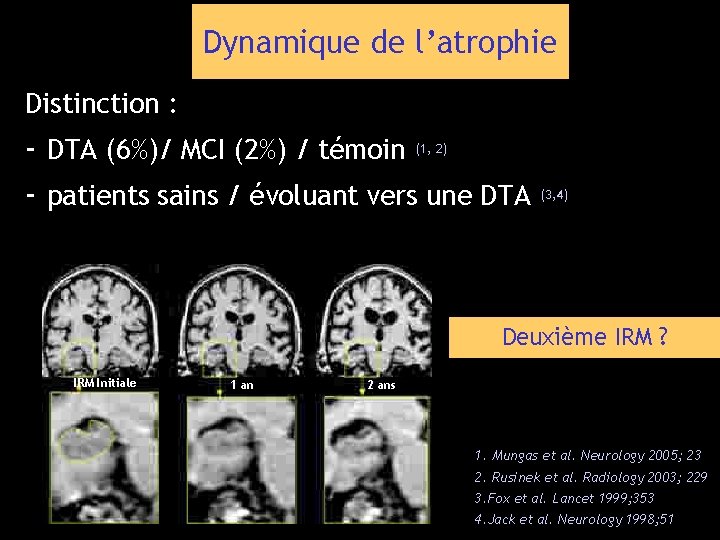
Dynamique de l’atrophie Distinction : - DTA (6%)/ MCI (2%) / témoin (1, 2) - patients sains / évoluant vers une DTA (3, 4) Deuxième IRM ? IRM Initiale 1 an 2 ans 1. Mungas et al. Neurology 2005; 23 2. Rusinek et al. Radiology 2003; 229 3. Fox et al. Lancet 1999; 353 4. Jack et al. Neurology 1998; 51

Démarche « positive » l’IRM permet elle de distinguer la DTA des autres démences dégénératives ?
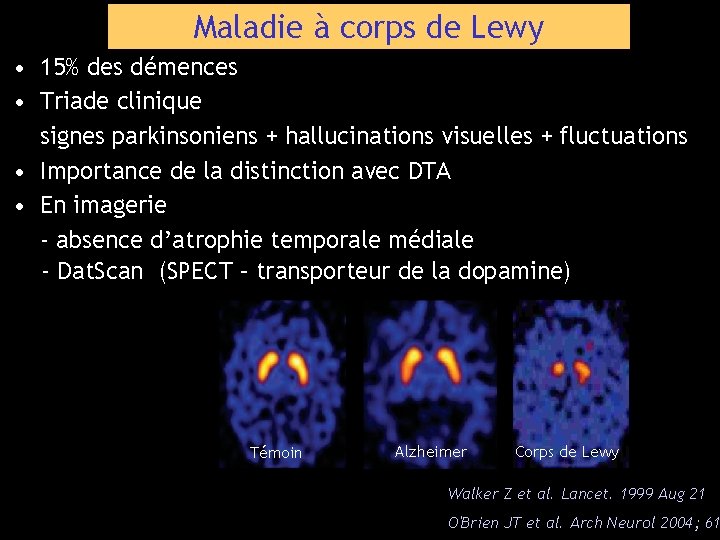
Maladie à corps de Lewy • 15% des démences • Triade clinique signes parkinsoniens + hallucinations visuelles + fluctuations • Importance de la distinction avec DTA • En imagerie - absence d’atrophie temporale médiale - Dat. Scan (SPECT – transporteur de la dopamine) Témoin Alzheimer Corps de Lewy Walker Z et al. Lancet. 1999 Aug 21 O'Brien JT et al. Arch Neurol 2004; 61
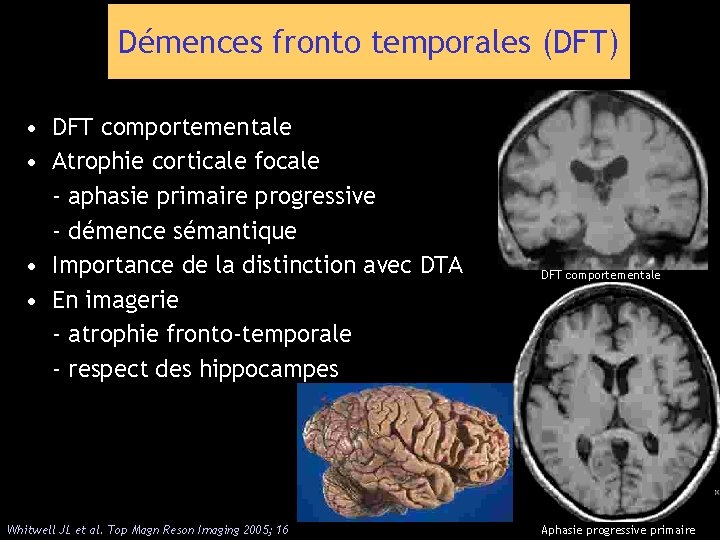
Démences fronto temporales (DFT) • DFT comportementale • Atrophie corticale focale - aphasie primaire progressive - démence sémantique • Importance de la distinction avec DTA • En imagerie - atrophie fronto-temporale - respect des hippocampes Whitwell JL et al. Top Magn Reson Imaging 2005; 16 DFT comportementale Aphasie progressive primaire

Quel est l’apport des nouvelles techniques d’IRM chez les sujets suspects de démence de type Alzheimer ?
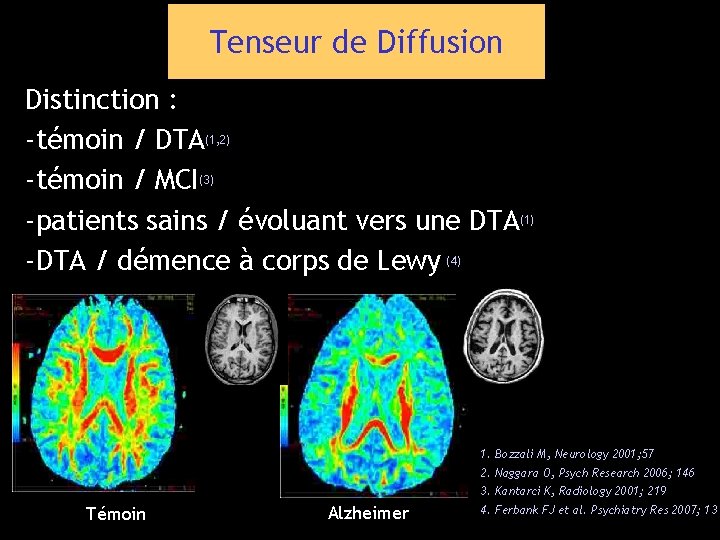
Tenseur de Diffusion Distinction : -témoin / DTA(1, 2) -témoin / MCI(3) -patients sains / évoluant vers une DTA(1) -DTA / démence à corps de Lewy (4) 1. Bozzali M, Neurology 2001; 57 2. Naggara O, Psych Research 2006; 146 3. Kantarci K, Radiology 2001; 219 Témoin Alzheimer 4. Ferbank FJ et al. Psychiatry Res 2007; 13
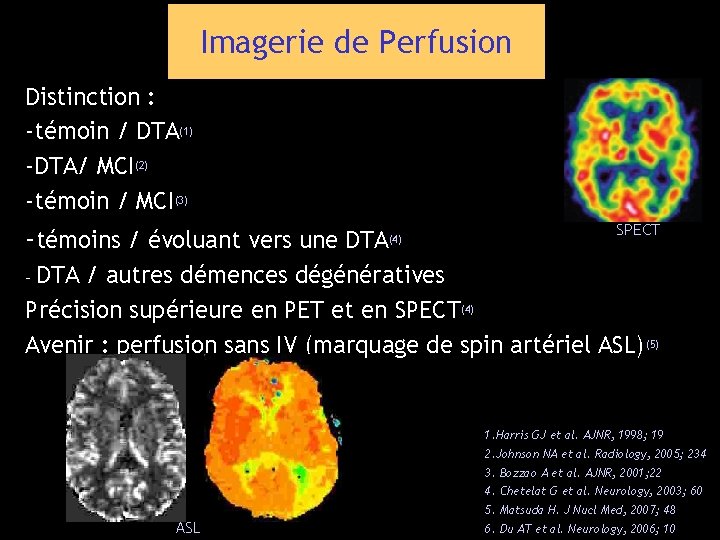
Imagerie de Perfusion Distinction : -témoin / DTA(1) -DTA/ MCI(2) -témoin / MCI(3) -témoins / évoluant vers une DTA (4) SPECT DTA / autres démences dégénératives Précision supérieure en PET et en SPECT(4) Avenir : perfusion sans IV (marquage de spin artériel ASL)(5) - 1. Harris GJ et al. AJNR, 1998; 19 2. Johnson NA et al. Radiology, 2005; 234 3. Bozzao A et al. AJNR, 2001; 22 4. Chetelat G et al. Neurology, 2003; 60 5. Matsuda H. J Nucl Med, 2007; 48 ASL 6. Du AT et al. Neurology, 2006; 10
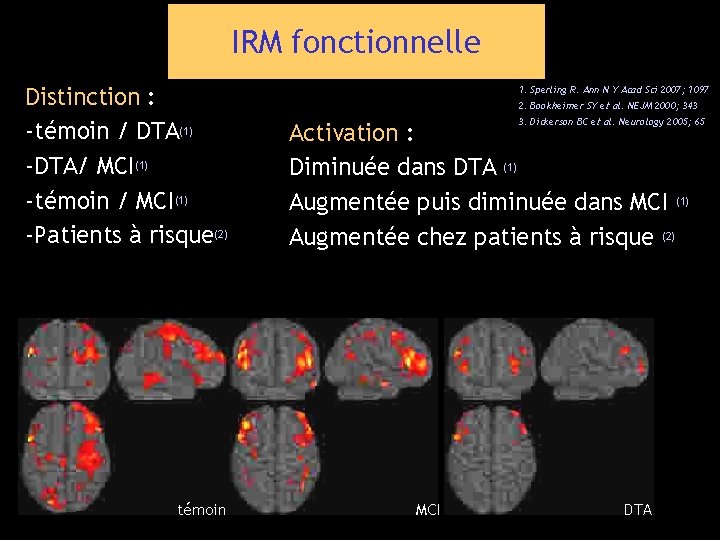
IRM fonctionnelle Distinction : -témoin / DTA(1) -DTA/ MCI(1) -témoin / MCI(1) -Patients à risque(2) témoin 1. Sperling R. Ann N Y Acad Sci 2007; 1097 2. Bookheimer SY et al. NEJM 2000; 343 3. Dickerson BC et al. Neurology 2005; 65 Activation : Diminuée dans DTA (1) Augmentée puis diminuée dans MCI (1) Augmentée chez patients à risque (2) MCI DTA
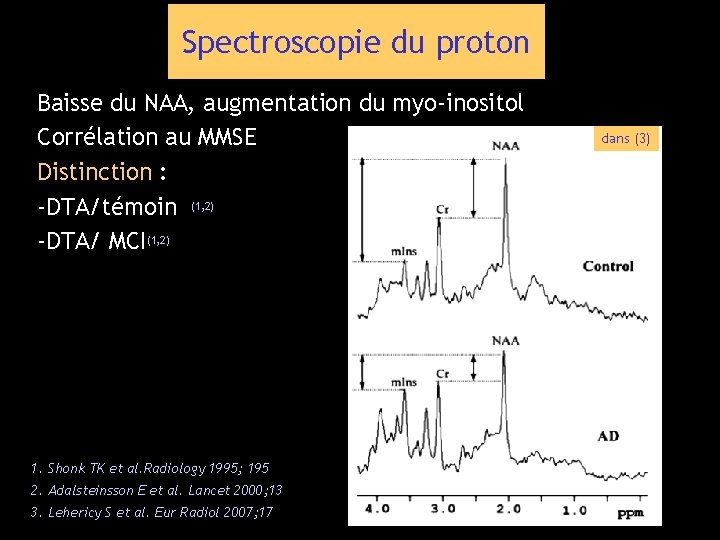
Spectroscopie du proton Baisse du NAA, augmentation du myo-inositol Corrélation au MMSE Distinction : -DTA/témoin (1, 2) -DTA/ MCI(1, 2) 1. Shonk TK et al. Radiology 1995; 195 2. Adalsteinsson E et al. Lancet 2000; 13 3. Lehericy S et al. Eur Radiol 2007; 17 dans (3)

Données de la littérature Niveau de preuve élevé L’imagerie (Scanner ou IRM) influence la prise en charge au début du déclin cognitif en mettant en évidence une cause potentiellement traitable Niveau de preuve modéré L’atrophie des hippocampes en volumétrie par IRM est corrélée au stade clinique dans la DTA La dynamique de l’atrophie des hippocampes est corrélée avec le déclin cognitif Niveau de preuve insuffisant Évaluation de l’éfficacité thérapeutique en imagerie Medina LS et al. Neuroimag Clin N Am 2003; 13

Déclin cognitif : IRM Ø T 1 volumique Ø T 2 (coupes frontales Ⱶ hippocampes) Atrophie Ø FLAIR (coupes axiales) Pathologie de la SB AVC ancien Ø Diffusion (coupes axiales) AVC récent Ø T 2* (coupes axiales) Microsaignements
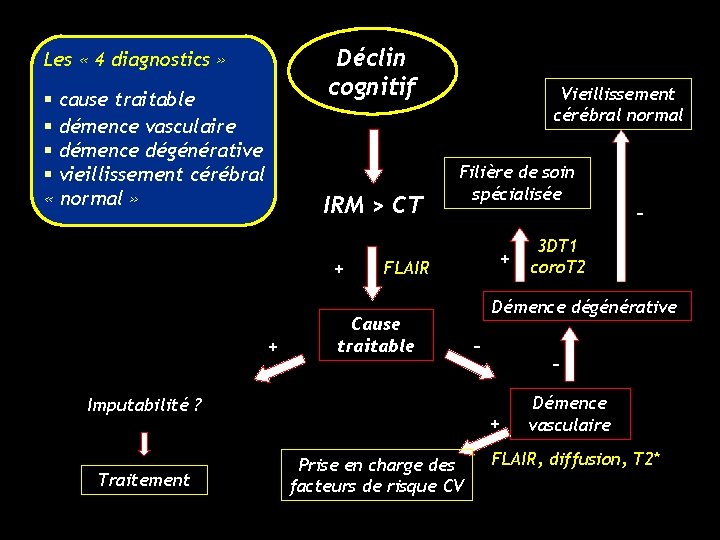
Déclin cognitif Les « 4 diagnostics » § cause traitable § démence vasculaire § démence dégénérative § vieillissement cérébral « normal » IRM > CT + + Vieillissement cérébral normal Filière de soin spécialisée Cause traitable Imputabilité ? Traitement + FLAIR 3 DT 1 coro. T 2 Démence dégénérative - + Prise en charge des facteurs de risque CV - Démence vasculaire FLAIR, diffusion, T 2*

Conclusion • Démarche « négative » : éliminer une cause « curable » • L’IRM en routine permet une démarche « positive » : - donner des arguments en faveur d’une étiologie - détecter la maladie précocement - mais diffusion limitée des outils de quantification fin 2007 Plaque sénile en IRM 7 T, séquence T 2*
- Slides: 66