IMAGERIE DU CANCER DE LA PROSTATE Dr BNOUACHIR

IMAGERIE DU CANCER DE LA PROSTATE Dr BNOUACHIR

Plan � INTRODUCTION � RAPPEL ANATOMIQUE � EPIDÉMIOLOGIE � ANATOMO-PATHOLOGIE � MOYENS D’EXPLORATION � DIAGNOSTIC POSITIF � BILAN D’EXTENSION � TRAITEMENT � SURVEILLANCE � CONCLUSION

INTRODUCTION � Kc prostate: 20 % de tous les cancers chez l'homme � Seconde cause de mortalité par cancer chez l’homme après 60 ans. � PSA+++: ◦ Dépistage ( incidence) ◦ Surveillance post-thérapeutique � Diagnostic= biopsie prostatique sous guidage EER � Evolution lente � Traitement dépend de plusieurs facteurs: ◦ ◦ L’âge Le degré d’altération de la qualité de vie Le grade histologique Le bilan d ’extension (IRM+++)

INTRODUCTION � Imagerie (Echodoppler, IRM) +++: ◦ Diagnostic ◦ Bilan d’extension ◦ Suivi post thérapeutique (récidives? ) � L’IRM est indispensable pour guider la prise en charge thérapeutique ( séquences fonctionnelles+++)

RAPPEL ANATOMIQUE
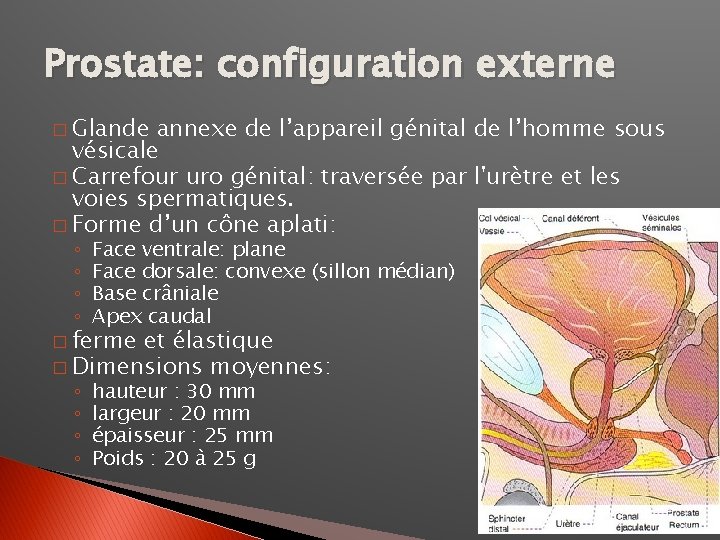
Prostate: configuration externe � Glande annexe de l’appareil génital de l’homme sous vésicale � Carrefour uro génital: traversée par l'urètre et les voies spermatiques. � Forme d’un cône aplati: ◦ ◦ Face ventrale: plane Face dorsale: convexe (sillon médian) Base crâniale Apex caudal ◦ ◦ hauteur : 30 mm largeur : 20 mm épaisseur : 25 mm Poids : 20 à 25 g � ferme et élastique � Dimensions moyennes:

Prostate: anatomie zonale selon Mac Neal Zone périphérique (ZP): 70% La portion postérieure et inférieure de la glande (l’apex est entièrement formé de ZP). la zone de prédilection des cancers (70%) Zone centrale (ZC): 25% Masse conique médiane et postérieure, rétro urétérale, entourant les canaux éjaculateurs, occupant la totalité de la base prostatique. 5% des cancers Zone de transition (ZT): 5% Siège antéro-médian. Constituée de 2 lobes distincts situés de part et d’autre de l’urètre prostatique. S’hypertrophie avec l’age 25% des cancers

Prostate: anatomie zonale selon Mac Neal Zone des glandes péri-urétrales (ZPU) 1% Sphincter urétral proximal Le développement prépondérant de la ZPU aboutit à la constitution du lobe médian. Zone non glandulaire: SFMA = Stroma fibro musculaire antérieur: recouvre la partie médiane de la face antérieure de la glande, peut constituer jusqu’à 30% du volume prostatique total chez le jeune
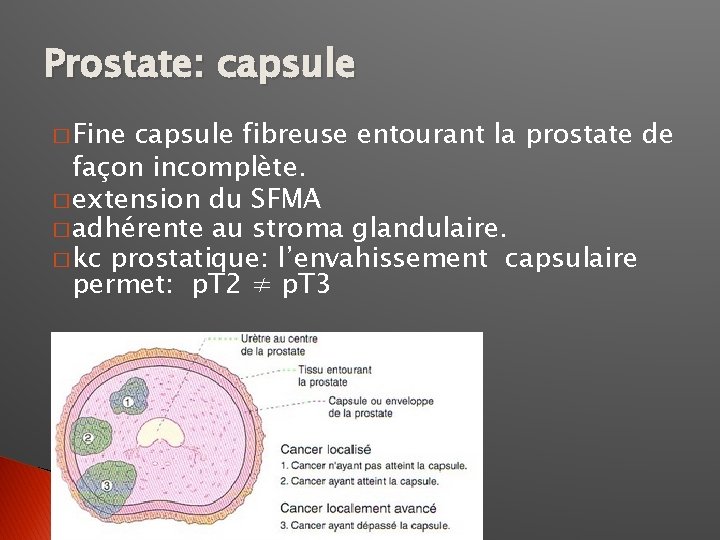
Prostate: capsule � Fine capsule fibreuse entourant la prostate de façon incomplète. � extension du SFMA � adhérente au stroma glandulaire. � kc prostatique: l’envahissement capsulaire permet: p. T 2 ≠ p. T 3

Prostate: rapports � Supérieur : ◦ Avt: base vésicale+ sphincter lisse ◦ Arr: VS, canaux déférents � Inférieur : ◦ sphincter strié � Latéraux : ◦ Pédicules N-Vx génito- vésicaux ◦ Releveur de l’anus ◦ obturateur interne � Antérieur : ◦ Espace rétro-pubien: graisse + plexus veineux de Santorini � Postérieur : ◦ Rectum
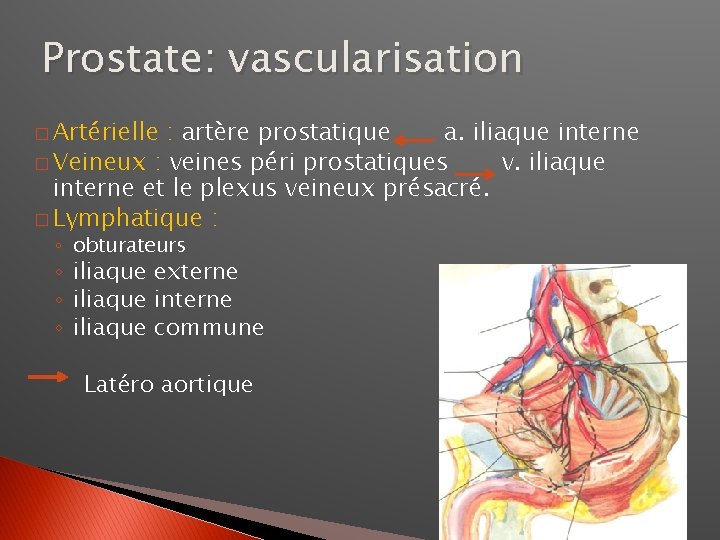
Prostate: vascularisation � Artérielle : artère prostatique a. iliaque interne � Veineux : veines péri prostatiques v. iliaque interne et le plexus veineux présacré. � Lymphatique : ◦ obturateurs ◦ iliaque externe ◦ iliaque interne ◦ iliaque commune Latéro aortique

EPIDEMIOLOGIE

Epidémiologie � Incidence: ◦ 20 % de tous les cancers chez l'homme ◦ En Europe et aux Etats Unis: 1 er cancer chez l'homme >50 ans. � ge: ◦ 70 % Kc prostate surviennent après 65 ans ◦ pic de fréquence : 8 ème décennie � 2ème cause de mortalité par cancer chez l'homme (10 %) après le Kc poumon (30 %) � Evolution lente: Survie à 5 ans: 80 %

Epidémiologie � Facteurs ◦ ◦ ◦ de risque: (encore mal connus) ge F. familial et génétique F. ethnique: Afrique, Ouest de l’Afrique F. hormonal F. alimentaire: �Régime: �riche en graisses animales saturés �pauvre en fibres �Aliments protecteurs: vit. D, selenium, antioxydants (lycopène++…. )

ANATOMO-PATHOLOGIE � Macroscopie: § lésion localisée unique ou multiples de taille variable § lésion diffuse infiltrante � Microscopie: Ø Adénocarcinome ± différencié (95%)+++ Ø Sarcome: rares Ø Carcinome épidermoïde : exceptionnels � Topographie § ZP 70 %, ZT 20 % , ZC 10 % § Multifocale : 56 à 67 %

� Grade � Étude de Gleason: de l'architecture histologique de la tumeur sur biopsies prostatiques ou pièce opératoire. � 5 grades selon différenciation � Le score de Gleason correspondant à l'addition des deux grades les plus représentés (1+1 5+5). ◦ Bien différencié : 2 à 4 ◦ Moyennement différencié : 5 à 6 ◦ Peu ou non différencié : 7 à 10 ( de mauvais Pc à potentiel agressif ) � Bonne corrélation entre le volume tumoral et le grade histologique

MOYENS D’EXPLORATION

Echographie doppler 1ère intention 2 voies d’abord: Endorectale+++ o pivot diagnostic des affections prostatiques. o 1ère modalité d’imagerie directe du tissu prostatique. o Indications : • • Appréciation du volume de la prostate Analyse fine de la structure Guidage des biopsies Bilan d’extension local o Technique: • Patient en DLG, hanches et genoux fléchis, vessie vide. • Sondes de haute fréquence entre 7, 5 et 10 MHz • Balayage précis et systématique dans les plans: • Axial: base apex • Sagittal: latérale, paramédiane, médiane • Complément par échographie doppler.

Echographie Sus pubienne o Technique: • Sonde sectorielle de moyenne fréquence de 3, 5 à 5 Mhz. • Nécessite une réplétion vésicale modérée. o Indication: • Apprécie le volume prostatique • Etudier la vessie et le RPM • Etudier: reins (retentissement), foie (métastases) o Limites: Etude médiocre de la structure prostatique

Echographie Echo doppler: § Détecter une lésion tumorale § Tm avasculaire (bas risque) ≠ Tm hypervasculaire (haut risque) § Diriger les biopsies Echo de contraste: o Principe: o Objectifs: § différencier la vascularisation tumorale de la vascularisation saine § Balayage rapide de la prostate à la recherche de zones de rehaussement précoce § Augmenter la spécificité des nodules hypoéchogènes § Déceler la présence de kc isoéchogène § Cibler une zone suspecte sur l’IRM fonctionnelle après une 1ère série de biopsies négatives

Echographie Limites: � Faux négatif: �kc < 3 mm �Isoéchogène �Siège ZT (hétérogène et spontanément hypervasculaire) � Opérateur dépendant
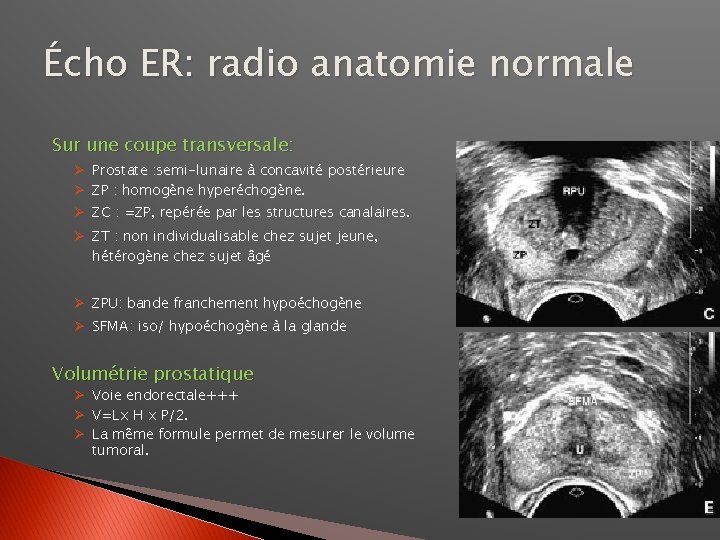
Écho ER: radio anatomie normale Sur une coupe transversale: Ø Prostate : semi-lunaire à concavité postérieure Ø ZP : homogène hyperéchogène. Ø ZC : =ZP, repérée par les structures canalaires. Ø ZT : non individualisable chez sujet jeune, hétérogène chez sujet âgé Ø ZPU: bande franchement hypoéchogène Ø SFMA: iso/ hypoéchogène à la glande Volumétrie prostatique Ø Voie endorectale+++ Ø V=Lx H x P/2. Ø La même formule permet de mesurer le volume tumoral.
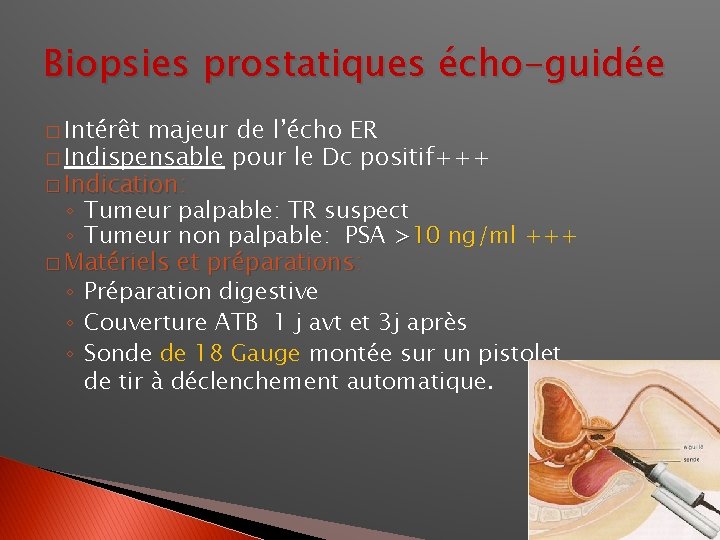
Biopsies prostatiques écho-guidée � Intérêt majeur de l’écho ER � Indispensable pour le Dc positif+++ � Indication: ◦ Tumeur palpable: TR suspect ◦ Tumeur non palpable: PSA >10 ng/ml +++ � Matériels et préparations: ◦ Préparation digestive ◦ Couverture ATB 1 j avt et 3 j après ◦ Sonde de 18 Gauge montée sur un pistolet de tir à déclenchement automatique.
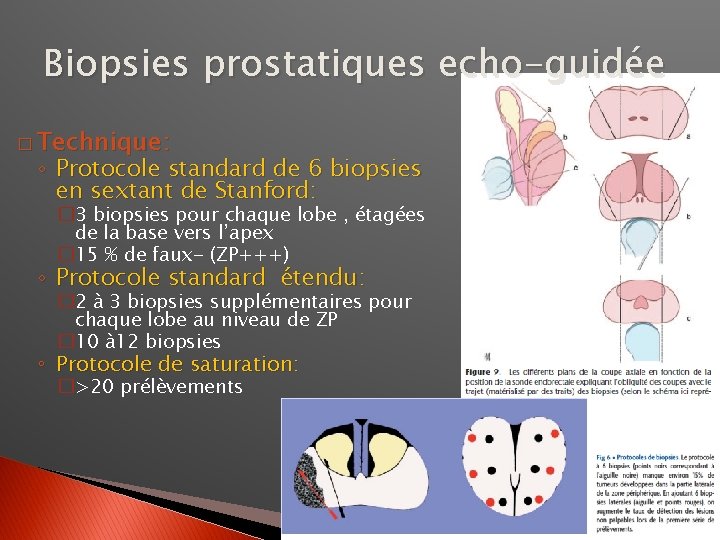
Biopsies prostatiques echo-guidée � Technique: ◦ Protocole standard de 6 biopsies en sextant de Stanford: � 3 biopsies pour chaque lobe , étagées de la base vers l’apex � 15 % de faux- (ZP+++) ◦ Protocole standard étendu: � 2 à 3 biopsies supplémentaires pour chaque lobe au niveau de ZP � 10 à 12 biopsies ◦ Protocole de saturation: �>20 prélèvements

IRM+++ � Gold standard dans l’imagerie du cancer de la prostate: Excellente spécificité et sensibilité � Evolutions techniques constantes: ◦ Antennes ◦ Séquences fonctionnelles � IRM multiparamétrique+++ � +/- Lympho IRM, IRM corps entier ◦ Séq morpho T 2, dynamique, diffusion , +/-spectro ◦ Logiciel de lecture traitant simultanément une zone suspecte sur plusieurs séries

IRM Indications: Bilan d’extension d’un cancer connu � Diagnostic positif: détection d’un cancer suspecté (clinique+PSA), mais non confirmé � (1 à 2 séries biopsiques négatives) � Surveillance post thérapeutique: récidive? Limites: � Incapacité � C. I à délimiter un Kc infiltrant

IRM Précautions: ◦ 6 semaines après la biopsie ou +/- avant : limite les artefacts liés au remaniements hémorragiques post biopsiques ◦ Lavement rectal + un antispasmodique IM : limite les artefacts liés au péristaltisme rectal au cours des séquences longues (T 2)

IRM Antenne: �Antenne endorectale: ◦ Utilisé si: Bilan d’extension péricapsulaire/ Spectroscopie ◦ Avantage: - Excellente résolution spatiale ◦ Inconvénients: - Rapide chute de signal en profondeur - Coût +++ (usage unique) - Inconfort, temps de mise en place �Antenne pelvienne ◦ Avantages : en réseau phasé+++ - Signal homogène: pas de limitation en profondeur - Meilleure analyse des régions antérieures - Meilleur confort des patients et des manipulateurs !

Séquences morphologiques Ø Ø Ø Champ d’exploration: pelvis jusqu’à la bifurcation aortique (extension gg) Coupes fines Pondérées en T 2: +++ ◦ Images anatomiques de la prostate ◦ 3 Plans de coupe: � Axial: � perpendiculaire au bord postérieur de la prostate � Meilleure corrélation anatomopathologique � Coronal: � Strictement perpendiculaire au plan axial, dans le plan des VS � Meilleure analyse du carrefour vésiculo-déférento-prostatique � Sagittal: +/� Étendue cranio-caudale des lésions � Mieux visualiser l’apex Ø Pondérées en T 1: ◦ Rôle modeste mais INDISPENSABLE ◦ Détection des zones hémorragiques post-biopsie +++ ◦ 1 seul plan (axial)

Séquences fonctionnelles Ø Intérêt: o Améliorer la détection des lésions tumorales ◦ Améliorer staging extracapsulaire ◦ Récidives +++ Ø Diffusion: ◦ Très sensible à l’hyper cellularité ◦ Mais non spécifique: Hypersignal : Cancer ou prostatite ◦ Cartographie de ADC+++

Ø Perfusion : Séquences d’EG, pondérées en T 1, en saturation graisse � répétées plusieurs fois (7 séries) /15 s après injection de Gado. � Acquisition en 3 D +++ou 2 D � Analyse de la PDC: � ◦ Visuelle ◦ Courbe « intensité de rehaussement / temps » dans une zone d’intérêt ◦ Analyse semi quantitative: wash-in, wash-out… ◦ Analyse quantitative++: cartes « paramétriques » en estimant la perméabilité tissulaire ds chaque point de l’image ( ktrans, kep…)

Ø Spectroscopie Recueille une information métabolique qui reflète les concentrations relatives de divers métabolites prostatiques: la choline+ la créatine et le citrate � Antenne ER indispensable �

IRM: radioanatomie normale � Prostate: ◦ T 1: même intensité des différentes structures ◦ T 2: - ZP: hyper - ZT et ZC: indissociables(glande centrale): hypo - Capsule: liseré en hypo T 2 +++ � VS et ampoules déférentielles : ◦ T 2: - Stroma: hypo - Lumière: très hyper
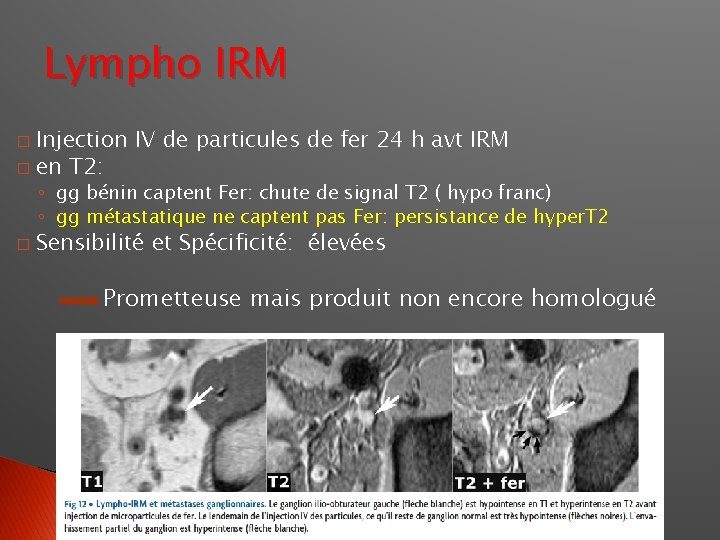
Lympho IRM Injection IV de particules de fer 24 h avt IRM � en T 2: � ◦ gg bénin captent Fer: chute de signal T 2 ( hypo franc) ◦ gg métastatique ne captent pas Fer: persistance de hyper. T 2 � Sensibilité et Spécificité: élevées Prometteuse mais produit non encore homologué
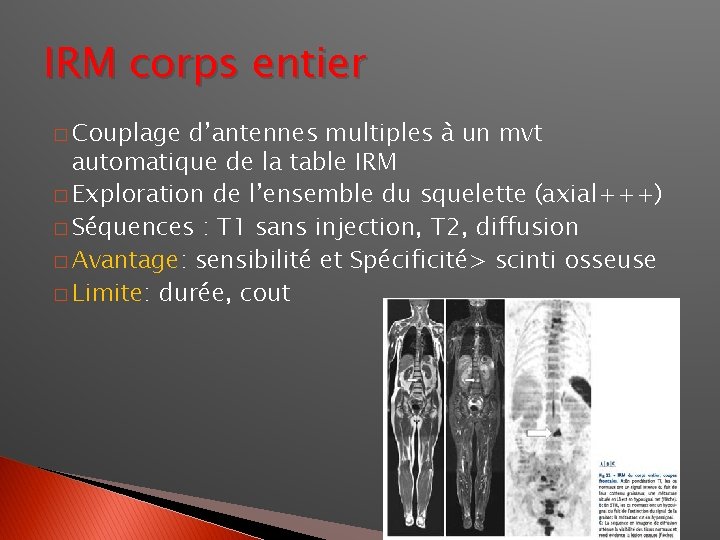
IRM corps entier � Couplage d’antennes multiples à un mvt automatique de la table IRM � Exploration de l’ensemble du squelette (axial+++) � Séquences : T 1 sans injection, T 2, diffusion � Avantage: sensibilité et Spécificité> scinti osseuse � Limite: durée, cout

AUTRES ØUIV : retentissement sur le haut appareil urinaire. ØTDM: extension à distance ØScintigraphie osseuse ØPET scan: • micrométastases ganglionnaires • métastases osseuses

DIAGNOSTIC POSITIF

� Diagnostic positif=biopsies++++ CDD: Ø Examen systématique: Ø Signes fonctionnels urinaires: Ø Ø TR: Prostate ↑de volume; dure pierreuse; douloureuse - prostatisme - pesanteurs - douleurs pelviennes Examen histo d’une résection transurétrale de la prostate Métastases révélatrices.

PSA ØSpécifique de la prostate mais non spécifique du cancer. ØDépistage +++ ØLa valeur normale du PSA total< 4 ng/ml ØMais ce seuil varie en fonction de: • L’âge. • volume de la prostate ++ • Méthode de dosage Ø PSA >10 ng/ml = BIOPSIE

Echographie ER � Echostructure du cancer: ◦ ◦ hypoéchogène : 70% ++ isoéchogène : 30% hyperéchogène: exceptionnel ( dans formes évoluées) hétérogène: 95% � Siège: ◦ zone périphérique : 70% ◦ Plurifocal : 50% � Limites ± régulières. � Doppler: ◦ Hypervascularisé+++ ◦ Le caractère hypovasculaire n’exclue pas le Kc!
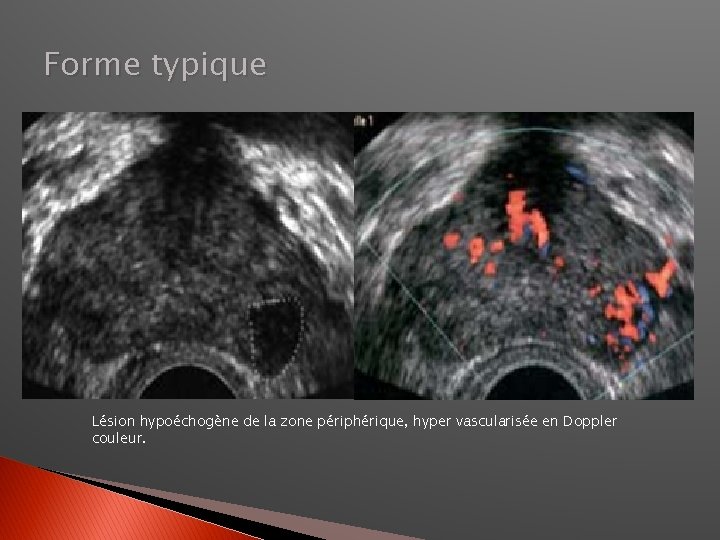
Forme typique Lésion hypoéchogène de la zone périphérique, hyper vascularisée en Doppler couleur.
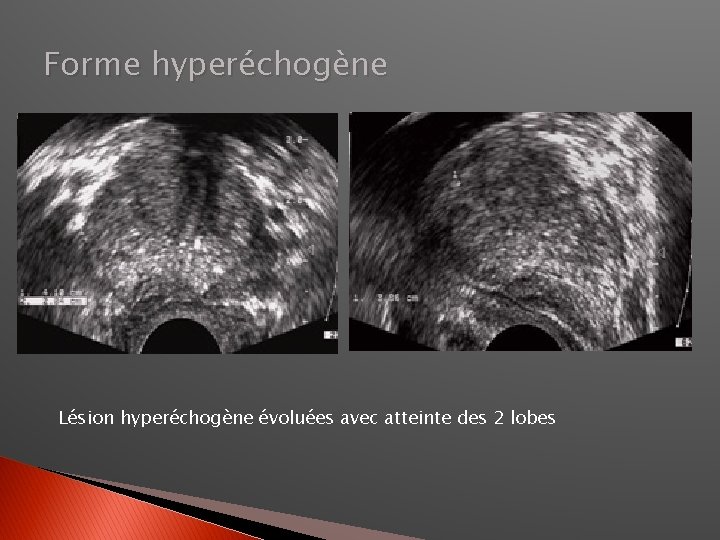
Forme hyperéchogène Lésion hyperéchogène évoluées avec atteinte des 2 lobes

Forme étendue
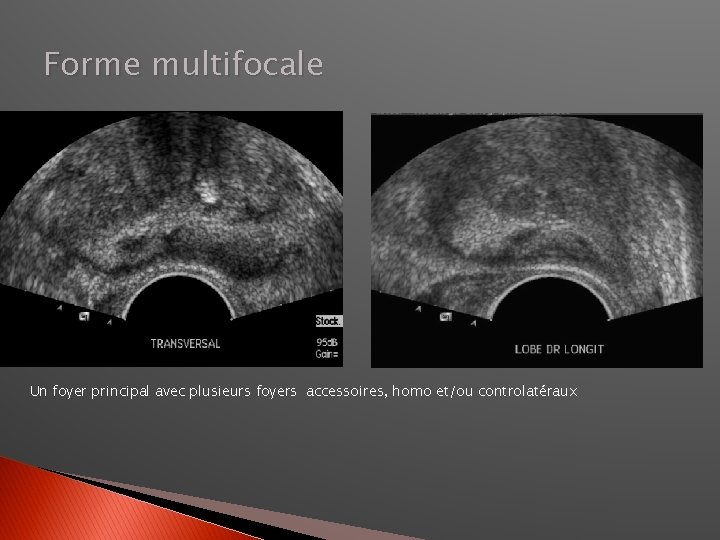
Forme multifocale Un foyer principal avec plusieurs foyers accessoires, homo et/ou controlatéraux
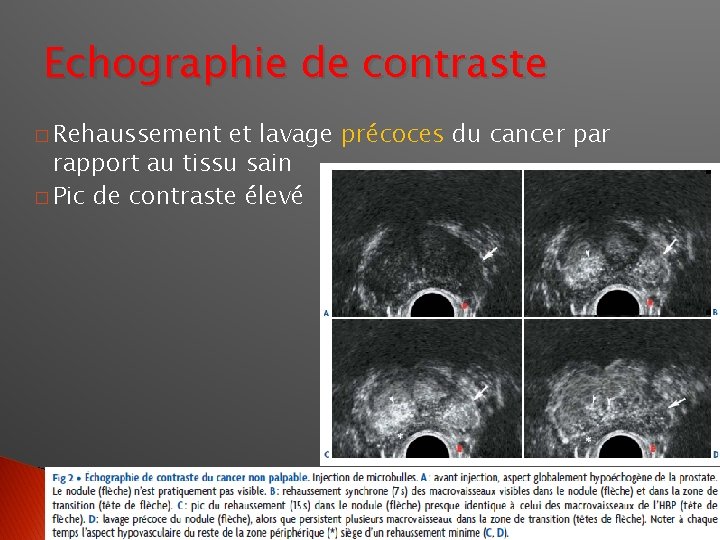
Echographie de contraste � Rehaussement et lavage précoces du cancer par rapport au tissu sain � Pic de contraste élevé

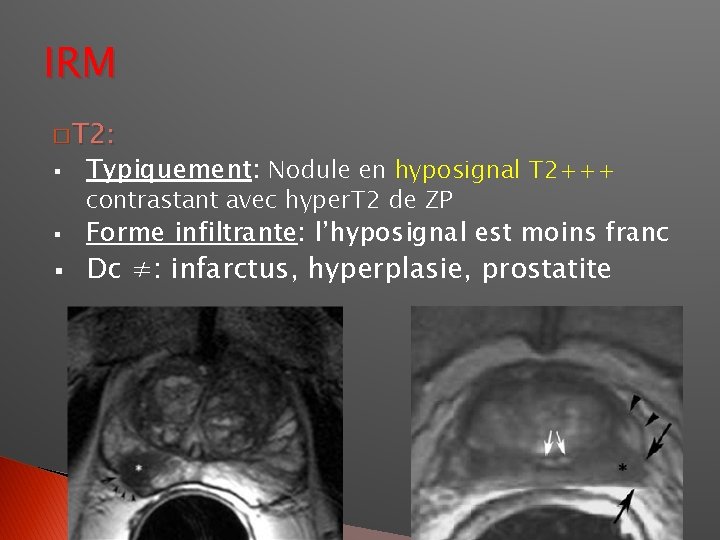
IRM � T 2: § Typiquement: Nodule en hyposignal T 2+++ § Forme infiltrante: l’hyposignal est moins franc § contrastant avec hyper. T 2 de ZP Dc ≠: infarctus, hyperplasie, prostatite

IRM � Perfusion: § wash-in: rehaussement intense et précoce wash-out plus rapide § Limites : § �ZT : cinétique vasculaire ~ cancer �HBP et prostatite �tumeur étendue: il n’y a pas suffisamment de tissu sain pour établir une discrimination fiable entre les deux tissus
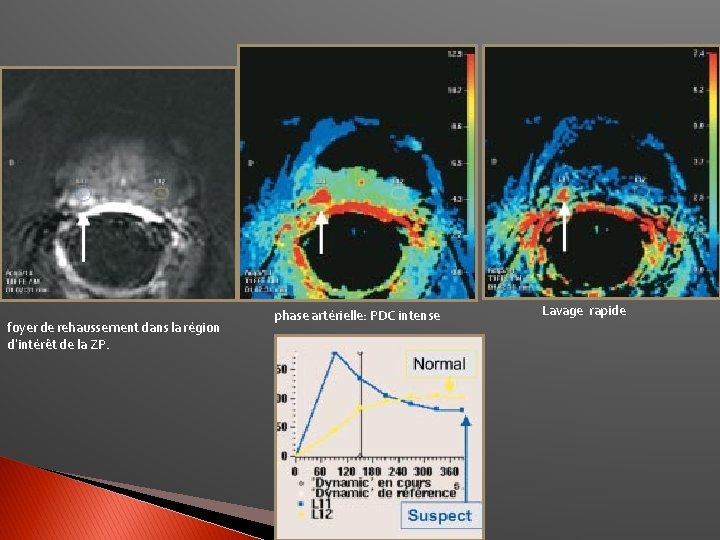
foyer de rehaussement dans la région d’intérêt de la ZP. phase artérielle: PDC intense Lavage rapide
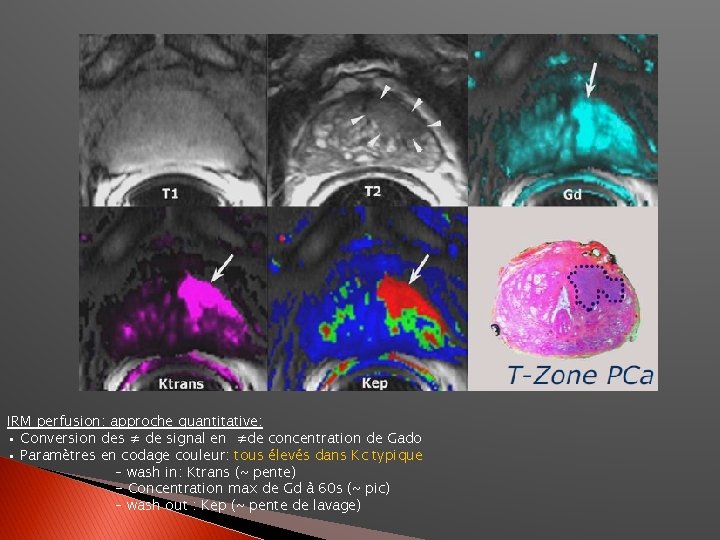
IRM perfusion: approche quantitative: • Conversion des ≠ de signal en ≠de concentration de Gado • Paramètres en codage couleur: tous élevés dans Kc typique – wash in: Ktrans (~ pente) - Concentration max de Gd à 60 s (~ pic) – wash out : Kep (~ pente de lavage)
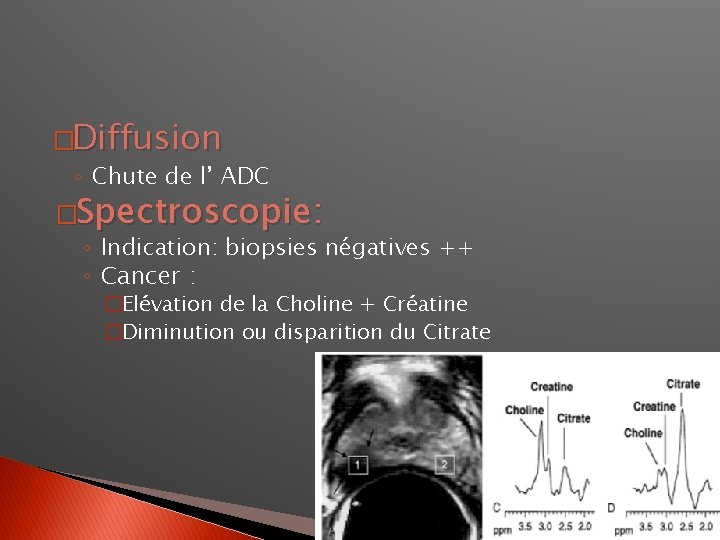
�Diffusion ◦ Chute de l’ ADC �Spectroscopie: ◦ Indication: biopsies négatives ++ ◦ Cancer : �Elévation de la Choline + Créatine �Diminution ou disparition du Citrate

BILAN D’EXTENSION

Extension capsulaire � Echographie: ◦ Déformation des contours de la capsule. ◦ Bombement irrégulier du liseré échogène périprostatique. ◦ Infiltration de la graisse périprostatique.

Extension capsulaire � IRM: ◦ ◦ ◦ Interruption, épaississement de la capsule Bombement focalisé du contour prostatique Infiltration de la graisse périprostatique Asymétrie des bandelettes neurovasculaires (lat) Interruption des plexus veineux périprostatiques (ant)
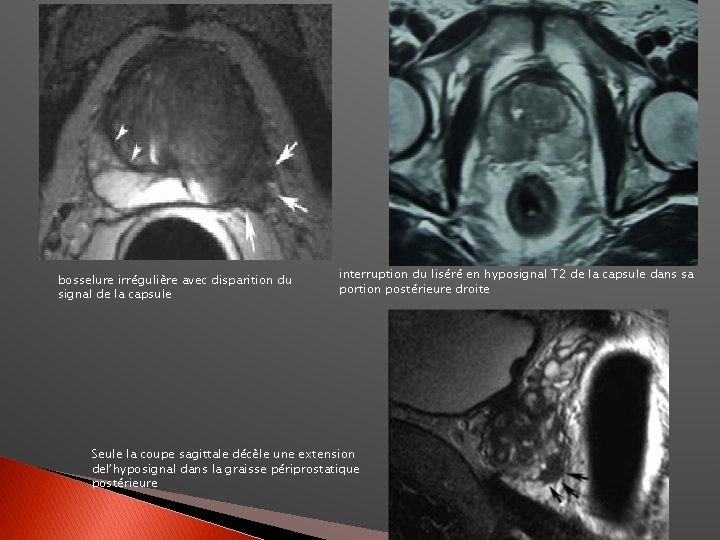
bosselure irrégulière avec disparition du signal de la capsule interruption du liséré en hyposignal T 2 de la capsule dans sa portion postérieure droite Seule la coupe sagittale décèle une extension del’hyposignal dans la graisse périprostatique postérieure
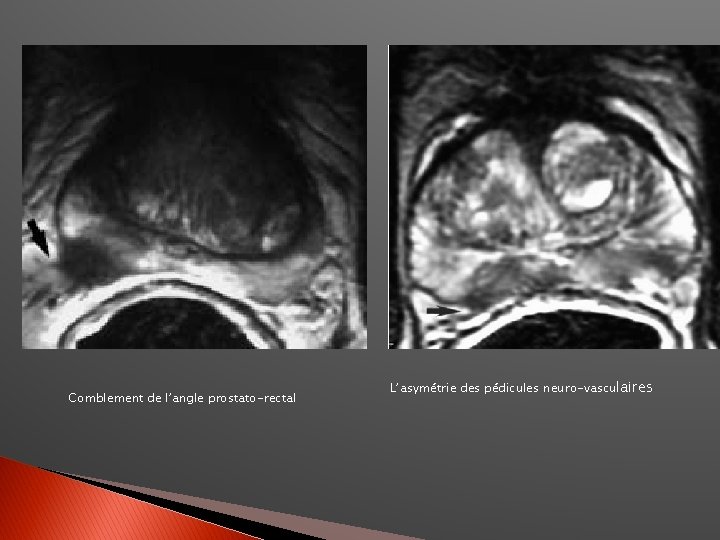
Comblement de l’angle prostato-rectal L’asymétrie des pédicules neuro-vasculaires

Envahissement des VS � Echographie: § Disparition de l’angle aigu échogène de l’espace graisseux entre les vésicules et la base de la prostate. § Modification de la taille ou de l’échostructure de la VS.

Envahissement des VS � IRM: ◦ Envahissement massif: Dc facile: �hyposignal uni ou bilatéral visible dans tout ou une partie de la vésicule. ◦ Envahissement extraprostatique débutant: �les images lacunaires dans la racine des vésicules sont plus discrètes comparaison avec le côté opposé +++ ◦ Envahissement tout débutant: � épaississement de la paroi des tubes glandulaires dont la lumière n’est pas comblée.

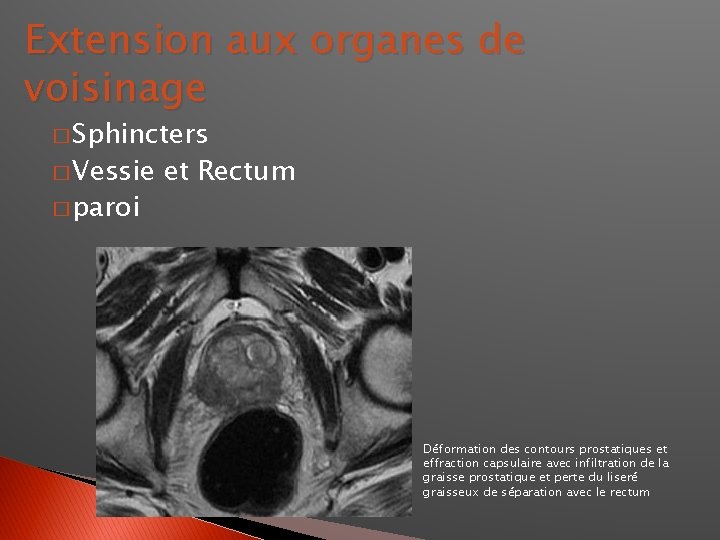
Extension aux organes de voisinage � Sphincters � Vessie � paroi et Rectum Déformation des contours prostatiques et effraction capsulaire avec infiltration de la graisse prostatique et perte du liseré graisseux de séparation avec le rectum

Extension ganglionnaire � implications pronostiques et thérapeutiques majeures. � IRM: � coupe coronale en séquence T 1+++ gg pelviens (obturateurs et iliaques) � Critères gg LA de malignité: ◦ Forme arrondie ◦ Taille : grand axe > 0, 8 mm Mais fréquence des métastases gg avec taille normale. � Lympho IRM
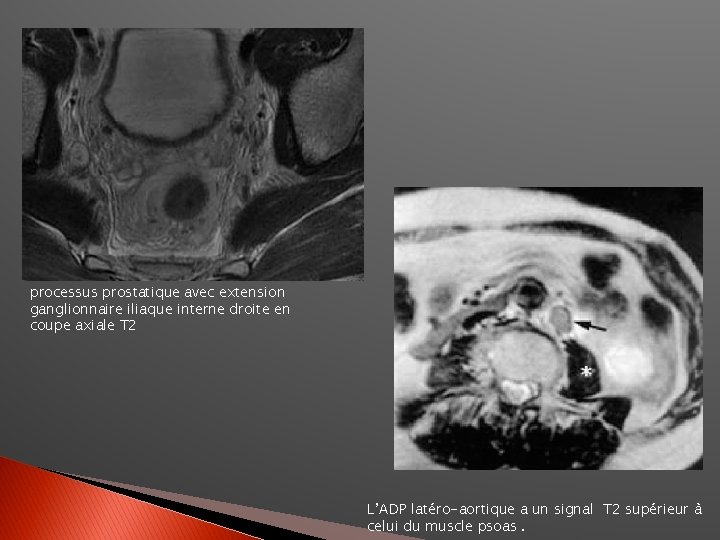
processus prostatique avec extension ganglionnaire iliaque interne droite en coupe axiale T 2 L’ADP latéro-aortique a un signal T 2 supérieur à celui du muscle psoas.
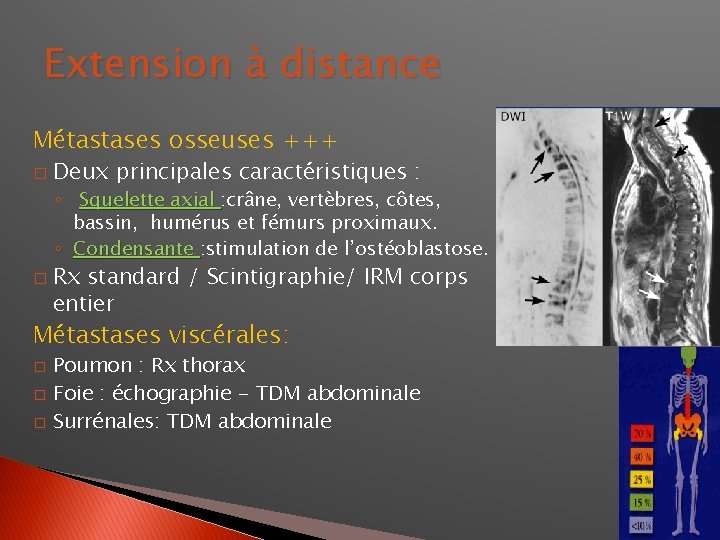
Extension à distance Métastases osseuses +++ � Deux principales caractéristiques : ◦ Squelette axial : crâne, vertèbres, côtes, bassin, humérus et fémurs proximaux. ◦ Condensante : stimulation de l’ostéoblastose. � Rx standard / Scintigraphie/ IRM corps entier Métastases viscérales: � � � Poumon : Rx thorax Foie : échographie - TDM abdominale Surrénales: TDM abdominale

Classification TNM � Stade T: ◦ Tx: tumeur non évaluable ◦ T 0: pas de tumeur locale décelable ◦ T 1: tumeur non palpable et non visible sur l'imagerie de découverte histologique � T 1 a: découverte histologique, moins de 5 % du tissu réséqué avec score de Gleason < 7 � T 1 b: découverte histologique, plus de 5 % du tissu réséqué, et/ou score de Gleason >= 7 � T 1 c: tumeur découverte sur des biopsies faite devant une élévation du PSA ◦ T 2: tumeur limitée à la prostate � T 2 a: tumeur limitée à un lobe � T 2 b: tumeur envahissant les deux lobes ◦ T 3: tumeur dépassant la capsule � T 3 a: envahissement capsulaire � T 3 b: envahissement des vésicules séminales ◦ T 4: tumeur fixée ou envahissant les structures voisines (sphincter externe, rectum, releveurs de l’anus, paroi pelvienne). � Stade N: ◦ Nx: ganglions locaux non évaluables ◦ N 0: pas d'envahissement ganglionnaire. ◦ N 1: atteinte ganglionnaire régionale. � Stade M: ◦ M 0: pas d'atteinte métastatique ◦ M 1: métastases à distance.

TRAITEMENT

Traitement � Buts: � Méthodes: multiples et en évolution: ◦ Curatif ◦ Palliatif ◦ Rattrapage (en cas de récidive) ◦ Surveillance ◦ Conservateurs: � Curithérapie � Thérapies focales: cryothérapie, ultrasons focalisés, photothérapie ◦ Radical: chirurgie ◦ hormonothérapie ◦ RTH: récidives � Indications dépendent de: ◦ ◦ Espérance de vie Rapport bénéfice /risque Stade +++ Grade

SURVEILLANCE POST THERAPEUTIQUE

Moyens de surveillance: ◦ PSA+++: �si ttt radical �Apres 3à 4 semaines �Toute élévation des PSA =récidive biologique recher une récidive locale par IRM. �Valeur seuil PSA variable / méthode thérapeutique: �PSA> 0, 2 ng/ml: après prostatectomie radicale �PSA > 2 ng/ ml: après RTH externe ◦ IRM: �Si récidive biologique après ttt radical �dynamique, spectro �Recher: �Récidive métastatique ( micro. M) �Récidive locale : ttt rattrapage! ◦ Echo ER: �si ttt conservateur � l’évolution du volume tumoral. � la normalisation des contours de la prostate.

Surveillance: § Récidive locale: ◦ IRM en T 2: �hyposignal diffus de la prostate �détection difficile d’une récidive ◦ IRM dynamique+++: �Récidive hypervasculaire au sein d’une fibrose post radique hypo vasculaire ◦ Spectro IRM: �réapparition d’un pic de choline �Non spécifique

Processus hétérogène en hyposignal T 2 an niveau de la loge de prostatectomie en coupes axiale et sagittale



CONCLUSION

Kc prostate actuellement bénéficie de: � PSA+++: dépistage précoce de la Tm initiale et de la récidive � Méthodes thérapeutiques plus efficaces � Développement de l’imagerie ( IRM fonctionnelle): joue actuellement un rôle primordiale dans la PEC pré et post thérapeutique du cancer de la prostate

Références � � � � F Cornud, O Rouvière. Imagerie du cancer de la prostate. FMC 2009 P Puech, A Sufana –lancu, B Renard, A. Villers. Pourquoi et comment detecter le cancer de la prostate en IRM? J Radiol 2012; 93: 291 -300 O Rouvière. Imagerie des récidives locales du cancer de la prostate. J Radiol 2012; 93: 302 -313 A Villlers, F Marliere, A Ouzzane, P Puech. L’IRM en complément ou en rempolacement des biopsies de la prostate? Le point de vue du clinicien. J Radiol 2012; 93: 285 -290 F Cornud, R Oyen. Place de l’imagerie dans le diagnostic et le bilan d’extension des adénocarcinomes de prostate. J Radiol 2002; 83: 863 -880 L. Lemaitre, A. Delebarre, A. Villers, P. Puech. Échographie et imagerie par résonance magnétique de la prostate normale. EMC 34420 -A-10 V Ravery, E Fontaine , A Villers. Biopsies prostatiques : modalités techniques et conditions de l’examen. Progrès en Urologie (2000), 10, 1271 -1276
- Slides: 75