Il vettore energetico idrogeno Metodi di produzione Francesco

















- Slides: 21

Il vettore energetico idrogeno Metodi di produzione Francesco La Fata

Introduzione • L’economia del petrolio e l’economia dell’idrogeno • Jeremy Rifkin • Protocollo di Kyoto (2010 = 6, 5 % sul 1990) • Negli ultimi 4 anni le emissioni sono cresciute del 5, 6 %.

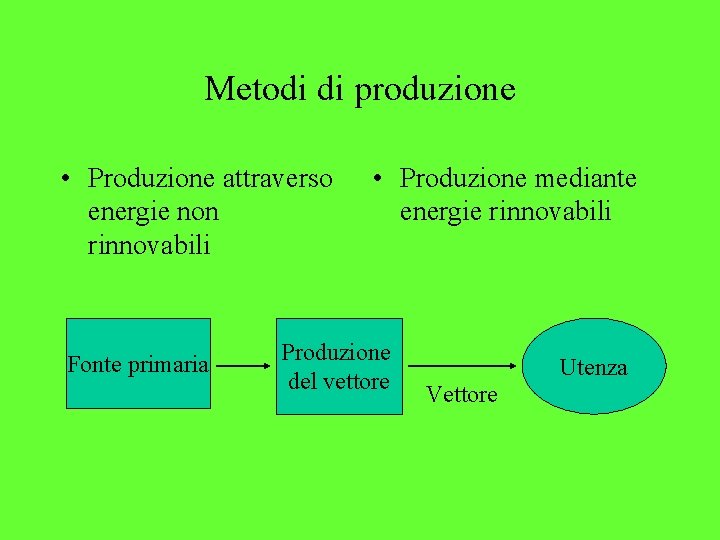
Metodi di produzione • Produzione attraverso energie non rinnovabili Fonte primaria • Produzione mediante energie rinnovabili Produzione del vettore Utenza Vettore

Metodi di produzione da fonti non rinnovabili • • • Scissione catalitica diretta del metano Reforming del metano Gassificazione del carbone Decomposizione termochimica dell’acqua Elettrolisi dell’acqua basata su energia elettrica (da idrocarburi e da nucleare)

Scissione catalitica diretta del metano • Rottura diretta della molecola di metano, in presenza di catalizzatori, ad una temperatura compresa fra i 640 e i 980 °C, secondo • CH 4 C + 2 H 2

Reforming del metano • • • Il processo di reforming del metano è basato su due reazioni. La prima, principale ed endotermica CH 4 + H 2 O CO + 3 H 2 La seconda, esotermica CO + H 2 O CO 2 +H 2 La somma delle due reazioni, endotermica • CH 4 + 2 H 2 O CO 2 + 4 H 2, • Affinché tale reazione avvenga bisogna fornire quantità di calore ad un temperatura compresa fra i 700 e i 900 °C.

Gassificazione del carbone 1 • Primo metodo • La gassificazione avviene due reazioni parziali, globalmente endotermiche • C + H 2 OVAP CO + H 2 • CO + H 2 O CO 2 + H 2 • C + 2 H 2 OVAP CO 2 + 2 H 2 • La reazione prende quantità di calore dalla stessa massa di carbone in reazione (900 °C<T<1100 °C)

Gassificazione del carbone 2 • Secondo metodo • • Si procede idrogenando il carbone secondo la C + 2 H 2 CH 4 + H 2 O CO + 3 H 2 CO + H 2 O CO 2 + H 2 • C + 2 H 2 O CO 2 + 2 H 2 • La reazione è sempre endotermica ma necessita di temperature inferiori (650 °C<T<850 °C)

Decomposizione termochimica dell’acqua • • • Il sistema si basa sulla realizzazione di un ciclo termochimico chiuso in presenza di catalizzatori. Si fanno avvenire una serie di reazioni, in genere ad elevata temperatura, fornendo quantità di energia. Un esempio di un ciclo è Ca. Br 2 + 2 H 2 O Ca(OH)2 + 2 HBr 730 °C 2 HBr + Hg Hg. Br 2 + H 2 200 °C Hg. Br 2 + Ca(OH)2 Ca. Br 2 +Hg. O + H 2 O 200 °C Hg. O Hg + 1/2 O 2 600 °C • H 2 O • • Questo ciclo è stato studiato da Marchetti presso l’Euratom di Ispra. I cicli, all’origine, utilizzavano elevate temperature e prodotti corrosivi e/o tossici. I più recenti minimizzano gli inconvenienti. Il rendimento si aggira sul 50%. 1/2 O 2 + H 2

Decomposizione elettrolitica dell’acqua • Si cita esclusivamente in quanto il processo è troppo noto ed è la base degli attuali metodi di produzione. • Elettrolisi acida (H 2 SO 4) • Catodo 4 H 3 O+ + 4 e • Anodo 6 H 2 O • 2 H 2 O 4 H + 4 H 2 O 2 O + 4 H 3 O+ + 4 e O 2 + 2 H 2

Metodi di produzione da fonti rinnovabili • • Energia solare indiretta Energia eolica Energia geotermica Energia solare diretta Energia da biomasse Processi microbici e biochimici Energia elettrica da impianti idroelettrici e similari (maree, etc)

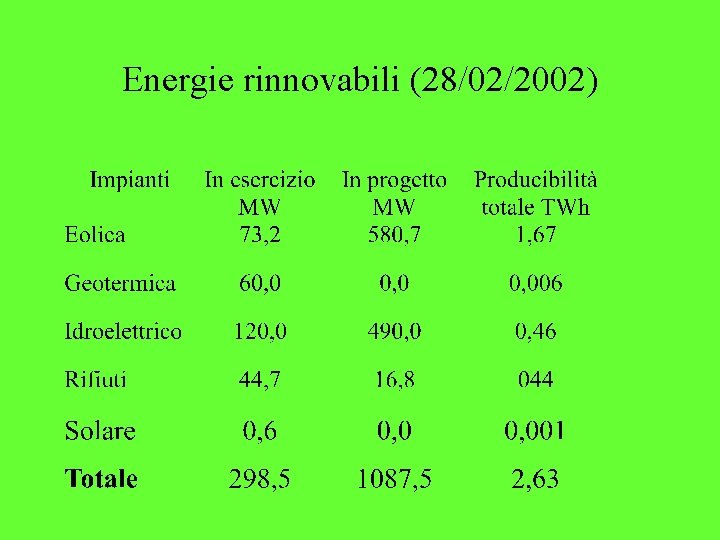
Energie rinnovabili (28/02/2002)

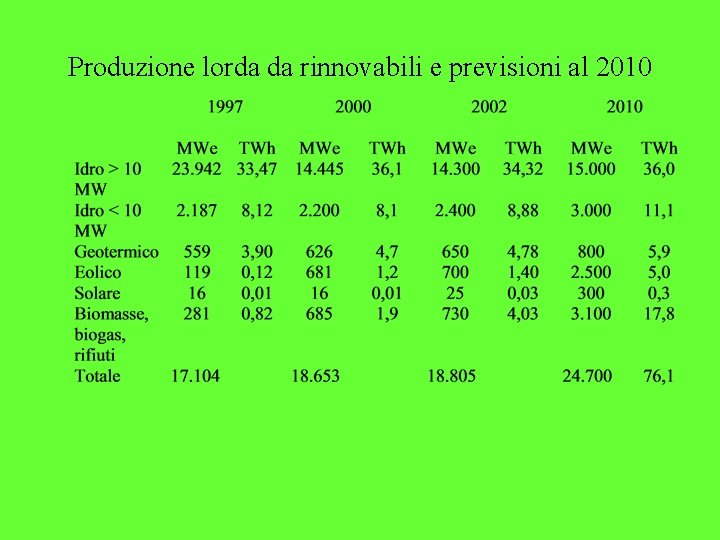
Produzione lorda da rinnovabili e previsioni al 2010

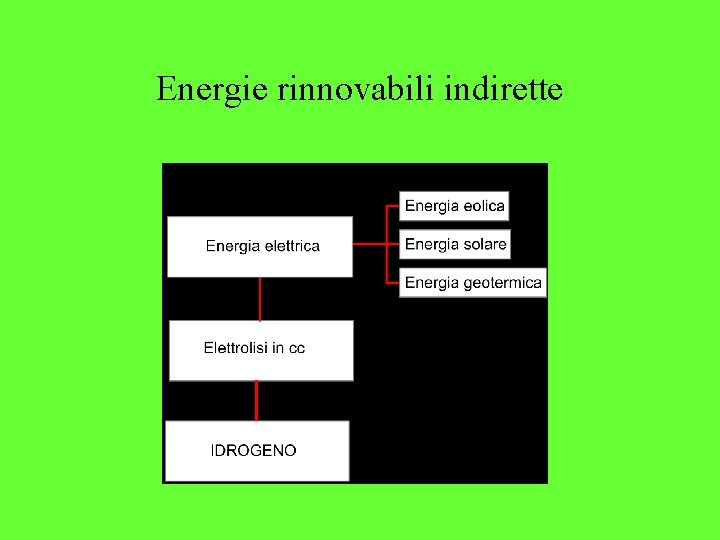
Energie rinnovabili indirette

Energia solare indiretta • L’energia solare viene utilizzata attraverso le celle fotovoltaiche trasformano la radiazione solare (1 k. W/m 2 valore medio incidente) direttamente e staticamente in energia elettrica continua che a sua volta alimenta un processo di elettrolisi dell’acqua. • Una strada di minor rendimento è quella di utilizzare centrali solari a specchi per produrre vapore d’acqua e, attraverso vari passaggi, energia elettrica da impiegare nell’elettrolisi.

Energia eolica • L’energia eolica viene sfruttata, tramite aerogeneratori (eliche e alternatori) per la produzione di energia elettrica che a sua volta viene utilizzata per la decomposizione elettrolitica dell’acqua.

Energia geotermica • L’energia geotermica sfrutta le sorgenti naturali di calore quali quelle di Larderello o Islandesi dalle quali si prelevano quantità di calore (vapore d’acqua ad elevata T) che attraverso l’espansione in turbina, producono energia meccanica che a sua volta viene trasformata da alternatori in energia elettrica utilizzata per l’elettrolisi dell’acqua.

Energie rinnovabili dirette

Energia solare diretta • Tale processo si basa su una reazione fotochimica diretta • H 2 O + Energia solare 1/2 H 2 O + H 2 • Utilizzando apposite cellule elettrofotochimiche dove il catalizzatore è Ti. O 2 si ha • Ti. O 2 + 2 hn 2 e- + 2 p+ • 2 p+ + 2 H 2 O • 2 H+ + 2 e- 1/O 2 + 2 H+ H 2 • 2 H 2 O + 2 hn 1/O 2 + H 2 • • • dove h = l’energia del fotone incidente n= frequenza dell’onda associata

Biomasse • Per biomassa si intende l’insieme totale degli organismi vegetali combustibili. Viene assimilato ad essa il biogas (CH 4) estratto dalla fermentazione delle masse vegetali, dai rifiuti organici e dalle deiezioni animali. • L’energia ricavabile dalla diretta combustione o la scomposizione diretta del metano può essere utilizzata per la produzione di idrogeno.

Processi microbici e biochimici • Processi a cellula intatta (microbici) • • • Sono processi naturali che sfruttano la capacità di molti batteri ed alghe fotosintetizzanti che esposti alla luce solare producono naturalmente H 2. Sono necessari ampie superfici di coltivazione, energia solare sufficiente e complessi sistemi di raccolta dell’idrogeno prodotto. Si ottengono sottoprodotti di notevole valore (mangimi animali, etc). • Processi a cellula libera (biochimici) • Il procedimento consiste nell’isolare dalla cellula sola la parte utile per la produzione di idrogeno per evitare la crescita e la moltiplicazione eccessiva del biocorpo (utilizzazione vivente ma statica). Anche in questo caso si ottengono sottoprodotti di notevole valore. Il rendimento aumenta anche per il risparmio energetico legato alla mancanza di fasi moltiplicative.