Il momento di dipolo elettrico assorbimento 2 M
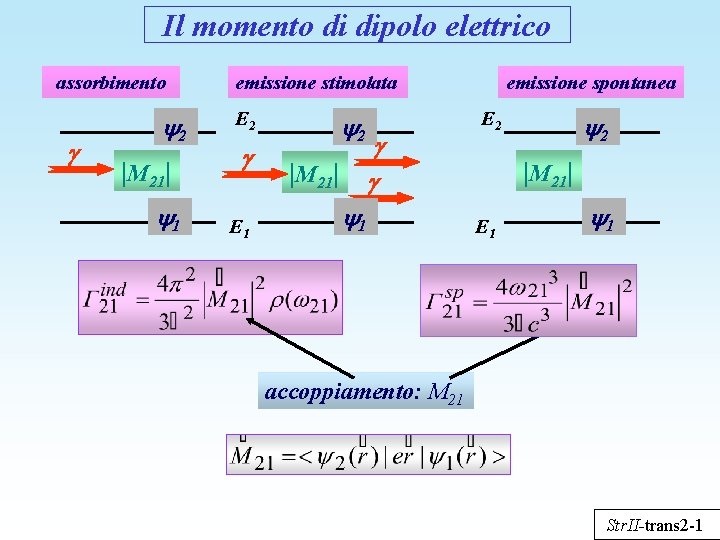
Il momento di dipolo elettrico assorbimento 2 |M 21| 1 emissione stimolata E 2 E 1 2 |M 21| 1 emissione spontanea E 2 2 |M 21| E 1 1 accoppiamento: M 21 Str. II-trans 2 -1
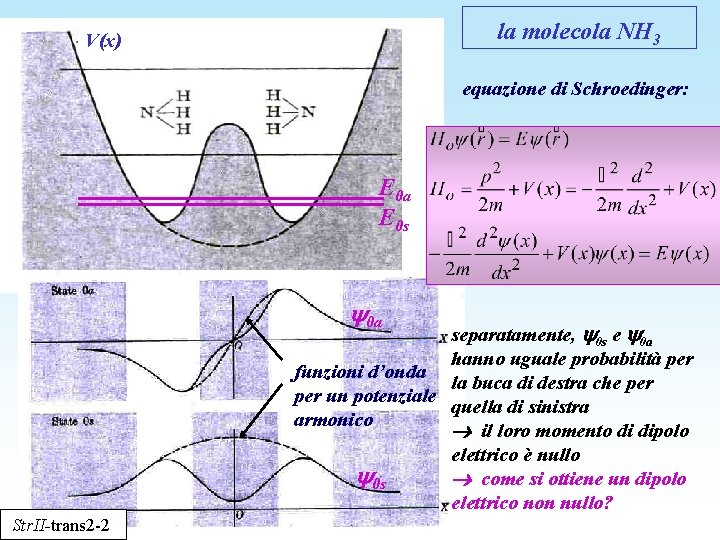
la molecola NH 3 V(x) equazione di Schroedinger: E 0 a E 0 s 0 a separatamente, 0 s e 0 a hanno uguale probabilità per funzioni d’onda la buca di destra che per un potenziale quella di sinistra armonico il loro momento di dipolo elettrico è nullo 0 s come si ottiene un dipolo elettrico non nullo? Str. II-trans 2 -2
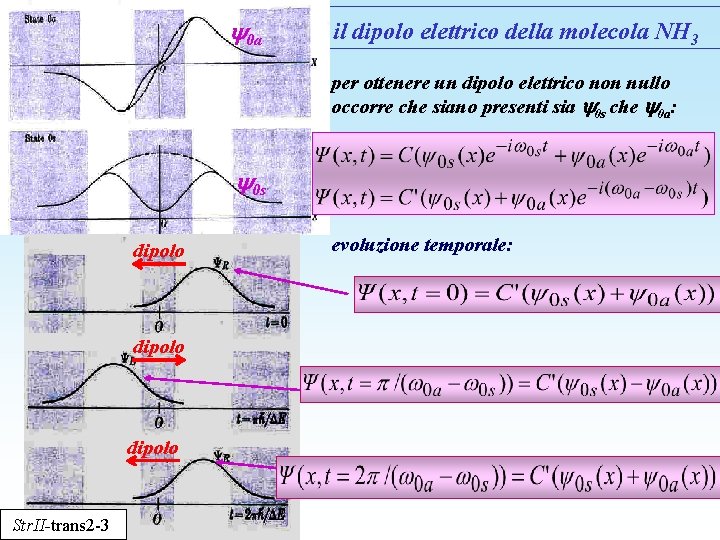
0 a il dipolo elettrico della molecola NH 3 per ottenere un dipolo elettrico non nullo occorre che siano presenti sia 0 s che 0 a: 0 s dipolo Str. II-trans 2 -3 evoluzione temporale:
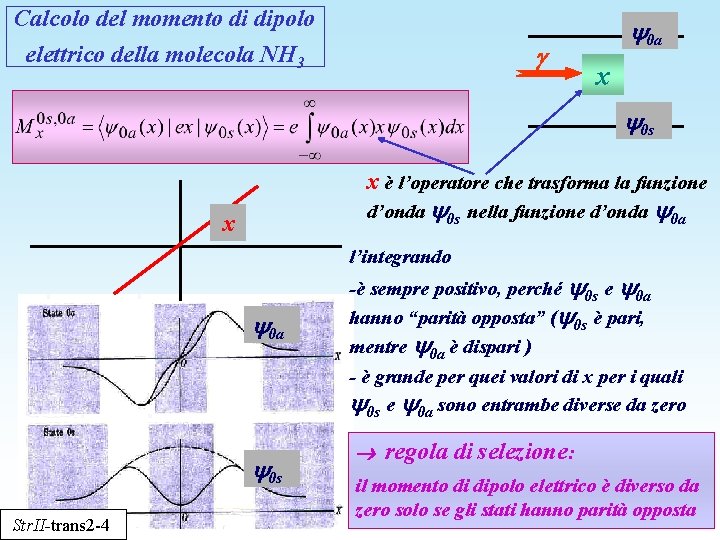
Calcolo del momento di dipolo elettrico della molecola NH 3 0 a x 0 s x è l’operatore che trasforma la funzione d’onda 0 s nella funzione d’onda x 0 a l’integrando 0 a -è sempre positivo, perché 0 s e 0 a hanno “parità opposta” ( 0 s è pari, mentre 0 a è dispari ) - è grande per quei valori di x per i quali 0 s e 0 a sono entrambe diverse da zero 0 s Str. II-trans 2 -4 regola di selezione: il momento di dipolo elettrico è diverso da zero solo se gli stati hanno parità opposta
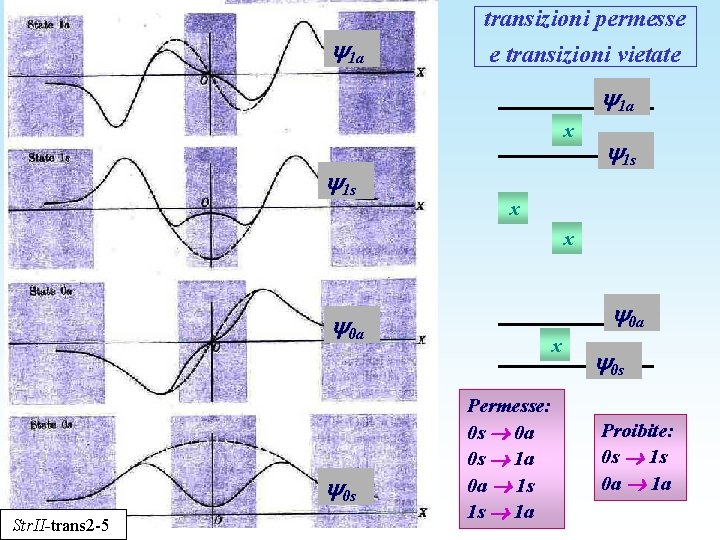
transizioni permesse 1 a e transizioni vietate 1 a x 1 s x x 0 a 0 s Str. II-trans 2 -5 x Permesse: 0 s 0 a 0 s 1 a 0 a 1 s 1 s 1 a 0 s Proibite: 0 s 1 s 0 a 1 a

atomi idrogenoidi: descrizione quantistica Potenziale: Hamiltoniana: Numeri quantici: - n energia totale - l momento angolare En= - ERZ 2/n 2 L 2 = l(l+1) - ml componente di L lungo l’asse z 2 L z= m l - ms componente dello spin lungo l’asse z S z= m s sono permessi solo i valori di E, L 2, Lz corrispondenti ai valori interi dei numeri quantici n 1 ; 0 l < n ; -l ml l Str. II-trans 2 -6
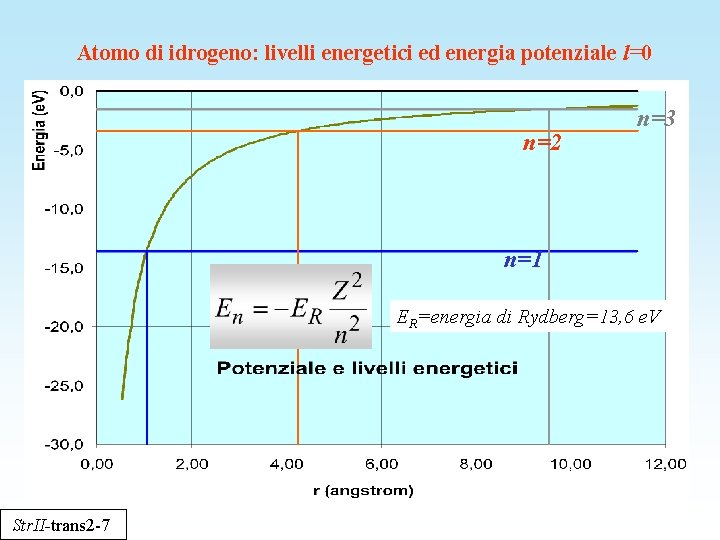
Atomo di idrogeno: livelli energetici ed energia potenziale l=0 n=2 n=3 n=1 ER=energia di Rydberg=13, 6 e. V Str. II-trans 2 -7

Atomo di idrogeno: equazione di Schrödinger z r y x probabilità di trovare l’elettrone nell’elemento di volume r 2 drd intorno al punto (x, y, z) Str. II-trans 2 -8
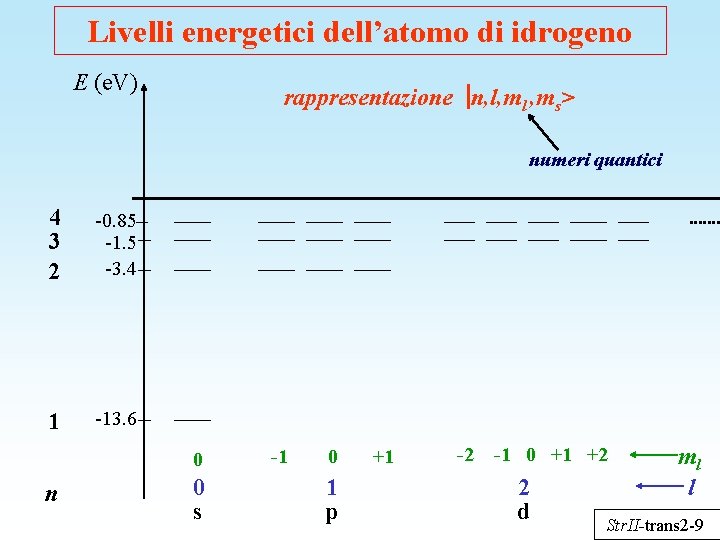
Livelli energetici dell’atomo di idrogeno E (e. V) rappresentazione n, l, ml , ms> numeri quantici 4 3 2 -0. 85 -1. 5 -3. 4 1 -13. 6 0 n 0 s -1 0 1 p +1 -2 -1 0 +1 +2 2 d ml l Str. II-trans 2 -9
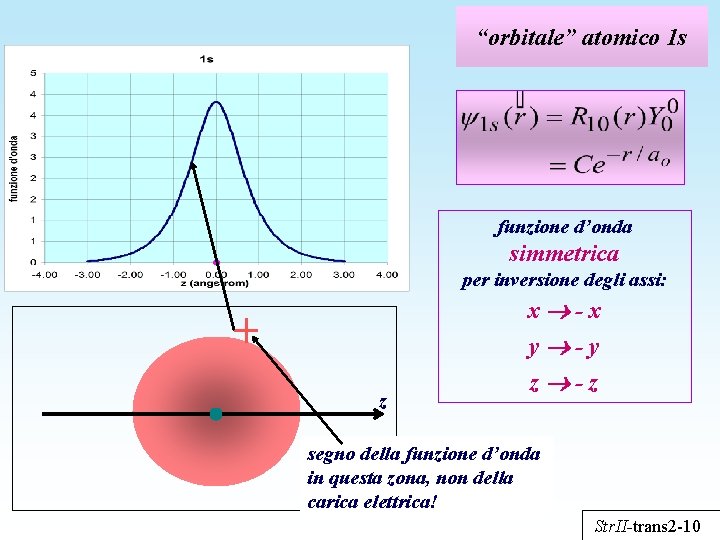
“orbitale” atomico 1 s funzione d’onda simmetrica per inversione degli assi: z x -x y -y z -z segno della funzione d’onda in questa zona, non della carica elettrica! Str. II-trans 2 -10
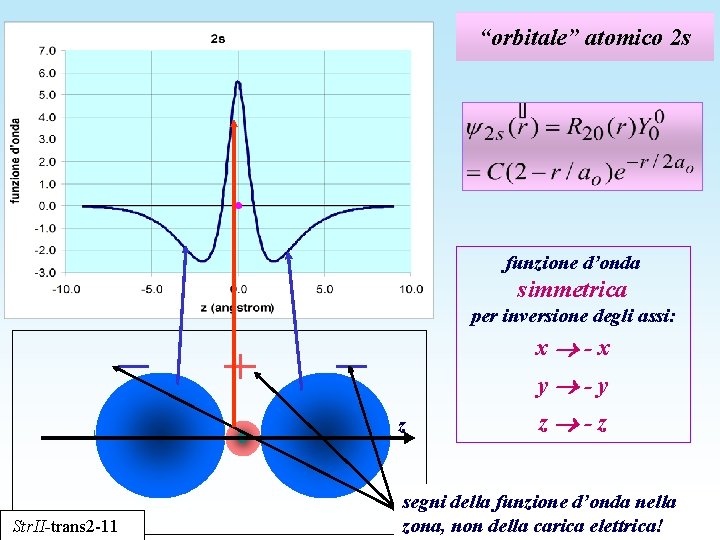
“orbitale” atomico 2 s funzione d’onda simmetrica per inversione degli assi: x -x y -y z Str. II-trans 2 -11 z -z segni della funzione d’onda nella zona, non della carica elettrica!
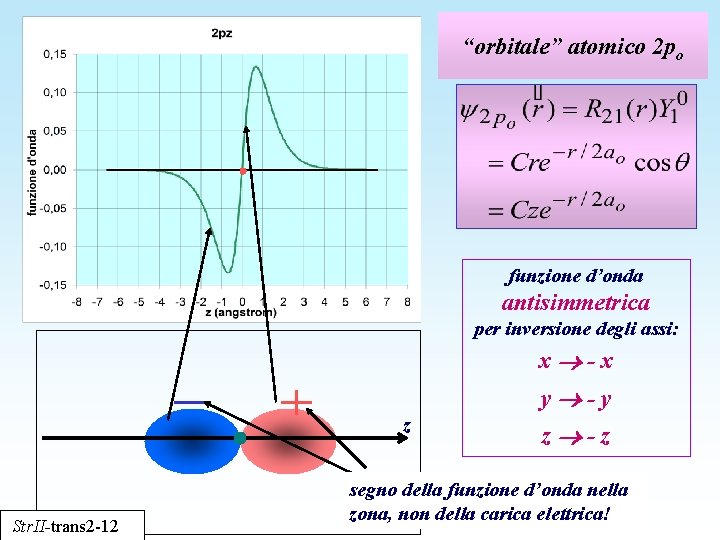
“orbitale” atomico 2 po funzione d’onda antisimmetrica per inversione degli assi: x -x y -y z Str. II-trans 2 -12 z -z segno della funzione d’onda nella zona, non della carica elettrica!
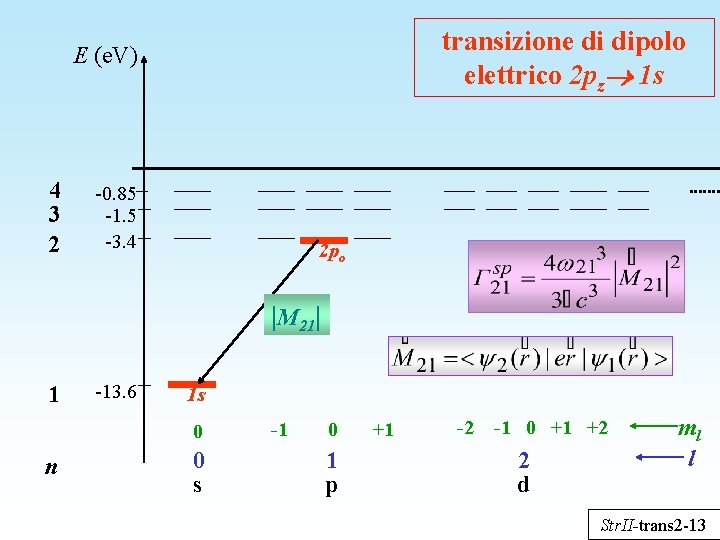
transizione di dipolo elettrico 2 pz 1 s E (e. V) 4 3 2 -0. 85 -1. 5 -3. 4 2 po |M 21| 1 -13. 6 1 s 0 n 0 s -1 0 1 p +1 -2 -1 0 +1 +2 2 d ml l Str. II-trans 2 -13
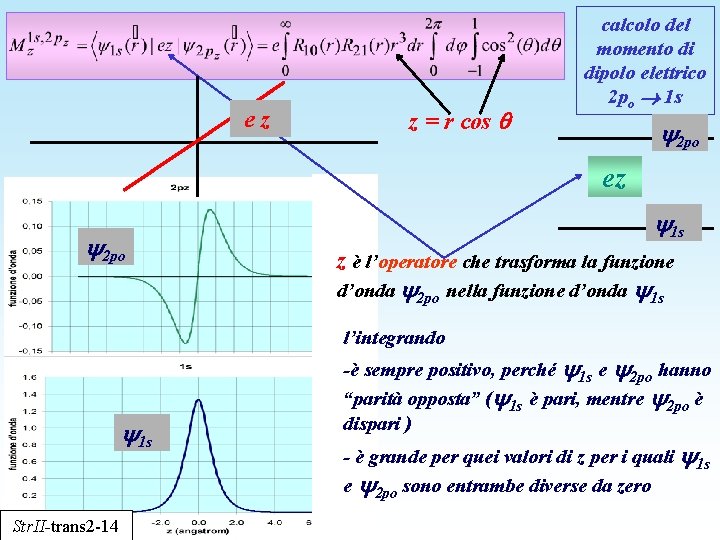
ez z = r cos calcolo del momento di dipolo elettrico 2 po 1 s 2 po ez 2 po 1 s z è l’operatore che trasforma la funzione d’onda 2 po nella funzione d’onda 1 s l’integrando 1 s Str. II-trans 2 -14 -è sempre positivo, perché 1 s e 2 po hanno “parità opposta” ( 1 s è pari, mentre 2 po è dispari ) - è grande per quei valori di z per i quali 1 s e 2 po sono entrambe diverse da zero
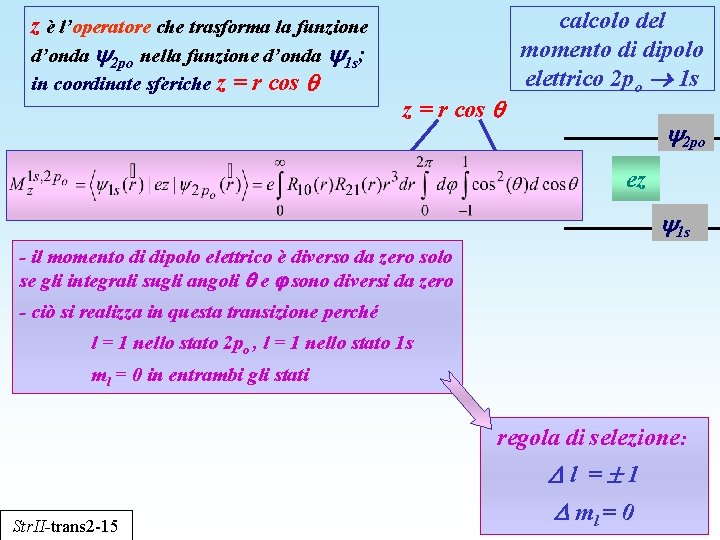
z è l’operatore che trasforma la funzione d’onda 2 po nella funzione d’onda 1 s; in coordinate sferiche z = r cos calcolo del momento di dipolo elettrico 2 po 1 s 2 po ez 1 s - il momento di dipolo elettrico è diverso da zero solo se gli integrali sugli angoli e sono diversi da zero - ciò si realizza in questa transizione perché l = 1 nello stato 2 po , l = 1 nello stato 1 s ml = 0 in entrambi gli stati regola di selezione: Str. II-trans 2 -15 l = 1 ml = 0
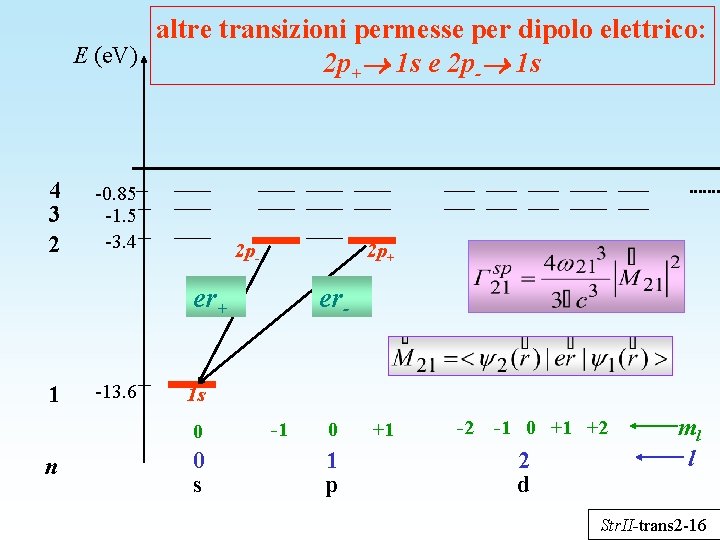
altre transizioni permesse per dipolo elettrico: E (e. V) 2 p+ 1 s e 2 p- 1 s 4 3 2 -0. 85 -1. 5 -3. 4 2 p- 2 p+ er+ 1 -13. 6 1 s 0 n er- 0 s -1 0 1 p +1 -2 -1 0 +1 +2 2 d ml l Str. II-trans 2 -16
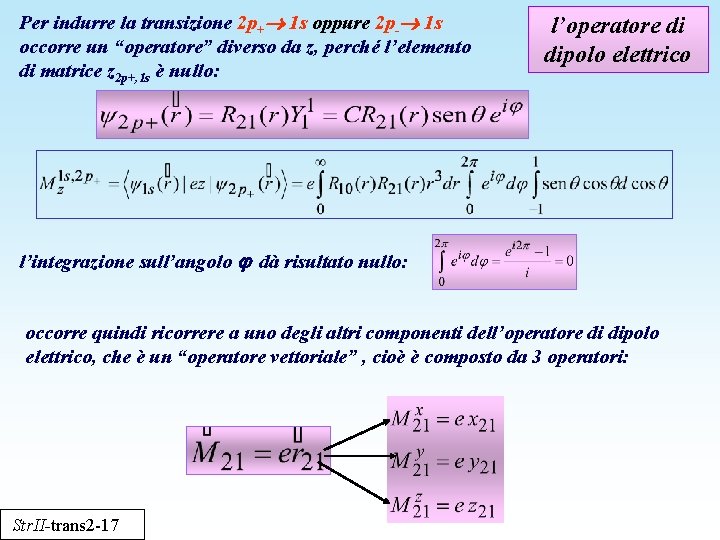
Per indurre la transizione 2 p+ 1 s oppure 2 p- 1 s occorre un “operatore” diverso da z, perché l’elemento di matrice z 2 p+, 1 s è nullo: l’operatore di dipolo elettrico l’integrazione sull’angolo dà risultato nullo: occorre quindi ricorrere a uno degli altri componenti dell’operatore di dipolo elettrico, che è un “operatore vettoriale” , cioè è composto da 3 operatori: Str. II-trans 2 -17
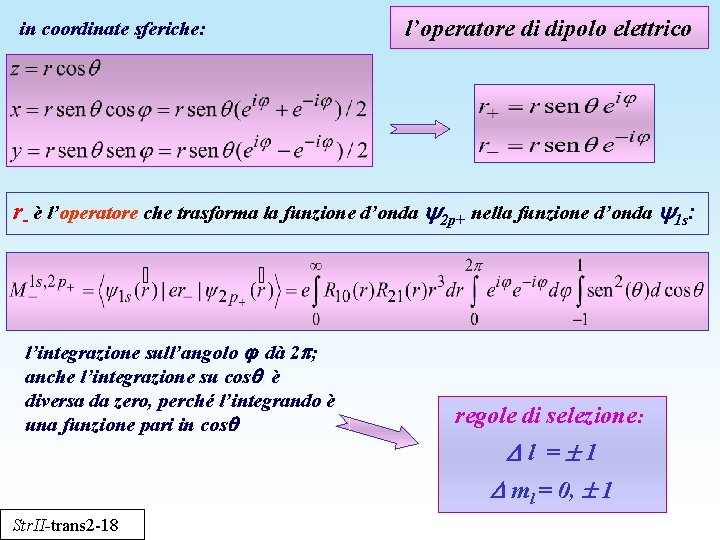
in coordinate sferiche: l’operatore di dipolo elettrico r- è l’operatore che trasforma la funzione d’onda 2 p+ nella funzione d’onda 1 s: l’integrazione sull’angolo dà 2 ; anche l’integrazione su cos è diversa da zero, perché l’integrando è una funzione pari in cos Str. II-trans 2 -18 regole di selezione: l = 1 ml = 0, 1
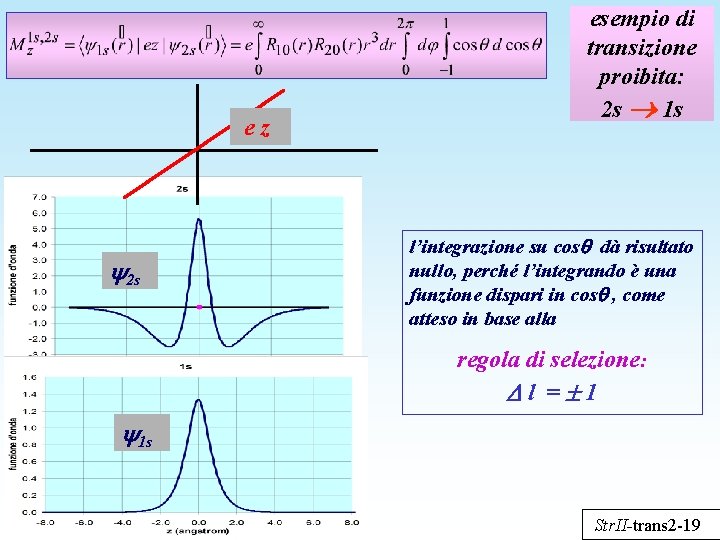
ez 2 s esempio di transizione proibita: 2 s 1 s l’integrazione su cos dà risultato nullo, perché l’integrando è una funzione dispari in cos , come atteso in base alla regola di selezione: l = 1 1 s Str. II-trans 2 -19
- Slides: 19