Il microbiota intestinale e la sua influenza sulla
Il microbiota intestinale e la sua influenza sulla fisiologia dell’ospite

Outline della lezione 1) Che cosa è il microbiota? 1) Maturazione del microbiota nel bambino; 1) Influenze del microbiota sul metabolismo; 1) Influenze del microbiota sul funzionamento neuronale e il comportamento.
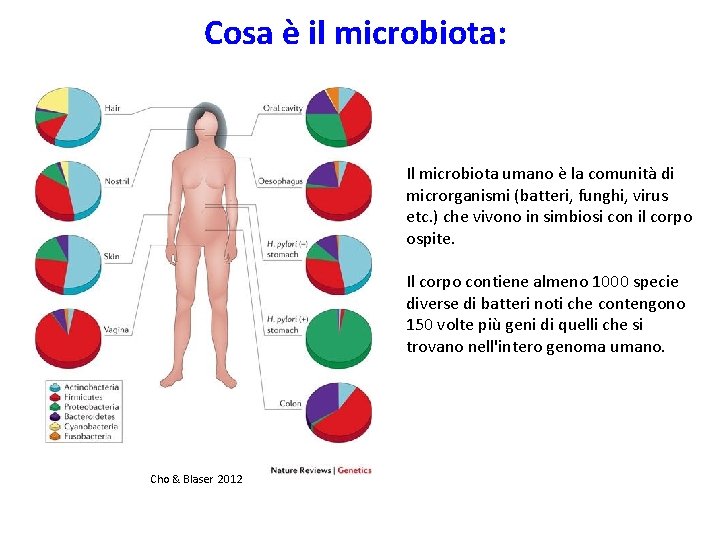
Cosa è il microbiota: Il microbiota umano è la comunità di microrganismi (batteri, funghi, virus etc. ) che vivono in simbiosi con il corpo ospite. Il corpo contiene almeno 1000 specie diverse di batteri noti che contengono 150 volte più geni di quelli che si trovano nell'intero genoma umano. Cho & Blaser 2012
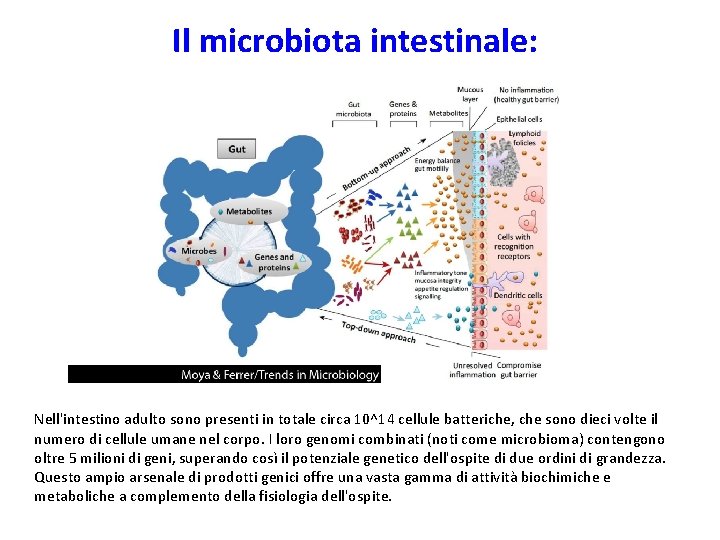
Il microbiota intestinale: Nell'intestino adulto sono presenti in totale circa 10^14 cellule batteriche, che sono dieci volte il numero di cellule umane nel corpo. I loro genomi combinati (noti come microbioma) contengono oltre 5 milioni di geni, superando così il potenziale genetico dell'ospite di due ordini di grandezza. Questo ampio arsenale di prodotti genici offre una vasta gamma di attività biochimiche e metaboliche a complemento della fisiologia dell'ospite.
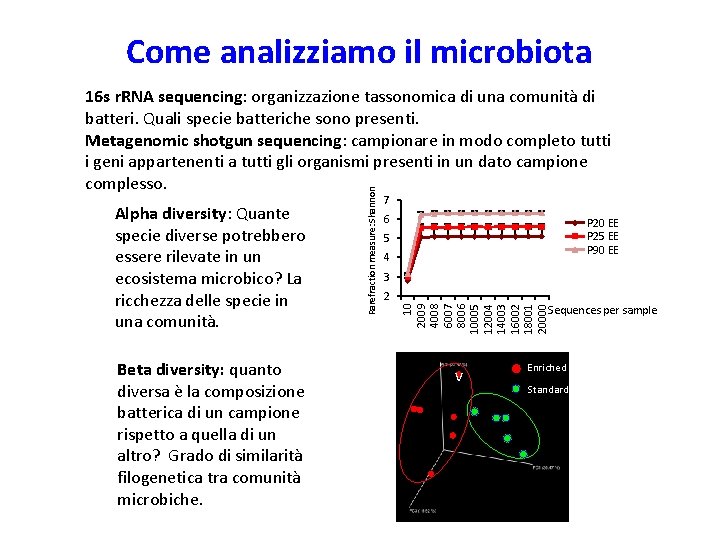
Come analizziamo il microbiota Beta diversity: quanto diversa è la composizione batterica di un campione rispetto a quella di un altro? Grado di similarità filogenetica tra comunità microbiche. 7 6 P 20 EE P 25 EE P 90 EE 5 4 3 2 Sequences per sample 10 2009 4008 6007 8006 10005 12004 14003 16002 18001 20000 Alpha diversity: Quante specie diverse potrebbero essere rilevate in un ecosistema microbico? La ricchezza delle specie in una comunità. Rarefraction measure: Shannon 16 s r. RNA sequencing: organizzazione tassonomica di una comunità di batteri. Quali specie batteriche sono presenti. Metagenomic shotgun sequencing: campionare in modo completo tutti i geni appartenenti a tutti gli organismi presenti in un dato campione complesso. v Enriched Standard

Glossario per la lezione ü Microbiota: I tipi di organismi presenti in un determinato ambiente, siano essi batteri, virus o eucarioti. ü Microbioma: L’insieme di diversi microbi e le loro funzioni o geni. ü ”Omica”: Un termine che descrive una serie di metodi, come la genomica, metabolomica, metagenomica, ecc. , che utilizziamo per esplorare interazioni tra i batteri nell'intestino e l'ospite. ü Metagenomica: Un metodo che ci consente di creare cataloghi di ciò che i batteri possono fare in base ai geni che hanno (e. g. funzioni metaboliche). ü Disbiosi: Un disturbo o uno squilibrio in un sistema biologico, ad esempio, cambiamenti nei tipi e nel numero di batteri nell'intestino che può portare allo sviluppo di diverse patologie. ü Probiotico: Microrganismi vivi che, quando somministrati in quantità adeguate, conferiscono un beneficio per la salute all'ospite. Esempi includono ceppi del genere Bifidobacterium e Lactobacillus. I probiotici possono avere interazioni multiple con l’ospite, compresa l'inibizione competitiva di altri microbi, effetti sulla funzione della barriera intestinale. ü Prebiotico: Composti presenti negli alimenti che inducono la crescita o l'attività di microrganismi benefici come batteri e funghi. Sono rappresentati in genere da fibre non digeribili che passano attraverso la parte superiore del tratto gastrointestinale e funzionando da substrati stimolando la crescita o l'attività di batteri vantaggiosi che colonizzano il colon.
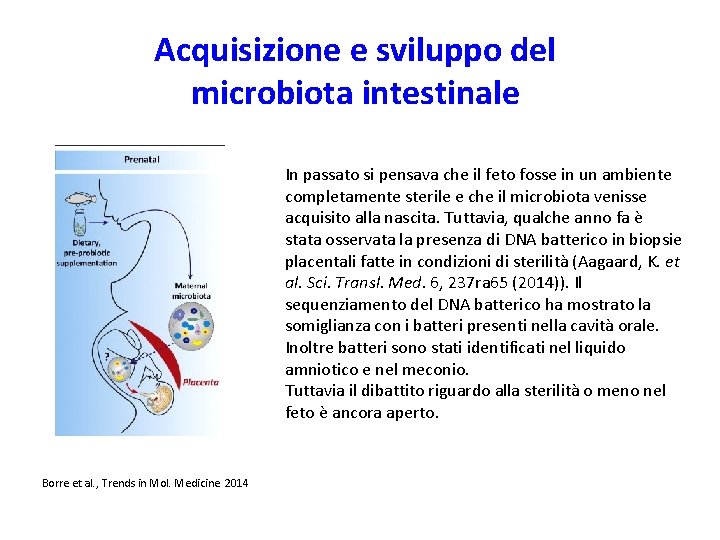
Acquisizione e sviluppo del microbiota intestinale In passato si pensava che il feto fosse in un ambiente completamente sterile e che il microbiota venisse acquisito alla nascita. Tuttavia, qualche anno fa è stata osservata la presenza di DNA batterico in biopsie placentali fatte in condizioni di sterilità (Aagaard, K. et al. Sci. Transl. Med. 6, 237 ra 65 (2014)). Il sequenziamento del DNA batterico ha mostrato la somiglianza con i batteri presenti nella cavità orale. Inoltre batteri sono stati identificati nel liquido amniotico e nel meconio. Tuttavia il dibattito riguardo alla sterilità o meno nel feto è ancora aperto. Borre et al. , Trends in Mol. Medicine 2014
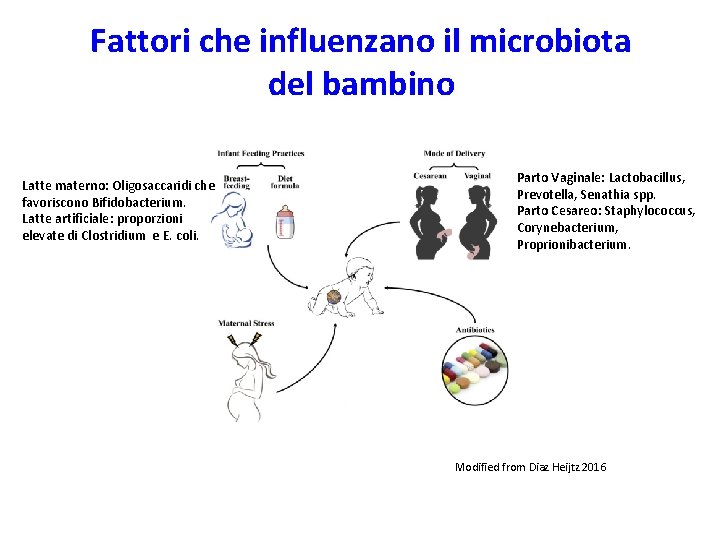
Fattori che influenzano il microbiota del bambino Latte materno: Oligosaccaridi che favoriscono Bifidobacterium. Latte artificiale: proporzioni elevate di Clostridium e E. coli. Parto Vaginale: Lactobacillus, Prevotella, Senathia spp. Parto Cesareo: Staphylococcus, Corynebacterium, Proprionibacterium. Modified from Diaz Heijtz 2016
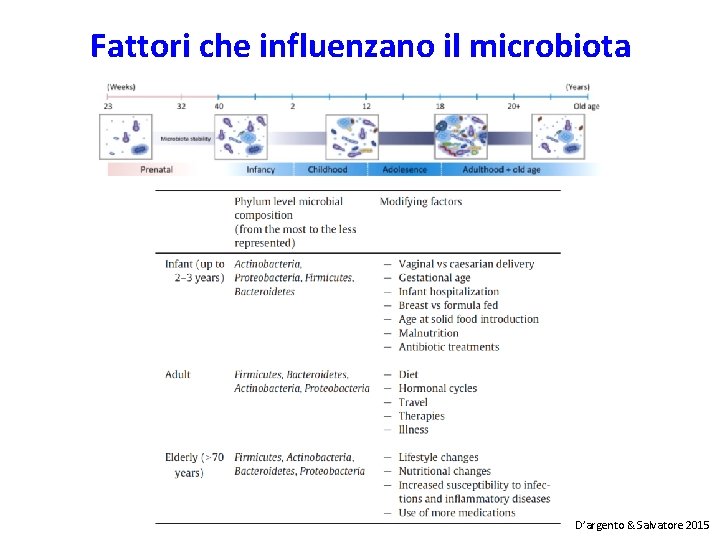
Fattori che influenzano il microbiota D’argento & Salvatore 2015

Principali funzioni del microbiota intestinale: • Interazione ospite-microbiota e sviluppo e mantenimento delle funzioni del sistema immunitario; • Mantenimento dell'integrità della barriera intestinale; • Funzioni metaboliche; • Gut-microbiota-brain axis e influenze sulla fisiologia neuronale e sul comportamento.

Principali funzioni metaboliche Prove recenti suggeriscono che il microbiota intestinale influenzi l'assorbimento dei nutrienti, l’estrazione delle componenti energetiche dai nutrienti stessi e diverse di vie metaboliche dell'ospite. Importanti funzioni metaboliche del microbioma intestinale sono: ü il catabolismo delle tossine alimentari, ü Il catabolismo delle sostanze cancerogene, ü la sintesi di micronutrienti (vitamine), ü la fermentazione di sostanze alimentari non digeribili; ü l'assistenza nell'assorbimento di elettroliti e minerali.
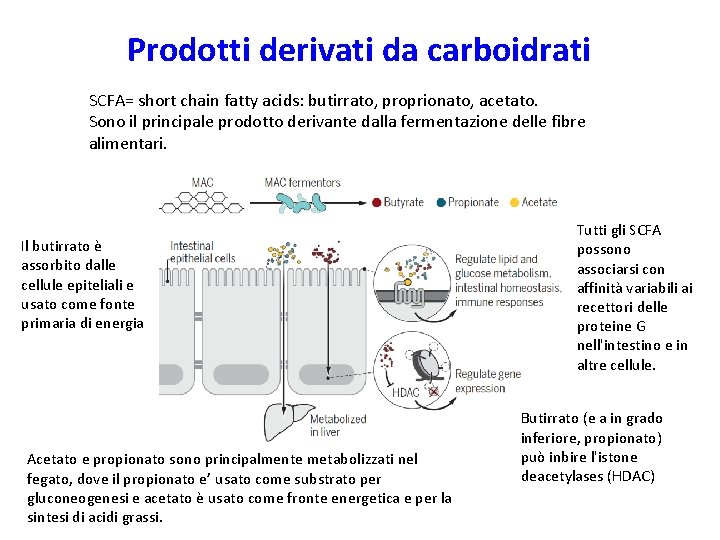
Prodotti derivati da carboidrati SCFA= short chain fatty acids: butirrato, proprionato, acetato. Sono il principale prodotto derivante dalla fermentazione delle fibre alimentari. Il butirrato è assorbito dalle cellule epiteliali e usato come fonte primaria di energia Acetato e propionato sono principalmente metabolizzati nel fegato, dove il propionato e’ usato come substrato per gluconeogenesi e acetato è usato come fronte energetica e per la sintesi di acidi grassi. Tutti gli SCFA possono associarsi con affinità variabili ai recettori delle proteine G nell'intestino e in altre cellule. Butirrato (e a in grado inferiore, propionato) può inbire l'istone deacetylases (HDAC)
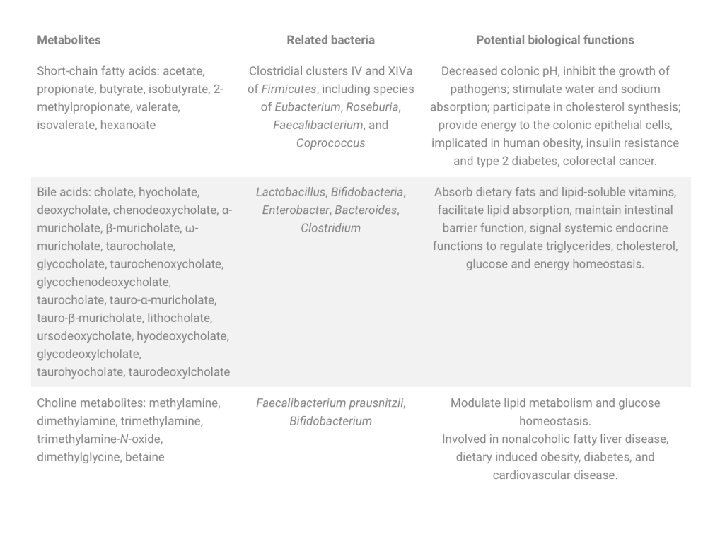
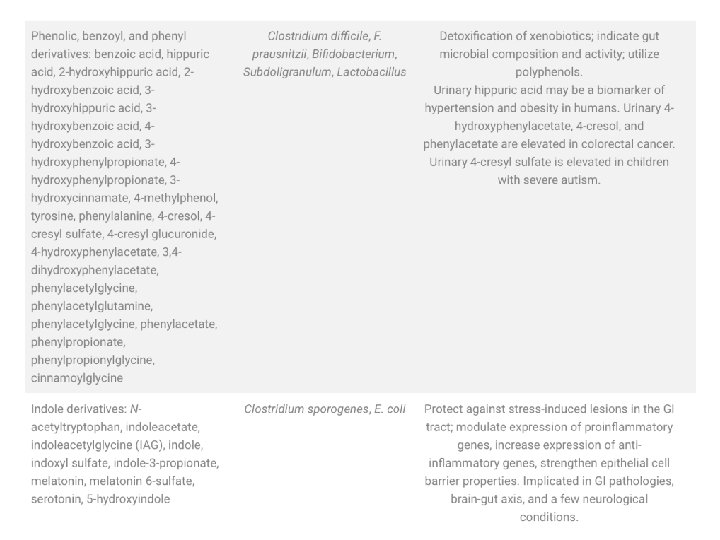
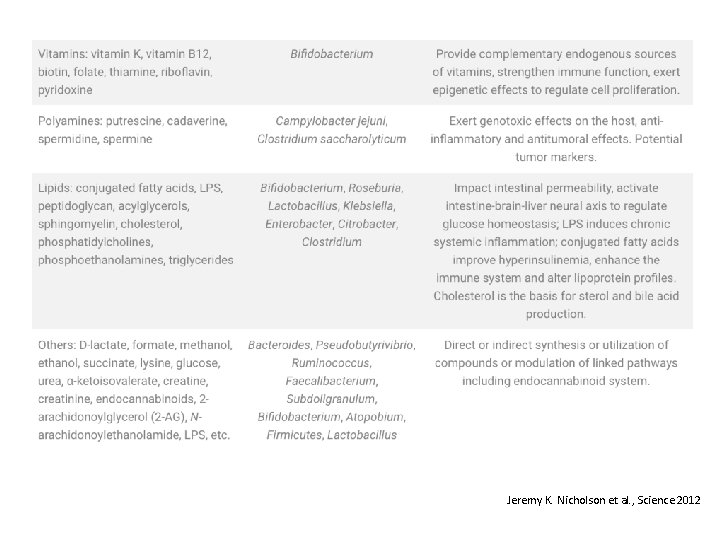
Jeremy K. Nicholson et al. , Science 2012

Regolazione dell’omeostasi metabolica Il legame tra i microbi nell'intestino umano e lo sviluppo di obesità, malattie cardiovascolari e sindrome metabolica (e. g. diabete di tipo 2), sta diventando sempre più chiaro. La composizione del microbiota intestinale è alterata nelle persone obese e può rispondere ai cambiamenti del peso corporeo. Obesità : incrementa l’abbondanza del philum Firmicutes e diminuisce quella del philum Bacteroidetes (vero per uomo e modello animale) I livelli di Bacteroidetes aumentano quando il peso viene ridotto, sia con diete povere di grassi o povere di carboidrati, suggerendo che i Bacteroidetes potrebbero essere sensibili all'apporto calorico. Un effetto simile è stato osservato anche nelle persone che hanno perso peso dopo una procedura di bypass gastrico Roux-en-Y. Tremaroli & Backhed, Nature 2012

Influenze del microbiota sul sistema nervoso centrale
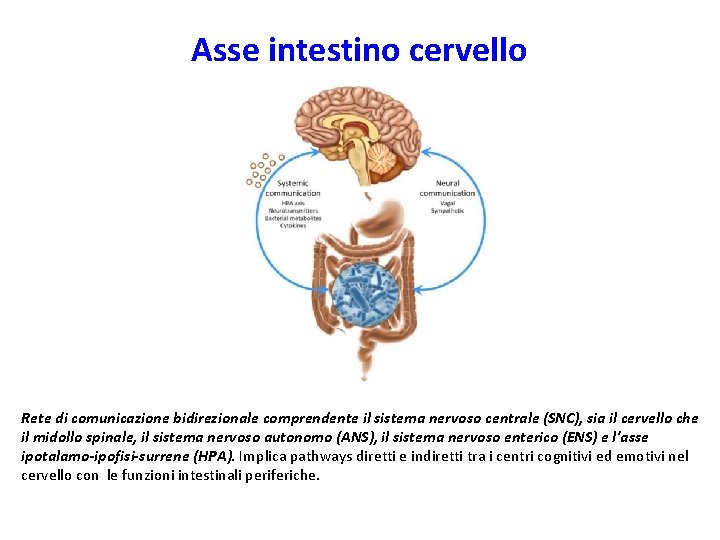
Asse intestino cervello Rete di comunicazione bidirezionale comprendente il sistema nervoso centrale (SNC), sia il cervello che il midollo spinale, il sistema nervoso autonomo (ANS), il sistema nervoso enterico (ENS) e l'asse ipotalamo-ipofisi-surrene (HPA). Implica pathways diretti e indiretti tra i centri cognitivi ed emotivi nel cervello con le funzioni intestinali periferiche.

Asse intestino-microbiota- cervello Prove cliniche e sperimentali suggeriscono che il microbiota enterico abbia un impatto importante sull’asse intestino-cervello, interagendo non solo localmente con le cellule intestinali e ENS, ma anche direttamente con il sistema nervoso centrale attraverso le vie neuroendocrine e metaboliche. Principali vie di comunicazione tra microbiota e SNC: 1) Il nervo vago- i neuroni sensoriali spinali e vagali afferenti trasmettono feedback dall'estremità intestinale al tronco encefalico che a sua volta coinvolge l'ipotalamo e il sistema limbico (responsabile della regolazione delle emozioni). Allo stesso modo, le proiezioni discendenti dal sistema limbico (attivato tramite stress) influenzano l'attività autonomica dell'intestino. 2) Il sistema immunitario - Il tessuto linfoide associato all'intestino comprende il 70% del sistema immunitario del corpo e può essere concettualizzato come il più grande organo immunitario del corpo. 3) Sistema circolatorio- Metaboliti microbici, neurotrasmettitori e altre molecole segnale sono rilasciate nella circolazione sistemica e possono raggiungere il sistema nervoso centrale. Sampson & Mazmanian 2015

Principali vie di comunicazione tra microbiota e SNC (2): 4) Interferenza con il metabolismo del triptofano - Circa il 95% della serotonina (5 -HT) è prodotta dalle cellule enterocromaffini della mucosa intestinale. A livello periferico, la 5 -HT è coinvolta nella regolazione della secrezione gastrointestinale, della motilità (contrazione muscolare regolare e rilassamento) e della percezione del dolore, mentre nel cervello la 5 -HT è implicato nella regolazione dell'umore e delle funzioni cognitive. Anche il microbiota intestinale svolge un ruolo importante nel metabolismo del triptofano, che è il precursore per la sintesi della serotonina. 5) Segnalazione neuroendocrina (ormone intestinale) - È noto che i prodotti batterici stimolano le cellule enteroendocrine (EEC) a produrre diversi neuropeptidi come il peptide YY, il neuropeptide Y (NPY), la colecistochinina, il peptide-1 e -2 del glucagone e la sostanza P. Questi neuropeptidi entrano quindi nel flusso sanguigno e / o influenzano direttamente il sistema nervoso enterico. 6) Permeabilità intestinale alterata - Lo stress cronico ha dimostrato di alterare la permeabilità intestinale (sindrome da alterata permeabilità intestinale), che è associata a un'infiammazione di basso grado che può essere funzionalmente collegata a disturbi psichiatrici come la depressione. In molti di questi casi, è la maggiore presenza di endotossine batteriche circolanti, note come lipopolisaccaridi, che sono fondamentali fattori di rischio per la malattia. In alternativa, altri studi hanno suggerito che il microbiota intestinale può produrre sostanze neuroattive che possono influenzare i sintomi fondamentali dei disturbi neuropsichiatrici. Questa ipotesi alternativa suggerisce un ruolo critico e rilevante del microbiota intestinale nella fisiopatologia di molti disturbi, tra cui schizofrenia, autismo, ansia e depressione.
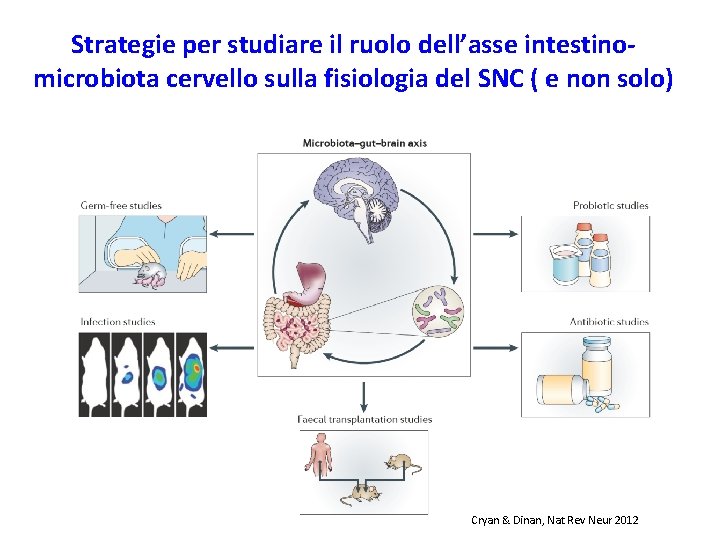
Strategie per studiare il ruolo dell’asse intestinomicrobiota cervello sulla fisiologia del SNC ( e non solo) Cryan & Dinan, Nat Rev Neur 2012
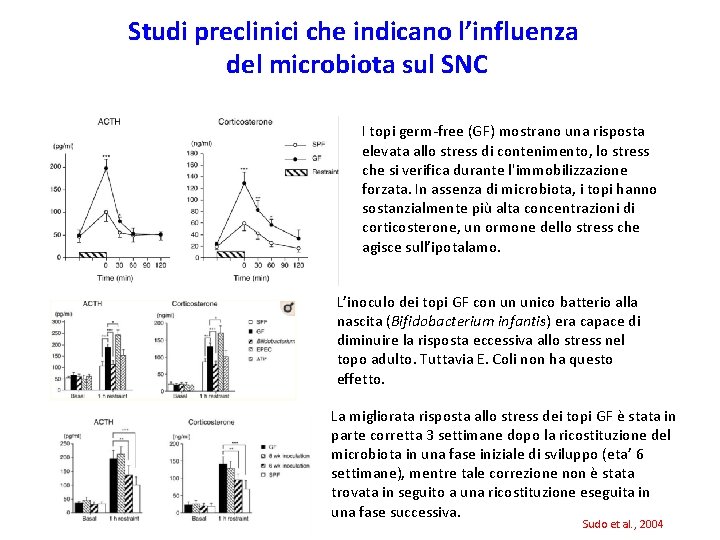
Studi preclinici che indicano l’influenza del microbiota sul SNC I topi germ-free (GF) mostrano una risposta elevata allo stress di contenimento, lo stress che si verifica durante l'immobilizzazione forzata. In assenza di microbiota, i topi hanno sostanzialmente più alta concentrazioni di corticosterone, un ormone dello stress che agisce sull’ipotalamo. L’inoculo dei topi GF con un unico batterio alla nascita (Bifidobacterium infantis) era capace di diminuire la risposta eccessiva allo stress nel topo adulto. Tuttavia E. Coli non ha questo effetto. La migliorata risposta allo stress dei topi GF è stata in parte corretta 3 settimane dopo la ricostituzione del microbiota in una fase iniziale di sviluppo (eta’ 6 settimane), mentre tale correzione non è stata trovata in seguito a una ricostituzione eseguita in una fase successiva. Sudo et al. , 2004
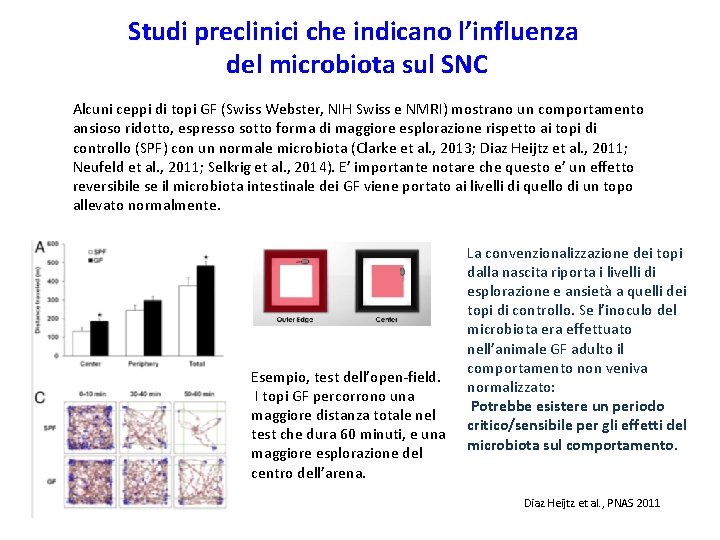
Studi preclinici che indicano l’influenza del microbiota sul SNC Alcuni ceppi di topi GF (Swiss Webster, NIH Swiss e NMRI) mostrano un comportamento ansioso ridotto, espresso sotto forma di maggiore esplorazione rispetto ai topi di controllo (SPF) con un normale microbiota (Clarke et al. , 2013; Diaz Heijtz et al. , 2011; Neufeld et al. , 2011; Selkrig et al. , 2014). E’ importante notare che questo e’ un effetto reversibile se il microbiota intestinale dei GF viene portato ai livelli di quello di un topo allevato normalmente. Esempio, test dell’open-field. I topi GF percorrono una maggiore distanza totale nel test che dura 60 minuti, e una maggiore esplorazione del centro dell’arena. La convenzionalizzazione dei topi dalla nascita riporta i livelli di esplorazione e ansietà a quelli dei topi di controllo. Se l’inoculo del microbiota era effettuato nell’animale GF adulto il comportamento non veniva normalizzato: Potrebbe esistere un periodo critico/sensibile per gli effetti del microbiota sul comportamento. Diaz Heijtz et al. , PNAS 2011

Un’ulteriore prova dell’esistenza dell’asse intestino microbiota cervello: i probiotici I probiotici sono organismi vivi (e. g. batteri, lieviti) che, quando ingeriti in quantità adeguate, esercitano un beneficio sula salute dell’organismo ricevente. Hanno dimostrato avere un’ ampia gamma di effetti negli studi sull'uomo e sugli animali. Esempio: nel trattamento dei disturbi del tratto gastrointestinale nell’uomo. Prove cliniche a supporto dei probiotici nel ridurre l'ansia, ridurre le risposte allo stress e nel miglioramento dell'umore nelle persone con malattia infiammatoria intestinale e con affaticamento cronico. L’associazione di Lactobacillus helveticus e B. longum in un cocktail probiotico ha ridotto il comportamento ansioso negli animali e, soprattutto volontari sani ne hanno tratto beneficio grazie a un miglioramento in certi effetti psicologici (ridotta risposta allo stress) e riduzione del cortisolo sierico (Messaoudi et al. , 2011).
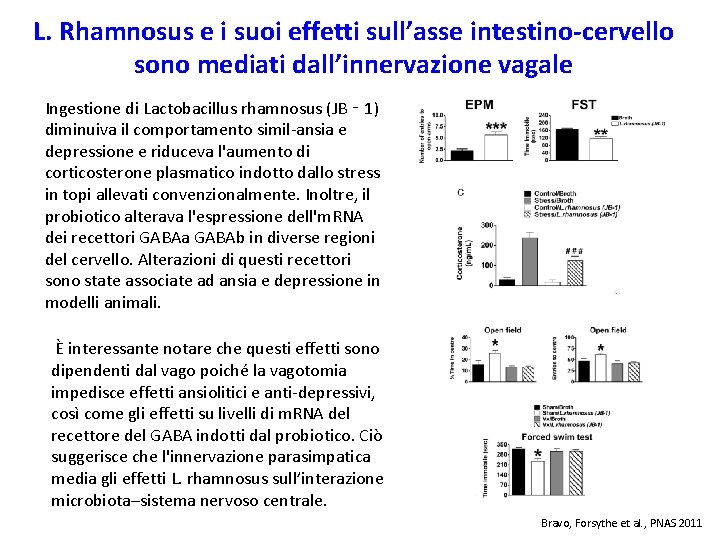
L. Rhamnosus e i suoi effetti sull’asse intestino-cervello sono mediati dall’innervazione vagale Ingestione di Lactobacillus rhamnosus (JB ‑ 1) diminuiva il comportamento simil-ansia e depressione e riduceva l'aumento di corticosterone plasmatico indotto dallo stress in topi allevati convenzionalmente. Inoltre, il probiotico alterava l'espressione dell'm. RNA dei recettori GABAa GABAb in diverse regioni del cervello. Alterazioni di questi recettori sono state associate ad ansia e depressione in modelli animali. È interessante notare che questi effetti sono dipendenti dal vago poiché la vagotomia impedisce effetti ansiolitici e anti-depressivi, così come gli effetti su livelli di m. RNA del recettore del GABA indotti dal probiotico. Ciò suggerisce che l'innervazione parasimpatica media gli effetti L. rhamnosus sull’interazione microbiota–sistema nervoso centrale. Bravo, Forsythe et al. , PNAS 2011
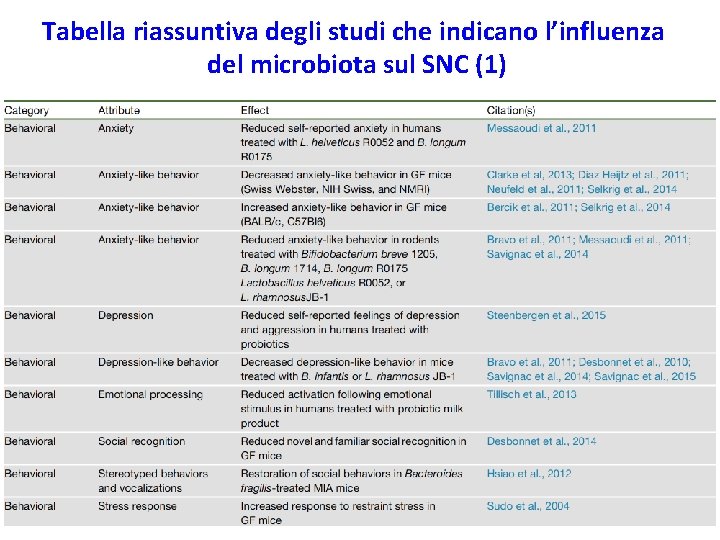
Tabella riassuntiva degli studi che indicano l’influenza del microbiota sul SNC (1)

Tabella riassuntiva degli studi che indicano l’influenza del microbiota sul SNC (2)
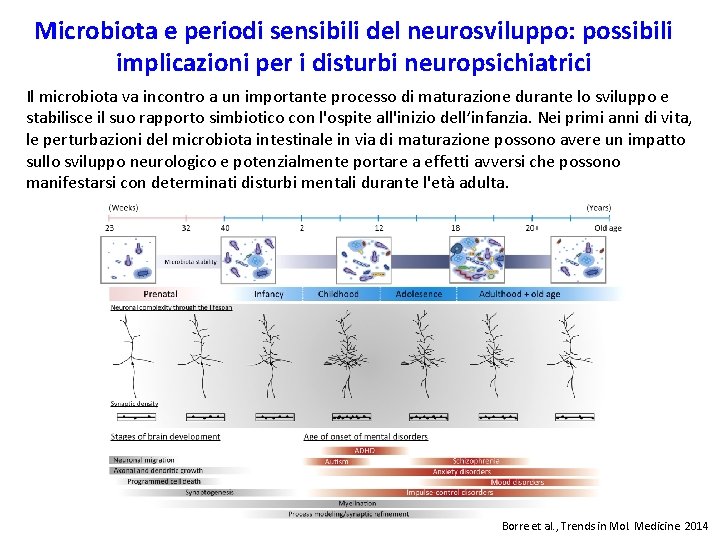
Microbiota e periodi sensibili del neurosviluppo: possibili implicazioni per i disturbi neuropsichiatrici Il microbiota va incontro a un importante processo di maturazione durante lo sviluppo e stabilisce il suo rapporto simbiotico con l'ospite all'inizio dell’infanzia. Nei primi anni di vita, le perturbazioni del microbiota intestinale in via di maturazione possono avere un impatto sullo sviluppo neurologico e potenzialmente portare a effetti avversi che possono manifestarsi con determinati disturbi mentali durante l'età adulta. Borre et al. , Trends in Mol. Medicine 2014
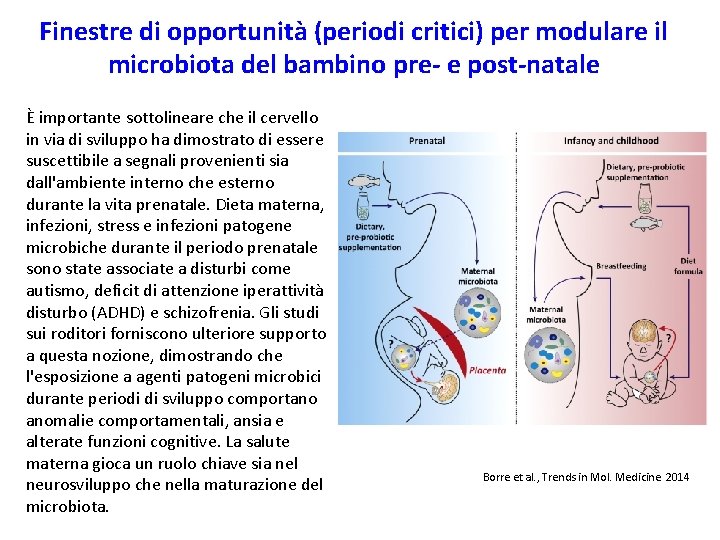
Finestre di opportunità (periodi critici) per modulare il microbiota del bambino pre- e post-natale È importante sottolineare che il cervello in via di sviluppo ha dimostrato di essere suscettibile a segnali provenienti sia dall'ambiente interno che esterno durante la vita prenatale. Dieta materna, infezioni, stress e infezioni patogene microbiche durante il periodo prenatale sono state associate a disturbi come autismo, deficit di attenzione iperattività disturbo (ADHD) e schizofrenia. Gli studi sui roditori forniscono ulteriore supporto a questa nozione, dimostrando che l'esposizione a agenti patogeni microbici durante periodi di sviluppo comportano anomalie comportamentali, ansia e alterate funzioni cognitive. La salute materna gioca un ruolo chiave sia nel neurosviluppo che nella maturazione del microbiota. Borre et al. , Trends in Mol. Medicine 2014

Gut-microbiota-brain axis: disordini del neurosviluppo e autismo I disturbi dello spettro autistico (ASD) sono disturbi dello sviluppo neurologico caratterizzati dalla presenza di comportamenti stereotipati, deficit nella comunicazione e di interazione sociale. Sebbene l'eziologia dell’ASD rimanga sconosciuta, si pensa che sia fattori genetici che ambientali abbiano un ruolo nella sua eziopatogenesi. Disturbi del tratto gastrointestinale associati ad ASD sono stati collegati a possibili alterazioni nella composizione e nella funzione del microbiota. Nonostante questi studi correlazionali, l'interpretazione dei dati clinici è compromessa da alti tassi di uso di antibiotici e marcate variazioni dietetiche nei pazienti con ASD. Questo rende molto difficile trarre delle conclusioni sugli effetti del microbiota sull’ASD.
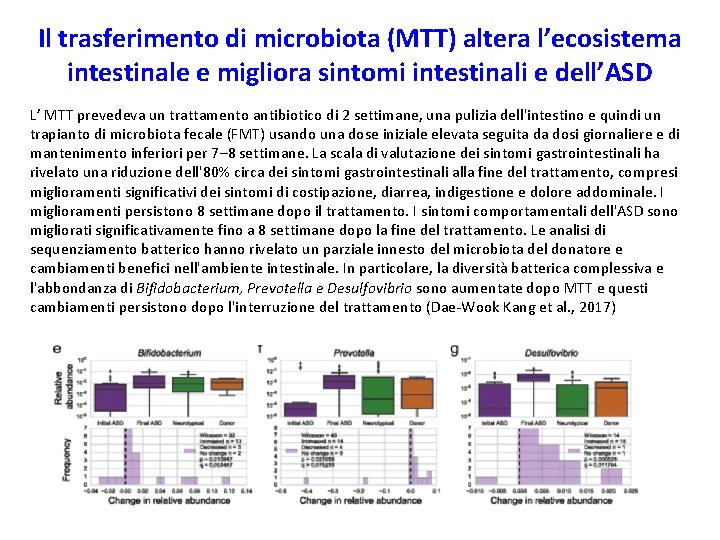
Il trasferimento di microbiota (MTT) altera l’ecosistema intestinale e migliora sintomi intestinali e dell’ASD L’ MTT prevedeva un trattamento antibiotico di 2 settimane, una pulizia dell'intestino e quindi un trapianto di microbiota fecale (FMT) usando una dose iniziale elevata seguita da dosi giornaliere e di mantenimento inferiori per 7– 8 settimane. La scala di valutazione dei sintomi gastrointestinali ha rivelato una riduzione dell'80% circa dei sintomi gastrointestinali alla fine del trattamento, compresi miglioramenti significativi dei sintomi di costipazione, diarrea, indigestione e dolore addominale. I miglioramenti persistono 8 settimane dopo il trattamento. I sintomi comportamentali dell'ASD sono migliorati significativamente fino a 8 settimane dopo la fine del trattamento. Le analisi di sequenziamento batterico hanno rivelato un parziale innesto del microbiota del donatore e cambiamenti benefici nell'ambiente intestinale. In particolare, la diversità batterica complessiva e l'abbondanza di Bifidobacterium, Prevotella e Desulfovibrio sono aumentate dopo MTT e questi cambiamenti persistono dopo l'interruzione del trattamento (Dae-Wook Kang et al. , 2017)
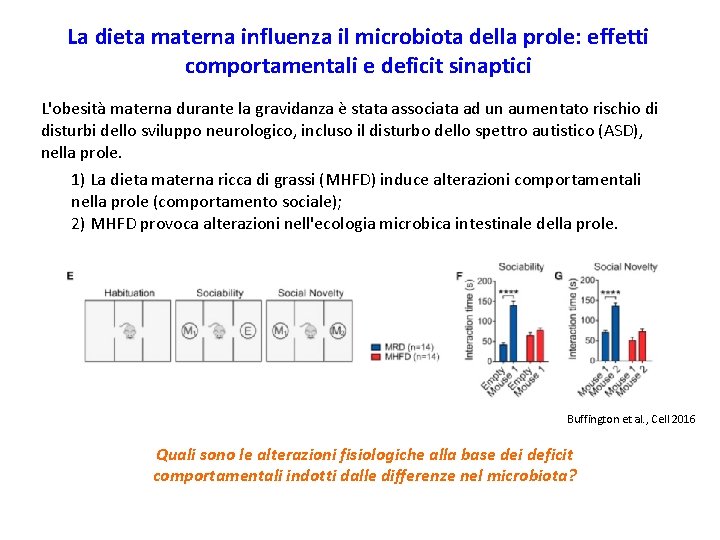
La dieta materna influenza il microbiota della prole: effetti comportamentali e deficit sinaptici L'obesità materna durante la gravidanza è stata associata ad un aumentato rischio di disturbi dello sviluppo neurologico, incluso il disturbo dello spettro autistico (ASD), nella prole. 1) La dieta materna ricca di grassi (MHFD) induce alterazioni comportamentali nella prole (comportamento sociale); 2) MHFD provoca alterazioni nell'ecologia microbica intestinale della prole. Buffington et al. , Cell 2016 Quali sono le alterazioni fisiologiche alla base dei deficit comportamentali indotti dalle differenze nel microbiota?
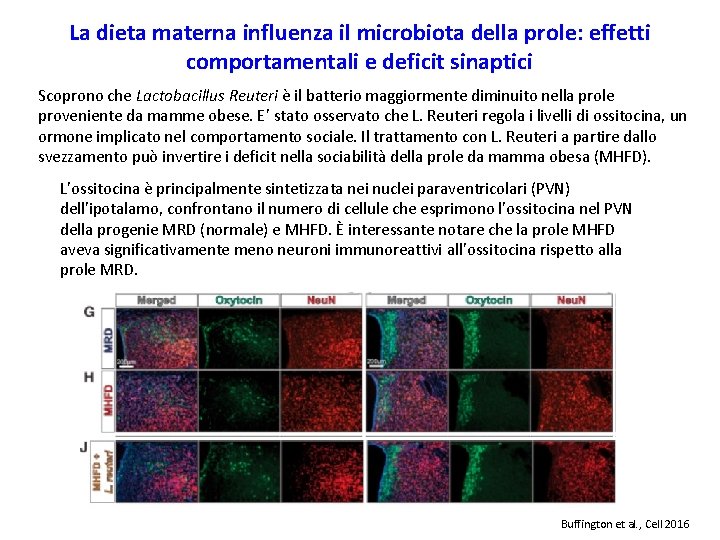
La dieta materna influenza il microbiota della prole: effetti comportamentali e deficit sinaptici Scoprono che Lactobacillus Reuteri è il batterio maggiormente diminuito nella prole proveniente da mamme obese. E’ stato osservato che L. Reuteri regola i livelli di ossitocina, un ormone implicato nel comportamento sociale. Il trattamento con L. Reuteri a partire dallo svezzamento può invertire i deficit nella sociabilità della prole da mamma obesa (MHFD). L’ossitocina è principalmente sintetizzata nei nuclei paraventricolari (PVN) dell'ipotalamo, confrontano il numero di cellule che esprimono l'ossitocina nel PVN della progenie MRD (normale) e MHFD. È interessante notare che la prole MHFD aveva significativamente meno neuroni immunoreattivi all’ossitocina rispetto alla prole MRD. Buffington et al. , Cell 2016
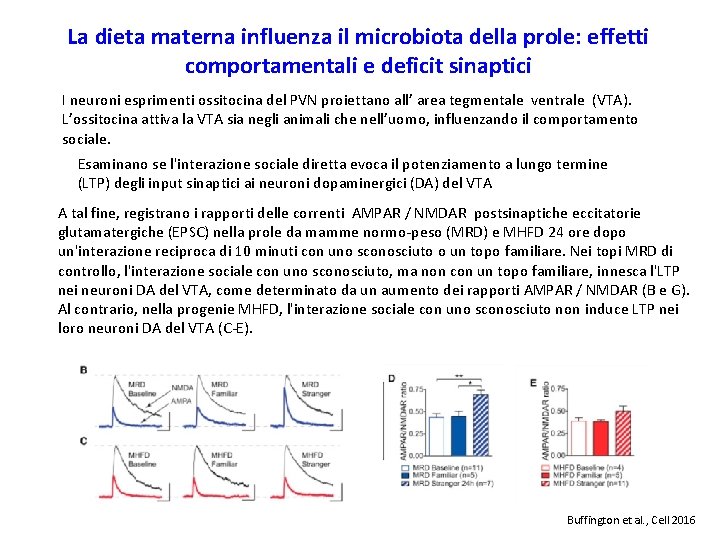
La dieta materna influenza il microbiota della prole: effetti comportamentali e deficit sinaptici I neuroni esprimenti ossitocina del PVN proiettano all’ area tegmentale ventrale (VTA). L’ossitocina attiva la VTA sia negli animali che nell’uomo, influenzando il comportamento sociale. Esaminano se l'interazione sociale diretta evoca il potenziamento a lungo termine (LTP) degli input sinaptici ai neuroni dopaminergici (DA) del VTA A tal fine, registrano i rapporti delle correnti AMPAR / NMDAR postsinaptiche eccitatorie glutamatergiche (EPSC) nella prole da mamme normo-peso (MRD) e MHFD 24 ore dopo un'interazione reciproca di 10 minuti con uno sconosciuto o un topo familiare. Nei topi MRD di controllo, l'interazione sociale con uno sconosciuto, ma non con un topo familiare, innesca l'LTP nei neuroni DA del VTA, come determinato da un aumento dei rapporti AMPAR / NMDAR (B e G). Al contrario, nella progenie MHFD, l'interazione sociale con uno sconosciuto non induce LTP nei loro neuroni DA del VTA (C-E). Buffington et al. , Cell 2016
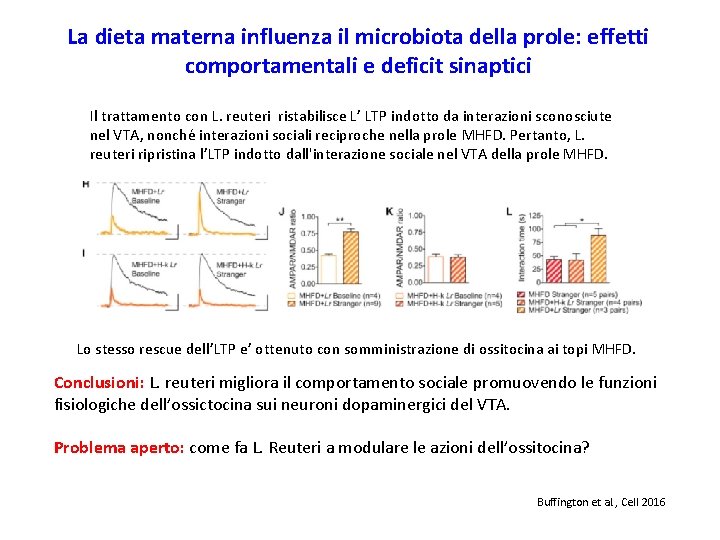
La dieta materna influenza il microbiota della prole: effetti comportamentali e deficit sinaptici Il trattamento con L. reuteri ristabilisce L’ LTP indotto da interazioni sconosciute nel VTA, nonché interazioni sociali reciproche nella prole MHFD. Pertanto, L. reuteri ripristina l’LTP indotto dall'interazione sociale nel VTA della prole MHFD. Lo stesso rescue dell’LTP e’ ottenuto con somministrazione di ossitocina ai topi MHFD. Conclusioni: L. reuteri migliora il comportamento sociale promuovendo le funzioni fisiologiche dell’ossictocina sui neuroni dopaminergici del VTA. Problema aperto: come fa L. Reuteri a modulare le azioni dell’ossitocina? Buffington et al. , Cell 2016

Meccanismo fisiologico responsabile del miglioramento di sintomi caratteristici dell’autismo tramite trattamento con probiotico Il trattamento selettivo con L. reuteri ripristina i deficit sociali in modelli preclinici genetici, ambientali, e idiopatici di autismo (ASD). È interessante notare che gli effetti di L. reuteri sul comportamento sociale non sono mediati dal ripristino del microbioma intestinale dell'ospite, che è completamente alterato in questi modelli ASD. Invece, L. reuteri ha un’azione dipendente dal nervo vago, tramite cui riesce a recuperare plasticità sinaptica indotta da interazioni sociali nell’area tegmentale ventrale dei topi ASD, ma non in topi con deficit del recettore dell'ossitocina. Sgritta et al. , Neuron 2019
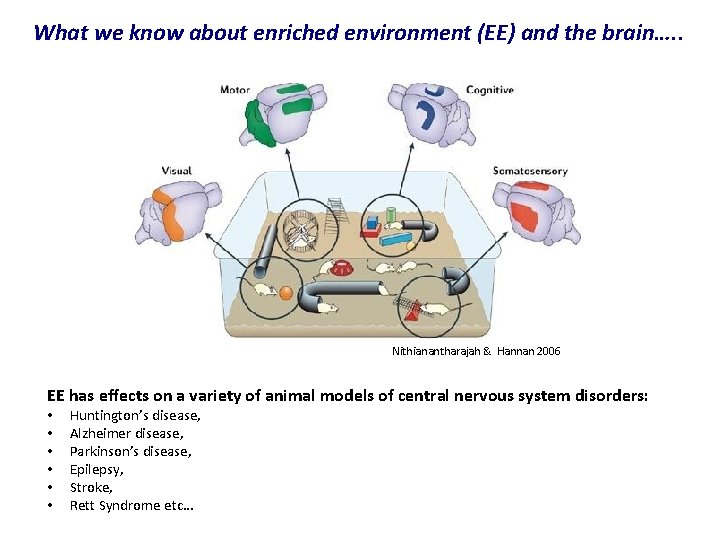
What we know about enriched environment (EE) and the brain…. . Nithianantharajah & Hannan 2006 EE has effects on a variety of animal models of central nervous system disorders: • • • Huntington’s disease, Alzheimer disease, Parkinson’s disease, Epilepsy, Stroke, Rett Syndrome etc…
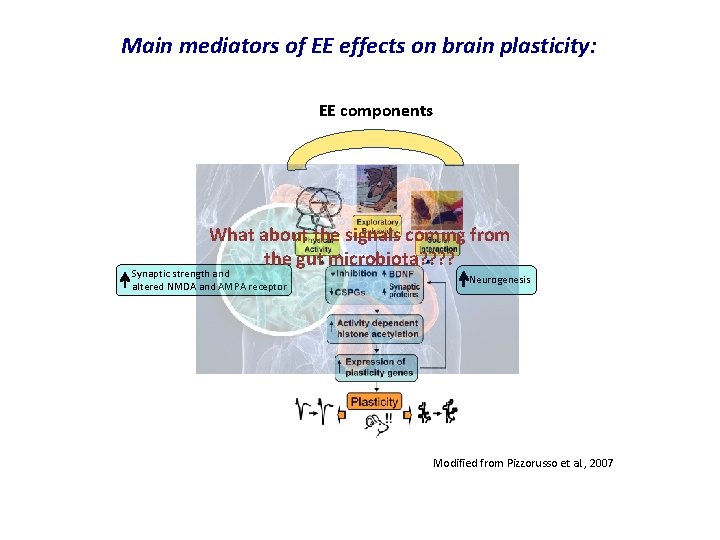
Main mediators of EE effects on brain plasticity: EE components What about the signals coming from the gut microbiota? ? Synaptic strength and altered NMDA and AMPA receptor Neurogenesis Modified from Pizzorusso et al. , 2007

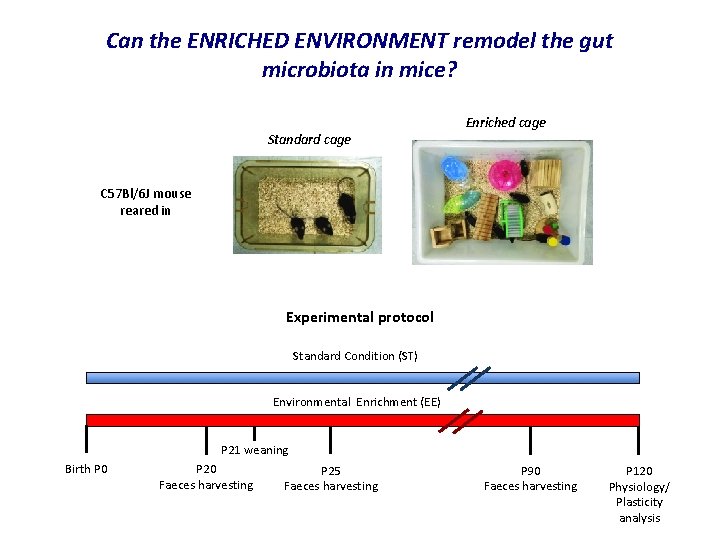
Can the ENRICHED ENVIRONMENT remodel the gut microbiota in mice? Standard cage Enriched cage C 57 Bl/6 J mouse reared in Experimental protocol Standard Condition (ST) Environmental Enrichment (EE) P 21 weaning Birth P 0 P 20 Faeces harvesting P 25 Faeces harvesting P 90 Faeces harvesting P 120 Physiology/ Plasticity analysis
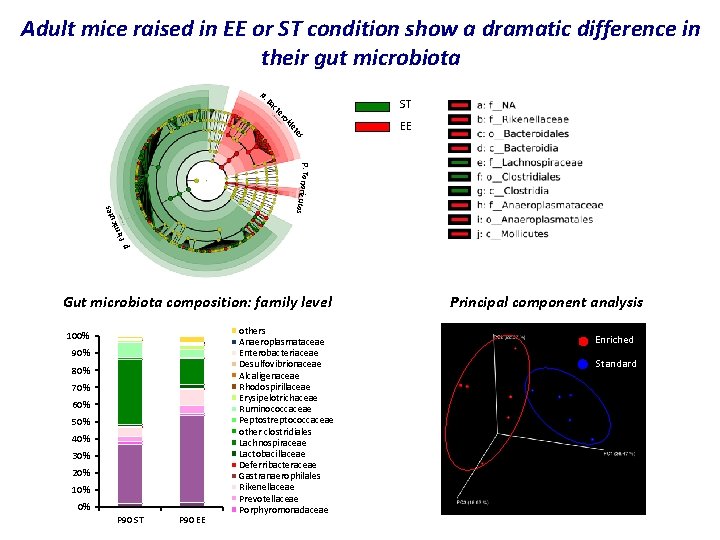
Adult mice raised in EE or ST condition show a dramatic difference in their gut microbiota p. EE s te de oi er ct Ba ST irm p. F icut es cutes p. Teneri Gut microbiota composition: family level 100% 90% 80% 70% 60% 50% 40% 30% 20% 10% 0% P 90 ST P 90 EE others Anaeroplasmataceae Enterobacteriaceae Desulfovibrionaceae Alcaligenaceae Rhodospirillaceae Erysipelotrichaceae Ruminococcaceae Peptostreptococcaceae other clostridiales Lachnospiraceae Lactobacillaceae Deferribacteraceae Gastranaerophilales Rikenellaceae Prevotellaceae Porphyromonadaceae Principal component analysis Enriched Standard
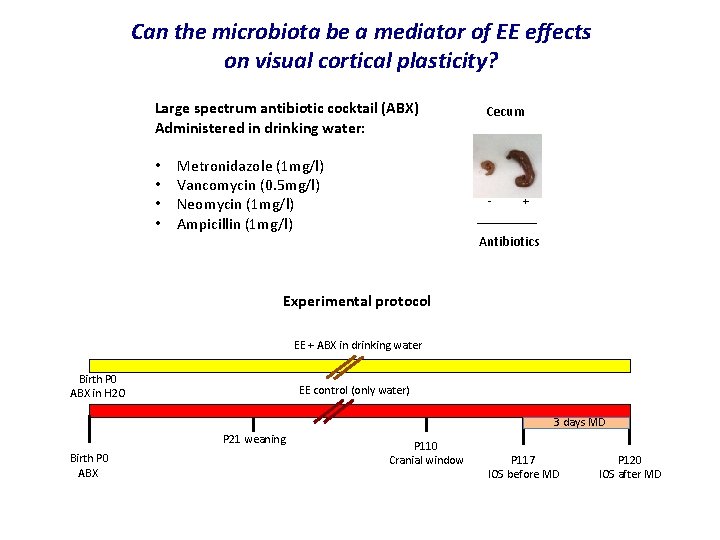
Can the microbiota be a mediator of EE effects on visual cortical plasticity? Large spectrum antibiotic cocktail (ABX) Administered in drinking water: • • Metronidazole (1 mg/l) Vancomycin (0. 5 mg/l) Neomycin (1 mg/l) Ampicillin (1 mg/l) Cecum - + Antibiotics Experimental protocol EE + ABX in drinking water Birth P 0 ABX in H 2 O EE control (only water) 3 days MD P 21 weaning Birth P 0 ABX P 110 Cranial window P 117 IOS before MD P 120 IOS after MD
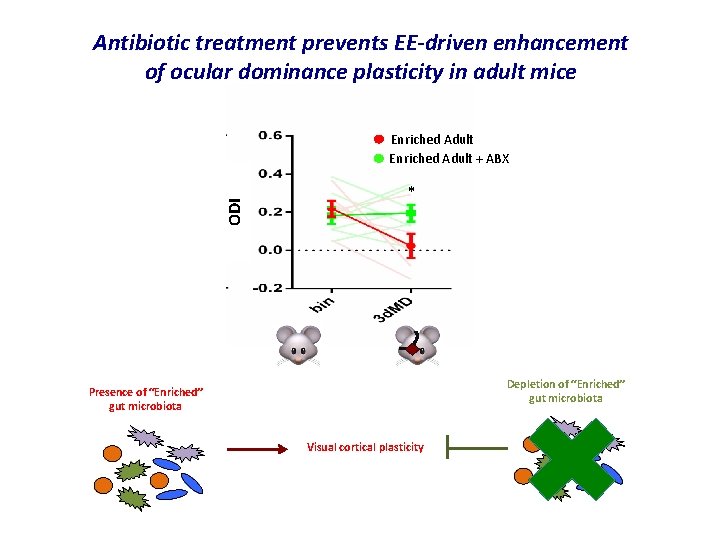
Antibiotic treatment prevents EE-driven enhancement of ocular dominance plasticity in adult mice ODI Enriched Adult + ABX * Depletion of “Enriched” gut microbiota Presence of “Enriched” gut microbiota Visual cortical plasticity
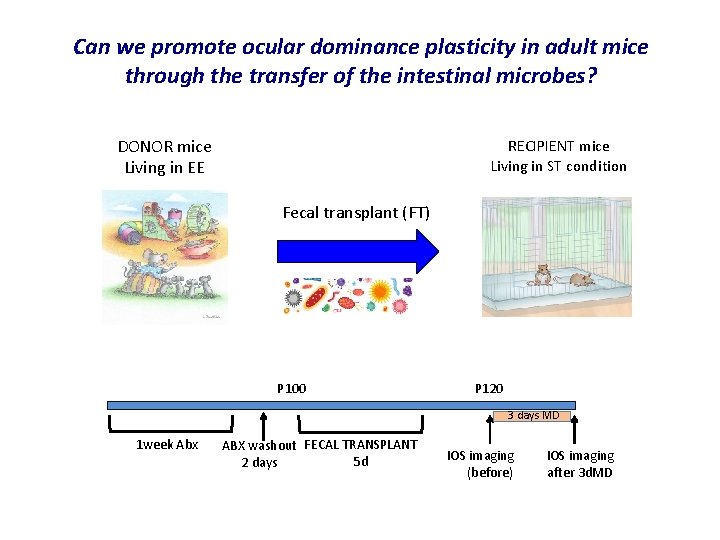
Can we promote ocular dominance plasticity in adult mice through the transfer of the intestinal microbes? DONOR mice Living in EE RECIPIENT mice Living in ST condition Fecal transplant (FT) P 100 P 120 3 days MD 1 week Abx ABX washout FECAL TRANSPLANT 5 d 2 days IOS imaging (before) IOS imaging after 3 d. MD
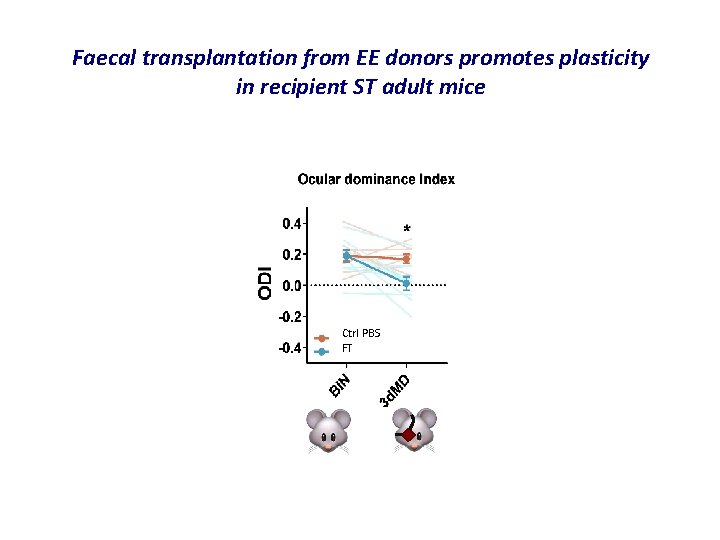
Faecal transplantation from EE donors promotes plasticity in recipient ST adult mice Ctrl PBS FT
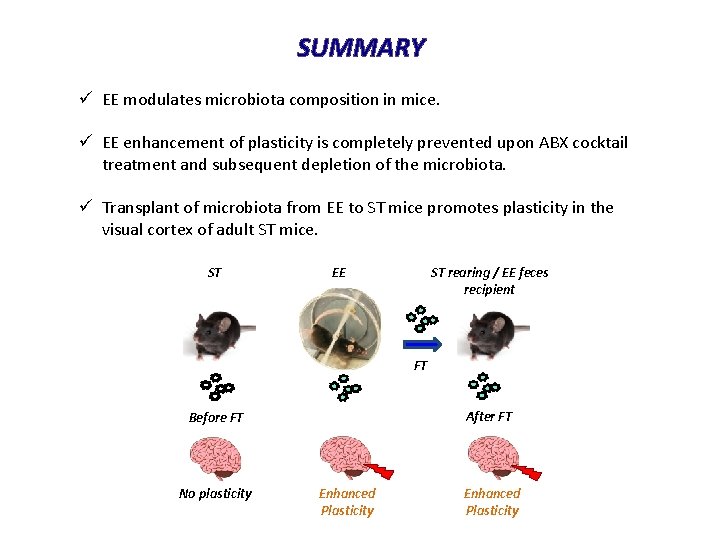
SUMMARY ü EE modulates microbiota composition in mice. ü EE enhancement of plasticity is completely prevented upon ABX cocktail treatment and subsequent depletion of the microbiota. ü Transplant of microbiota from EE to ST mice promotes plasticity in the visual cortex of adult ST mice. ST EE ST rearing / EE feces recipient FT After FT Before FT No plasticity Enhanced Plasticity

Sommario della lezione 1) Il microbiota ha una relazione simbiotica mutualistica con il suo ospite. Per esempio: l'ospite usa il microbiota intestinale per ottenere l'energia dal cibo e i nutrienti necessari per la sopravvivenza, mentre il microbiota intestinale guadagna habitat e nutrizione. 2) Il microbiota si sviluppa principalmente alla nascita e diversi fattori influenzano la sua maturazione e la composizione finale nell’adulto. 3) Il microbiota intestinale influisce sulla fisiologia dell’ospite influenzando diversi processi biologici, tra cui il metabolismo. 4) Il microbiota intestinale gioca un ruolo importante sull’asse intestino-cervello. In conseguenza di ciò la funzione neuronale e il comportamento sono influenzati dal microbiota intestinale.

Nel caso aveste bisogno paola. tognini@sns. it paola. tognini@unipi. it
- Slides: 48