Il laboratorio nella valutazione della funzionalit epatica e

Il laboratorio nella valutazione della funzionalità epatica e renale

The multiple functions of the liver are exceeded only by the biochemical methods designed to test them. . . Dame Sheila Sherlock Diseases of the Liver and Biliary System

Perchè vengono richiesti i test di funzionalità epatica? - 1 • Diagnosi – Questo paziente ha una malattia epatica? • Prognosi – Stima probabile della sopravvivenza nelle malattie croniche ed acute del fegato • Screening – Gruppi selezionati – Individuale • Progressione della malattia • Risposta alla terapia • Guarigione dopo chirurgia o altri interventi

Perchè vengono richiesti i test di funzionalità epatica? - 2 • Differenziazione del tipo di epatopatia – Ittero da colestasi, ostruttivo – Epatite - infettiva, autoimmune, alcolica • Guida per ulteriori indagini – Sierologia virale – Autoanticorpi – Imaging (radiologia, TAC, Ecografia) – ERCP (“Endoscopic retrograde colangiopancreatoscopy”)

Test di primo livello attualmente più utilizzati (Liver Function Tests - LFTs) • Transaminasi o Aminotransferasi, AST, ALT – danno parenchimale • Bilirubina – colestasi • Fosfatasi alcalina, -glutamiltranspeptidasi (GGT) – danno epitelio biliare ed ostruzione biliare (alcol) • Albumina – sintesi epatica • Tempo di protrombina (INR) – coagulazione (indicatore dinamico)

Aminotransferasi (transaminasi) • Aspartato aminotransferasi (AST) presente in: – Fegato, muscolo cardiaco e scheletrico, rene, cervello, pancreas, polmone, WBC e RBC – Isoforme mitocondriale e citoplasmatica (immunosottrazione) – m. AST (mitocondriale) proposta come marcatore per differenziare epatite alcolica vs non-alcolica • Alanina transaminasi (ALT) presente in: – Come AST ma in misura minore nei tessuti non-epatici – Enzima citoplasmatico

Cause di aumento AST/ALT • ? Origine epatica o non epatica – dosaggio CK (muscolo scheletrico), c. Tn. I (cuore), amilasi (pancreas), etc. • Se di origine epatica, un'aumento della AST indica un danno degli epatociti: – epatite : virale, autoimmune, alcolica, da farmaci • Se non di origine epatica, possibile danno muscolare: – Miosite, ipotiroidismo, droghe, IM (infarto miocardico)

Cause di un aumento di AST / ALT >10 x ULN (“upper limit of normality”) Epatite acuta, ipossiemia tessutale (shock) 5 -10 x ULN infarto miocardico, Trauma, malattie del muscolo scheletrico, Colestasi, Epatiti croniche, epatite autoimmune < 5 x ULN Condizioni fisiologiche (neonati), altre malattie epatiche (Wilson, emocromatosi, deficit di alfa 1 -antitripsina), pancreatite, emolisi in vivo e in vitro, abuso alcolico.

Aumento di AST/ALT di origine epatica • Associato a lieve incremento di altri test indica un'epatite: – Infettiva – A/B/C, CMV, EBV ed altri • ALT meglio di AST per il monitoraggio dell'epatite cronica B/C – Autoimmune – autoanticorpi – Tossine • Epatite alcolica non comune (bevitori occasionali) • Farmaci – paracetamolo ed altri (spesso idiosincrasia) • Metalli – rame (malattia di Wilson), ferro (emocromatosi) • Veleni – funghi etc. • Rigetto post-trapianto

Bilirubina • Vero ‘liver function’ test • Viene coniugata a livello epatico ed escreta nella bile • Differenziazione tra bilirubina coniugata e non coniugata: – Malattia epatica ostruttiva, iperbilirubinemia coniugata – Insufficienza epatica, quadro misto (pochi epatociti e alterata escrezione) – Iperbilirubinemia non coniugata nel neonato (immaturità degli epatociti)

Cause non-epatiche di aumento della bilirubina • Bilirubina viene prodotta dalla distruzione dei globuli rossi (emolisi eccessiva o distruzione cellulare – di solito non coniugata) – Emoglobinopatie – sickle cell disease, sferocitosi, etc – Emolisi intravascolare da altre cause • Tossine – rame (Wilson) può causare distruzione RBC (anemia normocitica) • Infezioni – malaria • Altro – CBP (cirrosi biliare primitiva), epatite autoimmune e alcolica

Sindrome di Gilbert • Coniugazione della bilirubina è mediata da UDPglucoronosil transferasi 1 A • Condizione benigna autosomica dominante con lieve iperbilirubinemia non coniugata • Inserzione TA nel TATA repeat box del gene promoter. L'omozigosi riduce la capacità di espressione genica – In condizioni normali non vi sono conseguenze ma in situazioni di aumentata richiesta (malattie, infezioni, digiuno) si può verificare un marcato aumento della bilirubina

Alkaline phosphatase (ALP) • Gruppo di enzimi che idrolizzano esteri di fosfato in soluzioni alcaline • Geni differenti codificano per isoenzimi non-tessuto specifici e isoenzimi tessuto-specifici (placenta, intestino, cellule germinali) • Modificazioni post-traslazionali (glicosilazione) producono diverse isoforme (epatica, renale, ossea) • La differenziazione delle isoforme può assumere importanza e può essere ottenuta mediante elettroforesi con PAGE o mediante dosaggi immunometrici specifici (per esempio, BAP bone alkaline phosphatase)

Aumento della ALP sierica • Di origine epatica per ostruzione delle vie biliari intraepatiche: – Meccanica – calcoli, neoplasie (pancreatiche/biliari) – Restringimenti – cirrosi biliare primitiva (PBC), colangite sclerosante (PSC), cirrosi criptogenetica – Ipertensione portale • Di origine non-epatica: – Isoforma ossea (osteoblasti) – Fisiologico – gravidanza – Iperfosfatasemia transitoria

Iperfosfatasemia transitoria • Originariamente descritta nei bambini, si può verificare anche negli adulti ed in gravidanza • Incremento marcato della ALP fino a parecchie migliaia di IU/L • Transitoria con ritorno alla normalità in 4 -6 settimane • Associata con infezioni, soprattutto del tratto gastroenterico • Si pensa sia dovuta a modificazione delle catene laterali glicidiche provocherebbero una ridotta eliminazione con aumento dell'emivita

Cause di aumento della fosfatasi alcalina Fisiologiche Gravidanza (terzo trimestre), infanzia Patologiche > 5 x ULN Morbo di Paget (osteoblasti), Osteomalacia, Colestasi, Cirrosi < 5 x ULN Tumori ossei, iperparatiroidismo primario, fratture ossee, tumori epatici, epatiti, malattia infiammatoria intestinale

Gamma-glutamil transpeptidasi o gammaglutamil transferasi (GGT) • Prodotta negli epatociti e nelle cellule dell'epitelio biliare • Enzima microsomiale (induzione da parte di farmaci che agiscono sul citocromo P 450) responsabile del trasferimento di gruppi glutamici tra peptidi • Presente anche in altri organi: – Cuore, reni, polmoni, pancreas, vescicole seminali – Nel plasma la forma predominante è l'isoenzima epatico

Aumento di GGT - 1 • Farmaci – Induzione - alcol, anti-epilettici etc. – Meccanismi diversi • • • antibiotici statine FANS Erbe e altri prodotti omeopatici Methotrexate

Aumento di GGT - 2 • Steatosi (accumulo di grasso) – Correlata all'alcol, obesità, diabete mellito, NASH (nonalcoholic steatohepatitis) • Fibrosi/cirrosi (accumulo di matrice extracellulare e collagene) – Cirrosi alcolica, PBC, PSC, emocromatosi, deficit di alfa-1 antitripsina, malattia di Wilson (accumulo di rame) etc. • Lesioni occupanti spazio – Tumori (carcinoma epatocellulare o metastasi) – Malattie granulomatose (sarcoidosi, tubercolosi)

Cause di aumento di GGT >10 x ULN Colestasi, malattia epatica alcolica 5 -10 x ULN Epatiti, Cirrosi, pancreatiti <5 x ULN alcol, farmaci induttori

Proteine plasmatiche • La maggior parte delle proteine (eccetto le immunoglobuline) sono prodotte dal fegato • La più significativa è rappresentata dalla ALBUMINA che contribuisce alla regolazione dell'osmolarità plasmatica • Le proteine di fase acuta sono prodotte a livello epatico • Proteine di trasporto di metalli e vitamine (transferrina, ceruloplasmina, Vitamin D binding protein) sono sintetizzate e immagazzinate nel fegato

Albumina • Per mantenere concentrazioni ottimali di albumina è sufficiente che vi siano solo il 10% degli epatociti funzionanti • Una bassa concentrazione plasmatica di albumina deve far pensare ad una malattia epatica dopo aver escluso una ridotta ingestione e/o una aumentata perdita renale o gastrointestinale

INR • “International normalised ratio” • E' un reale ‘liver function’ test dinamico • INR aumentato indica deficit di fatori II, VII, IX o di Vitamina K • Un INR > 3. 0 costituisce una controindicazione per la biopsia epatica ed altre manovre invasive (rischio di sanguinamento)

Altri test biochimici • AFP (alfa-fetoproteina) per tumori primitivi del fegato – Aumenta anche nel fegato in rigenerazione come nella cirrosi • CA 19 -9 per tumori delle vie biliari – Aumenta anche in tumori del colon-retto e del pancreas • Ferritina per l'emocromatosi (accumulo di ferro) • Urea e colesterolo – La produzione risulta molto ridotta nell'insufficienza epatica

LFTs: i pro e i contro • VANTAGGI – Poco costosi, ampiamente disponibili e conosciuti da tutti – Possono guidare indagini successive • SVANTAGGI – Vecchi marcatori (vi sono molte malattie di recente riconoscimento per le quali essi non hanno un valore diagnostico) – Scarso valore prognostico – Scarsa efficacia nella valutazione della risposta al trattamento – Non danno una valutazione funzionale quantitativa o dinamica

Cosa c'è di nuovo tra i marcatori biochimici di funzionalità epatica?

Nuove aree di interesse • Biologia molecolare – Malattie ereditarie o genetiche – (deficit di alfa-1 -antitripsina, malattia di Wilson) • Test per valutare l'assunzione di alcol – Carbohydrate deficient transferrin (CDT) • Biomarcatori di fibrosi – PIIINP

Carbohydrate deficienct transferrin • • Transferrina : glicoproteina con p. m. 80, 000 Singola catena polipeptidica di 679 aminoacidi Due siti di legame per il Ferro, emivita 6 -12 giorni Due unità di catene laterali oligosaccaridiche con 3 -4 residui di acido sialico (funzione di stabilizzazione della molecola e di regolazione dell'affinità per il recettore) • Eliminazione per via epatica (degradazione lisosomiale) • L'alcol interfersice direttamente con l'enzima che aggiunge o rimuove i residui di acido sialico e provoca un aumento delle forme asialo, mono- e di-sialo

Senbilità e specificità di nuovi marcatori di danno epatico da alcol Test CDT Sensibilità Specificità 65 -95 90 -100 Cut-off 6 % m. AST 79 93 5 U/L GST* 60 -90 55 -100 55 IU/L AST/ALT 20 -50 10 -30 50 IU/L *Glutatione-S-transferasi
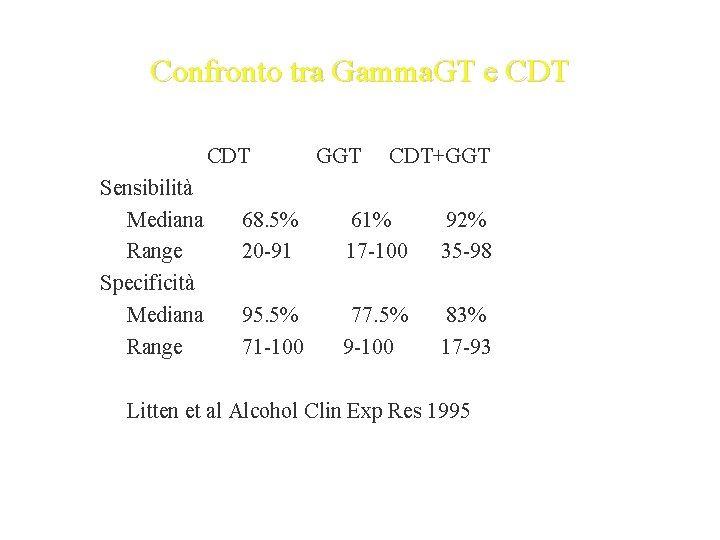
Confronto tra Gamma. GT e CDT Sensibilità Mediana Range Specificità Mediana Range GGT CDT+GGT 68. 5% 61% 92% 20 -91 17 -100 35 -98 95. 5% 77. 5% 83% 71 -100 9 -100 17 -93 Litten et al Alcohol Clin Exp Res 1995

Biomarcatori di fibrosi epatica - 1 Collagene/procollagene Tipo % nel fegato normale I 40 – 50 III 40 – 50 IV 1 V 2. 5 VI 0. 1 % nel cirrotico 60 – 70 20 – 30 1 – 2 5 – 10 0. 2

Biomarcatori di fibrosi epatica - 2 Componenti della matrice extracellulare Fibronectina (molecola di adesione) Vitronectina (molecola di adesione) Laminina (componente principale delle membrane basali cellulari) Acido ialuronico

Collagene di tipo I e III • Collageni a struttura fibrillare con tripla elica (300 nm). • Sintetizzati sotto forma di propeptidi ad entrambe le estremità delle fibrille (larghezza di 40 -50 nm). • La timozione dei propeptidi promuove la crescita delle fibrille. • I propeptidi possono essere trattenuti nella matrice extracellulare (tipo I) o rilasciati in circolo (III). • Sono disponibili immunodosaggi di PICP (propeptide C -terminale di tipo I), PINP (N-terminale), PIIINP (Nterminale di tipo III). • PIIINP appare il migliore nell'individuazione della fibrogenesi epatica.

PIIINP • Concentrazioni circolanti aumentate si riscontrano in numerose malattie epatiche: – Cirrosi alcolica, carcinoma epatocellulare, cirrosi biliare primitiva, epatite virale cronica da HCV • Possono aumentare anche in malattie non-epatiche con alterazioni del metabolismo del collagene: – Mielofibrosi, sclerosi sistemica, metastasi ossee da carcinoma mammario, ipertiroidismo
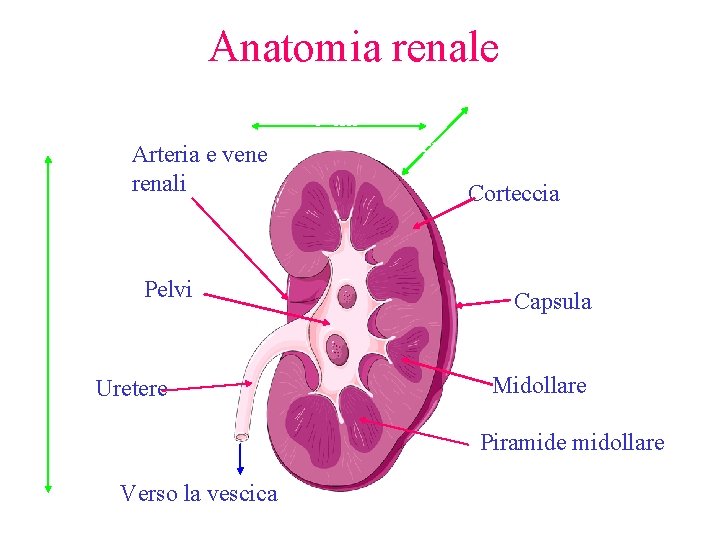
Anatomia renale 6 cm Arteria e vene renali 11 cm Pelvi Uretere 3 cm Corteccia Capsula Midollare Piramide midollare Verso la vescica

Quali sono le funzioni dei reni? • Regolazione del volume e dell'osmolarità dei liquidi corporei • Regolazione del bilancio elettrolitico • Regolazione dell'equilibrio acido-base • Escrezione di prodotti del metabolismo (urea, creatinina) e di sostanze esogene (farmaci) • Sintesi ed escrezione di ormoni • Gluconeogenesi
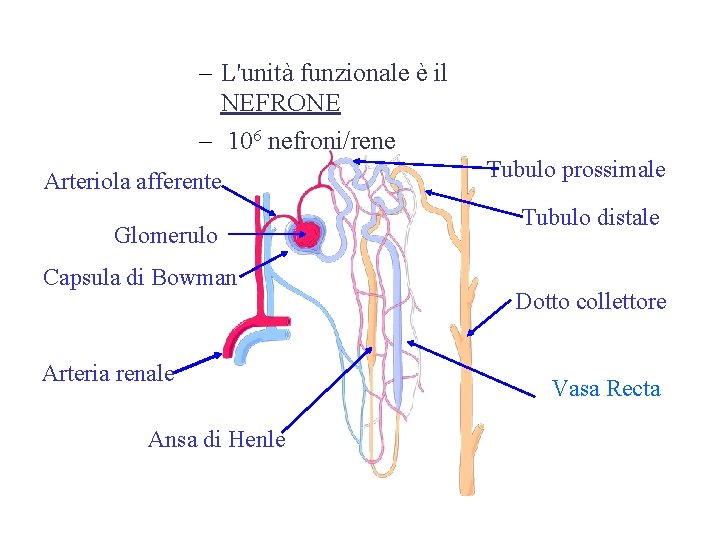
– L'unità funzionale è il NEFRONE – 106 nefroni/rene Arteriola afferente Glomerulo Capsula di Bowman Arteria renale Ansa di Henle Tubulo prossimale Tubulo distale Dotto collettore Vasa Recta
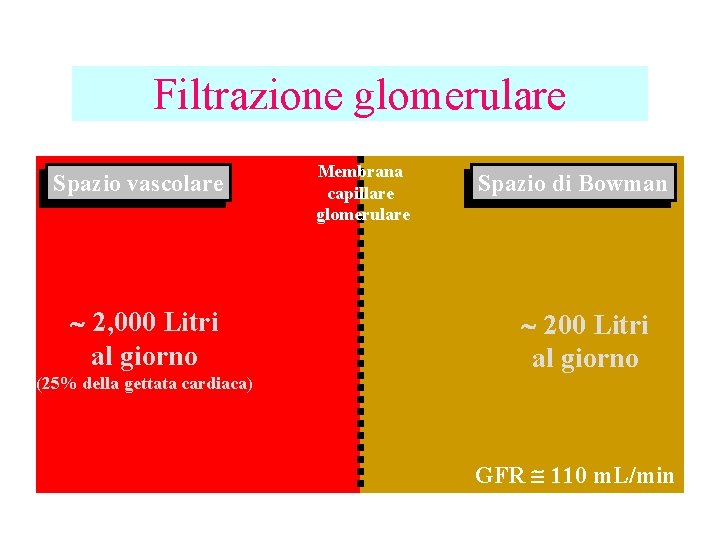
Filtrazione glomerulare Spazio vascolare 2, 000 Litri al giorno (25% della gettata cardiaca) Membrana capillare glomerulare Spazio di Bowman 200 Litri al giorno GFR 110 m. L/min

Fattori che influenzano la filtrazione • Dimensioni e forma delle molecole (<7 KDa facile, >70 KDa improbabile) • Carica negativa. La membrana basale ha una carica negativa • Pressione effettiva di filtrazione: – Un aumento della resistenza nei vasi efferenti determina un incremento della pressione nei vasi afferenti – Contro-pressione è rappresentata dalla pressione oncotica (dovuta principalmente alle proteine plasmatiche) – Il passaggio di sangue attraverso i glomeruli fa aumentare la pressione oncotica e così riduce la pressione di filtrazione

Processo dinamico • 200 litri di filtrato passano nei nefroni ogni giorno, ma solo 1 -2 litri di urina vengono prodotti, per cui oltre il 99% del filtrato viene riassorbito. • Riassorbimento – attivo o passivo – avviene praticamente a tuttti i livelli o segmenti funzionali del nefrone.

Cosa passa nel filtrato glomerulare? • Liberamente • Meno facilmente • Di solito non filtrati* filtrati – H 2 O – Na+, K+, Cl-, HCO 3 -, Ca++, Mg+, PO 4, etc. – Glucosio – Urea – Creatinina – Insulina � 2 -microglobulina# – RBP (retinolbinding protein) � 1 -microglobulin – Albumina – Immunoglobuline – Ferritina – Cellule *proteine di basso PM # talora usato come indicatore di funzionalità renale *dimensioni più grandi

Quindi, le funzioni dei tubuli renali sono: • Riassorbimento selettivo o escrezione di acqua e ioni al fine di mantenere costante la composizione idroelettrolitica dell’organismo. • Riassorbimento attivo di composti filtrati, quali glucosio ed aminoacidi.

RIASSORBIMENTO DAL FILTRATO GLOMERULARE Acqua Sodio Potassio Cloruri Bicarbonato Glucosio Albumina Urea Creatinina % riassorbimento 99. 2 99. 6 92. 9 99. 5 99. 9 100 95 -99 50 -60 0 (o negativo)

Riassorbimento tubulare e secrezione di sostanze organiche • Attivo – – Glucosio Aminoacidi Proteine (pinocitosi) 3 sistemi secretori finora identificati: • per acidi organici (per es. Penicilline) • per basi organiche forti • (per EDTA)

Riassorbimento tubulare e secrezione di sostanze organiche • Passivo – Urea: segue l’acqua e, perciò, segue Na+ & Cl • lenta diffusione attraverso la membrana, per cui vi è una escrezione netta. • Flusso più rapido causa una maggiore escrezione. – Acidi e basi deboli: • Diffusione non-ionica attraverso i lipidi della membrana.

Regolazione dell’equilibrio acido-base • Secrezione attiva di ioni idrogeno – Asse renina-aldosterone • Riassorbimento di bicarbonato. • Generazione di ammoniaca.
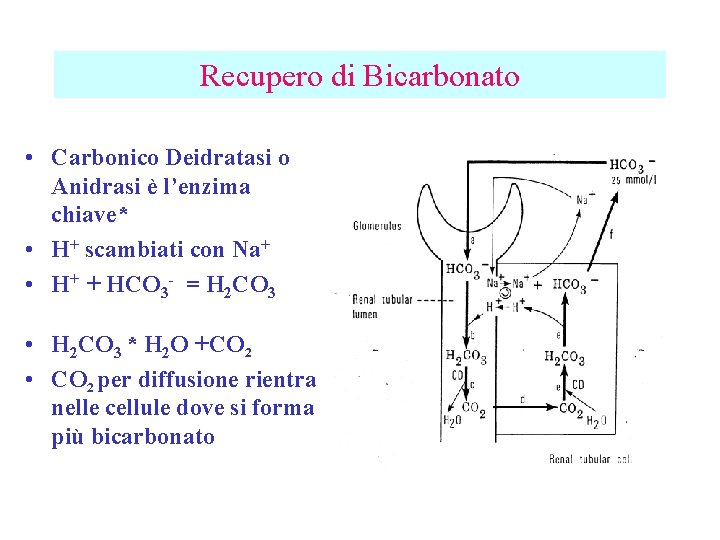
Recupero di Bicarbonato • Carbonico Deidratasi o Anidrasi è l’enzima chiave* • H+ scambiati con Na+ • H+ + HCO 3 - = H 2 CO 3 • H 2 CO 3 * H 2 O +CO 2 • CO 2 per diffusione rientra nelle cellule dove si forma più bicarbonato
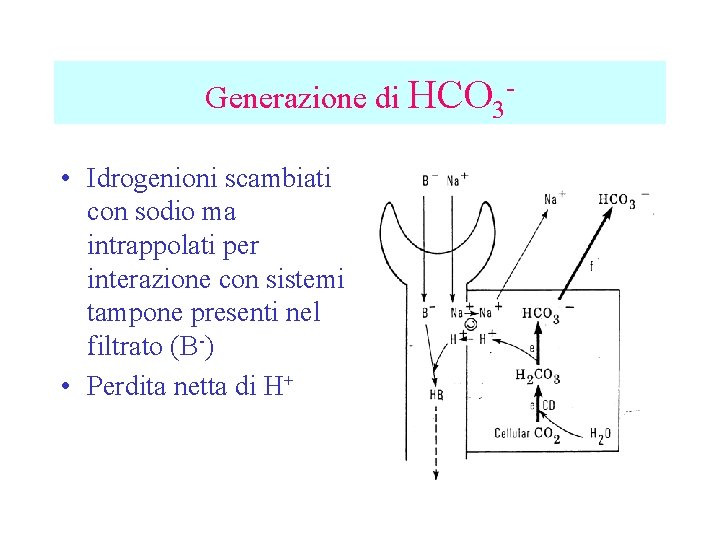
Generazione di HCO 3 - • Idrogenioni scambiati con sodio ma intrappolati per interazione con sistemi tampone presenti nel filtrato (B-) • Perdita netta di H+

Generazione di ammoniaca • Glutamina diretta verso la Gluconeogenesi • NH 3 intrappolata nel filtrato dalla reazione con idrogenioni

Funzioni endocrine del rene • Ormoni prodotti a livello renale – – Renina (apparato iuxta-glomerulare) Callikreina Prostaglandine Medullolipina (azione anti-ipertensiva, “renal medullary vasodepressor”) – 1, 25 di-idrossi-colecalciferolo (vitamina D 3) – eritropoietina

Perchè valutare la funzionalità renale? • • • Per identificare una disfunzione renale. Per diagnosticare una malattia renale. Per monitorare la progressione della malattia. Per monitorare la risposta al trattamento. Per valutare alterazioni della funzionalità che possono influenzare alcune terapie (per es. , digossina, chemioterapia).

Segni e sintomi di insufficienza renale • Sintomi dell’uremia (accumulo di prodotti tossici) (nausea, vomito, letargia) • Disordini della minzione (frequenza, nocturia, ritenzione, disuria) • Disordini del volume di urine (poliuria, oliguria, anuria) • Alterazioni della composizione delle urine (ematuria, proteinuria, bacteriuria, leucocituria, calcoli) • Dolore • Edema (ipoalbuminemia, ritenzione di acqua e sali)

Indagini biochimiche di funzionalità renale • Esame delle urine – Aspetto e colore (sangue, torbidità) – Osmolalità e peso specifico – p. H (di solito acido) – Glucosio / Corpi chetonici – Proteine – Analisi del sedimento (cellule, batteri, cristalli, cilindri*) *particelle che si formano come “stampo” mucoproteico dei tubuli del nefrone • Misurazione del filtrato glomerulare (GFR glomerular filtration rate): capacità del rene di rimuovere prodotti del catabolismo dal sangue – Test di clearance – Creatinina (insieme con urea e altri nitro-composti costituisce l'azotemia) • Test di funzionalità tubulare

Analisi delle urine • Glucosio – Aumento del glucosio plasmatico – Bassa soglia renale o altri disordini dei tubuli • Proteinuria – Normale < 200 mg/24 h. Sticks positività = >300 mg/L – Cause: • Iperafflusso (aumento di proteine a basso PM nel plasma) • Perdita glomerulare • Ridotto riassorbimento tubulare • Proteine di origine renale

Determinazione della velocità di filtrazione glomerulare (GFR) • Analisi più frequentemente utilizzata per valutare la funzionalità renale. • La misurazione è basata sul concetto di clearance: “determinazione del volume di plasma dal quale una sostanza viene rimossa attraverso la filtrazione glomerulare”

Determinazione della Clearance • Clearance = (U x. V)/P ove U è la concentrazione urinaria della sostanza x V è la velocità di formazione delle urine (m. L/min) P è la concentrazione plasmatica della sostanza x • Unità di misura = volume/unità di tempo (m. L/min) • Clearance = GFR, allora la sostanza x deve possedere le seguenti proprietà: - – viene filtrata liberamente dal glomerulo – il glomerulo rappresenta l’unica via di escrezione dal corpo (no secrezione o riassorbimento tubulare) – non è tossica ed è facilmente misurabile
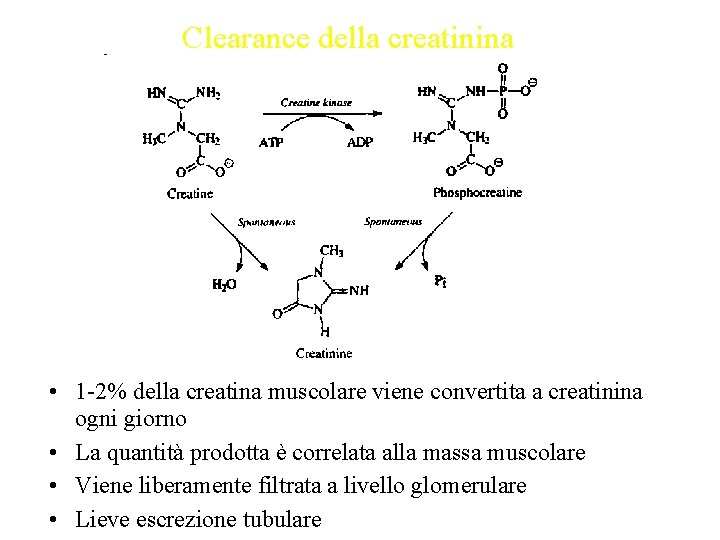
Clearance della creatinina • 1 -2% della creatina muscolare viene convertita a creatinina ogni giorno • La quantità prodotta è correlata alla massa muscolare • Viene liberamente filtrata a livello glomerulare • Lieve escrezione tubulare

Clearance della creatinina • Raccolta temporizzata delle urine per la determinazione della creatininuria (di solito 24 h) • Un campione di sangue prelevato entro il periodo di raccolta delle urine Problemi: • problemi pratici di un’accurata raccolta delle urine • Variabilità intra-soggetto = 11%, Differenza critica = 33% • Interferenze sulla misurazione della creatinina (reazione di Jaffè: bilirubina, Hb, sostanze ossido-riducenti)

Concentrazione plasmatica della Creatinina Difficoltà: • La concentrazione dipende dal bilancio tra entrate ed uscite. • La produzione è determinata dalla massa muscolare, correlata a età, sesso e peso corporeo. • Elevata variabilità inter-individuale nella popolazione a fronte di una minore variabilità intra-soggetto. • La concentrazione è inversamente proporzionale al GFR. – Piccole variazioni della creatinina portano a grandi variazioni del GFR.

Cistatina-C Newman et al Kidney Int 1995; 47: 312 -318 • Inibitore della cisteina-proteinasi C (PM 13000) • Liberamente filtrato dal glomerulo • Produzione costante da parte di tutte le cellule nucleate • Non note vie di escrezione extra-renali • Non influenzata dalla massa muscolare, dalla dieta o dal sesso • La concentrazione sierica ha una forte correlazione negativa con il GFR

Il marcatore endogeno ideale di GFR Tasso di produzione costante (creatinina dipende da massa muscolare, sesso, dieta, esercizio fisico, …) Rimosso dal circolo solo per filtrazione glomerulare (la creatinina viene eliminata anche per via intestinale e cutanea) Liberamente filtrato a livello glomerulare (è l’unico criterio soddisfatto dalla creatinina) Non riassorbito nè secreto dai tubuli renali (la creatinina ha un certo grado di riassorbimento e secrezione tubulare) La cistatina C soddisfa tutti i 4 criteri, richiede solo un prelievo di sangue, ma è un test più costoso ed ancora poco conosciuto …

Test di funzionalità tubulare (poco usati) • N-acetyl- -D-glucosaminidase (NAG) • Tubulo prossimale – – Riassorbimento di fosfati Aminoaciduria Glicosuria Escrezionale frazionale di HCO 3 - • Tubulo distale – Acidificazione (carico con cloruro d’ammonio) – Concentrazione

• Microalbuminuria – rapporto albumina: creatinina (ACR) 2. 5 mg/mmol (uomo) or 3. 5 mg/mmol (donna) o albumina 20 mg/l • Proteinuria – rapporto albumina: creatinina 30 mg/mmol o - albumina 200 mg/l

Insufficienza renale acuta • Ritenzione di: – – Urea & creatinina Na & acqua Potassio (iperkaliemia) Acidi (acidosi metabolica) Cause: • Pre-renali – Ridotta perfusione • Intrinsiche renali – – vascolari infiammatorie infiltrative tossicità • Post-renali – ostruzione

Definizione di insufficienza renale cronica

Insufficienza renale cronica: Cause • • • Glomerulonefrite Diabete mellito Ipertensione Pielonefrite cronica Rene policistico Etc.

Alterazioni degli esami di laboratorio nell’insufficienza renale cronica • • Aumento di creatinina Iperkaliemia Acidosi metabolica Ipocalcemia Iperfosfatemia Osteodistrofia (aumento della fosfatasi alcalina) Anemia normocromica normocitica
- Slides: 67