III PREDAVANJE KVALITET VODE BANJA LUKA Voda p

III PREDAVANJE “KVALITET VODE” BANJA LUKA Voda, p. H, jonska ravnoteža • Voda je medijum koja čini sastavni deo života! • Voda ulazi u sastav organizama sa 70 -90 %. • Voda i produkti jonizacije vode, hidrogenjoni (protoni) i hidroksid-joni daju značajan doprinos u karakterizaciji strukture i funkcije proteina, nukleinskih kiselina i membrana.
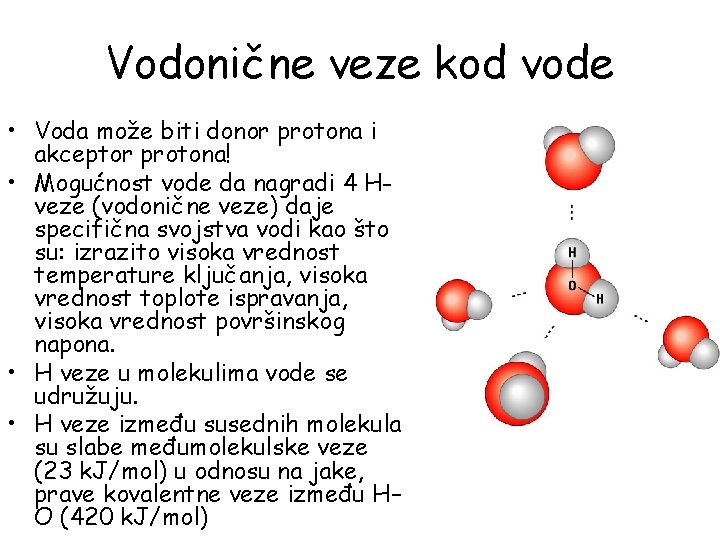
Vodonične veze kod vode • Voda može biti donor protona i akceptor protona! • Mogućnost vode da nagradi 4 Hveze (vodonične veze) daje specifična svojstva vodi kao što su: izrazito visoka vrednost temperature ključanja, visoka vrednost toplote ispravanja, visoka vrednost površinskog napona. • H veze u molekulima vode se udružuju. • H veze između susednih molekula su slabe međumolekulske veze (23 k. J/mol) u odnosu na jake, prave kovalentne veze između H– O (420 k. J/mol)

Struktura molekula vode • • • Kakva će biti struktura ugljen-dioksida? Da li će molekul ugljen-dioksida imati dipolni moment? Hoće li ugljen-dioksid graditi vodonične veze? Voda ima dva atoma vodonika koji su kovalentnom vezom povezani sa centralnim atomom kiseonika. Dva slobodna elektronska para kiseonika popunjavaju druge dve sp 3 orbitale. Struktura vode je nepravilni tetraedar. Geometrija molekula i elektronegativnost kiseonika doprinose udruženom dipolnom momentu. Normalne veze unutar tetraedra su pod uglom (kao kod metana) od 109, 5° Dipolni moment omogućava vodi da bude akceptor i donor vodonikovih jona.
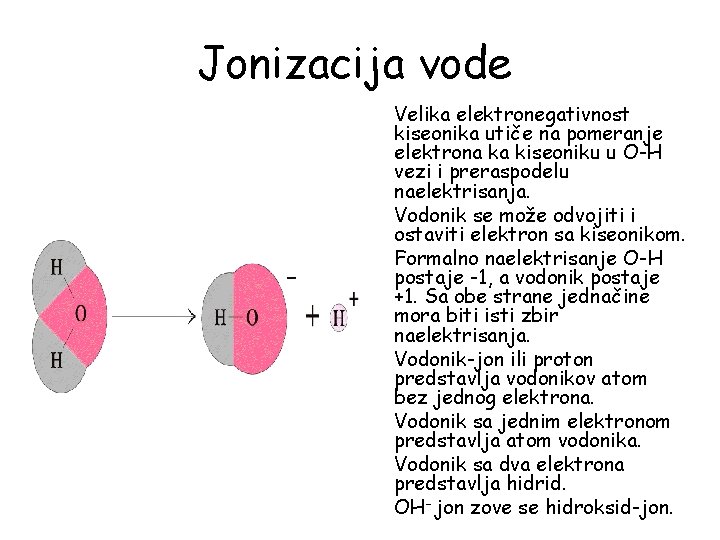
Jonizacija vode Velika elektronegativnost kiseonika utiče na pomeranje elektrona ka kiseoniku u O-H vezi i preraspodelu naelektrisanja. Vodonik se može odvojiti i ostaviti elektron sa kiseonikom. Formalno naelektrisanje O-H postaje -1, a vodonik postaje +1. Sa obe strane jednačine mora biti isti zbir naelektrisanja. Vodonik-jon ili proton predstavlja vodonikov atom bez jednog elektrona. Vodonik sa jednim elektronom predstavlja atom vodonika. Vodonik sa dva elektrona predstavlja hidrid. OH– jon zove se hidroksid-jon.
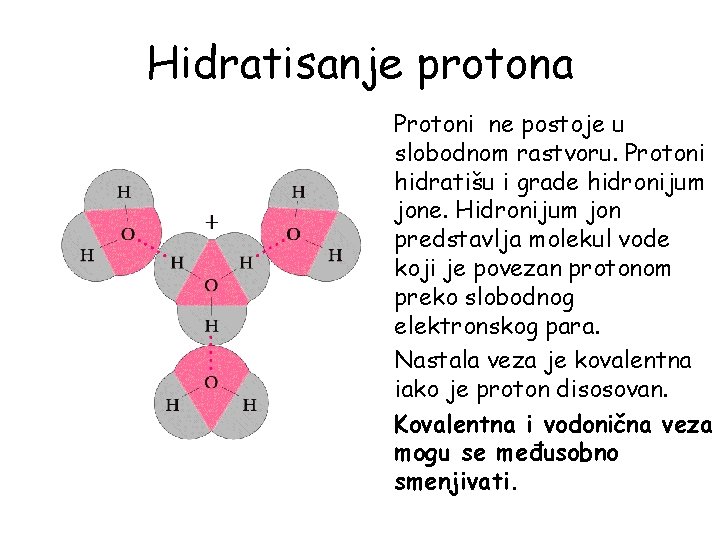
Hidratisanje protona Protoni ne postoje u slobodnom rastvoru. Protoni hidratišu i grade hidronijum jone. Hidronijum jon predstavlja molekul vode koji je povezan protonom preko slobodnog elektronskog para. Nastala veza je kovalentna iako je proton disosovan. Kovalentna i vodonična veza mogu se međusobno smenjivati.

Disocija vode 2 H 2 O ⇌ H 3 O+(aq) + OH-(aq) Jonski proizvod vode, Kw Kw = [H 3 O+] [OH-] • Konstanta ravnoteže može se napisati za reakciju disocijacije vode. • Na 25 °C, voda disosuje na [H+] i [OH–] jone, čija je koncentracija 1 x 10 -7 M. • Jonski proizvod vode, Kw, ima bojnu vrednost 1 x 10 -14. • U vodi proizvod koncentracije [H+] i [OH–] mora uvek biti 1 x 10 -14.

Šta predstavlja p. H? • • • Kako bi se izbeglo glomazno i komplikovano pisanje negativnih eksponenata, p. H skala je formirana. p. H se definiše kao negativan logaritam koncentracije vodonikovih jona. Izraz za jonski proizvod vode može se jednostavnije napisati ako se koncentracija hidoksid-jon i hidronijum-jona prikaže sa negativnim logaritomom sa obe strane jednačine. Kada je koncentracija vodonikovih i hidroksidnih jona ista p. H vrednost je 7 a sredina se smatra neutralnom. Zbir p. H i p. OH uvek mora biti 14.

Tabela 1. Izračunavanje koncentracije H 3 O+ i OH--jona u vodenim rastvorima kiselina, baza i soli

ZADATAK 1. Izračunati p. H vrednost vodenog rastvora HCl koncentracije 0, 100 mol/dm 3. Podatak: K(HCl) 103, (HCl) = 1, 00.

2. Izračunati p. H vrednost vodenog rastvora Ba(OH)2 koncentracije 0, 100 mol/dm 3. Podatak: K 1(Ba(OH)2)>1, K 2(Ba(OH)+) 2, 3 10 -1, = 1, 00

3. Izračunati p. H rastvora: a) HCl. O 4, koncentracije 0, 200 mol/dm 3, b) HNO 3, koncentracije 2, 00 10 -6 mol/dm 3.

4. Izračunati p. H vrednost nekog neutralnog vodenog rastvora na: a) 0 C; b) 25 C i c) 60 C. Podaci: Kw = 0, 12 10 -14 (0 C); Kw = 1, 0 10 -14 (25 C); Kw = 9, 6 10 -14 (60 C).

5. U rastvoru u kome je p. H=5, 00 razblaživanjem je koncentracija hidronijum-jona smanjena na polovinu prvobitne vrednosti. Izračunati p. H vrednost razblaženog rastvora?

6. Izračunati p. H rastvora koji nastaje mešanjem jednakih zapremina rastvora iste jednobazne kiseline čije su p. H vrednosti bile: 0, 00 i 1, 00.

7. Izračunati p. H vrednost vodenog rastvora NH 4 Cl koncentracije 0, 100 mol/dm 3. Podatak: K(NH 3)=1, 8 10 -5

8. Izračunati p. H vrednost u 50, 00 cm 3 rastvora NH 4 Cl koncentracije 1, 00 mol/dm 3. Podatak: K(NH 3)=1, 8 10 -5

9. Izračunati p. H rastvora koji se dobija rastvaranjem 1, 20 g NH 4 Cl u 500 cm 3 vode. Podatak: K (NH 3)=1, 8 10 -5

10. Izračunati p. H rastvora (koncentracije 0, 100 mol/dm 3): а) Na. Cl, b) Ca. Cl 2.
- Slides: 18