II Nombres quantiques configuration lectronique II Nombres quantiques

II. Nombres quantiques & configuration électronique II. Nombres quantiques et structure électronique des atomes

II. Nombres quantiques & configuration électronique 1. Les 4 nombres quantiques de l ’atome En mécanique quantique : la position et la vitesse d ’une particule ne peuvent être connues précisément (cf. fin du cours). Pour obtenir les informations (probabilité de présence, . . . ) sur l ’e- d ’un atome d ’hydrogène, on doit connaître 4 valeurs fondamentales : les nombres quantiques.

II. Nombres quantiques & configuration électronique 1. 1 L ’expérience de Stern et Gerlach Rappel : le dipôle magnétique M Circuit fermé parcouru par un courant I ; moment magnétique : Analogie : électron se déplaçant sur une orbite circulaire autour du noyau : courant I = dq/dt = -e/T , avec T = 2 r/v I D ’où : Force s ’exerçant sur le dipôle (/ l ’atome) lorsque celui-ci est placé dans un champ magnétique :
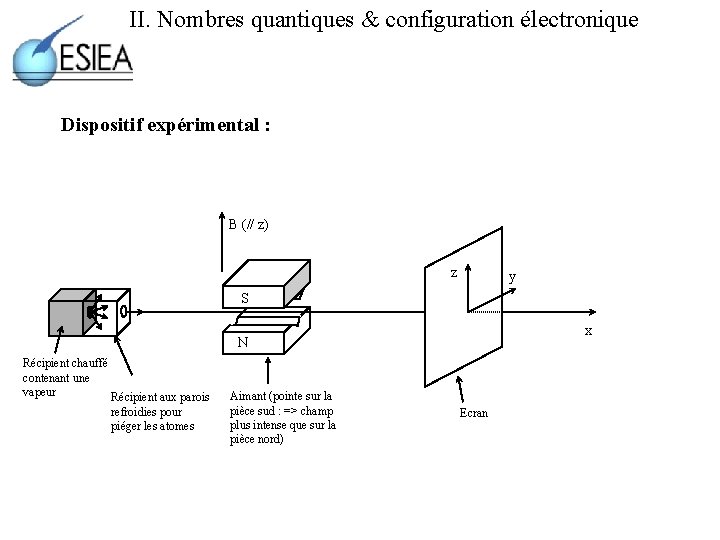
II. Nombres quantiques & configuration électronique Dispositif expérimental : B (// z) z y S x N Récipient chauffé contenant une vapeur Récipient aux parois refroidies pour piéger les atomes Aimant (pointe sur la pièce sud : => champ plus intense que sur la pièce nord) Ecran

II. Nombres quantiques & configuration électronique Force subie par les atomes passant dans le champ de l ’aimant : PFD : F = ma ; donc les atomes sont d ’autant plus déviés de leur trajectoire (selon Oz) que « leur Mz » est grand (si Mz = 0, c ’est à dire si M perpendiculaire à B : aucune déviation - les atomes continuent leur trajet en ligne droite vers l ’écran) Septembre 2001 Cours de physique atomique
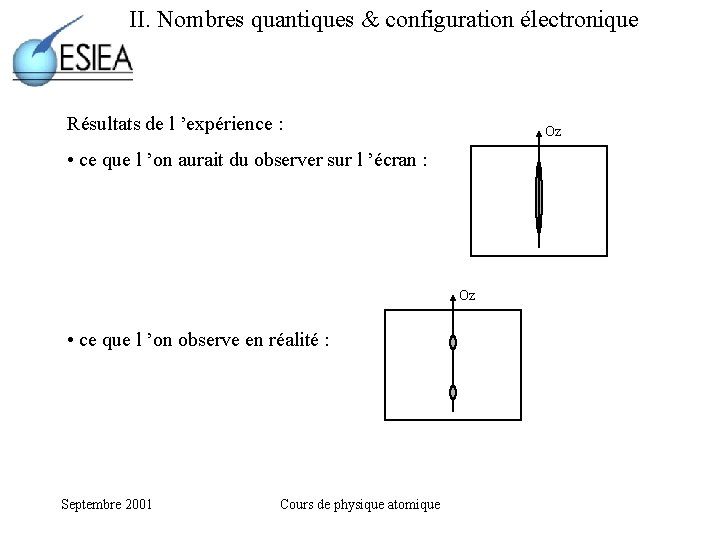
II. Nombres quantiques & configuration électronique Résultats de l ’expérience : Oz • ce que l ’on aurait du observer sur l ’écran : Oz • ce que l ’on observe en réalité : Septembre 2001 Cours de physique atomique

II. Nombres quantiques & configuration électronique Aucun atome ne fut détecté en z = 0. . . Tous les atome étaient déviés dans deux directions bien précises, opposées l ’une de l ’autre par rapport à z = 0. Conclusion : la composante selon z du moment magnétique Mz ne peut prendre que des valeurs discrètes, opposées l ’une de l ’autre ; c ’est la quantification spatiale. Par la suite, les recherches ont permis d ’aboutir à la quantification de plusieurs grandeurs physiques. Des recherches plus poussées basées sur l ’expérience de Stern et Gerlach ont donné l ’idée à Uhlenbeck (1925) d ’introduire la notion de spin de l ’électron : certains résultats expérimentaux ne pouvaient s ’expliquer que par l ’existence d ’un moment magnétique propre de l ’électron, comme si celui-ci tournait sur lui-même. . . Septembre 2001 Cours de physique atomique

II. Nombres quantiques & configuration électronique Remarque : Pour décrire complètement le comportement de l ’atome, il faut tenir compte des contributions des moments cinétiques du noyau, de l ’e(spin) et surtout des interactions entre ces grandeurs… Impossible en physique classique : => recours à la mécanique quantique indispensable (addition des moments cinétiques). Septembre 2001 Cours de physique atomique

II. Nombres quantiques & configuration électronique 1. 2 Le nombre quantique principal n : • Détermine l ’énergie de l ’électron (et le rayon de sa trajectoire si celle ci est supposée circulaire - modèle de Bohr). • Ne peut prendre que des valeurs entières de 1 à l ’infini. • Pour un certain n on parle de « couche » électronique, désignée par la lettre K si n=1, L si n=2, M si n=3, etc. . .

II. Nombres quantiques & configuration électronique 1. 3 Le nombre quantique orbital l : • Détermine, sur une orbite de l ’électron, le moment de la quantité de mouvement. • Ne peut prendre que des valeurs entières de 0 à n-1. 1. 4 Le nombre quantique magnétique ml : • Lié à la quantification de la projection du moment cinétique orbital selon un axe Oz (axe selon lequel on applique un champ magnétique) • Ne peut prendre que les 2 l+1 valeurs entières comprises entre -l et l. 1. 5 Le nombre quantique de spin ms : • Même rôle par rapport au spin de l ’e- que ml par rapport à l. • Ne peut prendre pour valeurs que 1/2 ou -1/2

II. Nombres quantiques & configuration électronique 2. Le principe de Pauli Chaque état permis de l ’e- dans un atome, état caractérisé par l ’ensemble des quatre nombres quantiques (n, l, ms) , ne peut contenir qu ’un seul e- au maximum. (principe ne découlant d ’aucune théorie, n ’étant directement démontrable par aucune expérience…) Septembre 2001 Cours de physique atomique

II. Nombres quantiques & configuration électronique 4. La classification périodique des éléments • Structure électronique des atomes liée directement à la classification de Mendeleïev. • Un état électronique correspond à un quadruplet des 4 nombres quantiques. Le nombre quantique principal n correspondant à une « couche » est noté en chiffres (1, 2, 3, …), le nombre quantique secondaire l correspondant à une « sous couche » est noté en lettres (s, p, d, f pour l = 0, 1, 2, 3). Ex : sous couche l = 1 de la couche n = 2 : notée « 2 p » . • Dans une sous couche (n, l) : on peut avoir jusqu ’à 2*(2 l+1) e-. Le nombre d ’e- dans une sous couche est noté en exposant du symbole de la sous couche. Ex : 3 p 2 désigne deux e- dans la sous couche (n=3, l=1). Septembre 2001 Cours de physique atomique

II. Nombres quantiques & configuration électronique Règles de remplissage des couches et sous couches électroniques des atomes : Règle de Klechkowsky : • Remplissage à (n+l) croissant • Si plusieurs valeurs de (n+l) identiques : remplissage du n le plus petit en priorité. • => 1 s 2 s 2 p 3 s 3 p 4 s 3 d 4 p 5 s etc. . . Septembre 2001 Cours de physique atomique

II. Nombres quantiques & configuration électronique Notation symbolique : Ex d ’un atome à 6 électrons (carbone, C) : 1 s 2 2 p 2 => Règle de Hund : si un atome est caractérisé par des états de même énergie, les e- se répartissent en occupant le maximum d ’états et avec des spins parallèles. Ex : Azote (N) 1 s 2 2 p 3 Oxygène (O) 1 s 2 2 s 2 Septembre 2001 2 p 4 Cours de physique atomique

II. Nombres quantiques & configuration électronique Le cas des gaz rares : = atomes les plus stables, car dont les couches sont toutes complètement remplies. Les autres atomes : peuvent s ’associer pour mettre en commun les e- de leurs couches de valence et retomber ainsi vers des configurations plus stables avec toutes leurs couches remplies : = formation des molécules. Ex : l ’eau H 2 O : liaison covalente entre deux atomes d ’H et un atome d ’O Oxygène (O) 1 s 2 2 s 2 O 2 p 3 + H Hydrogène (H) 1 s 1 Septembre 2001 = Cours de physique atomique H O H

II. Nombres quantiques & configuration électronique La classification périodique • éléments classés par ordre croissant de numéro atomique • éléments ayant les mêmes propriétés chimiques classés dans une même colonne • dernière colonne : les gaz rares (couche de valence pleine => pas d ’association possible avec d ’autres atomes : se trouvent dans la nature dans leur état monoatomique) • colonne 17 : les halogènes ; manque un e- pour arriver à la configuration électronique du gaz rare le plus proche : => grande affinité électronique • colonne 1 : les alcalins ; un e- en trop pour arriver à la configuration du gaz rare le plus proche : => énergie d ’ionisation faible Septembre 2001 Cours de physique atomique

II. Nombres quantiques & configuration électronique Septembre 2001 Cours de physique atomique
- Slides: 17