IFRN Campus Apodi Equilbrio Qumico Parte 2 Profa

IFRN - Campus Apodi Equilíbrio Químico Parte 2 Profa. Karen

Relação entre Kc e Kp Embora Kc e Kp representem valores constantes à mesma temperatura, elas não são necessariamente iguais. A relação entre elas é dada considerando-se a equação de estado dos gases : P. V = n. R. T 2

Considere a reação abaixo: N 2 O 4 (g) ↔ 2 NO 2 (g) Observe a relação entre Kc e Kp: Kc = [NO 2]2 / [N 2 O 4] Kp = (PNO 2)2 / PN 2 O 4 Aplicando a equação dos gases para NO 2 e para N 2 O 4: PNO 2 = n. R. T V = [NO 2]. R. T PN 2 O 4 = n. R. T = [N 2 O 4]. R. T V 3
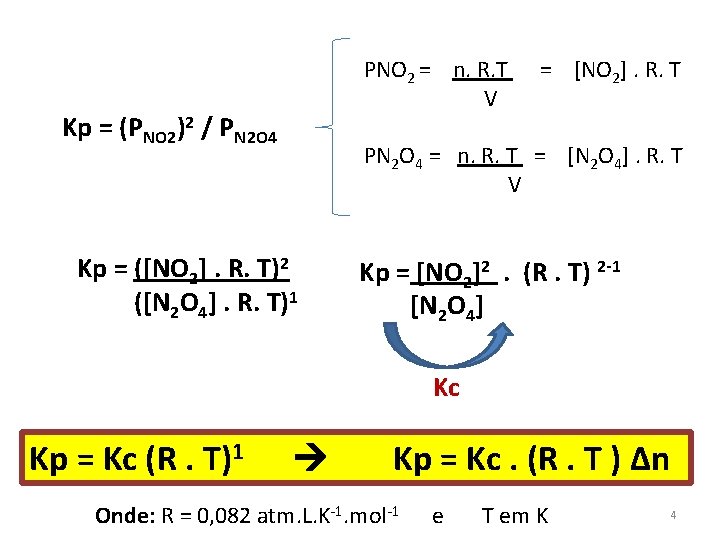
PNO 2 = n. R. T V Kp = (PNO 2)2 / PN 2 O 4 = [NO 2]. R. T PN 2 O 4 = n. R. T = [N 2 O 4]. R. T V Kp = ([NO 2]. R. T)2 ([N 2 O 4]. R. T)1 Kp = [NO 2]2. (R. T) 2 -1 [N 2 O 4] Kc Kp = Kc (R. T)1 Kp = Kc. (R. T ) Δn Onde: R = 0, 082 atm. L. K-1. mol-1 e T em K 4
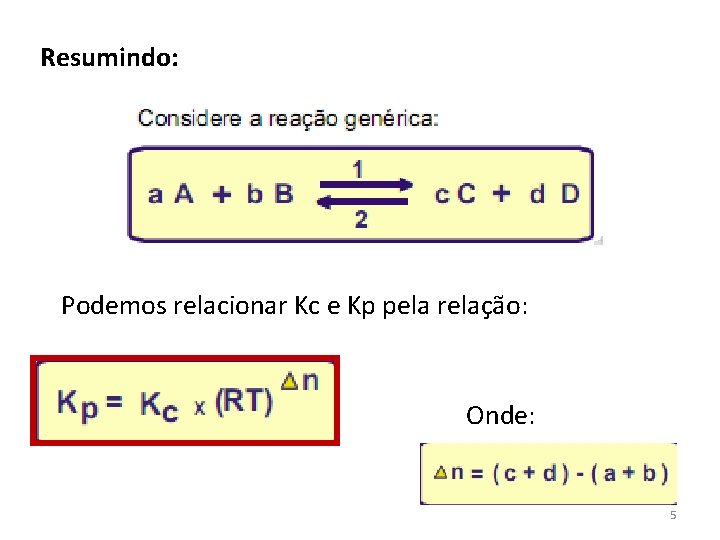
Resumindo: Podemos relacionar Kc e Kp pela relação: Onde: 5

Para a reação de síntese do metanol, CH 3 OH, a partir de hidrogênio e monóxido de carbono: 2 H 2(g) + CO (g) ↔CH 3 OH (g) Kc vale 300, a 425 o. C. Qual o valor de Kp a essa temperatura? 6

7

1 Na equação a A + b B c C + d D, após atingir o 2 equilíbrio químico, podemos concluir a respeito da constante de equilíbrio que: a) Quanto maior for o valor de Kc, menor será o rendimento da reação direta. b) Kc independe da temperatura. c) Se as velocidades das reações direta e inversa forem iguais, então K 2 = 0. d) Kc depende das molaridades iniciais dos reagentes. e) Quanto maior for o valor de Kc, maior será a concentração dos produtos. 8

9

Cálculo das constantes de equilíbrio Quando são conhecidas as pressões parciais no equilíbrio de todos os reagentes e produtos, a constante de equilíbrio pode ser calculada diretamente a partir da expressão de constante de equilíbrio. 10

Uma mistura de hidrogênio e nitrogênio em um recipiente de reação atinge o equilíbrio a 472 o. C. A mistura de gases em equilíbrio foi analisada e descobriu-se que ela contém 7, 38 atm de H 2, 2, 46 atm de N 2 e 0, 166 atm de NH 3. A partir desses dados calcule a constante de equilíbrio para: N 2(g) + 3 H 2(g) 2 NH 3 (g) 11

Aplicações das constantes de equilíbrio Determinando o sentido da reação Suponha que coloquemos uma mistura de 2 mol de H 2, 1 mol de N 2 e 2 mol de NH 3 em um recipiente de 1 L a 472 o. C. N 2 e H 2 reagirão para formar mais NH 3. Nessa instância devemos: 1) calcular a pressão parcial inicial de cada espécie, usando a equação de gás ideal. 2) Inserir as pressões parciais de N 2, H 2 e NH 3 na expressão da constante de equilíbrio. 3) Analise o resultado e compare com o Kc calculado anteriormente para a mesma equação na mesma temperatura. 12

Aplicações das constantes de equilíbrio Quando substituímos as pressões parciais ou concentração dos produtos e reagentes na expressão da constante de equilíbrio, o resultado é conhecido como quociente da reação, representado pela letra Q. 13

Aplicações das constantes de equilíbrio Determinando o sentido de reação • Definimos Q, o quociente da reação, para uma reação geral como • Sendo que : Q = K somente com o sistema em equilíbrio. 14

Aplicações das constantes de equilíbrio Prevendo o sentido da reação • Se Q > K, então a reação inversa deve ocorrer para atingir o equilíbrio (ex. , produtos são consumidos, reagentes são formados, o numerador na expressão da constante de equilíbrio diminui e Q diminui até se igualar a K). • Se Q < K, então a reação direta deve ocorrer para atingir o equilíbrio. 15
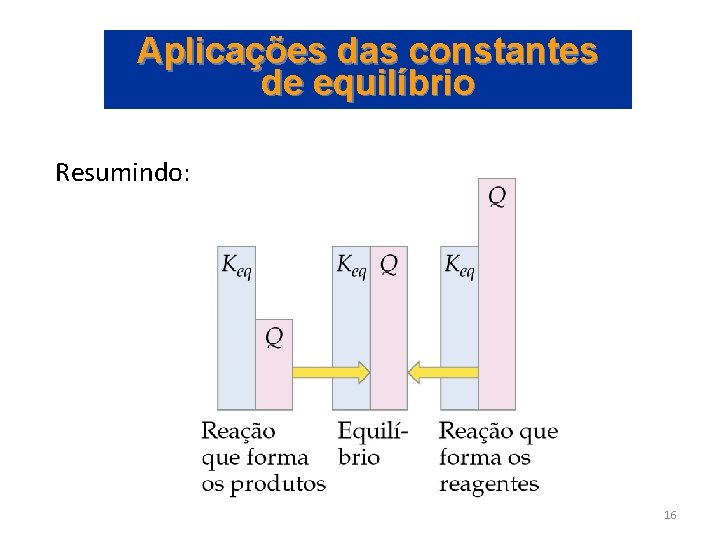
Aplicações das constantes de equilíbrio Resumindo: 16

Ex. : A 448 o. C a constante de equilíbrio , Keq, para a reação: H 2 (g) + I 2(g) 2 HI (g) é 51. Determine como a reação prosseguirá para atingir o equilíbrio a 448 o. C se começarmos com 2 x 10 -2 mol de HI, 1 x 10 -2 mol de H 2 e 3 x 10 -2 mol de I 2 em um recipiente de 2 L. 17

Notas do 4º BIM 1 prova: peso 2 1 atividade extra-classe (sábado letivo): peso 2 Grupo de 5 pessoas: (Seminário individual (70%) + roteiro de prática (30%))

Temas: Grupo 1 Gases Grupo 2 Soluções Grupo 3 Soluções Grupo 4 Cinética Química Grupo 5 Termoquímica Grupo 6 Equilíbrio Químico Grupo 7 Eletroquímica

Seminário: Objetivo da prática Introdução teórica Reagentes e materiais utilizados Desenvolvimento/procedimento experimental Resultados e discussões Aplicação do tema no cotidiano Conclusão Obs. : Apresentar vídeo e/ou fotos da prática

Roteiro da prática Objetivo Introdução teórica Materiais e reagentes utilizados Procedimento experimental Pré-laboratório Referências bibliográficas

Cálculo das concentrações em equilíbrio Para a reação N 2(g) + 3 H 2 (g) 2 NH 3 (g), Keq = 1, 45 x 10 -5 a 500 o. C. Em uma mistura em equilíbrio dos três gases a 500 o. C, a pressão parcial de H 2 é 0, 928 atm e a pressão parcial de N 2 é 0, 432 atm. Qual a pressão parcial de NH 3 nessa mistura no equilíbrio? 22

Um frasco de 1 L é preenchido com 1 mol de H 2 e 2 mol de I 2 a 448 o. C. O valor da constante de equilíbrio, Keq, para a reação: H 2(g) + I 2(g) 2 HI (g) A 448 o. C é 50, 5. Quais são as pressões parciais de H 2, I 2 e HI no equilíbrio? 23
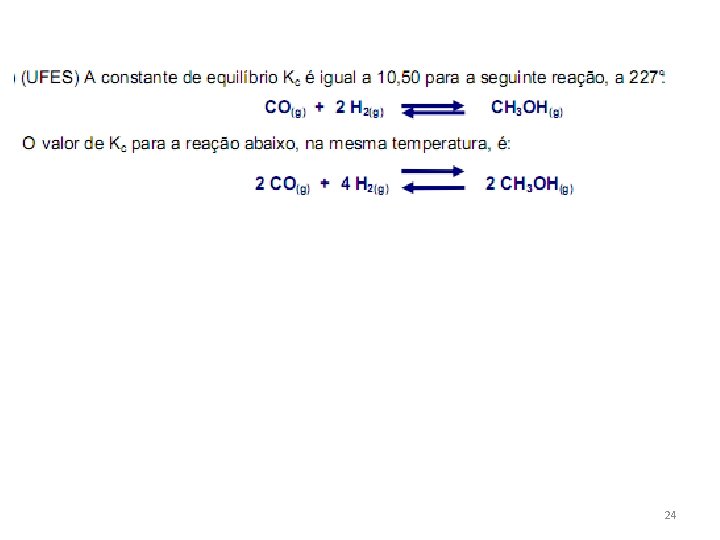
24

A reação reversível abaixo é endotérmica e admite os seguintes valores da constante K: Partindo-se de uma mistura equimolar de CO(g) e H 2 O(g), todas afirmativas a seguir estão corretas, exceto: a) Os compostos que predominam, no equilíbrio, a 250°C, são CO (g) e H 2 O(g). b) Os compostos que predominam, no equilíbrio, a 950°C, são CO 2(g) e H 2(g). c) Com o aumento da temperatura, a constante de equilíbrio K aumenta. d) À temperatura de 850°C, as concentrações de reagentes e produtos, no equilíbrio, são iguais. e) Aumentando a temperatura, haverá predominância, no equilíbrio, dos compostos CO(g) e H 2 O(g). 25

Deslocamento de equilíbrio É possível alterar um equilíbrio químico por meio de algumas ações externas. Tal tipo de ação é chamado pertubação do equilíbrio, e a sua consequência é denominada deslocamento de equilíbrio. Existe um importantíssimo princípio químico que permite prever qual será o efeito de uma pertubação sobre um equilíbrio. Ele é denominado Princípio de Le Chantelier.

Deslocamento de equilíbrio Consideremos um sistema em equilíbrio químico, com as substâncias A, B, C e D.
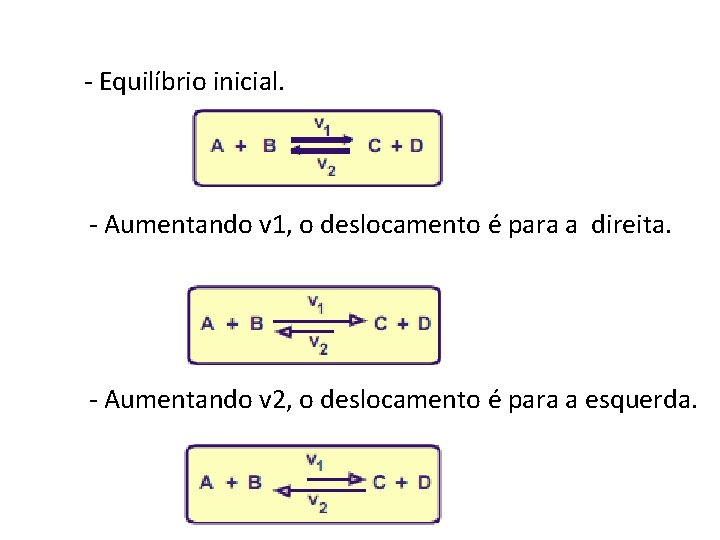
- Equilíbrio inicial. - Aumentando v 1, o deslocamento é para a direita. - Aumentando v 2, o deslocamento é para a esquerda.

“Quando um sistema em equilíbrio sofre algum tipo de perturbação externa, ele se deslocará no sentido de minimizar essa perturbação, a fim de atingir novamente uma situação de equilíbrio”.

É possível provocar alteração em um equilíbrio químico por variações de: - temperatura, - concentração de participantes da reação e - pressão total sobre o sistema.
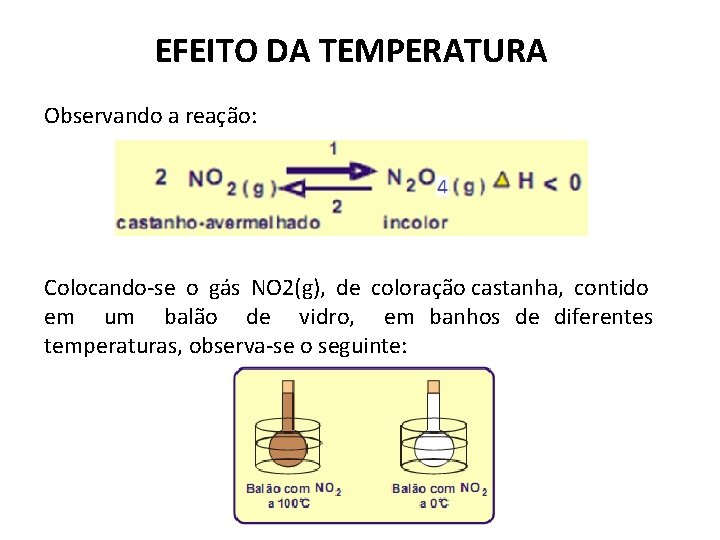
EFEITO DA TEMPERATURA Observando a reação: Colocando-se o gás NO 2(g), de coloração castanha, contido em um balão de vidro, em banhos de diferentes temperaturas, observa-se o seguinte:
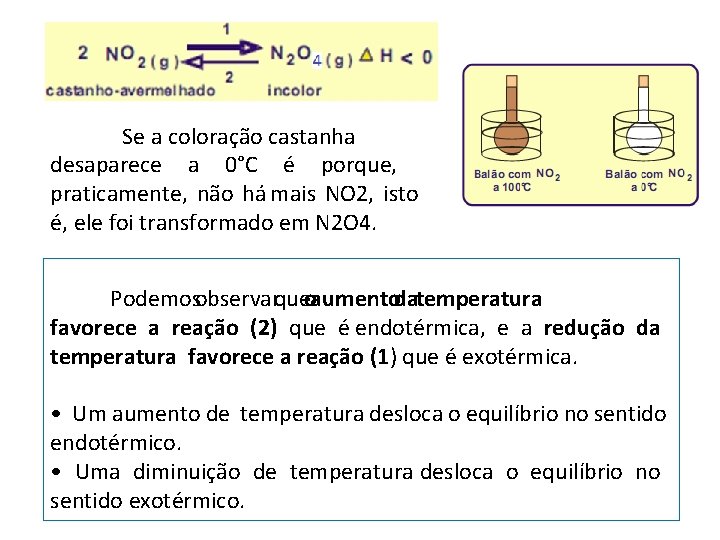
Se a coloração castanha desaparece a 0°C é porque, praticamente, não há mais NO 2, isto é, ele foi transformado em N 2 O 4. Podemosobservarqueoaumentodatemperatura favorece a reação (2) que é endotérmica, e a redução da temperatura favorece a reação (1) que é exotérmica. • Um aumento de temperatura desloca o equilíbrio no sentido endotérmico. • Uma diminuição de temperatura desloca o equilíbrio no sentido exotérmico.

No exemplo em questão, temos: endo Calor + N 2 O 4 (g) exo 2 NO 2 (g) AH= +57, 2 k. J (Reação direta endot) Aumento da T desloca o equilíbrio no sentido endo Diminuição da T desloca o equilíbrio no sentido exo
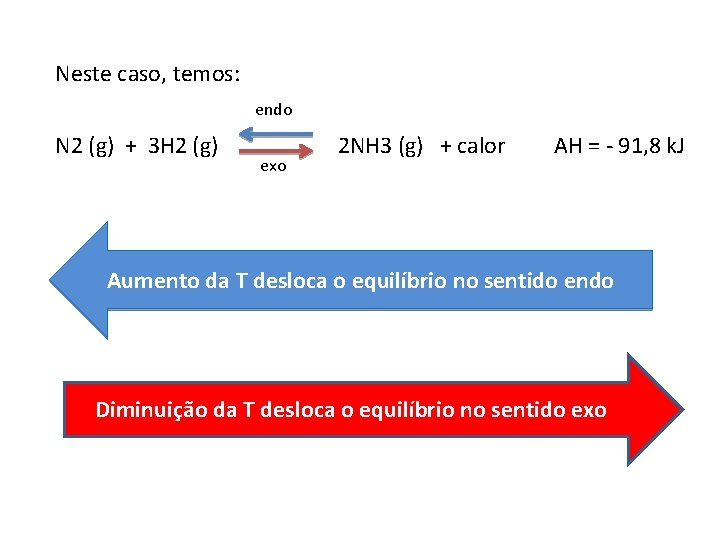
Neste caso, temos: endo N 2 (g) + 3 H 2 (g) exo 2 NH 3 (g) + calor AH = - 91, 8 k. J Aumento da T desloca o equilíbrio no sentido endo Diminuição da T desloca o equilíbrio no sentido exo

Variação de Kc com a temperatura Por meio de investigações experimentais, verificou-se que o aquecimento pode aumentar ou diminuir o valor da constante de equilíbrio e que isso depende do valor do AH da reação. O aumento da temperatura provoca aumento da constante de equilibrio para reações endotérmicas (AH>0) e diminuição para exotérmicas (AH<0).
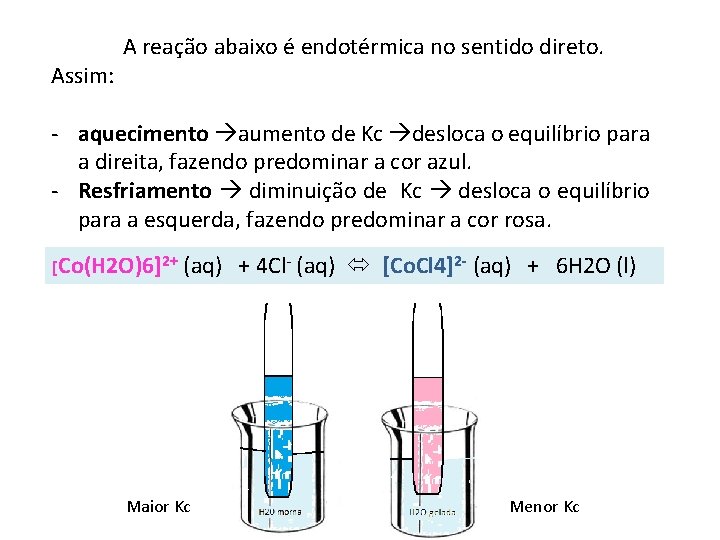
Assim: A reação abaixo é endotérmica no sentido direto. - aquecimento aumento de Kc desloca o equilíbrio para a direita, fazendo predominar a cor azul. - Resfriamento diminuição de Kc desloca o equilíbrio para a esquerda, fazendo predominar a cor rosa. [Co(H 2 O)6]2+ (aq) + 4 Cl- (aq) [Co. Cl 4]2 - (aq) + 6 H 2 O (l) Maior Kc Menor Kc


EFEITO DA CONCENTRAÇÃO Supondo o equilíbrio: N 2(g) + 3 H 2(g) ⇐> 2 NH 3(g) Se tivermos colocado N 2, H 2 e NH 3 em um recipiente mantido à temperatura constante e que seja esperado até que o sistema atinja o equilíbrio. Será medido em seguida a concentração de equilíbrio de cada uma das três substâncias.

N 2(g) + 3 H 2(g) ⇐> 2 NH 3(g) Seqüencialmente, o equilíbrio será perturbado adicionando H 2 no recipiente. A [ ] de cada substância mostra ser cte à esquerda do gráfico: o sistema está em equilíbrio. Repentinamente, a [H 2] aumenta, quando maior quantidade é adicionada ao recipiente. A [N 2] e de [H 2] imediatamente começou a diminuir, ao mesmo tempo a [NH 3] começou a aumentar. Estas mudanças ocorrem quando falamos que o equilíbrio "foi deslocado para a direita".
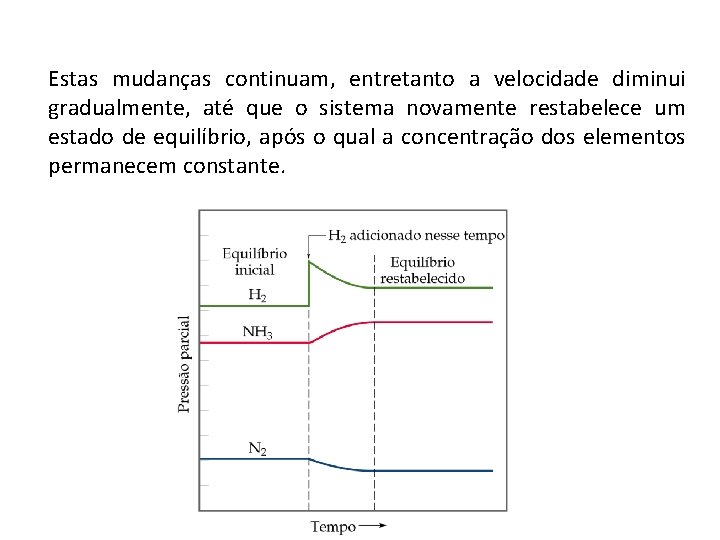
Estas mudanças continuam, entretanto a velocidade diminui gradualmente, até que o sistema novamente restabelece um estado de equilíbrio, após o qual a concentração dos elementos permanecem constante.

Neste experimento, parte da quantidade de H 2 adicionado é consumida no deslocamento do equilíbrio, assim, o efeito da adição (aumento na concentração) é parcialmente compensado. Em outras palavras, o ajuste do sistema tende a minimizar o efeito de adição de H 2, como prevê o princípio de Le Châtelier.

N 2(g) + 3 H 2(g) ⇐> 2 NH 3(g) - Um aumento na [reagentes] ou uma diminuição na [produtos] desloca o equilíbrio para a direita. - Uma diminuição da [reagentes] ou um aumento da [produtos] desloca o equilíbrio para a esquerda.

EFEITO DA PRESSÃO Alterações de pressão influenciam em equilíbrios que possuem espécies químicas no estado gasoso. Considere a reação química em equilíbrio abaixo:
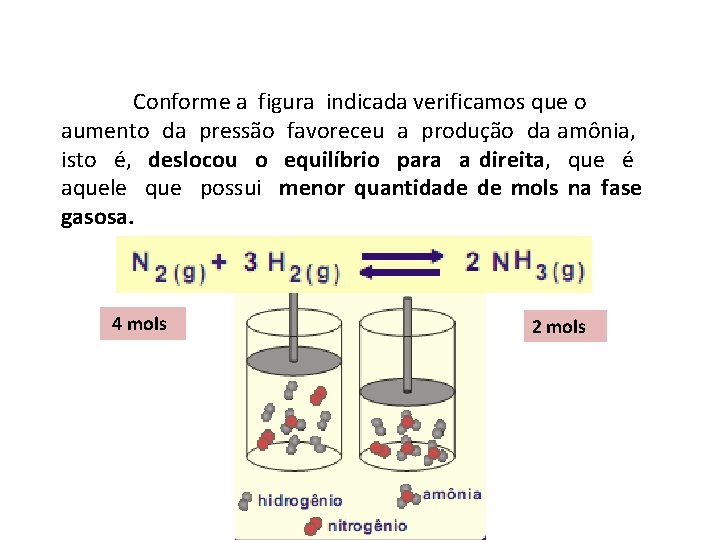
Conforme a figura indicada verificamos que o aumento da pressão favoreceu a produção da amônia, isto é, deslocou o equilíbrio para a direita, que é aquele que possui menor quantidade de mols na fase gasosa. 4 mols 2 mols

Se a pressão fosse diminuída o equilíbrio se deslocaria para a esquerda, favorecendo o consumo de amônia, isto é, no sentido da maior quantidade de mols na fase gasosa Generalizando: • O aumento da P sobre o sistema desloca o equilíbrio químico no sentido do menor número de mols na fase gasosa. • A diminuição da P sobre o sistema desloca o equilíbrio químico no sentido do maior número de mols na fase gasosa.

Exercícios: 01)Considere a reação em equilíbrio químico: N 2 (g) + O 2 (g) 2 NO(g) É possível deslocá-lo para a direita: a) Retirando o N 2 existente. b) Removendo o NO formado. c) Introduzindo um catalisador. d) Diminuindo a pressão, à temperatura constante. e) Aumentando a pressão, à temperatura constante.

02)Temos o equilíbrio: CO (g) + H 2 O (g) CO 2 (g) + H 2 (g) Queremos aumentar a concentração de CO 2(g) nesse equilíbrio. Para isso ocorrer, devemos: a) b) c) d) e) Aumentar a pressão sobre o sistema. Diminuir a pressão sobre o sistema. Adicionar H 2 (g) ao sistema. Retirar H 2 O (g) do sistema. Adicionar CO (g) ao sistema.

03)O equilíbrio gasoso representado pela equação: N 2(g) + O 2(g) 2 NO(g) – 88 kj É deslocado no sentido de formação de NO(g), se: a) b) c) d) e) a pressão for abaixada. N 2 for retirado. a temperatura for aumentada. for adicionado um catalisador sólido ao sistema. o volume do recipiente for diminuído

04) O equilíbrio N 2 (g) + 3 H 2 (g) 2 NH 3 (g) é deslocado para os produtos com o aumento da pressão e com a diminuição da temperatura. Pode-se concluir que a reação de formação do gás amoníaco é: a) b) c) d) e) Exotérmica e ocorre com o aumento de volume. Exotérmica e ocorre com a conservação do volume. Exotérmica e ocorre com a diminuição do volume. Endotérmica e ocorre com aumento de volume. Endotérmica e ocorre com diminuição de volume.

05)Nitrogênio e hidrogênio reagem para formar amônia segundo a equação: N 2(g) + 3 H 2(g) 2 NH 3(g) + 22 kcal Se a mistura dos três gases estiver em equilíbrio e provocarmos: I. Compressão da mistura. II. Aumento de temperatura. III. Introdução de hidrogênio adicional. O efeito sobre a quantidade de amônia, em cada situação, será:

EFEITO DO CATALISADOR O catalisador não desloca o equilíbrio • um catalisador faz com que um processo chegue mais rapidamente à situação de equilíbrio. • O catalisador reduz a barreira de energia de ativação Ea para a reação.
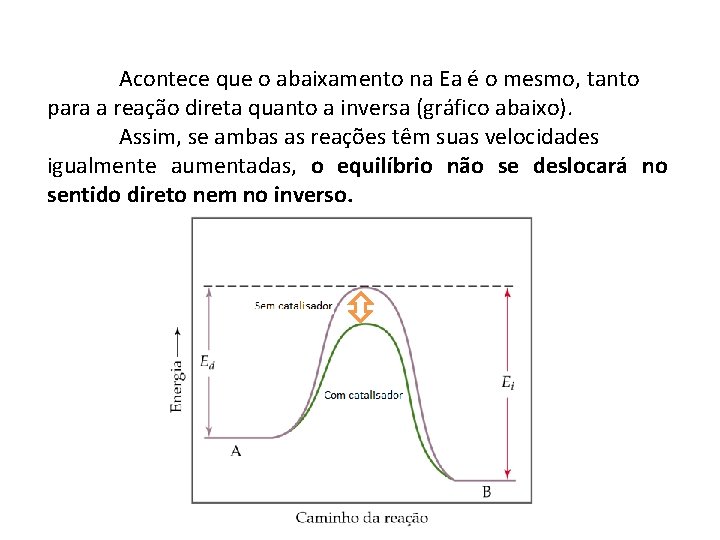
Acontece que o abaixamento na Ea é o mesmo, tanto para a reação direta quanto a inversa (gráfico abaixo). Assim, se ambas as reações têm suas velocidades igualmente aumentadas, o equilíbrio não se deslocará no sentido direto nem no inverso.

U. F. R. S) A reação genérica A B, a 25 o. C, tem por constante de velocidade, para a reação direta, 6 min – 1, e, para a reação inversa, 3 min – 1. O valor da constante de equilíbrio naquela temperatura é:

(UFAM) A reação química genérica, abaixo representada, possui constante de equilíbrio igual a 120, a 25°C. É correto afirmar que: A(g) + B(g) C(g) + D(g) K = 120 a) Em 50°C a constante de equilíbrio terá valor igual a 240. b) No equilíbrio haverá maior quantidade de reagentes que de produtos. c) No equilíbrio, as quantidades de reagentes e produtos são iguais. d) No equilíbrio haverá maior quantidade de produto que de reagentes.

Considere um sistema em equilíbrio a 25°C e 1 atm representado pela equação: Fe. O(s) + CO(g) CO 2(g) + Fe(s) + 19 kj/mol Se K for constante de equilíbrio, qual das seguintes ações poderá aumentar seu valor numérico? a) b) c) d) e) aumentar a pressão. aumentar a temperatura. aumentar a concentração do CO. triturar mais o óxido de ferro. utilizar um catalisador


(Vunesp-SP) Sabendo que a reação representada pela equação: H 2(g) + Br 2(g) 2 HBr(g) É exotérmica, é correto afirmar que o equilíbrio: a) se deslocará para a esquerda, no sentido da formação de H 2 e do Br 2, com o aumento da pressão. b) se deslocará para a direita, no sentido de formação do HBr, com o aumento da pressão. c) se deslocará para a direita, no sentido de formação do HBr, com o aumento da temperatura. d) se deslocará para a direita, no sentido de formação do HBr, com a diminuição da temperatura. e) não é alterado por mudanças apenas na temperatura do sistema.
- Slides: 57