IEVADS NAS BIOLOIJ I DZVBAS MIJA ORGANISKO VIELU

IEVADS ŠŪNAS BIOLOĢIJĀ I DZĪVĪBAS ĶĪMIJA ORGANISKO VIELU KLASIFIKĀCIJAS PAMATI UN GALVENĀS FUNKCIONĀLĀS GRUPAS

4. LEKCIJA ORGANISKO VIELU KLASIFIKĀCIJAS PAMATI UN GALVENĀS FUNKCIONĀLĀS GRUPAS • • Vielu struktūras atveidošanas principi Galvenās funkcionālās grupas Kondensēšanās un hidrolīzes reakcijas Ēteri un esteri Alkāni, alkēni, aromatiskie savienojumi Spirti, cukuri Aminoskābes Nukleotīdi
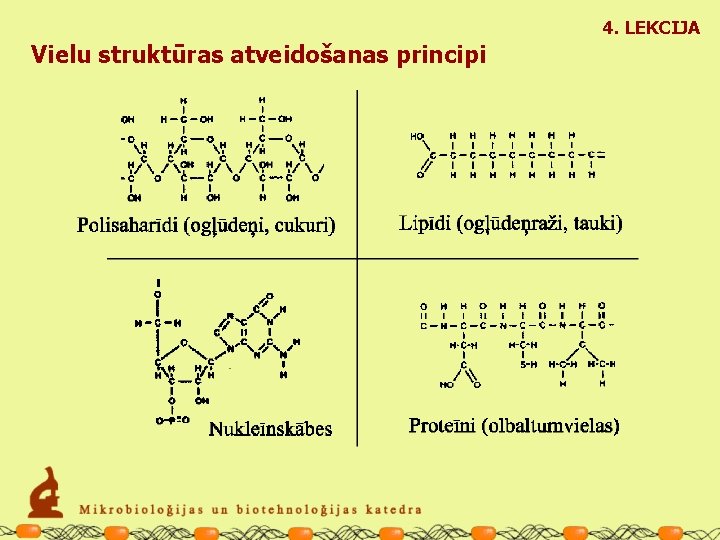
4. LEKCIJA Vielu struktūras atveidošanas principi
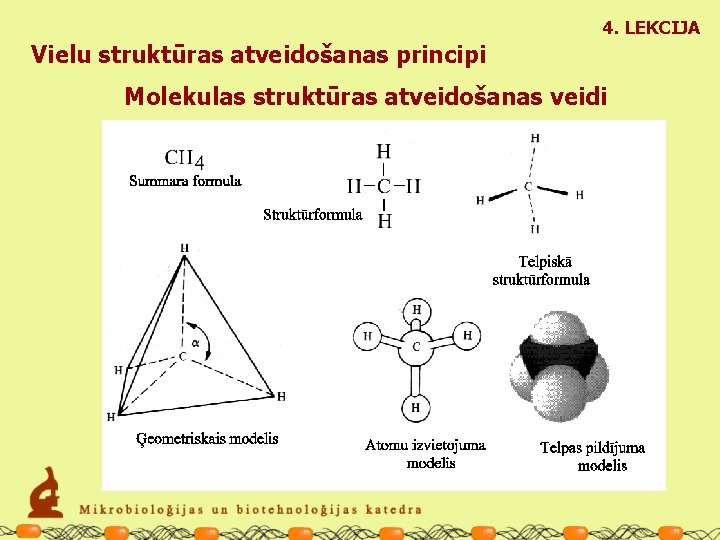
4. LEKCIJA Vielu struktūras atveidošanas principi Molekulas struktūras atveidošanas veidi
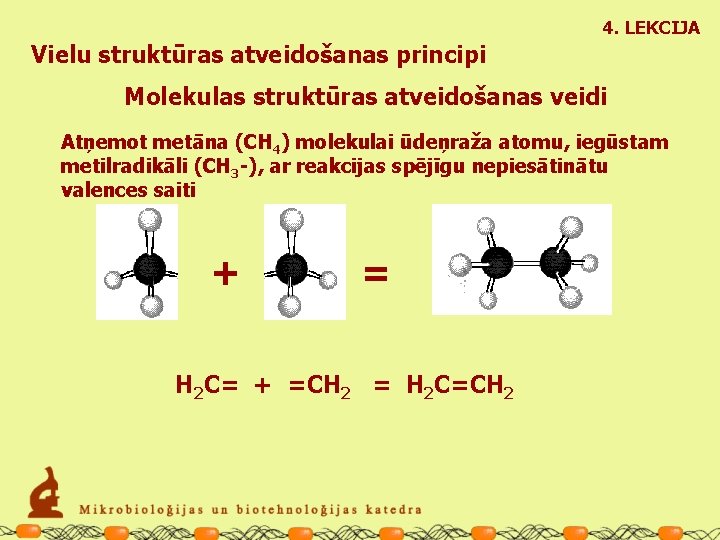
4. LEKCIJA Vielu struktūras atveidošanas principi Molekulas struktūras atveidošanas veidi Atņemot metāna (CH 4) molekulai ūdeņraža atomu, iegūstam metilradikāli (CH 3 -), ar reakcijas spējīgu nepiesātinātu valences saiti + = H 2 C= + =CH 2 = H 2 C=CH 2
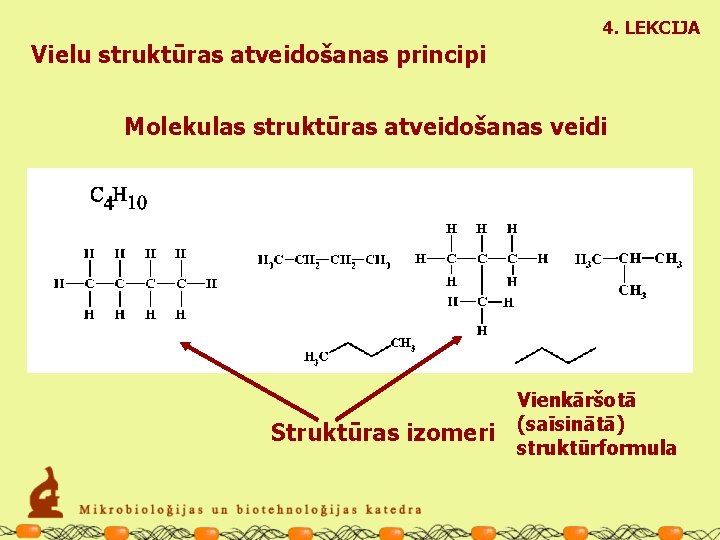
4. LEKCIJA Vielu struktūras atveidošanas principi Molekulas struktūras atveidošanas veidi Struktūras izomeri Vienkāršotā (saīsinātā) struktūrformula
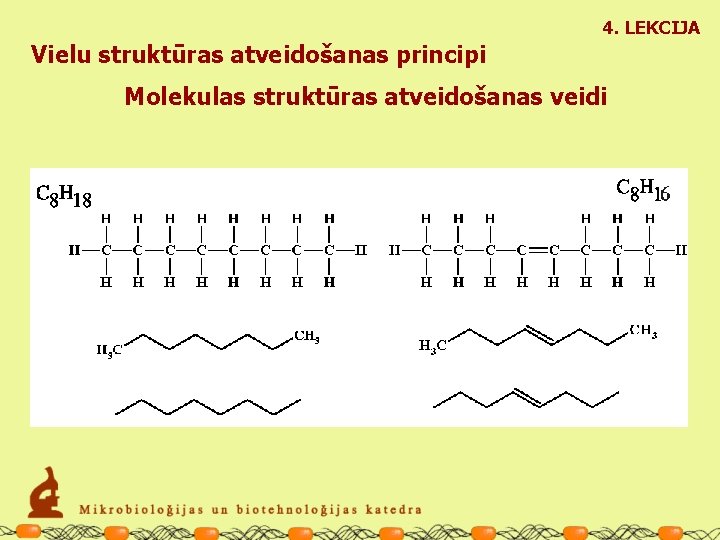
4. LEKCIJA Vielu struktūras atveidošanas principi Molekulas struktūras atveidošanas veidi
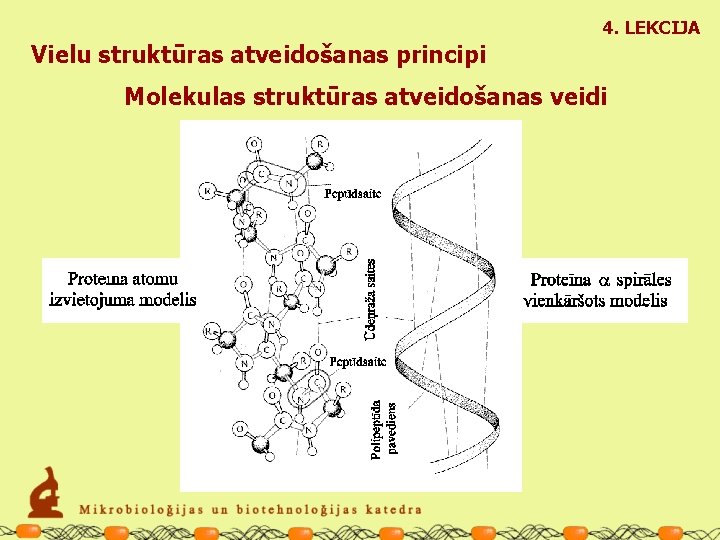
4. LEKCIJA Vielu struktūras atveidošanas principi Molekulas struktūras atveidošanas veidi

4. LEKCIJA Vielu struktūras atveidošanas principi Molekulas struktūras atveidošanas veidi
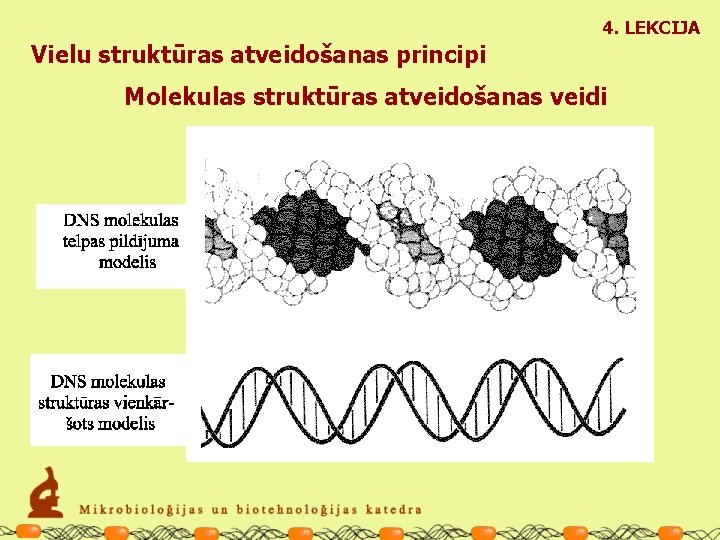
4. LEKCIJA Vielu struktūras atveidošanas principi Molekulas struktūras atveidošanas veidi
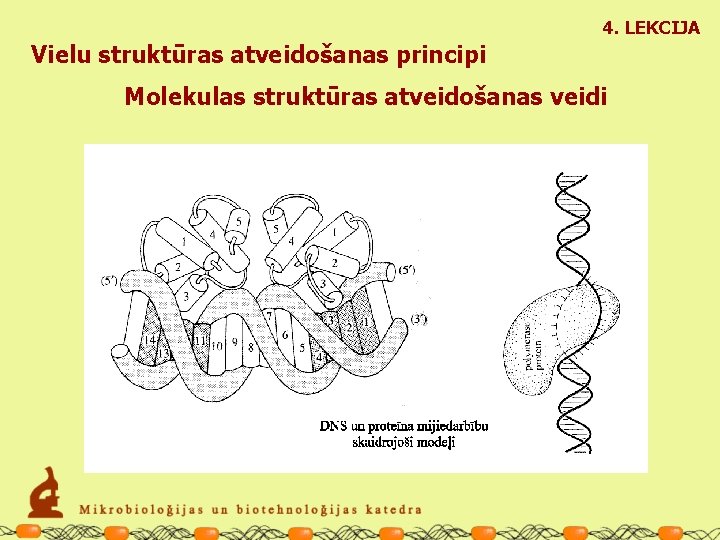
4. LEKCIJA Vielu struktūras atveidošanas principi Molekulas struktūras atveidošanas veidi
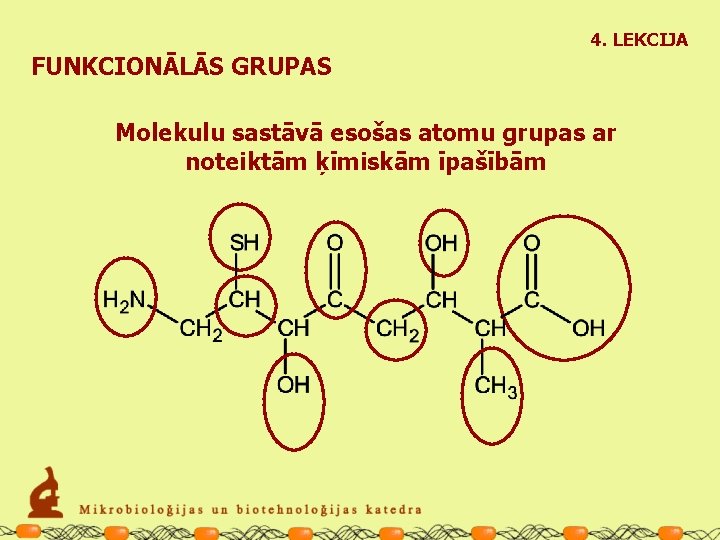
4. LEKCIJA FUNKCIONĀLĀS GRUPAS Molekulu sastāvā esošas atomu grupas ar noteiktām ķīmiskām īpašībām

4. LEKCIJA FUNKCIONĀLĀS GRUPAS Pārējo, ar funkcionālo grupu savienoto molekulas daļu apzīmē ar R-

4. LEKCIJA FUNKCIONĀLĀS GRUPAS Funkcionālo grupu klātbūtni molekulās apzīmē ar specifiskām galotnēm ķīmiskajos nosaukumos
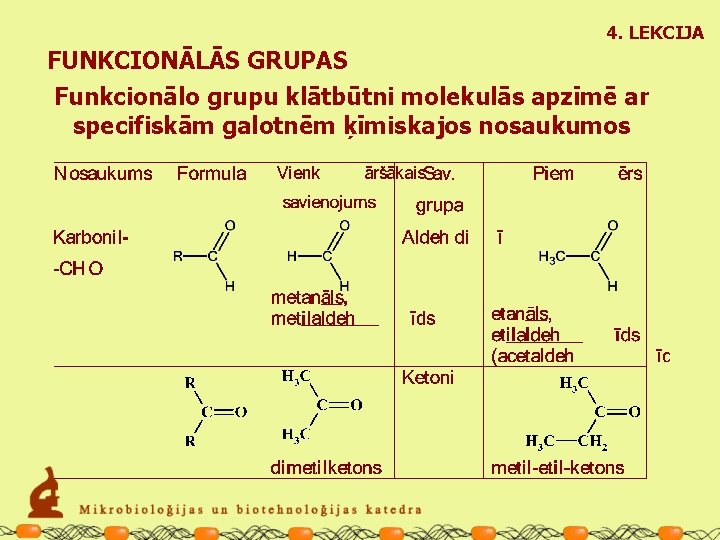
4. LEKCIJA FUNKCIONĀLĀS GRUPAS Funkcionālo grupu klātbūtni molekulās apzīmē ar specifiskām galotnēm ķīmiskajos nosaukumos
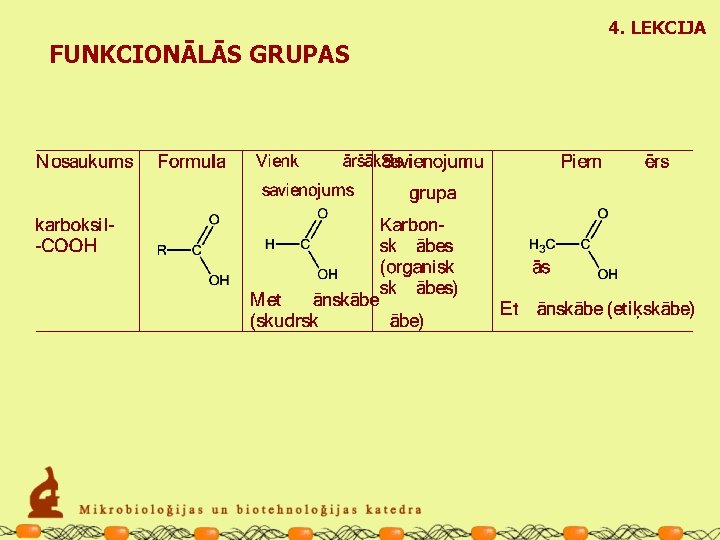
4. LEKCIJA FUNKCIONĀLĀS GRUPAS
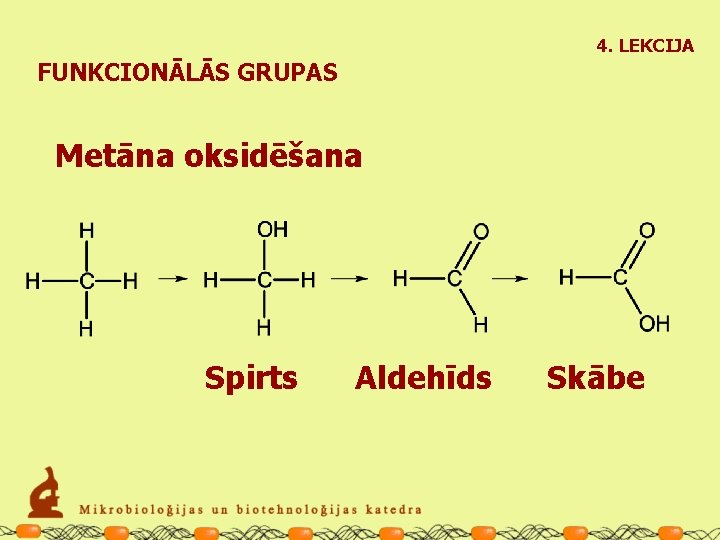
4. LEKCIJA FUNKCIONĀLĀS GRUPAS Metāna oksidēšana Spirts Aldehīds Skābe
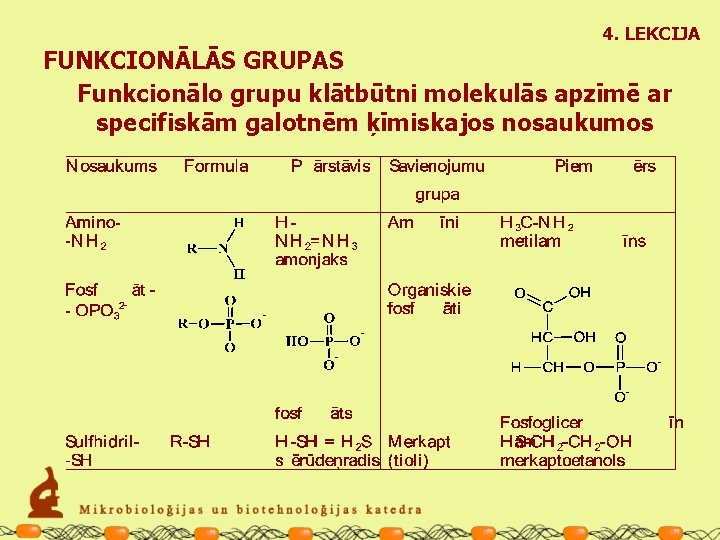
4. LEKCIJA FUNKCIONĀLĀS GRUPAS Funkcionālo grupu klātbūtni molekulās apzīmē ar specifiskām galotnēm ķīmiskajos nosaukumos

4. LEKCIJA FUNKCIONĀLĀS GRUPAS Vienā molekulā var atrasties vairākas vienādas vai dažādas funkcionālās grupas Daudzvērtīgie spirti – polioli. Glicerols (glicerīns) Kompleksās karbonskābes. Pienskābe
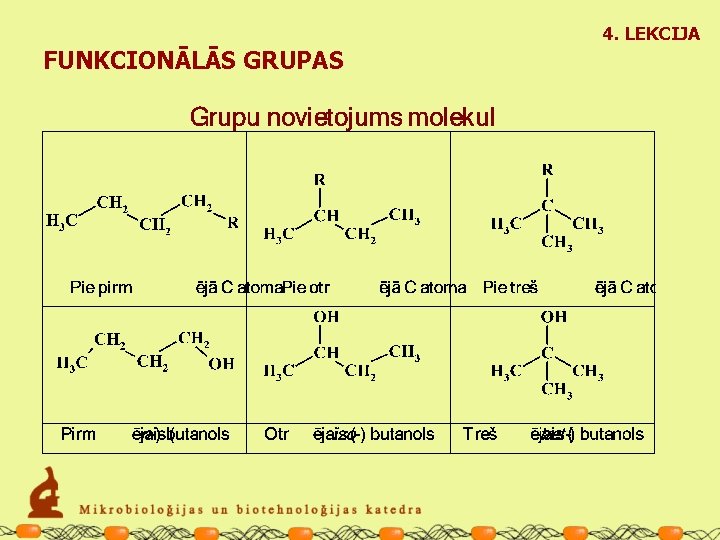
4. LEKCIJA FUNKCIONĀLĀS GRUPAS
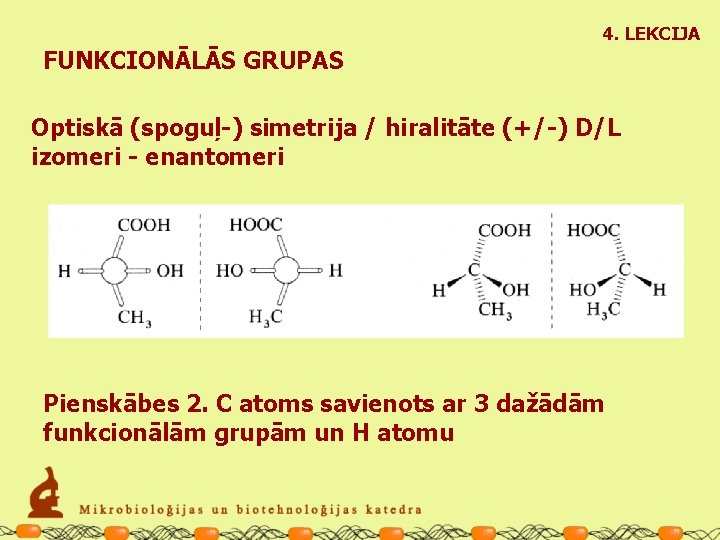
4. LEKCIJA FUNKCIONĀLĀS GRUPAS Optiskā (spoguļ-) simetrija / hiralitāte (+/-) D/L izomeri - enantomeri Pienskābes 2. C atoms savienots ar 3 dažādām funkcionālām grupām un H atomu

4. LEKCIJA Funkcionālās grupas spēj savā starpā reaģēt • Kondensācijas (savienošana, atņemot ūdens molekulu) reakcija. • Hidrolīzes (sašķelšana, pievienojot ūdens molekulu) reakcija. R -OH + OH-R R-O-R +H 2 O R -OH + OH-R

4. LEKCIJA FUNKCIONĀLĀS GRUPAS Kondensējoties divām spirta molekulām, veidojas ēteri
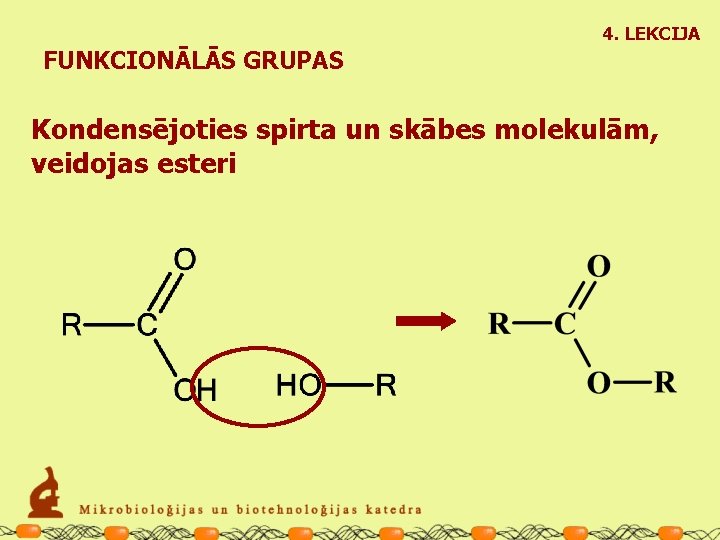
4. LEKCIJA FUNKCIONĀLĀS GRUPAS Kondensējoties spirta un skābes molekulām, veidojas esteri

4. LEKCIJA FUNKCIONĀLĀS GRUPAS Kondensējoties spirta un skābes molekulām, veidojas esteri Etiķskābes metilesteris, metilacetāts

4. LEKCIJA Organisko vielu grupas Alkāni– visvienkāršākās organiskās molekulas, kuras veido tikai C un H atomi, kopējā ķīmiskā formula: Cn. H 2 n+2 Vienkāršākais alkāns: metāns: CH 4

4. LEKCIJA ORGANISKO VIELU GRUPAS Alkānu radikāli veidojas, ja no alkāna molekulas atņem vienu ūdeņraža atomu. Radikālu nosaukumus atvasina ar galotni –il (decil-) no atbilstošo alkānu nosaukumiem.
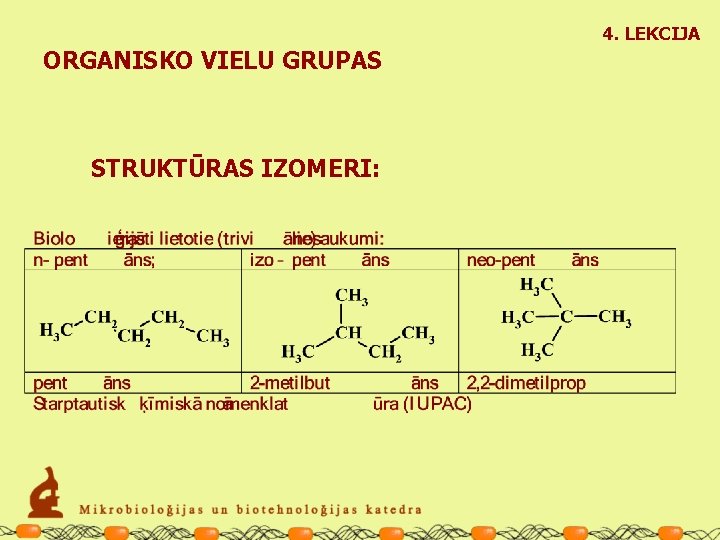
4. LEKCIJA ORGANISKO VIELU GRUPAS STRUKTŪRAS IZOMERI:
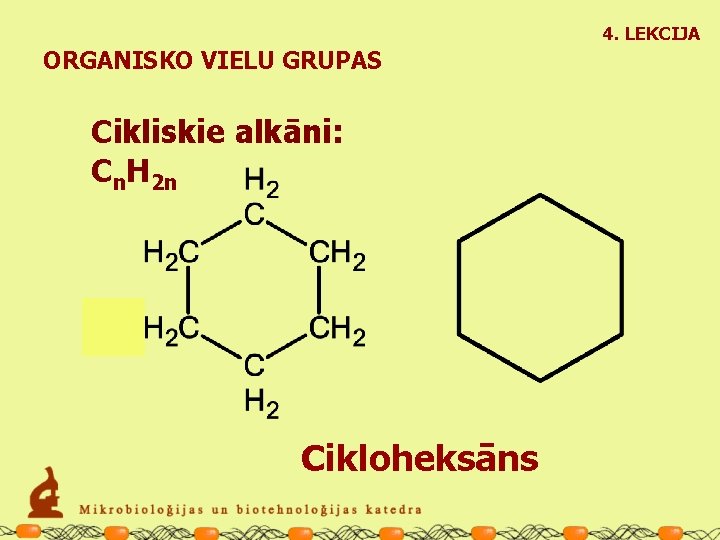
4. LEKCIJA ORGANISKO VIELU GRUPAS Cikliskie alkāni: Cn. H 2 n Cikloheksāns

4. LEKCIJA ORGANISKO VIELU GRUPAS Alkēni Ja no diviem blakusesošiem oglekļa atomiem atņem pa vienam ūdeņraža atomam (dehidrēšana), veidojas kovalenta dubultsaite. Ogļūdeņražus, kas satur vienu vairākas dubultsaites sauc par alkēniem.
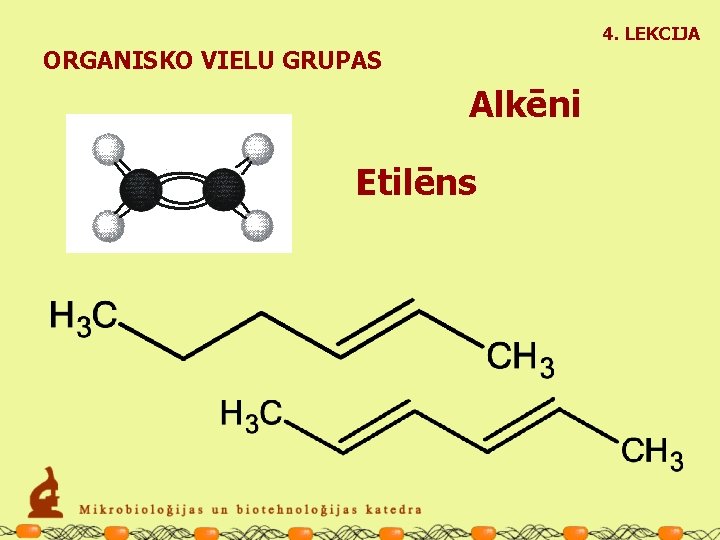
4. LEKCIJA ORGANISKO VIELU GRUPAS Alkēni Etilēns
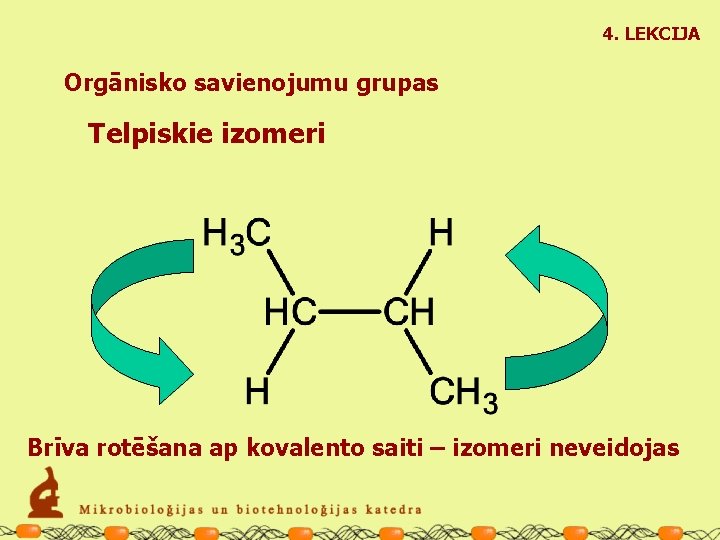
4. LEKCIJA Orgānisko savienojumu grupas Telpiskie izomeri Brīva rotēšana ap kovalento saiti – izomeri neveidojas
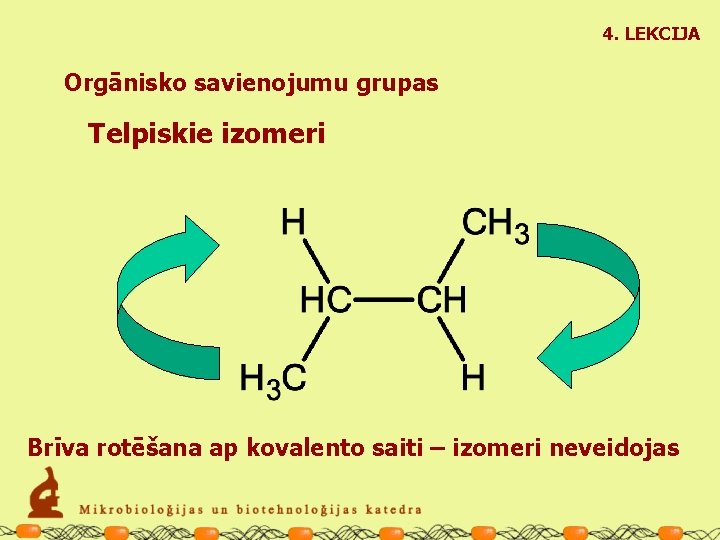
4. LEKCIJA Orgānisko savienojumu grupas Telpiskie izomeri Brīva rotēšana ap kovalento saiti – izomeri neveidojas
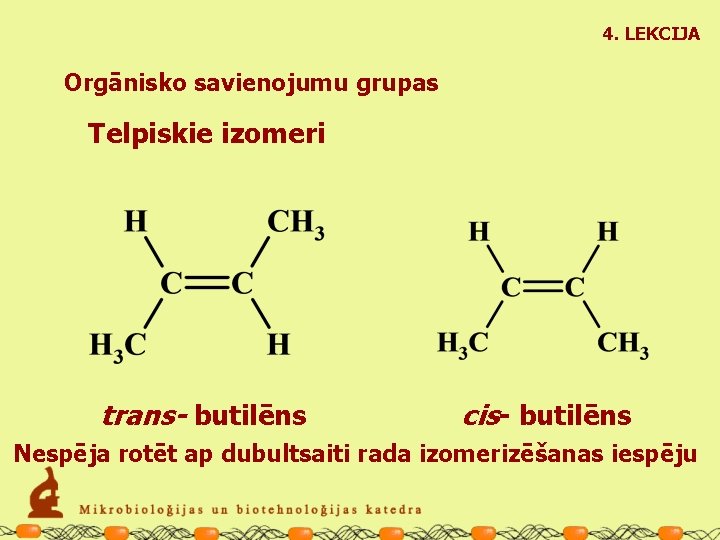
4. LEKCIJA Orgānisko savienojumu grupas Telpiskie izomeri trans- butilēns cis- butilēns Nespēja rotēt ap dubultsaiti rada izomerizēšanas iespēju

ORGANISKO VIELU GRUPAS 4. LEKCIJA Aromātiskie savienojumi (arēni) Benzola gredzenā konjugētās (saistītās) dubultsaites nav cieši saistītas pie viena vai otra oglekļa atoma. Tās pārviertojas (fluktuē) molekulas sastāvā.

4. LEKCIJA ORGANISKO VIELU GRUPAS Alkīni Ja no diviem blakusesošiem oglekļa atomiem atņem pa diviem ūdeņraža atomiem (dehidrēšana), veidojas trīskāršā kovalentā saite. Ogļūdeņražus, kas satur vienu vairākas trīskāršās saites sauc par alkīniem. . To nosaukumus atvasina no atbistošo alkānu nosaukumiem, aizstājot galotni -āns ar galotni -īns. Lieto arī triviālos nosaukumus, piem. : etīns = acetilēns

4. LEKCIJA Organisko vielu grupas OGĻŪDEŅI (CUKURI) Vispārīgā ķīmiskā formula (CH 2 O) = ogļhidrāti Vienkāršas molekulas – monosaharīdi: 3 – 6 C atomu ķēde + viena karbonil- (aldehīd-) un vairākas hidroksil- funkcionālās grupas. Kondensācijas reakcijās veidojas di-, tri- un polisaharīdi.
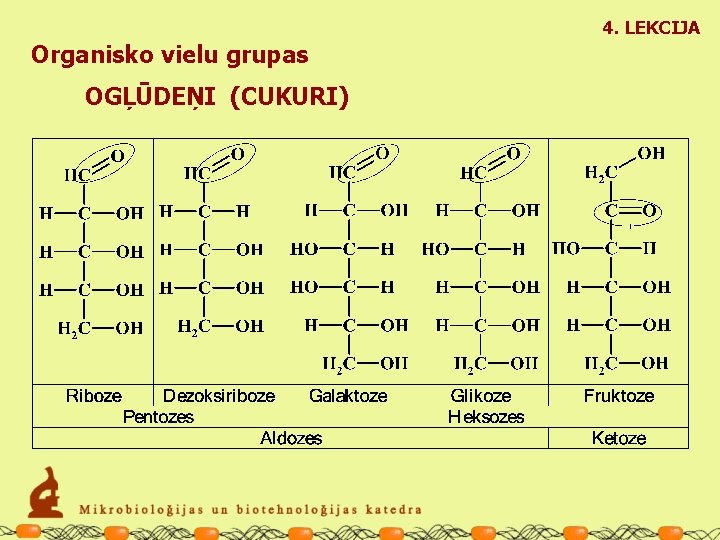
4. LEKCIJA Organisko vielu grupas OGĻŪDEŅI (CUKURI)
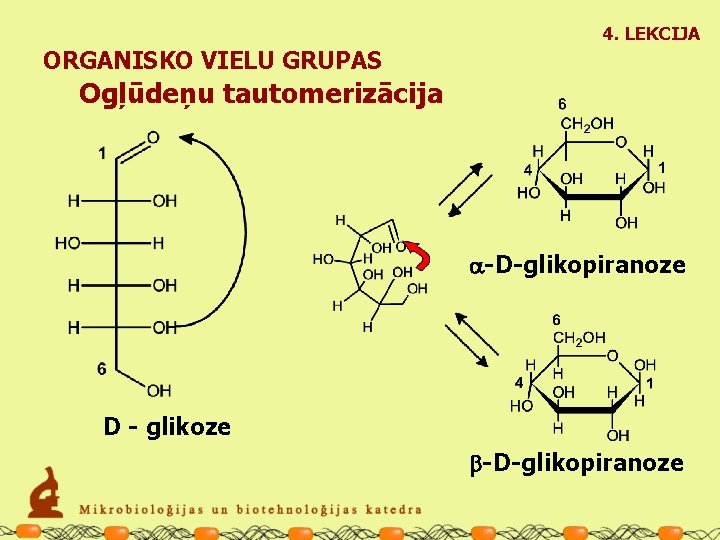
4. LEKCIJA ORGANISKO VIELU GRUPAS Ogļūdeņu tautomerizācija a-D-glikopiranoze D - glikoze b-D-glikopiranoze
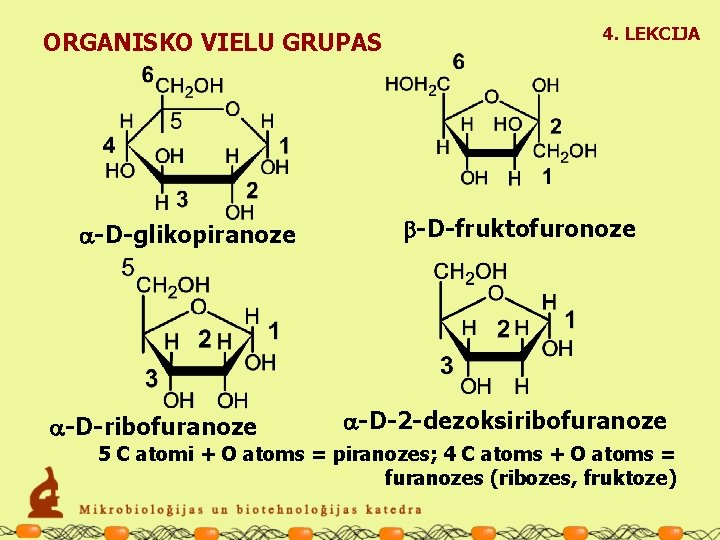
ORGANISKO VIELU GRUPAS a-D-glikopiranoze a-D-ribofuranoze 4. LEKCIJA b-D-fruktofuronoze a-D-2 -dezoksiribofuranoze 5 C atomi + O atoms = piranozes; 4 C atoms + O atoms = furanozes (ribozes, fruktoze)
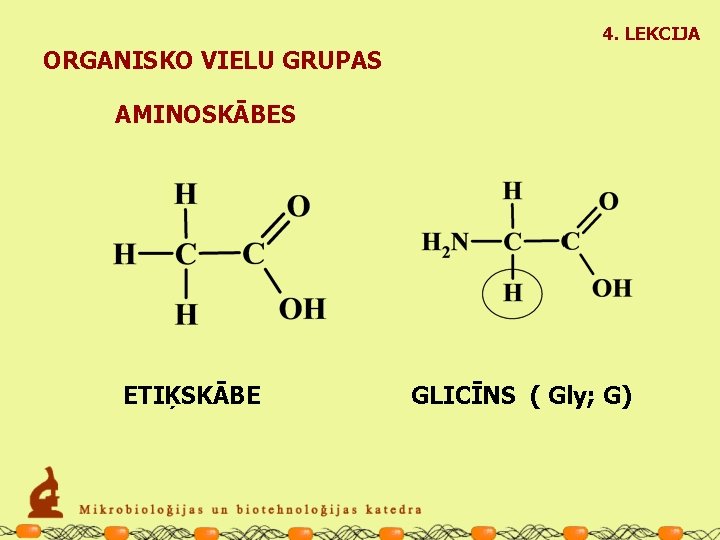
4. LEKCIJA ORGANISKO VIELU GRUPAS AMINOSKĀBES ETIĶSKĀBE GLICĪNS ( Gly; G)
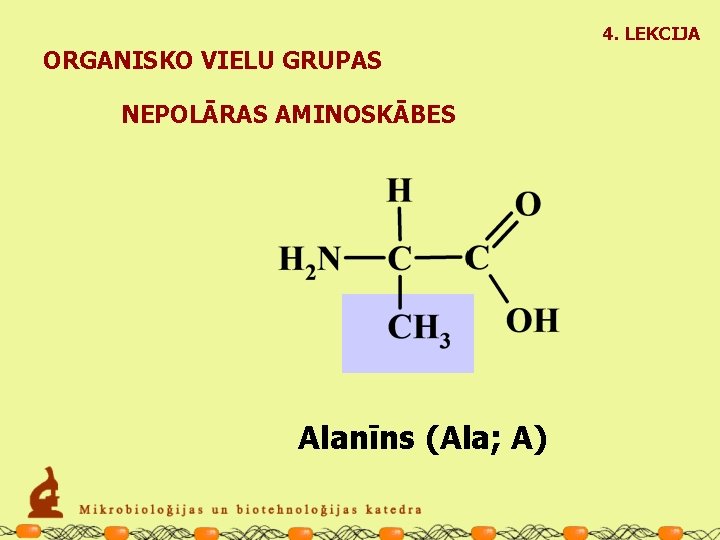
4. LEKCIJA ORGANISKO VIELU GRUPAS NEPOLĀRAS AMINOSKĀBES Alanīns (Ala; A)
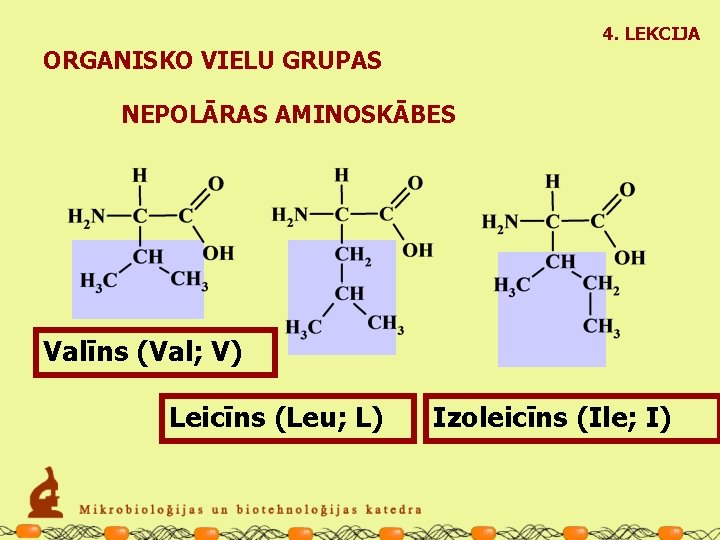
4. LEKCIJA ORGANISKO VIELU GRUPAS NEPOLĀRAS AMINOSKĀBES Valīns (Val; V) Leicīns (Leu; L) Izoleicīns (Ile; I)
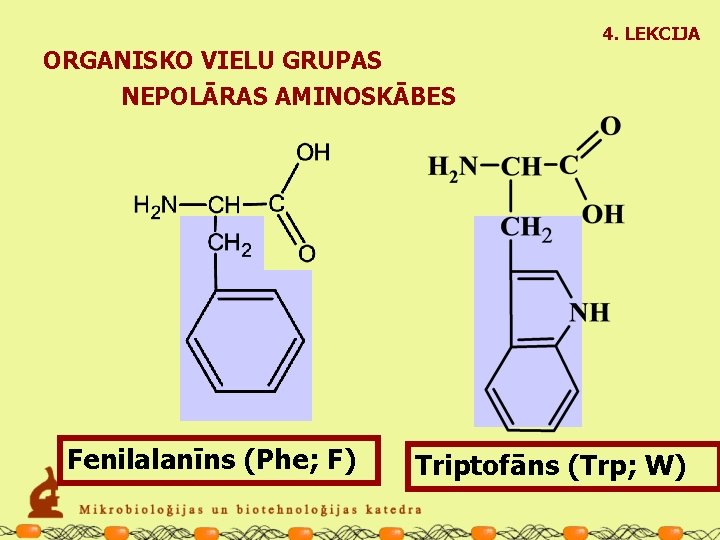
4. LEKCIJA ORGANISKO VIELU GRUPAS NEPOLĀRAS AMINOSKĀBES Fenilalanīns (Phe; F) Triptofāns (Trp; W)
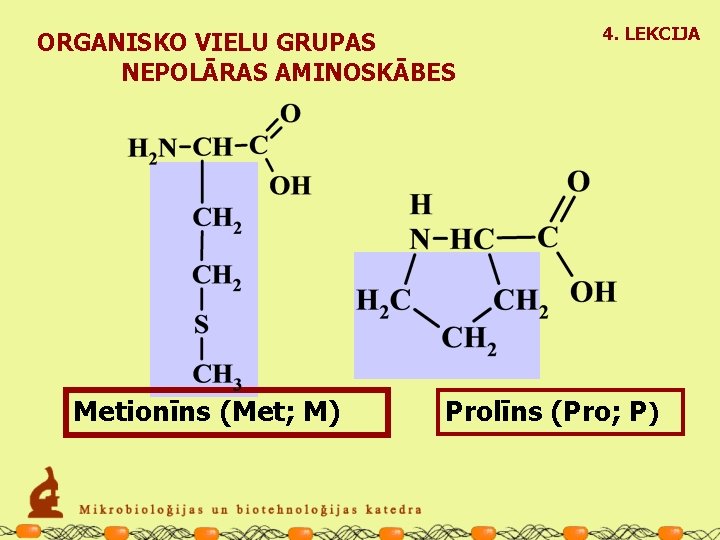
ORGANISKO VIELU GRUPAS NEPOLĀRAS AMINOSKĀBES Metionīns (Met; M) 4. LEKCIJA Prolīns (Pro; P)
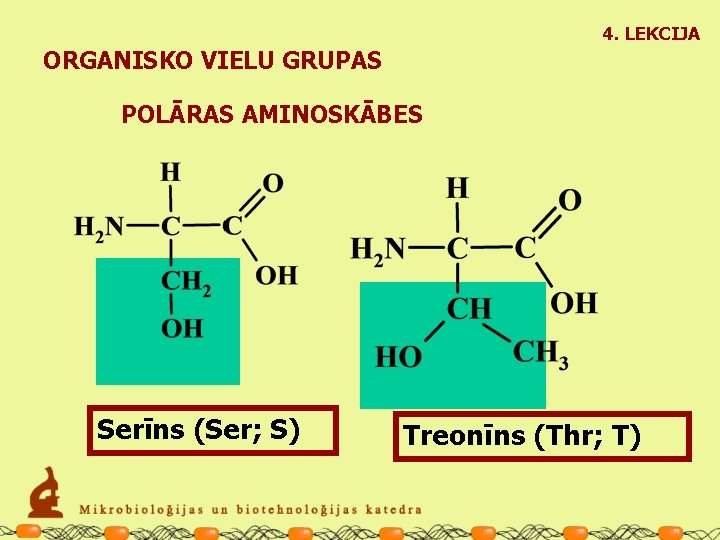
4. LEKCIJA ORGANISKO VIELU GRUPAS POLĀRAS AMINOSKĀBES Serīns (Ser; S) Treonīns (Thr; T)
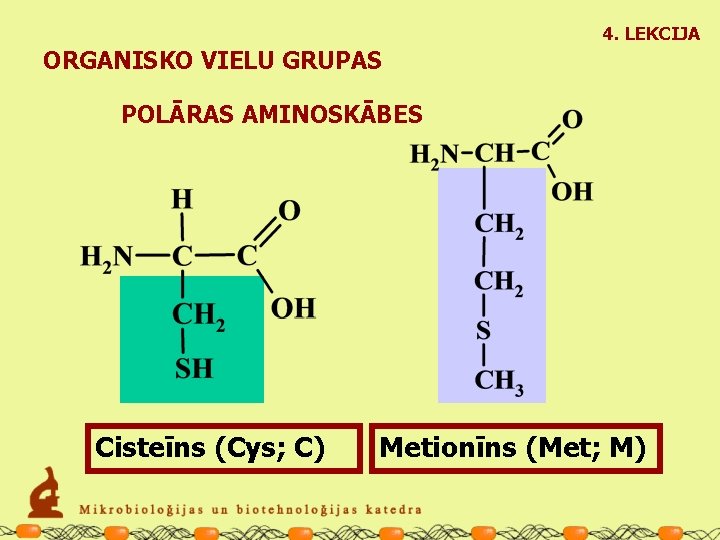
4. LEKCIJA ORGANISKO VIELU GRUPAS POLĀRAS AMINOSKĀBES Cisteīns (Cys; C) Metionīns (Met; M)
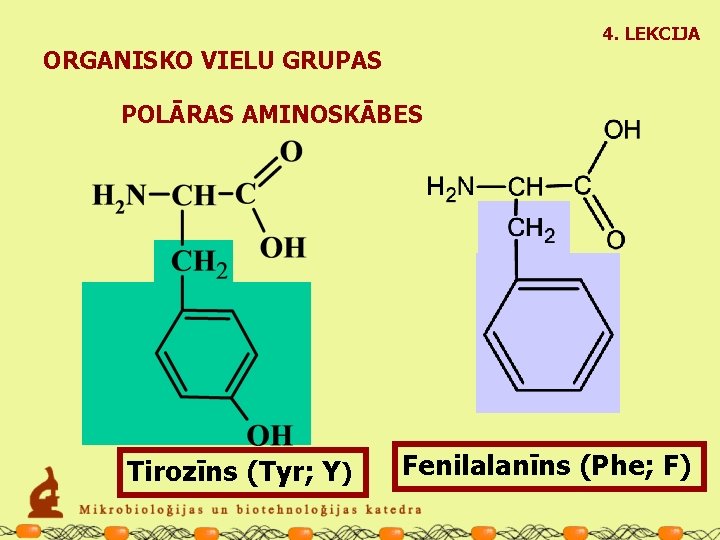
4. LEKCIJA ORGANISKO VIELU GRUPAS POLĀRAS AMINOSKĀBES Tirozīns (Tyr; Y) Fenilalanīns (Phe; F)
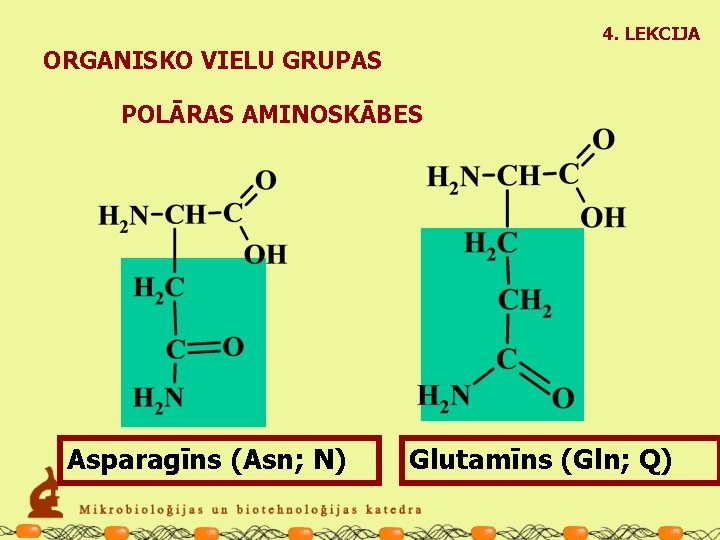
4. LEKCIJA ORGANISKO VIELU GRUPAS POLĀRAS AMINOSKĀBES Asparagīns (Asn; N) Glutamīns (Gln; Q)
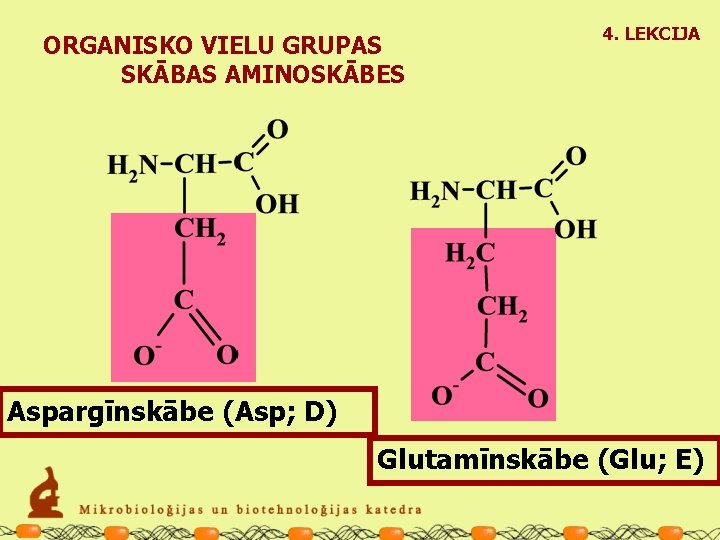
ORGANISKO VIELU GRUPAS SKĀBAS AMINOSKĀBES 4. LEKCIJA Aspargīnskābe (Asp; D) Glutamīnskābe (Glu; E)
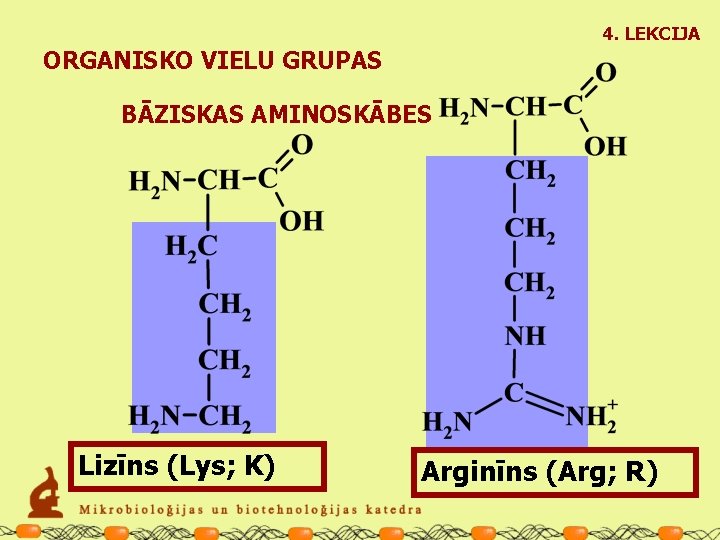
4. LEKCIJA ORGANISKO VIELU GRUPAS BĀZISKAS AMINOSKĀBES Lizīns (Lys; K) Arginīns (Arg; R)
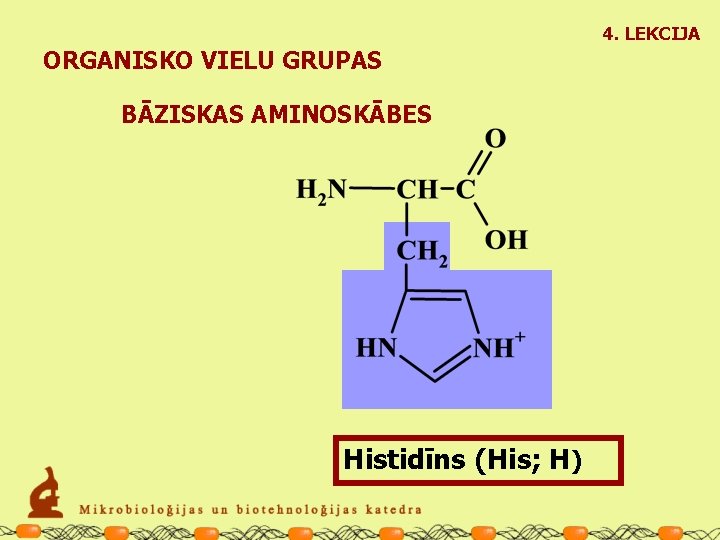
4. LEKCIJA ORGANISKO VIELU GRUPAS BĀZISKAS AMINOSKĀBES Histidīns (His; H)
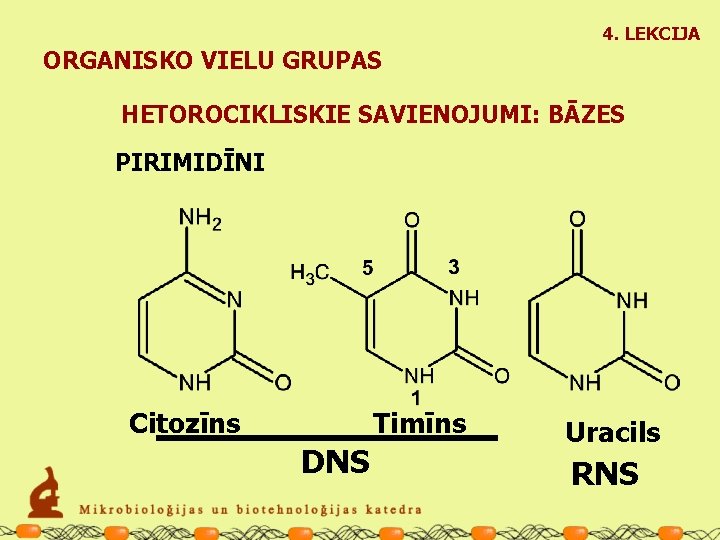
4. LEKCIJA ORGANISKO VIELU GRUPAS HETOROCIKLISKIE SAVIENOJUMI: BĀZES PIRIMIDĪNI Citozīns Timīns DNS Uracils RNS
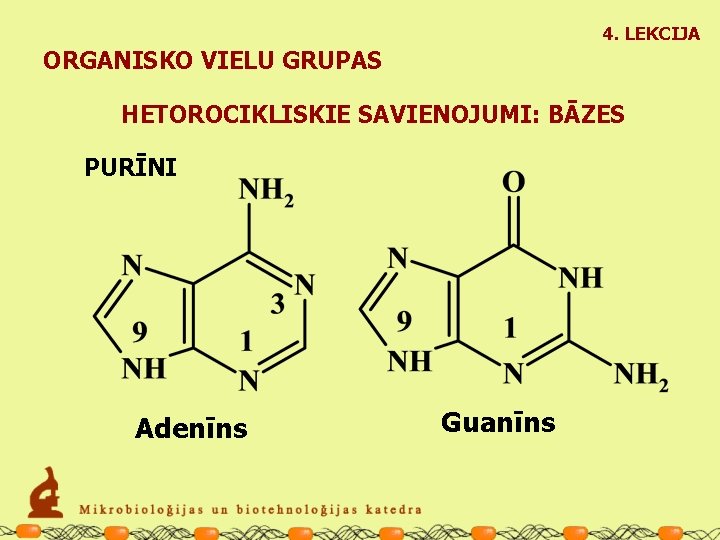
4. LEKCIJA ORGANISKO VIELU GRUPAS HETOROCIKLISKIE SAVIENOJUMI: BĀZES PURĪNI Adenīns Guanīns
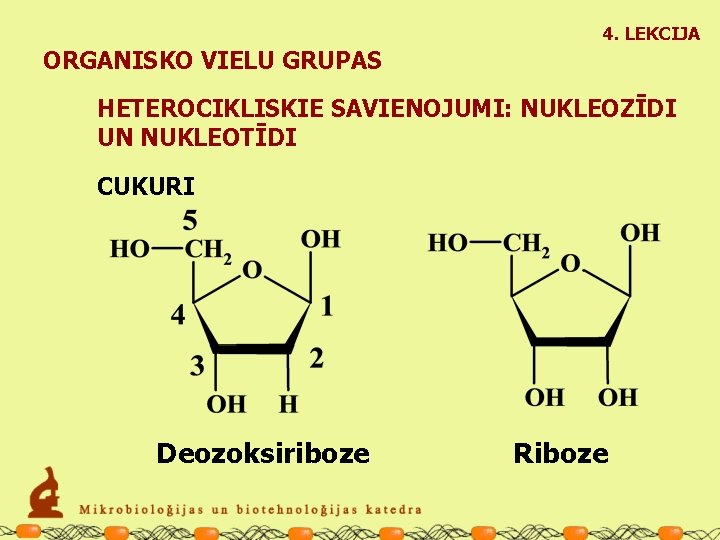
4. LEKCIJA ORGANISKO VIELU GRUPAS HETEROCIKLISKIE SAVIENOJUMI: NUKLEOZĪDI UN NUKLEOTĪDI CUKURI Deozoksiriboze Riboze

4. LEKCIJA ORGANISKO VIELU GRUPAS HETEROCIKLISKIE SAVIENOJUMI: NUKLEOZĪDI UN NUKLEOTĪDI FOSFĀTS FOSFORSKĀBE
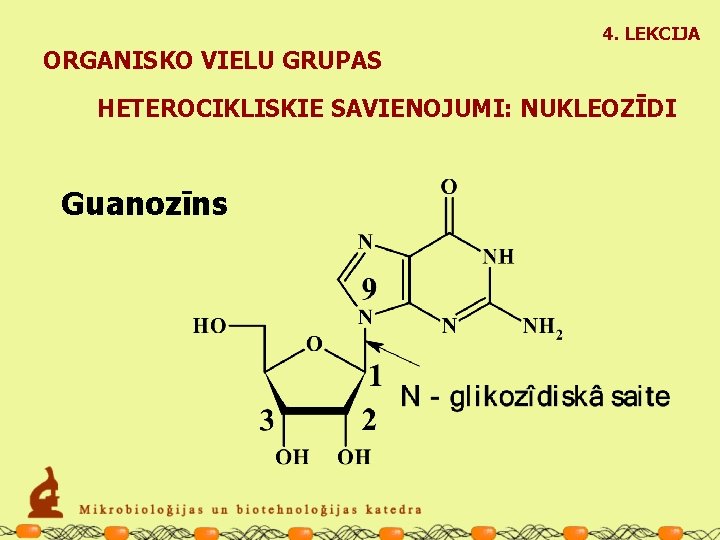
4. LEKCIJA ORGANISKO VIELU GRUPAS HETEROCIKLISKIE SAVIENOJUMI: NUKLEOZĪDI Guanozīns
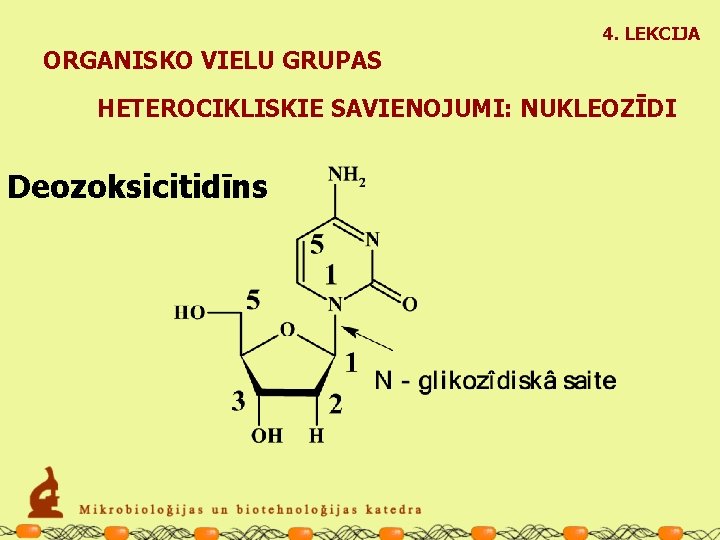
4. LEKCIJA ORGANISKO VIELU GRUPAS HETEROCIKLISKIE SAVIENOJUMI: NUKLEOZĪDI Deozoksicitidīns
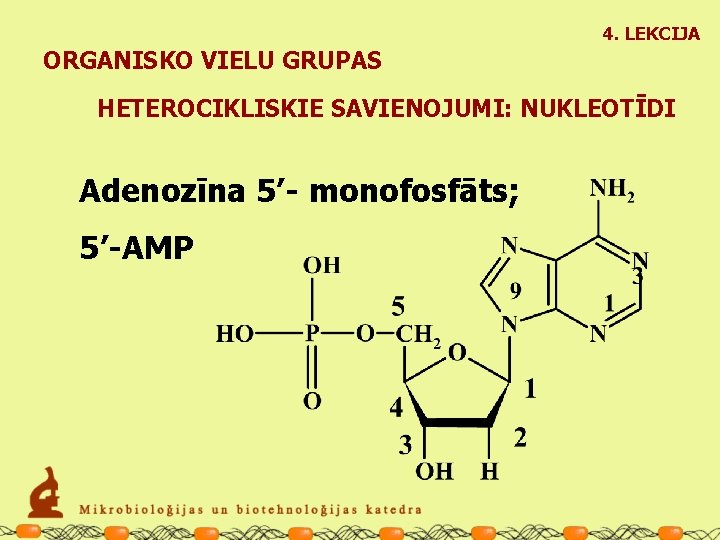
4. LEKCIJA ORGANISKO VIELU GRUPAS HETEROCIKLISKIE SAVIENOJUMI: NUKLEOTĪDI Adenozīna 5’- monofosfāts; 5’-AMP
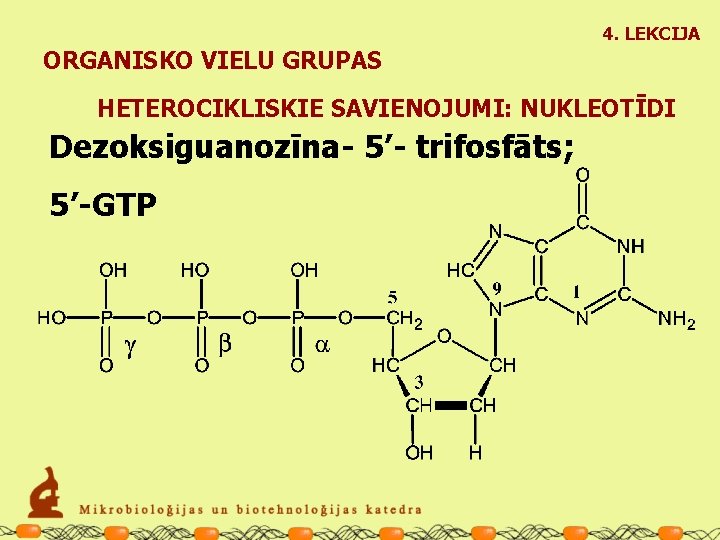
4. LEKCIJA ORGANISKO VIELU GRUPAS HETEROCIKLISKIE SAVIENOJUMI: NUKLEOTĪDI Dezoksiguanozīna- 5’- trifosfāts; 5’-GTP
- Slides: 60