IEVADS NAS BIOLOIJ I DZVBAS MIJA MISKS SAITES

IEVADS ŠŪNAS BIOLOĢIJĀ I DZĪVĪBAS ĶĪMIJA ĶĪMISKĀS SAITES, STARPMOLEKULU MIJIEDARBĪBAS. ŪDENS ĪPAŠĪBAS, p. H

3. LEKCIJA ĶĪMISKĀS SAITES, STARPMOLEKULU MIJIEDARBĪBAS. ŪDENS ĪPAŠĪBAS, BUFERŠĶĪDUMI • • Kovalentā saite Van der Valsa spēki Hidrofobās mijiedarbības Ūdeņraža saite Bioloģiski nozīmīgās ūdens īpašības p. H, skābes un sārmi Buferšķīdumi

3. LEKCIJA Ķīmiskā saite Daļiņas, kuras veidojas atomiem atdodot vai piesaistot elektronus sauc par JONIEM.
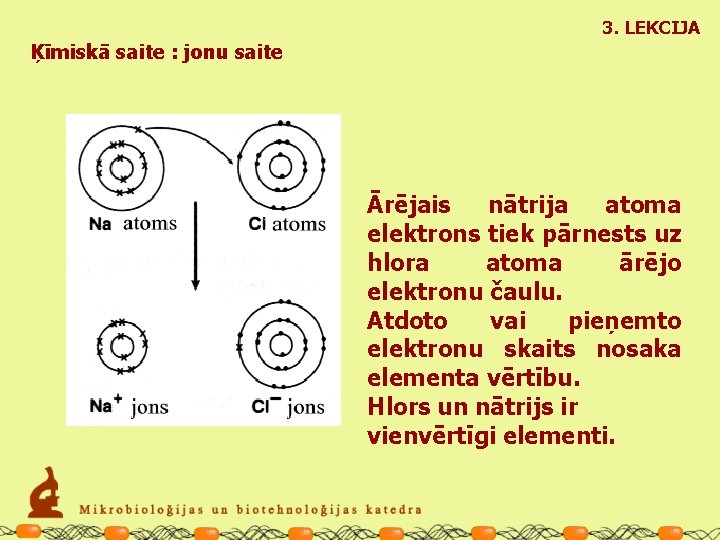
3. LEKCIJA Ķīmiskā saite : jonu saite Ārējais nātrija atoma elektrons tiek pārnests uz hlora atoma ārējo elektronu čaulu. Atdoto vai pieņemto elektronu skaits nosaka elementa vērtību. Hlors un nātrijs ir vienvērtīgi elementi.

3. LEKCIJA Ķīmiskā saite : jonu saite Jonizēt var ne tikai atoms, bet arī funkcionālās grupas, ja tām pievieno vai atņem ūdeņraža jonus (protonus). Protona piesaistīšana - reducēšanās; protona atdošana - oksidēšanās

3. LEKCIJA Ķīmiskā saite : jonu saite Jonu saite piedalās proteīna telpiskās struktūras veidošanā
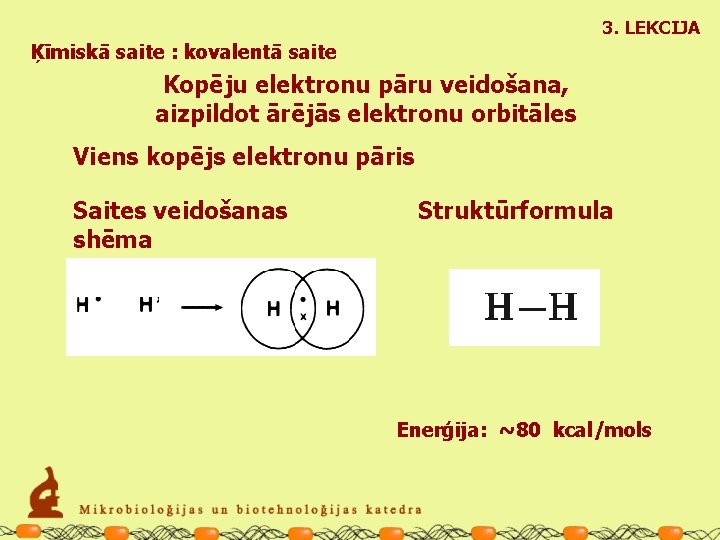
3. LEKCIJA Ķīmiskā saite : kovalentā saite Kopēju elektronu pāru veidošana, aizpildot ārējās elektronu orbitāles Viens kopējs elektronu pāris Saites veidošanas shēma Struktūrformula Enerģija: ~80 kcal/mols

3. LEKCIJA Ķīmiskā saite : kovalentā saite Kopēju elektronu pāru veidošana, aizpildot ārējās elektronu orbitāles Divi kopēji elektronu pāri Saites veidošanas shēma Struktūrformula Enerģija: ~150 kcal/mols
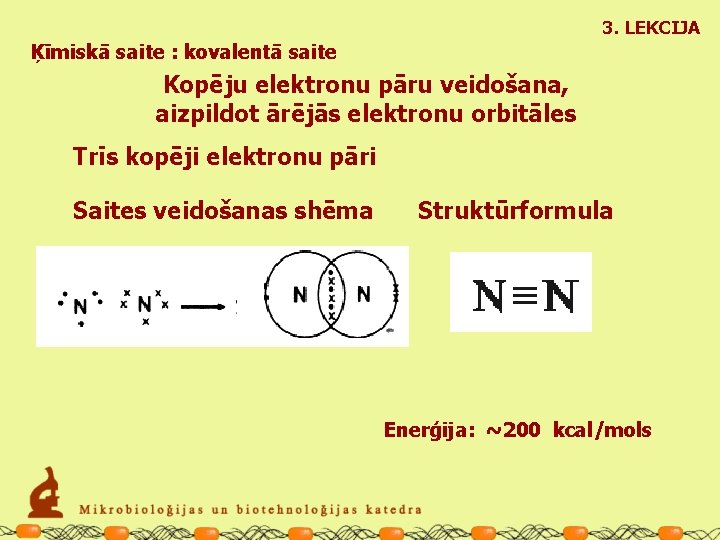
3. LEKCIJA Ķīmiskā saite : kovalentā saite Kopēju elektronu pāru veidošana, aizpildot ārējās elektronu orbitāles Trīs kopēji elektronu pāri Saites veidošanas shēma Struktūrformula Enerģija: ~200 kcal/mols
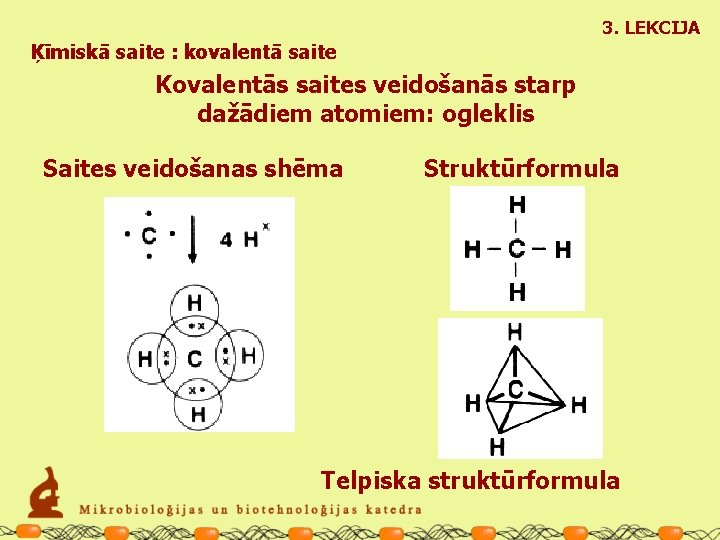
3. LEKCIJA Ķīmiskā saite : kovalentā saite Kovalentās saites veidošanās starp dažādiem atomiem: ogleklis Saites veidošanas shēma Struktūrformula Telpiska struktūrformula
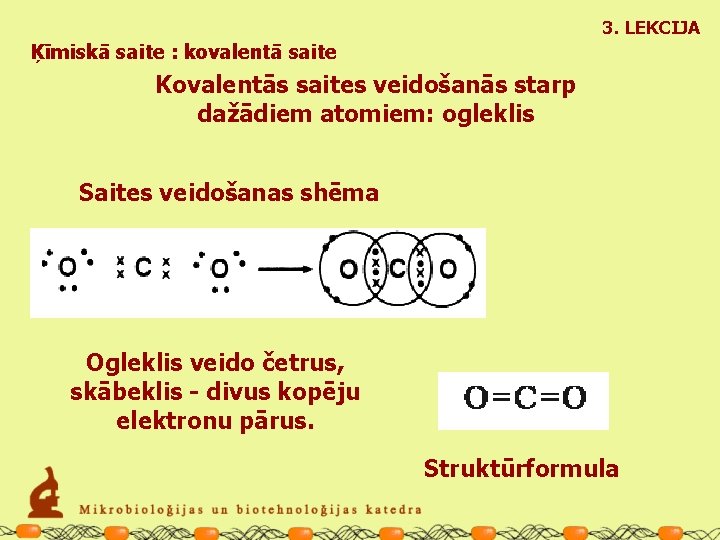
3. LEKCIJA Ķīmiskā saite : kovalentā saite Kovalentās saites veidošanās starp dažādiem atomiem: ogleklis Saites veidošanas shēma Ogleklis veido četrus, skābeklis - divus kopēju elektronu pārus. Struktūrformula
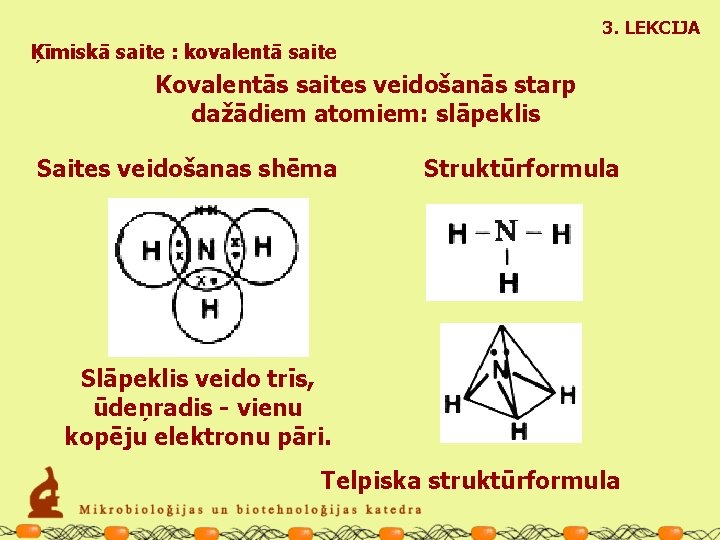
3. LEKCIJA Ķīmiskā saite : kovalentā saite Kovalentās saites veidošanās starp dažādiem atomiem: slāpeklis Saites veidošanas shēma Struktūrformula Slāpeklis veido trīs, ūdeņradis - vienu kopēju elektronu pāri. Telpiska struktūrformula

3. LEKCIJA Ķīmiskā saite : kovalentā saite Kovalentās saites veido organisko savienojumu struktūru un nodrošina tās stabilitāti

2. LEKCIJA Ķīmiskās saites Jonu saiti veidojot, atomu ķīmisko vērtību (valenci) nosaka atdoto vai pārņemto elektronu skaits. Kovalento saiti veidojot, atomu ķīmisko vērtību (valenci) nosaka kopējo elektronu pāru skaits. Bioloģisko makromolekulu struktūras pamatu veido kovalentās saites.

3. LEKCIJA Starpmolekulu mijiedarbības spēki Mijiedarbības starp molekulām stabilizē elektrisko lādiņu sadalījumu.

3. LEKCIJA Starpmolekulu mijiedarbības spēki Van der Valsa spēki Elektronu kustība atomos vai molekulās rada pārejošu, nevienmērīgu elektriskā lādiņa izvietojumu. Atoms vai molekula tiek polarizēti, veidojas nestabils dipols.

3. LEKCIJA Starpmolekulu mijiedarbības spēki Van der Valsa spēki Viena atoma vai molekulas īslaicīgi negatīvā daļa izraisa pretējas zīmes lādiņa veidošanos tuvumā esošajās daļiņās. Pretēji orientētie dipoli viens otru stabilizē.
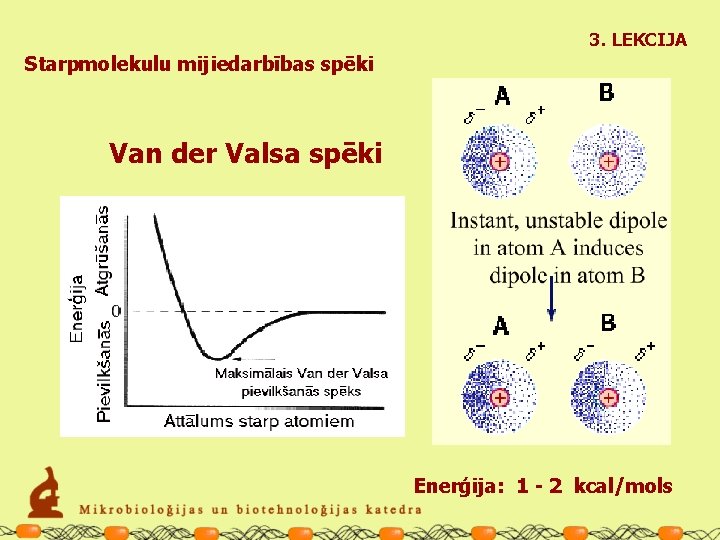
3. LEKCIJA Starpmolekulu mijiedarbības spēki Van der Valsa spēki Enerģija: 1 - 2 kcal/mols

3. LEKCIJA Starpmolekulu mijiedarbības spēki Van der Valsa spēki Lielās molekulās (polimeros) šādu mijiedarbību spēks var būt ļoti liels. Bioloģisko makromolekulu struktūru veidošanā Van der Valsa spēkiem ir būtiska loma. Enerģija: 1 - 2 kcal/mols
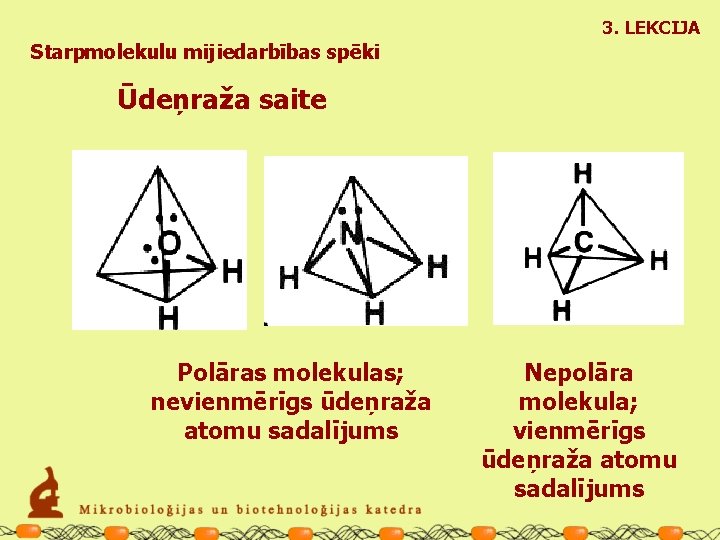
3. LEKCIJA Starpmolekulu mijiedarbības spēki Ūdeņraža saite Polāras molekulas; nevienmērīgs ūdeņraža atomu sadalījums Nepolāra molekula; vienmērīgs ūdeņraža atomu sadalījums
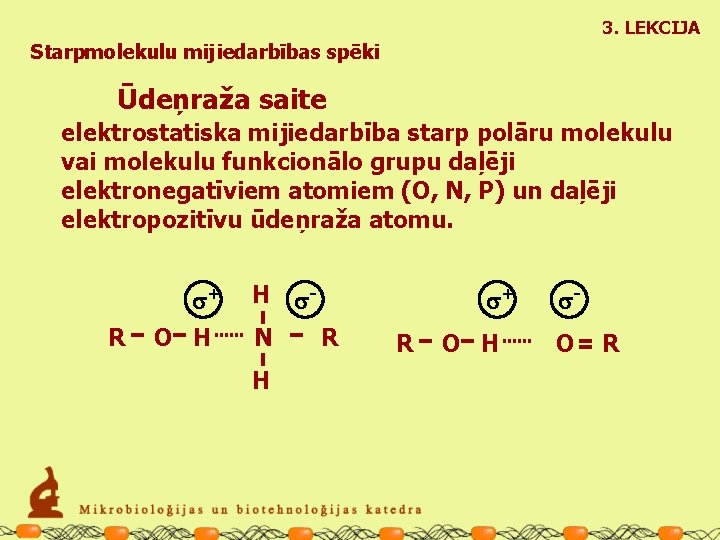
3. LEKCIJA Starpmolekulu mijiedarbības spēki Ūdeņraža saite elektrostatiska mijiedarbība starp polāru molekulu vai molekulu funkcionālo grupu daļēji elektronegatīviem atomiem (O, N, P) un daļēji elektropozitīvu ūdeņraža atomu. s+ R O H H s. N H s+ R R O H s. O R
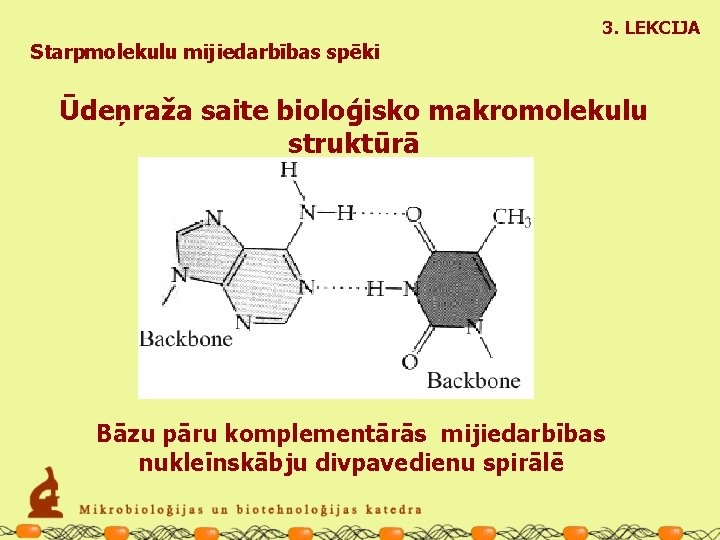
3. LEKCIJA Starpmolekulu mijiedarbības spēki Ūdeņraža saite bioloģisko makromolekulu struktūrā Bāzu pāru komplementārās mijiedarbības nukleīnskābju divpavedienu spirālē
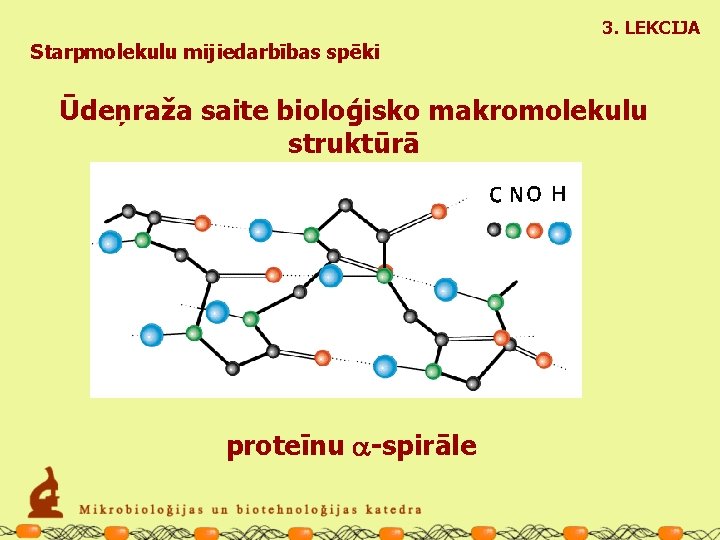
3. LEKCIJA Starpmolekulu mijiedarbības spēki Ūdeņraža saite bioloģisko makromolekulu struktūrā proteīnu a-spirāle
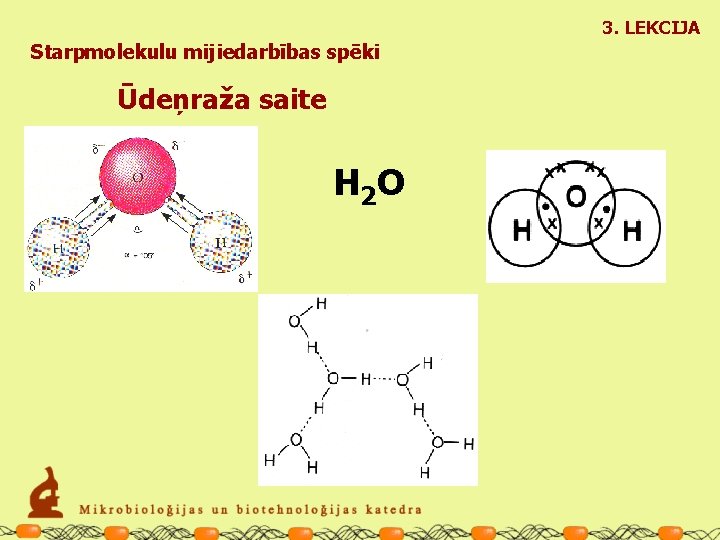
3. LEKCIJA Starpmolekulu mijiedarbības spēki Ūdeņraža saite H 2 O
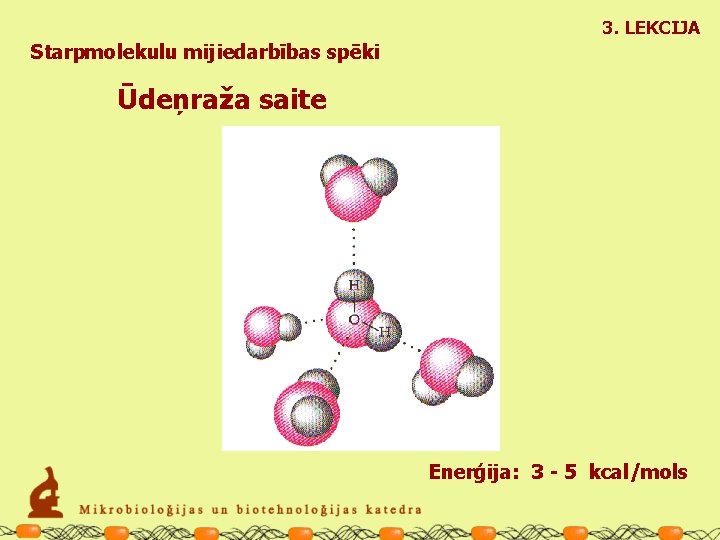
3. LEKCIJA Starpmolekulu mijiedarbības spēki Ūdeņraža saite Enerģija: 3 - 5 kcal/mols

3. LEKCIJA Bioloģiski nozīmīgās ūdens īpašības Virsmas spraigums

3. LEKCIJA Bioloģiski nozīmīgās ūdens īpašības Kohēzija

3. LEKCIJA Bioloģiski nozīmīgās ūdens īpašības Siltumietilpība, dzišana iztvaikojot

3. LEKCIJA Bioloģiski nozīmīgās ūdens īpašības Siltumietilpība, dzišana iztvaikojot

3. LEKCIJA Bioloģiski nozīmīgās ūdens īpašības Siltumietilpība, dzišana iztvaikojot

3. LEKCIJA Bioloģiski nozīmīgās ūdens īpašības Blīvuma samazināšanās sasalstot

3. LEKCIJA Bioloģiski nozīmīgās ūdens īpašības Blīvuma samazināšanās sasalstot

3. LEKCIJA Bioloģiski nozīmīgās ūdens īpašības Spēja šķīdināt polārus savienojumus

3. LEKCIJA Bioloģiski nozīmīgās ūdens īpašības Spēja šķīdināt polārus savienojumus Polāri savienojumi ir hidrofīli Šķīdumu koncentrāciju mēra molos uz litru

Bioloģiski nozīmīgās ūdens īpašības 3. LEKCIJA Šķīdumu koncentrāciju mēra molos litrā Cik molārs ir ūdens ?

3. LEKCIJA Bioloģiski nozīmīgās ūdens īpašības Atgrūšanās no nepolāru savienojumu virsmas Nepolāri savienojumi ir hidrofobi

3. LEKCIJA Starpmolekulu mijiedarbības spēki Hidrofobās mijiedarbības Daudzām molekulas ir ūdenī nešķīstošas (ogļūdeņraži, tauki) vai satur nepolāras, hidrofobas daļas (dažas aminoskābes). Šādas molekulas ūdens vidē cenšas savākties vienkopus, samazinot pret ūdeni atklātās virsmas laukumu (eļlas piliens ūdenī). Mazākais virsmas laukums pret ūdeni nodrošina hidrofobām molekulām enerģētiski izdevīgāko stāvokli.

3. LEKCIJA Starpmolekulu mijiedarbības spēki Hidrofobās mijiedarbības Taukskābju micella Enerģija: 3 - 4 kcal/mols
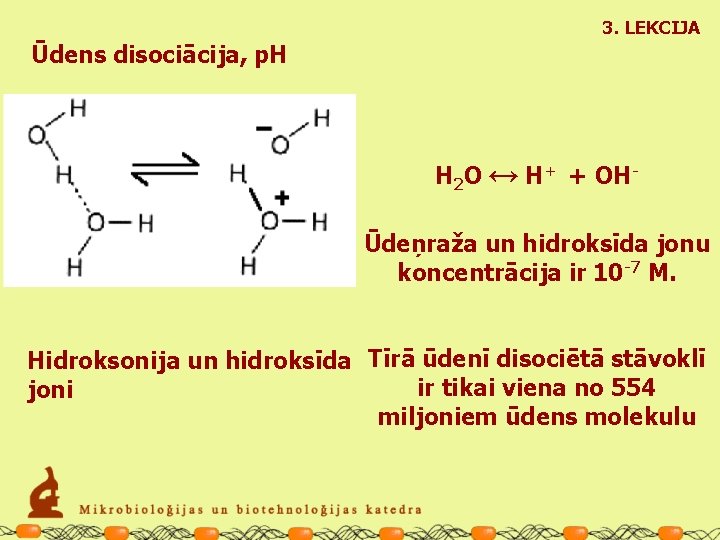
3. LEKCIJA Ūdens disociācija, p. H H 2 O ↔H + + OH- Ūdeņraža un hidroksīda jonu koncentrācija ir 10 -7 M. Hidroksonija un hidroksīda Tīrā ūdenī disociētā stāvoklī ir tikai viena no 554 joni miljoniem ūdens molekulu
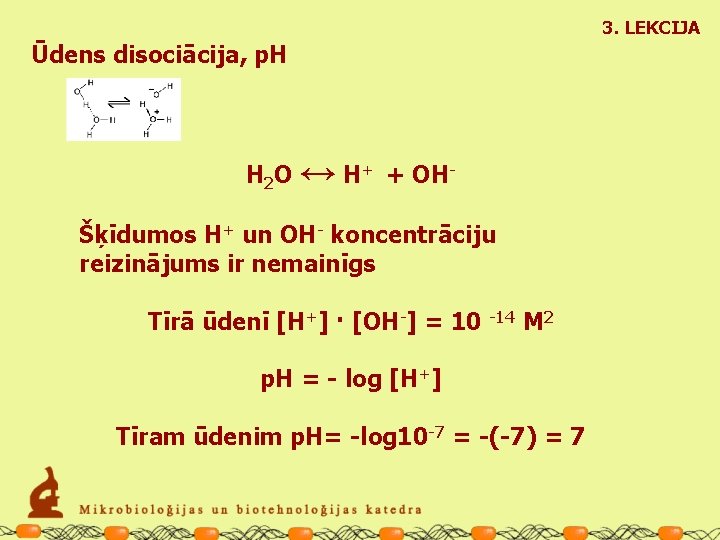
3. LEKCIJA Ūdens disociācija, p. H H 2 O ↔ H+ + OHŠķīdumos H+ un OH- koncentrāciju reizinājums ir nemainīgs Tīrā ūdenī [H+] · [OH-] = 10 -14 M 2 p. H = - log [H+] Tīram ūdenim p. H= -log 10 -7 = -(-7) = 7

3. LEKCIJA SKĀBES UN SĀRMI Skābes palielina H+ jonu koncentrāciju šķīdumā Vājas skābes disociē (sadalās) jonos tikai daļēji, stipras – pilnīgi. Stipras HCl H+ + Cl. Vājas ogļskābe H 2 CO 3 ↔ H+ + HCO 3 hidrogēnkarbonāta jons, konjugētā (saistītā) bāze

3. LEKCIJA SKĀBES UN SĀRMI Vājas skābes disociē (sadalās) jonos tikai daļēji, stipras – pilnīgi. Stipras skābes šķiduma p. H aprēķins: 0, 1 M sālskābe šķīdumā ir pilnīgi disociējusi. Tātad H+ jonu koncentrācija šķīdumā būs 10 -1 M. p. H = -log 10 -1 = -(-1) = 1
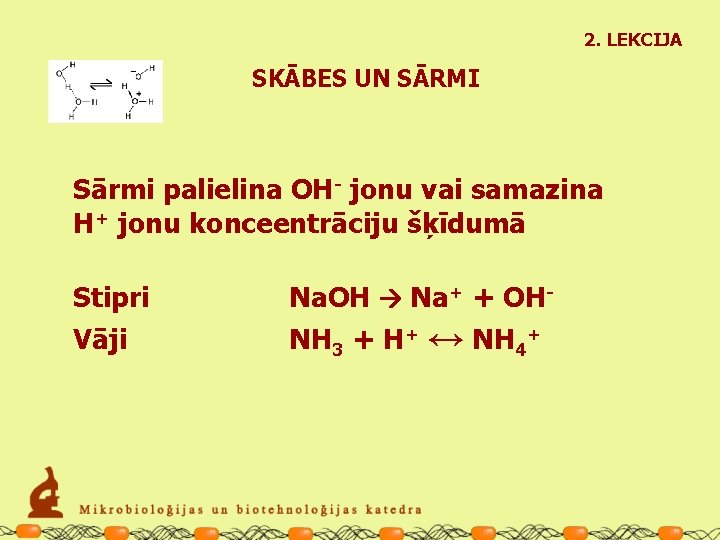
2. LEKCIJA SKĀBES UN SĀRMI Sārmi palielina OH- jonu vai samazina H+ jonu konceentrāciju šķīdumā Stipri Vāji Na. OH Na+ + OHNH 3 + H+ ↔ NH 4+

3. LEKCIJA SKĀBES UN SĀRMI Skābju un sārmu stiprumu raksturo disociācijas konstante p. K. Jo mazāks p. K, jo stiprāka skābe. p. K ir skaitliski vienāds ar p. H, pie kura puse skābes molekulu šķīdumā ir disociētā stāvoklī. Div- un trīsvērtīgām skābēm katrai disociācijas stadijai ir savs p. K. H 3 PO 4 ↔ H 2 PO 4 - + H+ p. K = 1. 8 H 2 PO 4 - ↔ HPO 42 - + H+ p. K = 7. 2

3. LEKCIJA SKĀBES UN SĀRMI Dažādu šķīdumu p. H vērtības

4. LEKCIJA SKĀBES UN SĀRMI Dažādu šķīdumu p. H vērtības

4. LEKCIJA BUFERŠĶĪDUMI Šķīduma p. H ir atkarīgs no hidroksonija vai hidroksīda jonu koncentrācijas. Noteikta, optimāla p. H saglabāšana organismam ir vitāli svarīga.

4. LEKCIJA Buferšķīdumi Vājas skābes un saistītās (konjugētās) bāzes šķīdumi, kas spēj pretoties straujām p. H izmaiņām, pievienojot nelielus stipras skābes vai sārma daudzumu.
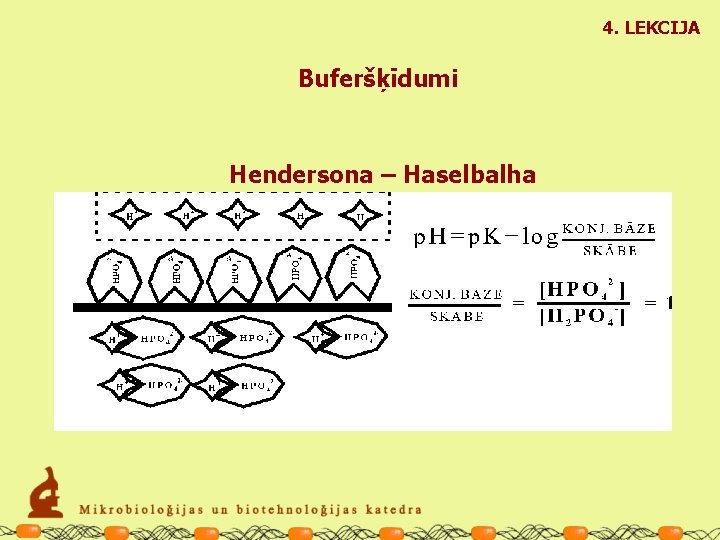
4. LEKCIJA Buferšķīdumi Hendersona – Haselbalha vienādojums:
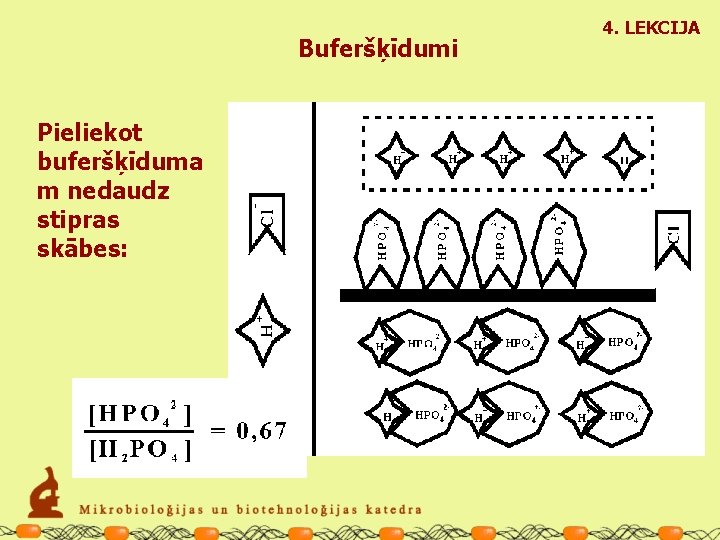
Buferšķīdumi Pieliekot buferšķīduma m nedaudz stipras skābes: 4. LEKCIJA

BUFERŠĶĪDUMI 4. LEKCIJA Pievienojot HCl līdz 0. 01 M koncentrācijai ūdenim, p. H būs 2. Pievienojot HCl līdz 0. 01 M koncentrācijai 0. 05 M hidrogēnfosfāta/dihidrogēnfosfāta buferšķīdumam pie p. H 7. 2, p. H būs: p. H = 7. 2 + log 0. 67 = 7. 2 + (-0. 174) = ~ 7. 0

4. LEKCIJA Buferšķīdumi Pieliekot buferšķīduma m nedaudz stipra sārma:
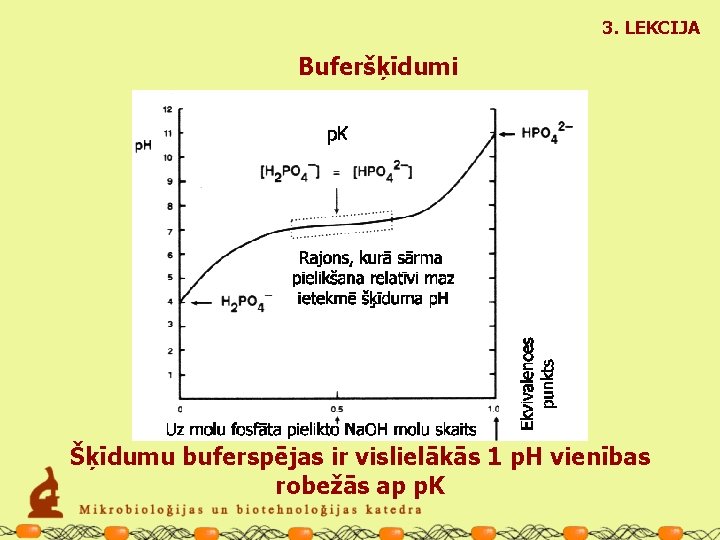
3. LEKCIJA Buferšķīdumi Šķīdumu buferspējas ir vislielākās 1 p. H vienības robežās ap p. K
- Slides: 53