Identificao Laboratorial de Leveduras de Importncia Mdica Inneke

Identificação Laboratorial de Leveduras de Importância Médica Inneke Marie van der Heijden Laboratório de Bacteriologia (LIM-54) Instituto de Medicina Tropical II Hospital das Clínicas - FMUSP

Características gerais Grupo heterogêneo Unicelulares Diversidade n Cor das colônias n Textura Reprodução

Reprodução das leveduras Assexuada n n n Estado anamorfo Por brotamento ou gemulação Formação blastoconídios e pseudo-hifas

Reprodução das leveduras Reprodução sexuada: conjugação n Ascosporadas Candida guilliermondii (anamorfo) Pichia guilliermondii (teleomorfo) n Anascosporadas Candida famata (anamorfo) Debaryomyces hansenii (teleomorfo) n Balistosporadas Rhodotorula rubra n Basidiosporadas Cryptococcus neoformans (anamorfo) Filobasidiella neoformans (teleomorfo)

Procedimentos laboratoriais Diagnóstico laboratorial n Exame direto: levedura ou fungo filamentoso ? n Cultura: isolamento e identificação Condições adequadas de incubação n Meio de cultivo n Temperatura n Tempo

Meios mais utilizados na micologia Agar Sabouraud com cloranfenicol (leveduras e fungos filamentosos) Agar PDA (batata-dextrose) (fungos filamentosos) Agar Mycobiotic=Mycosel= agar seletivo para fungos patogênicos (uso restrito=inibe vários fungos sensíveis à cicloheximida, inclusive leveduras)

Exame direto da amostra “a fresco” entre lâmina e lamínula após clarificação com KOH (10 a 20%) com tinta da China (nanquim) após coloração: . esfregaços (Gram, Giemsa e outras). cortes histológicos (Mucicarmin de Mayer, Gomori-Grocott, H. E. e outras)

Exame da cultura: achados microscópicos Leveduras com filamentação (hifas) n n abundante: Candida spp. escassa: Candida spp e outras dezenas de gêneros (p. ex. hifas curtas, curvas=Malassezia spp) Leveduras sem filamentação n Sem cápsula: Candida spp e outros gêneros n capsuladas: Cryptococcus neoformans
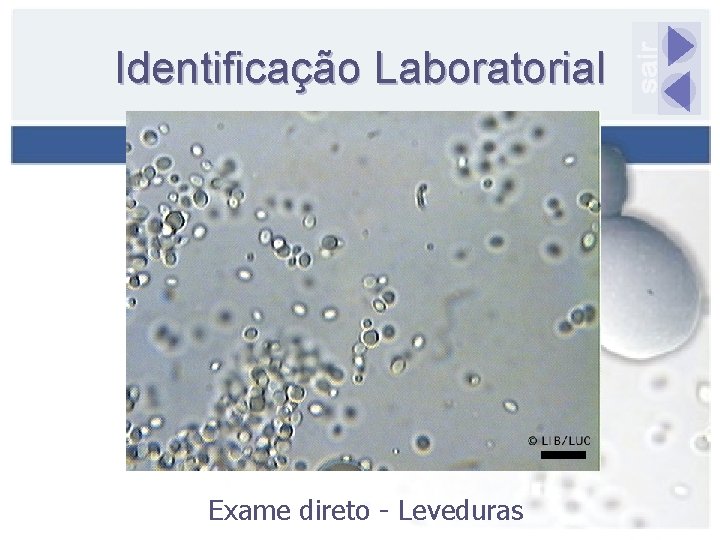
Identificação Laboratorial Exame direto - Leveduras
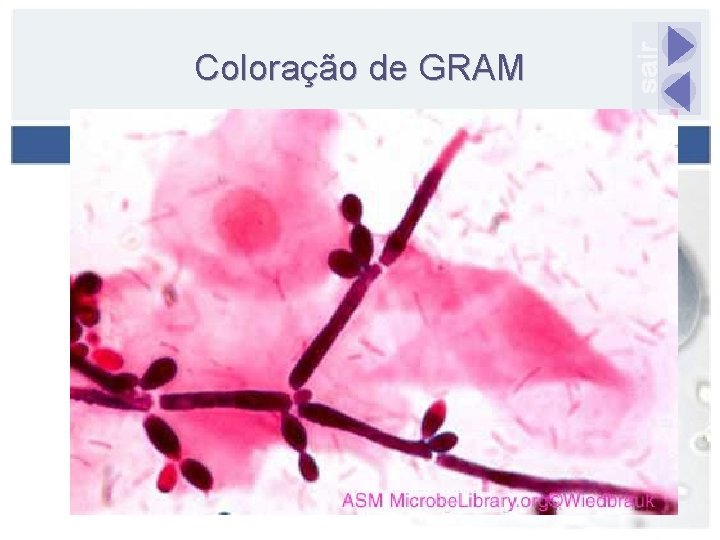
Coloração de GRAM
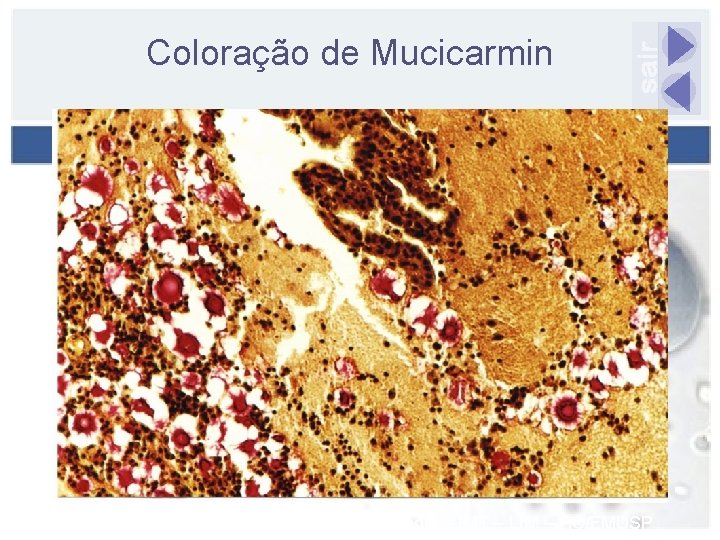
Coloração de Mucicarmin Fonte: Laboratório de Micologia – IMT – LIM – HC/FMUSP

Coloração de Gomori-Grocott Fonte: Laboratório de Micologia – IMT – LIM – HC/FMUSP

Identificação Laboratorial Pureza das colônias n Detecção por exame direto n Sub-cultivo n Técnica de esgotamento n Meios seletivos Cloranfenicol: inibir bactérias Cicloheximida: inibir fungos anemófilos
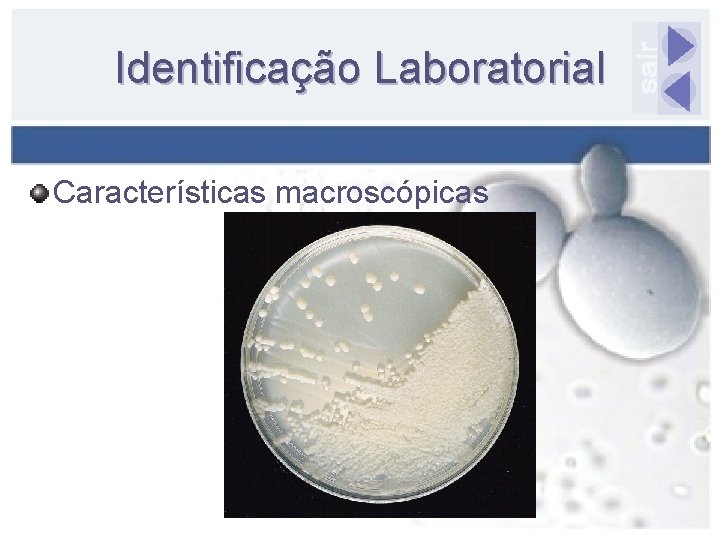
Identificação Laboratorial Características macroscópicas
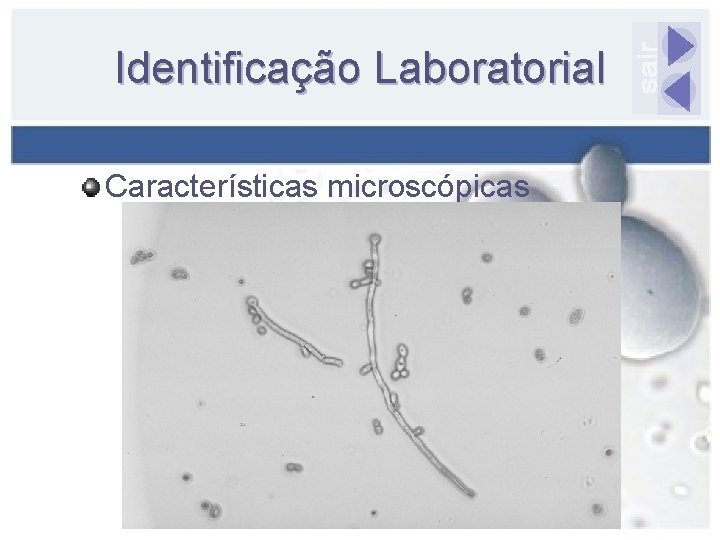
Identificação Laboratorial Características microscópicas
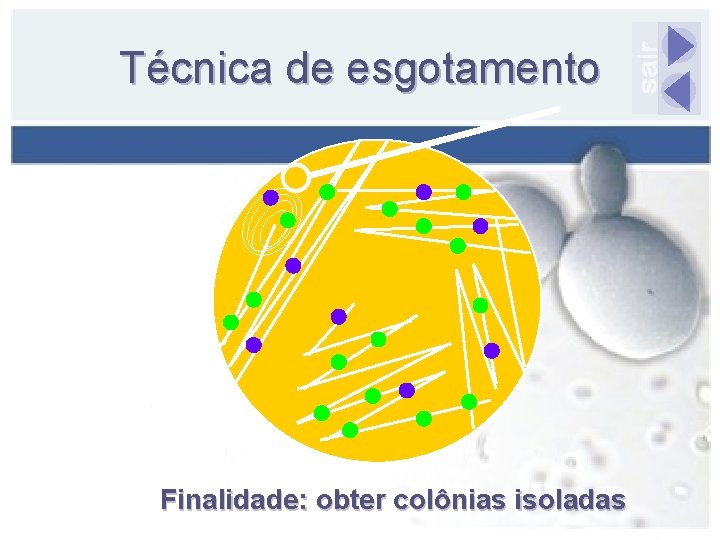
Técnica de esgotamento Finalidade: obter colônias isoladas

Pureza das colônias Alternativa: meios cromogênicos CHROMagar Candida Sugere espécie conforme cor da colônia: Verde = C. albicans Azul = C. tropicalis Rosa = C. krusei Branco = outras espécies e outros gêneros

Identificação Laboratorial Métodos clássicos n Análise morfológica n Assimilação de fontes de carbono e nitrogênio n Fermentação de carboidratos n Hidrólise da uréia (teste da urease) Métodos comerciais

Métodos clássicos de identificação de leveduras Análise morfológica n n n presença de cápsula produção de tubo germinativo, em geral leitura às 2 h cultivo em lâmina (micromorfologia, filamentação e presença de clamidosporos)

Tubo germinativo Identificação presuntiva e rápida de Candida albicans Descrito em 1960 Capacidade de formar filamentos na presença de soro (1 -3 h) n Humano, fetal bovino ou cavalo Técnica simples 94 -97% de positividade para C. albicans Sidrim et al. , 1999
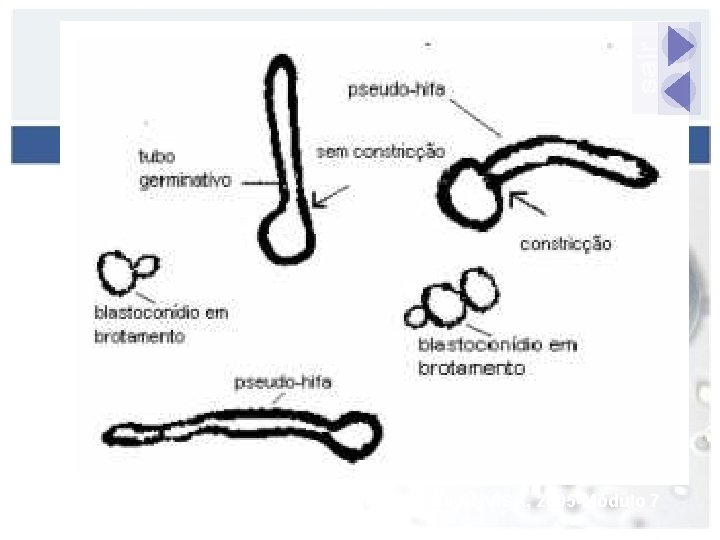
Fonte: Manual da ANVISA, 2005 -Módulo 7
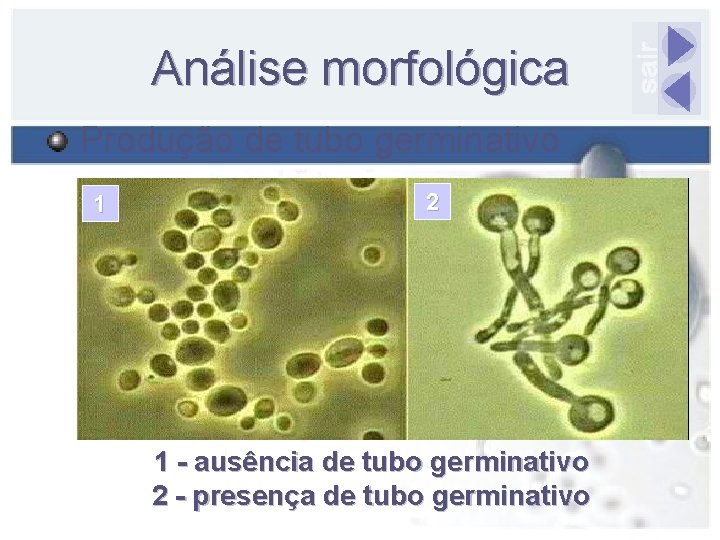
Análise morfológica Produção de tubo germinativo 1 2 1 - ausência de tubo germinativo 2 - presença de tubo germinativo
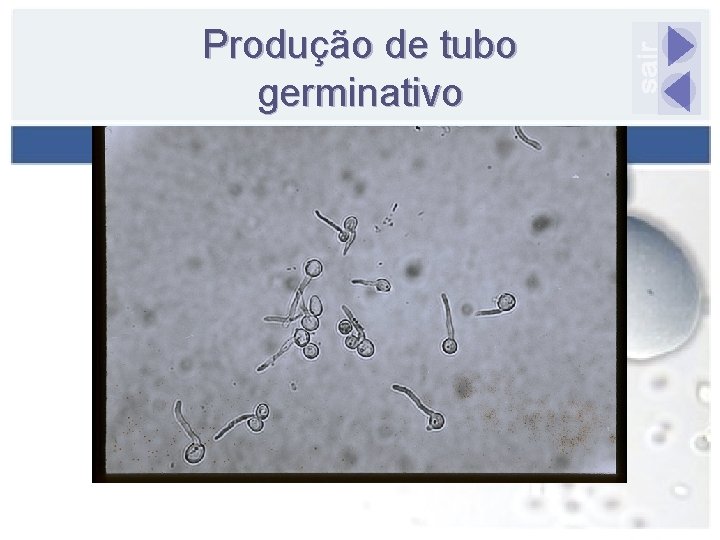
Produção de tubo germinativo
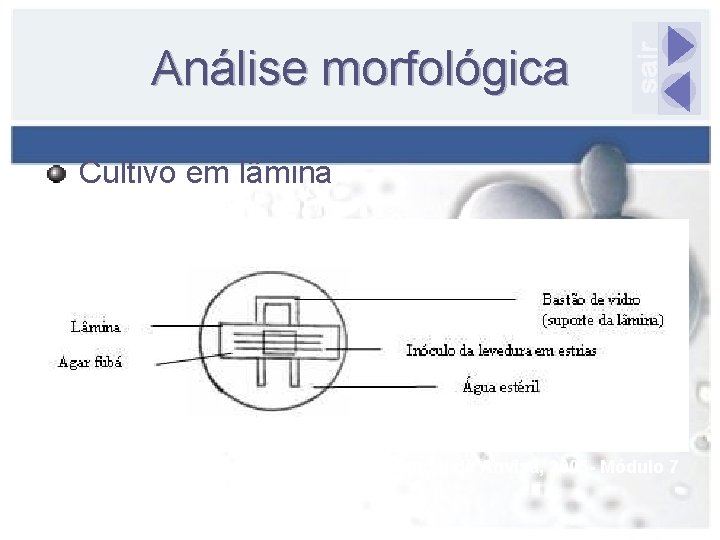
Análise morfológica Cultivo em lâmina Fonte: Manual da Anvisa, 2005 - Módulo 7

Cultivo em lâmina Espécies de Candida spp
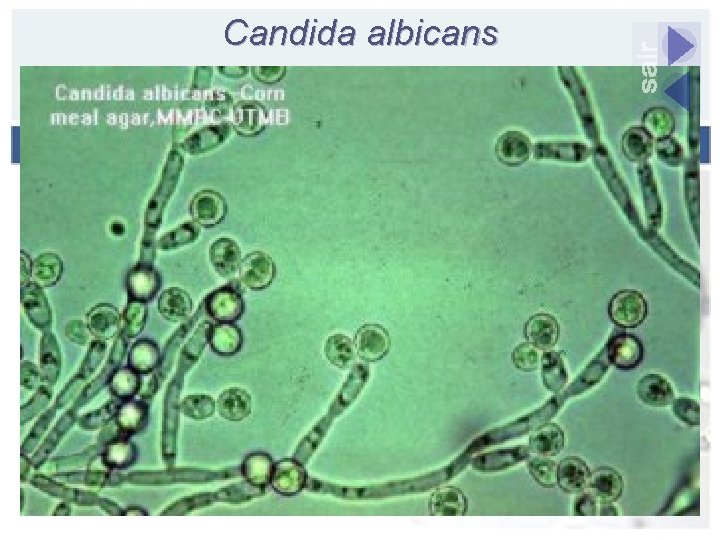
Candida albicans
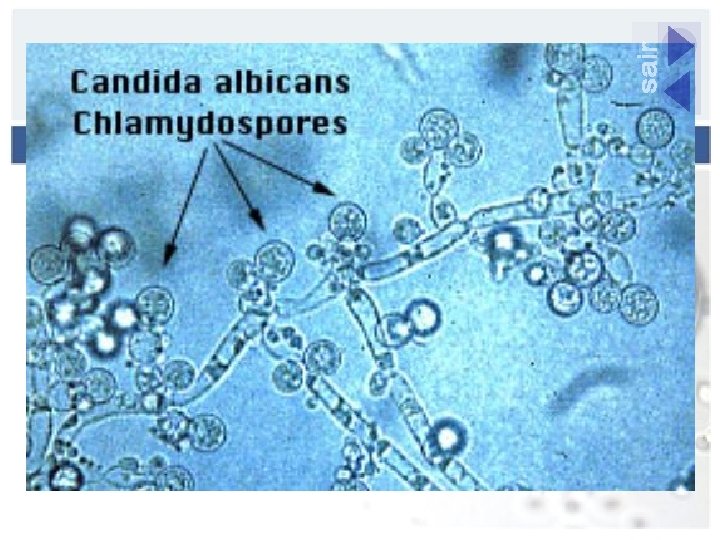
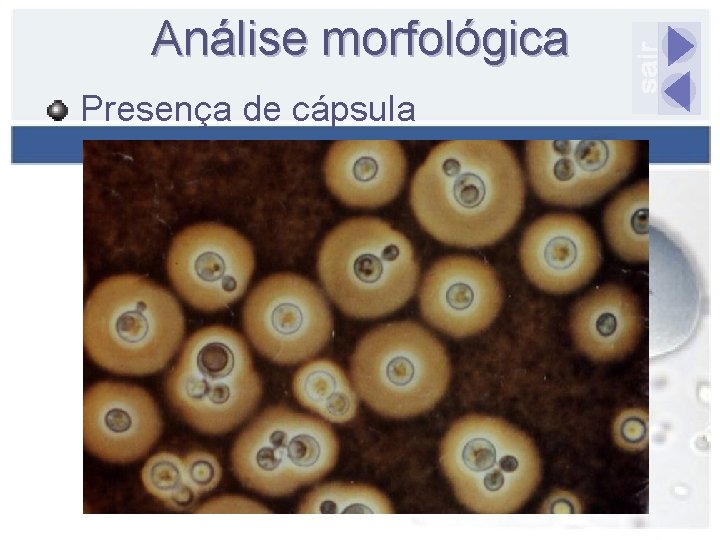
Análise morfológica Presença de cápsula
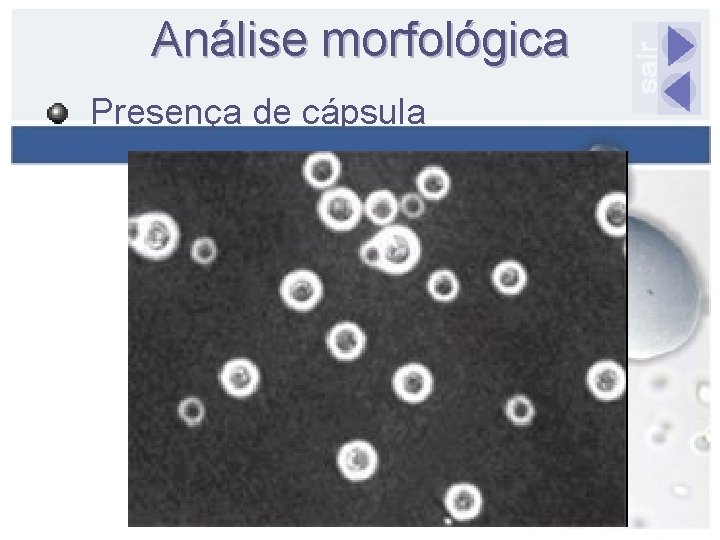
Análise morfológica Presença de cápsula

Métodos clássicos de identificação de leveduras Assimilação de fontes de C Assimilação de nitrogênio } AUXANOGRAMA Fermentação de carboidratos n ZIMOGRAMA Hidrólise da uréia (teste da urease) }

AUXANOGRAMA Presença de oxigênio Utilização de fontes de: n Carbono (a partir de açúcares) n Nitrogênio (a partir de nitrato) CQ: cepas ATCC

AUXANOGRAMA Meio basal sem fonte de carbono n Sólido ou líquido n Yeast Nitrogen Base (YNB)- 40 m. L Inóculo: escala 1 Mc. Farland (2 m. L) Incorporar suspensão de levedura ao meio Aplicação de discos ou açúcar in natura Incubação 30 o. C por 24 -48 h
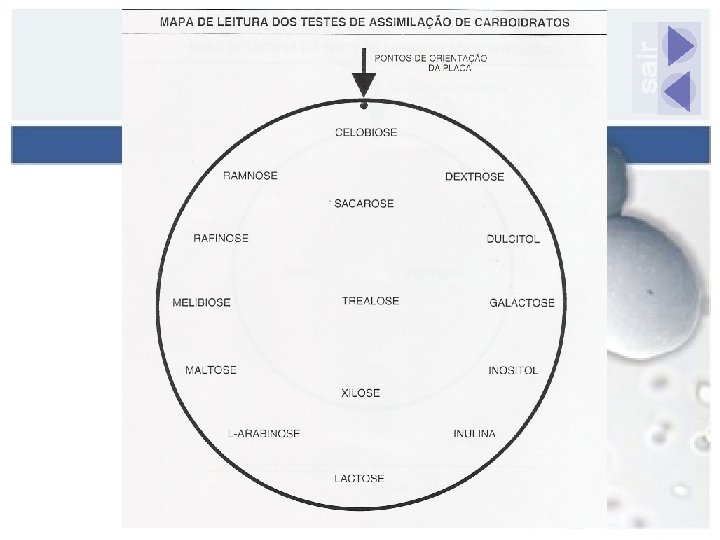

AUXANOGRAMA Meio basal sem fonte de nitrogênio n Sólido n Yeast Carbon Base (YCB)- 20 m. L Inóculo: escala 1 Mc. Farland (1 m. L) Incorporar suspensão de levedura ao meio

Auxanograma Aplicação de compostos nitrogenados n Peptona (controle positivo) n Nitrato de potássio Incubação 30 o. C por 24 -48 h até 7 dias Resultados: presença de zona de crescimento (leitura visual)
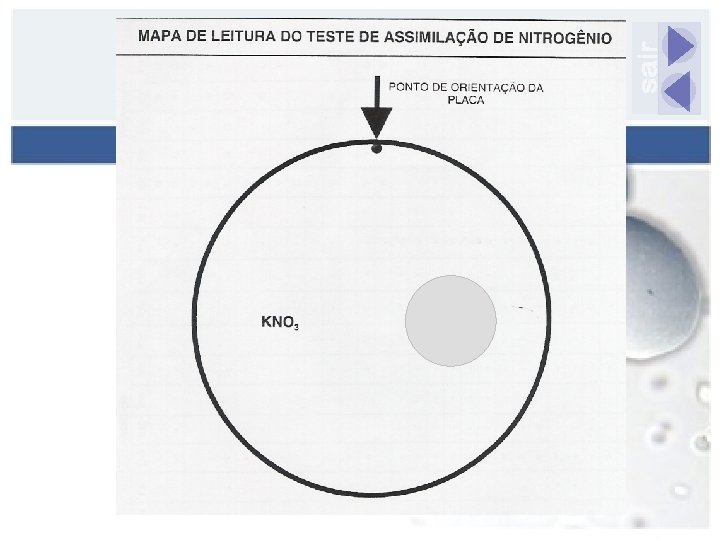

ZIMOGRAMA Baixa tensão de oxigênio Fermentação Utilização de fontes de Carbono n a partir de açúcares n produção de CO 2 Meio líquido ou semi-sólido gelosado a 0, 6%

ZIMOGRAMA Meio basal (3 m. L) n Azul de bromotimol (opcional), extrato de levedura, peptona, etanol 95% e água Solução de açúcar 6% (1, 5 m. L) Suspensão levedura: 2 Mc. Farland (0, 2 m. L/tubo) Leitura após 10 -14 dias de incubação a 37 o. C Resultados: presença ou ausência de bolhas no tubo de Durham

Testes adicionais Teste da urease n Positiva: Cryptococcus neoformans n Negativa: Candida albicans Resistência à cicloheximida n Resistentes: C. albicans, C. stellatoidea, C. guilliermondii e C. pseudotropicalis
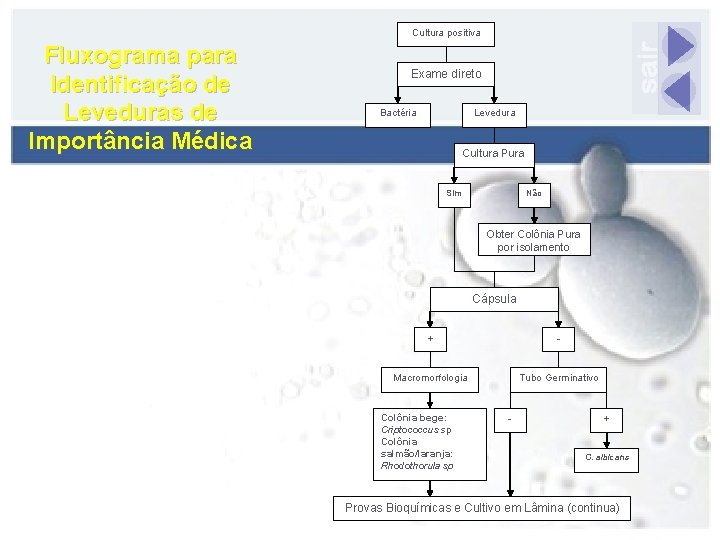
Cultura positiva Fluxograma para Identificação de Leveduras de Importância Médica Exame direto Bactéria Levedura Cultura Pura Sim Não Obter Colônia Pura por isolamento Cápsula + - Macromorfologia Tubo Germinativo Colônia bege: Criptococcus sp Colônia salmão/laranja: Rhodothorula sp - + C. albicans Provas Bioquímicas e Cultivo em Lâmina (continua)
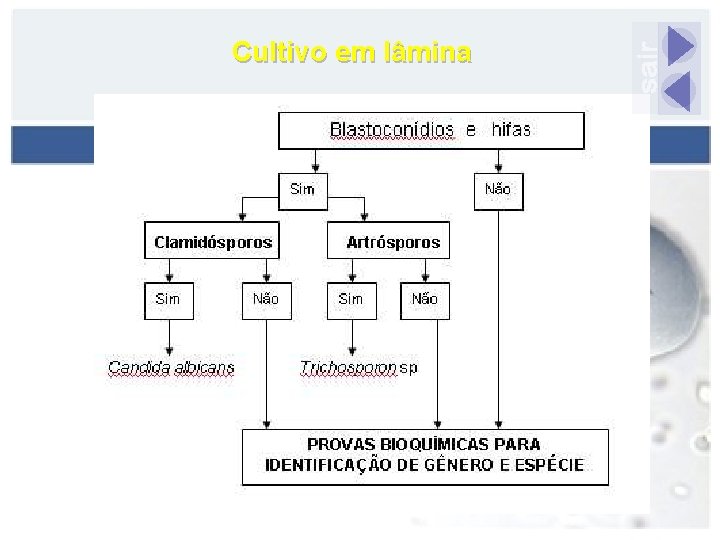
Cultivo em lâmina

Provas bioquímicas Blastoconídios - Urease positiva: n Inositol - : Rhodotorula n Inositol + : Cryptococcus Presença de artrósporos(=artroconidios) n Urease - : Geotrichum n Urease + : Trichosporon (brotamento +)

Artrósporos Geotrichum sp. www. botany. utoronto. ca www. mycology. adelaide. edu. au
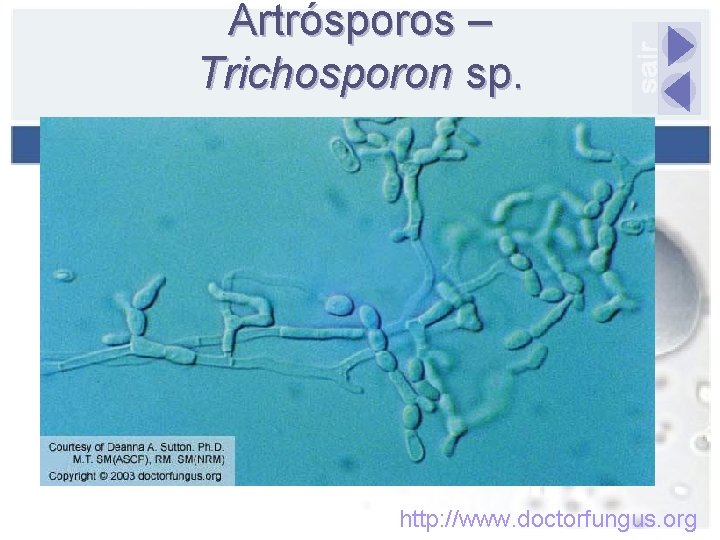
Artrósporos – Trichosporon sp. http: //www. doctorfungus. org
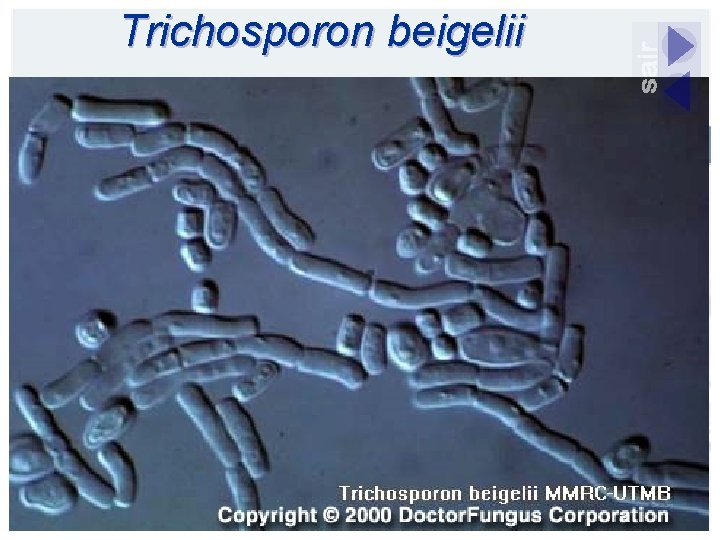
Trichosporon beigelii
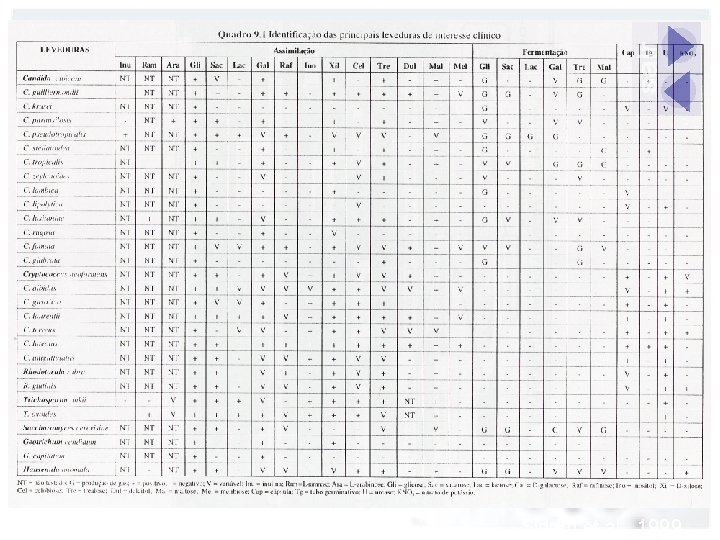
Sidrim et al. , 1999

Métodos comerciais de identificação de leveduras Chromoagar Candida API 20 C AUX (Bio. Mérieux) ID 32 C (Bio. Mérieux) Candifast (International Microbio) Vitek (Bio. Mérieux)

Meios cromogênicos Cromogênicos: detectam enzimas através de substratos específicos ou substratos cromógenos Permitem detecção de colônias mistas Rápida identificação de C. albicans
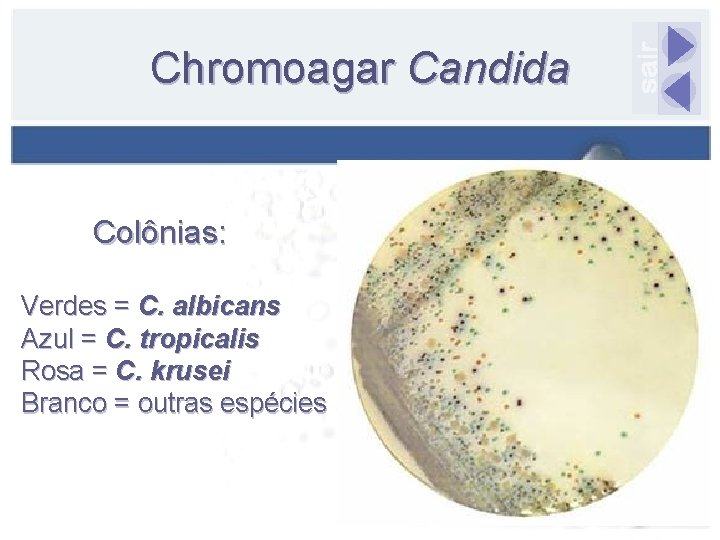
Chromoagar Candida Colônias: Verdes = C. albicans Azul = C. tropicalis Rosa = C. krusei Branco = outras espécies

Painel de identificação API 20 C AUX system (Bio. Mérieux) 19 testes assimilativos - incubação 30 o. C - 24, 48 e 72 horas Leitura por verificação de crescimento - turbidez Necessidade de correlação com a análise morfológica Informa a necessidade de testes adicionais Método de referência Acurácia entre 96 e 98% para as espécies patogênicas mais comuns, sem testes adicionais

API 20 C AUX system (Bio. Mérieux)
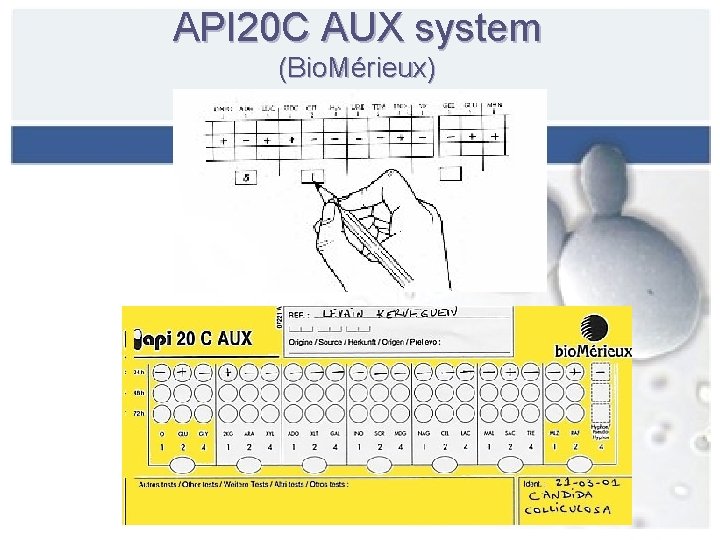
API 20 C AUX system (Bio. Mérieux)
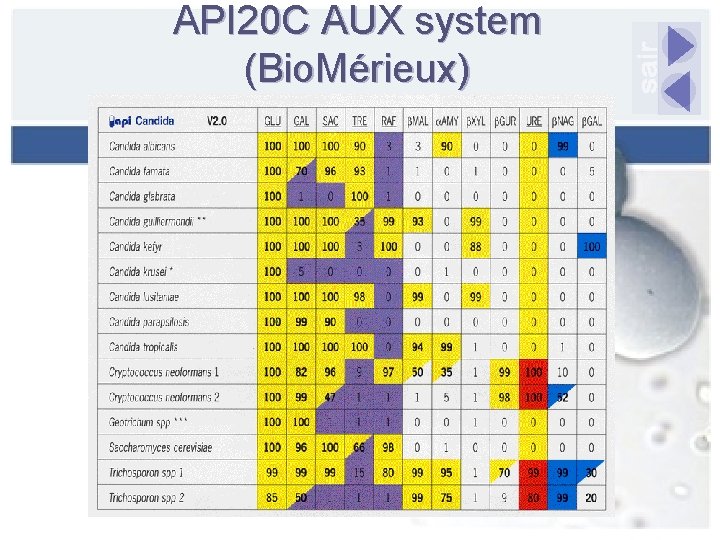
API 20 C AUX system (Bio. Mérieux)

ID 32 C STRIPS (Bio. Mérieux) 29 testes leitura após 24/48 horas de incubação a 30 o. C visual ou automatizada taxas de identificação variam de 94 a 98 % Ramani et al, 1998 n n taxa de identificação de 92% para as espécies comuns de leveduras 85 % para isolados raros apresenta uma base de dados bastante ampliada

Comparação entre os métodos comerciais semi-automatizados mais utilizados na identificação de leveduras Fonte: Sidrim e Moreira, 1999.

Candifast (International Microbio) Identificação e teste de sensibilidade Gêneros: Candida, Trichosporon, Cryptococcus, Rhodotorula e Saccharomyces Único inóculo e leitura colorimétrica Resultados em 24 a 72 horas (37 o. C) Identificação n sensibilidade actidione n fermentação de 7 açúcares n hidrólise da uréia Teste de Sensibilidade n sete antifúngicos: 1 concentração www. int-microbio. com

Vitek system (Bio. Mérieux) Sistema automatizado: leitura turbidimétrica 26 substratos baseado nos métodos convencionais Bionúmero - banco de dados do sistema Resultado: percentual de probabilidade de ser a espécie identificada

Vitek system (Bio. Mérieux) 16 espécies de Candida 6 espécies de Cryptococcus 3 espécies de Rhodotorula 2 espécies de Trichosporon 3 espécies de Geotrichum 2 espécies de Prototheca, Pichia anomala, Pichia ohmeri, Saccharomyces cerevisiae e Yarrowia lipolytyca

Vitek system (Bio. Mérieux) Percentual de probabilidade é baixo = testes adicionais 93 % das leveduras comuns foram identificadas 55 % das leveduras menos comum foram corretamente identificadas Falhas na identificação: n 42% de C. krusei n 80 % de C. lambica n 88 % de T. beigelli n 83 % de Cryptococcus (não C. neoformans)

Vitek system (Bio. Mérieux) Sistema rápido e adequado para identificar os isolados clínicos comuns Falhas na identificação de leveduras não usuais (Dooley et al, 1994)

Vitek 2 ID YST Card 47 testes (29 clássicos e 18 enzimáticos) leitura fluorescente automatizada 15 horas de incubação base de dados com 51 espécies inclui Candida dubliniensis e a atualização sistemática dos gêneros Rhodotorula e Trichosporon taxa de identificação de 96, 8%

Comparação entre métodos comerciais para identificação de leveduras Candifast X Vitek n 98% de concordância (www. int-microbio. com) Candifast X API 20 C AUX (Gundes et al. , 2001) n 116 isolados clínicos (C. albicans, C. parapsilosis, C. glabrata e outras leveduras) n 87% de identificações corretas para API 20 C n 82, 7% de identificações corretas para Candifast
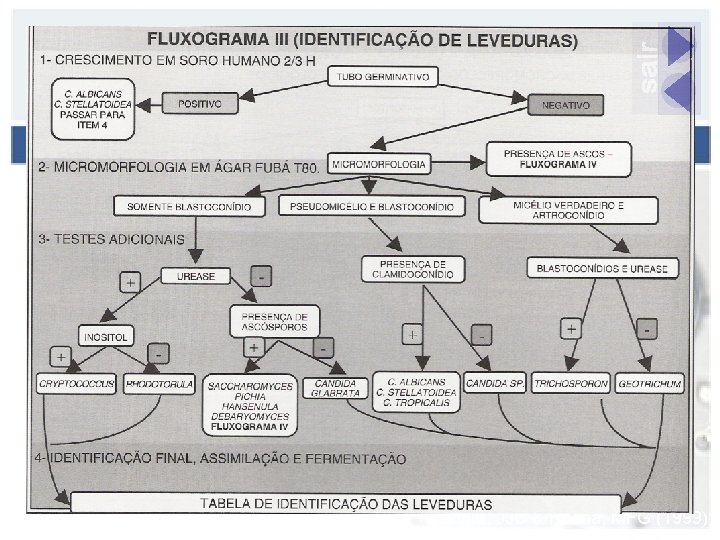
Sidrim, JJC & Rocha, MFG (1999).
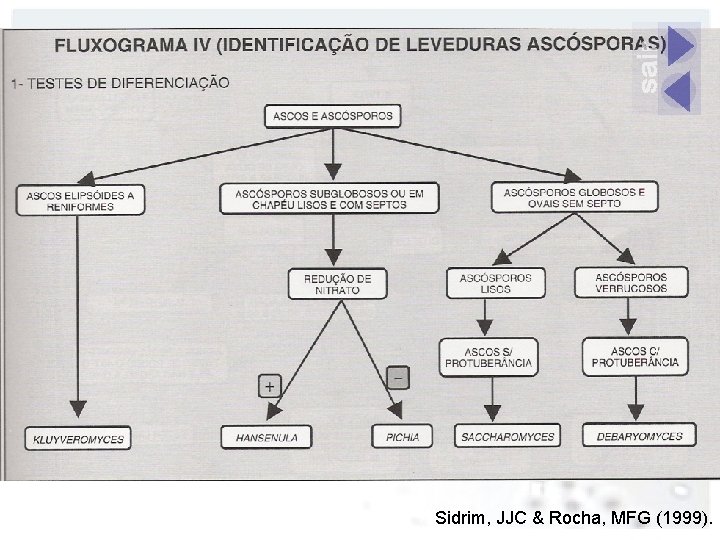
Sidrim, JJC & Rocha, MFG (1999).
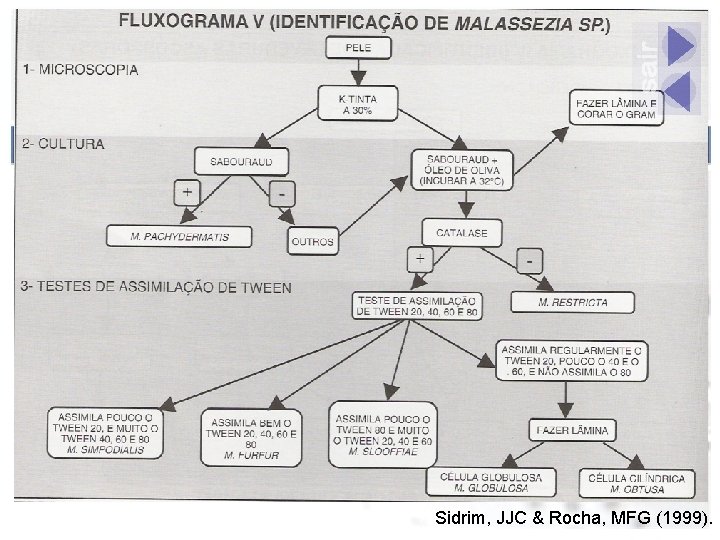
Sidrim, JJC & Rocha, MFG (1999).

Considerações finais Diversos métodos Diferentes níveis de sensibilidade, especificidade e acurácia em cada sistema Necessidade de estudo morfológico e/ou a complementação com testes tradicionais Escolha do(s) método(s) n Realidade de cada laboratório n Freqüência de isolamento n Custo do teste n Eficácia do teste
- Slides: 66