I V tr trong bng h thng tun

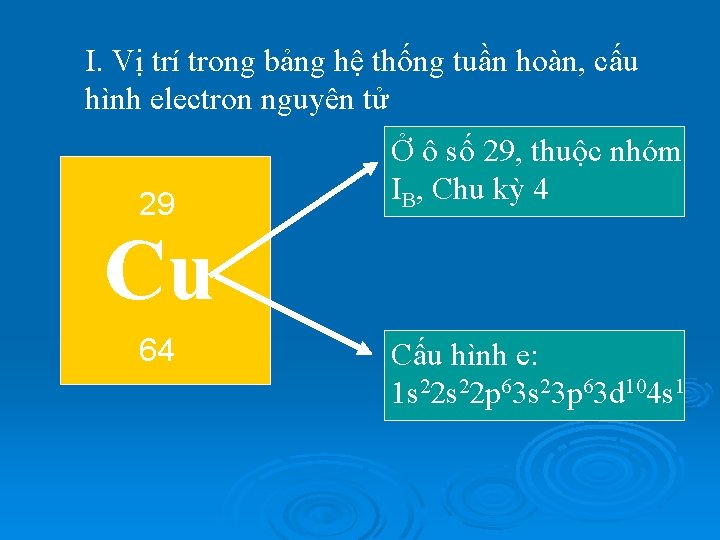
I. Vị trí trong bảng hệ thống tuần hoàn, cấu hình electron nguyên tử 29 Ở ô số 29, thuộc nhóm IB, Chu kỳ 4 Cu 64 Cấu hình e: 1 s 22 p 63 s 23 p 63 d 104 s 1

II. Tính chất vật lí: SGK III. Tính chất hóa học: - Kém hoạt động, tính khử yếu 1. Tác dụng với phi kim Ở nhiệt độ thường, đồng tác dụng với flo, brom. Ở nhiệt độ cao, đồng tác dụng với O 2, S, . . t 0 2 Cu + O 2 → 2 Cu. O

2. Tác dụng với axit Cu đứng sau H, trước Ag trong dãy điện hóa nên Cu không pư HCl, H 2 SO 4 l Cu + 2 H 2 SO 4đ → Cu. SO 4 + SO 2 +2 H 2 O 3 Cu + 8 HNO 3 l → 3 Cu(NO 3)2 +2 NO +4 H 2 O Cu + 4 HNO 3đ → Cu(NO 3)2 +2 NO 2 +2 H 2 O IV. Hợp chất của Cu: 1. Tính chất:

Cu. O -Chất rắn màu đen. Là oxit bazo. Khi đun nóng dễ bị khử bởi H 2, CO, C. Cu. O + H 2 SO 4 → Cu. SO 4 + H 2 O Cu. O + H 2 → Cu + H 2 O Cu(OH)2 -Chất rắn màu xanh, không tan trong nước. Là 1 bazo dễ bị nhiệt phân Cu(OH)2 + 2 HCl → Cu. Cl 2 + H 2 O Cu(OH)2 → Cu. O +H 2 O Cr. O 3 -Chất rắn màu đỏ thẫm. Là oxit axit. Có tính oxi hóa manh Cr. O 3 + H 2 O → H 2 Cr. O 4 axit cromic Cr. O 3 + H 2 O → H 2 Cr 2 O 7 axit đicromic Cu 2+ -dd Cu 2+: màu xanh. Cu. SO 4 khan màu trắng, ở dạng ngậm nước Cu. SO 5 H O màu xanh

V. Ứng dụng -Trong ngành công nghiệp, kỹ thuật -Trong xây dựng -Trong nông nghiệp
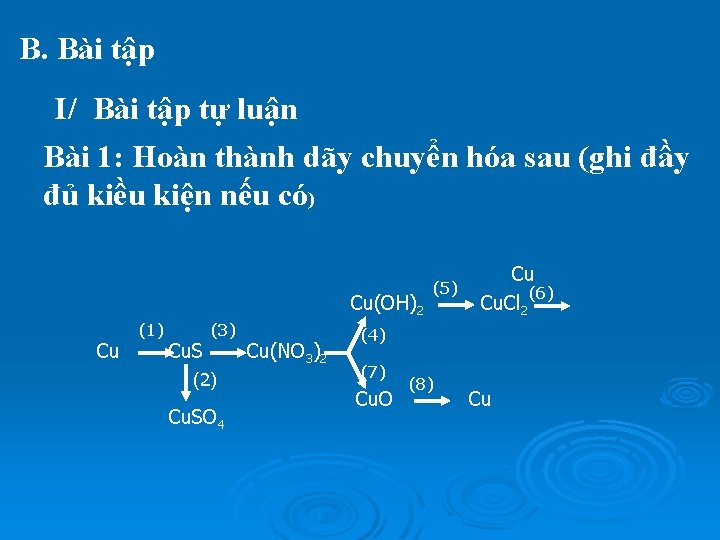
B. Bài tập I/ Bài tập tự luận Bài 1: Hoàn thành dãy chuyển hóa sau (ghi đầy đủ kiều kiện nếu có) Cu(OH)2 Cu (1) Cu. S (3) (2) Cu. SO 4 Cu(NO 3)2 (5) Cu (6) Cu. Cl 2 (4) (7) Cu. O (8) Cu

Bài giải (1) Cu + St 0→ Cu. S (2) Cu. S + H 2 SO 4 → Cu. SO 4 + H 2 S (3) Cu. S + 2 HNO 3 → Cu(NO 3)2 + H 2 S (4) Cu(NO 3)2 + 2 Na. OH → Cu(OH)2 + 2 Na. NO 3 (5) Cu(OH)2Đpdd + 2 HCl → Cu. Cl 2 +2 H 2 O (6) Cu. Cl 2 → Cu + Cl 2 to (7) Cu(NO 3)2 → Cu. O + 2 NO 2+ 1/2 O 2 (8) Cu. O + CO → Cu + CO 2

Bài 2: Viết các phương trình phản ứng điều chế : * Cu từ dung dịch Cu(OH)2

Bài 3 Cho Cu tác dụng với Na. NO 3 và H 2 SO 4 loãng sẽ giải phòng khí gì? . Viết ptpư

BÀI GiẢI Bài 3: Sinh ra khí NO Na. NO 3 → Na+ + NO 3 H 2 SO 4 → 2 H+ + SO 423 Cu + 2 NO 3 - +8 H+ → 3 Cu 2+ + 2 NO +4 H 2 O

B. Bài tập trắc nghiệm : Câu 1: Cấu hình e của Cu A. [Ar]3 d 7 B. [Ar]3 d 9 C. [Ar]3 d 8 D. [Ar]3 d 10

Câu 2: Cho 19, 2 g kim loại M tác dụng với dung dịch HNO 3 loãng dư, thu được 4, 48 L khí duy nhất NO(đktc). Kim loại M là: A. Mg B. Fe C. Zn D. Cu Câu 3: Cho các thí nghiệm sau : (1) Sục khí NH 3 dư vào dung dịch Cu. SO 4 (2) Cho dd Na. OH dư vào dung dịch Cu. SO 4 (3) Nhỏ từ từ đến dư dung dịch KOH vào dung dịch Cu. Cl 2. Các thí nghiệm có hiện tượng giống nhau là : A. (1), (2) B. (1), (3) C. (2), (3) D. (1), (2), (3)

Câu 4: Hoà tan 9, 7 gam hỗn hợp gồm Cu, Zn bằng dung dịch HCl dư. Sau phản ứng thu được 2, 24 l khí (đktc). Vậy khối lượng Cu và Zn trong hỗn hợp ban đầu lần lược là : A. 6, 4 g ; 3, 3 g B. 3, 2 g ; 6, 5 g C. 5, 6 g , 4, 1 g D. 4, 6 g ; 5, 1 g

- Slides: 15