I gruppi funzionali La sostituzione in un idrocarburo
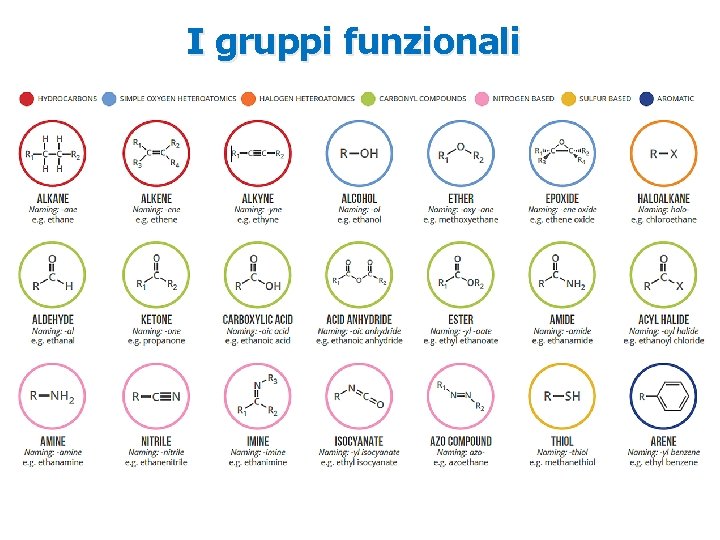
I gruppi funzionali
La sostituzione, in un idrocarburo, di uno (o più) H con un atomo differente da C e H (sostanzialmente ossigeno, ossigeno azoto, azoto zolfo ed alogeni), alogeni modifica profondamente le proprietà chimiche e fisiche del composto. Le molecole che presentano lo stesso atomo (o gruppo atomico) sostitutivo dell’H manifestano proprietà chimico-fisiche simili, simili per questo costituiscono una classe specifica di composti. Gli atomi o i gruppi atomici che caratterizzano ciascuna classe di composti organici sono detti gruppi funzionali

Radicale organico alifatico o aromatico CH 3 -Cl Clorometano (cloruro di metile) R (Ar) X CH-Cl 3 Triclorometano (cloroformio) (X=F, Cl, Br, I) CCl 4 Tetraclorometano (tetracloruro di carbonio) Sono indicati come alogenuri organici o alogenoalcani Il nome specifico si ricava dall’alogeno seguito da quello dell’idrocarburo oppure dall’alogenuro seguito dal nome del radicale organico.
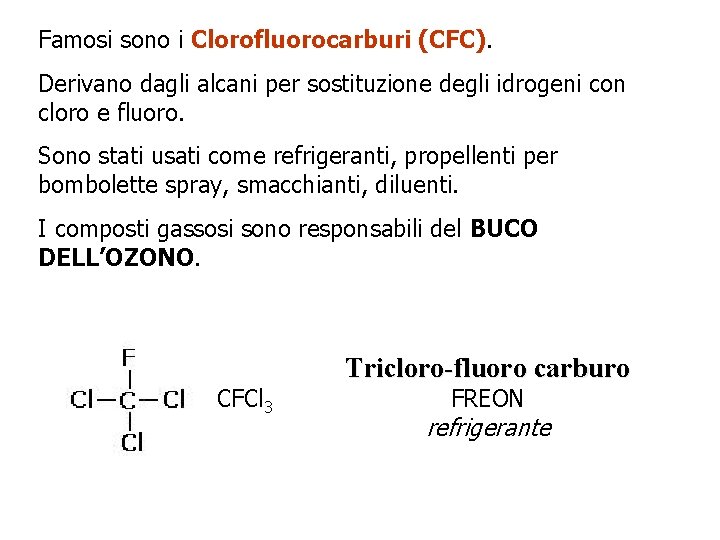
Famosi sono i Clorofluorocarburi (CFC). Derivano dagli alcani per sostituzione degli idrogeni con cloro e fluoro. Sono stati usati come refrigeranti, propellenti per bombolette spray, smacchianti, diluenti. I composti gassosi sono responsabili del BUCO DELL’OZONO. CFCl 3 Tricloro-fluoro carburo FREON refrigerante

Ovviamente esistono gli alogenoalcheni 2 -cloro-1, 3 -butadiene Cloroprene Dalla sua polimerizzazione si ottiene il neoprene (gomma sintetica)
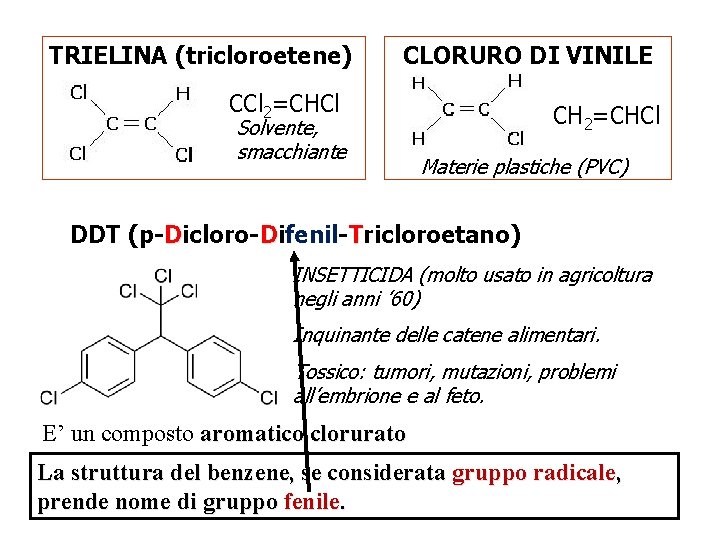
TRIELINA (tricloroetene) CLORURO DI VINILE CCl 2=CHCl Solvente, smacchiante CH 2=CHCl Materie plastiche (PVC) DDT (p-Dicloro-Difenil-Tricloroetano) INSETTICIDA (molto usato in agricoltura negli anni ’ 60) Inquinante delle catene alimentari. Tossico: tumori, mutazioni, problemi all’embrione e al feto. E’ un composto aromatico clorurato La struttura del benzene, se considerata gruppo radicale, prende nome di gruppo fenile.

ALCOLI Radicale organico alifatico o aromatico R (Ar) OH Gruppo ossidrile Prefisso Idrossi La presenza dell’ossigeno tende a polarizzare la molecola, per cui quasi tutti gli alcoli sono liquidi e solubili in solventi polari, ad es. acqua (legami H). Il radicale organico, organico invece, tende ad abbassare la polarità: più è grande, minore è la polarità. Grazie ad esso, comunque, questi composti sono solubili anche in solventi neutri. Tendono ad avere reazione di condensazione con altri alcoli, con acidi organici e con basi inorganiche (es. Na. OH, KOH ecc. ) nomenclatura: Nome Organico + olo

Metile-OH METANOLO (alcool metilico) TOSSICO Presente nel distillato di legno. Ha stesso odore dell’etanolo, stessi suoi effetti, ma potenziati. E’ normalmente presente nelle bevande alcooliche (limite: 0, 25 m. L di metanolo per 100 m. L per i vini rossi: concentrazioni maggiori sono considerate adulteranti). Etile-OH ETANOLO (alcool etilico) TOSSICO Presente nelle bevande alcooliche. Si ricava dalla fermentazione batterica a partire dal glucosio C 6 H 12 O 6 2 C 2 H 5 OH+2 CO 2

POLIALCOLI 2 o più gruppi -OH GLICOLE ETILENICO (1, 2 -etandiolo) TOSSICO (velenoso) - ANTICONGELANTE GLICOLE propilenico (1, 2 -propandiolo) Inerte: utilizzato come antigelo, come refrigerante, come fumogeno (macchina del fumo), come additivo alimentare e cosmetico, come solvente (ad es. per farmaci). GLICEROLO (glicerina) (1, 2, 3 -propantriolo) CH 2 OH-CH 2 OH base per la struttura dei gliceridi Si indicano le posizioni dei gruppi -OH e, davanti al suffisso -olo si antepone il prefisso per il numero complessivo di tali gruppi.
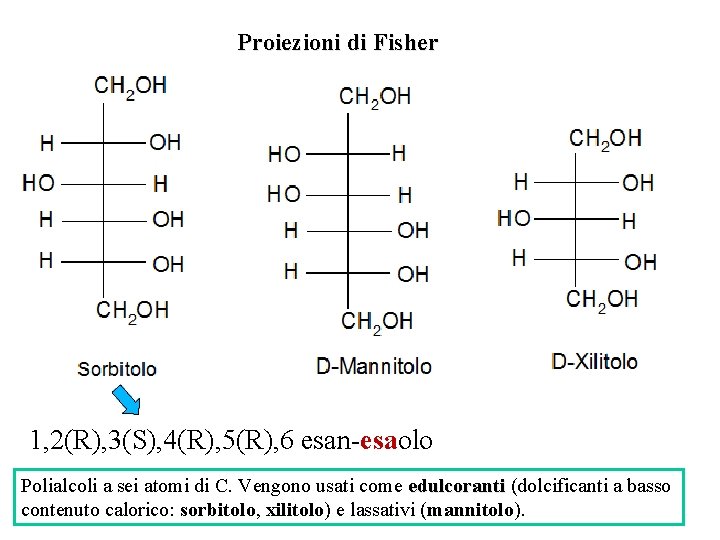
Proiezioni di Fisher 1, 2(R), 3(S), 4(R), 5(R), 6 esan-esaolo Polialcoli a sei atomi di C. Vengono usati come edulcoranti (dolcificanti a basso contenuto calorico: sorbitolo, xilitolo) e lassativi (mannitolo).
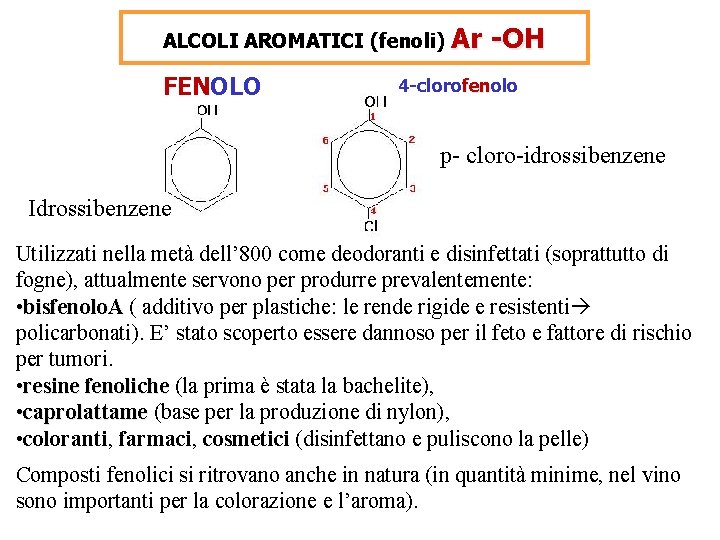
ALCOLI AROMATICI (fenoli) FENOLO Ar -OH 4 -clorofenolo fen p- cloro-idrossibenzene Idrossibenzene Utilizzati nella metà dell’ 800 come deodoranti e disinfettati (soprattutto di fogne), attualmente servono per produrre prevalentemente: • bisfenolo. A ( additivo per plastiche: le rende rigide e resistenti policarbonati). E’ stato scoperto essere dannoso per il feto e fattore di rischio per tumori. • resine fenoliche (la prima è stata la bachelite), • caprolattame (base per la produzione di nylon), • coloranti, farmaci, cosmetici (disinfettano e puliscono la pelle) Composti fenolici si ritrovano anche in natura (in quantità minime, nel vino sono importanti per la colorazione e l’aroma).
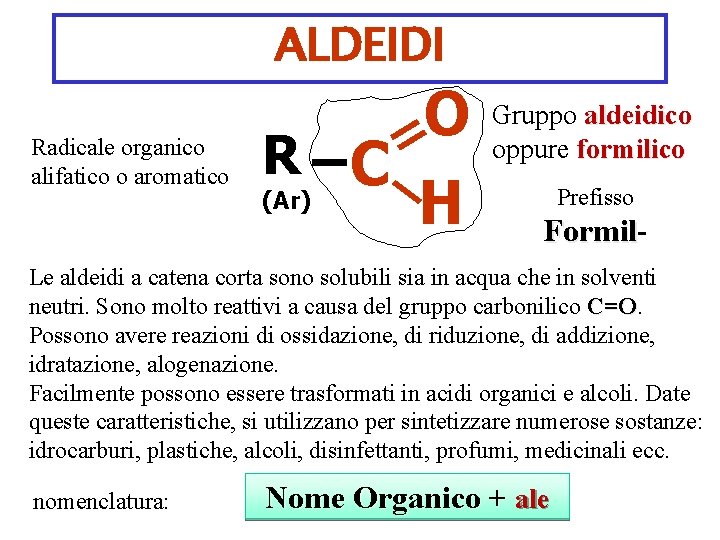
ALDEIDI Radicale organico alifatico o aromatico O R C H (Ar) Gruppo aldeidico oppure formilico Prefisso Formil Le aldeidi a catena corta sono solubili sia in acqua che in solventi neutri. Sono molto reattivi a causa del gruppo carbonilico C=O Possono avere reazioni di ossidazione, di riduzione, di addizione, idratazione, alogenazione. Facilmente possono essere trasformati in acidi organici e alcoli. Date queste caratteristiche, si utilizzano per sintetizzare numerose sostanze: idrocarburi, plastiche, alcoli, disinfettanti, profumi, medicinali ecc. nomenclatura: Nome Organico + ale
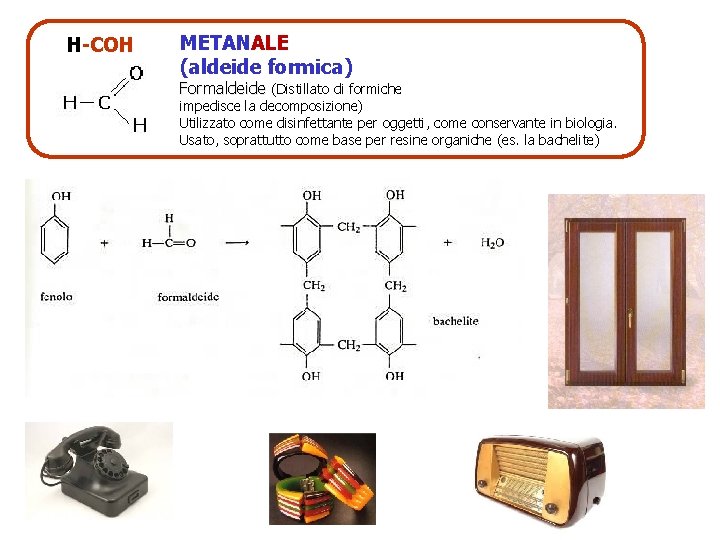
H-COH METANALE (aldeide formica) Formaldeide (Distillato di formiche impedisce la decomposizione) Utilizzato come disinfettante per oggetti, come conservante in biologia. Usato, soprattutto come base per resine organiche (es. la bachelite)
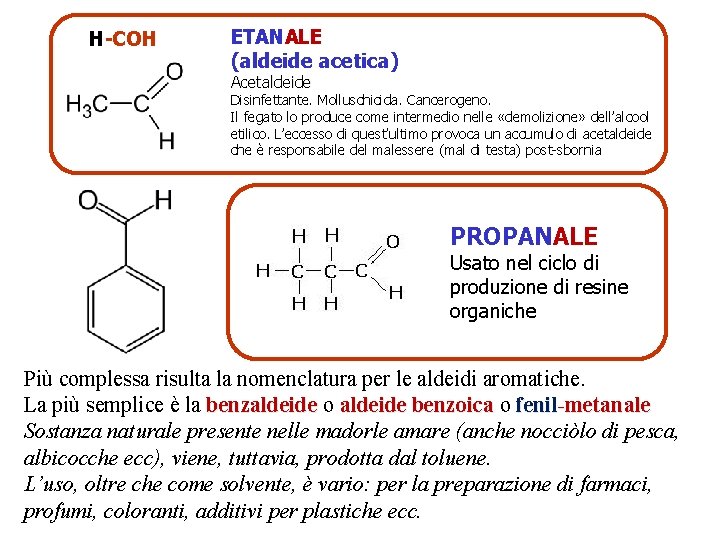
H-COH ETANALE (aldeide acetica) Acetaldeide Disinfettante. Molluschicida. Cancerogeno. Il fegato lo produce come intermedio nelle «demolizione» dell’alcool etilico. L’eccesso di quest’ultimo provoca un accumulo di acetaldeide che è responsabile del malessere (mal di testa) post-sbornia PROPANALE Usato nel ciclo di produzione di resine organiche Più complessa risulta la nomenclatura per le aldeidi aromatiche. La più semplice è la benzaldeide o aldeide benzoica o fenil-metanale Sostanza naturale presente nelle madorle amare (anche nocciòlo di pesca, albicocche ecc), viene, tuttavia, prodotta dal toluene. L’uso, oltre che come solvente, è vario: per la preparazione di farmaci, profumi, coloranti, additivi per plastiche ecc.
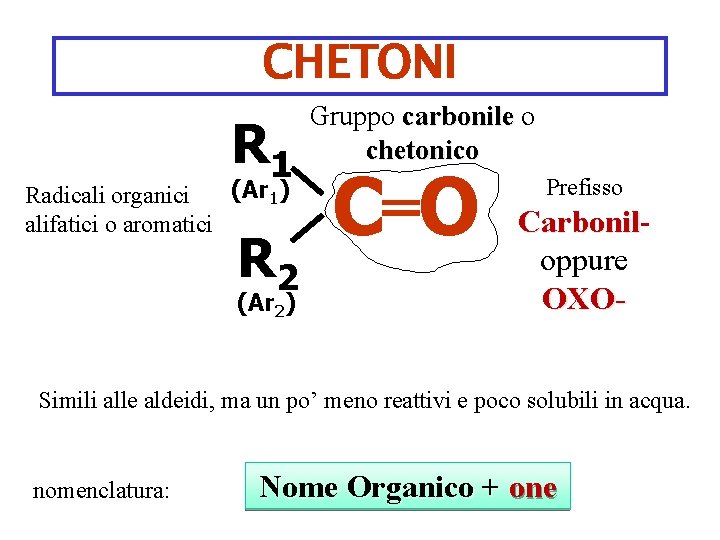
CHETONI R 1 (Ar 1) Radicali organici alifatici o aromatici R 2 (Ar 2) Gruppo carbonile o chetonico C O Prefisso Carbonil oppure OXO- Simili alle aldeidi, ma un po’ meno reattivi e poco solubili in acqua. nomenclatura: Nome Organico + one
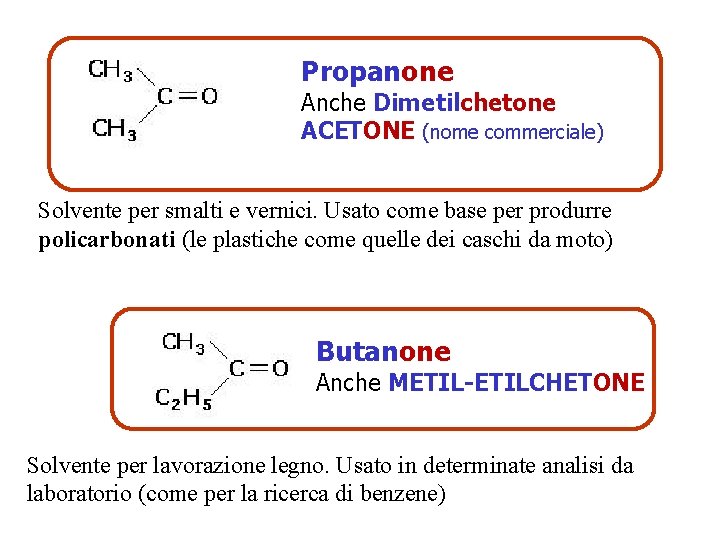
Propanone Anche Dimetilchetone ACETONE (nome commerciale) Solvente per smalti e vernici. Usato come base per produrre policarbonati (le plastiche come quelle dei caschi da moto) Butanone Anche METIL-ETILCHETONE Solvente per lavorazione legno. Usato in determinate analisi da laboratorio (come per la ricerca di benzene)
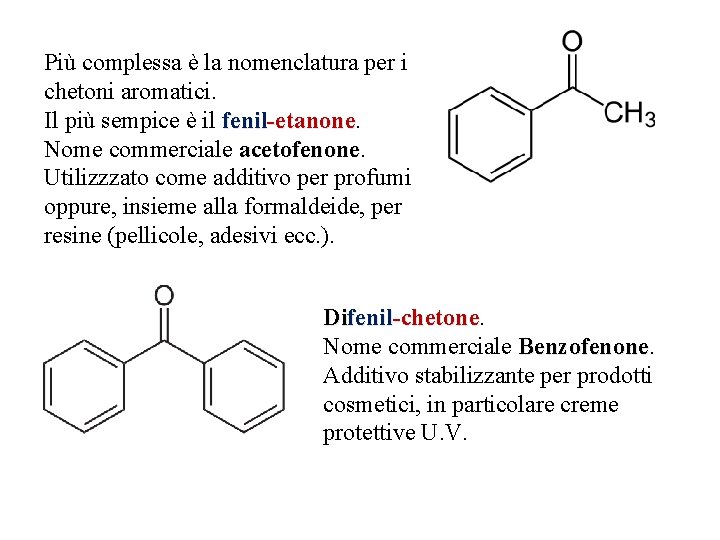
Più complessa è la nomenclatura per i chetoni aromatici. Il più sempice è il fenil-etanone Nome commerciale acetofenone Utilizzzato come additivo per profumi oppure, insieme alla formaldeide, per resine (pellicole, adesivi ecc. ). Difenil-chetone Nome commerciale Benzofenone Additivo stabilizzante per prodotti cosmetici, in particolare creme protettive U. V.

Esercizi 1. a. b. c. Scrivere le formule condensate dei seguenti composti 2 -metil-3 -etilpentanale 2 -cloro-1 -propanolo 3 -metil-2, 4 -pentadiolo 2. Assegnare il nome IUPAC ai seguenti composti a. 3. a. b. c. b. Esistono? 2 -metilbutanale d. 2 -metil-3 -etil-2 -pentanolo 2 -metil-3 -etil-2 -pentanone e. 2, 2, 4 -trimetil-4 -ottanone 2, 2, 4 -trimetil-2 -esanolo f. 2 -metil-2 -butanone 4. Verificare se i seguenti nomi sono corretti secondo la nomenclatura IUPAC. Eventualmente correggerli. a. 2, 2 -dimetilpentanale d. 1 -metil-2 -esanolo b. 4, 4 -dimetil-2 -pentanone e. 3 -metil-4 -etil-2 -pentanolo c. 2, 3 -dimetil-1 -butanolo f. 3 -metil-2 -butanone
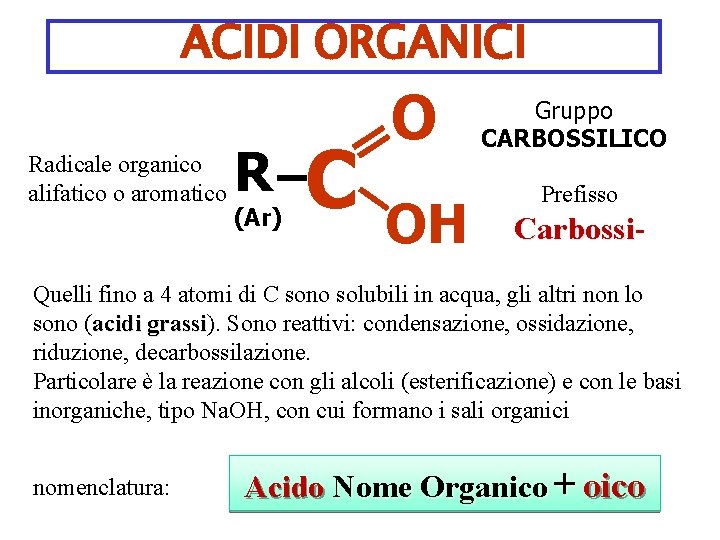
ACIDI ORGANICI Radicale organico alifatico o aromatico R (Ar) C O OH Gruppo CARBOSSILICO Prefisso Carbossi Quelli fino a 4 atomi di C sono solubili in acqua, gli altri non lo sono (acidi grassi). grassi Sono reattivi: condensazione, ossidazione, riduzione, decarbossilazione. Particolare è la reazione con gli alcoli (esterificazione) e con le basi inorganiche, tipo Na. OH, con cui formano i sali organici nomenclatura: Acido Nome Organico + oico
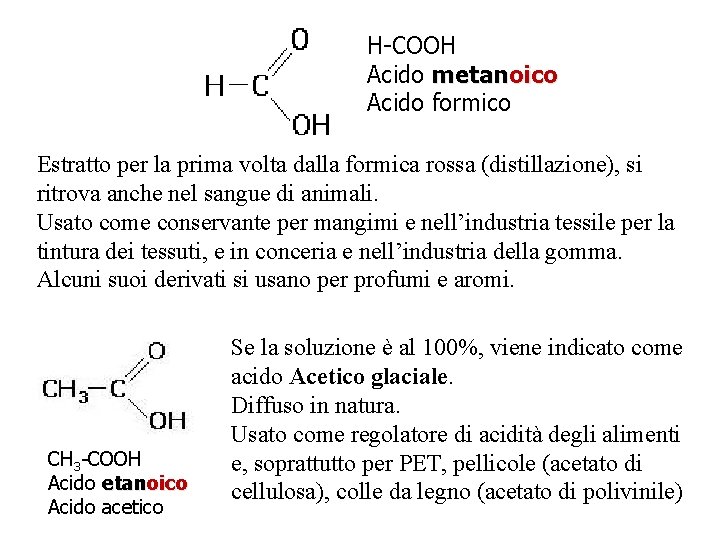
H-COOH Acido metanoico Acido formico Estratto per la prima volta dalla formica rossa (distillazione), si ritrova anche nel sangue di animali. Usato come conservante per mangimi e nell’industria tessile per la tintura dei tessuti, e in conceria e nell’industria della gomma. Alcuni suoi derivati si usano per profumi e aromi. CH 3 -COOH Acido etanoico Acido acetico Se la soluzione è al 100%, viene indicato come acido Acetico glaciale. Diffuso in natura. Usato come regolatore di acidità degli alimenti e, soprattutto per PET, pellicole (acetato di cellulosa), colle da legno (acetato di polivinile)

CH 3 -CH 2 - COOH Acido butirrico Acido butanoico • Presente nel latte animale (scarso in quello umano). La sua concentrazione aumenta nel burro rancido e nei formaggi stagionati. • Importante per l’intestino (meglio se some butirrato di sodio), sia per nutrimento della mucosa, sia perché è anticancerogeno (soprattutto a livello del colon). • I batteri naturali della pelle ne producono in abbondanza dal metabolismo dei grassi del sudore e del sebo: è il responsabile dell’odore caratteristico. Date le sue proprietà antibatterica (pochi ceppi) e antimuffa, viene utilizzato come conservante per alimenti (anche pane) soprattutto come proprionato di calcio, sodio o ammonio. CH 3 -CH 2 -COOH Acido propionico Acido propanoico

CH 3 -CH 2 - COOH Acido butanoico Acido butirrico Presente nel latte animale (scarso in quello umano). La sua concentrazione aumenta nel burro rancido e nei formaggi stagionati. Importante per l’intestino (meglio se some butirrato di sodio), sia per nutrimento della mucosa, sia perché è anticancerogeno (soprattutto a livello del colon). I batteri naturali della pelle ne producono in abbondanza dal metabolismo dei grassi del sudore e del sebo: è il responsabile dell’odore caratteristico. Acido propanoico Acido propionico Ha proprietà antibatteriche e antimuffa. Viene utilizzato come conservante per alimenti (anche pane) soprattutto nella forma salificata di proprionato di calcio, sodio o ammonio.
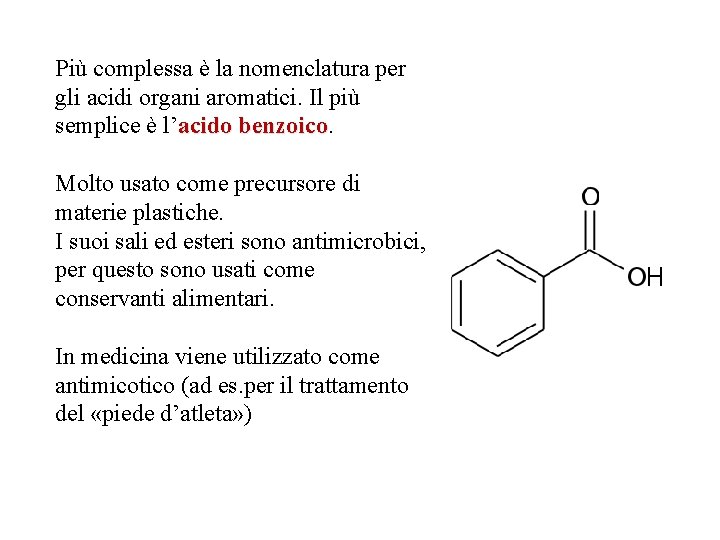
Più complessa è la nomenclatura per gli acidi organi aromatici. Il più semplice è l’acido benzoico Molto usato come precursore di materie plastiche. I suoi sali ed esteri sono antimicrobici, per questo sono usati come conservanti alimentari. In medicina viene utilizzato come antimicotico (ad es. per il trattamento del «piede d’atleta» )

Acidi grassi ACIDI organici con catena alifatica > 4 C Sono la materia prima per i grassi saponificabili: i GLICERIDI ACIDI GRASSI SATURI Presentano solo legami semplici tra i C ACIDI GRASSI INSATURI Presentano uno o più legami doppi, doppi o tripli, tripli lungo la catena di C
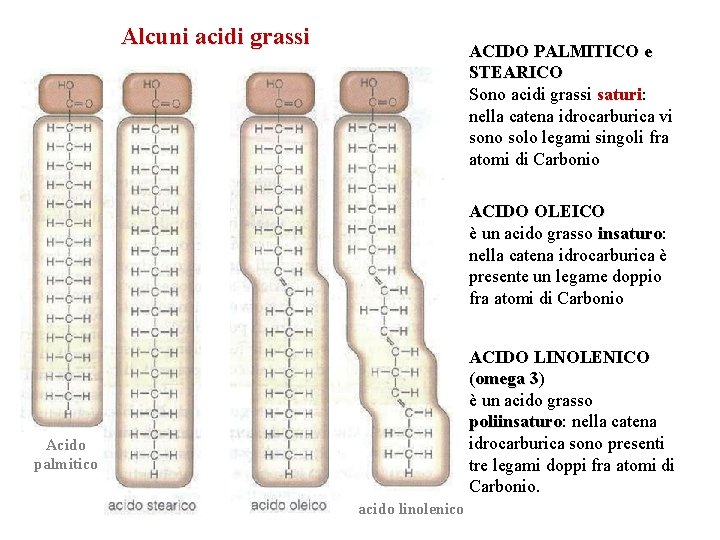
Alcuni acidi grassi ACIDO PALMITICO e STEARICO Sono acidi grassi saturi: saturi nella catena idrocarburica vi sono solo legami singoli fra atomi di Carbonio ACIDO OLEICO è un acido grasso insaturo: insaturo nella catena idrocarburica è presente un legame doppio fra atomi di Carbonio ACIDO LINOLENICO (omega 3) è un acido grasso poliinsaturo: poliinsaturo nella catena idrocarburica sono presenti tre legami doppi fra atomi di Carbonio. Acido palmitico acido linolenico
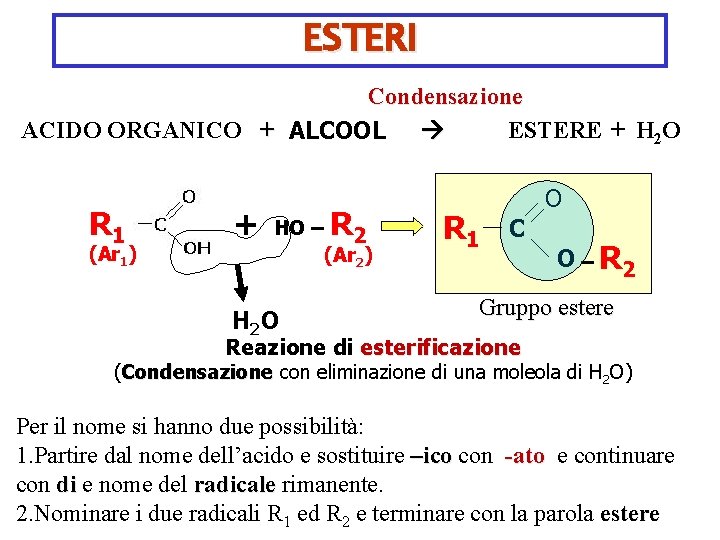
ESTERI Condensazione ACIDO ORGANICO + ALCOOL ESTERE + H 2 O R 1 (Ar 1) + HO – R 2 (Ar 2) H 2 O R 1 O C O – R 2 Gruppo estere Reazione di esterificazione (Condensazione con eliminazione di una moleola di H 2 O) Per il nome si hanno due possibilità: 1. Partire dal nome dell’acido e sostituire –ico con -ato e continuare con di e nome del radicale rimanente. 2. Nominare i due radicali R 1 ed R 2 e terminare con la parola estere
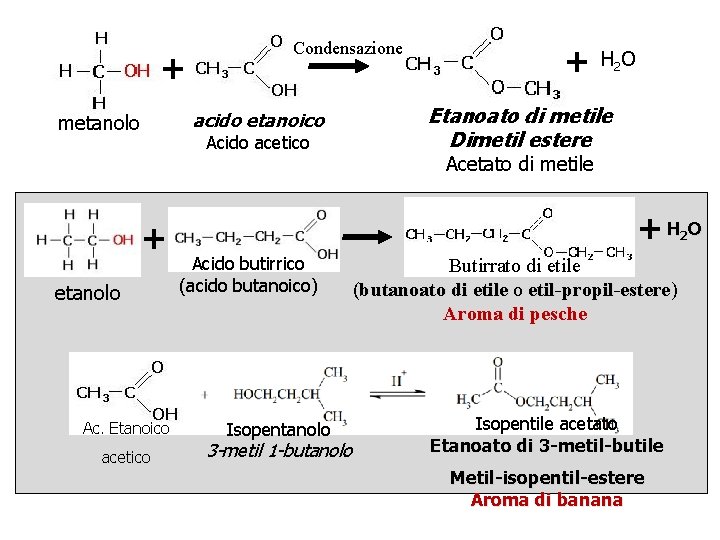
+ Condensazione acido etanoico metanolo Acido acetico + etanolo Ac. Etanoico acetico + H 2 O Etanoato di metile Dimetil estere Acetato di metile +H O 2 Acido butirrico (acido butanoico) Isopentanolo 3 -metil 1 -butanolo Butirrato di etile (butanoato di etile o etil-propil-estere) etil-propil-estere Aroma di pesche Isopentile acetato Etanoato di 3 -metil-butile Metil-isopentil-estere Aroma di banana
![Sali organici In reazione con le BASI INORGANICHE [Na. OH, KOH, Ca(OH)2], gli acidi Sali organici In reazione con le BASI INORGANICHE [Na. OH, KOH, Ca(OH)2], gli acidi](http://slidetodoc.com/presentation_image_h2/320b831f95a493cbb34c23dee3dd5086/image-28.jpg)
Sali organici In reazione con le BASI INORGANICHE [Na. OH, KOH, Ca(OH)2], gli acidi organici formano sali organici + Acido etanoico Acido acetico + Na. OH Idrossido di sodio H 2 O Etanoato di sodio Acetato di sodio Conservante, neutralizzante dell’acido solforico. Scaldamani: viene preparata una soluzione supersatura di acetato e messa in un dischetto. Quando il dischetto si schiaccia, l’acetato cristallizza con reazione esotermica.

SAPONI Se viene utilizzato un acido grasso a catena lunga (10 - 12 atomi di C) in reazione con una base forte, si ottengono i saponi Stearato di sodio (uno dei componenti più comuni del sapone) C 17 H 35 COOH + Na. OH C 17 H 35 COONa + H 2 O Acido stearico (insaturo) Stearato di sodio 3 3 C 17 H 35 CO-O-Na + glicerolo Stearato di sodio Tristearina Estere (Trigliceride: grasso saponificabile)
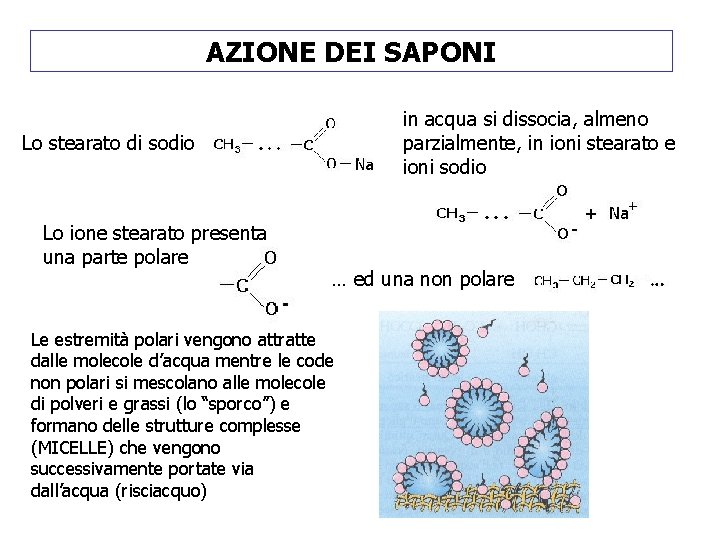
AZIONE DEI SAPONI in acqua si dissocia, almeno parzialmente, in ioni stearato e ioni sodio Lo stearato di sodio Lo ione stearato presenta una parte polare … ed una non polare Le estremità polari vengono attratte dalle molecole d’acqua mentre le code non polari si mescolano alle molecole di polveri e grassi (lo “sporco”) e formano delle strutture complesse (MICELLE) che vengono successivamente portate via dall’acqua (risciacquo)

ETERI Due radicali organici uniti da un atomo di ossigeno Gruppo Etere (Ar 1) (Ar 2) Suffisso intermedio -osso- Si ottengono per condensazione di due alcoli. Il nome si ricava in uno dei due modi seguenti: 1. nominare i radicali alchilici legati al gruppo –O- e terminare con la parola etere 2. interponendo –ossi- tra il prefisso indicante il numero di C del primo radicale e il nome del secondo radicale.
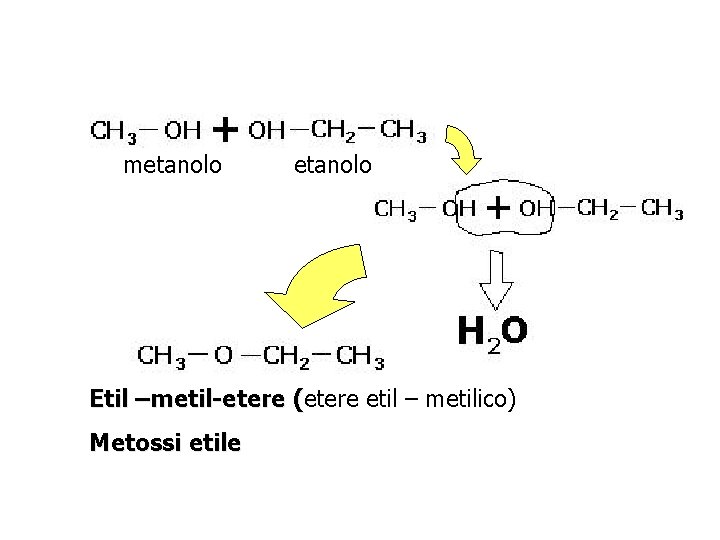
metanolo Etil –metil-etere (etere etil – metilico) ( Metossi etile
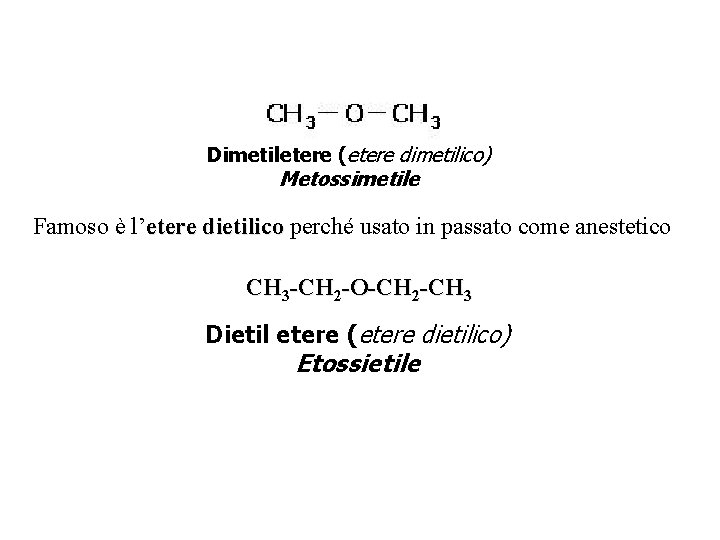
Dimetiletere (etere dimetilico) Metossimetile Famoso è l’etere dietilico perché usato in passato come anestetico CH 3 -CH 2 -O-CH 2 -CH 3 Dietil etere (etere dietilico) Etossietile
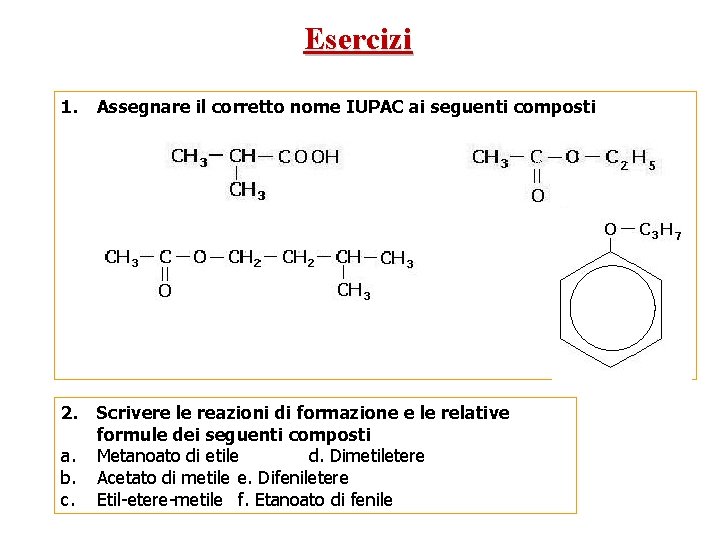
Esercizi 1. Assegnare il corretto nome IUPAC ai seguenti composti a. b. c. 2. Scrivere le reazioni di formazione e le relative formule dei seguenti composti a. Metanoato di etile d. Dimetiletere b. Acetato di metile e. Difeniletere c. Etil-etere-metile f. Etanoato di fenile d.

Acidi- Eteri – Esteriesercizi 2 3. Scrivere le formule di struttura semplificate (condensate) dei seguenti composti a. Acido 2, 2 -dimetilbutanoico b. Etil-butil-etere c. Butanoato di etile d. Acido 2, 3 -diclorobutanoico

Soluzioni degli esercizi Acidi organici - Esteri - Eteri

1. A È un ACIDO (-COOH) 2 -metil Catena principale 3 C (propano) B È un estere: Acido etanoico + alcool etilico Acido 2 -metil-propanoico C È un estere: Acido etanoico + alcool 3 -metil-butilico Etanoato di 3 -metil-butile Etanoato di etile D È un etere: Fenile-O-propile Etere fenilpropilico
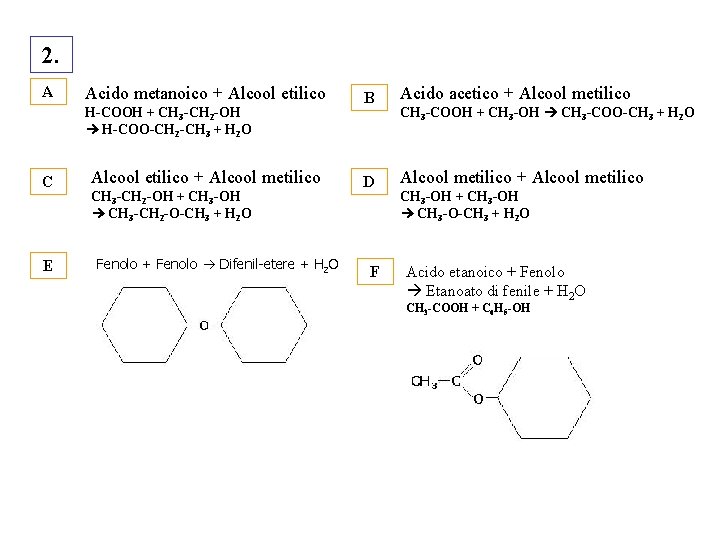
2. A Acido metanoico + Alcool etilico H-COOH + CH 3 -CH 2 -OH H-COO-CH 2 -CH 3 + H 2 O C E Alcool etilico + Alcool metilico CH 3 -CH 2 -OH + CH 3 -OH CH 3 -CH 2 -O-CH 3 + H 2 O Fenolo + Fenolo Difenil-etere + H 2 O B Acido acetico + Alcool metilico D Alcool metilico + Alcool metilico F CH 3 -COOH + CH 3 -OH CH 3 -COO-CH 3 + H 2 O CH 3 -OH + CH 3 -OH CH 3 -O-CH 3 + H 2 O Acido etanoico + Fenolo Etanoato di fenile + H 2 O CH 3 -COOH + C 6 H 5 -OH
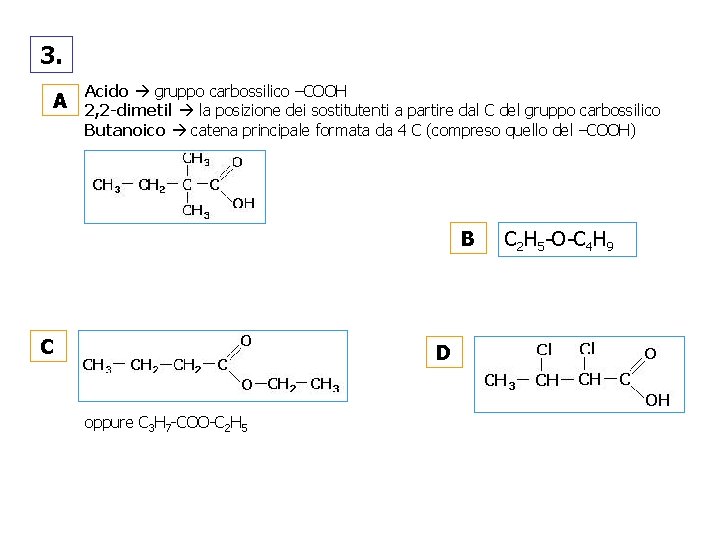
3. A Acido gruppo carbossilico –COOH 2, 2 -dimetil la posizione dei sostitutenti a partire dal C del gruppo carbossilico Butanoico catena principale formata da 4 C (compreso quello del –COOH) B C D oppure C 3 H 7 -COO-C 2 H 5 -O-C 4 H 9

AMMINE Possono essere considerati derivati dall’ammoniaca NH 3 per sostituzione di uno o più H con RADICALI IDROCARBURICI In base al numero di H sostituiti si classificano in AMMINE PRIMARIE, PRIMARIE SECONDARIE, SECONDARIE TERZIARIE Suffisso iniziale e intermedio: ammino-ammino. Il nome si ricava dal radicale alchilico con l’aggiunta di -ammina
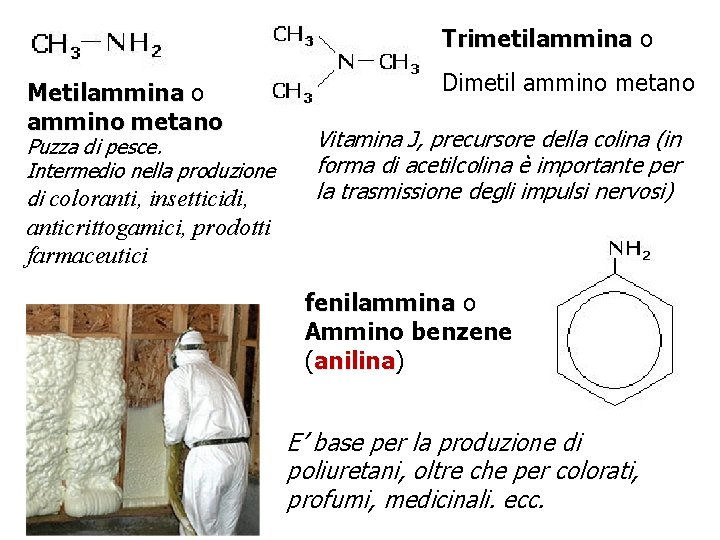
Trimetilammina o Metilammina o ammino metano Puzza di pesce. Intermedio nella produzione di coloranti, insetticidi, Dimetil ammino metano Vitamina J, precursore della colina (in forma di acetilcolina è importante per la trasmissione degli impulsi nervosi) anticrittogamici, prodotti farmaceutici fenilammina o Ammino benzene (anilina) anilina E’ base per la produzione di poliuretani, oltre che per colorati, profumi, medicinali. ecc.

AMMINOACIDI Come si evince dal nome, contengono un gruppo AMMINICO -NH 2 e un gruppo CARBOSSILICO -COOH FORMULA DI STRUTTURA GENERALE DI UN AMMINOACIDO RADICALE caratterizza l’amminoacido specifico Gruppo AMMINO (basico) Gruppo CARBOSSILICO (acido)
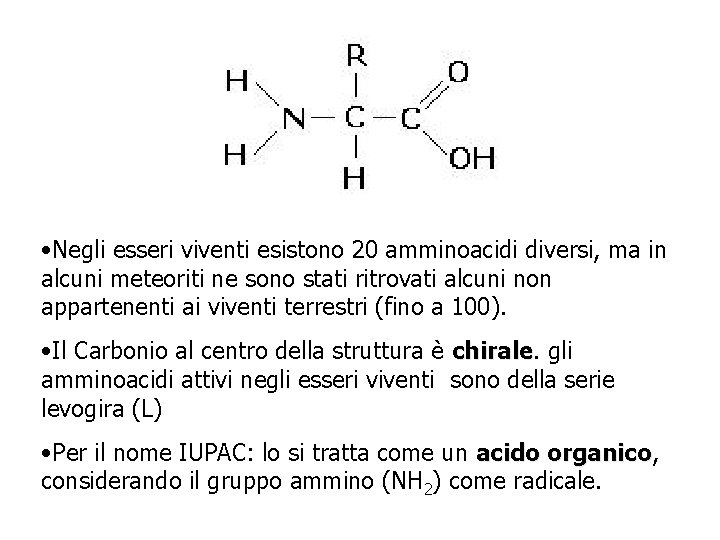
• Negli esseri viventi esistono 20 amminoacidi diversi, ma in alcuni meteoriti ne sono stati ritrovati alcuni non appartenenti ai viventi terrestri (fino a 100). • Il Carbonio al centro della struttura è chirale gli amminoacidi attivi negli esseri viventi sono della serie levogira (L) • Per il nome IUPAC: lo si tratta come un acido organico, organico considerando il gruppo ammino (NH 2) come radicale.
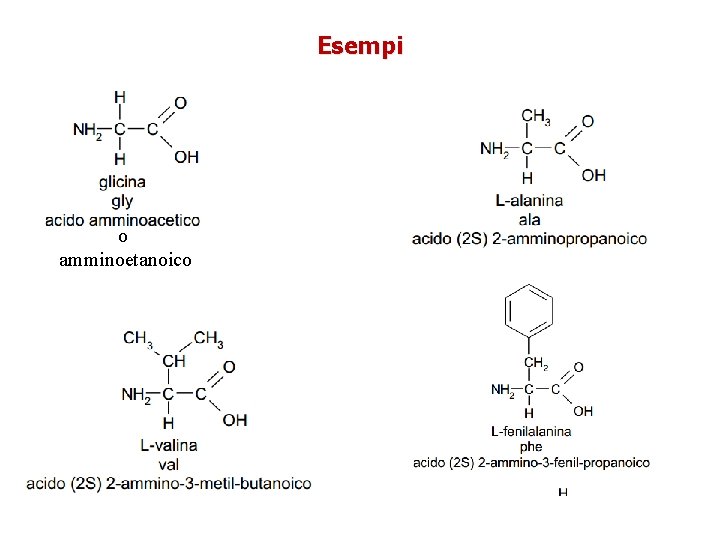
Esempi o amminoetanoico
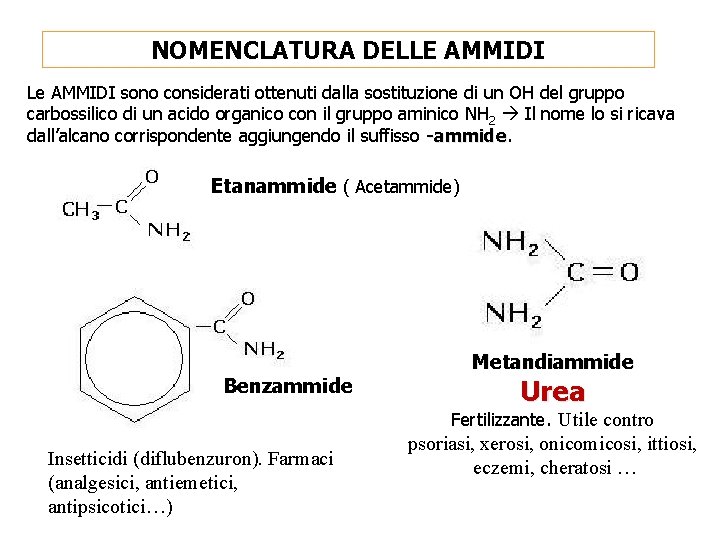
NOMENCLATURA DELLE AMMIDI Le AMMIDI sono considerati ottenuti dalla sostituzione di un OH del gruppo carbossilico di un acido organico con il gruppo aminico NH 2 Il nome lo si ricava dall’alcano corrispondente aggiungendo il suffisso -ammide Etanammide ( Acetammide) Benzammide Metandiammide Urea Fertilizzante. Utile contro Insetticidi (diflubenzuron). Farmaci (analgesici, antiemetici, antipsicotici…) psoriasi, xerosi, onicomicosi, ittiosi, eczemi, cheratosi …
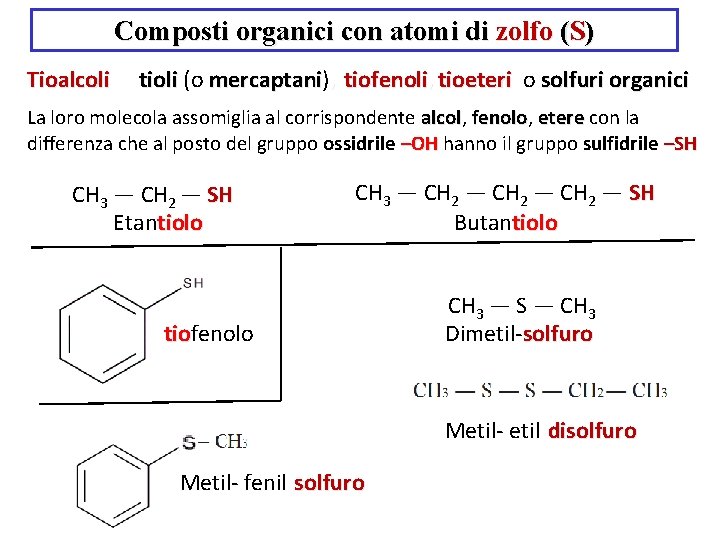
Composti organici con atomi di zolfo (S) Tioalcoli (o tioli (o mercaptani) mercaptani , tiofenoli, tioeteri (o solfuri organici) La loro molecola assomiglia al corrispondente alcol, alcol fenolo, fenolo etere con la differenza che al posto del gruppo ossidrile –OH hanno il gruppo sulfidrile –SH CH 3 ― CH 2 ― SH Etantiolo CH 3 ― CH 2 ― SH Butantiolo tiofenolo tio CH 3 ― S ― CH 3 Dimetil-solfuro Metil-disolfuro Metil- fenil-solfuro

Composti organici polifunzionali Moltissimi composti organici hanno più gruppi funzionali In caso di gruppi alcolici, alcolici aldeidici, aldeidici chetonici e acidi è possibile usare, in sequenza, gli specifici suffissi preceduti dal numero di posizione. Esan-2, 5 diolo-3 one E’ più frequente, invece, considerare un gruppo (a scelta) come principale, principale da cui prendere il suffisso, e trattare gli altri gruppi funzionali come radicali (utilizzando i relativi prefissi). prefissi

I prefissi più comuni per i radicali - OH (alcolico) idrossi- = O (chetonico) chetonico oxo- - CHO (aldeidico) formil- COOH (acido) carbossi- - O - (etere) -ossi- - NHx -ammino- - NO 2 nitro- - SH sulfidril-
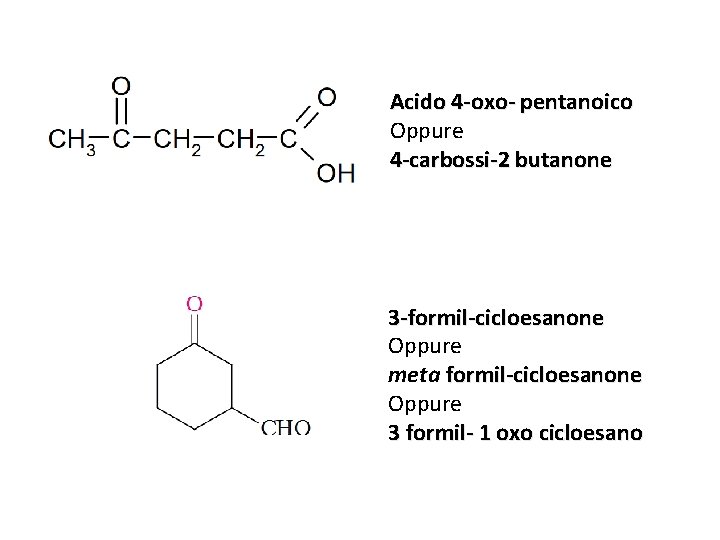
Acido 4 -oxo- pentanoico Oppure 4 -carbossi-2 butanone 3 -formil-cicloesanone Oppure meta formil-cicloesanone Oppure 3 formil- 1 oxo cicloesano
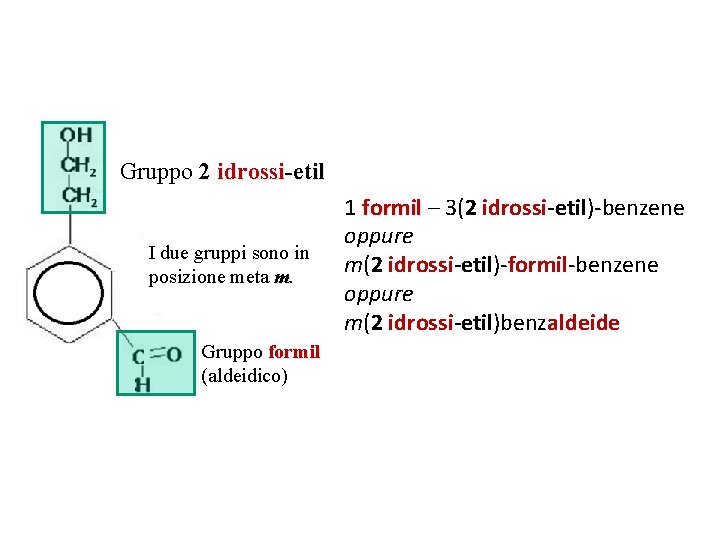
Gruppo 2 idrossi-etil I due gruppi sono in posizione meta m. Gruppo formil (aldeidico) 1 formil – 3(2 idrossi-etil)-benzene oppure m(2 idrossi-etil)-formil-benzene oppure m(2 idrossi-etil)benzaldeide

In caso di esteri o eteri, conviene mantenere il nome della classe più complessa e trattare gli altri gruppi funzionali come radicali. idrossi 2 idrossi butanoato di etile Oppure 1 idrossi propil-etil-estere 1 idrossi propiletil 1 idrossi propil-etere

Raffaele Moscagiuri – ISISS «A. Scarpa» – Motta di Livenza (TV) - 2017
- Slides: 52