I cz W jaki sposb mona opisa budow

(I cz. ) W jaki sposób można opisać budowę cząsteczki? Wartościowość pierwiastka Wzory strukturalne i sumaryczne

Wartościowość pierwiastka v Atomy pierwiastków dążąc do osiągnięcia trwałej konfiguracji elektronowej (dubletu lub oktetu elektronowego – konfiguracji najbliższego sobie helowca) łączą się w cząsteczki za pomocą wiązań: Ø atomowe (kowalencyjne), kowalencyjne spolaryzowanie – przez uwspólnienie pary lub par elektronowych Ø jonowe – przekształcają się w jony: ü kationy - oddając elektrony walencyjne ü aniony – przyjmując elektrony na powłokę walencyjną v Liczba wiązań jest cechą charakterystyczną dla danego pierwiastka i jest zależna od liczby elektronów walencyjnych.

Wartościowość pierwiastka (cd) v. Przykłady: cząsteczki homoatomowe Ø H 2 H – H (wiązanie pojedyncze) Ø F 2 F – F (wiązanie pojedyncze) Ø Cl 2 Cl – Cl (wiązanie pojedyncze) Ø Br 2 Br – Br (wiązanie pojedyncze) Ø O 2 O = O (wiązanie podwójne) Ø S 2 S = S (wiązanie podwójne) Ø N 2 N ≡ N (wiązanie potrójne) Ø P 2 P ≡ P (wiązanie potrójne)
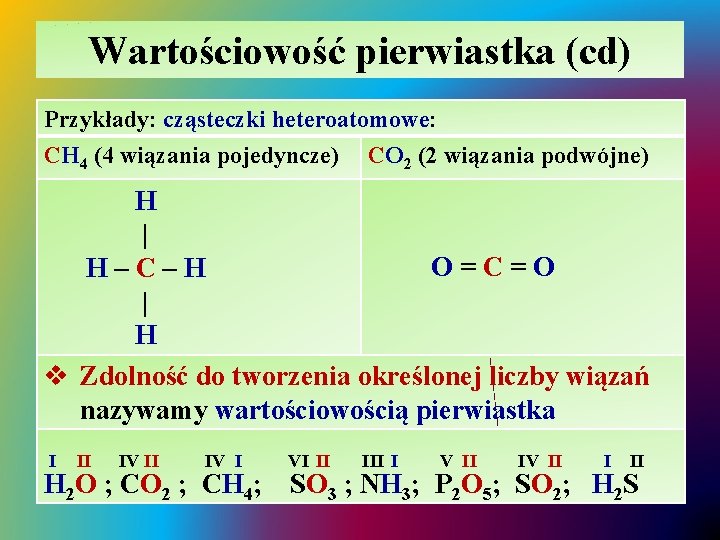
Wartościowość pierwiastka (cd) Przykłady: cząsteczki heteroatomowe: CH 4 (4 wiązania pojedyncze) CO 2 (2 wiązania podwójne) H | O=C=O H–C–H | H v Zdolność do tworzenia określonej liczby wiązań nazywamy wartościowością pierwiastka I II IV I H 2 O ; CO 2 ; CH 4; VI II I V II I II SO 3 ; NH 3; P 2 O 5; SO 2; H 2 S
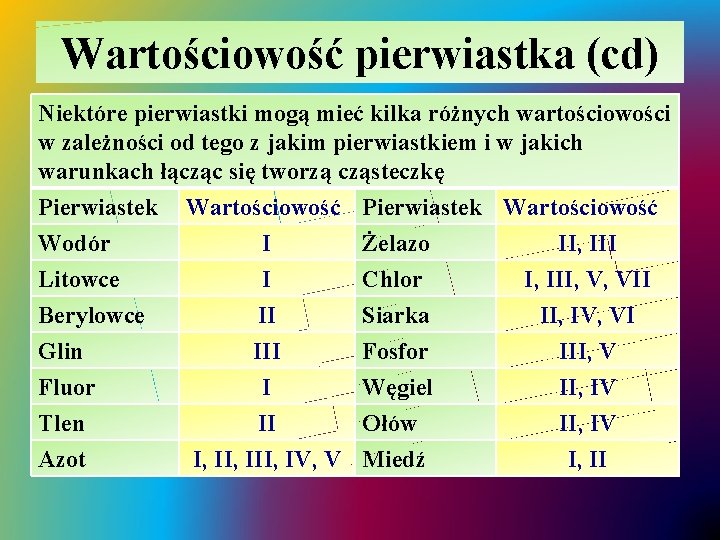
Wartościowość pierwiastka (cd) Niektóre pierwiastki mogą mieć kilka różnych wartościowości w zależności od tego z jakim pierwiastkiem i w jakich warunkach łącząc się tworzą cząsteczkę Pierwiastek Wartościowość Wodór I Żelazo II, III Litowce I Chlor I, III, V, VII Berylowce II Siarka II, IV, VI Glin III Fosfor III, V Fluor I Węgiel II, IV Tlen II Ołów II, IV Azot I, III, IV, V Miedź I, II

Cząsteczki – molekuły v. Atomy pierwiastków połączone wiązaniami kowalencyjnymi lub kowalencyjnymi spolaryzowanymi stanowią cząsteczkę (molekułę): Cząsteczka homoatomowa złożona z atomów tego samego pierwiastka: (H 2, N 2, S 8, C 60, O 2, Cl 2, Br 2, F 2, I 2) Cząsteczka heteroatomowa złożona jest z atomów przynajmniej dwóch różnych pierwiastków: (H 2 O, HCl, CO 2, CH 4, C 2 H 6, H 2 S, SO 3, N 2 O 5, HNO 3, NH 3, H 2 SO 4)

Wzór sumaryczny i strukturalny (elektronowy) kreskowy Wzór sumaryczny Określa rodzaj i liczbę atomów tworzących cząsteczkę H 2 SO 4 Ø 2 atomy wodoru (H), 1 atom siarki (S), 4 atomy tlenu (O) Wzór strukturalny – kreskowy Określa rodzaj i liczbę atomów w cząsteczce oraz pokazuje wiązania pomiędzy poszczególnymi atomami (sposób powiązania między atomami) H–O O S H–O O

Indeks i współczynnik stechiometryczny v Indeks – (O 2) cyfra zapisania po prawej stronie symbolu pierwiastka informuje o liczbie atomów w pierwiastka w cząsteczce (indeksu w wartości 1 nie zapisuje się) v Współczynnik stechiometryczny – (2 HCl) cyfra/liczba zapisania przed wzorem sumarycznym cząsteczki określa liczbę cząsteczek (współczynnika o wartości 1 nie zapisuje się) v Przykłady: Ø 5 N 2 – pięć cząsteczek dwuatomowych azotu (10 at. N) Ø 3 HNO 3 – trzy cząsteczki kwasu azotowego(V) na które składają się: ü 3 ∙ 1 at. H = 3 atomy wodoru; ü 3 ∙ 1 at. N = 3 atomy azotu ü 3 ∙ 3 at. O = 9 atomów tlenu
- Slides: 8