I Congresso Brasileiro sobre Uso Racional de Medicamentos

I Congresso Brasileiro sobre Uso Racional de Medicamentos Regulamento Técnico de Farmácia Hospitalar Flávia Freitas de Paula Lopes Gerente Geral de Tecnologia em Serviços de Saúde Agência Nacional de Vigilância Sanitária www. anvisa. gov. br

DESAFIO: O UNIVERSO População 183. 702. 696 habitantes Fonte: IBGE Maio/2005 Cadastro Nacional de Estabelecimentos de Saúde – CNES 101. 747 Fonte: CNES Maio/2005 Agência Nacional de Vigilância Sanitária www. anvisa. gov. br
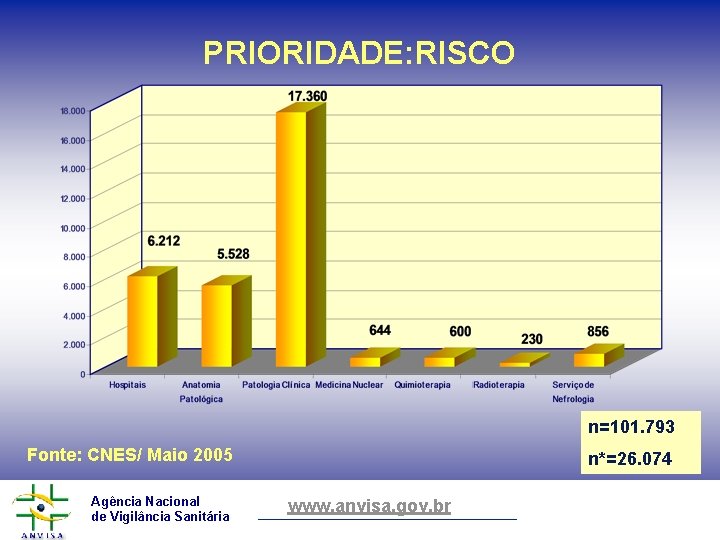
PRIORIDADE: RISCO n=101. 793 Fonte: CNES/ Maio 2005 Agência Nacional de Vigilância Sanitária n*=26. 074 www. anvisa. gov. br

? A ocorrência de Surtos e Eventos Adversos associados a atenção à saúde PROBLEMA Agência Nacional de Vigilância Sanitária www. anvisa. gov. br

Ø Estudos da década de 50 e 60 já apresentavam relatos de eventos adversos Ø Diferentes Conceitos: “Complicações indesejadas decorrentes dos cuidados prestados ao paciente, não atribuídas à evolução natural da doença de base” (Gallotti, 2004) Ø Estima-se que 50 a 60% são evitáveis Risco X Eventos Adversos Agência Nacional de Vigilância Sanitária www. anvisa. gov. br

Estudos de Harvard / 1991 Ø 4% pacientes sofrem algum tipo de dano no Hospital Ø 70% dos eventos adversos provocam uma incapacidade temporal Ø 14% dos incidentes são mortais Fonte: World Alliance for Patient Safety : forward programme. World Health Organization 2004, apud: Harvard Medical Practice Study in 1991 ( 1, 2). MAGNITUDE DOS EVENTOS ADVERSOS Agência Nacional de Vigilância Sanitária www. anvisa. gov. br

Instituto de Medicina / 1999 Ø Os “erros médicos” causam entre 44. 000 e 98. 000 disfunções a cada ano nos hospitais dos Estados Unidos Fonte: To err is human: building a safer health system by the Institute of Medicine, 1999. USA MAGNITUDE DOS EVENTOS ADVERSOS Agência Nacional de Vigilância Sanitária www. anvisa. gov. br

Ø Em 1999, nos EUA, o informe do Committee on Quality of Health Care in America destacou que os erros de medicação ocasionam mais de 7. 000 mortes por ano, que no âmbito hospitalar motivam eventos adversos em 2% dos pacientes, e no nível ambulatorial esses eventos, derivados de erros, provavelmente são mais numerosos. Fonte: Erros de medicação: importante problema de saúde pública Tânia Azevedo Anacleto e Mário Borges Rosa Erros de medicação Agência Nacional de Vigilância Sanitária www. anvisa. gov. br

Grupo de Trabalho Hospitalar/2000 sobre a Qualidade da Atenção ØUm a cada dez pacientes dos hospitais europeus sofrem danos evitáveis e efeitos adversos ocasionados por cuidados recebidos. Fonte: World Alliance for Patient Safety : forward programme. World Health Organization 2004, apud: Standing Committee of the Hospitals of the EU. The quality of health care/hospital activities: Report by the Working Party on quality care in hospitals of the subcommittee on coordination. September 2000. MAGNITUDE DOS EVENTOS ADVERSOS Agência Nacional de Vigilância Sanitária www. anvisa. gov. br

Produtos X Realidade Agência Nacional de Vigilância Sanitária www. anvisa. gov. br

• Medicamentos • Saneantes • Produtos de higiene • Kits diagnósticos • Outros produtos Farmácia Hospitalar Agência Nacional de Vigilância Sanitária www. anvisa. gov. br
Serviços de Saúde USO Prescrição Farmácia Hospitalar X Processo Agência Nacional de Vigilância Sanitária www. anvisa. gov. br

Ø Amostra de 250 hospitais (> 20 leitos e diferentes complexidades) Ø Realização do NAF/ENSP, OPAS e financiamento do MS Ø Resultados (OSÓRIO DE CASTRO, Cláudia (org. ), 2004) ü 25% das farmácias hospitalares pesquisadas não tem farmacêutico ü 84, 4% não realizam programação de medicamentos ü 88, 4% não realizam atividades de informação ü 71, 6% não realizam programação ü 57% da manipulação de não estéreis não atendem a legislação Diagnóstico da Farmácia Hospitalar Agência Nacional de Vigilância Sanitária www. anvisa. gov. br
Acesso Uso Racional Qualidade Efetividade Agência Nacional de Vigilância Sanitária www. anvisa. gov. br
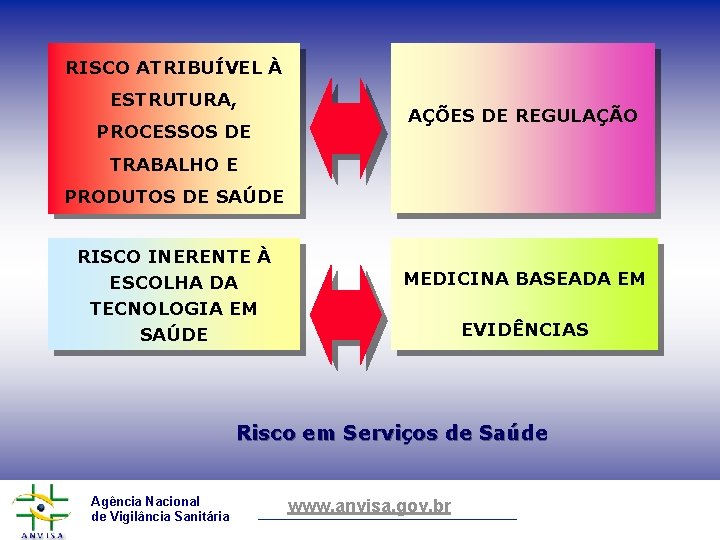
RISCO ATRIBUÍVEL À ESTRUTURA, PROCESSOS DE AÇÕES DE REGULAÇÃO TRABALHO E PRODUTOS DE SAÚDE RISCO INERENTE À ESCOLHA DA TECNOLOGIA EM SAÚDE MEDICINA BASEADA EM EVIDÊNCIAS Risco em Serviços de Saúde Agência Nacional de Vigilância Sanitária www. anvisa. gov. br
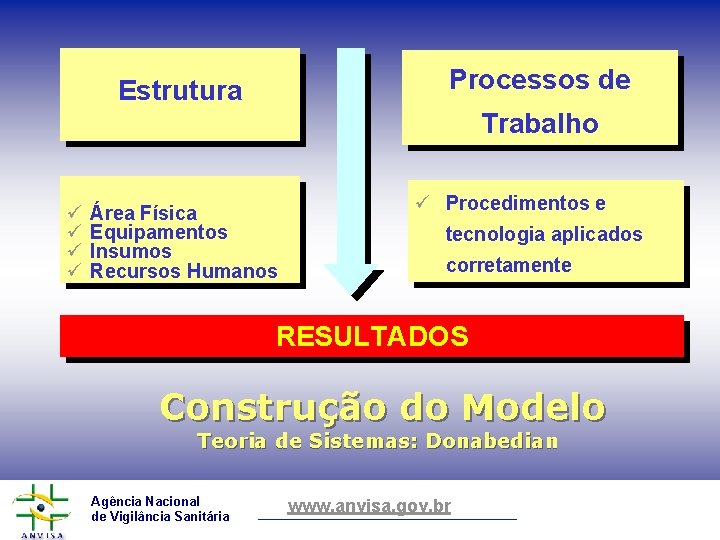
Processos de Estrutura Trabalho ü ü Área Física Equipamentos Insumos Recursos Humanos ü Procedimentos e tecnologia aplicados corretamente RESULTADOS Construção do Modelo Teoria de Sistemas: Donabedian Agência Nacional de Vigilância Sanitária www. anvisa. gov. br
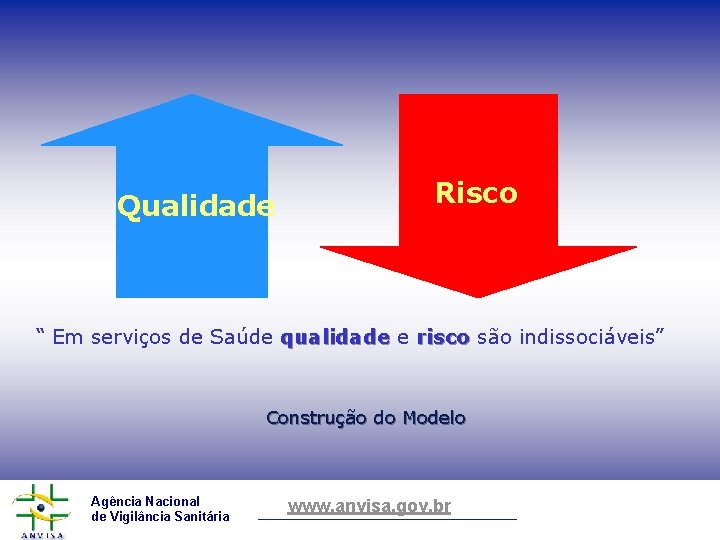
Qualidade Risco “ Em serviços de Saúde qualidade risco são indissociáveis” risco Construção do Modelo Agência Nacional de Vigilância Sanitária www. anvisa. gov. br

Risco Associado a Medicamentos e Produtos para saúde üPaciente/cliente üTrabalhador üMeio Ambiente Agência Nacional de Vigilância Sanitária www. anvisa. gov. br

REGULAÇÃO Objetivos § Prevenção e minimização de risco aos usuários, trabalhadores e meio ambiente § Racionalização de uso Vantagens § Segurança para usuários, trabalhadores e meio ambiente § Uso de processos e métodos aperfeiçoados § Redução de custos § Facilidade de interpretação e de comunicação § Melhoria da qualidade Agência Nacional de Vigilância Sanitária www. anvisa. gov. br

ü Padrão Ouro X Padrão Mínimo ü Foco nos processos de trabalho ü Diferenças regionais, complexidade dos processos e risco ü Serviços na Ilegalidade Regulamentação Agência Nacional de Vigilância Sanitária www. anvisa. gov. br
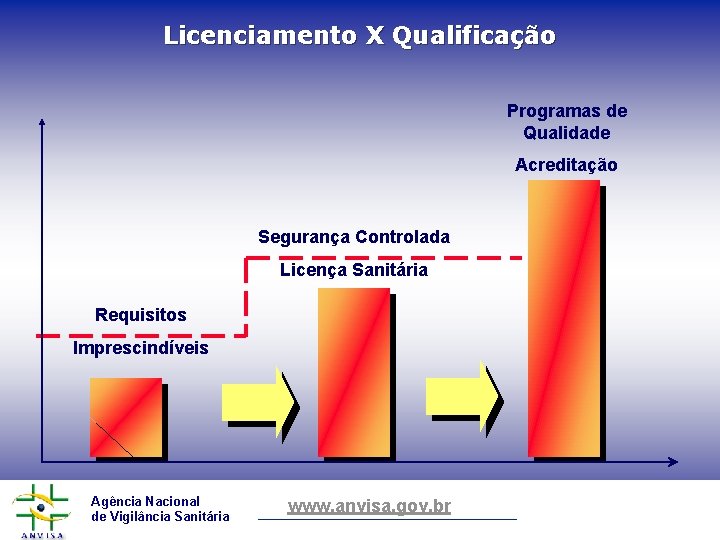
Licenciamento X Qualificação Programas de Qualidade Acreditação Segurança Controlada Licença Sanitária Requisitos Imprescindíveis Agência Nacional de Vigilância Sanitária www. anvisa. gov. br

Prevenir eventos adversos associados à utilização de medicamentos e produtos Agência Nacional de Vigilância Sanitária www. anvisa. gov. br

PORTARIA Nº 559, DE 10 DE SETEMBRO DE 2004. Art. 1° Instituir Grupo de Trabalho, integrado por representantes das áreas e instituições abaixo relacionadas: • • • Agência Nacional de Vigilância Sanitária – ANVISA/MS SAS / SCTIE / MS Organização Panamericana de Saúde - OPAS/OMS Fundação Oswaldo Cruz - FIOCRUZ - Núcleo de Assistência Farmacêutica (NAF) Sociedade Brasileira de Farmacêuticos em Oncologia - SOBRAFO Sociedade Brasileira de Farmácia Hospitalar - SBRAFH Hospital de Clínicas de Curitiba - Universidade Federal do Paraná Instituto da Criança - FMUSP - SP Vigilância Sanitária Estadual Agência Nacional de Vigilância Sanitária www. anvisa. gov. br

PORTARIA Nº 559, DE 10 DE SETEMBRO DE 2004. Art. 2º Conferir ao Grupo de Trabalho atribuição para: Elaborar proposta de Regulamento Técnico sobre as Boas Práticas para o Gerenciamento de Medicamentos e Produtos em Serviços de Saúde. Agência Nacional de Vigilância Sanitária www. anvisa. gov. br
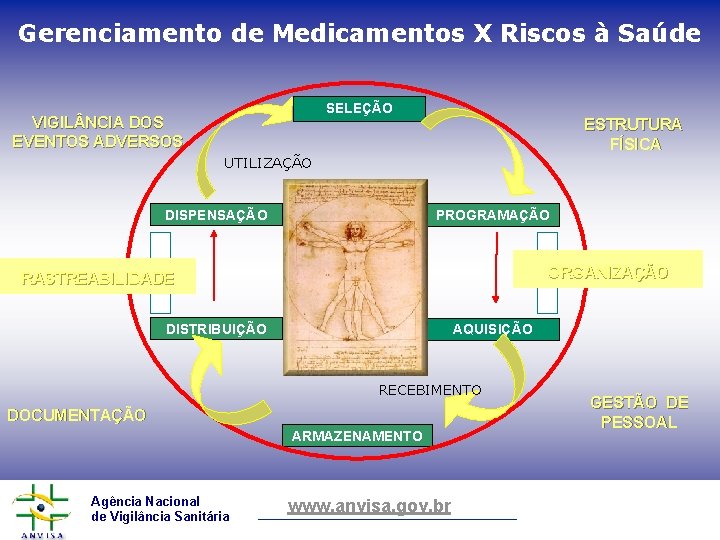
Gerenciamento de Medicamentos X Riscos à Saúde SELEÇÃO VIGIL NCIA DOS EVENTOS ADVERSOS ESTRUTURA FÍSICA UTILIZAÇÃO DISPENSAÇÃO PROGRAMAÇÃO PR OD UÇ ÃO PRE SCR IÇÃ O ORGANIZAÇÃO RASTREABILIDADE DISTRIBUIÇÃO AQUISIÇÃO RECEBIMENTO DOCUMENTAÇÃO ARMAZENAMENTO Agência Nacional de Vigilância Sanitária www. anvisa. gov. br GESTÃO DE PESSOAL

Regulamento Técnico Considerações Gerais Ø Independente do tema da Resolução, o enfoque deve ser o risco que a atividade ou o produto acarreta à população Ø Deve prever os requisitos mínimos necessários para a redução máxima possível de riscos Ø Deve ser clara e objetiva, evitando-se desta forma interpretações diversas Agência Nacional de Vigilância Sanitária www. anvisa. gov. br

Conteúdo Técnico Ø Definição de Requisitos ü Aquisição; ü Recebimento; ü Armazenamento e conservação; ü Manipulação; ü Distribuição; ü Dispensação; ü Registros e Rastreabilidade ü Vigilância de Eventos Adversos. Agência Nacional de Vigilância Sanitária www. anvisa. gov. br

Melhoria da Qualidade Ø Padronização de medicamentos, germicidas e produtos para saúde Ø Promover o uso seguro e racional de medicamentos e produtos para saúde; Ø Controle de Infecções hospitalares Ø Controle da resistência microbiana Ø Redução de gastos Ø Sistema racional medicamentos; de estocagem de Ø Dar suporte às unidades de apoio diagnóstico e terapia; Agência Nacional de Vigilância Sanitária www. anvisa. gov. br

Próximos Passos a) Finalização do documento após consenso b) Apreciação das propostas do GT pela Diretoria Colegiada da ANVISA; d) Consulta pública – previsão e) Avaliação das contribuições f) Apreciação do documento final pela Diretoria Colegiada g) Publicação na forma de Resolução - RDC Agência Nacional de Vigilância Sanitária www. anvisa. gov. br

Agência Nacional de Vigilância Sanitária www. anvisa. gov. br GGTES (61) 34481258 ggtes@anvisa. gov. br Agência Nacional de Vigilância Sanitária www. anvisa. gov. br
- Slides: 30