HYPOGLYCMIANTS ORAUX METFORMIN OU GLYBURIDE EN COMPARAISON LINSULINE

HYPOGLYCÉMIANTS ORAUX (METFORMIN OU GLYBURIDE) EN COMPARAISON À L’INSULINE DANS LE TRAITEMENT DU DIABÈTE GESTATIONNEL LEYLA GAFAROVA ET CHLOÉ-ALEXANDRA SAWAN RÉSIDENTES 1 EN MÉDECINE DE FAMILLE UMF BORDEAUX-CARTIERVILLE mai 2019

Introduction ● Le diabète est la maladie métabolique la plus fréquemment rencontrée chez les femmes enceintes. ● La prévalence du diabète gestationnel varie entre 3 -20% chez les femmes enceintes au Canada. ● 30% des femmes enceintes atteintes du diabète gestationnel vont nécessiter un traitement afin d’atteindre un état de normoglycémie durant leur grossesse.

Introduction ● Mère: risque d’hypertension gestationnelle, de prééclampsie, de trauma obstétrical, dév diabète de type 2 dans le futur (maladies cardiovasculaires +) ● Les nouveaux-nés: risque de macrosomie, de dystocie des épaules, de césariennes d’urgence, des accouchements instrumentés, de détresse respiratoire, de complications métaboliques (hyperbilirubinémie, hypocalcémie, polycythémie) et d’admission aux soins intensifs néonataux.

Traitement 1 er ligne actuel : Insuline ● ● ● risque d’hypoglycémie prise de multiple fois par jour calcul de la dose / ajustement de dose réaction site d’injection gain de poids

Chez les femmes enceintes atteintes de diabète gestationnel, l’utilisation d’un HGO (metformin ou glyburide) permet-elle d’atteindre les mêmes cibles glycémiques tout en offrant une innocuité meilleure ou semblable à l’insuline?

PICO P : Femmes atteintes d’un diabète gestationnel I : Hypoglycémiants oraux (Metformin ou Glyburide) C : Insuline O : Efficacité, effets indésirables maternels, néonataux et périnataux, innocuité
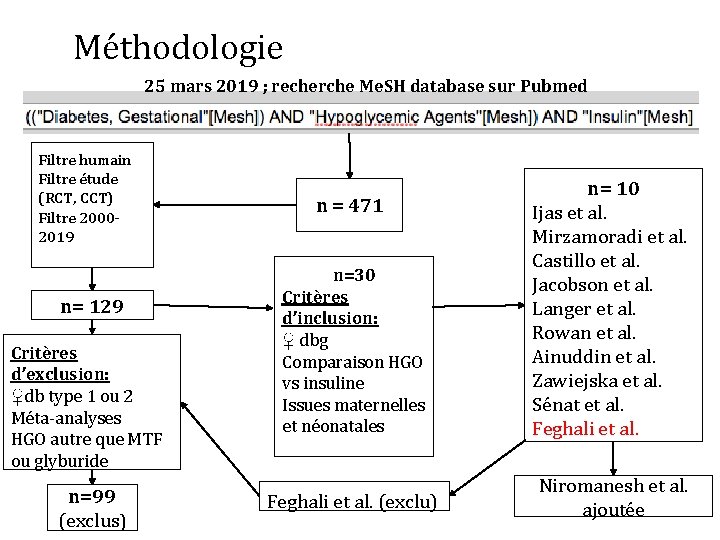
Méthodologie 25 mars 2019 ; recherche Me. SH database sur Pubmed Filtre humain Filtre étude (RCT, CCT) Filtre 20002019 n= 129 Critères d’exclusion: ♀db type 1 ou 2 Méta-analyses HGO autre que MTF ou glyburide n=99 (exclus) n=30 Critères d’inclusion: ♀ dbg Comparaison HGO vs insuline Issues maternelles et néonatales n= 10 Ijas et al. Mirzamoradi et al. Castillo et al. Jacobson et al. Langer et al. Rowan et al. Ainuddin et al. Zawiejska et al. Sénat et al. Feghali et al. (exclu) Niromanesh et al. ajoutée n = 471
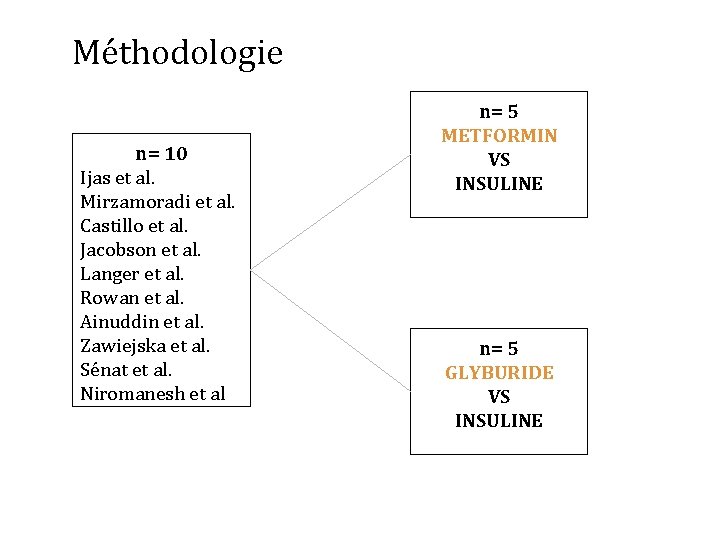
Méthodologie n= 10 Ijas et al. Mirzamoradi et al. Castillo et al. Jacobson et al. Langer et al. Rowan et al. Ainuddin et al. Zawiejska et al. Sénat et al. Niromanesh et al n= 5 METFORMIN VS INSULINE n= 5 GLYBURIDE VS INSULINE
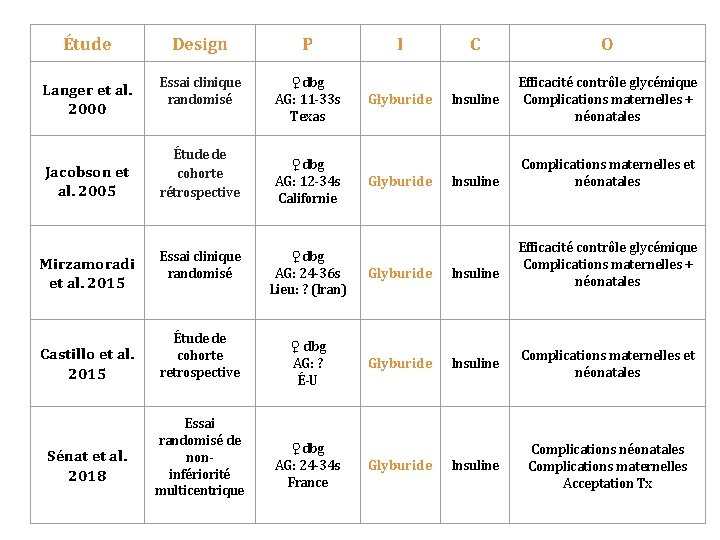
Étude Design P Langer et al. 2000 Essai clinique randomisé ♀dbg AG: 11 -33 s Texas Jacobson et al. 2005 Mirzamoradi et al. 2015 Castillo et al. 2015 Sénat et al. 2018 Étude de cohorte rétrospective Essai clinique randomisé Étude de cohorte retrospective Essai randomisé de noninfériorité multicentrique ♀dbg AG: 12 -34 s Californie I Glyburide C O Insuline Efficacité contrôle glycémique Complications maternelles + néonatales Insuline Complications maternelles et néonatales Efficacité contrôle glycémique Complications maternelles + néonatales ♀dbg AG: 24 -36 s Lieu: ? (Iran) Glyburide Insuline ♀ dbg AG: ? É-U Glyburide Insuline Complications maternelles et néonatales Insuline Complications néonatales Complications maternelles Acceptation Tx ♀dbg AG: 24 -34 s France Glyburide
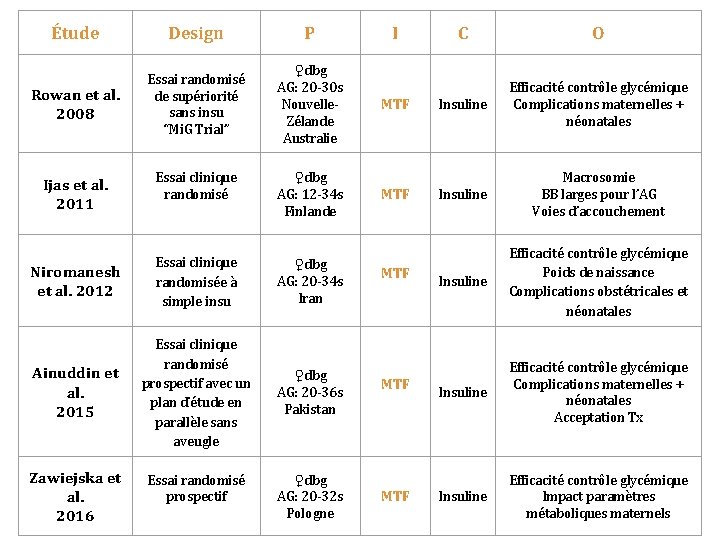
Étude Design P Rowan et al. 2008 Essai randomisé de supériorité sans insu “Mi. G Trial” ♀dbg AG: 20 -30 s Nouvelle. Zélande Australie Essai clinique randomisé ♀dbg AG: 12 -34 s Finlande Niromanesh et al. 2012 Essai clinique randomisée à simple insu ♀dbg AG: 20 -34 s Iran Ainuddin et al. 2015 Essai clinique randomisé prospectif avec un plan d’étude en parallèle sans aveugle ♀dbg AG: 20 -36 s Pakistan Ijas et al. 2011 Zawiejska et al. 2016 Essai randomisé prospectif ♀dbg AG: 20 -32 s Pologne I MTF MTF MTF C O Insuline Efficacité contrôle glycémique Complications maternelles + néonatales Insuline Macrosomie BB larges pour l’AG Voies d’accouchement Insuline Efficacité contrôle glycémique Poids de naissance Complications obstétricales et néonatales Insuline Efficacité contrôle glycémique Complications maternelles + néonatales Acceptation Tx Insuline Efficacité contrôle glycémique Impact paramètres métaboliques maternels
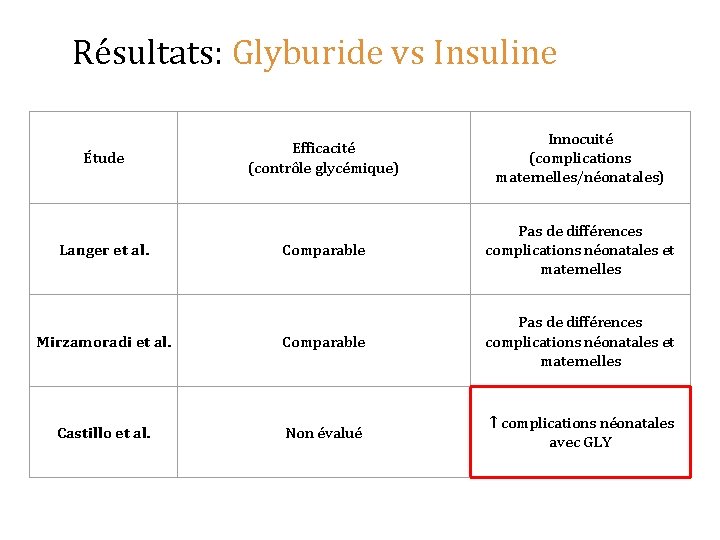
Résultats: Glyburide vs Insuline Efficacité (contrôle glycémique) Innocuité (complications maternelles/néonatales) Comparable Pas de différences complications néonatales et maternelles Mirzamoradi et al. Comparable Pas de différences complications néonatales et maternelles Castillo et al. Non évalué ↑ complications néonatales avec GLY Étude Langer et al.

Résultats: Glyburide vs Insuline Étude Jacobson et al. Sénat et al. Efficacité (contrôle glycémique) Innocuité (complications maternelles/néonatales) Glyburide > Insuline 86% vs 63% P < 0. 001 ↑ Pré-éclampsie (12% GLY vs 6% Ins, P=0. 02) ↑ Photothérapie (9% GLY vs 5% Ins, P<0. 05) ↓ Admission aux SIN (24% Ins vs 15% GLY, P=0. 008) Glyburide > Insuline “Bon contrôle” 71. 7% vs 63% p= 0. 003 GLY: ⌀ non-inférieur complications néonatales 27. 6% GLY vs 23. 4% Ins Δ 4. 2% (-∞à 10. 5%, p= 0. 19) ↑hypo. G maternelle Meilleure acceptation Tx
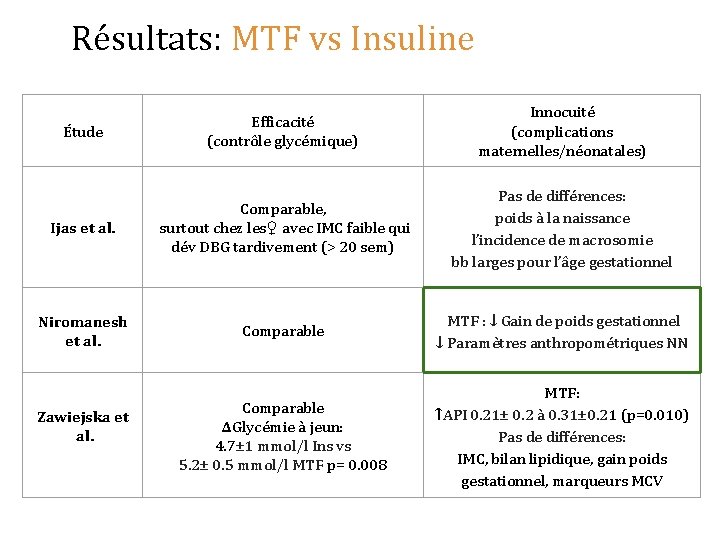
Résultats: MTF vs Insuline Étude Efficacité (contrôle glycémique) Innocuité (complications maternelles/néonatales) Ijas et al. Comparable, surtout chez les♀ avec IMC faible qui dév DBG tardivement (> 20 sem) Pas de différences: poids à la naissance l’incidence de macrosomie bb larges pour l’âge gestationnel Niromanesh et al. Comparable MTF : ↓ Gain de poids gestationnel ↓ Paramètres anthropométriques NN Comparable ΔGlycémie à jeun: 4. 7± 1 mmol/l Ins vs 5. 2± 0. 5 mmol/l MTF p= 0. 008 MTF: ↑API 0. 21± 0. 2 à 0. 31± 0. 21 (p=0. 010) Pas de différences: IMC, bilan lipidique, gain poids gestationnel, marqueurs MCV Zawiejska et al.
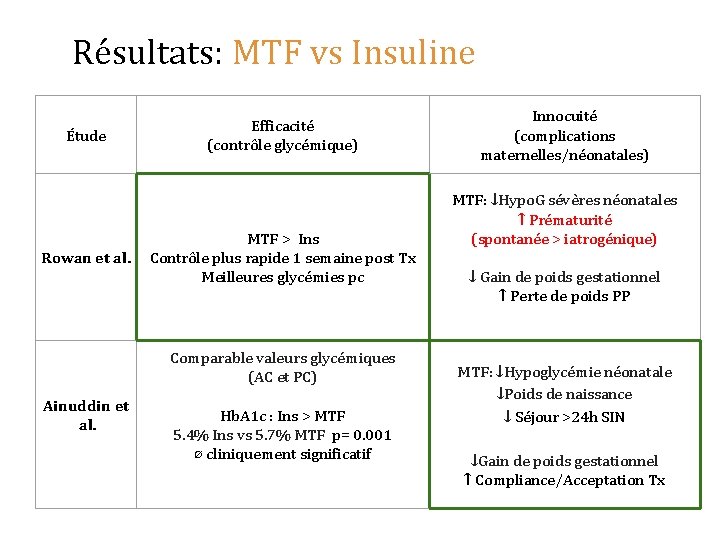
Résultats: MTF vs Insuline Étude Rowan et al. Efficacité (contrôle glycémique) MTF > Ins Contrôle plus rapide 1 semaine post Tx Meilleures glycémies pc Comparable valeurs glycémiques (AC et PC) Ainuddin et al. Hb. A 1 c : Ins > MTF 5. 4% Ins vs 5. 7% MTF p= 0. 001 ⌀ cliniquement significatif Innocuité (complications maternelles/néonatales) MTF: ↓Hypo. G sévères néonatales ↑ Prématurité (spontanée > iatrogénique) ↓ Gain de poids gestationnel ↑ Perte de poids PP MTF: ↓Hypoglycémie néonatale ↓Poids de naissance ↓ Séjour >24 h SIN ↓Gain de poids gestationnel ↑ Compliance/Acceptation Tx

Discussion ● Efficacité comparable ou meilleure (HGO > Ins) ● Bonne innocuité MTF à court terme ○ Prématurité: cause ⌀ claire ● Avantages administration, coût, acceptation = Meilleure compliance ● Moins de gain de poids = important en diabète ● Suivi plus facile pour les professionnels de la santé

Discussion ● Innocuité GLY: pas optimale ● Grande hétérogénéité des études ○ critères diagnostiques différents ○ instruments de mesure différents ○ échantillons étudiés varient (caractéristiques de base) ○ manque de données ○ petits échantillons ○ peu d’études randomisés contrôlés avec insu

Discussion ● Puissance ⌀ atteinte ● Plusieurs biais introduits ● 9/10 études: Validité interne faible à modérée ● 1/10 études: Bonne validité interne (Niromanesh et al. ) ● 6/10 études : Limitation validité externe

Conclusion ● HGO (MTF ou GLY) ne peut remplacer l’Ins comme 1 ere ligne de Tx ○ Efficacité comparable ou meilleure ○ Innocuité : GLY < Ins ● Études mieux bâties et plus puissantes ● Études sur complications à long terme (Mi. G TOFU) en cours ○ Innocuité à long terme sur les NN

Références 1. 2. 3. 4. 5. 6. 7. 8. 9. 10. 11. 12. 13. 14. 15. 16. 17. https: //www. diabete. qc. ca/fr/comprendre-le-diabete/tout-sur-le-diabete/types-de-diabete/diabete-de-grossesse, visité le 8 avril 2019. SMFM Statement: Pharmacological treatment of gestational diabetes. Am J Obstet Gynecol. 2018 May; 218(5): B 2 -B 4. doi: 10. 1016/j. ajog. 2018. 01. 041. Epub 2018 Feb 2. https: //www. ncbi. nlm. nih. gov/pubmed? holding=icahmrlib&term=29409848 https: //www. uptodate. com/contents/gestational-diabetes-mellitus-glycemic-control-and-maternalprognosis? search=gestational%20 diabetes&source=search_result&selected. Title=1~86&usage_type=default&display_rank=1 ACOG committee on practice bulletins. ACOG practice bulletin. Clinical management guidelines for obstetricians-gynecologists. Number 60, march 2005. Pregestational diabetes mellitus. Obstet gynecol 2005; 105(3): 675 -685. Feghali et al. Glycemic Control and Pregnancy Outcomes in Women with Type 2 Diabetes Treated with Oral Hypoglycemic Agents. Am J Perinatol. 2017 Jun; 34(7): 697 -704. Castillo et al. Association of Adverse Pregnancy Outcomes With Glyburide vs Insulin in Women With Gestational Diabetes. JAMA Pediatrics, May 2015, Volume 169, Number 5, p. 452 -458. Langer et al. A Comparison of Glyburide and Insulin in Women with Gestational Diabetes Mellitus. The New England Journal of Medicine, October 2000, Volume 343, Number 16, p. 1134 -1138. Jacobson et al. Comparision of Glyburide and Insulin for the Management of Gestational Diabetes in a Large Managed Care Organization. El Sevier. American Journal of Obstetrics and Gynecology, 2005, Volume 193, p. 118 -124. Ijas et al. Metformin should be considered in the treatment of gestational diabetes: a prospective randomised study. BJOG, June 2011, Volume 118, Number 7, p. 880 -885. Niromanesh et al. Metformin compared with insulin in the management of gestational diabetes mellitus: A randomized clinical trial. Diabetes Research and Clininical Practice. December 2012, Volume 98, Number 3: p. 422 -429. Mirzamoradi et al. Comparison of Glyburide and Insulin in Women with Gestational Diabetes Mellitus and Associated Perinatal Outcome: a Randomized Clinical Trial. Acta Medica Iranica, 2015; 53(2): 97 -103. Zawiejska et al. Short-term antidiabetic treatment with insulin or metformin has a similar impact on the components of metabolic syndrome in women with gestational diabetes mellitus requiring antidiabetic agents: Results of a prospective, randomised study. Journal of Physiology and Pharmacology. 2016 Apr; 67(2): 227 -33. Ainuddin et al. Metformin versus insulin treatment in gestational diabetes in pregnancy in a developing country. A randomized control trial. Diabetes Res and Clin Pract. 2015; 107(2): 290 -9. Sénat et al. Effect of glyburide vs subcutaneous insulin on perinatal complications among women with gestational diabetes. A randomized clinical trial. JAMA 2018 May 1; 319(17): 1773 -1780. Rowan et al. Metformin versus Insulin for the treatment of gestional diabetes. New England Journal of Medicine. 2008 May 8; 358(19): 2003 -15. https: //creogsovercoffee. com/episodes/2018/12/23/gestational-diabetes-and-special-interview-with-dr-donald-coustan, visité le 21 avril 2019. Niroumand et al. Atherogenic Index of Plasma (AIP): A marker of cardiovascular disease. Med J Islam Repub Iran. 2015; 29: 240. https: //www. ncbi. nlm. nih. gov/pubmed/26793631, visité le 12 avril 2019.

Remerciements Merci à l’ensemble de l’équipe de l’UMF Bordeaux-Cartierville. Merci à nos patrons d’être toujours présents afin de nous guider dans les bonnes directions. Merci à vous pour votre écoute.

Questions
- Slides: 21