Hybridation Hybridation Les orbitales hybrides Dans ce modle

Hybridation

Hybridation Les orbitales hybrides Dans ce modèle de représentation, on observe comment les orbitales s et p se recouvrent quand il y a partage d’électrons. Ceci permet à un atome de créer plus de liaisons. Ce modèle s’applique surtout au carbone.

Hybridation 3 sp

Hybridation sp 3 Le carbone compte 4é périphérique : 1 s 22 p 2, lors d’une liaison avec d’autres atomes, l’orbitale s et les 3 orbitales p (px, py et pz) semblent se regrouper pour former 4 orbitales hybrides équivalents (sp 3) quant à l’énergie et à la forme.
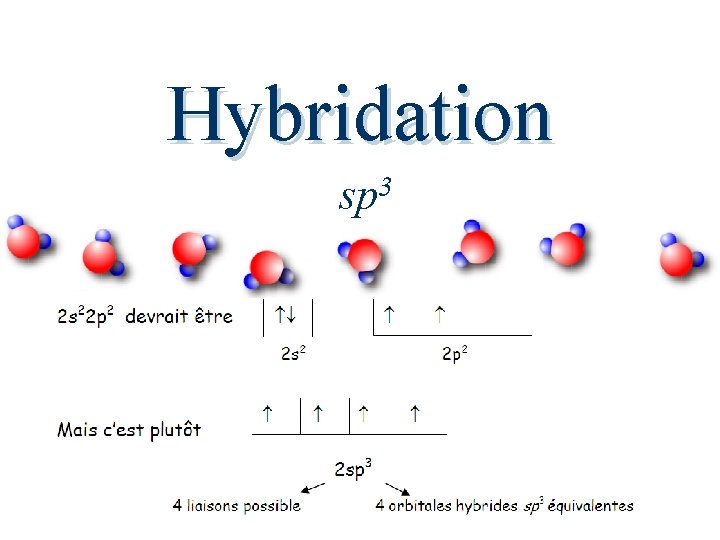
Hybridation sp 3

3 Hybridation sp du carbone CH 4

Configuration électronique de C
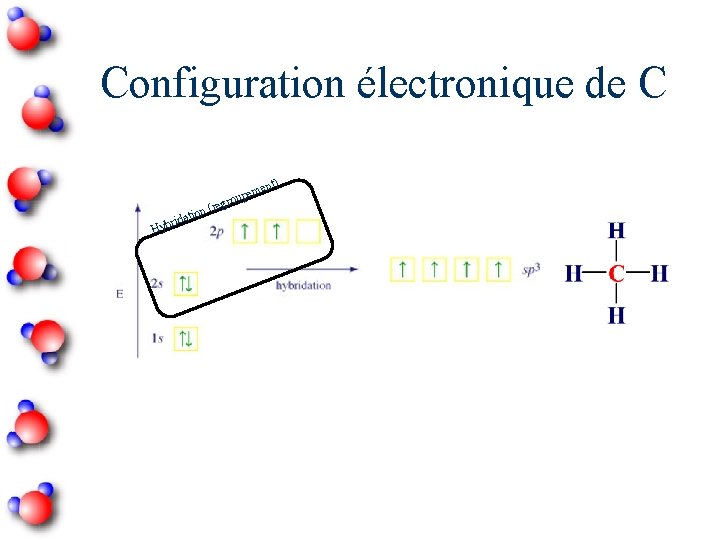
Configuration électronique de C ent) reg em roup ri Hyb on ( dati
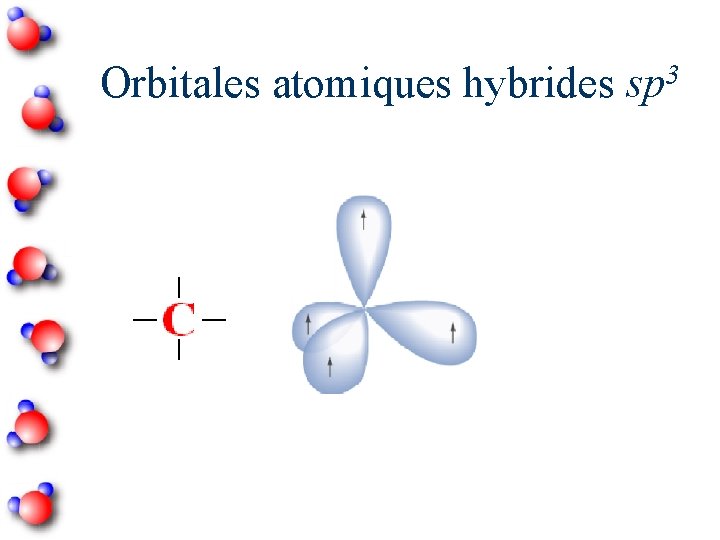
3 Orbitales atomiques hybrides sp
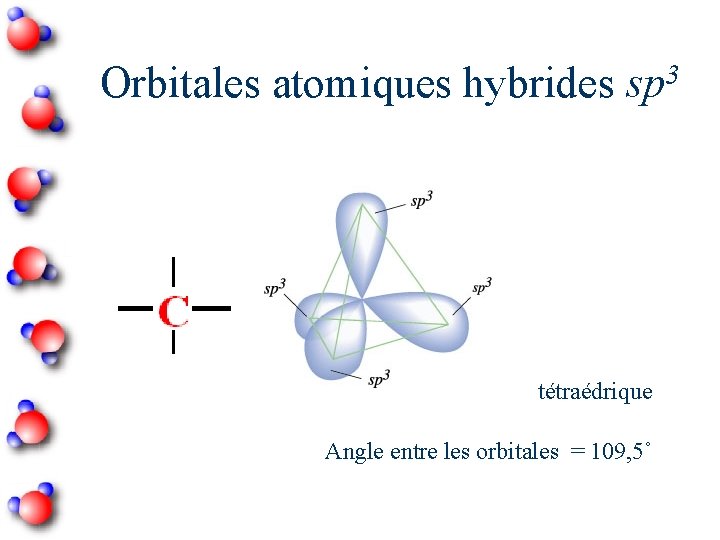
3 Orbitales atomiques hybrides sp tétraédrique Angle entre les orbitales = 109, 5˚
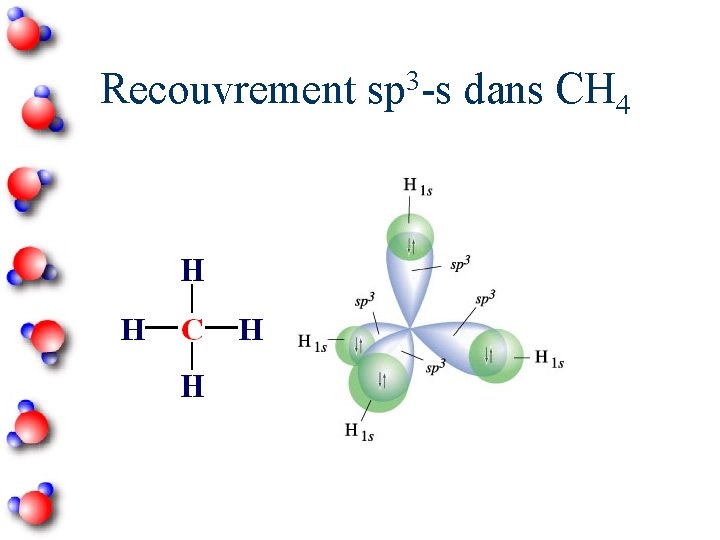
Recouvrement sp 3 -s dans CH 4
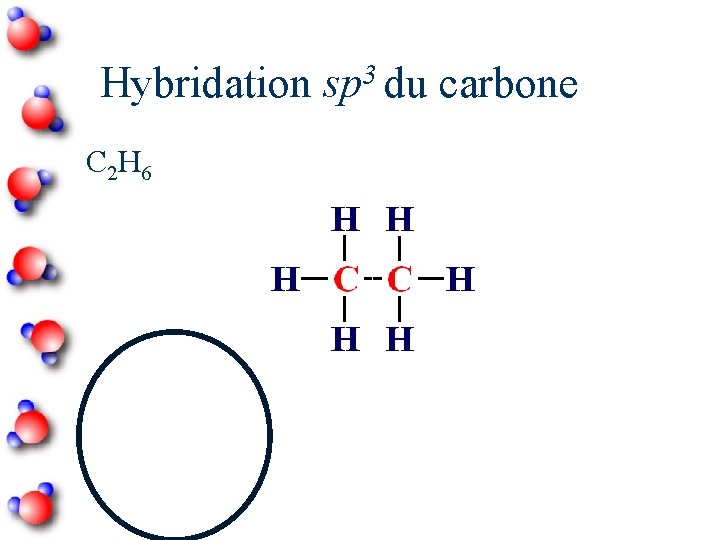
3 Hybridation sp du carbone C 2 H 6
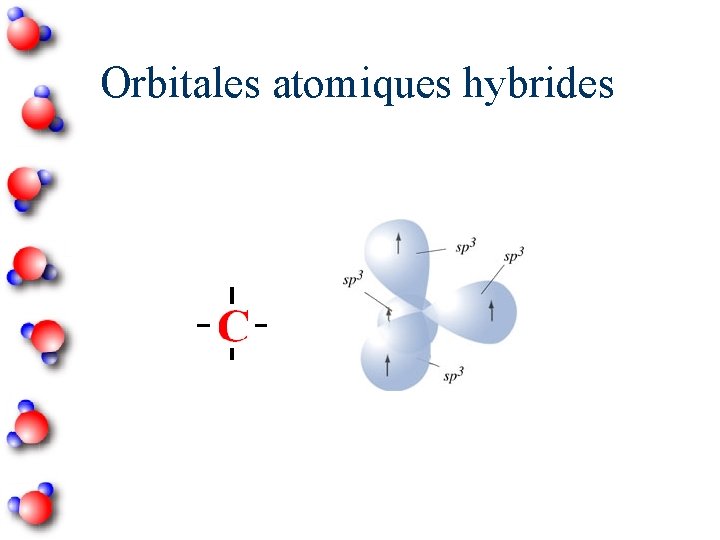
Orbitales atomiques hybrides
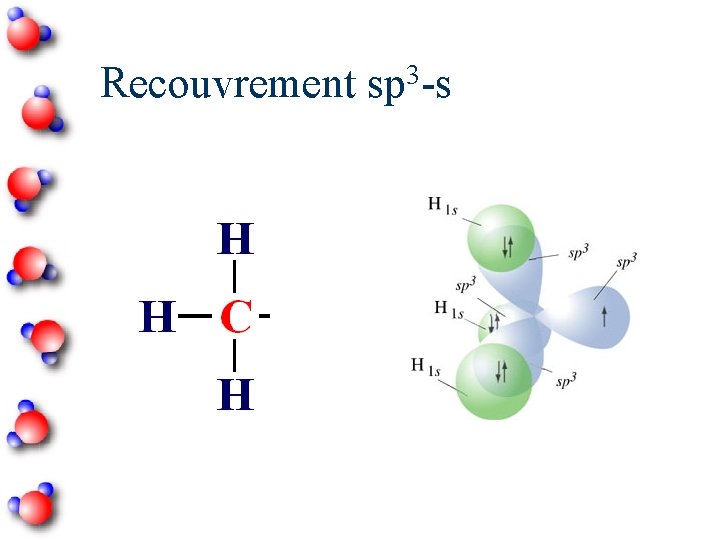
3 Recouvrement sp -s

3 Recouvrement sp -s
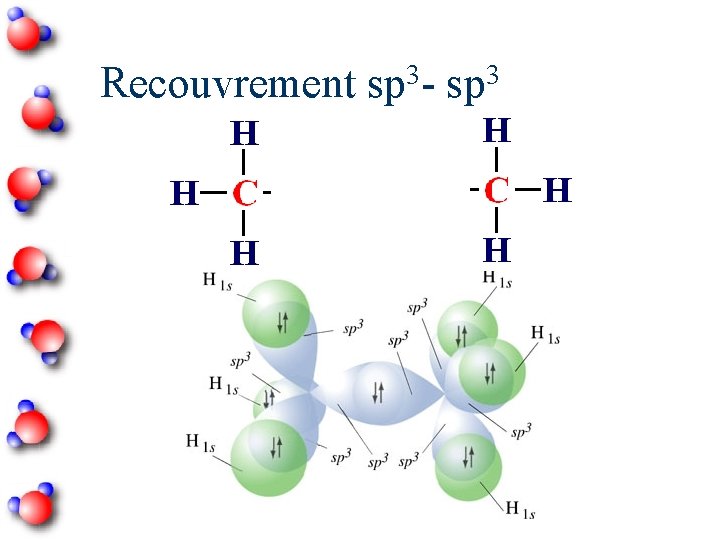
3 3 Recouvrement sp - sp

3 Récapitulation - Hybridation sp Nombre d’atomes liés + le nombre de doublets libres = 4 Angle entre les orbitales hybrides = 109, 5˚
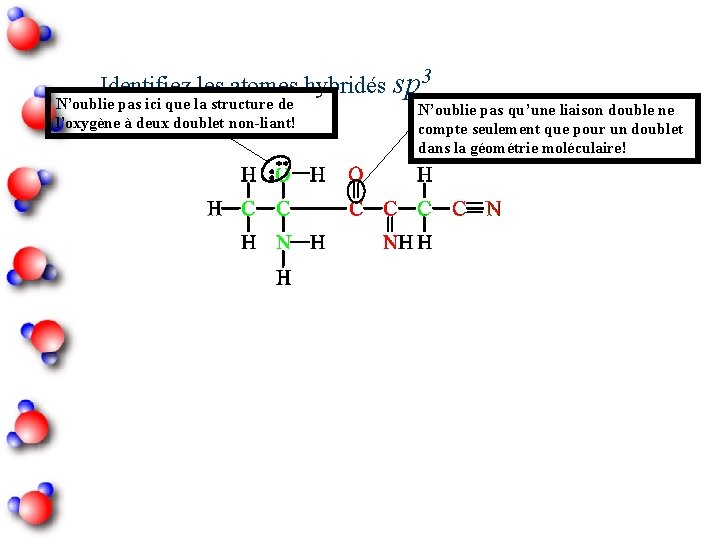
Identifiez les atomes hybridés sp 3 N’oublie pas ici que la structure de l’oxygène à deux doublet non-liant! N’oublie pas qu’une liaison double ne compte seulement que pour un doublet dans la géométrie moléculaire!

Hybridation 2 sp

Hybridation sp 2 Le modèle d’hybridation sp 2 permet de décrire les liaisons covalentes doubles. Le bore comprend 3 électrons périphériques : 1 s 22 p 1 lors d’une liaison avec d’autres atomes, l’orbitale s et les 2 orbitales p (px et py) occupés par 1 électron, semblent se regrouper pour former 3 orbitales hybrides équivalents (sp 2) quant à l’énergie et à la forme.
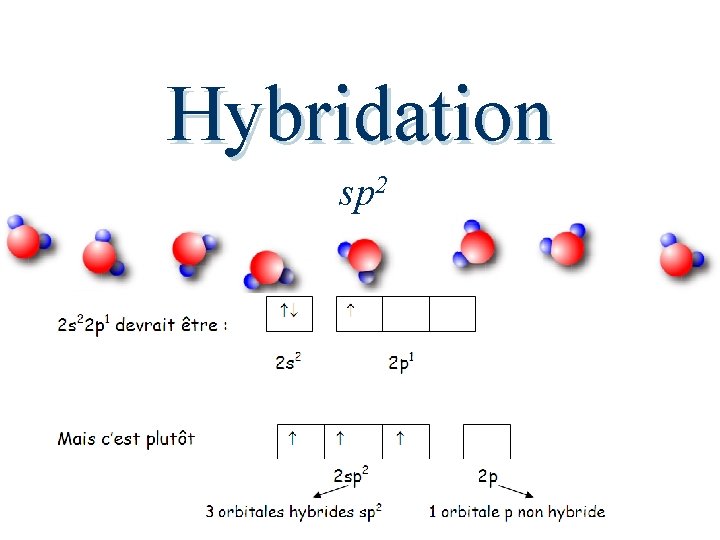
Hybridation sp 2
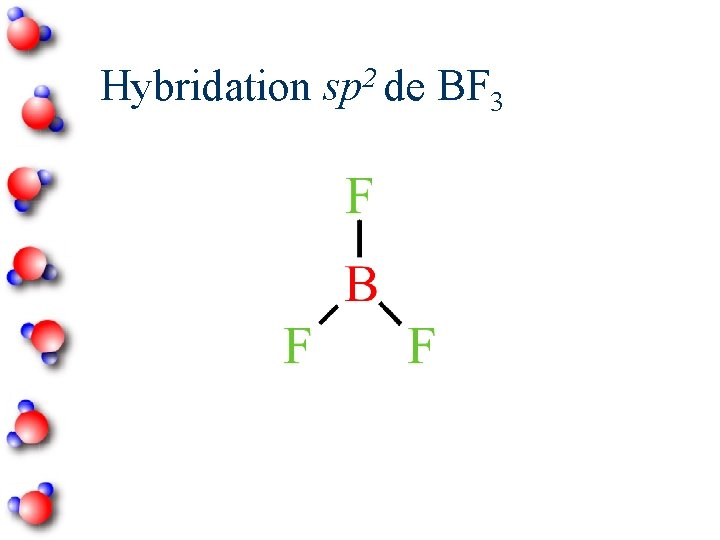
2 Hybridation sp de BF 3
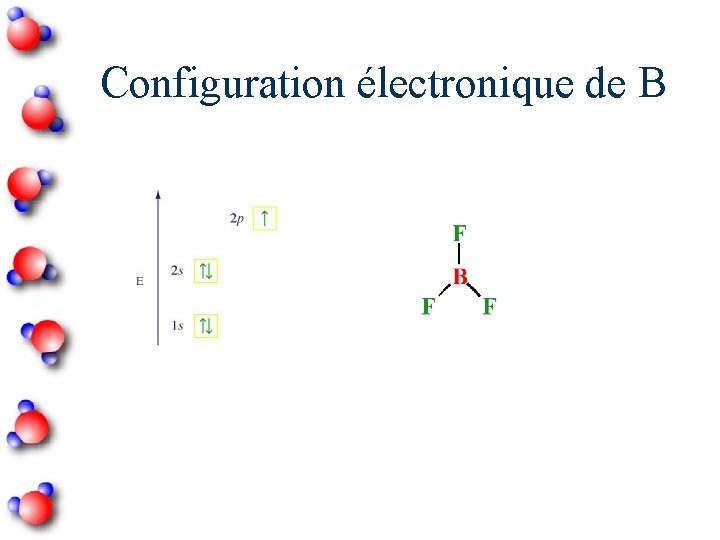
Configuration électronique de B
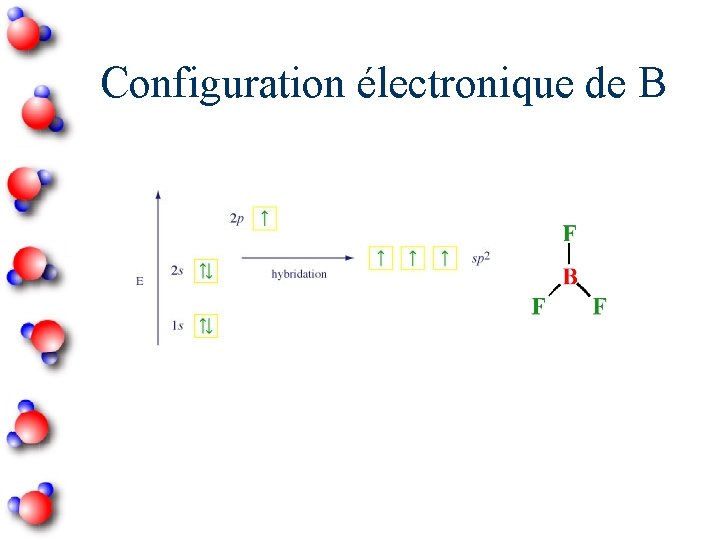
Configuration électronique de B
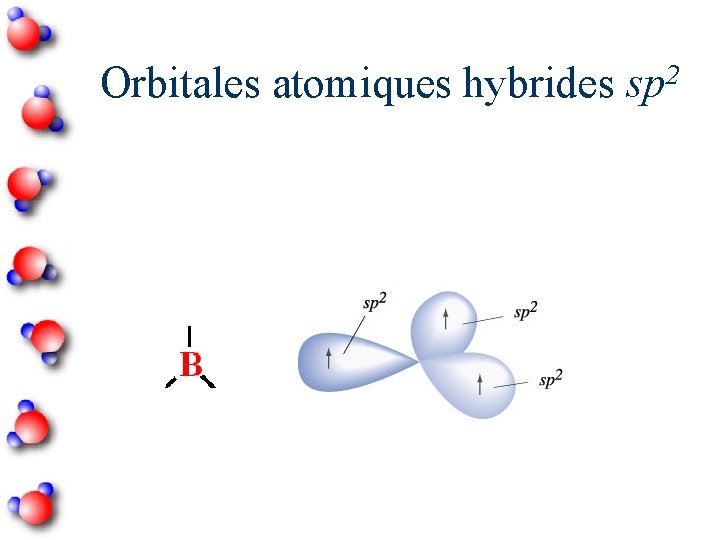
2 Orbitales atomiques hybrides sp
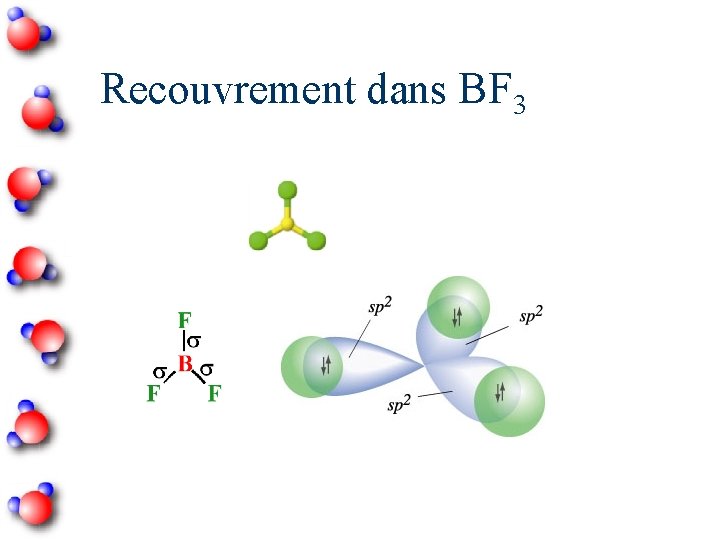
Recouvrement dans BF 3
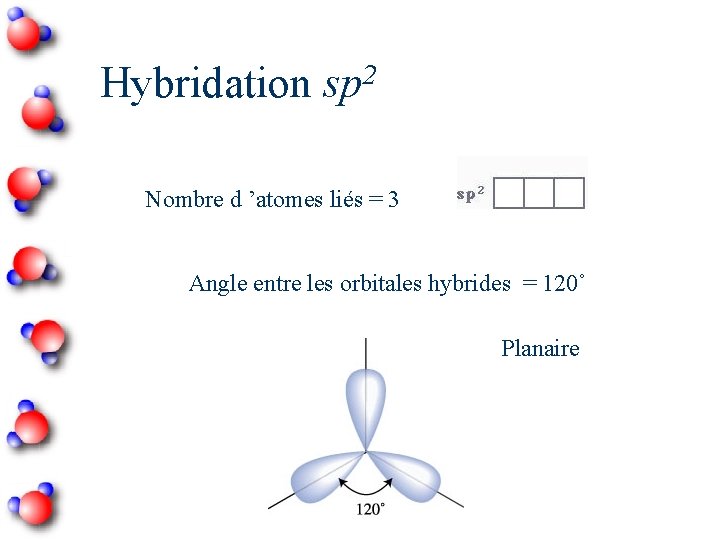
2 Hybridation sp Nombre d ’atomes liés = 3 Angle entre les orbitales hybrides = 120˚ Planaire
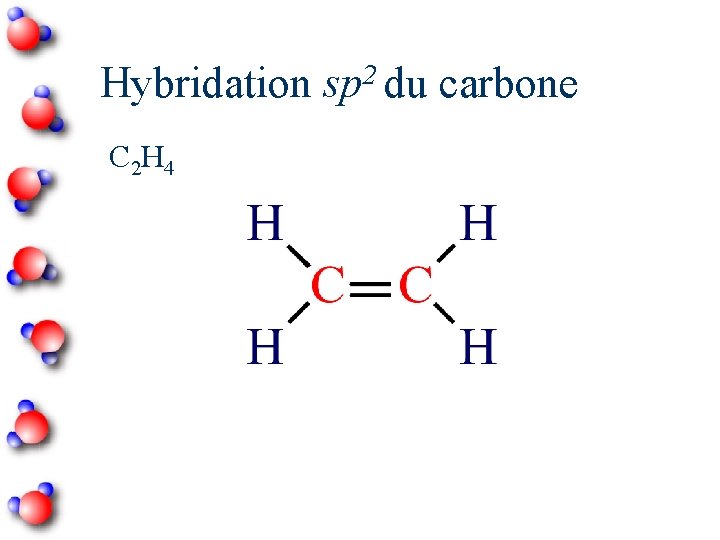
2 Hybridation sp du carbone C 2 H 4
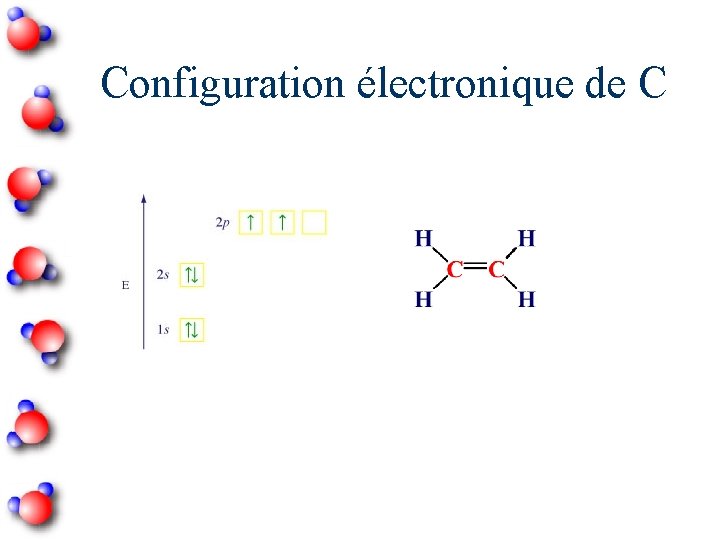
Configuration électronique de C
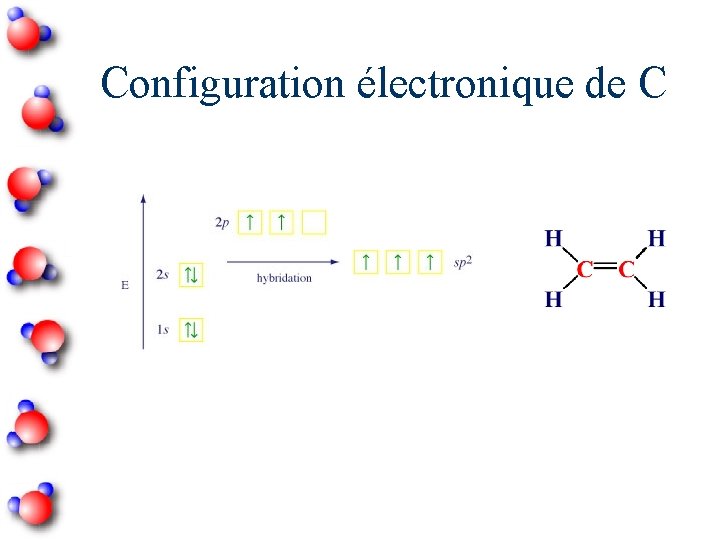
Configuration électronique de C

2 Orbitales atomiques hybrides sp
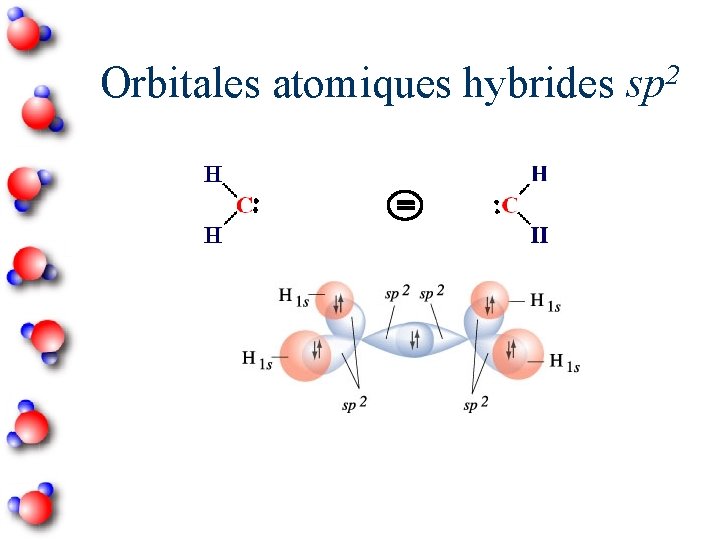
2 Orbitales atomiques hybrides sp

Hybridation sp

Hybridation sp Le modèle d’hybridation sp permet de décrire les liaisons covalentes triples. Le béryllium comprend 2 électrons périphériques : 1 s 22 s 2, lors d’une liaison avec d’autres atomes, l’électron de spin négatif situé dans l’orbitale s se déplace dans l’orbitale px. Par la suite, il y a hybridation des orbitales s et p (px). La formation de 2 orbitales hybrides sp et de 2 orbitales p non hybrides sera le résultat de ce type d’hybridation. .
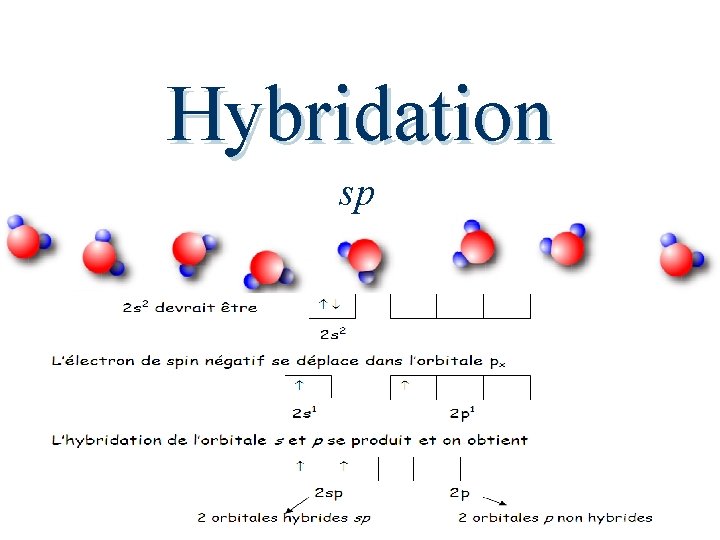
Hybridation sp
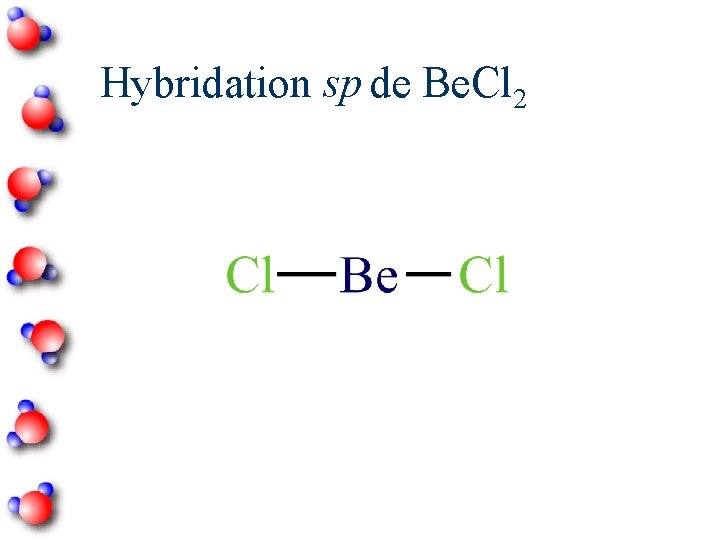
Hybridation sp de Be. Cl 2

Configuration électronique de Be
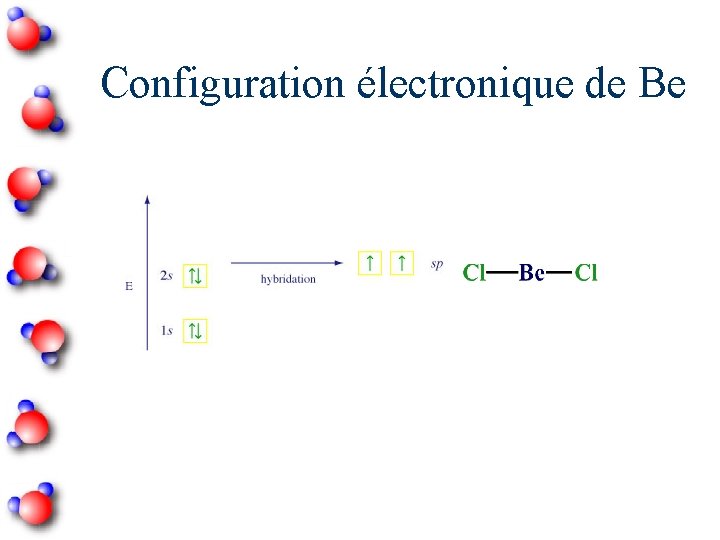
Configuration électronique de Be
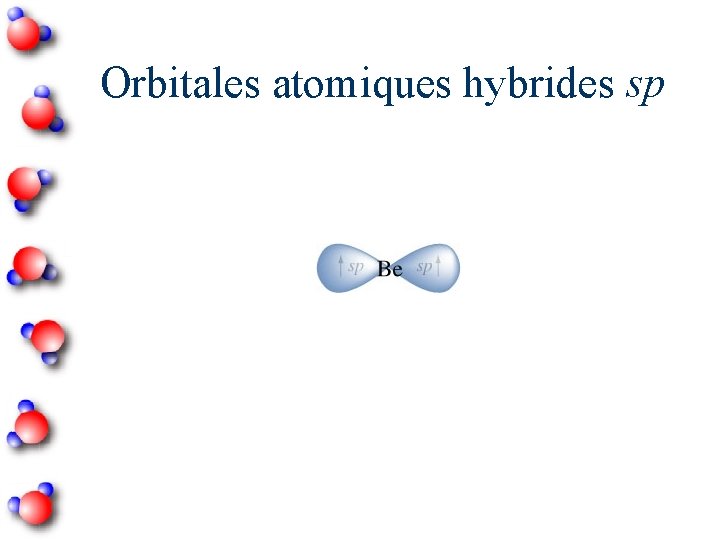
Orbitales atomiques hybrides sp
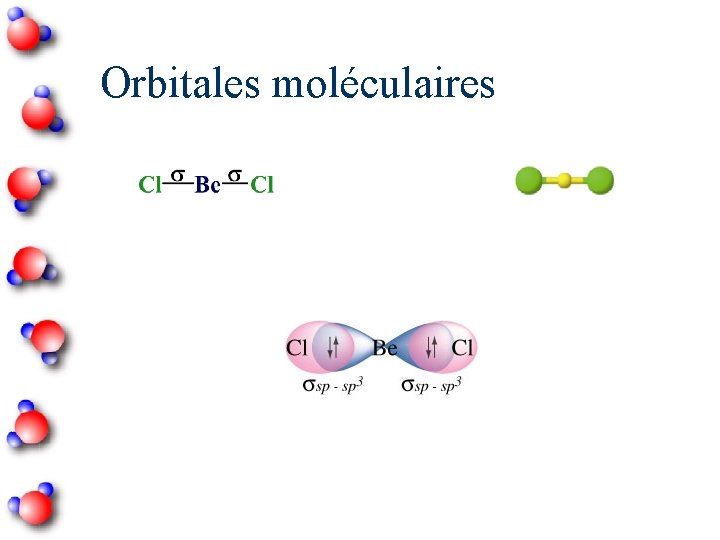
Orbitales moléculaires

Hybridation sp Nombre d ’atomes liés = 2 Angle entre les orbitales hybrides = 180˚ Linéaire
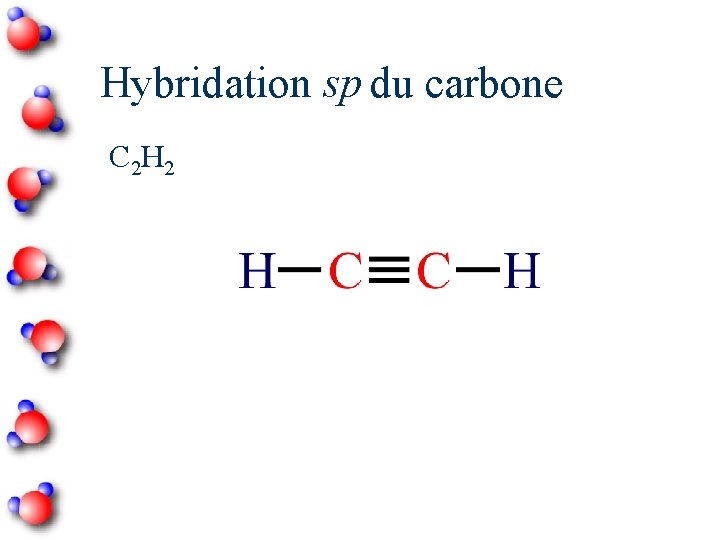
Hybridation sp du carbone C 2 H 2

Configuration électronique de C

Configuration électronique de C
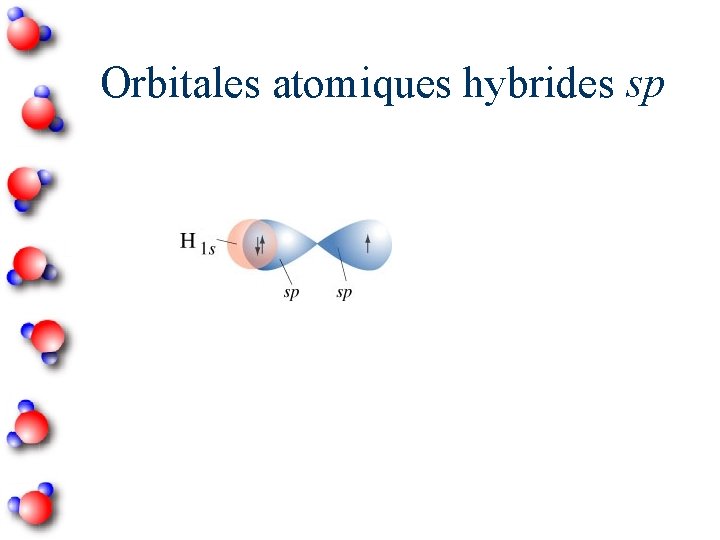
Orbitales atomiques hybrides sp
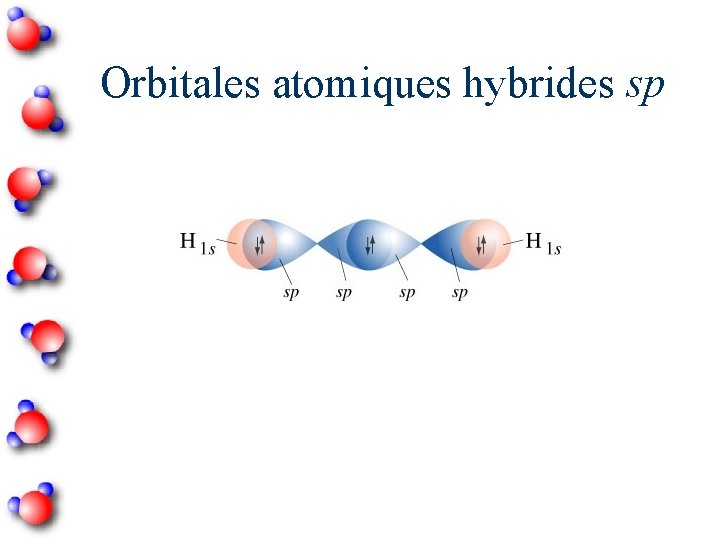
Orbitales atomiques hybrides sp

Configuration électronique de C
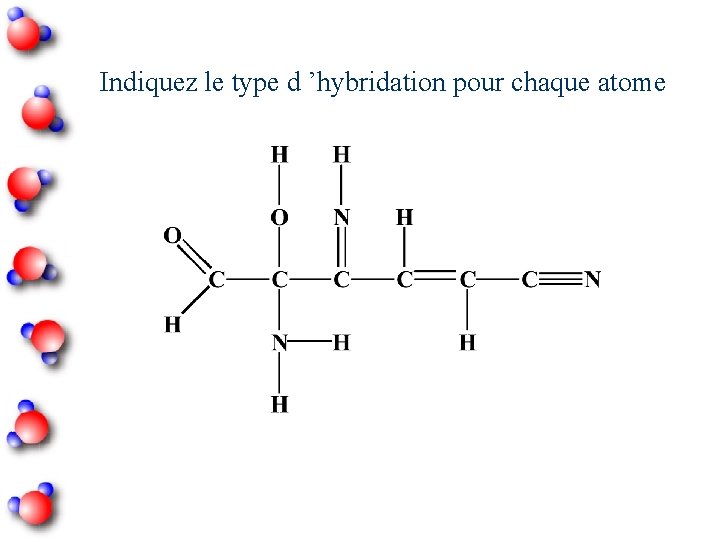
Indiquez le type d ’hybridation pour chaque atome
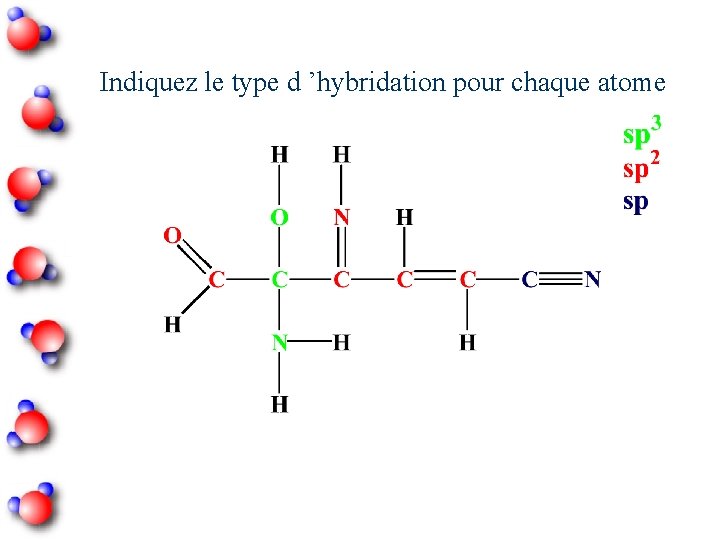
Indiquez le type d ’hybridation pour chaque atome

Résumé des orbitales hybrides Type de liaisons entre les carbones Résultat de l’hybridation 4 liaisons simples 4 orbitales hybrides sp 3 1 liaison double (et 2 liaisons simples) 3 orbitales hybrides sp 2 et 1 orbitale p non hybride 1 liaison triple (et 1 liaison simple) 2 orbitales hybrides sp et 2 orbitales p non hybrides

Travail à remettre Géométrie moléculaire 1 à 10
- Slides: 51