Human immunodeficiency virus HIV Foto http www medicinenet



































































- Slides: 119

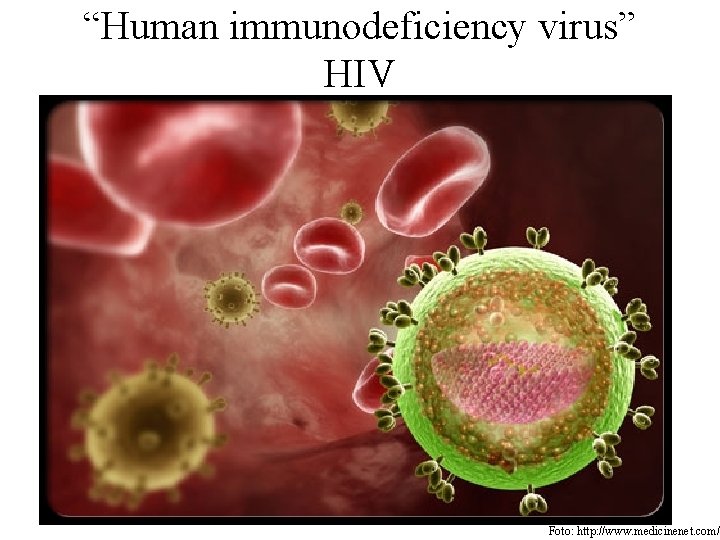
“Human immunodeficiency virus” HIV Foto: http: //www. medicinenet. com/

Como tudo começou?

HIV-1 - origem: chimpanzé (Pan troglodytes) HIV-2 - "sooty mangabey” (Cercocebus atys) Pan troglodytes Cercocebus atys

Retrovírus humanos HIV 1 e 2: AIDS HTLV-1: leucemias / linfomas de células T paraparesia espástica tropical (TSP) ou mielopatia associada ao HTLV (HAM) HTLV-2: patologia ? - RNA diplóide, fita simples, positiva - transcriptase reversa

HIV - dois tipos: HIV-1 e HIV-2 - HIV-1: mais freqüente - HIV-2 mais freqüente na África (40% homologia com HIV-1)

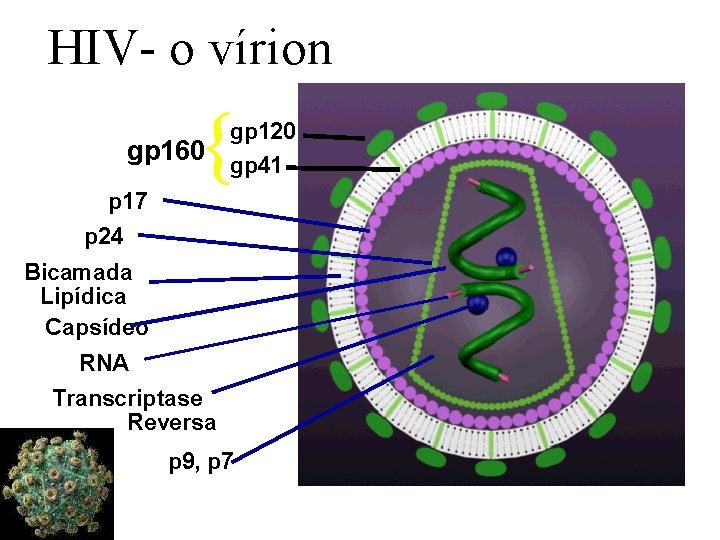
HIV- o vírion gp 160 gp 120 gp 41 p 17 p 24 Bicamada Lipídica Capsídeo RNA Transcriptase Reversa p 9, p 7

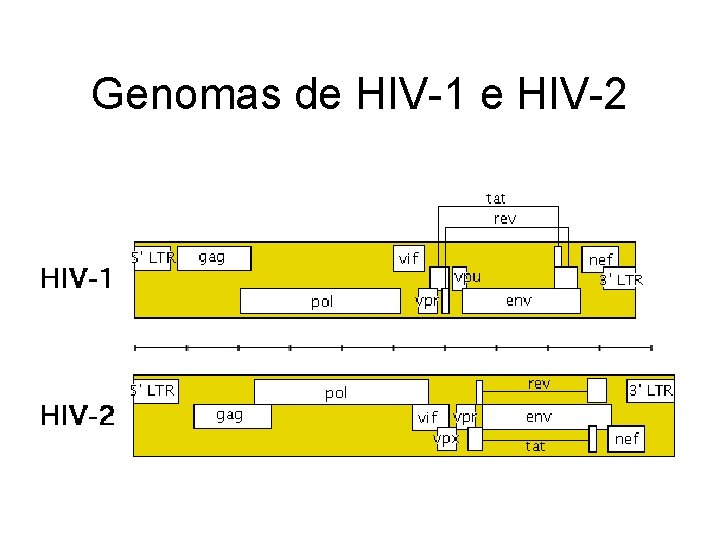
Genomas de HIV-1 e HIV-2

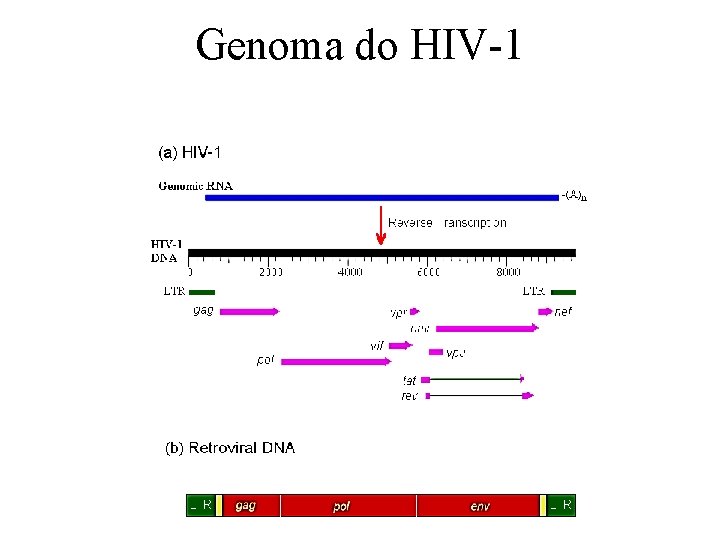
Genoma do HIV-1

– Gag (group antigen). O gene gag sintetiza o capsídeo viral em forma de cone (p 24, ou CA), a proteína do núcleocapsídeo (p 17, NC) e um proteína da matriz (MA). – Pol (polimerase). O gene pol codifica as proteínas enzimaticamente ativas do vírus. A mais importante é a chamada transcriptase reversa(RT), integrase (IN) polcodificadora e a protease (PR). Essa enzima cliva o gag e as proteínas derivadas de gag e pol em pedaços funcionais. – env. (envelope). Codifica gp 120 e a proteína transmembrana gp 41. – Tat (transativadora). Um porção da estrutura do RNA do HIV é uma estrutura como um grampo de cabelo que inicialmente impede que a transcrição completa ocorra. Parte do RNA é transcrita (ie. antes do grampo) e codifica a proteína tat. A tat liga-se à Cd. K 9/Cyc. T e a fosforila, ajudando a alterar sua forma e a eliminar o efeito do grampo. Isso por si só aumenta a taxa de transcrição, fornecendo um ciclo de retroalimentação positiva. Isto permite que o HIV tenha uma resposta explosiva, uma vez que uma grande quantidade de tat é produzida. – rev. A rev suprime proteínas regulatórias e estimula a produçáo de proteínas virais. Permite que fragmentos do m. RNA do HIV que contém um elemento responsivo à rev (RRE) sejam exportados sem serem clivados, do núcleo ao citoplasma. Na ausência da rev, a maquinaria de splicing do RNA no núcleo rapidamente cliva o RNA. Na presença da rev, o RNA é exportado do núcleo antes de ser clivado, num mecanismo de retroalimentação positiva. RNA clivado codifica proteinas regulaórias, como tat e nef; RNA integral codifica proteinas virais, como envelope e capsídeo. – Fonte: http: //www. mcld. co. uk/hiv/

Genes do HIV • • "vif" ("virion infectivity factor“) => aumenta a infectividade do vírion. Vif é encontrada dentro de células infectadas – interfere com a proteína celular chamada APOBEC 3 G. Vif se liga a APOBEC 3 G e estimula a célula a degradá -la. • • Massa de vif 23 k. D APOBEC: Apoliprotein B m. RNA-editing enzyme-catalytic polypeptide-like 3 G nef ("negative replication factor“) codifica uma proteína que permanece no citopolasme e retarda a replicação do HIV. Provavelmente o faz por modificar proteínas reguladoras da transcrição. • • Massa de nef 27 k. D

Genes do HIV • • Vpr: ("Viral protein R“) acelera a produção de proteinas do HIV. Também facilita a localização nuclear do complexo pre-integração - um aglomerado de RNA viral, transcriptase reversa e integrase que deve ser formado para que o genoma do HIV possa ser integradoi. Vpr carrega “sinais de localização nuclear” (sequencias de prote[inas que são reconhecidas pela célula e que indicam que deve ser transportada para oi núcleo), semelhante à proteína celular chamada importin-beta. Parace haver participação da Vpr na obstrução do ciclo de replicação celular normal. Células em "G 2“ são mais aptas à replicação do HIV. More information: Massa devpr : 15 k. D Há 100 copies desta proteína em cada vírion. A proteína celular cyclophilin A é importante para a produçãop de Vpr.

Genes do HIV • Vpu ("Viral protein U“) participa na montagem de novos vírions e brotamento. • Vpu também aumenta a degradação de proteínas CD 4 diminuindo a chance de superinfecção. • Secundariamente, a vpu atrasa o efeito citopático, mantendo-a viva por mais tempo e produzindo mais vírions. Sem o gene vpu gene, HIV mata a célula mais rápido! • Fonte: http: //www. mcld. co. uk/hiv/? q=vpu

HIV - Afinidade por receptores CD 4 Linfócitos T auxiliares (Th) Macrófagos/monócitos Co-receptores importantes (CCR 5, CXCR 4)

Adsorção - HIV • Adsorção via CCR 5 e CD 4 permite que o vírus penetre em macrófagos e células T (“M-tropismo”); • Adsorção via CXCR 4 e CD 4 permite que o vírus penetre somente células T (“T-tropismo”).

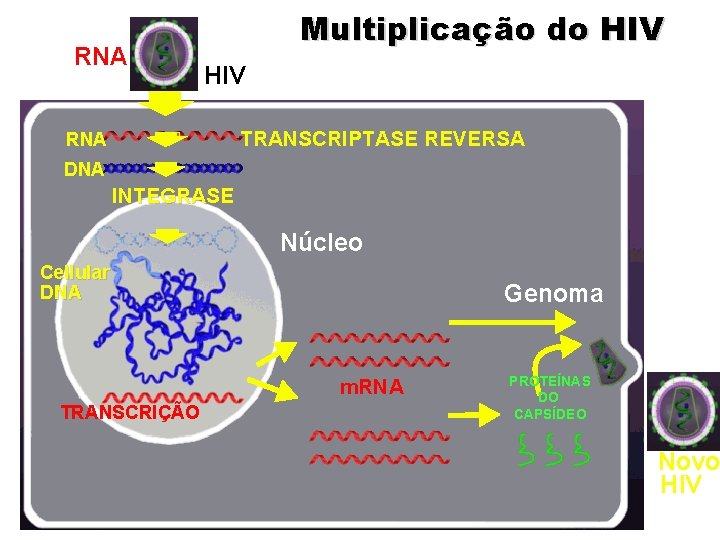
RNA Multiplicação do HIV TRANSCRIPTASE REVERSA RNA DNA INTEGRASE Núcleo Cellular DNA Genoma m. RNA TRANSCRIÇÃO PROTEÍNAS DO CAPSÍDEO Novo HIV

TRANSMISSÃO MECANISMO DE INFECÇÃO SÊMEN SANGUE

HIV - transmissão - sangue - sêmen Pequenas quantidades de vírus: insuficientes para transmitir a infecção


HIV - suscetibilidade portadores de alelos recessivos para os co-receptores CCR 5, CXCR 4 => refratários (proteínas de adesão intercelular)

HIV – infecções crônicas • Infecções crônicas assintomáticas: 3 a 20 anos, dependendo do indivíduo (Levi, 2009) • Carga viral decresce de muitos milhões para 11 -50 mil cópias RNA/m. L na fase crônica

HIV: Definição das populações de “controladores” mais frequentes (Poropatich & Sullivan 2011) EC LTNP Quant. de céls T CD 4+ ≥ 500 Carga viral (cópias/m. L) ≤ 50 ≤ 10 000 Terapia antiretroviral Não Anos sem AIDS Meses- anos ≥ 7 -20

HIV - exemplos de alto risco - pessoas com contato sexual com contaminados - usuários de drogas injetáveis - crianças de mães infectadas - trabalhadores da área da saúde - laboratoristas (contato com sangue) - hemofílicos - transfusionados - pacientes de transplantes

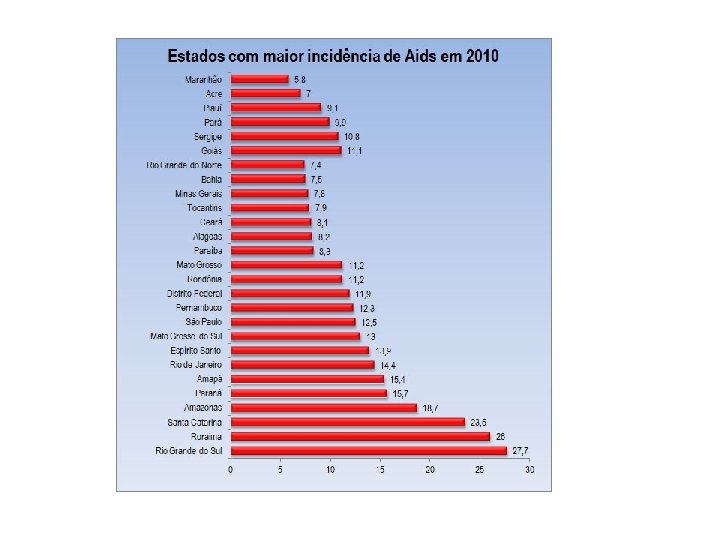
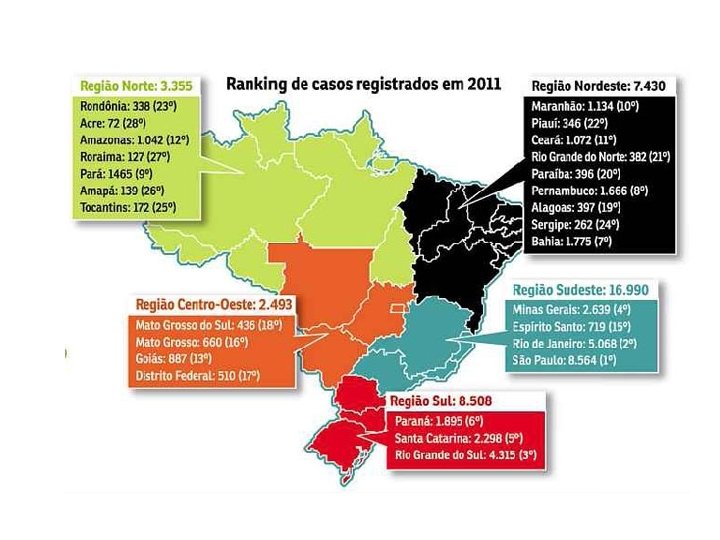
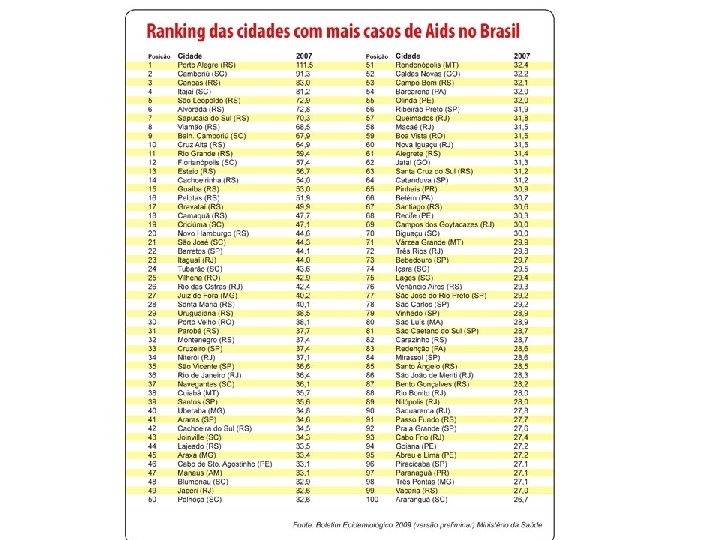
AIDS no Brasil




HIV - PATOGENIA - infecção de céls T CD 4 + e macrófagos - infecção disseminada - resposta imune específica: imunidade humoral imunidade celular - destruição da maior parte dos vírus - alguns persistem - destruição gradual de células T CD 4+ - desorganização da resposta imune

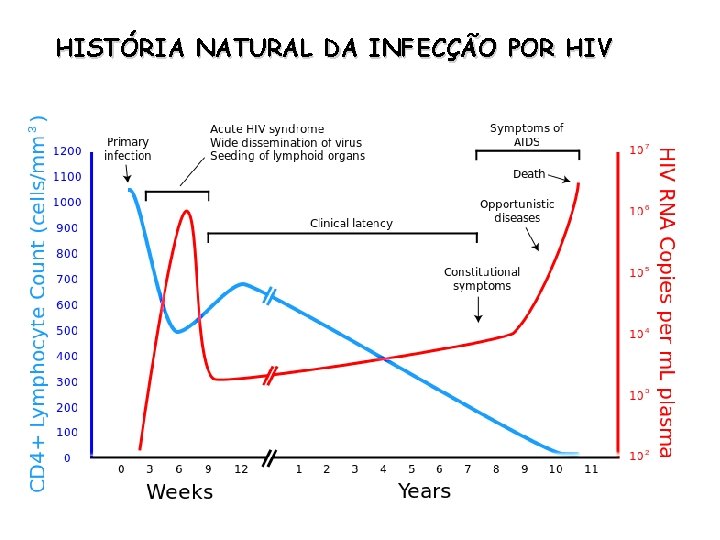
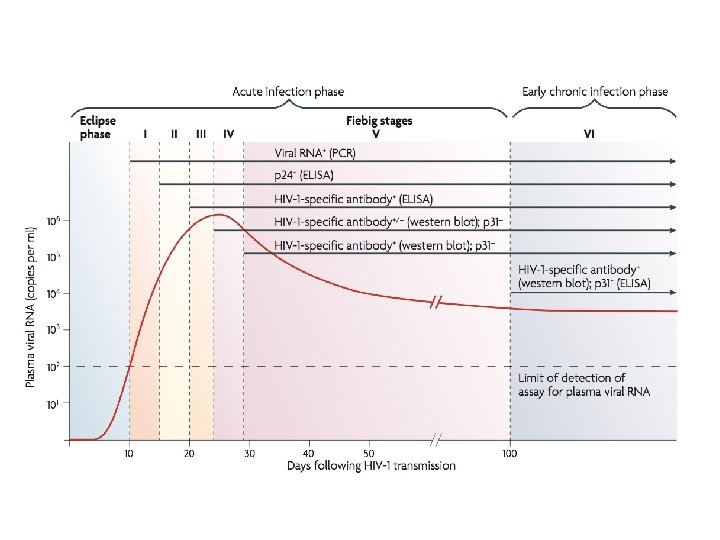
HISTÓRIA NATURAL DA INFECÇÃO POR HIV

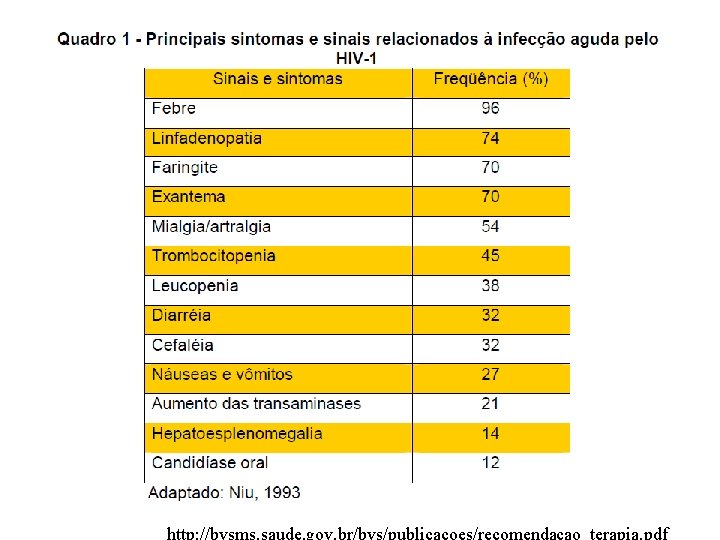
HIV - infecção primária - doença ~ resfriado, coincidindo com soroconversão 2 a 4 semanas após exposição - febre, suores noturnos, dor de garganta, linfadenopatia, diarréia - auto-limitante Fase assintomática: variável (2 a 10 anos)

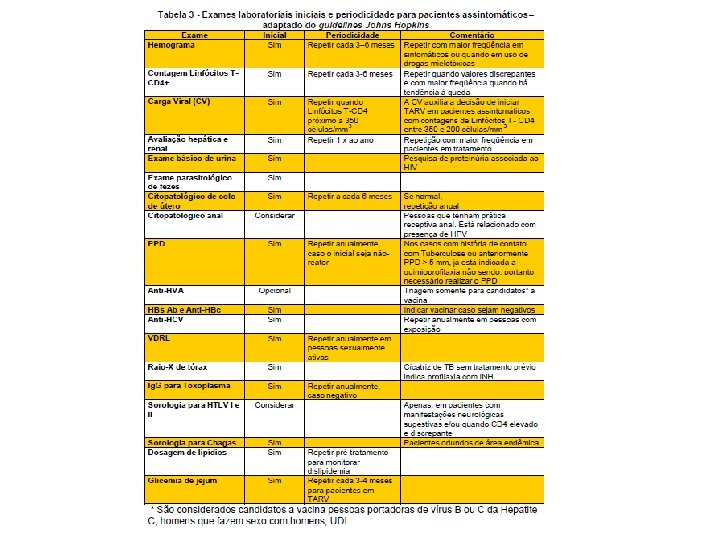
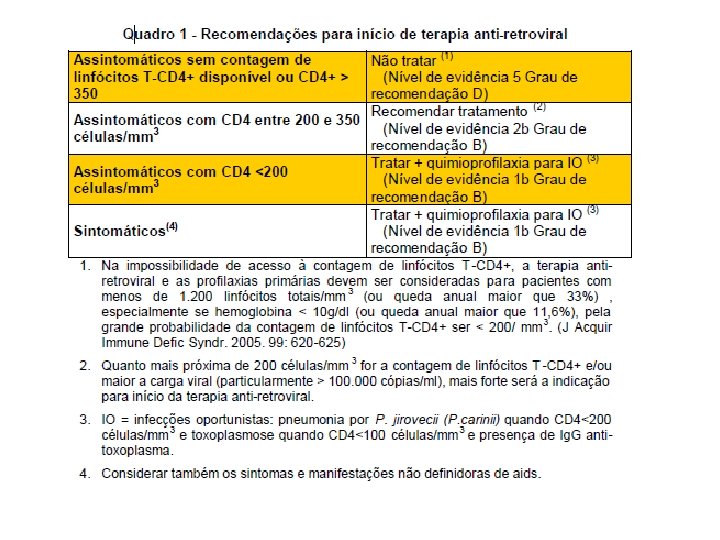
http: //bvsms. saude. gov. br/bvs/publicacoes/recomendacao_terapia. pdf

Patogenia – HIV • Carga viral na fase aguda: muitos milhões de cópias de RNA/m. L sangue • Progressores rápidos: tipicamente desenvolvem AIDS em 3 -5 anos

HIV- não progressores • • • Não progressores de longo termo, ou “Long-term non-progressors” (LTNPs): Também chamados “controladores virêmicos” Mantém entre 5 a 15 mil cópias de RNA/m. L, sendo a maioria com < 10 mil cópias; alguns: 50 a 2000 cópias/m. L • Alguns LTNPs e mantém-se sem carga viral detectável passados 1 -2 anos da infecção (Madec et al, 2005; Okulicz et al. 2009) • Alguns chamados “controladores de elite” ( CEs), ou “supressores de elite”, tem níveis de RNA indetectáveis ( <50 cópias/m. L) por meses ou anos, sem terapia- estimados em cerca de 0, 55% dos infectados (em 4586 pacientes acompanhados desde 1986). • Nestes 4586, 3, 32% se mantiveram LTNPs por 7 anos; 2, 04% se mantiveram LTNPs por 10 anos (Okulicz et al. 2009); • • - Nunca receberam terapia anti HIV; • - Infectados com HIV por até 20 -25 anos; • - Representam 2 a 5% de todos os HIV-infectados • - Durante o curso da infecção, os LTNPs mantém baixos níveis de viremia e T CD 4 + elevados ( > 500 µL)

LTNPs e HIV • A maioria dos ECs e LTNPs tem TCD 4+ normais • Alguns podem progredir para imunodeficiência por depleção de TCD 4+ • No estudo CASCADE (“Concerted Action on Seroconversion to AIDS and Death in Europe”): 7% progrediram para AIDS (Madec et al. 2005)

Controladores de Elite (ECs) - HIV • • Em uma coorte de 30 ECs: infectados por > 16 anos com carga viral muito baixa (<75 cópias/m. L), Tinham < 350 céls. T CD 4+ µL e AIDS.


HIV: “progressores lentos” • Progressores lentos , ou “slow progressors” ( SPs): • - tem níveis de T CD 4+ < 500 céls/µL • - tem cargas virais mais elevadas do que os LTNPs;

HIV: Definição das populações de “controladores” mais frequentes (Poropatich & Sullivan 2011) EC LTNP Quant. de céls T CD 4+ ≥ 500 Carga viral (cópias/m. L) ≤ 50 ≤ 10 000 Terapia antiretroviral Não Anos sem AIDS Meses- anos ≥ 7 -20

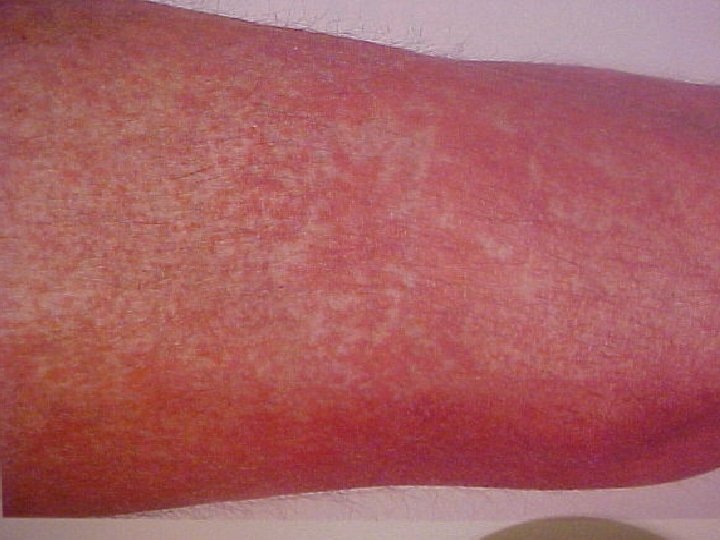
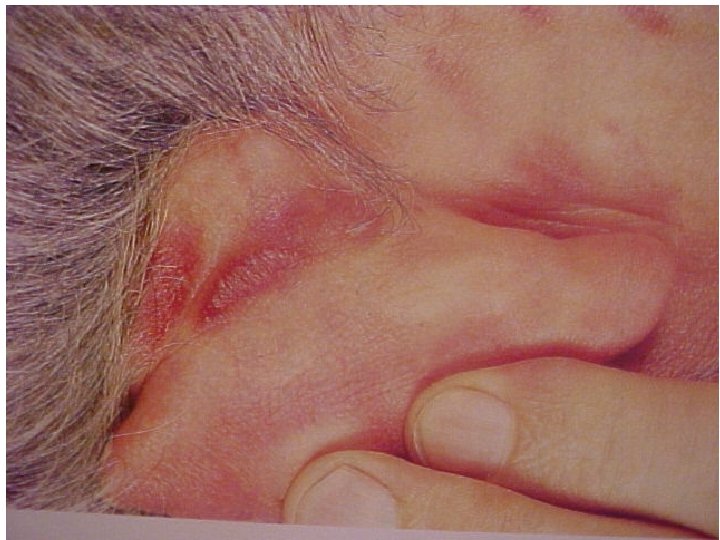
AIDS 1) doença constitucional: febre, diarréia, perda de peso, exantemas 2) doença neurológica: demência, mielopatia, neuropatia periférica 3) Imunodeficiência (suscetibilidade aumentada a infecções oportunísticas) 4) tumores raros (KS, leucoplaquia oral, linfomas)

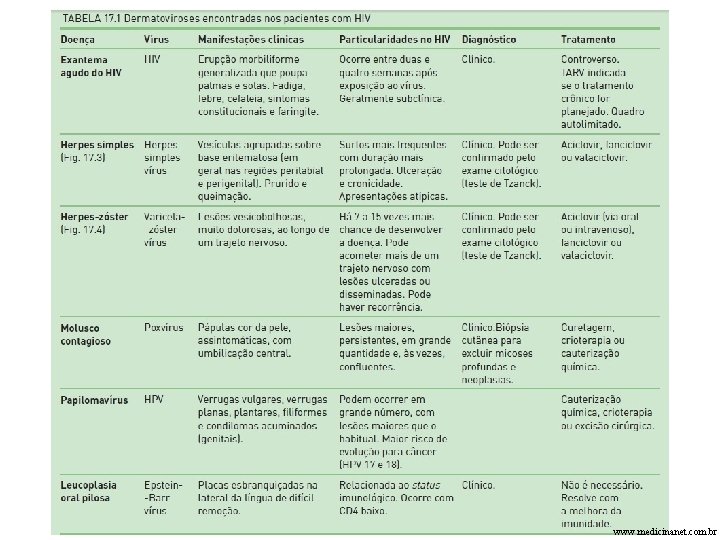
HIV- INFECÇÕES OPORTUNÍSTICAS COMUNS - Pneumocistis carinii - Criptosporidiose crônica - Toxoplasmose - Candidíase - Criptococose - Tuberculose e outras micobacterioses - Citomegalovírus (CMV) - Herpes simples (HSV 1 ; HSV 2) - Vírus Epstein Barr (EBV) - Sarcoma de Kaposi (KS) - Leucoencefalopatia Multifocal progressiva (poliomavírus) -

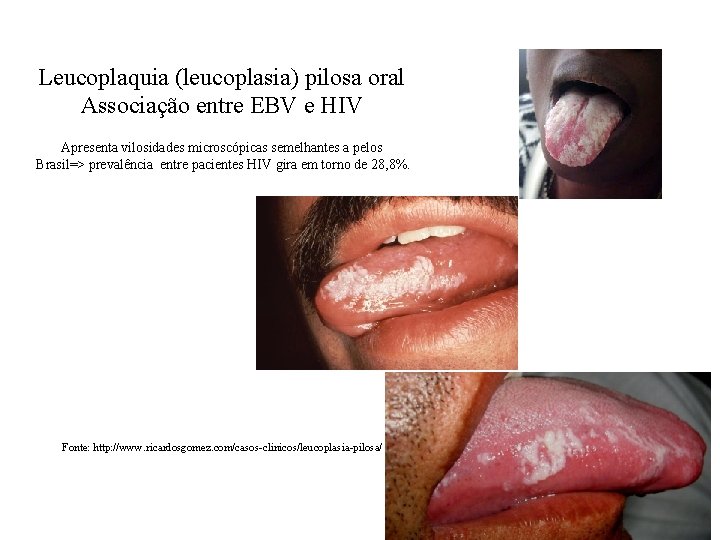
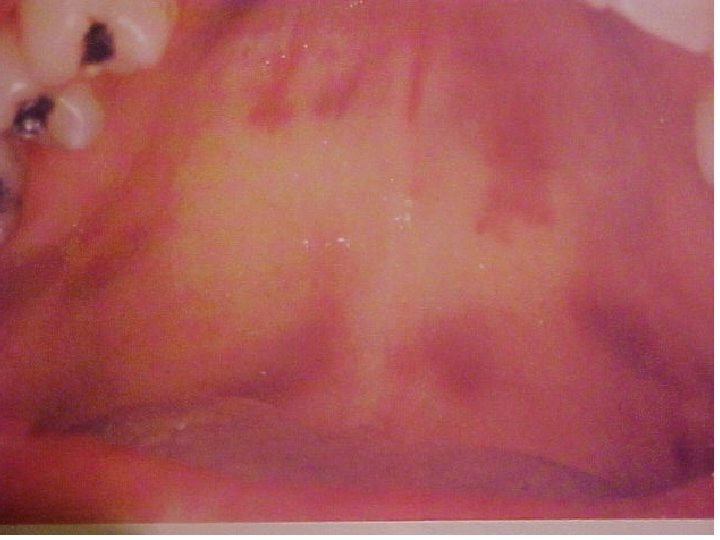
Leucoplaquia (leucoplasia) pilosa oral Associação entre EBV e HIV Apresenta vilosidades microscópicas semelhantes a pelos Brasil=> prevalência entre pacientes HIV gira em torno de 28, 8%. Fonte: http: //www. ricardosgomez. com/casos-clinicos/leucoplasia-pilosa/

www. medicinanet. com. br

HIV e Tuberculose Fonte: Recomendações para terapia anti-retroviral em adultos e adolescentes infectados pelo HIV - 2007/2008 - Documento preliminar 4: http: //bvsms. saude. gov. br/bvs/publicacoes/recomendacao_terapia. pdf

HIV – diversidade genética Tipo-grupo - subtipo- cepa- quasispécie Infecção dupla/múltipla e recombinação=> formação de híbridos O que direciona a evolução viral é a resposta do hospedeiro!

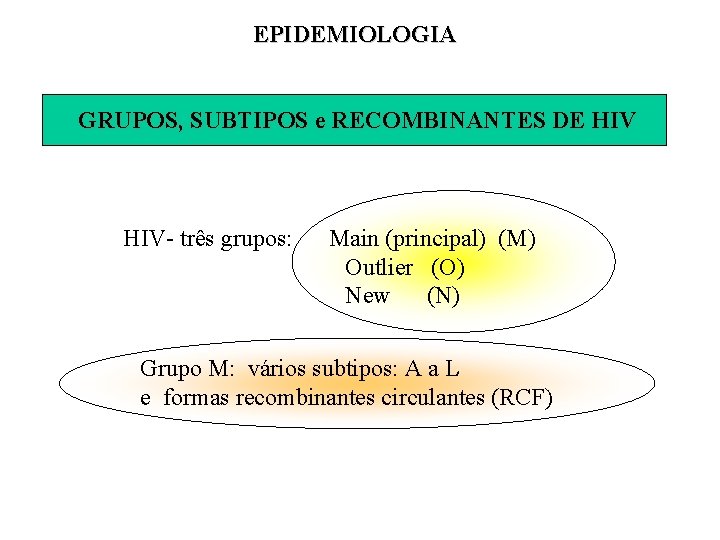
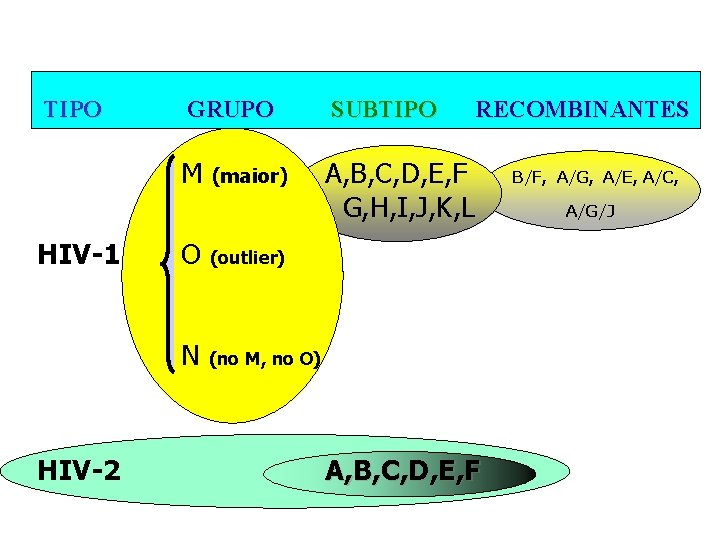
EPIDEMIOLOGIA GRUPOS, SUBTIPOS e RECOMBINANTES DE HIV- três grupos: Main (principal) (M) Outlier (O) New (N) Grupo M: vários subtipos: A a L e formas recombinantes circulantes (RCF)

TIPO HIV-1 HIV-2 GRUPO SUBTIPO M A, B, C, D, E, F G, H, I, J, K, L (maior) O (outlier) N (no M, no O) RECOMBINANTES A, B, C, D, E, F B/F, A/G, A/E, A/C, A/G/J

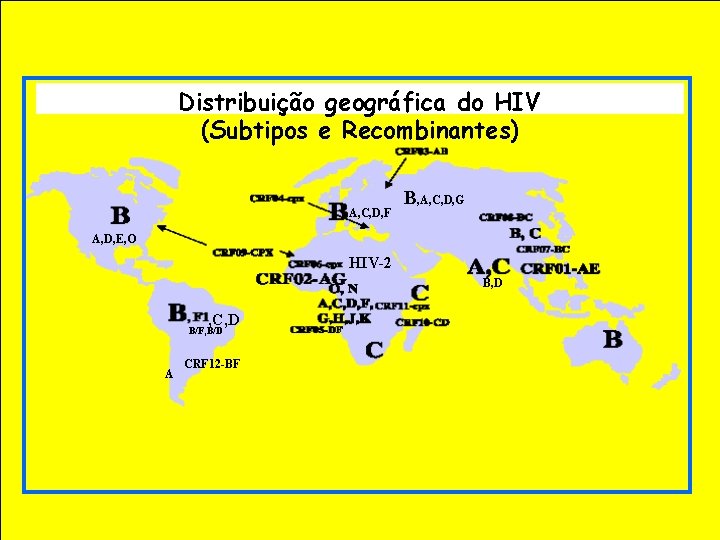
Distribuição geográfica do HIV (Subtipos e Recombinantes) A, C, D, F B, A, C, D, G A, D, E, O HIV-2 B, D , C, D B/F, B/D A CRF 12 -BF

Ø Ø Ø Ø Ø 25 milhões de mortos desde 1981. Em 2007, estimava-se que viviam com o HIV entre 30, 6 e 36, 1 milhões de pessoas. Morte ~ 2, 1 milhões sendo 330 000 crianças; e que tenham ocorrido 2, 5 milhões de novas infeções. 81 A África subsaariana é de longe a região mais afetada, 21, 6 a 27, 4 milhões de pessoas infectadas. Destes 2 milhões =>crianças com <15 anos. Mais de 64% de todas as pessoas portadoras de HIV vivem na África subsaariana, assim como mais de 75% de todas as mulheres portadoras do vírus. Em 2005 havia na região entre 10, 6 e 13, 6 milhões de órfãos em consequência da SIDA. 3 A África do Sul tem o maior número de casos de VIH no mundo, seguida pela Nigéria. Nos 35 países com a maior prevalência de VIH, a expectativa média de vida é de 48, 3 anos, ou <6, 5 anos do que seria esperado. 83 A introdução da HAART (coquetel) reduziu de forma substancial a mortalidade relacionada com o HIV nas áreas onde exista o acesso generalizado a cuidados de saúde. No entanto, à medida que aumentou a esperança de vida de portadores de VIH em países desenvolvidos, aumentaram também a probabilidade de disseminação da doença e, de forma substancial, o número de portadores vivos. 84 Fonte: http: //pt. wikipedia. org/wiki/V%C 3%ADrus_da_imunodefici%C 3%AAncia_humana

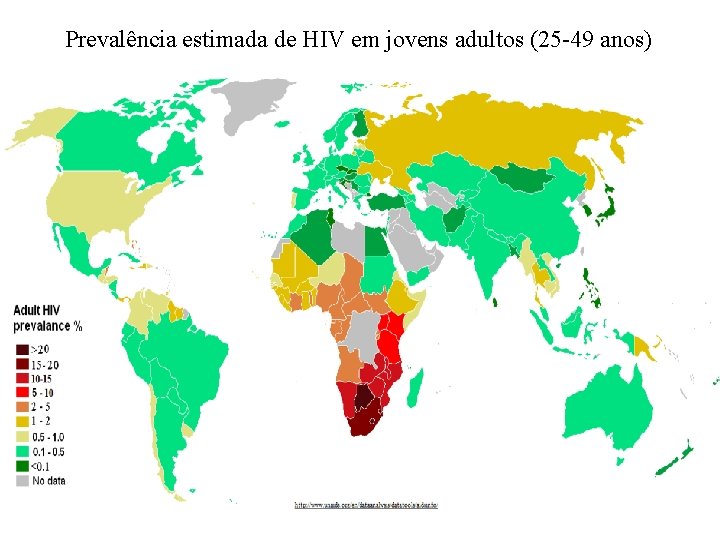
Prevalência estimada de HIV em jovens adultos (25 -49 anos)

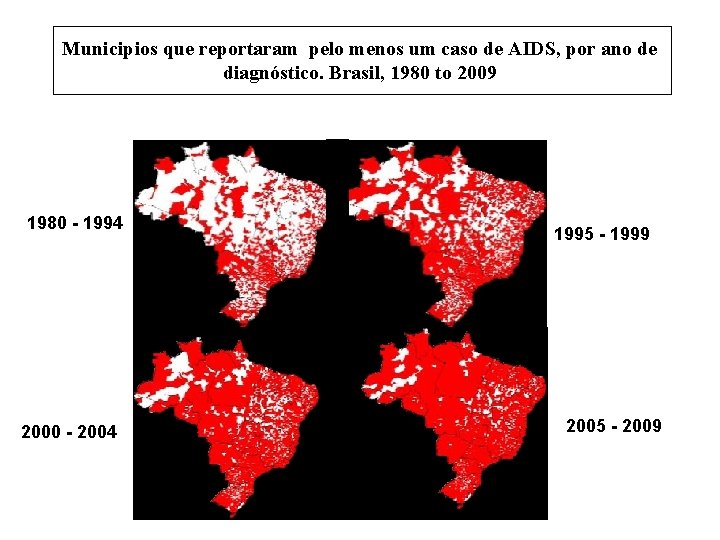
Municipios que reportaram pelo menos um caso de AIDS, por ano de diagnóstico. Brasil, 1980 to 2009 1980 - 1994 2000 - 2004 1995 - 1999 2005 - 2009

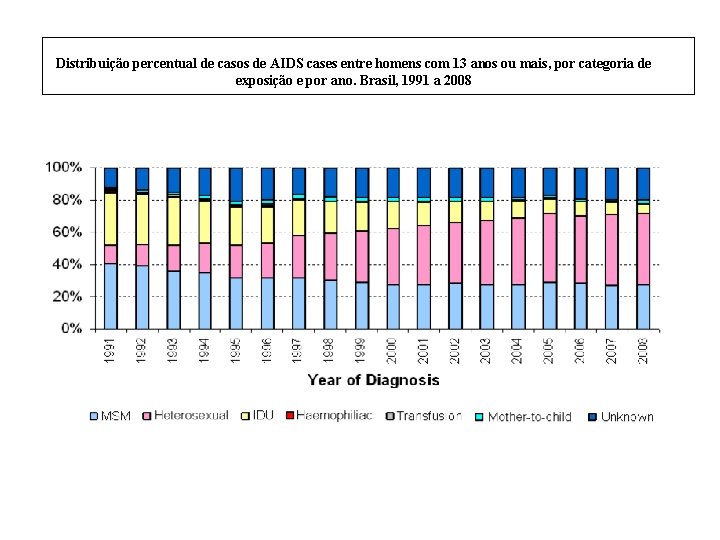
Distribuição percentual de casos de AIDS cases entre homens com 13 anos ou mais, por categoria de exposição e por ano. Brasil, 1991 a 2008

AIDS no Brasil – resumo • Epidemia concentrada: anos 80 => principalmente os usuários de drogas injetáveis, gays e outros HSH, transfusionados e receptores de produtos derivados de sangue • Anos 80 e início dos 90 => transmissão heterossexual => principal via de transmissão do HIV • Esta vem apresentando maior tendência de crescimento em anos recentes, com participação das mulheres na dinâmica da epidemia. • Além disso: • Nos últimos anos => interiorização e pauperização da epidemia => Passou dos estratos sociais de maior escolaridade para os menos escolarizados. Fonte: http: //www. aids. gov. br/data/Pages/LUMISD 3352823 PTBRIE. htm

Diagnóstico de HIV - Se a dose infectante é baixa ( p. ex. infecção c/ agulha o processo pode ser muito retardado - Antigenemia p 24 e viremia seguida de anticorpos Ig. M => doença aguda - Usar teste de captura de antígeno p 24 (ELISA) este contém anticorpos anti-p 24 na fase sólida => 30% sensibilidade

Testes específicos para detecção de infecção por HIV - Detecção de antígeno p 24 Isolamento viral Detecção de genoma viral ou DNA pró-viral Detecção de anticorpos

Diagnóstico de HIV - Isolamento viral pode ser realizado a partir de orgãos e de linfócitos periféricos - Utiliza-se co-cultivo de linfócitos do paciente com linfócitos não infectados na presença de IL-2 - A replicação viral pode ser detectada por ensaios em busca de transcriptase reversa - Isolamento somente em laboratórios com condições de segurança adequadas


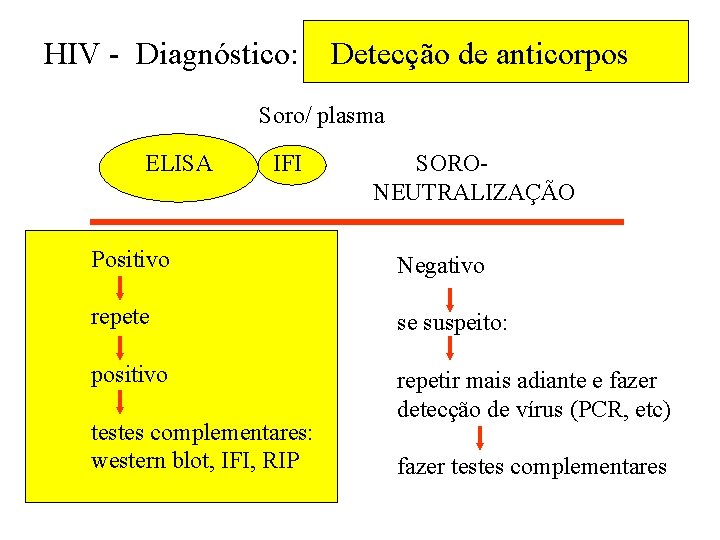
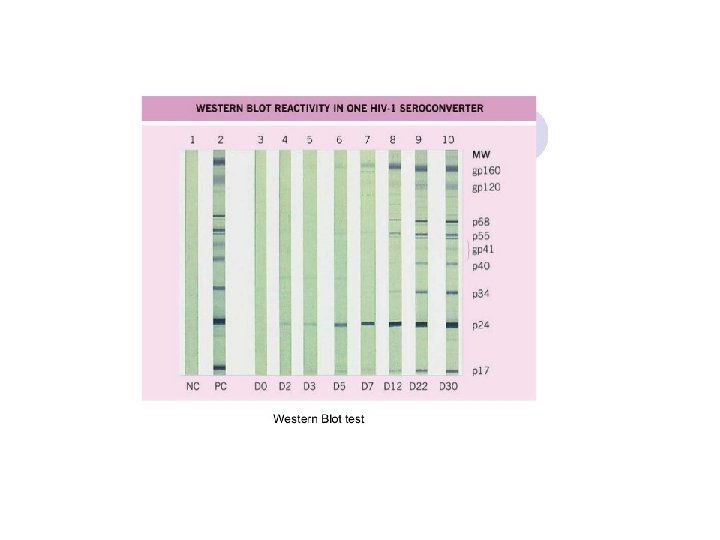
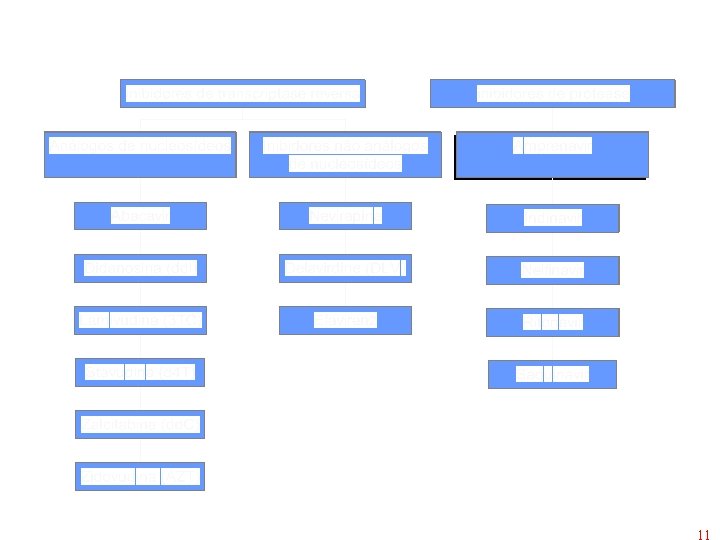
HIV - Diagnóstico: Detecção de anticorpos Soro/ plasma ELISA IFI SORO NEUTRALIZAÇÃO Positivo Negativo repete se suspeito: positivo repetir mais adiante e fazer detecção de vírus (PCR, etc) testes complementares: western blot, IFI, RIP fazer testes complementares

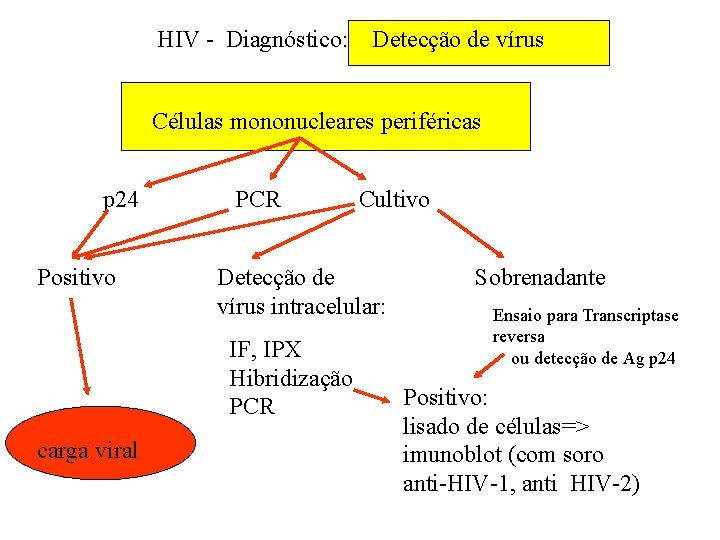
HIV - Diagnóstico: Detecção de vírus Células mononucleares periféricas p 24 PCR Cultivo Positivo Detecção de vírus intracelular: IF, IPX Hibridização PCR carga viral Sobrenadante Ensaio para Transcriptase reversa ou detecção de Ag p 24 Positivo: lisado de células=> imunoblot (com soro anti-HIV-1, anti HIV-2)


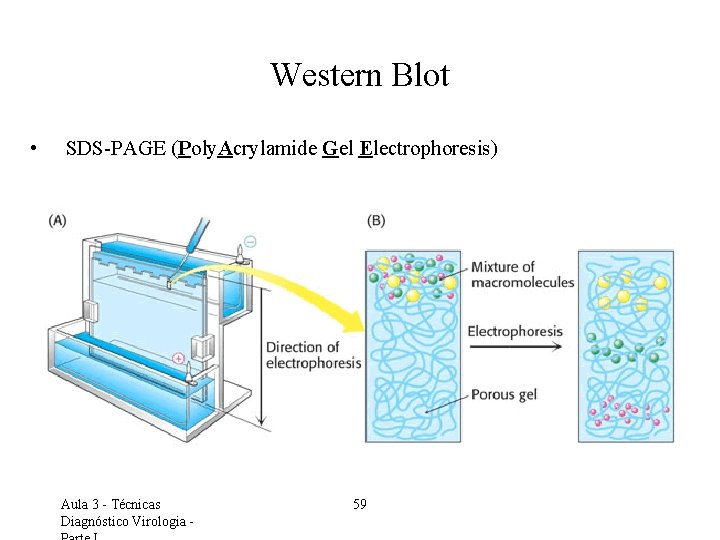
Western Blot • SDS-PAGE (Poly. Acrylamide Gel Electrophoresis) Aula 3 - Técnicas Diagnóstico Virologia - 59

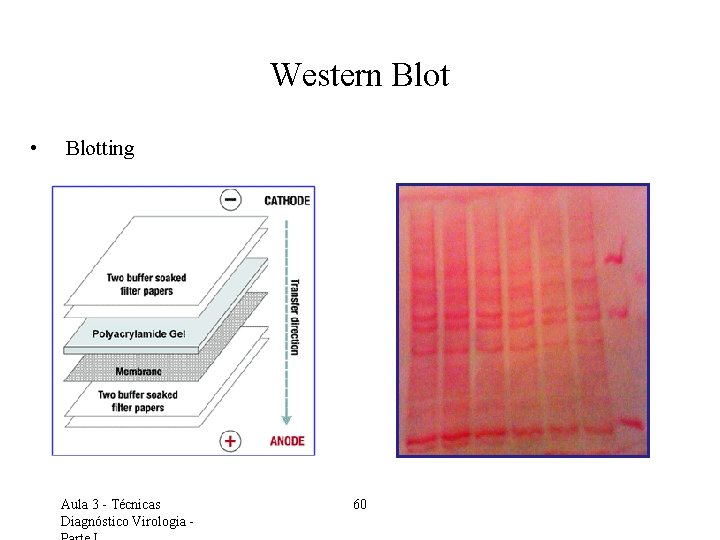
Western Blot • Blotting Aula 3 - Técnicas Diagnóstico Virologia - 60

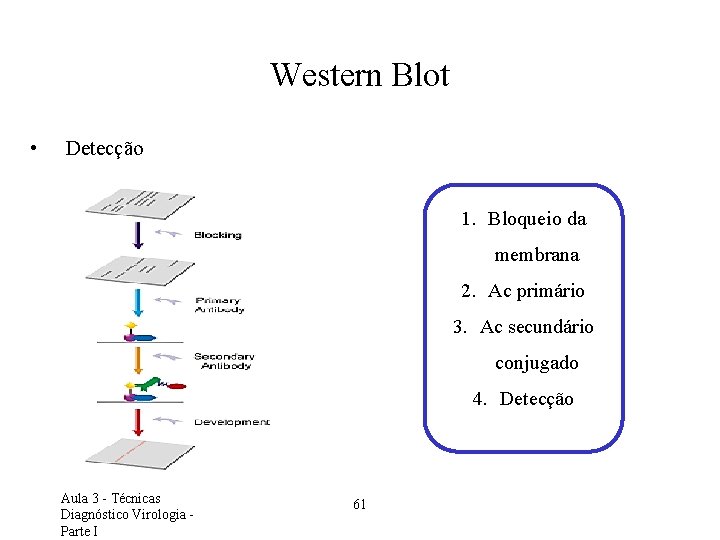
Western Blot • Detecção 1. Bloqueio da membrana 2. Ac primário 3. Ac secundário conjugado 4. Detecção Aula 3 - Técnicas Diagnóstico Virologia - Parte I 61

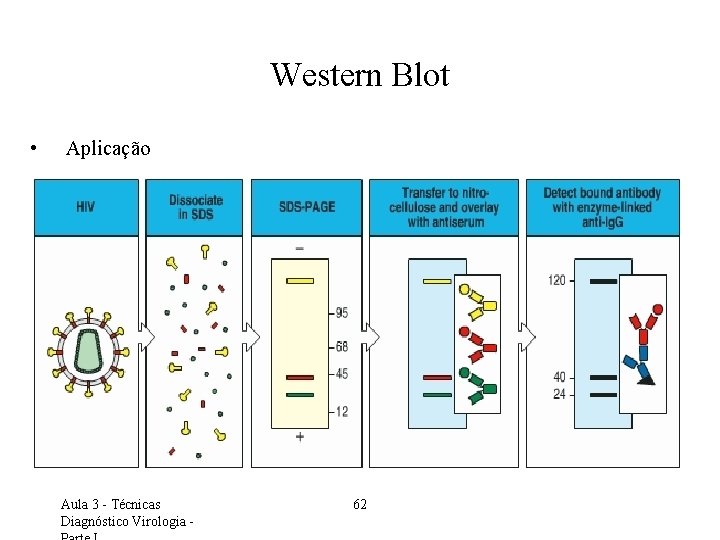
Western Blot • Aplicação Aula 3 - Técnicas Diagnóstico Virologia - 62


Testes não-específicos – HIV - Contagem total de linfócitos e leucócitos usualmente abaixo de 2000/m. L - Céls. T CD 4+ menos de 350/m. L - Trombocitopenia - Níveis de Ig. A e Ig. G elevados

HIV: Diagnóstico em crianças - até 18 -24 meses: anticorpos maternos - testes para anticorpos: falsos positivos - testar para p 24 ou PCR

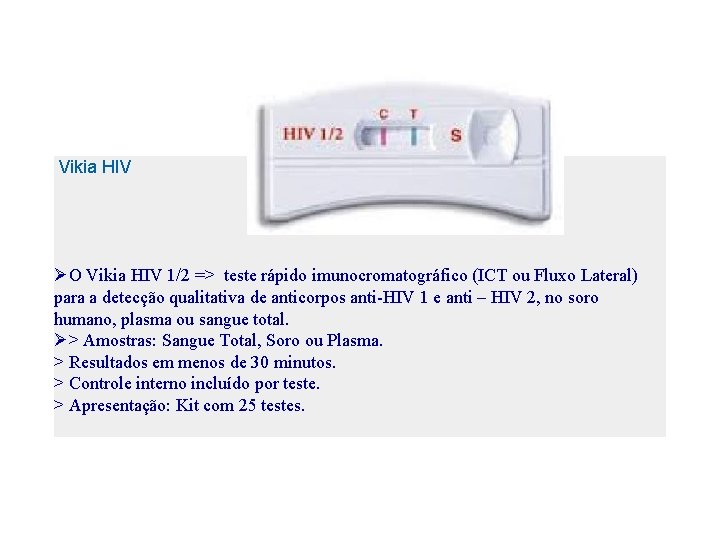
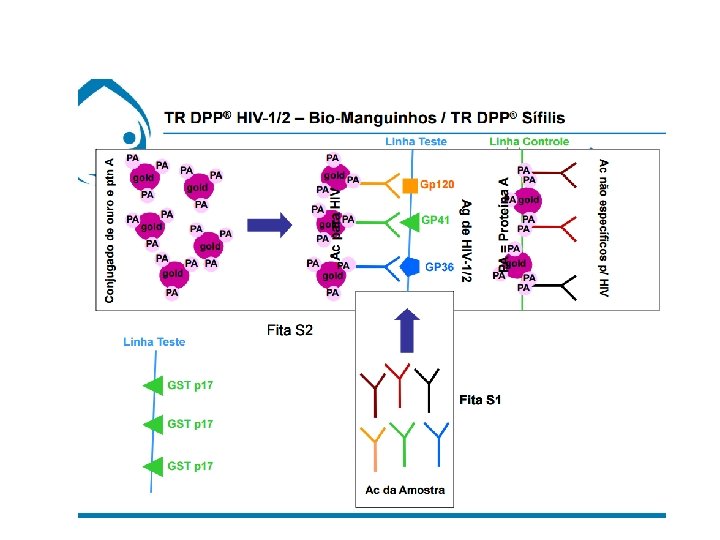
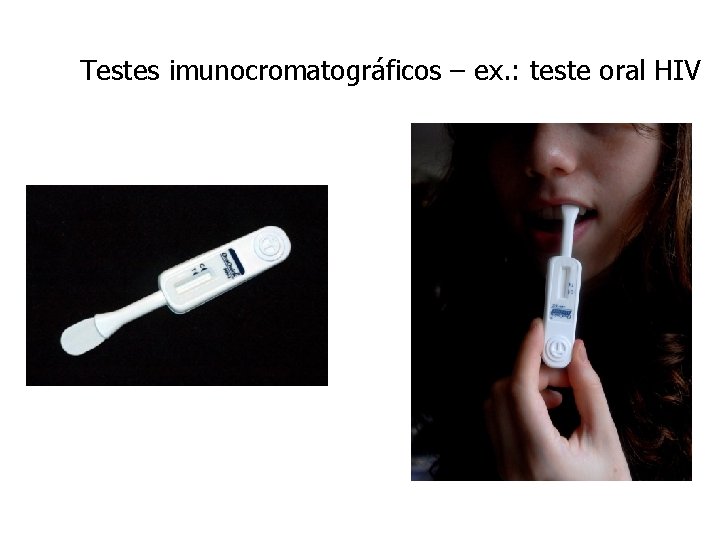
Vikia HIV ØO Vikia HIV 1/2 => teste rápido imunocromatográfico (ICT ou Fluxo Lateral) para a detecção qualitativa de anticorpos anti-HIV 1 e anti – HIV 2, no soro humano, plasma ou sangue total. Ø> Amostras: Sangue Total, Soro ou Plasma. > Resultados em menos de 30 minutos. > Controle interno incluído por teste. > Apresentação: Kit com 25 testes.



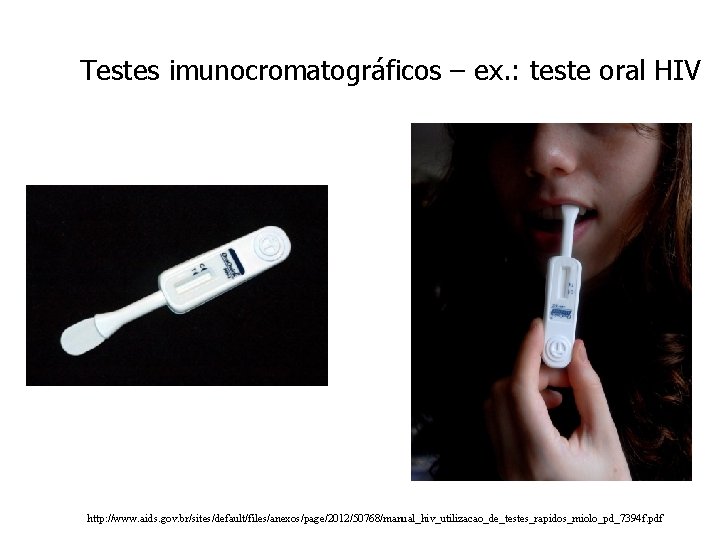
Testes imunocromatográficos – ex. : teste oral HIV http: //www. aids. gov. br/sites/default/files/anexos/page/2012/50768/manual_hiv_utilizacao_de_testes_rapidos_miolo_pd_7394 f. pdf


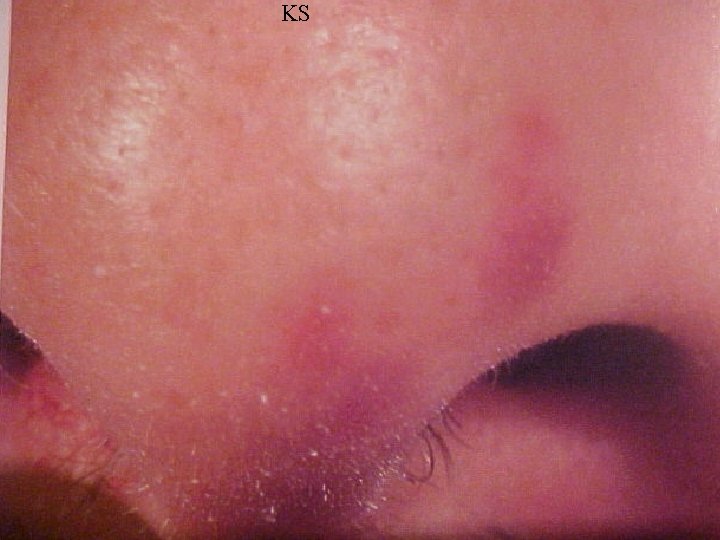
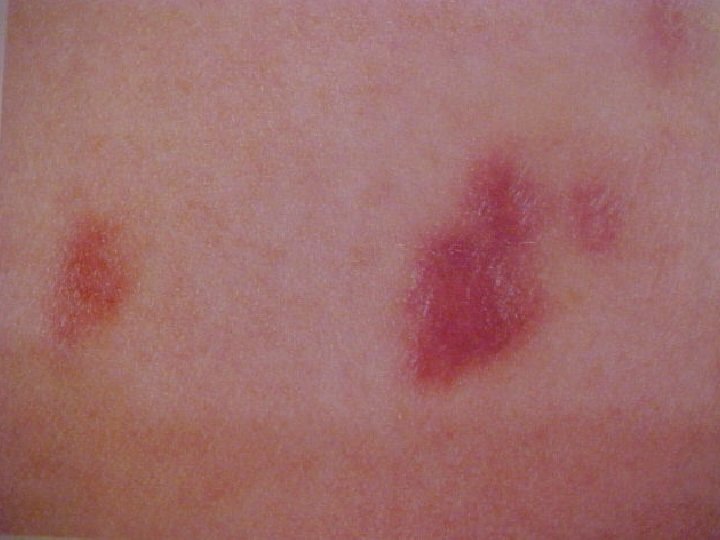
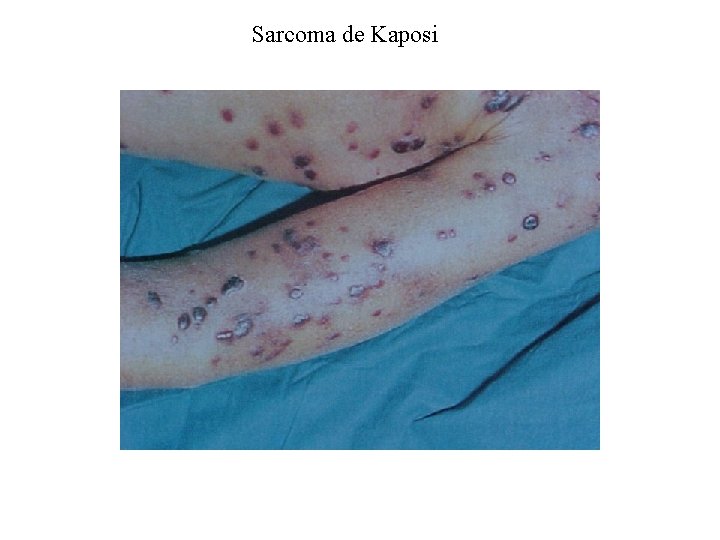
Sarcoma de Kaposi - É um tumor de células endoteliais - antigamente prevalente em homens judeus africanos e mediterrâneos - frequente em homossexuais masculinos aidéticos - pacientes apresentam uma forma muito agressiva - associado ao herpesvírus humano 8 (HHV-8; KSHV)

KS




Sarcoma de Kaposi



Tratamento - HIV positivo: monitorar a carga viral antes de tratar. - Monitorar o nível de linfócitos T CD 4. - Se CD 4 baixar de 350 iniciar o tratamento - O objetivo do tratamento é reduzir o nível de HIV no paciente

Carga viral - Estima o número de cópias do genoma viral circulando no paciente - Expresso em número de cópias do RNA de HIV/m. L. - Há vários métodos; Presentemente os testes de real time PCR, também chamados PCR quantitativa (q. PCR) - Os testes são capazes de detectar até ~50 cópias/m. L ou menos - Abaixo disso – é considerado negativo ou não detectável.

Inibidores de transcriptase reversa nucleosídicos (ITRN) AZT (zidovudine, Retrovir), dd. I (didanosine, Videx), 3 TC (lamivudine, Epivir), d 4 T (stavudine, Zerit), Abacavir (Ziagen), FTC (emtricitabine, Emtriva) Tenofovir (Viread). AZT e 3 TC combinados em uma pílula = Combivir AZT + 3 TC + abacavir em uma única pílula= Trizivir. AZT + abacavir = Kivexa. FTC(emtricitabine) + tenofovir = Truvada. FTC + tenofovir + um ITRNN chamado efavirenz (Sustiva) = Atripla

Inibidores de transcriptase reversa não-nucleosídicos (ITRNN) Efavirenz (Sustiva) Etravirine (Intelence) Nevirapine (Viramune).

Inibidores de Protease (IP) atazanavir (Reyataz), darunavir (Prezista), fosamprenavir (Telzir), indinavir (Crixivan), lopinavir/ritonavir (Kaletra), nelfinavir (Viracept), ritonavir (Norvir) saquinavir (Invirase) tipranavir (Aptivus). Todos estes tem ação potenciada pelo Ritonavir (IP/r), à exceção de Nelfinavir. Como tal devem sempre ser associados a este (IP/r = inibidor de protease + ritonavir).

Inibidores de fusão, adsorção e integrase Todos correntemente reservados para pacientes que já tomaram múltiplos anti-retrovirais: Um só inibidor de fusão: T 20 (enfuvirtide, Fuzeon). É o único que precisa ser injetável. Maraviroc (Celcentri) é um inibidor de CCR 5, bloqueando a adsorção do vírus à célula. Vicriviroc é outro inibidor de CCR 5 (em avaliação). Raltegravir (Isentress) é um inibidor de integrase.

Truvada TRUVADA é uma combinação de EMTRIVA e VIREAD (emtricitabine & tenofovir), ambos análogos nucleosídicos inibidores da transcriptase reversa do HIV-1. TRUVADA é indicado em combinação com outros anti-retrovirais em adultos ou crianças com idade maior ou igual a 12 anos. TRUVADA é indicado em combinação com práticas sexuais mais seguras para profilaxia pré-exposição (PPr. E) para reduzir o risco de HIV-1 sexualmente adquirido em adultos em grupos de comportamento de alto risco. Recentemente liberado pelo FDA para esse uso; porém, ainda não liberado para tal finalidade no Brasil.

Terapia HIV Primeira escolha de ITRN inicial: associação AZT/3 TC ITRNN, o efavirenz (EFZ) -primeira escolha. Apresenta elevada potência de supressão viral, comprovada eficácia em longo prazo e ao menor risco de efeitos adversos sérios. Em gestantes, primeira escolha: nevirapina (NVP). IP: sempre associados ao ritonavir!

Profilaxia pós-exposição: Esquema preferencial: independentemente do tipo de exposição e material biológico envolvido: Tenofovir (TDF) + Lamivudina (3 TC) + Atazanavir/ritonavir (ATV/r) Duração da PEP: 28 dias. http: //www. aids. gov. br/sites/default/files/anexos/publicacao/2015/58168/pcdt_pep_20_10_1. pdf

Transmissão materno-infantil do HIV Gestantes portadoras: iniciar tratamento a partir da 14ª semana com terapia Antiretroviral (ARV) tripla Referência: http: //www. aids. gov. br/sites/default/files/consenso_gestantes_2010_vf. pdf



HIV e vacinas - desafios O HIV integra-se no genoma celular rapidamente O HIV infecta e destrói células-chave da resposta imune As amostras de HIV isoladas são hiper-variáveis A resposta imune natural do hospedeiro não elimina a infecção Os antígenos necessários para induzir uma resposta protetora ainda são desconhecidos Testes de eficácia de vacinas são longos e complexos Fonte: Anatoli Kamali MRC/UVRI Uganda Research Unit on AIDS

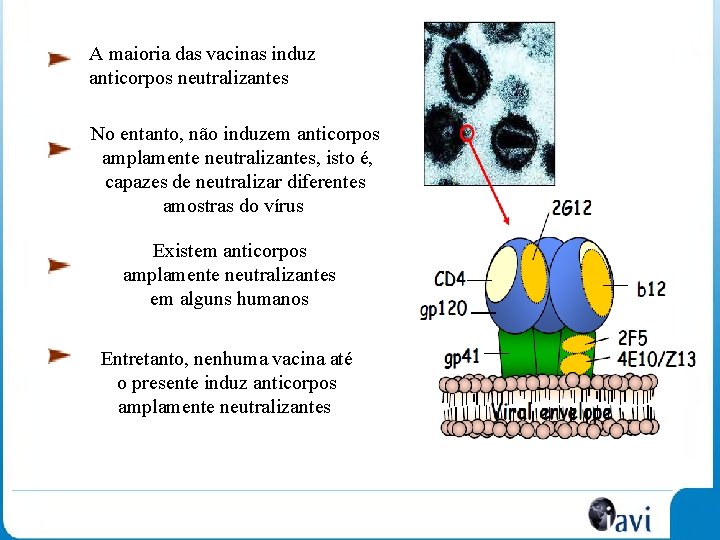
O desafio dos anticorpos neutralizantes Tipicamente, as vacinas não produzem anticorpos do tipo desejado, ou seja, anticorpos amplamente neutralizantes. Alguns indivíduos infectados naturalmente desenvolvem estes anticorpos Anticorpos amplamente neutralizantes podem ser o caminho adequado em busca de uma vacina

A maioria das vacinas induz anticorpos neutralizantes No entanto, não induzem anticorpos amplamente neutralizantes, isto é, capazes de neutralizar diferentes amostras do vírus Existem anticorpos amplamente neutralizantes em alguns humanos Entretanto, nenhuma vacina até o presente induz anticorpos amplamente neutralizantes

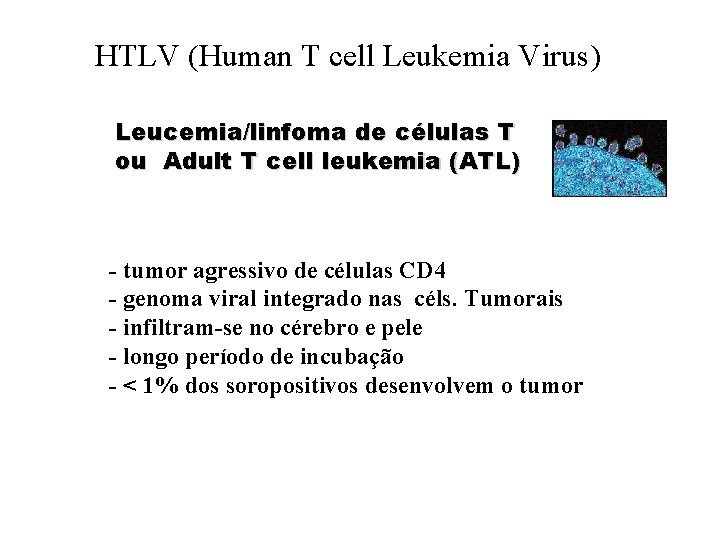
HTLV (Human T cell Leukemia Virus) Leucemia/linfoma de células T ou Adult T cell leukemia (ATL) - tumor agressivo de células CD 4 - genoma viral integrado nas céls. Tumorais - infiltram-se no cérebro e pele - longo período de incubação - < 1% dos soropositivos desenvolvem o tumor

Paraparesia espástica tropical (TSP) ou Mielopatia associada ao HTLV (HAM) - mielopatia crônica HTLV 1 paresia espástica (membros inferiores) entre 4 a e 5 a década 20 -30 anos pós-infecção > mulheres risco em portadores (HTLV +): 0, 18 a 0, 26%

Testes imunocromatográficos – ex. : teste oral HIV

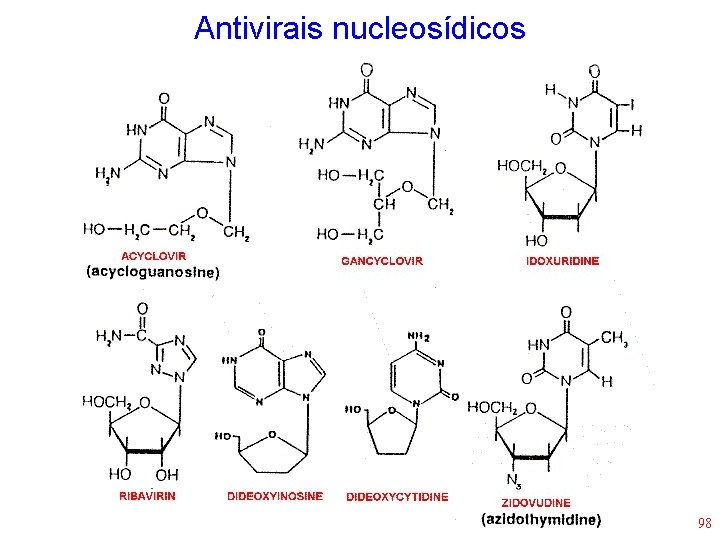
Análogos de nucleosídeos • Muitas drogas antivirais são nucleosídeos sintéticos que interferem de alguma maneira com a síntese de DNA ou RNA • Exemplos: – – – Ribavirina - Ganciclovir Aciclovir - Trifluridina Cidofovir - Didanosina (ddl) Famciclovir - Lamivudina (3 TC) Idoxuridina - Zidovudina (AZT) 97

Antivirais nucleosídicos 98

Inibidores enzimáticos • São aqueles que interferem com os processos de replicação viral, mas não são análogos de nucleosídeos • Podem inativar as enzimas virais por ligarem-se diretamente a elas ou por serem inibidores da protease • Exemplos: – Fosfato de oseltamivir - Efavirenz – Foscarnet - Indinavir – Nevirapina - Ritonavir – Delavirdine - Saquinavir 99

Nucleosídeos inibidores da transcriptase reversa • Drogas utilizadas contra retrovirus (HIV) • Uso prolonga e melhora a qualidade de vida • Não cura a infecção • Zidovudine (AZT), Abacavir (ABC) • Lamivudine (3 TC), Didanosine (ddl) • Zalcitabine (dd. C), Stavudine (d 4 T) 100

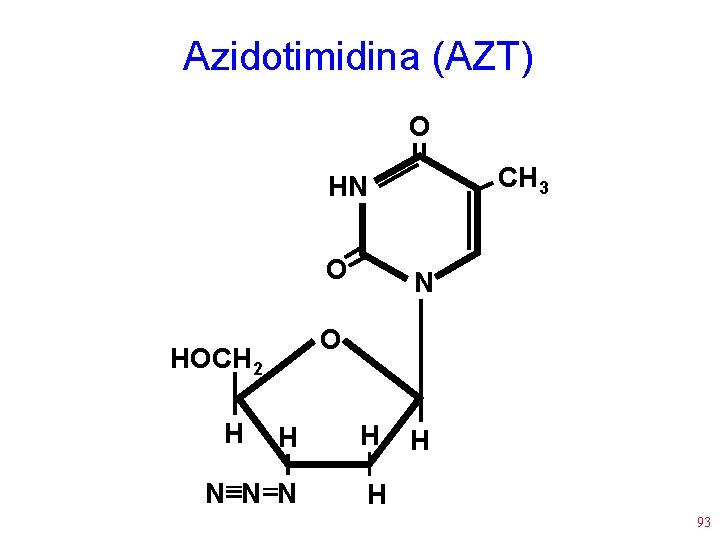
Azidotimidina (AZT) O CH 3 HN O O HOCH 2 H N H H N N N H H 93

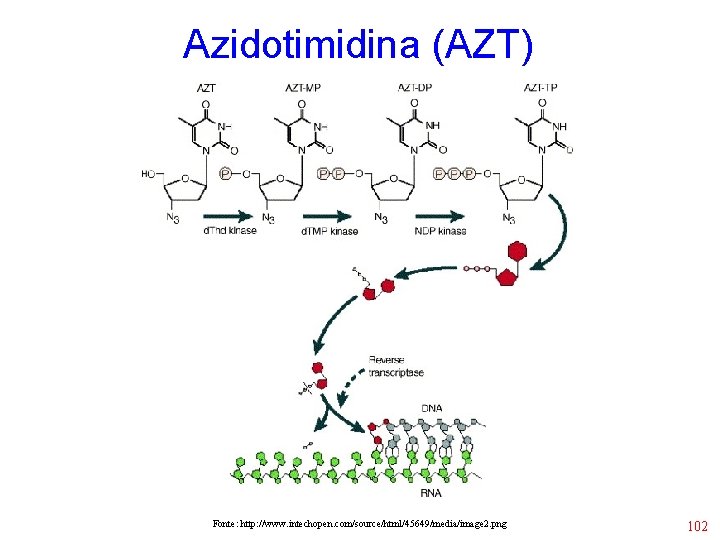
Azidotimidina (AZT) Fonte: http: //www. intechopen. com/source/html/45649/media/image 2. png 102

Azidotimidina (AZT) • Inibe a transcriptase reversa • Previne a infecção de novas células pelo HIV • Resistencia: mutação pontual que altera a transcriptase reversa • Cinética: Biodisponibilidade: 60 a 80% – Meia-vida: 1 hora / intracelular: 3 horas 103

Azidotimidina (AZT) • Efeitos colaterais: – Anemia, náusea, vomito, dor abdominal • Interação: paracetamol (inibe o metabolismo de AZT) • Uso: HIV em combinação com Lamivudine (3 TC) e NVP 104

Duovir-N • Composto contendo: Ø Lamivudine: 150 mg Ø Zidovudine: 300 mg Ø Nevirapine: 200 mg Fonte: http: //www. dropshipmd. com/wp-images/hiv/duovir-n_tablets. jpg 105

Inibidores não-nucleosídicos da transcriptase reversa • Nevirapine (NVP), Delavirdine (DLV) Efavirenz (EFZ), • Inibem diretamente a transcriptase reversa sem fosforilação intracelular • Se liga próximo sitio a catalítico causa e desnaturação • Mais potente que AZT contra HIV-1, mas não contra HIV-2 106

Não-nucleosideos inibidores da transcriptase reversa • Cinética: • Administração oral • Meia vida: 20 min no plasma • Pode prevenir a transmissão de HIV da mãe para o feto se administrado em ambos • Efeito colateral: febre, dor de cabeça, letargia, hepatite 107

Inibidores de protease • Saquinavir (SQV), Nelfanir (NFV), Indinavir (IDV), Ritonavir (RTV), Lopinavir e Aprenavir (AMP) • Se ligam a poliproteina e impedem a clivagem em proteínas funcionais • Administrado oralmente • Saquivir: meia-vida de 12 horas 108

Terapia combinada contra o HIV • Objetivos: alcançar eficácia máxima, minimizar a toxicidade pela redução da dosagem individual da droga e diminuir as chances de desenvolvimento de resistência. • Combinação usual: 1 inibidor de protease + 2 inibidores de transcriptase reversa


HAART • Highly active antiretroviral therapy Fonte: http: //www. amfar. org/uploaded. Images/_amfarorg/Articles/In_The_Lab/2013/HAART. jpg 111

HAART • Highly active antiretroviral therapy • Terapia antiretroviral agressiva com o objetivo de suprimir a carga viral no plasma • Combinação de várias drogas: • 2 NRTIs + 1 NNRTI (Z+L+Efavirenz) • 2 NRTIs + 1 ou 2 inibidor de protease (Z+L+Lopinavir) 112

Terapia combinada contra HIV 2 drogas 3 drogas AZT + ddl AZT + dd. C AZT + DLV AZT + 3 TC ddl + DLV d 4 T + ddl Ritonavir + 1 análogo de nucleotídeo Ritonavir + AZT Indinavir + AZT Norvir + AZT + 3 TC Indinavir + AZT + dd. I 11


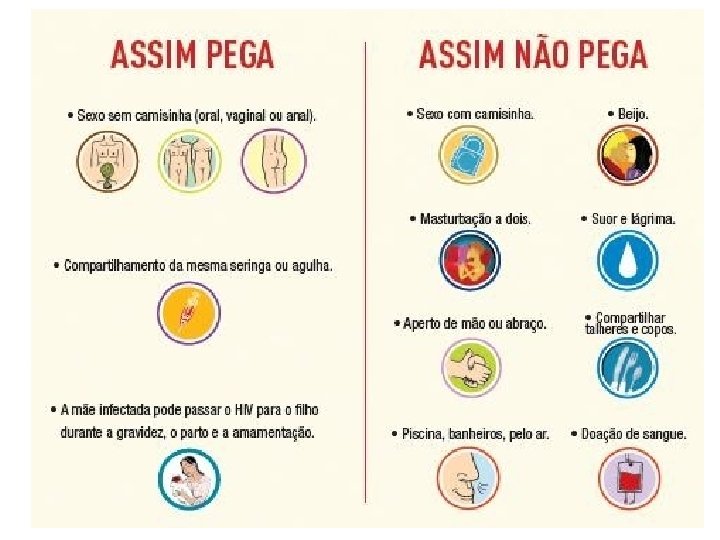
CONTROLE- PREVENÇÃO Medidas comportamentais: - educação sexual contato com infectados toxicômanos bancos de sangue e hemoderivados manuseio de sangue

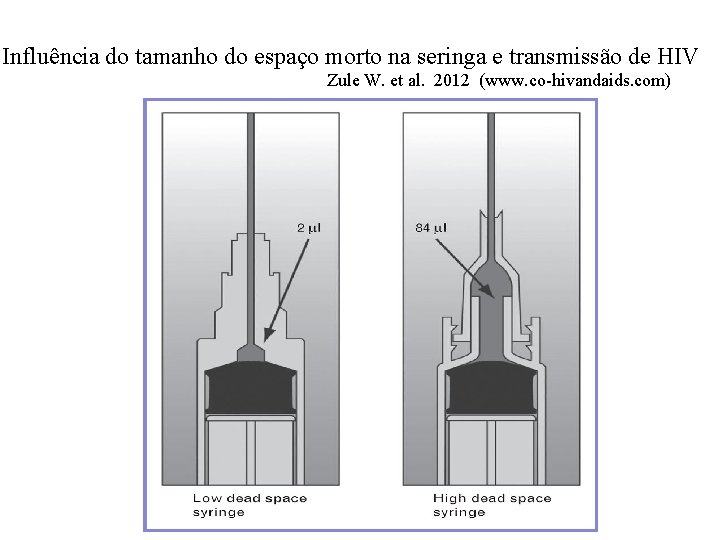
Influência do tamanho do espaço morto na seringa e transmissão de HIV Zule W. et al. 2012 (www. co-hivandaids. com)

Fonte: Dráuzio Varela

