HUBUNGAN ANTARA HIBRIDISASI DAN SUDUT IKATAN Sudut antara


HUBUNGAN ANTARA HIBRIDISASI DAN SUDUT IKATAN : Sudut antara dua ikatan s : % karakter orbital s p : % karakter orbital p
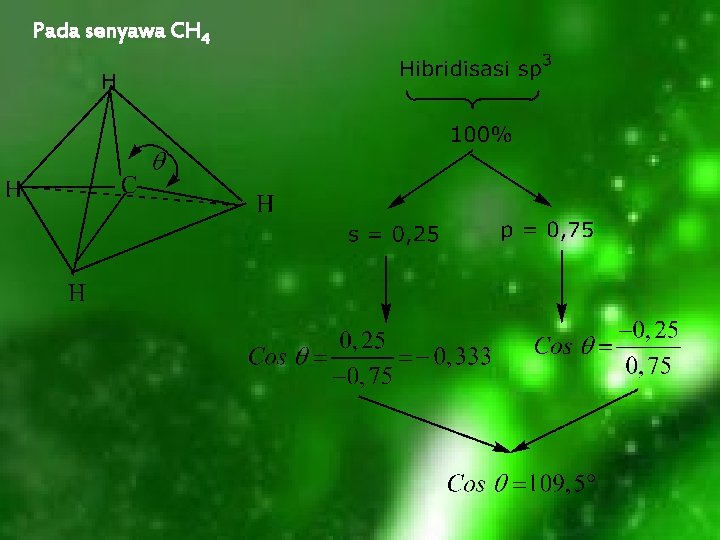
Pada senyawa CH 4
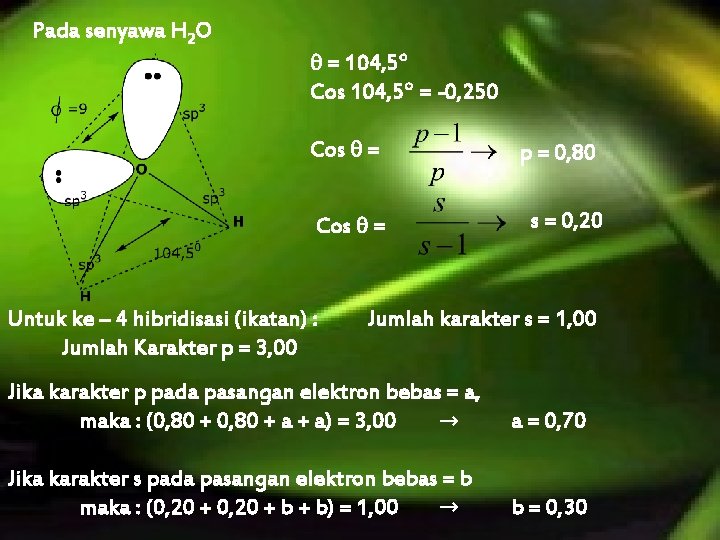
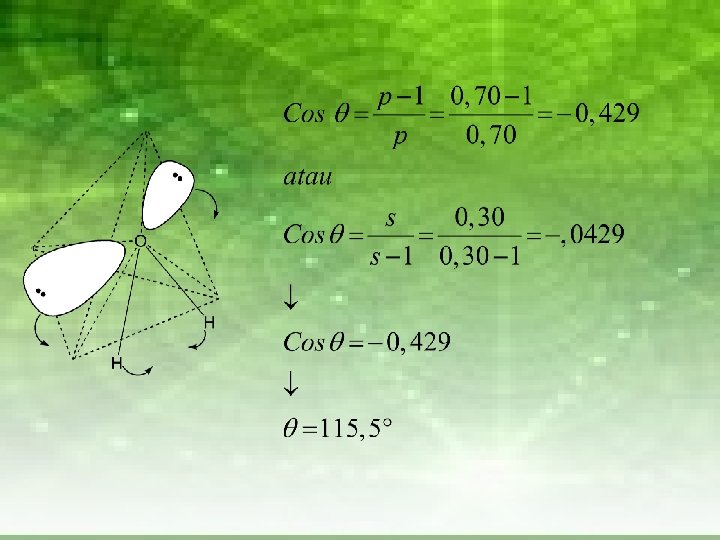
Pada senyawa H 2 O = 104, 5 Cos 104, 5 = -0, 250 Cos = p = 0, 80 Cos = s = 0, 20 Untuk ke – 4 hibridisasi (ikatan) : Jumlah Karakter p = 3, 00 Jumlah karakter s = 1, 00 Jika karakter p pada pasangan elektron bebas = a, maka : (0, 80 + a + a) = 3, 00 → a = 0, 70 Jika karakter s pada pasangan elektron bebas = b maka : (0, 20 + b + b) = 1, 00 → b = 0, 30

Karakter p non bonding < Karakter p bonding Karakter s non bonding < Karakter s bonding Makin tinggi karakter S → makin elektronegatif
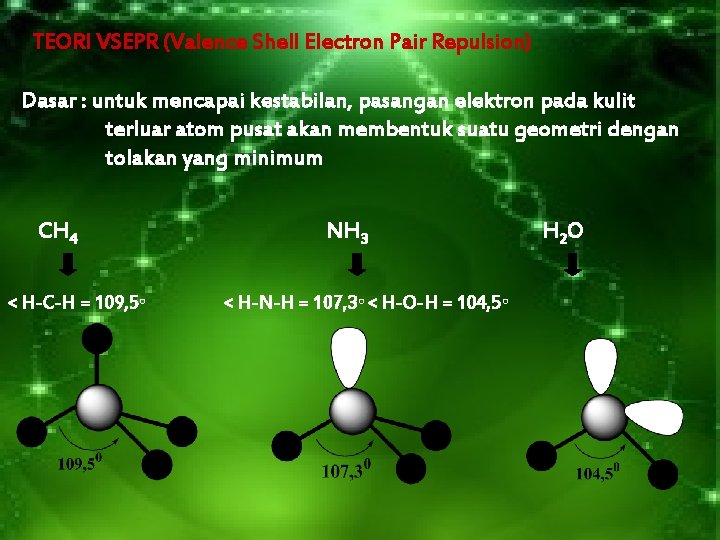
TEORI VSEPR (Valence Shell Electron Pair Repulsion) Dasar : untuk mencapai kestabilan, pasangan elektron pada kulit terluar atom pusat akan membentuk suatu geometri dengan tolakan yang minimum CH 4 < H-C-H = 109, 5◦ NH 3 < H-N-H = 107, 3◦ < H-O-H = 104, 5◦ H 2 O
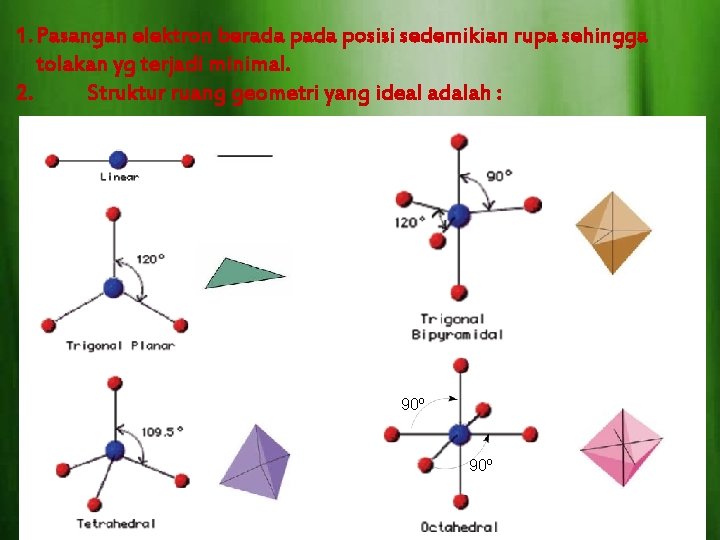
1. Pasangan elektron berada posisi sedemikian rupa sehingga tolakan yg terjadi minimal. 2. Struktur ruang geometri yang ideal adalah : 90º
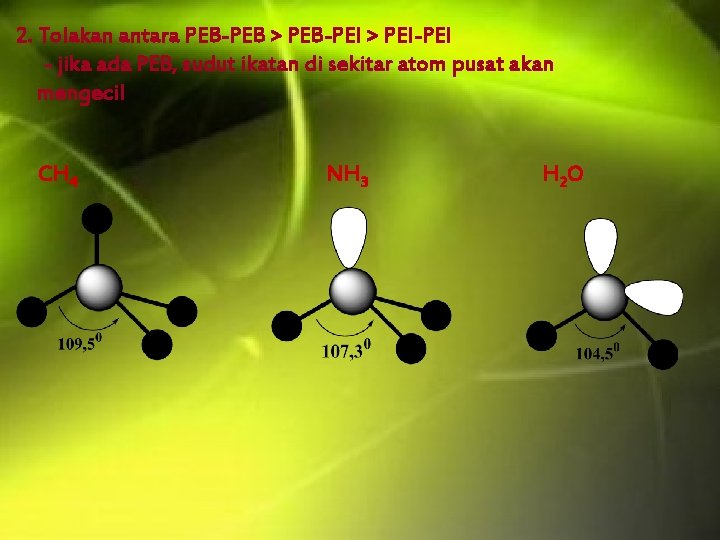
2. Tolakan antara PEB-PEB > PEB-PEI > PEI-PEI - jika ada PEB, sudut ikatan di sekitar atom pusat akan mengecil CH 4 NH 3 H 2 O
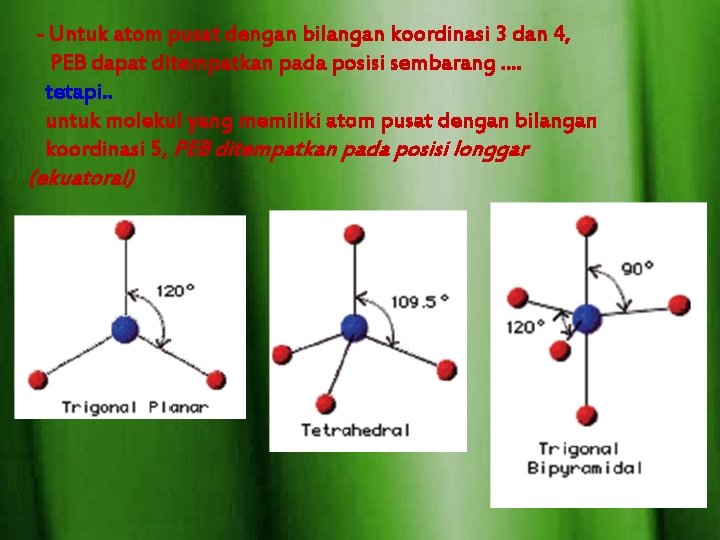
- Untuk atom pusat dengan bilangan koordinasi 3 dan 4, PEB dapat ditempatkan pada posisi sembarang. . tetapi. . untuk molekul yang memiliki atom pusat dengan bilangan koordinasi 5, PEB ditempatkan pada posisi longgar (ekuatoral)
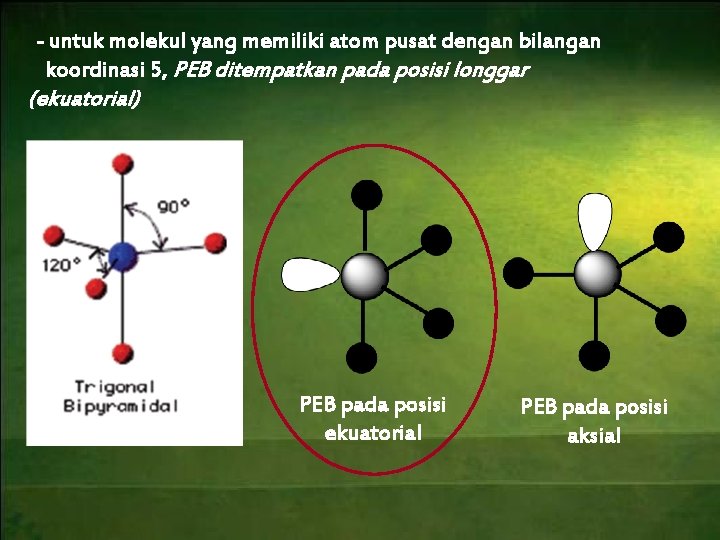
- untuk molekul yang memiliki atom pusat dengan bilangan koordinasi 5, PEB ditempatkan pada posisi longgar (ekuatorial) PEB pada posisi ekuatorial PEB pada posisi aksial
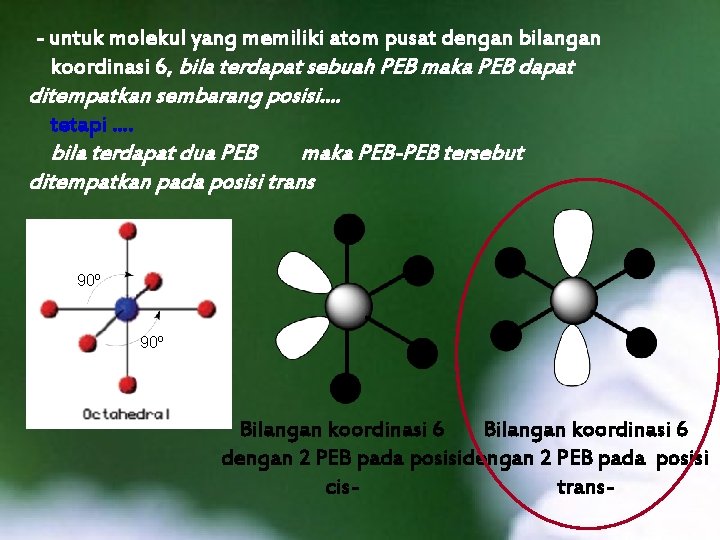
- untuk molekul yang memiliki atom pusat dengan bilangan koordinasi 6, bila terdapat sebuah PEB maka PEB dapat ditempatkan sembarang posisi. . tetapi. . bila terdapat dua PEB maka PEB-PEB tersebut ditempatkan pada posisi trans 90º Bilangan koordinasi 6 dengan 2 PEB pada posisi cistrans-
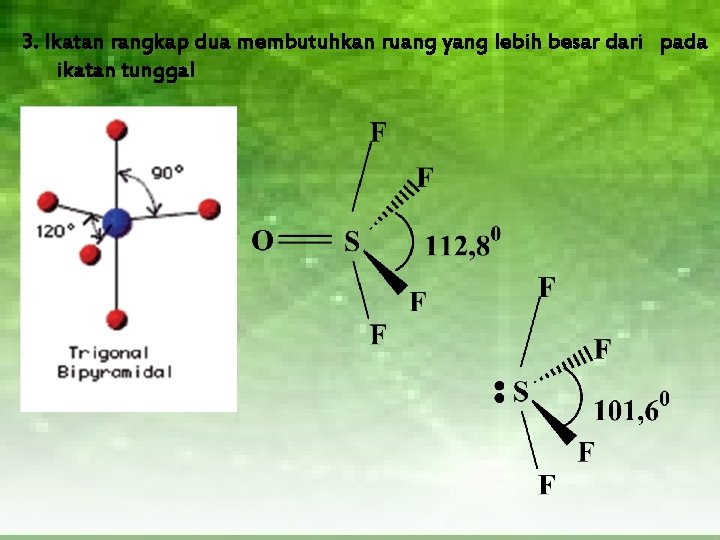
3. Ikatan rangkap dua membutuhkan ruang yang lebih besar dari pada ikatan tunggal
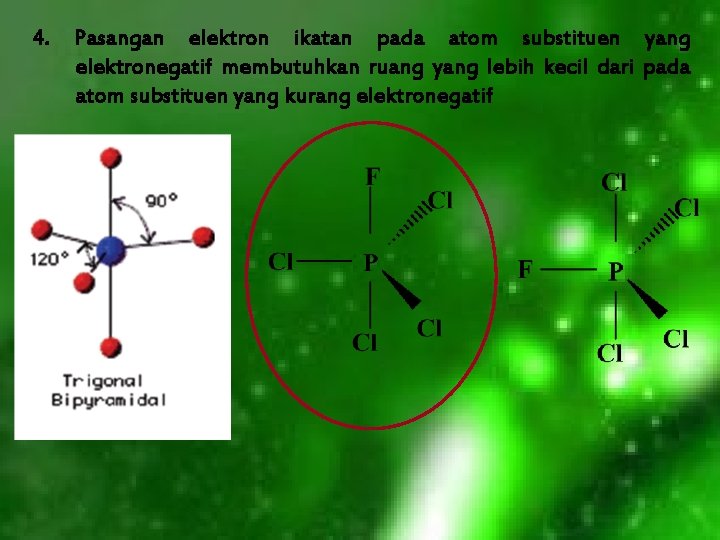
4. Pasangan elektron ikatan pada atom substituen yang elektronegatif membutuhkan ruang yang lebih kecil dari pada atom substituen yang kurang elektronegatif
TEORI VSEPR untuk meramalkan bentuk senyawa kompleks Apabila senyawa tersebut memenuhi bilangan atom efektif (Effective Atomic Number Rule = EAN Rule) Apabila harga EAN = jumlah elektron pada gas mulia Aturan EAN terpenuhi Dapat diramalkan bentuk molekulnya dengan teori VSEPR
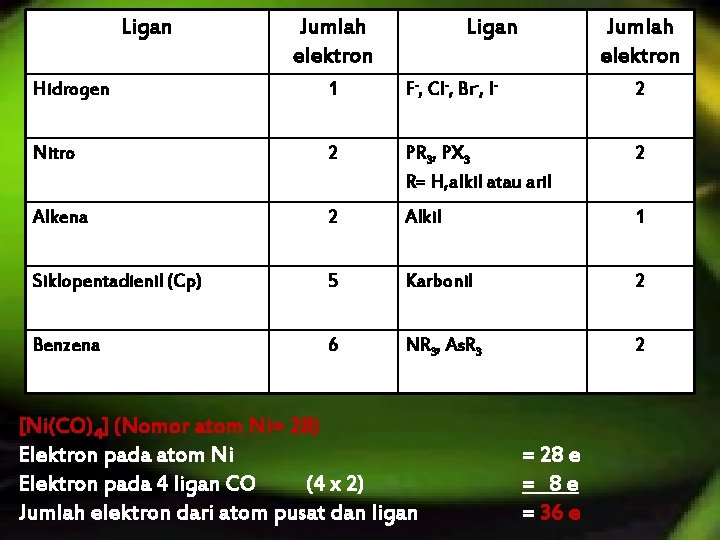
Ligan Jumlah elektron Hidrogen 1 F-, Cl-, Br-, I- 2 Nitro 2 PR 3, PX 3 R= H, alkil atau aril 2 Alkena 2 Alkil 1 Siklopentadienil (Cp) 5 Karbonil 2 Benzena 6 NR 3, As. R 3 2 [Ni(CO)4] (Nomor atom Ni= 28) Elektron pada atom Ni Elektron pada 4 ligan CO (4 x 2) Jumlah elektron dari atom pusat dan ligan = 28 e = 8 e = 36 e
![[Ni(CO)4] (Nomor atom Ni= 28) Elektron pada atom Ni Elektron pada 4 ligan CO [Ni(CO)4] (Nomor atom Ni= 28) Elektron pada atom Ni Elektron pada 4 ligan CO](http://slidetodoc.com/presentation_image_h2/9e02be8f69f9cf91eb34f25ef79996df/image-17.jpg)
[Ni(CO)4] (Nomor atom Ni= 28) Elektron pada atom Ni Elektron pada 4 ligan CO (4 x 2) Jumlah elektron dari atom pusat dan ligan = 28 e = 8 e = 36 e Tetrahedral Tentukan apakah senyawa ini dapat diramalkan bentuknya dengan menggunakan teori VSEPR ! a. [Fe(Cp)2] (no atom Fe = 26) b. [Cr(NH 3)6]3+ (no atom Cr = 24)
- Slides: 17