Htan BMEGEENATMH 5 Tbbfzis rendszerek Leidenfrosttnemny 200 240C

Hőtan BMEGEENATMH 5. Többfázisú rendszerek
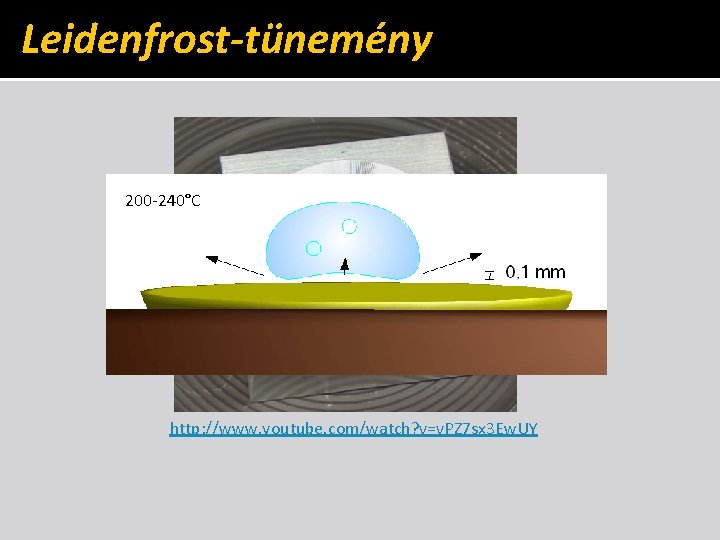
Leidenfrost-tünemény 200 -240°C http: //www. youtube. com/watch? v=v. PZ 7 sx 3 Ew. UY

Fázisátalakulások, fázisegyensúly �Elsőrendű (hőhatással járnak, ΔV és lehet Δs is) Halmazállapot változás ▪ Olvadás / fagyás: szilárd ↔ folyadék ▪ Párolgás / kondenzáció: folyadék ↔ gőz ▪ Szublimáció / deszublimáció: szilárd ↔ gőz Metastabil állapot: melegítő párna („hot ice”) Nátrium-acetát https: //www. youtube. com/watch? v=1 aec. S_gk. LUc https: //www. youtube. com/watch? v=mx. O 9 rt. Vjo. R 4 Átkristályosodás: szilárd ↔ szilárd

Fázisátalakulások, fázisegyensúly �Másodrendű (nincs hőhatás, nincs „Δ”) He szuperfolyékonnyá válik : 4 He a folyékony héliumot hűtve az néhány kelvin körül súrlódás nélkül képes áramlani (http: //www. youtube. com/watch? v=2 Z 6 UJbwx. BZI) Mágnesesség ferromágneses→paramágneses, dia~ a mágneses anyagok, pl. vas, bizonyos hőmérsékletre hevítve elvesztik mágnesességüket (Curie – hőmérséklet) (https: //www. youtube. com/watch? v=r. Og. GJa. O 5 C 00) Szupravezetés alacsony hőmérsékleten egyes anyagok elektromos ellenállása hirtelen nullára esik, és „kizárják magukból a mágneses mezőt” https: //www. youtube. com/watch? v=BGNM 6 i. Ch. Kk. U https: //www. youtube. com/watch? v=GHt. Aw. QXVsuk https: //www. youtube. com/watch? v=j. J 1 k. Wk. GCaek �Egyensúly dinamikus, feltétele: p, T, µ
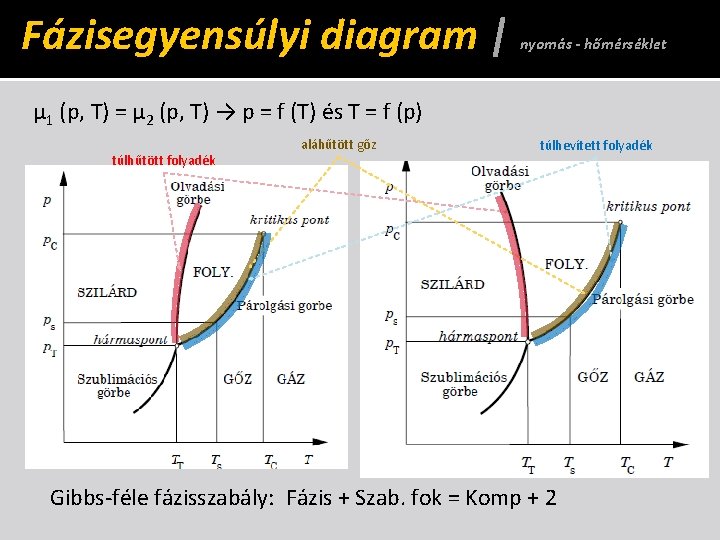
Fázisegyensúlyi diagram | nyomás - hőmérséklet µ 1 (p, T) = µ 2 (p, T) → p = f (T) és T = f (p) túlhűtött folyadék aláhűtött gőz túlhevített folyadék Gibbs-féle fázisszabály: Fázis + Szab. fok = Komp + 2

Szuperkritikus állapot http: //www. youtube. com/watch? v=GEr 3 Nxs. PTOA
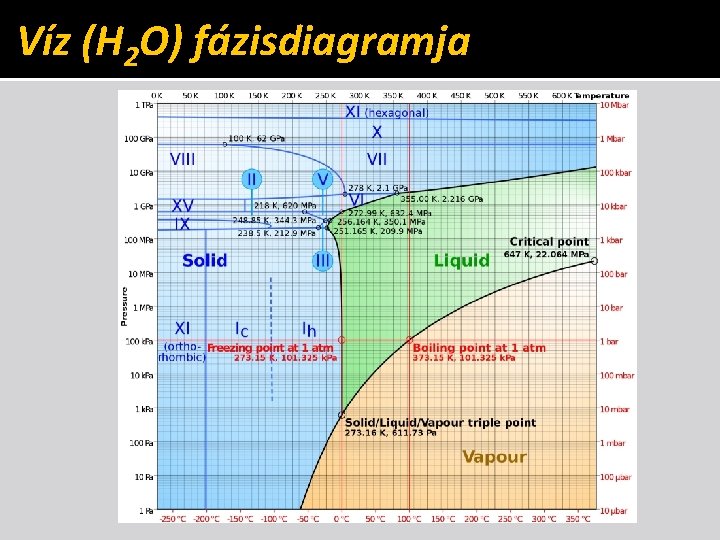
Víz (H 2 O) fázisdiagramja
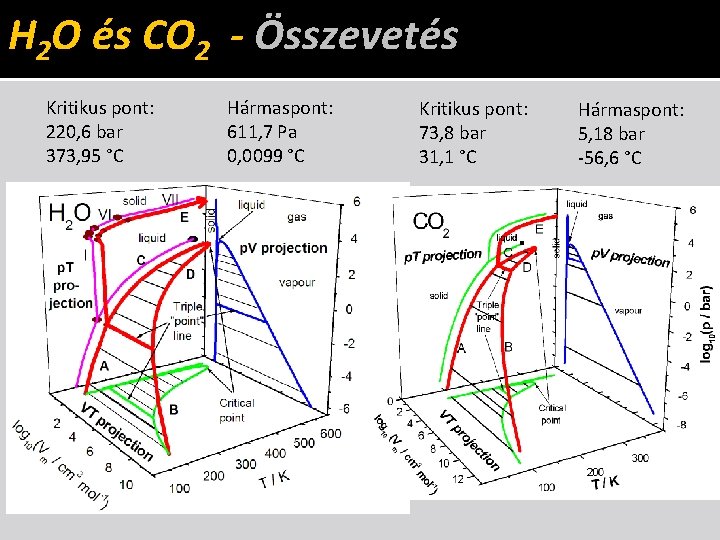
H 2 O és CO 2 - Összevetés Kritikus pont: 220, 6 bar 373, 95 °C Hármaspont: 611, 7 Pa 0, 0099 °C Kritikus pont: 73, 8 bar 31, 1 °C Hármaspont: 5, 18 bar -56, 6 °C

Mit tud a víz. . . „Brutális” Fizika
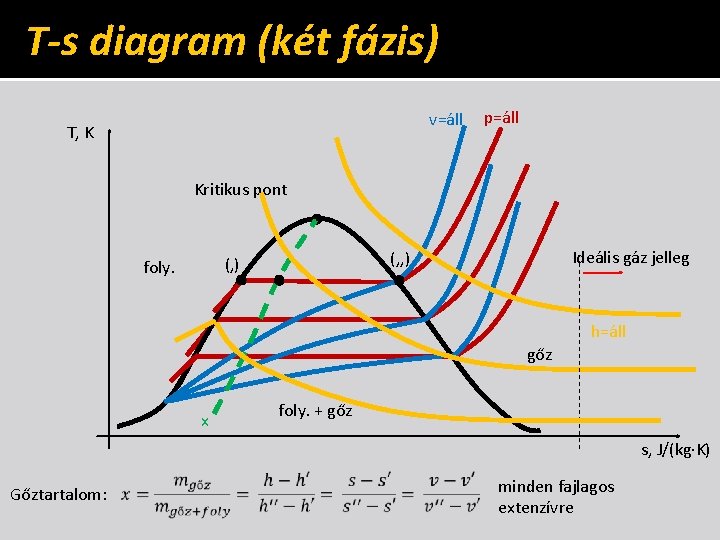
T-s diagram (két fázis) v=áll T, K p=áll Kritikus pont Ideális gáz jelleg (‚‚) (‚) foly. h=áll gőz x foly. + gőz s, J/(kg·K) Gőztartalom: minden fajlagos extenzívre
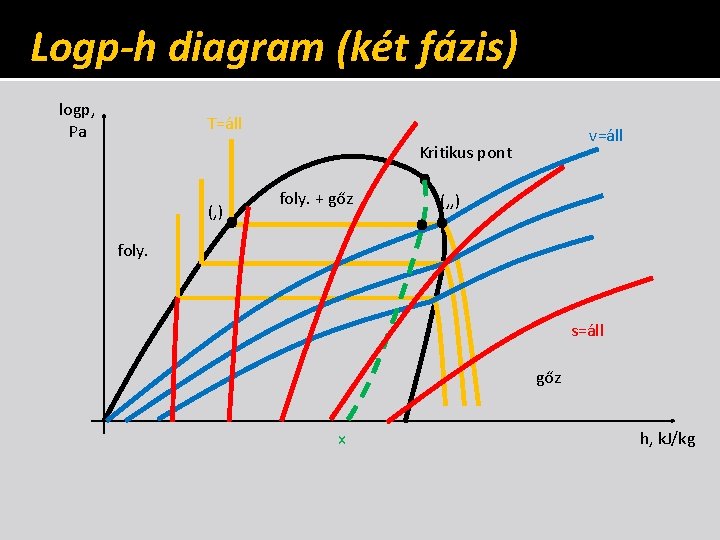
Logp-h diagram (két fázis) logp, Pa T=áll v=áll Kritikus pont (‚) foly. + gőz (‚‚) foly. s=áll gőz x h, k. J/kg
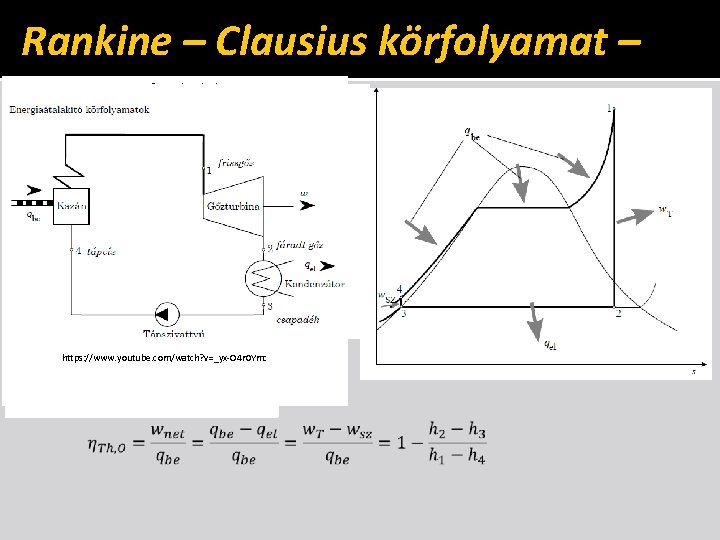
Rankine – Clausius körfolyamat – elméleti Veszteségmentes https: //www. youtube. com/watch? v=_yx-O 4 r 0 Ymc https: //www. youtube. com/watch? v=i 7 Sm. VAOXs_I

Munkagépek �Hűtőgép �Hőszivattyú �Megvalósításuk: Fordított Carnot-körfolyamat kétfázisú rendszerben (Fordított Brayton-körfolyamat) Kompresszoros hűtőkörfolyamat
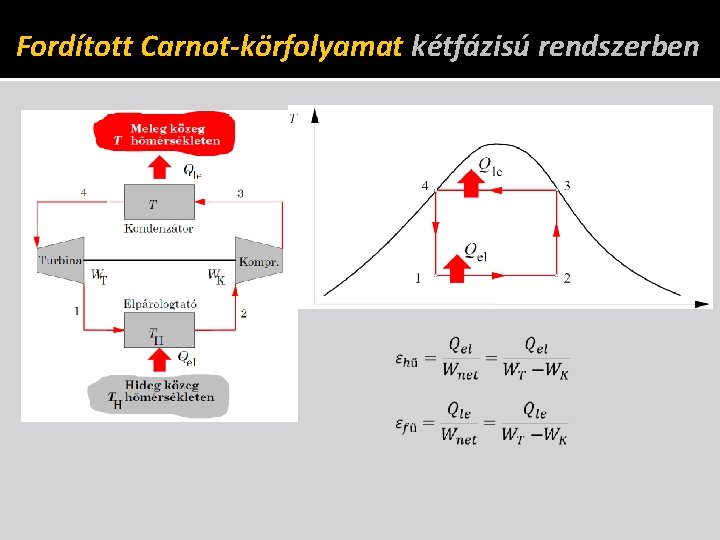
Fordított Carnot-körfolyamat kétfázisú rendszerben
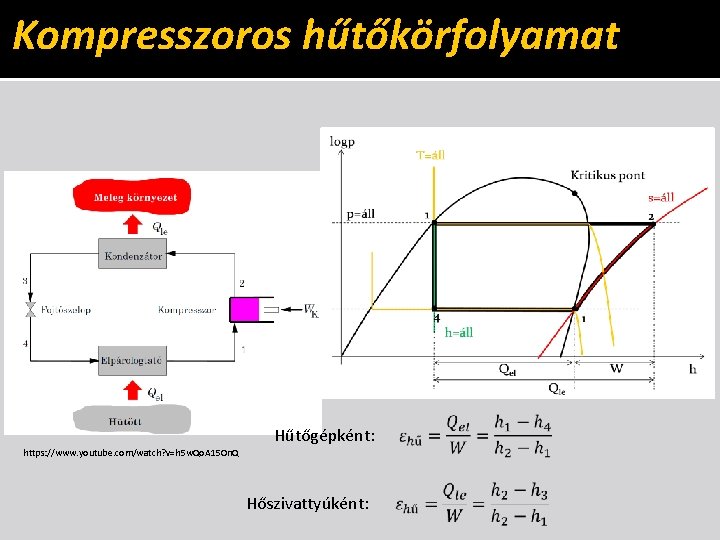
Kompresszoros hűtőkörfolyamat Hűtőgépként: https: //www. youtube. com/watch? v=h 5 w. Qo. A 15 On. Q Hőszivattyúként:

HŐTAN BMEGEENATMH Termodinamika Részösszefoglalás Hőközlés ráhangolódás

Termodinamika részösszefoglalás � Ideális gáz � Többfázisú rendszerek � TDR leírása Állapothatározók: p, V, T, m, U, H, S Anyagjellemzők: cp, cv, R, κ Transzportmennyiségek: W, Q � Főtételek 0. Egyensúly 1. Energia-megmaradás 2. Munka és a hő egyenértékűsége 3. Anyagok viselkedése 0 K-en � Körfolyamatok Munkaszolgáltatók: hatásfok Munkát igénylők (fordított ~): teljesítmény tényezők

TERMODINAMIKA - Hőközlés �Termodinamika: MENNYI? �Hőközlés: + HOGYAN? Hősugárzás (radiáció) Hővezetés (kondukció) Hőszállítás (konvekció) �Mitől függ? } HŐÁTADÁS Állapothatározók, anyagjellemzők Geometria Áramlási viszonyok

Hőközlés Ráhangolódás �Hőközlés hol? https: //www. yout ube. com/watch? v =2 vk 5 B 6 Gga 10 https: //www. youtube. com/watch? v=T bdm 3 Pq. Nx. V 8 https: //www. youtube. com/watch? v=Xq. A 8 sr. YTtbk https: //www. youtube. com/watch? v=BLGmwe 3 wt 0 Y
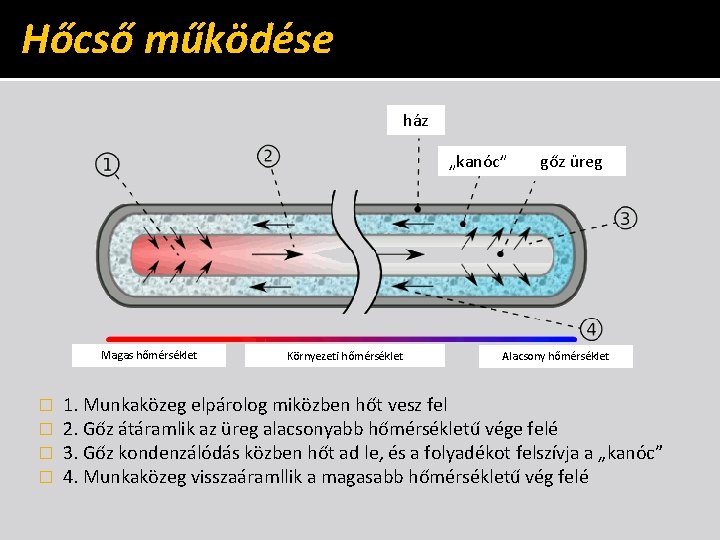
Hőcső működése ház „kanóc” Magas hőmérséklet � � Környezeti hőmérséklet gőz üreg Alacsony hőmérséklet 1. Munkaközeg elpárolog miközben hőt vesz fel 2. Gőz átáramlik az üreg alacsonyabb hőmérsékletű vége felé 3. Gőz kondenzálódás közben hőt ad le, és a folyadékot felszívja a „kanóc” 4. Munkaközeg visszaáramllik a magasabb hőmérsékletű vég felé
- Slides: 20