HIV diagnostic virologique et suivi des patients infects

































- Slides: 49

HIV: diagnostic virologique et suivi des patients infectés Cours D 1 2011 -2012

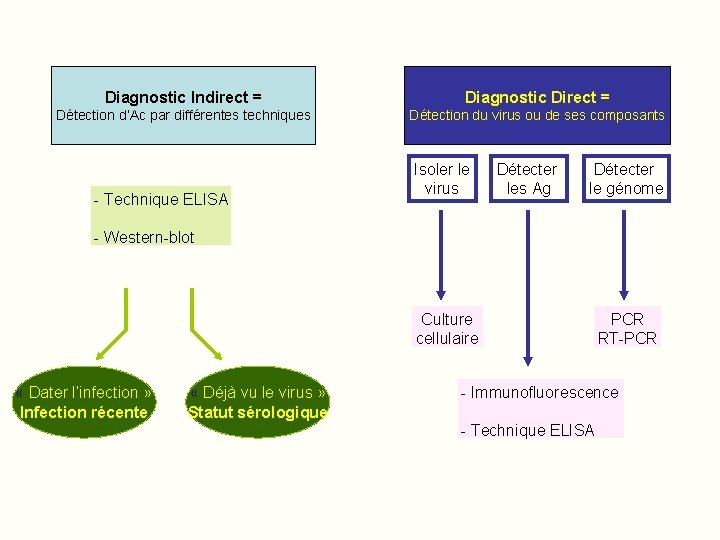
Diagnostic Indirect = Diagnostic Direct = Détection d’Ac par différentes techniques Détection du virus ou de ses composants - Technique ELISA Isoler le virus Détecter les Ag Détecter le génome - Western-blot Culture cellulaire « Dater l’infection » Infection récente « Déjà vu le virus » Statut sérologique PCR RT-PCR - Immunofluorescence - Technique ELISA

DIAGNOSTIC ET SUIVI VIROLOGIQUES HIV q Techniques q Diagnostic virologique d’une infection VIH chez l’adulte q Suivi virologique d’un sujet infecté par le VIH

Les techniques 1) Techniques de diagnostic indirect Ø Techniques de recherche des anticorps anti VIH q Tests de dépistage : techniques ELISA q Tests rapides q Tests de confirmation: test sur bandelette (Western blot ou test apparenté) 2) Techniques de diagnostic direct Ø Techniques permettant la mise en évidence du virus lui-même: q Antigénémie P 24 q ARN plasmatique q DNA proviral Ø Tests de résistance du virus aux ARV: technique de séquençage

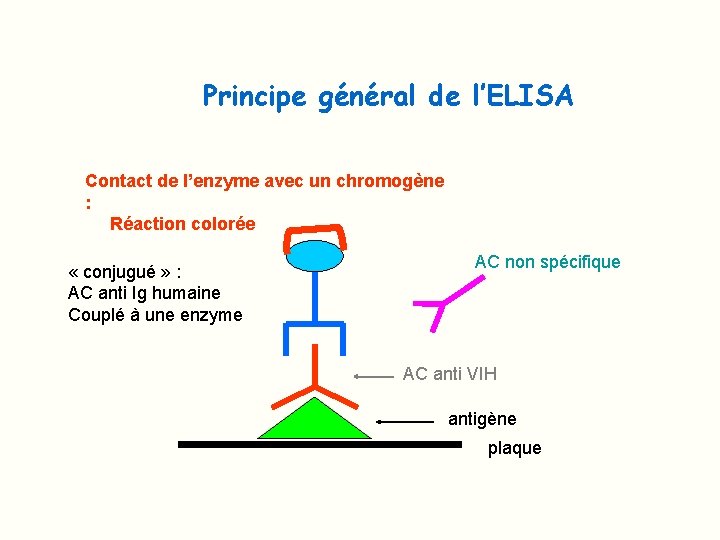
Principe général de l’ELISA Contact de l’enzyme avec un chromogène : Réaction colorée « conjugué » : AC anti Ig humaine Couplé à une enzyme AC non spécifique AC anti VIH antigène plaque

Principe de l’ELISA - phase solide revêtue d'antigènes VIH - les anticorps anti-VIH se lient sur les antigènes - révélation par : . des Ac anti-Ig humaines conjugués à une enzyme. puis le substrat chromogène est ajouté si Ac anti-VIH : coloration de la cupule grâce à un chromogène soluble

Test de dépistage VIH = technique ELISA Tests ELISA de 4ème génération: Caractéristiques: Ø Test mixte = HIV 1 et HIV 2 Ø Test combiné = détecte § les AC § et en même temps l’antigène p 24 Particularité de ce dépistage VIH

Tests rapides Test immunochromatographique ou par immunofiltration: Ø Antigènes recombinants et peptides de synthèse immobilisés sur une membrane Ø Dépôt du sérum contenant éventuellement des AC spécifiques Ø Migration du sérum jusqu’aux AG immobilisés Ø Liaison des AC avec les Ag donnant une coloration visible à l’œil nu Ø Moins sensibles que l’ ELISA Ø Détection des AC anti VIH 1 et 2 (pas de détection de l’Ag p 24)

Principe du TDR Bande témoin Bande HIV - + Immuno - chromatographie Test Determine Immuno - filtration Test INSTI

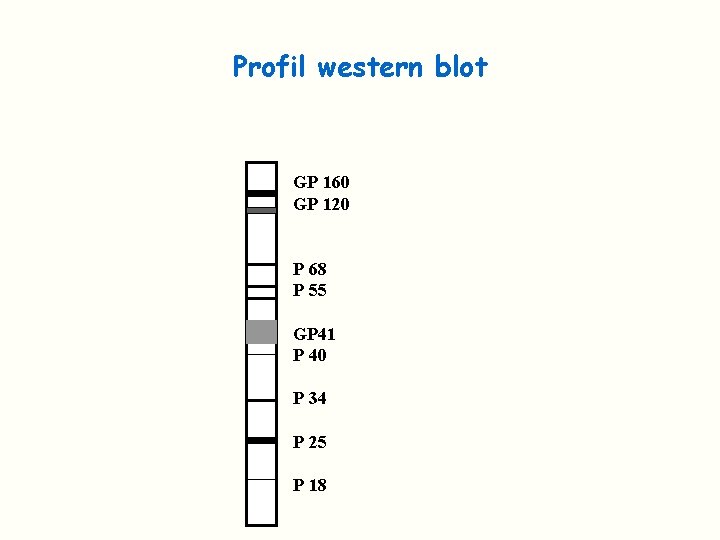
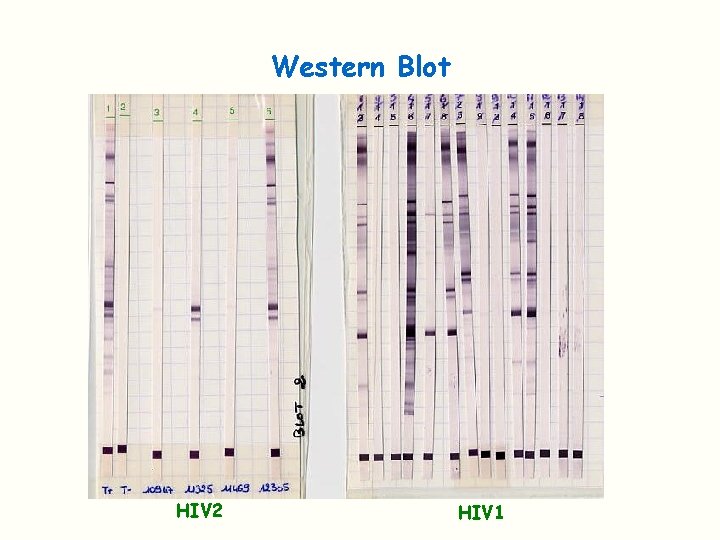
Test de confirmation Confirme la spécificité antigénique des anticorps détectés en ELISA Le test utilisé classiquement est le Western Blot On peut également utiliser un immunoblot avec des protéines recombinantes et des peptides synthétiques Bandelette de nitrocellulose sur laquelle les principaux antigènes viraux sont séparés et disposés en bande Lorsque les AC correspondants sont présents dans le sérum: réaction Ag/Ac et visualisation de la bande Des critères de positivité ont été définis (OMS)

Profil western blot GP 160 GP 120 P 68 P 55 GP 41 P 40 P 34 P 25 P 18

Western Blot HIV 2 HIV 1

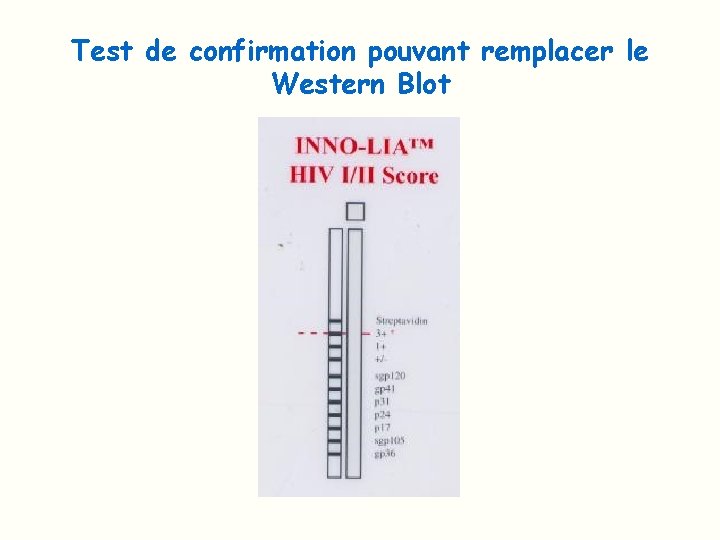
Test de confirmation pouvant remplacer le Western Blot

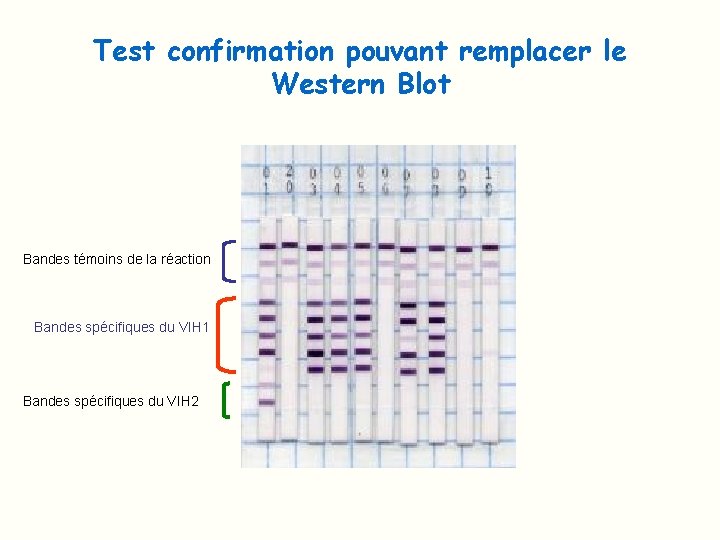
Test confirmation pouvant remplacer le Western Blot Bandes témoins de la réaction Bandes spécifiques du VIH 1 Bandes spécifiques du VIH 2

Techniques de mise en évidence du virus Ø Antigénémie P 24 Ø Quantification de l’ARN VIH plasmatique = charge virale plasmatique Ø Recherche (quantification) du DNA proviral

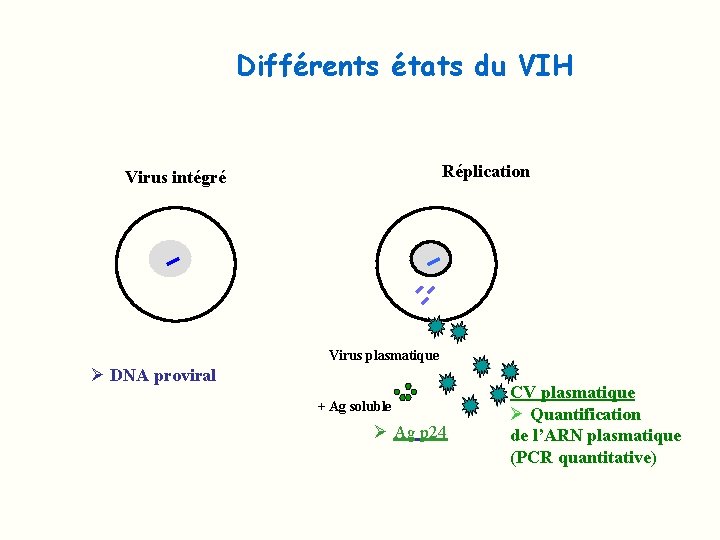
Différents états du VIH Réplication Virus intégré Virus plasmatique Ø DNA proviral + Ag soluble Ø Ag p 24 CV plasmatique Ø Quantification de l’ARN plasmatique (PCR quantitative)

Antigénémie P 24 Ø L'antigénémie P 24 constitue un marqueur de réplication virale Ø Elle détecte les antigènes solubles produits en même temps que les particules virales lors de la réplication virale Ø La technique est un test ELISA qui met en évidence les antigènes HIV présents dans le sang

Charge virale Ø Dans le sang, évaluation de la charge virale : cellulaire : quantité de virus dans les cellules mononuclées = réservoir de virus plasmatique : quantité de virus libre dans le plasma = marqueur de réplication Ø Ces charges virales cellulaires et plasmatiques peuvent être évaluées par : des techniques de culture en dilution limite abandonnées au profit des techniques de biologie moléculaire Basées sur le principe de la PCR

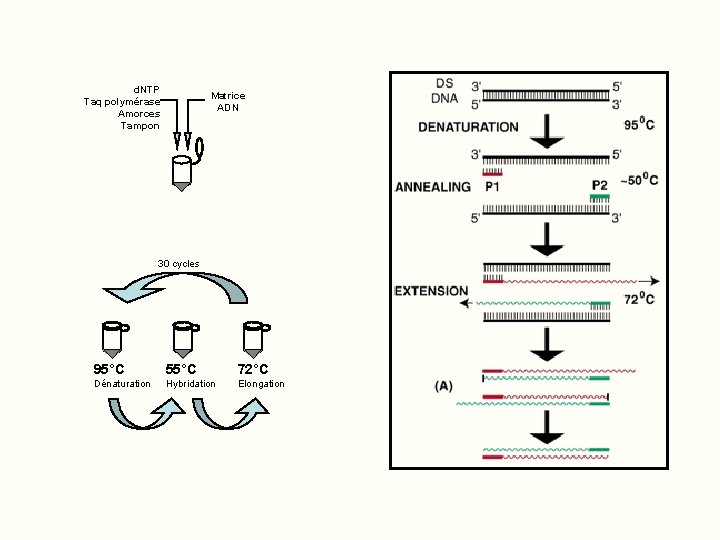
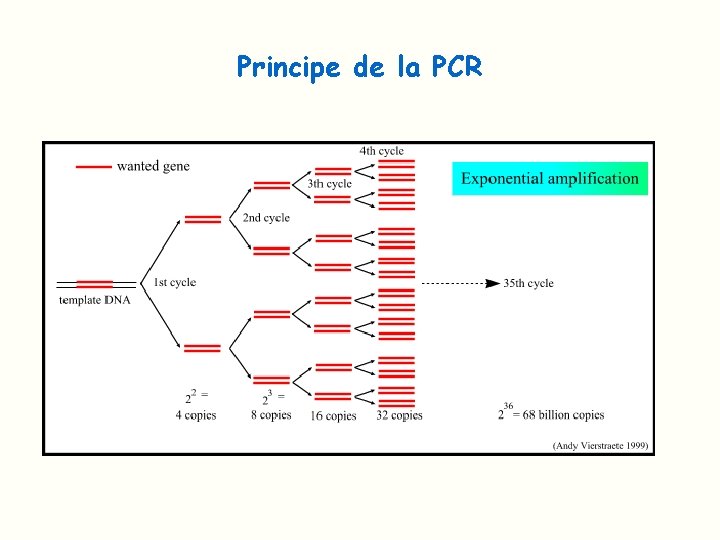
Principe de la PCR Ø Amplification exponentielle d’un ADN cible Ø 20 à 40 cycles d’amplification Ø Chaque cycle comprend 3 étapes: Ø Dénaturation de l’ADN par la chaleur à 95° : séparation des 2 brins Ø Hybridation avec 2 amorces de 10 à 20 nucléotides encadrant la région à amplifier Ø Élongation à partir des amorces grâce à une enzyme thermostable agissant à 72°

d. NTP Taq polymérase Amorces Tampon Matrice ADN 30 cycles 95°C 55°C 72°C Dénaturation Hybridation Elongation

Principe de la PCR

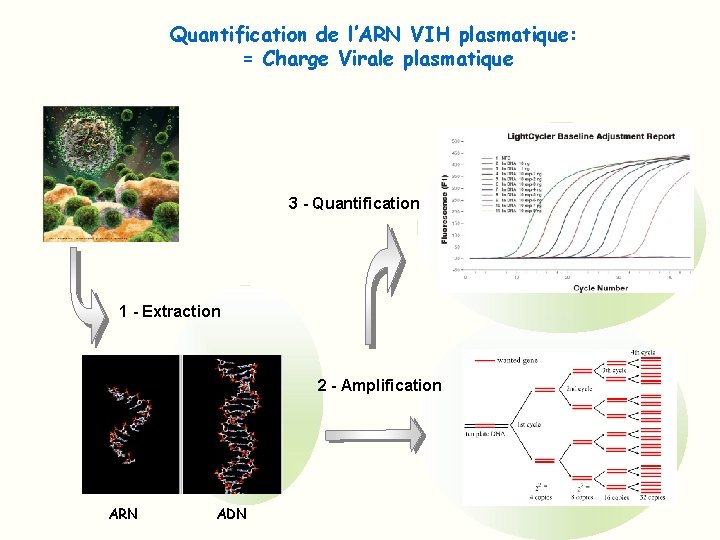
Quantification de l’ARN VIH plasmatique: = Charge Virale plasmatique 3 - Quantification 1 - Extraction 2 - Amplification ARN ADN

Quantification de l’ARN VIH plasmatique: = Charge Virale plasmatique Ø Prélèvement de sang sur anticoagulant (EDTA) Ø Centrifugation pour obtenir le plasma Ø Extraction de l’ARN des virus présents dans le plasma Ø RT PCR quantitative: Technique de PCR en temps réel Utilisation d’un standard interne

Charge virale: plateformes automatisées Extraction ARN plasmatique Quantification par PCR temps réel Roche Abbott Quantifie: HIV 1 groupe M, O, N Ne quantifie pas HIV 2

Charge virale VIH Ø Résultats exprimés en nombre de copies / ml ou en log de ce nombre de copies / ml Ø Seule une différence de 0. 5 log entre 2 résultats peut être considérée comme significative Ø Seuil de détection : 40 copies / ml Ø Pour un meilleur suivi, il est recommandé d’utiliser des résultats de tests obtenus par la même technique et si possible par le même labo Ø Les VIH 2 ne sont pas quantifiés par les techniques commercialisées

PCR - précautions q Risques de contaminations Problème majeur de ces techniques: contamination par les produits amplifiés d’une manip précédante Ø Bonnes pratiques +++ : précautions dans les manipulations, pièces dédiées, système Ampérase. q Résultats faussement négatifs: Peuvent être liés à la présence de substances inhibitrices dans les prélèvements Ø Techniques d’extraction du matériel génétique avant amplification sont capitales

Diagnostic virologique d’une infection HIV chez l’adulte

Diagnostic d’infection VIH chez l’adulte q Première étape : dépistage Permet la mise en évidence dans le sang périphérique: Ø des AC spécifiques dirigés contre les protéines de structure du virus Ø de l’antigène p 24 q Deuxième étape : confirmation

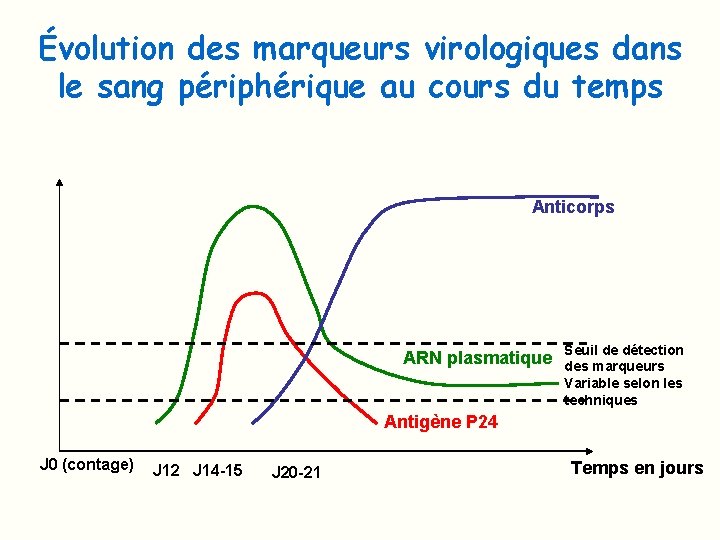
Évolution des marqueurs virologiques dans le sang périphérique au cours du temps Anticorps ARN plasmatique Seuil de détection des marqueurs Variable selon les techniques Antigène P 24 J 0 (contage) J 12 J 14 -15 J 20 -21 Temps en jours

Détection des différents marqueurs virologiques au cours de la primo-infection Tests rapides J 25 -26: AC anti VIH par WB J 20 -21: AC anti. VIH par ELISA 3° génération J 15 -16: pic d’Ag P 24 Tests ELISA 4° génération Dure environ 10 jours J 12 -14: ARN plasmatique Charge virale Fenêtre silencieuse J 0 : contage temps

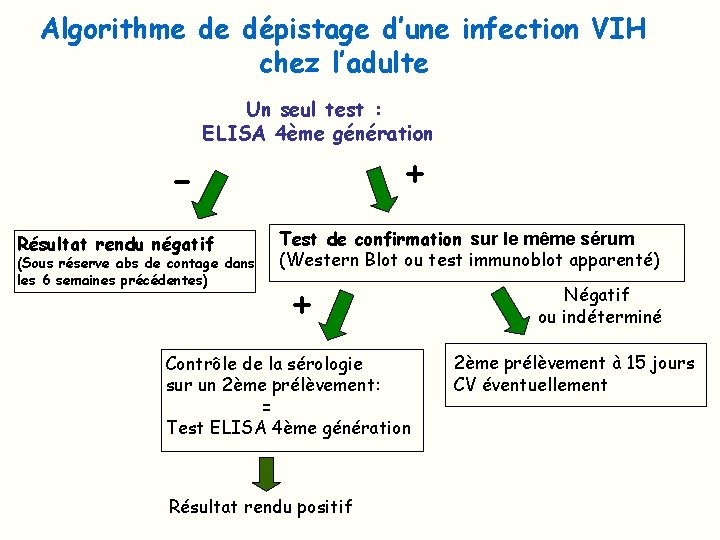
Algorithme de dépistage d’une infection VIH chez l’adulte Un seul test : ELISA 4ème génération + Résultat rendu négatif (Sous réserve abs de contage dans les 6 semaines précédentes) Test de confirmation sur le même sérum (Western Blot ou test immunoblot apparenté) + Contrôle de la sérologie sur un 2ème prélèvement: = Test ELISA 4ème génération Résultat rendu positif Négatif ou indéterminé 2ème prélèvement à 15 jours CV éventuellement

Interprétation du test de confirmation Ø moins sensible que l’ELISA Ø reste cependant obligatoire pour le diagnostic Ø test de confirmation positif: nouveau dépistage sur un 2° prélèvement obligatoire pour affirmer le diagnostic de séropositivité VIH Ø Test de confirmation indéterminé: plusieurs hypothèses

Test de confirmation indéterminé q Infection par VIH 2 Ø Western blot spécifique VIH 2 q Séroconversion en cours Ø Ag P 24, et surtout actuellement CV Ø Évolutivité des tests AC sur un 2° prélèvement 15 jours plus tard q Réactivité non spécifique Ø Seulement après avoir éliminé les autres hypothèses

Utilisation de la Charge virale dans le dépistage Ø La CV n’est pas utilisée pour faire un dépistage HIV sauf Ø Exceptionnellement en cas de suspicion de primo-infection Après discussion avec le clinicien

Règles à respecter pour le dépistage q Consentement obligatoire q Confidentialité absolue q Dépistage obligatoire pour : don de sang, de sperme, de tissu ou d’organe q Déclaration anonymisée des positifs

Suivi virologique d’un patient infecté par le VIH 2 techniques virologiques sont utilisées en routine pour le suivi des sujets infectés: Ø Charge virale Ø Test de résistance génotypique

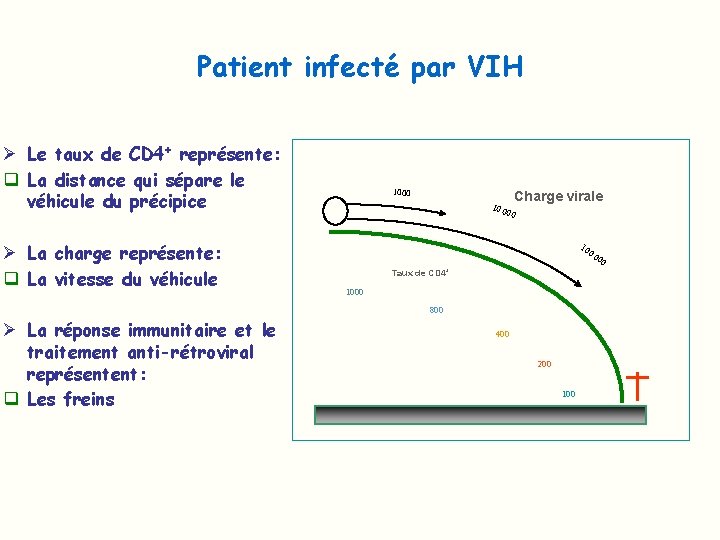
Patient infecté par VIH Ø Le taux de CD 4+ représente: q La distance qui sépare le véhicule du précipice Ø La charge représente: q La vitesse du véhicule 1000 Charge virale 10 0 00 10 00 Taux de CD 4+ 1000 800 Ø La réponse immunitaire et le traitement anti-rétroviral représentent: q Les freins 400 200 100 00

Charge virale plasmatique La charge virale représente: Ø Un marqueur pronostic Ø Un marqueur permettant de suivre l’évolution de la maladie Ø Un marqueur permettant de suivre l’efficacité d’un traitement antirétroviral

Suivi virologique d’un patient infecté par VIH Ø patient non traité ==> Charge virale tous les 4 à 6 mois si CD 4 > 500/mm 3 ==> Charge virale tous les 3 mois si CD 4 < 550/mm 3 Ø Mise sous traitement -Test génotypique de résistance - CV initiale Suivi de l’efficacité du traitement CV 1 mois après le début du traitement puis tous les 3 mois la 1° année Le but est d’obtenir une CV indétectable (<50 copies/ml) Ø au-delà d’un an de TRT: CV tous les 3 à 6 mois selon la clinique et les CD 4 Echappement virologique = CV redevient détectable tests de résistance aux ARV (et dosages pharmaco)

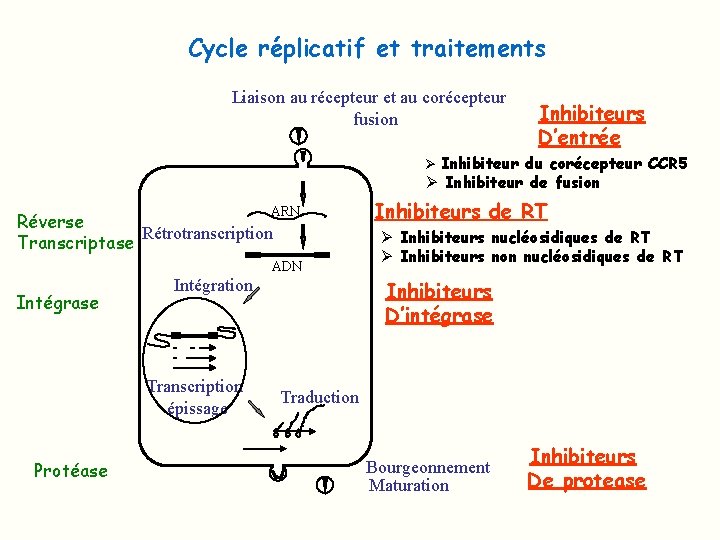
Cycle réplicatif et traitements Liaison au récepteur et au corécepteur fusion Inhibiteurs D’entrée Ø Inhibiteur du corécepteur CCR 5 Ø Inhibiteur de fusion ARN Réverse Rétrotranscription Transcriptase ADN Intégrase Intégration Transcription épissage Protéase Inhibiteurs de RT Ø Inhibiteurs nucléosidiques de RT Ø Inhibiteurs non nucléosidiques de RT Inhibiteurs D’intégrase Traduction Bourgeonnement Maturation Inhibiteurs De protease

Le VIH a une tendance naturelle à la mutation Multiplicité des cycles de réplication (1 à 10 milliards de particules /jour) + Grande variabilité au cours de la réplication = Variants génétiquement distincts provenant du virus initial contaminant (quasi-espèces)

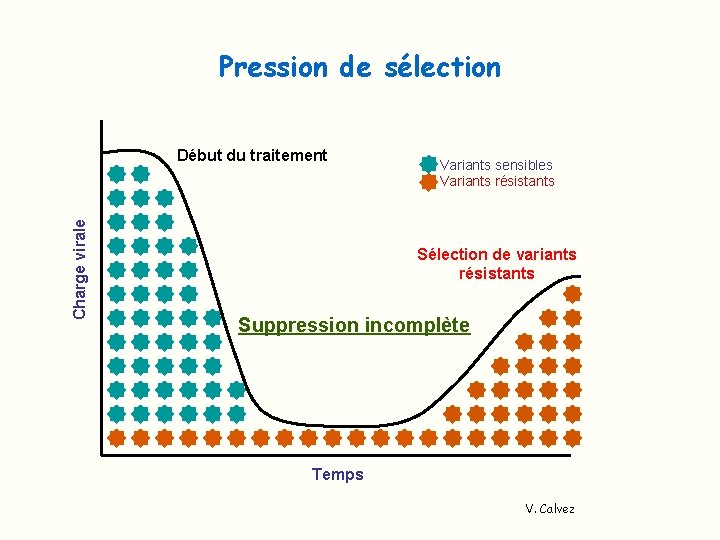
Phénomène de résistance Lié à des mutations entraînant une diminution de l’affinité de l’enzyme pour son inhibiteur Ø Préexistence des virus mutés chez les patients non traités Variabilité génétique importante des VIH q taux d’erreur important de la RT lors de la réplication q dynamique élevée de la réplication virale (109 particules/jour) --> population existe sous forme de quasi-espèces Ø Emergence des virus mutés résistants sous la pression de sélection thérapeutique

Pression de sélection Charge virale Début du traitement Variants sensibles Variants résistants Sélection de variants résistants Suppression incomplète Temps V. Calvez

Mesure de la résistance En routine, la mesure de la résistance est effectuée par la mise en évidence des mutations génétiques au niveau des sites d’action des médicaments = Résistance Génotypique Ce test de résistance est pratiqué chez les patients VIH traités et qui ont un échappement au traitement

Tests génotypiques Séquençage des gènes codant pour la RT, la protéase et l’intégrase : Pour les inhibiteurs de RT, Inhibiteurs de protéase, Inhibiteurs d’intégrase Séquençage du gène codant pour la gp 41 Pour les inhibiteurs de fusion Rétrotranscription de l'ARN viral PCR grâce à une enzyme thermostable 2ème PCR Séquençage du fragment PCR avec différent oligonucléotides Séparation des brins synthétisés par chromatographie Lecture de la séquence sur un séquenceur automatique

Séquenceur automatique

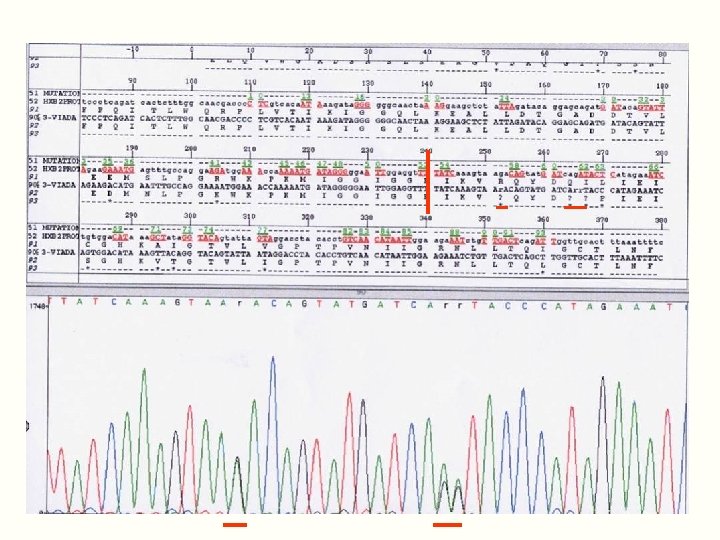
Lecture et interprétation des séquences

Tests génotypiques Ø Comparaison avec la séquence d’une souche de référence non mutée Ø Mise en évidence des mutations connues pour être associées à la résistance à un médicament Ø Rendu des résultats pour chaque médicament grâce à des algorithmes d’interprétation des mutations Ces algorithmes sont élaborés d’après les résultats des études cliniques (corrélations mutations/échec au médicament) Ø Adaptation du traitement anti-rétroviral en fonction des résistances
