Histosminaire 27 janvier 2010 Benjamin Ellezam Rsident V

Histoséminaire 27 janvier 2010 Benjamin Ellezam Résident V Anatomo-pathologie Université de Montréal Dr Luc Oligny CHU Ste-Justine

Femme de 37 ans, fumeuse et nullipare, consulte pour saignement vaginal après un test de grossesse positif. Dernières menstruations il y a 12 sem. Échographie pelvienne: fétus non-identifié Dilatation et curetage
P 57 kip 2

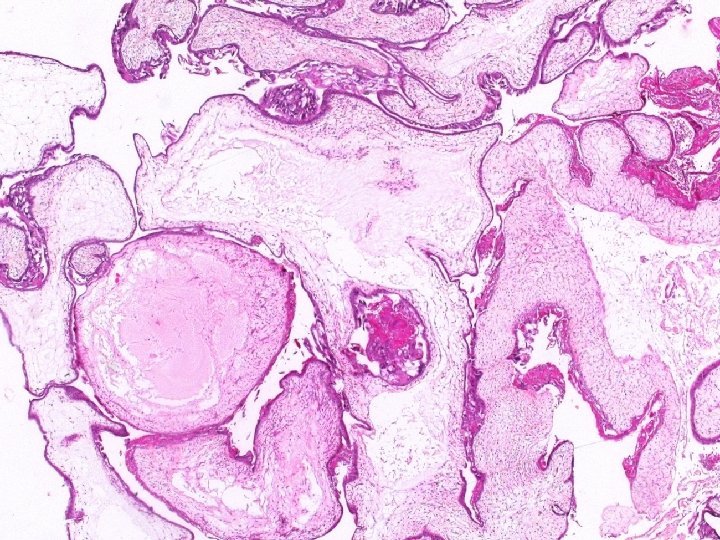
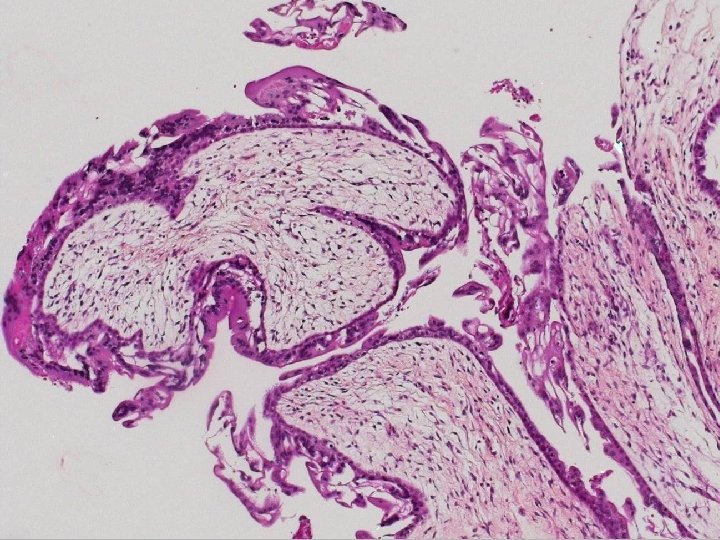
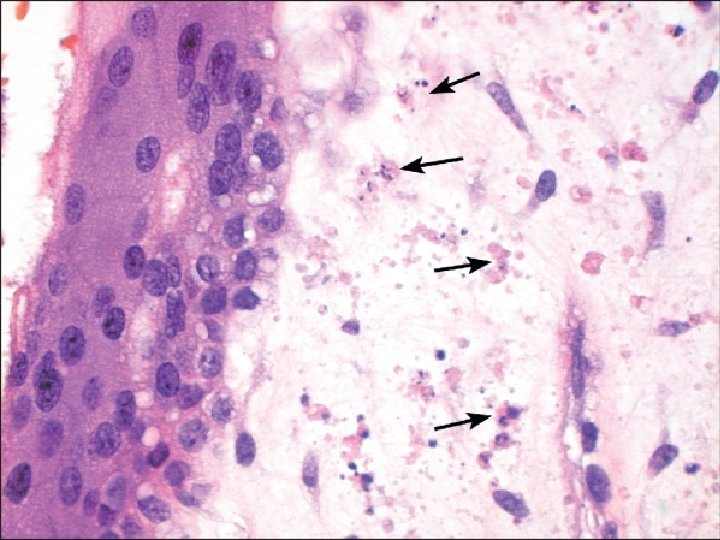
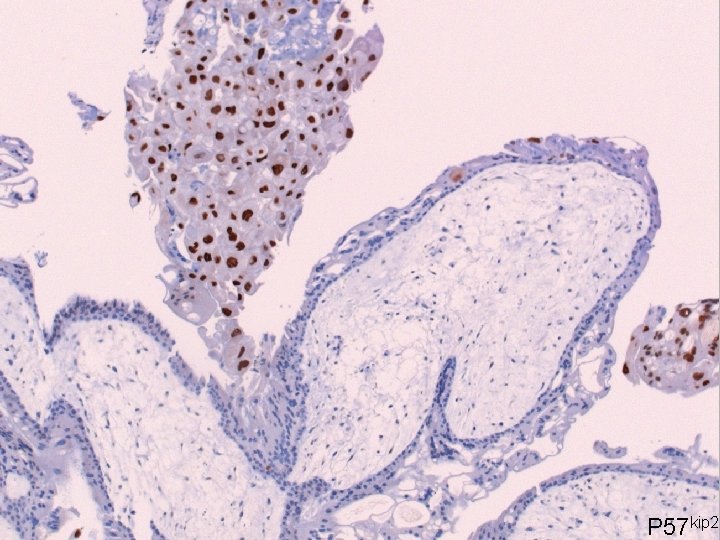
Morphologie: suggestif de môle P 57 kip 2: négatif Cytométrie de flux: diploïdie DX: Môle complète

Môles hydatiformes • Anomalie de conception avec: – sur-développement du placenta – sous-développement du fétus • Déséquilibre entre le matériel génétique provenant du père et celui provenant de la mère
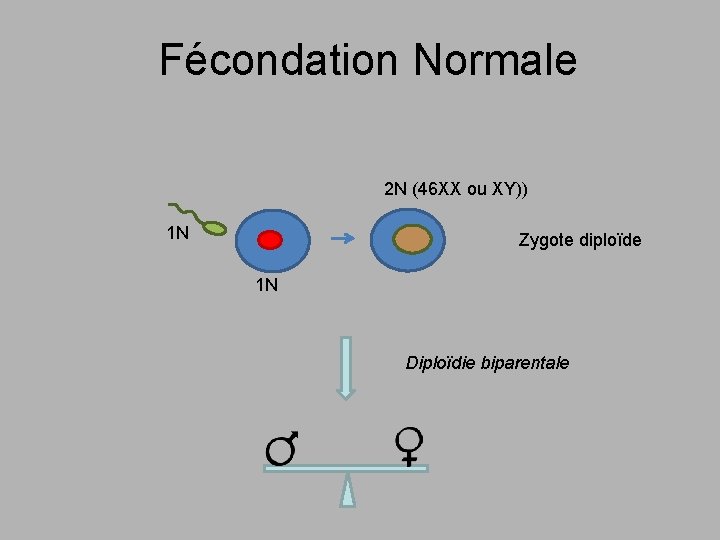
Fécondation Normale 2 N (46 XX ou XY)) 1 N Zygote diploïde 1 N Diploïdie biparentale
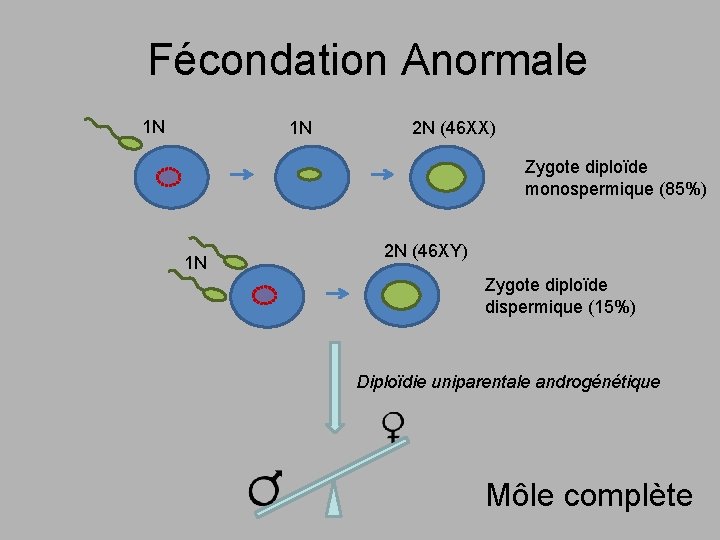
Fécondation Anormale 1 N 1 N 2 N (46 XX) Zygote diploïde monospermique (85%) 1 N 2 N (46 XY) Zygote diploïde dispermique (15%) Diploïdie uniparentale androgénétique Môle complète
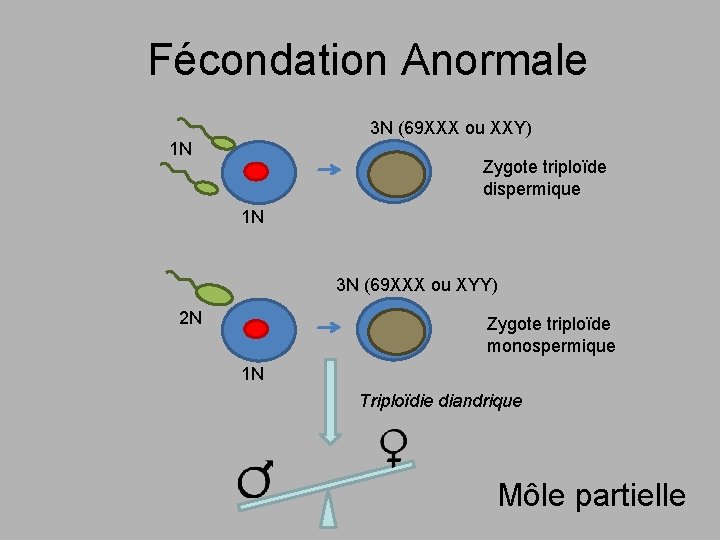
Fécondation Anormale 3 N (69 XXX ou XXY) 1 N Zygote triploïde dispermique 1 N 3 N (69 XXX ou XYY) 2 N Zygote triploïde monospermique 1 N Triploïdie diandrique Môle partielle
Excès de matériel génétique paternel Mécanisme? Croissance excessive du placenta
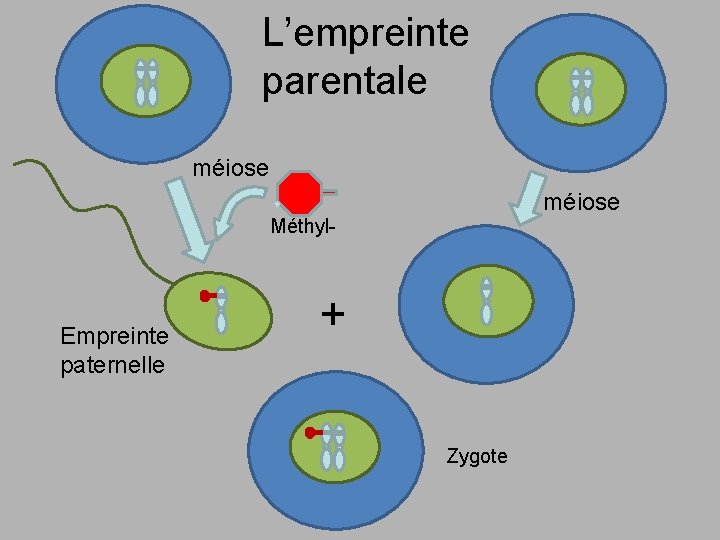
L’empreinte parentale méiose Méthyl- Empreinte paternelle + Zygote
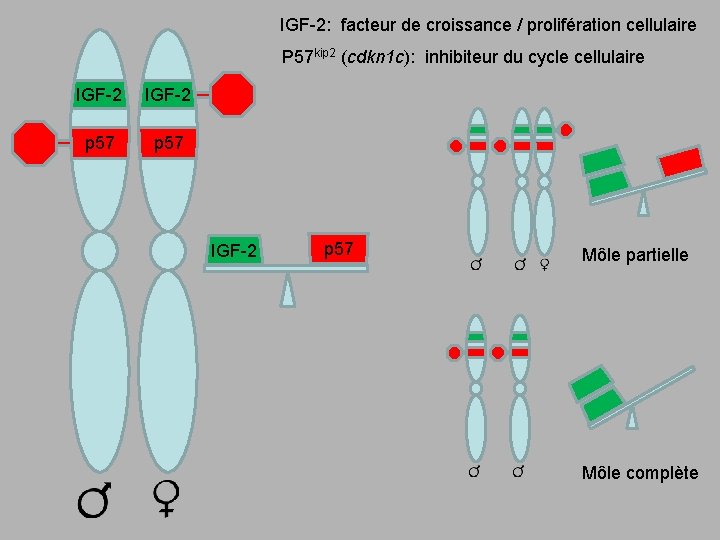
IGF-2: facteur de croissance / prolifération cellulaire P 57 kip 2 (cdkn 1 c): inhibiteur du cycle cellulaire IGF-2 p 57 Môle partielle Môle complète

Môles hydatiformes – facteurs de risque « Extrêmes » de l’âge reproducteur: <16 ans (RR=6) >40 ans (RR =5) Asiatiques (Indonésie 1: 100) (USA 1: 1000) Milieux défavorisés Tabagisme / nulliparité / multiparité ≠ RR ↑

Môles hydatiformes – présentation clinique Môle complète Môle partielle 1. « Classiquement » : • nausées et vomissements ++ • saignements @ 11 -25 semaines • hauteur utérine excessive • « tempête de neige » à l’échographie • βh. CG très élevés • Avortement spontané / manqué / incomplet 2. Aujourd’hui: • diagnostic souvent plus précoce (<14 sem) 1. « Classiquement » : • peu de signes et symptômes francs • avortement manqué • βh. CG légèrement élevés

Môles hydatiformes – traitement et évolution Môle complète Môle partielle 1. Curetage utérin 2. βh. CG sériés q sem • ad βh. CG = 0 m. UI/ml • N: ~8 -12 sem 1. Curetage utérin 2. βh. CG sériés (ad = 0) 3. 15 -20% de risque de maladie trophoblastique gestationnelle persistante 3. 0, 2 -4% de risque de maladie trophoblastique gestationnelle persistante

Maladie trophoblastique gestationnelle persistante >95% = môle persistante/invasive/métastatique 3 -5% = néoplasie trophoblastique gestationnelle maligne (3 cas décrits seulement suite à une môle partielle)

Môle persistante/invasive/métastatique βh. CG : plateau ou ↑ x 2 -3 sem (64% de risque MTGp si >2000 m. UI/ml @ 4 sem) Imagerie: écho pelvienne + RXP Persistante = villosités résiduelles s/p D&C Invasive = villosités a/n myomètre Métastatique = poumons/vagin/bassin/cerveau/foie Tx empirique: methotrexate ou actinomycine. D Px: excellent (<5% de récidive @ 12 mo)

Néoplasies trophoblastiques gestationnelles malignes • 1. Choriocarcinome gestationnel • Durant la surveillance post-môle (ou après môle manquée ou grossesse non-môlaire): • Saignement vaginal • Masse utérine • Métastases symptom. (poumons/cerveau) • Histo (rare): tumeur biphasique hémorragique maligne • Stratification du risque selon critères cliniques de l’OMS/FIGO • Px: bas risque ~100% survie // haut risque ~75%

Néoplasies trophoblastiques gestationnelles malignes • 2. Tumeur trophoblastique du site placentaire • Beaucoup plus rare (<2% des cas de NTG) • Présentation tardive (3 ans post-grossesse N ou môle) • Saignements ou métastases symptomatiques • Pas d’augmentation du βh. CG sérique • Histo: tumeur monophasique du trophoblaste intermédiaire (PLAP+ βh. CG-) • Px: excellent avec hystérectomie + chimio
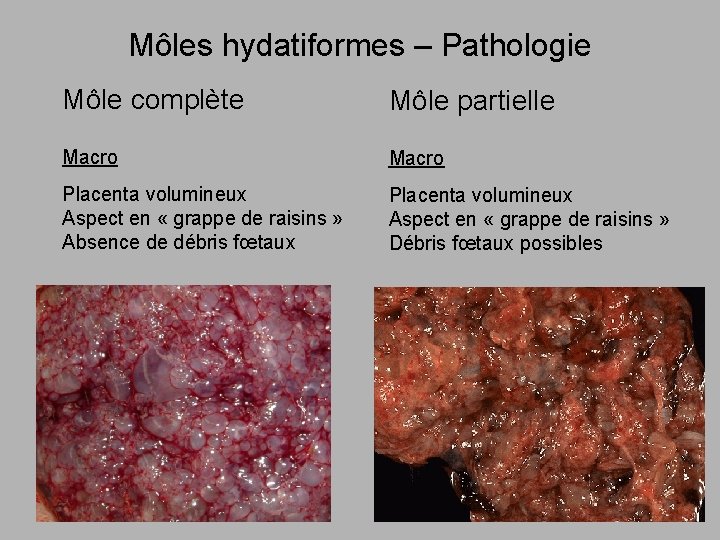
Môles hydatiformes – Pathologie Môle complète Môle partielle Macro Placenta volumineux Aspect en « grappe de raisins » Absence de débris fœtaux Placenta volumineux Aspect en « grappe de raisins » Débris fœtaux possibles
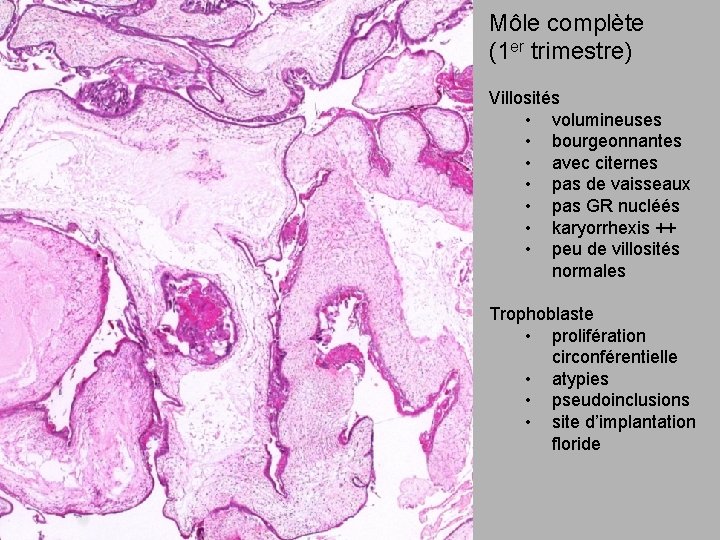
Môle complète (1 er trimestre) Villosités • volumineuses • bourgeonnantes • avec citernes • pas de vaisseaux • pas GR nucléés • karyorrhexis ++ • peu de villosités normales Trophoblaste • prolifération circonférentielle • atypies • pseudoinclusions • site d’implantation floride
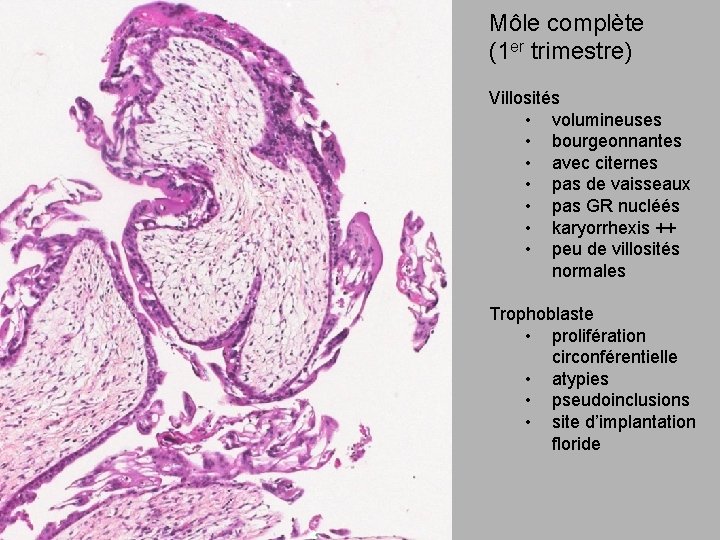
Môle complète (1 er trimestre) Villosités • volumineuses • bourgeonnantes • avec citernes • pas de vaisseaux • pas GR nucléés • karyorrhexis ++ • peu de villosités normales Trophoblaste • prolifération circonférentielle • atypies • pseudoinclusions • site d’implantation floride
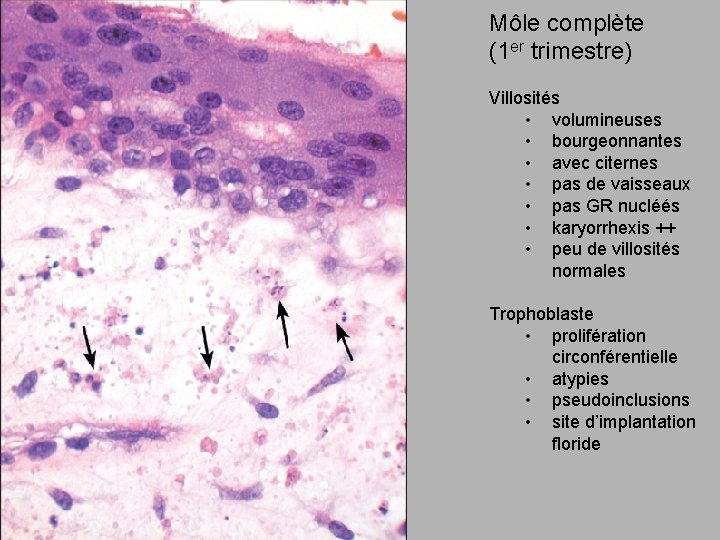
Môle complète (1 er trimestre) Villosités • volumineuses • bourgeonnantes • avec citernes • pas de vaisseaux • pas GR nucléés • karyorrhexis ++ • peu de villosités normales Trophoblaste • prolifération circonférentielle • atypies • pseudoinclusions • site d’implantation floride
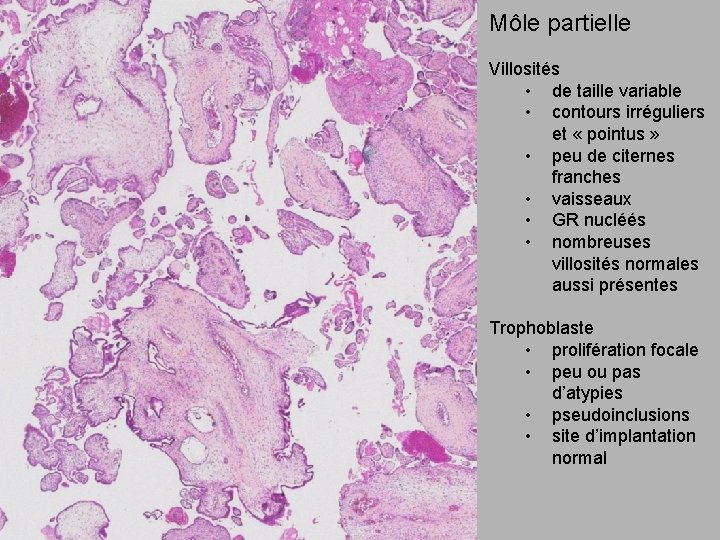
Môle partielle Villosités • de taille variable • contours irréguliers et « pointus » • peu de citernes franches • vaisseaux • GR nucléés • nombreuses villosités normales aussi présentes Trophoblaste • prolifération focale • peu ou pas d’atypies • pseudoinclusions • site d’implantation normal
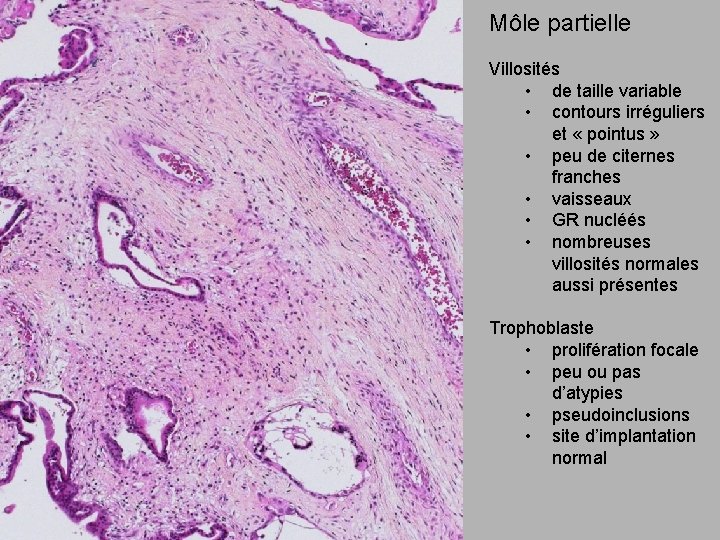
Môle partielle Villosités • de taille variable • contours irréguliers et « pointus » • peu de citernes franches • vaisseaux • GR nucléés • nombreuses villosités normales aussi présentes Trophoblaste • prolifération focale • peu ou pas d’atypies • pseudoinclusions • site d’implantation normal
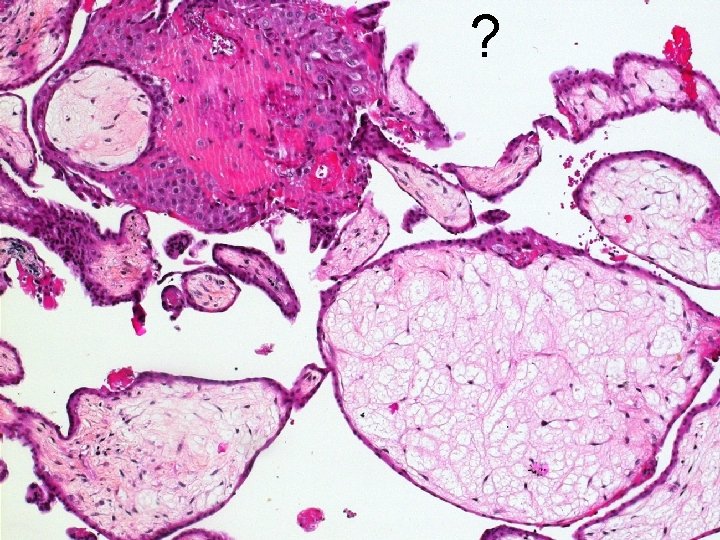
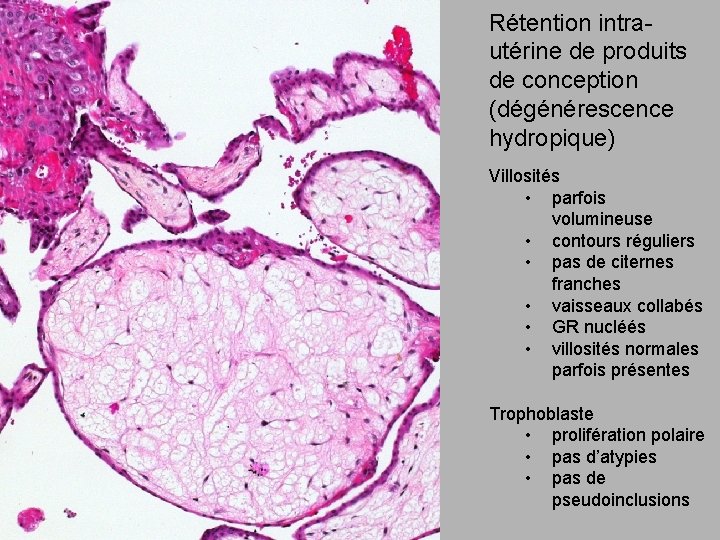
Rétention intrautérine de produits de conception (dégénérescence hydropique) Villosités • parfois volumineuse • contours réguliers • pas de citernes franches • vaisseaux collabés • GR nucléés • villosités normales parfois présentes Trophoblaste • prolifération polaire • pas d’atypies • pas de pseudoinclusions

Mais, malgré critères publiés… Beaucoup de variation interobservateur! % de cas ne faisant pas consensus parmi un groupe de 4 -5 pathologistes placentaires: 36% (15/42) Am J Surg Pathol 2009; 33: 805– 817 40% (20/50) Am J Surg Pathol 2005; 29: 942– 947 30% (35/50) J Clin Pathol 1993; 46: 599 -602 Donc…

Autres outils? Môle complète Môle partielle Grossesse non-môlaire Matériel génétique Paternel Maternel et paternel Ploïdie Diploïde Triploïde Diploïde
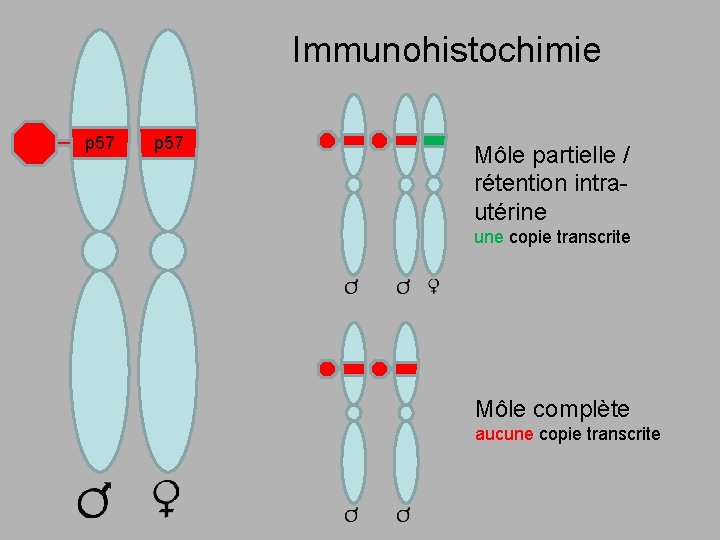
Immunohistochimie p 57 Môle partielle / rétention intrautérine une copie transcrite Môle complète aucune copie transcrite
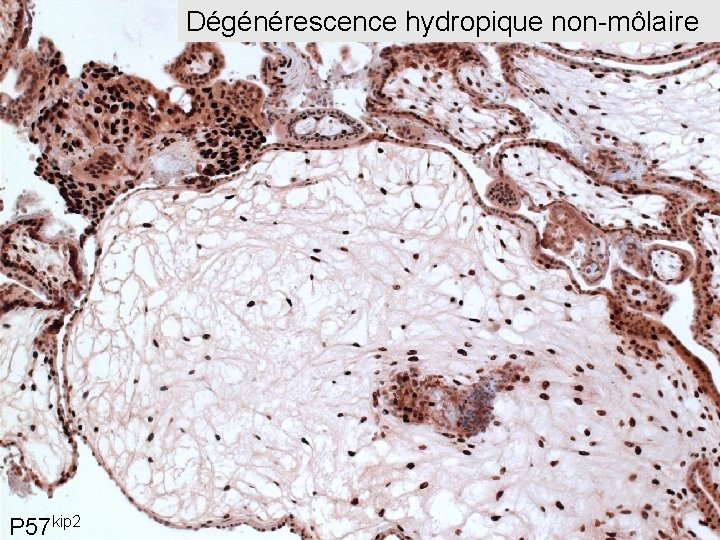
Dégénérescence hydropique non-môlaire P 57 kip 2
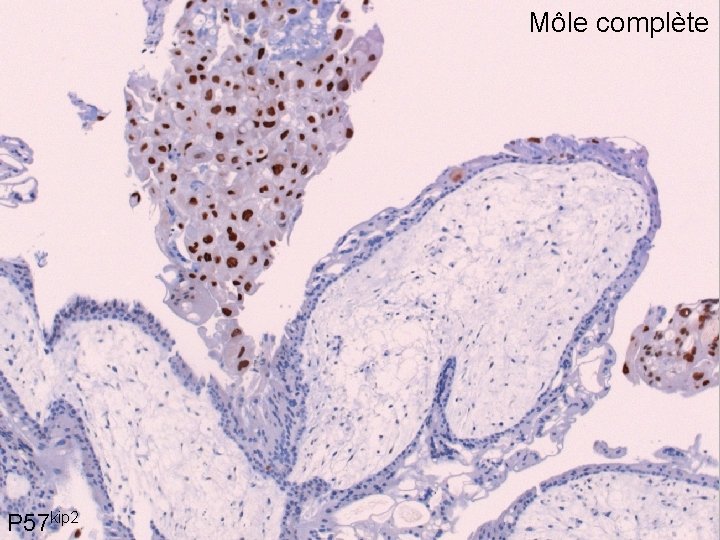
Môle complète P 57 kip 2

Immunohistochimie avec p 57 • Technique fiable • Mise au point facile • Validée dans de nombreuses études • ex. étude prospective sur 42 cas consécutifs (AJSP 2009; 33: 805) Taux de résultat équivoque: 3/42 = môle partielle avec marquage faible Taux de résultat aberrant: 1/42 = môle complète avec marquage positif (rétention d’un chromosome 11 maternel)

Ploïdie 2 techniques: 1) Cytométrie de flux 2) Génotypage moléculaire
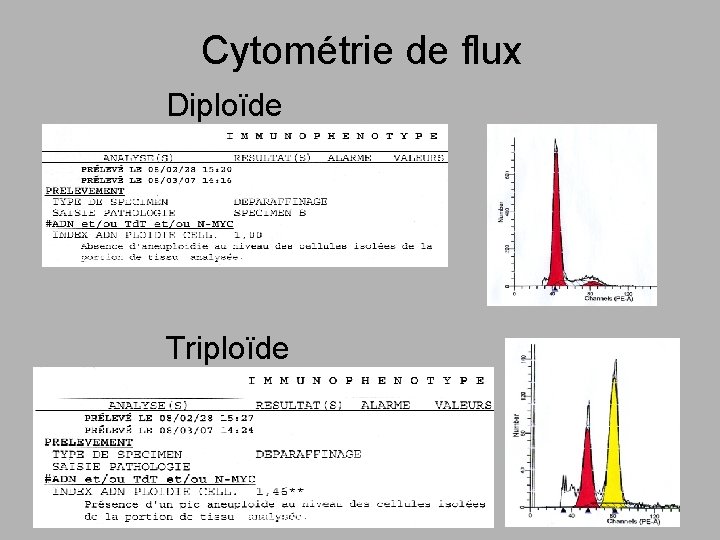
Cytométrie de flux Diploïde Triploïde

Cytométrie de flux Avantages: • faible coût • équipement déjà disponible dans plusieurs laboratoires de pathologie • pas de microdissection Inconvénient principal: • diploïdie biparentale et uniparentale ne peuvent être différenciés • (ex: distinction entre môle complète et dégénérescence hydropique lorsque le p 57 est équivoque)
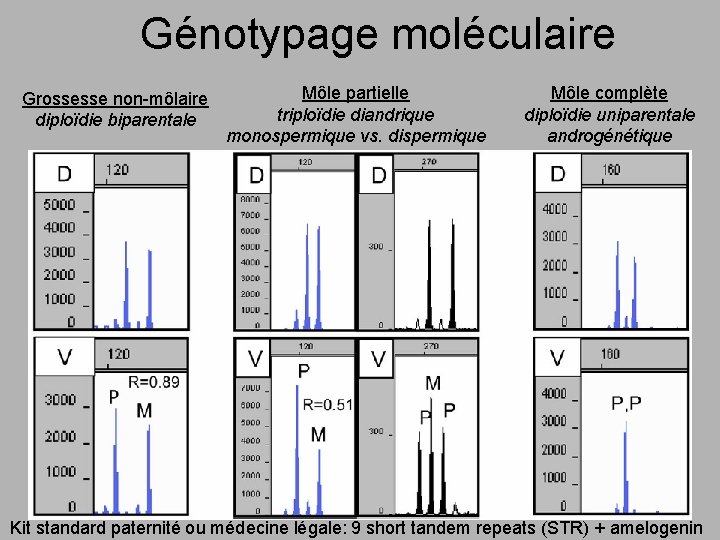
Génotypage moléculaire Grossesse non-môlaire diploïdie biparentale Môle partielle triploïdie diandrique monospermique vs. dispermique Môle complète diploïdie uniparentale androgénétique Kit standard paternité ou médecine légale: 9 short tandem repeats (STR) + amelogenin

Génotypage moléculaire Avantages: • diploïdie biparentale et uniparentale peuvent être différenciés (si échec du p 57) Inconvénients: • microdissection nécessaire • utilisation de kits commerciaux coûteux • équipement peu disponible actuellement • nécessite de l’ADN de bonne qualité
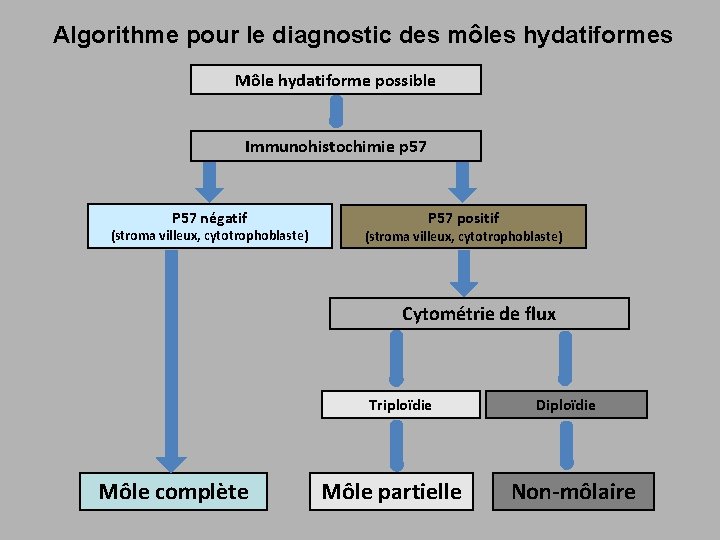
Algorithme pour le diagnostic des môles hydatiformes Môle hydatiforme possible Immunohistochimie p 57 P 57 négatif (stroma villeux, cytotrophoblaste) P 57 positif (stroma villeux, cytotrophoblaste) Cytométrie de flux Triploïdie Môle complète Môle partielle Diploïdie Non-môlaire
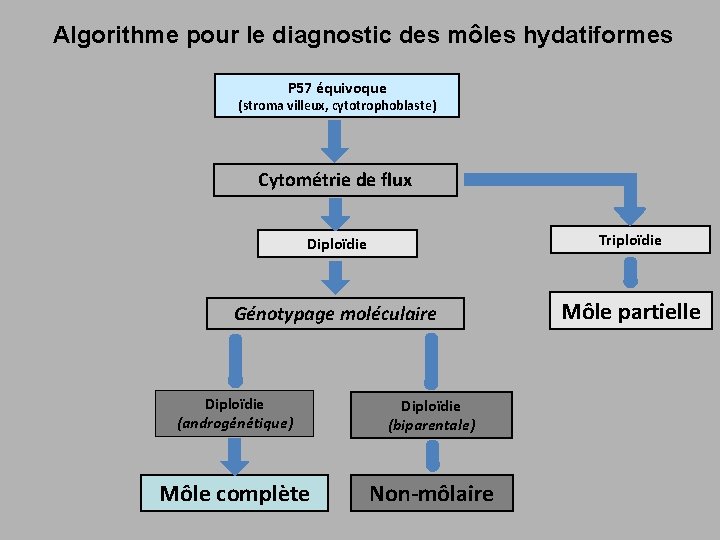
Algorithme pour le diagnostic des môles hydatiformes P 57 équivoque (stroma villeux, cytotrophoblaste) Cytométrie de flux Diploïdie Triploïdie Génotypage moléculaire Môle partielle Diploïdie (androgénétique) Diploïdie (biparentale) Môle complète Non-môlaire

Conclusion Importance du diagnostic précis pour le pronostic Môle complète: 15 -20% risque de chimio 3 -5% risque de choriocarcinome Môle partielle: 0. 5 -4% risque de chimio ~0% risque de choriocarcinome La morphologie seule n’est pas fiable (attention au 1 er trimestre!) L’immunohistochimie avec p 57 a été validée de façon prospective et permet de prouver une môle complète La ploïdie par cytométrie de flux ou par génotypage permettent de prouver une môle partielle

Merci au Dr Oligny et aux techniciens du CHU Ste-Justine qui m’ont aidé à mettre au point l’anticorps p 57 avec le système Ventana!
- Slides: 44