Histoplasmoses Patrick BOIRON Laboratoire de Mycologie Facult de

Histoplasmoses Patrick BOIRON Laboratoire de Mycologie Faculté de Pharmacie, Lyon, France

Introduction • Les histoplasmoses sont des mycoses profondes dues à des champignons dimorphiques • Il en existe 2 formes : • • L'histoplasmose américaine due à Histoplasma capsulatum, dite « à petites formes » • Et l'histoplasmose africaine due à Histoplasma duboisii, dite « à grandes formes » Depuis une quinzaine d'années, il y a une augmentation importante des cas d'histoplasmose, en raison de l'immunodépression due au SIDA

Histoplasmose à Histoplasma capsulatum

Histoplasmose à Histoplasma capsulatum • 1904 (JAMA) : Darling (Panama) découverte de corps principalement intracellulaires (protozoaire ? ) à l’autopsie d’un cas fatal d’infection fulminante • • • Différent de Leishmania car pas de kinétoplaste : Histoplasma capsulatum • 1940 -1960 : 1912 : da Rocha-Lima : levure et non protozoaire 1934 : croissance sous forme filamenteuse à température ambiante et sous forme levure à 37 °C (dimorphisme) • • Test cutané à partir de filtrat de culture de la phase filamenteuse (histoplasmine) • Diagnostic différentiel de la tuberculose Découverte d’une forte prévalence dans certaines régions des USA (infection asymptomatique)

Histoplasmose à Histoplasma capsulatum • • Rapportée dans de nombreuses régions du monde sauf Antarctique Endémique • Continent américain (vallées de l’Ohio, du Mississipi, du Saint-Laurent et du Rio Grande aux USA) : 80 % des sujets ont été en contact avec Histoplasma capsulatum • • • Amérique Centrale (Honduras, Panama, Mexique, Costa Rica, Guatemala) Amérique Latine (Guyane Française, Venezuela, Argentine, Brésil, Uruguay, Colombie, Equateur, Paraguay, Chili, Pérou) Caraïbes (Antilles Françaises, Haïti, Porto Rico, Trinidad, Cuba)
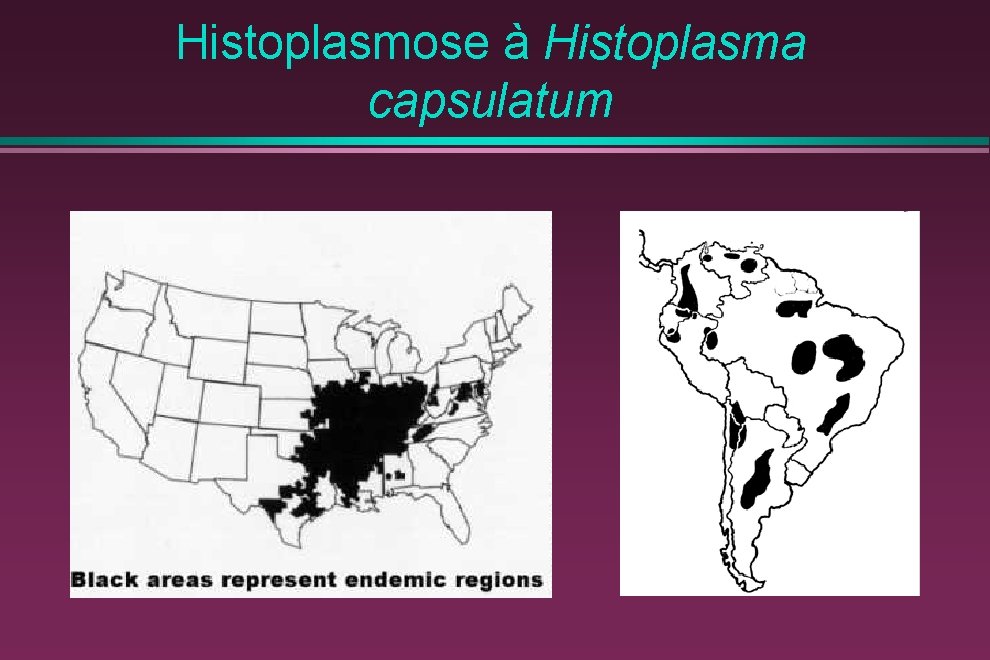
Histoplasmose à Histoplasma capsulatum

Histoplasmose à Histoplasma capsulatum • Également • Afrique du Sud • Afrique équatoriale (Zaïre, Tanzanie, Djibouti, Cameroun, Kenya) • Asie du Sud-Est (Malaisie, Indonésie, Thaïlande, Inde, Singapour, Vietnam) • Europe : cas d’importation (50 cas en 25 ans rapportés en France) • Proche-Orient (Turquie) • Océanie (Australie, Nouvelle-Zélande, Nouvelle-Calédonie)

Réservoirs de Histoplasma capsulatum Sol • Isolé à partir de sols acides, riches en azote, enrichis en déjections d’oiseaux ou de chauvesouris

Réservoirs de Histoplasma capsulatum Sol • Près des vieux poulaillers, dans des grottes et des caves, aux alentours de maisons ou d’immeubles abritant des chauves souris

Réservoirs de Histoplasma capsulatum Sol • Aux environs des perchoirs (arbres) d’étourneaux et de pigeons

Réservoirs de Histoplasma capsulatum Sol • Dans une couche de 15 cm de profondeur • Histoplasma capsulatum peut être transporté par les ailes, les pattes et les becs d’oiseaux (étourneaux, merles, pigeons, …)

Réservoirs de Histoplasma capsulatum Animaux • Oiseaux : déjections = substrat nutritif favorable à la croissance de Histoplasma capsulatum lorsqu’il est présent dans la terre • Les oiseaux eux-mêmes ne sont pas colonisés ou infectés en raison de leur température corporelle (42 °C) trop élevée • Les déjections fraîches d’oiseaux ne présenteraient pas de risque infectieux sur des surfaces telles que le trottoir ou les rebords de fenêtre

Réservoirs de Histoplasma capsulatum Animaux • Chauves-souris : contrairement aux oiseaux, les chauves-souris peuvent être infectées (lésions intestinales) par Histoplasma capsulatum (ce qui est paradoxal, car leur température corporelle est aussi élevée que celle des oiseaux) • Les chauves-souris excrètent le champignon par leurs déjections • Leur guano est reconnu comme facteur de croissance pour le champignon

Réservoirs de Histoplasma capsulatum Animaux • Poulets : ils ne sont pas touchés par l’histoplasmose dans les conditions naturelles, même si Histoplasma capsulatum a été retrouvé dans des déjections fraîches de poulet • Après injection par voie intraveineuse de fortes doses de spores de Histoplasma capsulatum, le champignon peut être isolé des tissus ou des plumes • Dans des conditions non expérimentales, le champignon n’a pas été retrouvé au niveau des plumes de poulet vivants, mais il a été isolé de plumes utilisées pour rembourrer un oreiller

Transmission de Histoplasma capsulatum • Histoplasma capsulatum peut être transporté par le vent à des kilomètres du site contaminé, et les patients peuvent ne pas être conscients de leur exposition • La transmission de personne à personne semble peut probable, même si un cas possible de contamination interhumaine a été évoquée • Il est actuellement admis que les patients hospitalisés n’ont pas besoin d’être mis en isolement • Quelques cas de transmission par transplantation rénale ont été rapportés

Circonstances de contamination humaine • Porte d’entrée respiratoire • Inhalation de spores jusqu’aux alvéoles pulmonaires

Circonstances de contamination humaine • Microfoyers de Histoplasma capsulatum dans le sol de parcs en ville et près de vieux immeubles, de zones commerciales bordées d’arbres abritant des oiseaux • • Personnel et clients exposés aux poussières atmosphérique de ces zones Ouvriers de construction ou démolition d’immeubles Petites épidémies lors du creusement d’un puits ou du percement d’un tunnel Activités rurales : nettoyage de poulaillers, de pigeonniers, exploration de grottes infectées par des chauves souris

Marqueur épidémiologique Test cutané à l’histoplasmine • Histoplasmine = filtrat de culture stérile d’un bouillon d’asparagine – glucose de la forme mycélienne de Histoplasma capsulatum cultivée pendant 2 à 3 mois • Sans intérêt diagnostique (anergie en cas d’immunodépression) • Intérêt épidémiologique : formes asymptomatiques ou anciennes d’histoplasmose ; délimitation des zones d’endémie • Sensibilité : 90 % chez le sujet sain (négativation possible en l’absence prolongée de stimulation antigénique et chez les personnes âgées) • Spécificité médiocre : réaction croisée avec les agents de la blastomycose et de la coccidioïdomycose

Fréquence USA • Population générale • 500. 000 nouveaux cas annuels (dont 200. 000 cas d’histoplasmose pulmonaire aiguë) • Taux d’histoplasmose pulmonaire chronique en zone de forte endémie : 1 / 100. 000 • Incidence annuelle à Kansas City (histoplasmose subclinique ou symptomatique) : 4, 7 % • Positivité des tests cutanés à l’histoplasmine : • • • Population générale : 20 % > 40 % dans certaines régions d’hyper-endémie 85 à 95 % chez les enfants de 10 à 15 ans

Fréquence USA • Patients sidéens • En zone d’endémie, l’histoplasmose survient chez 2 à 5 % atteints du SIDA, mais peut toucher jusqu’à 30 % dans certaines villes • Etat d’Indiana : 26, 7 % des patients d’Indianapolis et 2 % des patients sidéens des autres villes de l’Etat sont atteints d’histoplasmose disséminée • A Kansas City, 25 % des patients sidéen ont une histoplasmose disséminée

Fréquence Autres pays • En Amérique Latine, en Afrique de l’Ouest et en Asie du Sud-Est, presque 30 % de la population présente un test positif à l’histoplasmine • Au Brésil, les tests positifs à l’histoplasmine varient de 6, 3 % dans l’Etat de Santa Catarina, au sud du Brésil, à 27, 5 % dans l’Etat de Para (région amazonienne, au nord)

Fréquence Autres pays • Les Caraïbes présentent les conditions favorables au développement de Histoplasma capsulatum (climat tropical chaud et humide, nombreux Chiroptères, multiples grottes) et sont donc considérées comme une zone d’endémie • Aux Antilles Françaises, les tests cutanés à l’histoplasmine sont positifs chez 12 % de la population générale (valeur comparable à celle des zones d’endémie moyenne aux USA)

Personnes à risque • Prédominance des hommes (4 / 1) • Pas de prédominance ethnique • La situation est différente selon le statut immunitaire des patients

Personnes à risque Patients non immunodéprimés • Après une exposition au champignon, le degré de maladie dépendra : • De la quantité de spores inhalées • De l’âge de l’individu • De sa susceptibilité à la maladie • Mais l’inoculum minimum infectant est inconnu

Personnes à risque Activités à risque les plus fréquentes • Risques physiologiques : • • • Nouveaux-nés Jeunes enfants Personnes âgées, surtout si atteintes de pathologies pulmonaires chroniques • Risques professionnels : • • • Personnels travaillants sur les ponts Ramoneurs Ouvriers en construction et démolition Fermiers et jardiniers Installateurs de systèmes d’air conditionné et de chauffage Personnels de laboratoire Destructeurs d’animaux nuisibles Restaurateurs d’immeubles historiques ou abandonnés Couvreurs Spéléologues

Personnes à risque • Toute personne ayant exercé l’une de ces activités et qui développe des symptômes pseudo-grippaux des jours – ou des semaines – après avoir été en contact avec du matériel potentiellement contaminé par Histoplasma capsulatum, avec une aggravation après quelques semaines, devra aller consulter son médecin et l’avertir de l’exposition

Personnes à risque Patients immunodéprimés • Premières populations à risque : patients infectés par VIH et patients cancéreux (surtout leucémie) • Neutropénie prolongée suite à chimiothérapie, mais aussi corticothérapie par voie systémique • Transplantation d’organe (la thérapie anti-rejet : aziathioprine, prednisone, globulines antithymocytes, tacrolimus et ciclosporine lymphocytes T)

Recommandations • « … les personnes infectées par le VIH devraient éviter les activités connues comme étant associées à une augmentation des risques » (nettoyer les cages de poules, remuer la terre sous les endroits où les oiseaux se perchent et explorer les grottes) * * Prevention of Opportunistic Infections Working Group de l’US Public Health Service et de l’Infectious Diseases Society of America (USPHS / IDSA)

Physiopathologie de l’histoplasmose à Histoplasma capsulatum Macrophages • Principales cellules effectrices : résistance de l’hôte à la levure • Migration de la forme levure dans ganglions de drainage + foie + rate ; l’activation de l’immunité cellulaire nécessite 15 jours au stade de primo -infection • La plupart des levures sont localisées dans les phago-lysosomes des macrophages murins ; capacité de survie par alcalinisation du phagolysosome (> p. H 6) • • NO : produit par macrophages murins chélation du fer = fongicide Différences entre macrophages murins et humains (opsonisation vs pas d’opsonisation)

Physiopathologie de l’histoplasmose à Histoplasma capsulatum VIH • Patients VIH+ : déficit qualitatif des macrophages (fixation des levures) corrélé au déficit quantitatif lymphocytaire T CD 4+ • Croissance plus rapide des levures dans les macrophages de sujets infectés par le VIH ou in vitro • Patients atteints du SIDA sensibles à histoplasmose +++

Physiopathologie de l’histoplasmose à Histoplasma capsulatum Lymphocytes T • • Importance des lymphocytes CD 4 • Mort des souris inoculées par Histoplasma capsulatum si lymphocytes CD 4 déficients • Transfert de lymphocytes CD 4 de souris immunisées par levures : diminution de la charge fongique Libération de cytokines stimulant les macrophages murins (++ IFN-γ, IL-12, TNF -α) • Souris déficientes en IFN-γ ou blocage de l’une des 3 cytokines => plus grande sensibilité à l’infection • IL-12 importante pour primo-infection ; IFN- γ et TNF- α pour infections primaires et secondaires Stimulation des macrophages humains par M-CSF, GM-CSF et IL-3 Importance moindre des CD 8

Physiopathologie de l’histoplasmose à Histoplasma capsulatum Neutrophiles • • • Migration précoce dans poumons (infection expérimentale) Inhibition de la croissance des levures Pas de neutrophiles : moins bonne défense chez la souris Autres cellules • • • NK (souris Beige déficientes => plus grande susceptibilité) Cellules dendritiques Pas de stérilisation des tissus, possibilité de réactivation

Clinique de l’histoplasmose à Histoplasma capsulatum • • • Symptomatologie proche de la tuberculose Primo-infection pulmonaire : incubation = 7 à 21 jours (médiane 14 j) • Asymptomatique ≥ 90 % des cas, laissant comme séquelles des nodules ou des adénopathies calcifiés visibles à la radiographie du thorax • Pouvant se manifester par pneumopathie aiguë d’allure virale + douleurs thoraciques ; résolution < 10 jours • • • Parfois arthralgies ± érythème noueux ± érythème polymorphe ± péricardite Pauvreté de l’examen clinique + biologie de routine Radio : pneumopathie virale + ganglions ± péricardite Chez immunodéprimé, âges extrêmes ou inoculation massive • • Forme fulminante avec miliaire Insuffisance respiratoire aiguë
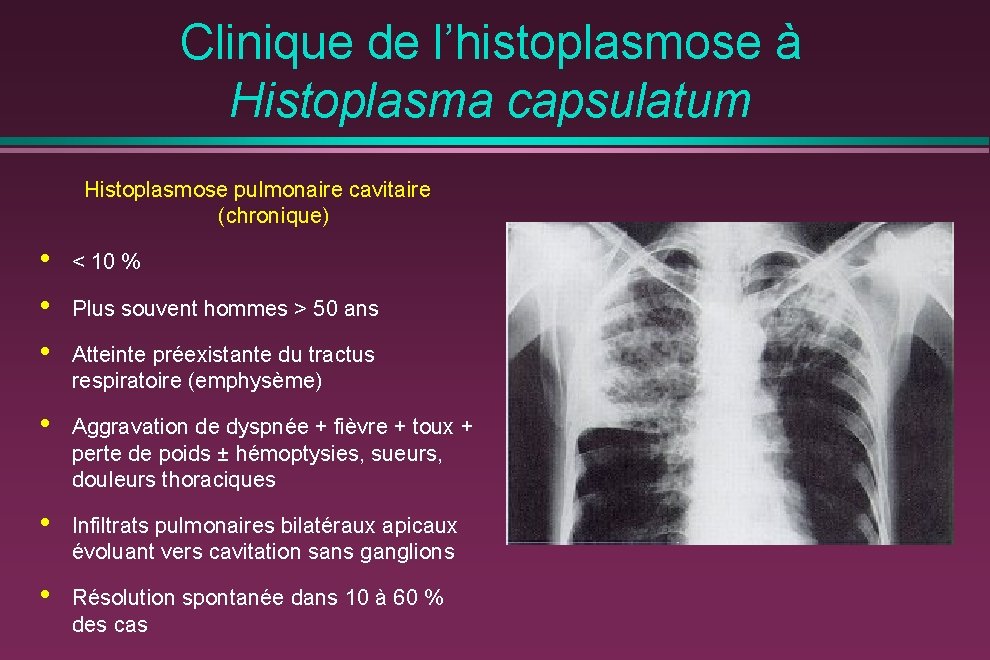
Clinique de l’histoplasmose à Histoplasma capsulatum Histoplasmose pulmonaire cavitaire (chronique) • • • < 10 % • Aggravation de dyspnée + fièvre + toux + perte de poids ± hémoptysies, sueurs, douleurs thoraciques • Infiltrats pulmonaires bilatéraux apicaux évoluant vers cavitation sans ganglions • Résolution spontanée dans 10 à 60 % des cas Plus souvent hommes > 50 ans Atteinte préexistante du tractus respiratoire (emphysème)

Clinique de l’histoplasmose à Histoplasma capsulatum Granulome médiastinal et médiastinite fibrosante • Rétraction des voies respiratoires lors de la fibrose ganglionnaire • Dilatation des bronches, compression de l’œsophage, ± fistules • Réalisation au maximum d’une médiastinite fibrosante

Clinique de l’histoplasmose à Histoplasma capsulatum Histoplasmose disséminée • • Réinfection ou réactivation ? Forme aiguë rare chez l’immunocompétent Principalement chez : • • Sujets âgés > 50 ans et enfants • • Transplantés rénaux (2, 1 % à Indianapolis) Immunodéprimés, notamment ceux infectés par le VIH (incidence = 25 % en zones endémiques avant 1996) Hémopathies malignes lymphoïdes Mortalité spontanée proche de 100 %
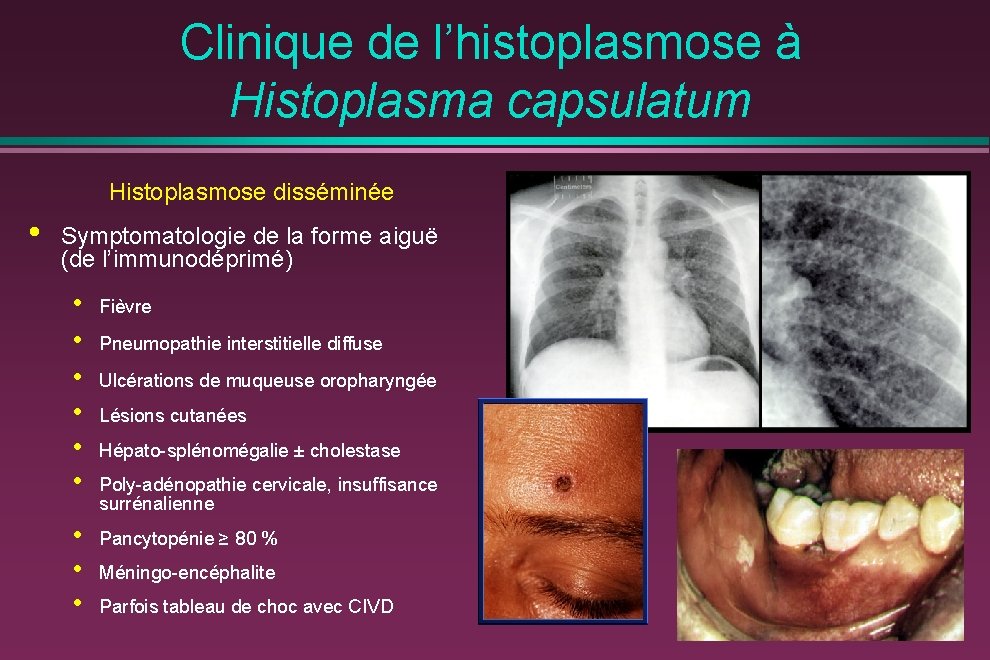
Clinique de l’histoplasmose à Histoplasma capsulatum Histoplasmose disséminée • Symptomatologie de la forme aiguë (de l’immunodéprimé) • • • Fièvre • • • Pancytopénie ≥ 80 % Pneumopathie interstitielle diffuse Ulcérations de muqueuse oropharyngée Lésions cutanées Hépato-splénomégalie ± cholestase Poly-adénopathie cervicale, insuffisance surrénalienne Méningo-encéphalite Parfois tableau de choc avec CIVD

Clinique de l’histoplasmose à Histoplasma capsulatum Histoplasmose disséminée • Principales données d’une étude française chez VIH+ (1984 -1994) • • 56 patients (44 hommes = 78, 6 %) ; 37 ± 7 ans, médiane CD 4 = 20 / mm 3 Durée médiane en zone d’endémie = 17, 5 ans (< 1 mois - 52 ans) Délai médian après retour = 5 ans (< 1 mois - 27 ans) 51 / 56 = formes disséminées • Fièvre = 93 % • Symptômes respiratoires = 59 % • Atteinte cutanée = 48, 2 % • Atteinte digestive = 21, 4 % • Atteinte système nerveux central = 14, 3 % • Sepsis sévère = 14, 3 %
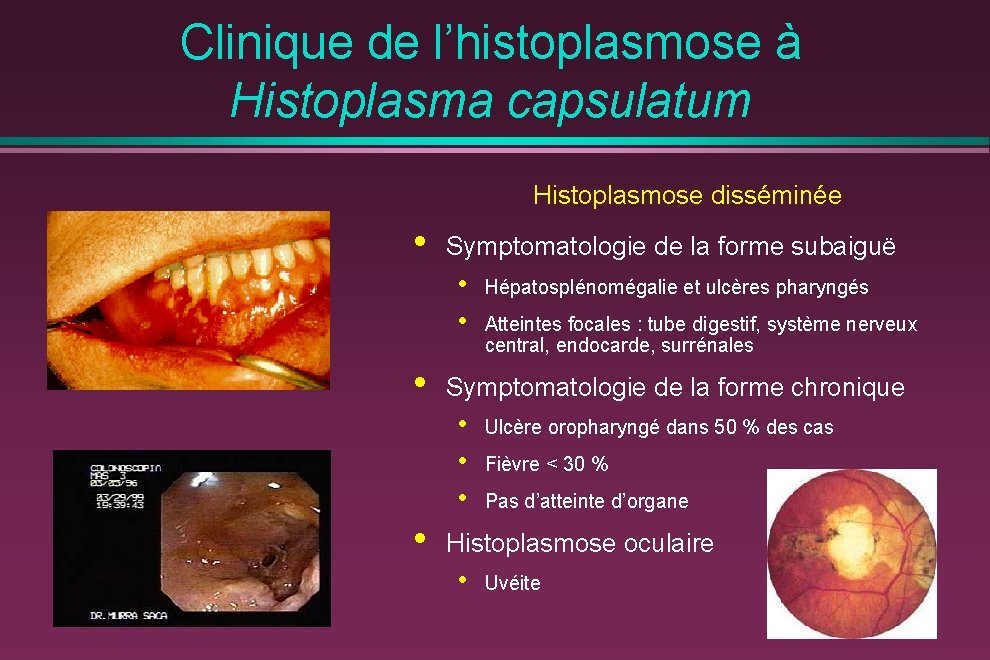
Clinique de l’histoplasmose à Histoplasma capsulatum Histoplasmose disséminée • Symptomatologie de la forme subaiguë • • • Atteintes focales : tube digestif, système nerveux central, endocarde, surrénales Symptomatologie de la forme chronique • • Hépatosplénomégalie et ulcères pharyngés Ulcère oropharyngé dans 50 % des cas Fièvre < 30 % Pas d’atteinte d’organe Histoplasmose oculaire • Uvéite
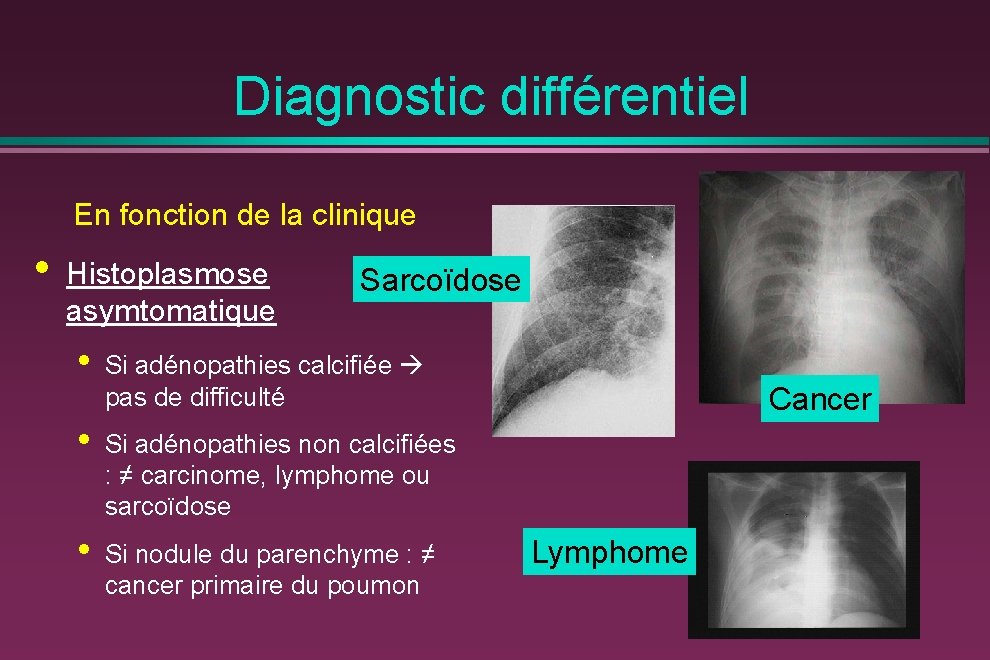
Diagnostic différentiel En fonction de la clinique • Histoplasmose asymtomatique Sarcoïdose • Si adénopathies calcifiée pas de difficulté • Si adénopathies non calcifiées : ≠ carcinome, lymphome ou sarcoïdose • Si nodule du parenchyme : ≠ cancer primaire du poumon Cancer Lymphome
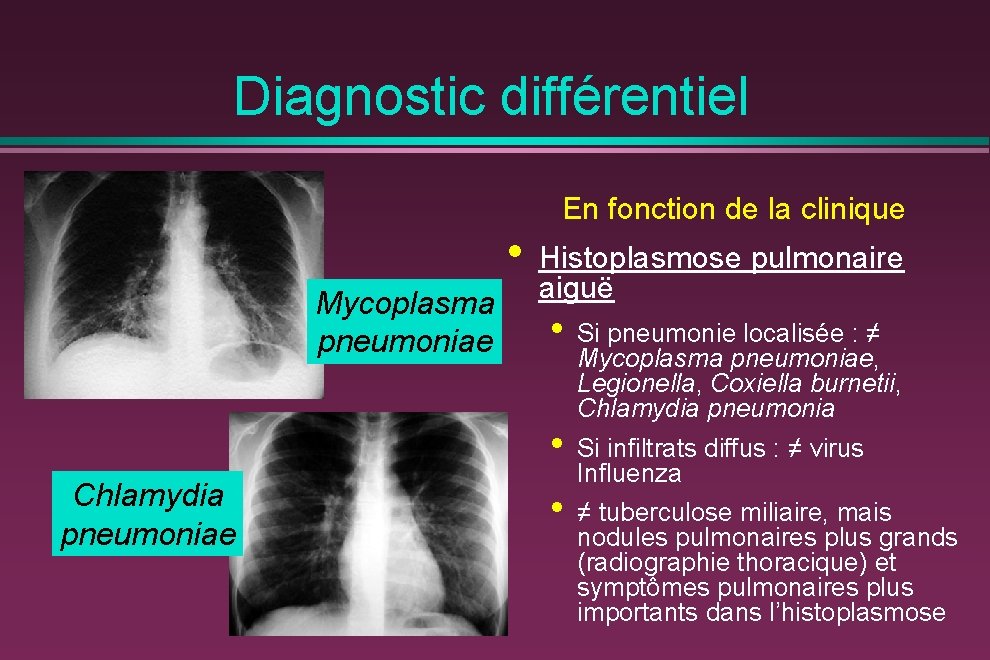
Diagnostic différentiel En fonction de la clinique • Mycoplasma pneumoniae Histoplasmose pulmonaire aiguë • • Chlamydia pneumoniae • Si pneumonie localisée : ≠ Mycoplasma pneumoniae, Legionella, Coxiella burnetii, Chlamydia pneumonia Si infiltrats diffus : ≠ virus Influenza ≠ tuberculose miliaire, mais nodules pulmonaires plus grands (radiographie thoracique) et symptômes pulmonaires plus importants dans l’histoplasmose
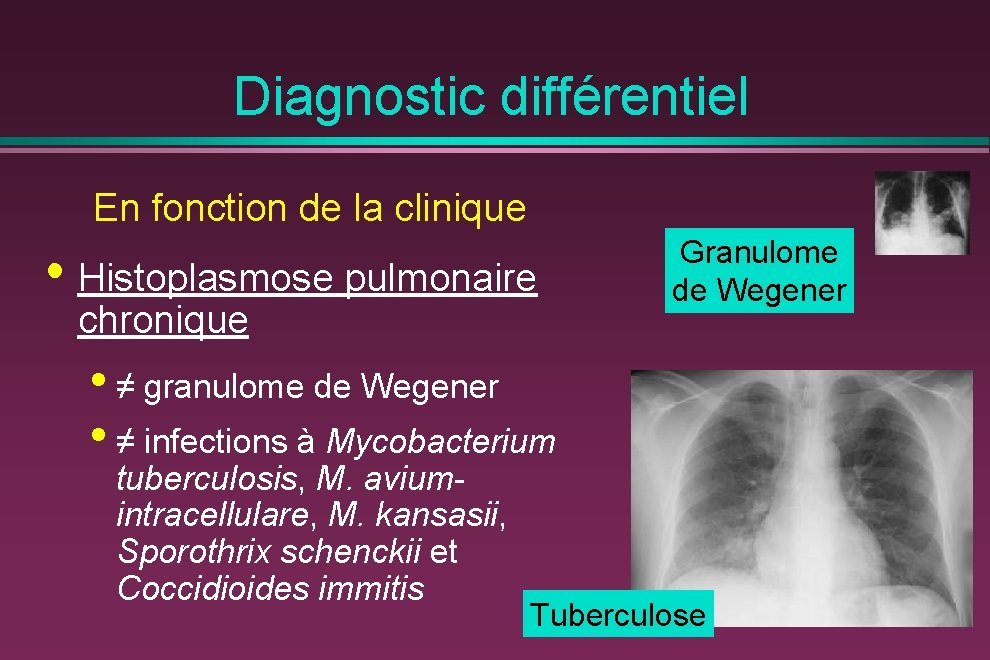
Diagnostic différentiel En fonction de la clinique • Histoplasmose pulmonaire chronique Granulome de Wegener • ≠ granulome de Wegener • ≠ infections à Mycobacterium tuberculosis, M. aviumintracellulare, M. kansasii, Sporothrix schenckii et Coccidioides immitis Tuberculose

Diagnostic différentiel En fonction de la clinique • Histoplasmose disséminée • ≠ tuberculose, leishmaniose viscérale • En Asie : ≠ pénicilliose à Penicillium marneffei (mais épidémiologie différente)
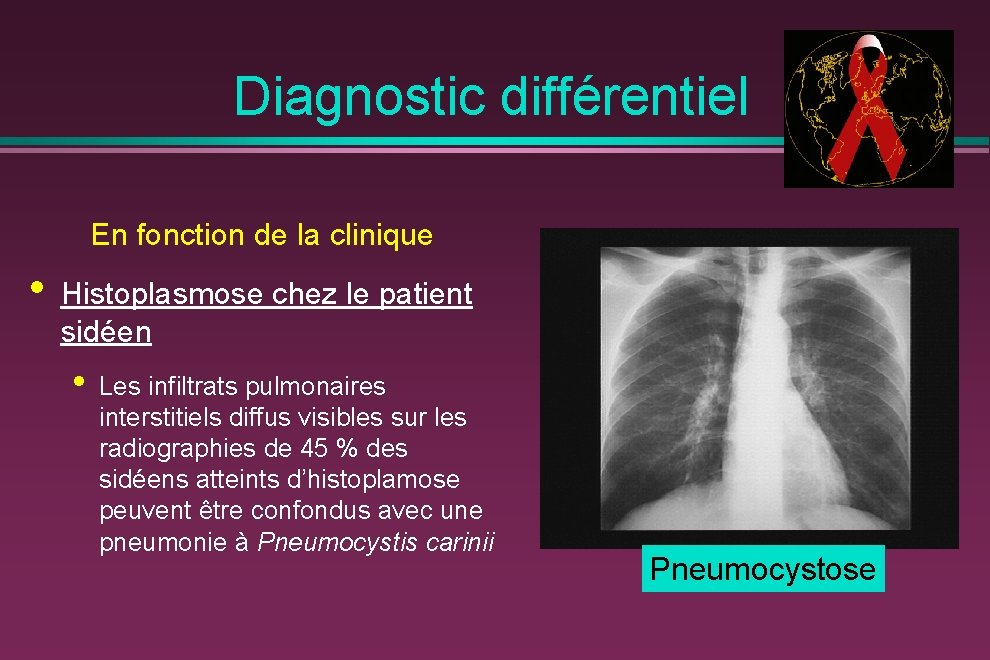
Diagnostic différentiel En fonction de la clinique • Histoplasmose chez le patient sidéen • Les infiltrats pulmonaires interstitiels diffus visibles sur les radiographies de 45 % des sidéens atteints d’histoplamose peuvent être confondus avec une pneumonie à Pneumocystis carinii Pneumocystose
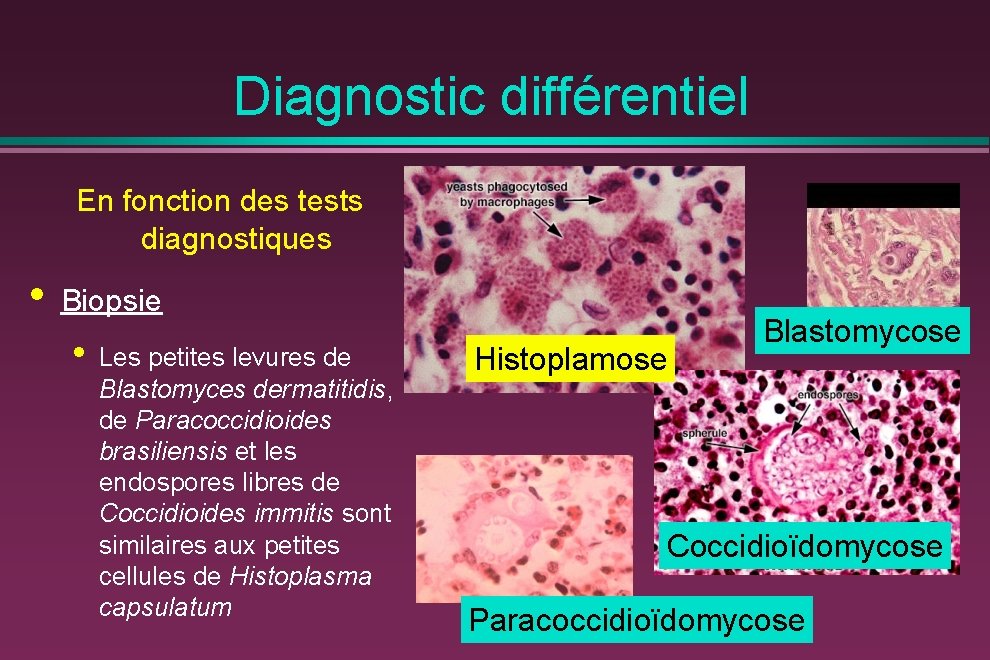
Diagnostic différentiel En fonction des tests diagnostiques • Biopsie • Les petites levures de Blastomyces dermatitidis, de Paracoccidioides brasiliensis et les endospores libres de Coccidioides immitis sont similaires aux petites cellules de Histoplasma capsulatum Histoplamose Blastomycose Coccidioïdomycose Paracoccidioïdomycose
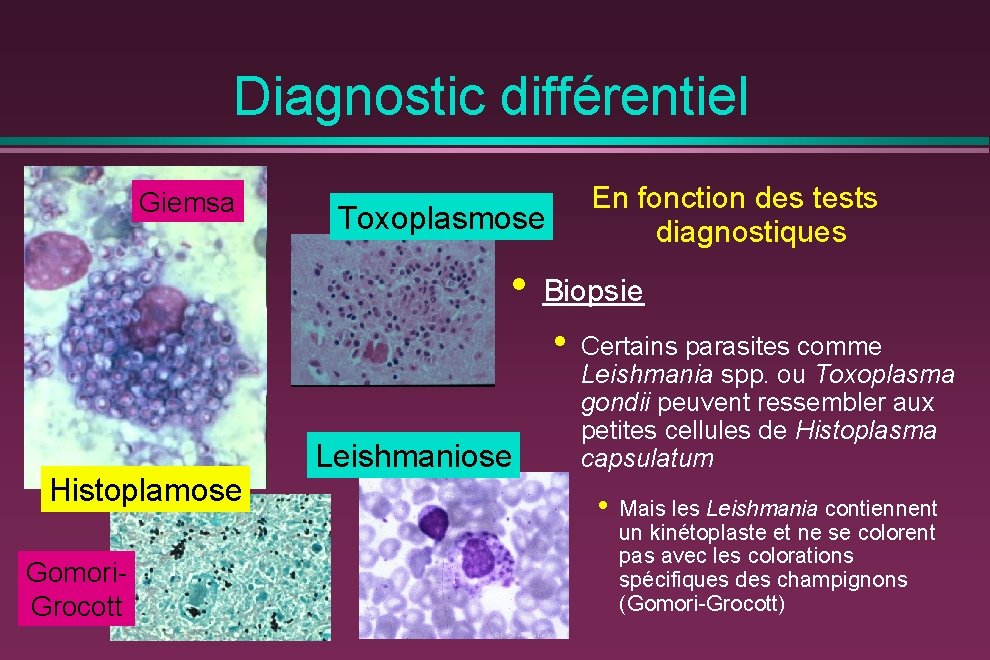
Diagnostic différentiel Giemsa En fonction des tests diagnostiques Toxoplasmose • Biopsie • Histoplamose Gomori. Grocott Leishmaniose Certains parasites comme Leishmania spp. ou Toxoplasma gondii peuvent ressembler aux petites cellules de Histoplasma capsulatum • Mais les Leishmania contiennent un kinétoplaste et ne se colorent pas avec les colorations spécifiques des champignons (Gomori-Grocott)
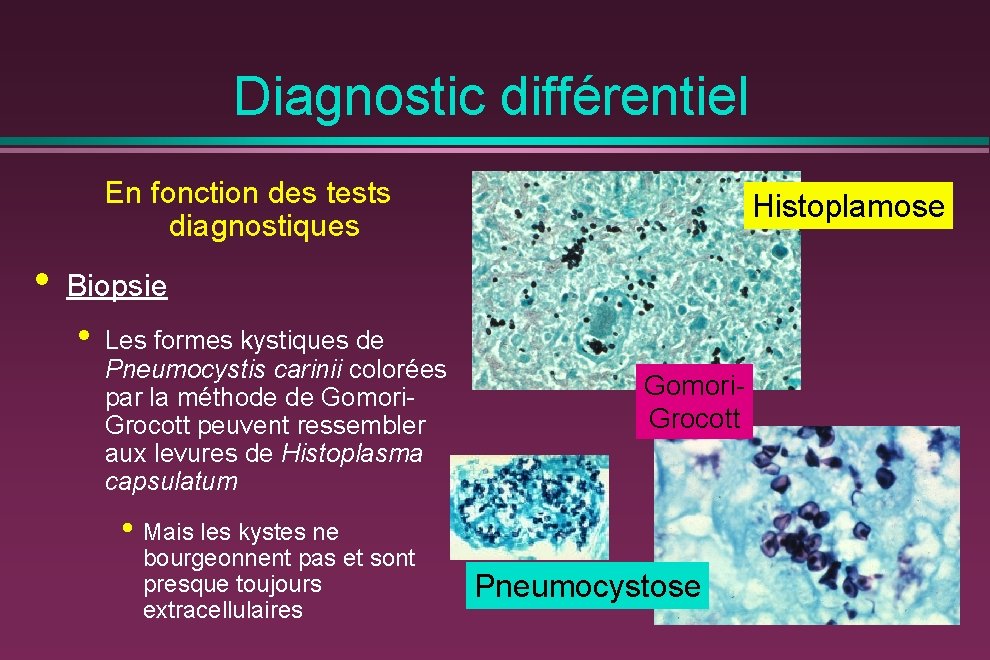
Diagnostic différentiel En fonction des tests diagnostiques • Histoplamose Biopsie • Les formes kystiques de Pneumocystis carinii colorées par la méthode de Gomori. Grocott peuvent ressembler aux levures de Histoplasma capsulatum Gomori. Grocott • Mais les kystes ne bourgeonnent pas et sont presque toujours extracellulaires Pneumocystose
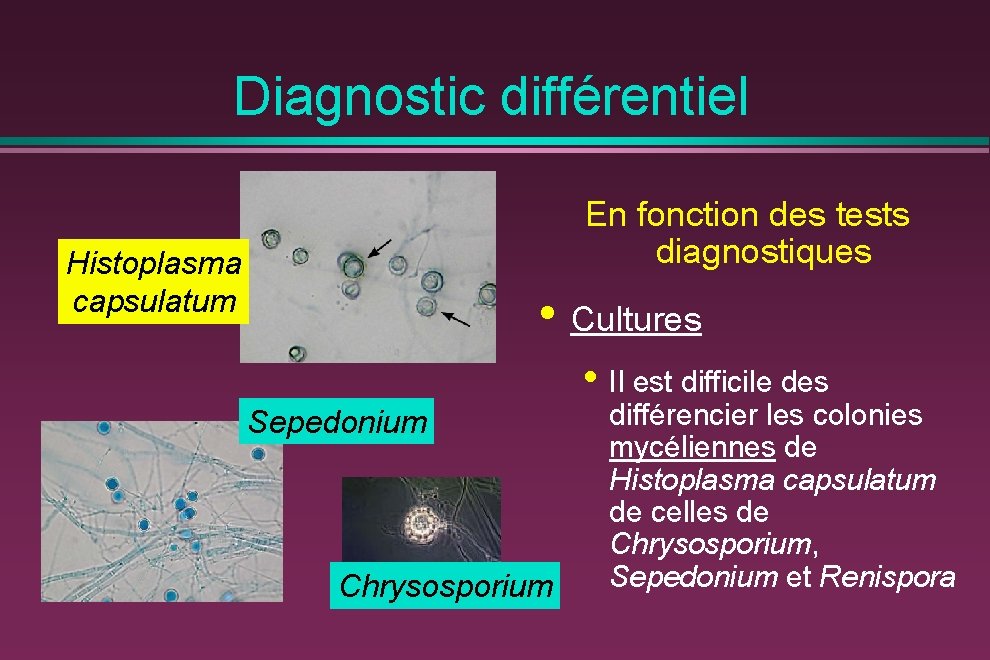
Diagnostic différentiel En fonction des tests diagnostiques Histoplasma capsulatum • Cultures • Il est difficile des Sepedonium Chrysosporium différencier les colonies mycéliennes de Histoplasma capsulatum de celles de Chrysosporium, Sepedonium et Renispora
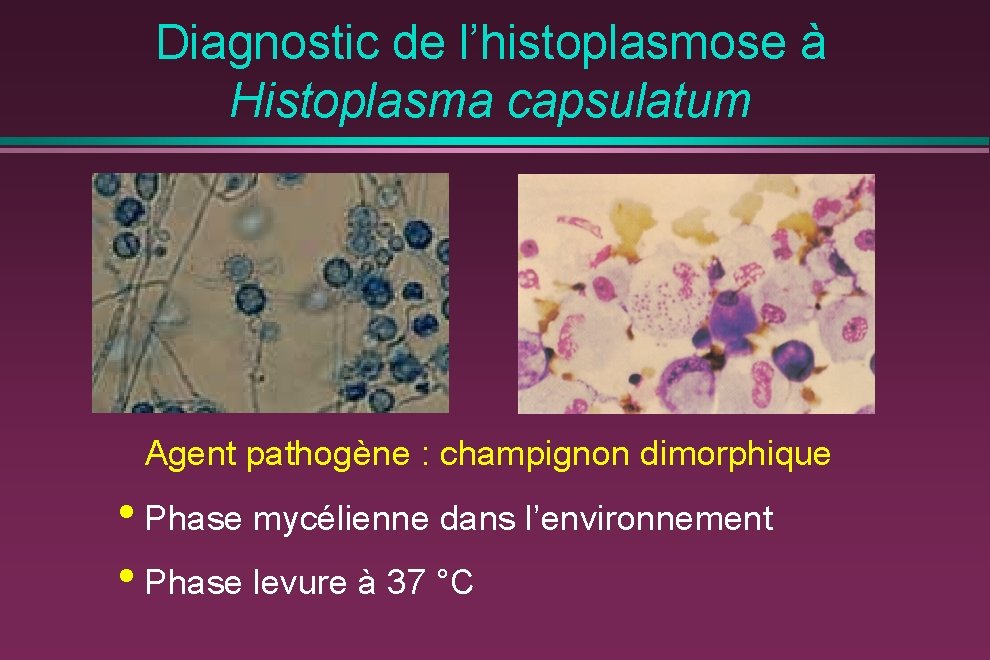
Diagnostic de l’histoplasmose à Histoplasma capsulatum Agent pathogène : champignon dimorphique • Phase mycélienne dans l’environnement • Phase levure à 37 °C

Diagnostic de l’histoplasmose à Histoplasma capsulatum Prélèvements • D'origine pulmonaire : lavage broncho alvéolaire > aspiration bronchique > expectoration • Superficiels = présence de champignons saprophytes des muqueuses peut gêner recherche des levures • Sang • • Frottis sanguin (exceptionnel) Couche leucocytaire par leucocytoconcentration (55 % à 90 % au cours du SIDA)

Diagnostic de l’histoplasmose à Histoplasma capsulatum Prélèvements • Mœlle par ponction sternale ou biopsie (70 à 75 %) • Frottis ou biopsies de lésions de muqueuse buccale, pharyngée ou laryngée • Biopsies diverses : ganglionnaire, hépatique, splénique, intestinale, surrénalienne, … • Fluides divers : LCR, liquide gastrique, urine, …
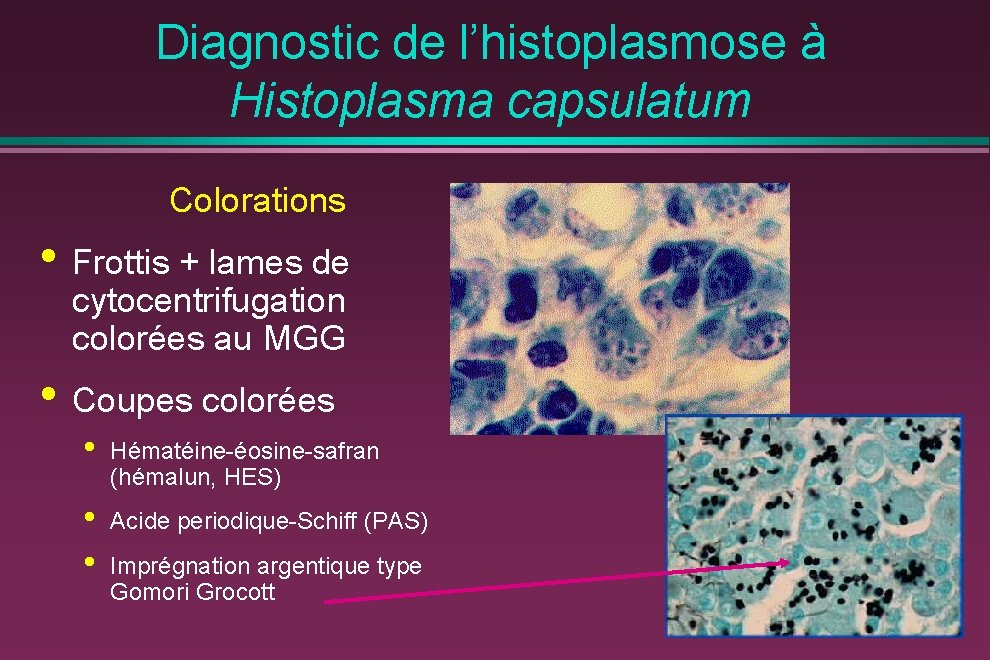
Diagnostic de l’histoplasmose à Histoplasma capsulatum Colorations • Frottis + lames de cytocentrifugation colorées au MGG • Coupes colorées • Hématéine-éosine-safran (hémalun, HES) • • Acide periodique-Schiff (PAS) Imprégnation argentique type Gomori Grocott

Diagnostic de l’histoplasmose à Histoplasma capsulatum Anomalies biologiques fréquentes • Pancytopénie dans 55 % des cas • Anomalies hépatiques : augmentation phosphatases alcalines + transaminases • Syndrome d’activation macrophagique
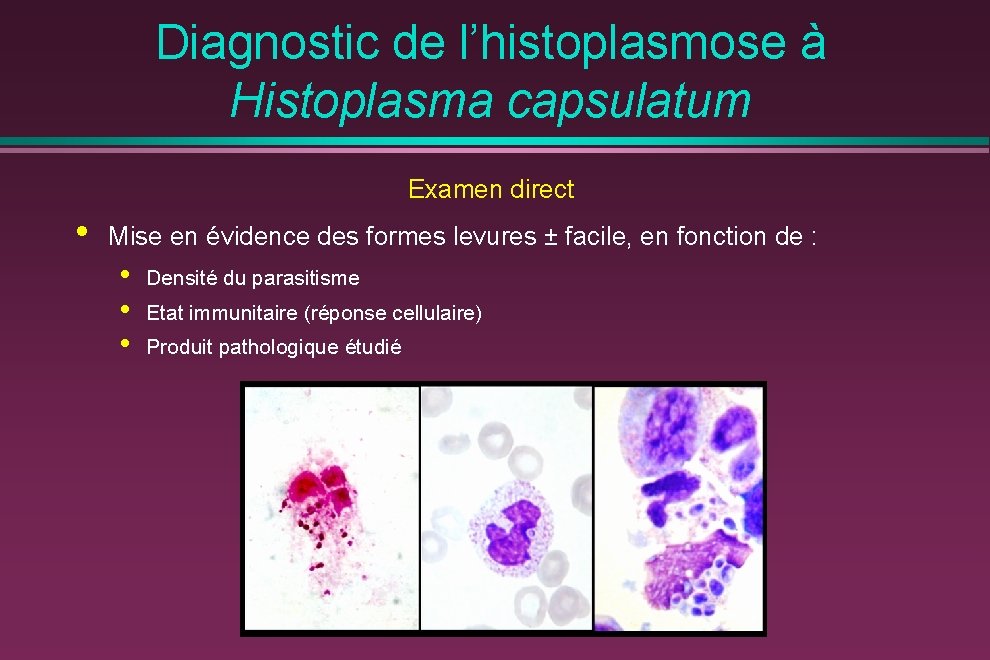
Diagnostic de l’histoplasmose à Histoplasma capsulatum Examen direct • Mise en évidence des formes levures ± facile, en fonction de : • • • Densité du parasitisme Etat immunitaire (réponse cellulaire) Produit pathologique étudié
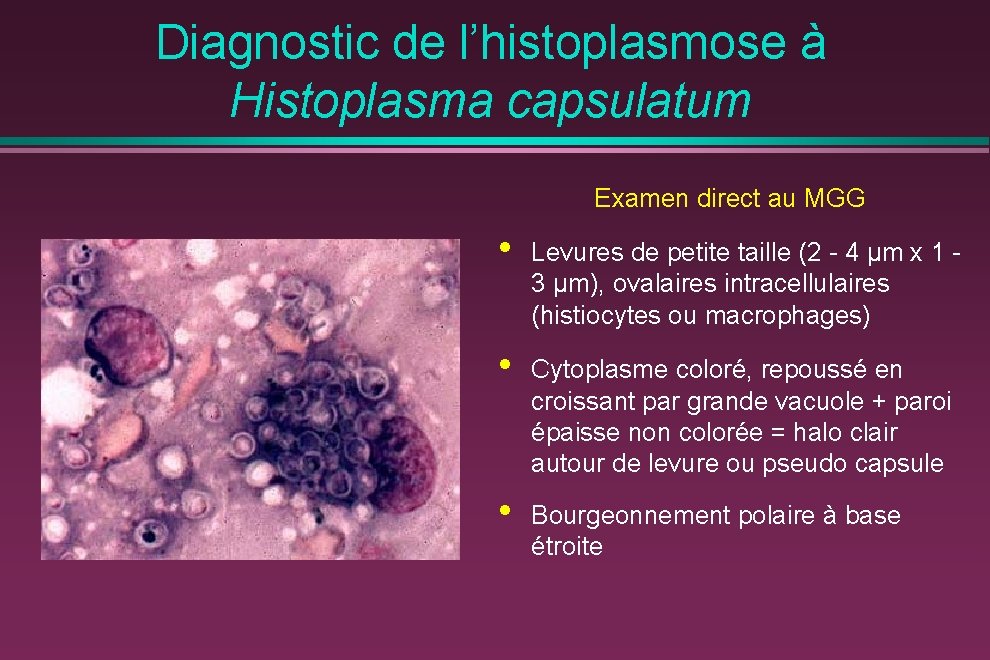
Diagnostic de l’histoplasmose à Histoplasma capsulatum Examen direct au MGG • Levures de petite taille (2 - 4 μm x 1 3 μm), ovalaires intracellulaires (histiocytes ou macrophages) • Cytoplasme coloré, repoussé en croissant par grande vacuole + paroi épaisse non colorée = halo clair autour de levure ou pseudo capsule • Bourgeonnement polaire à base étroite
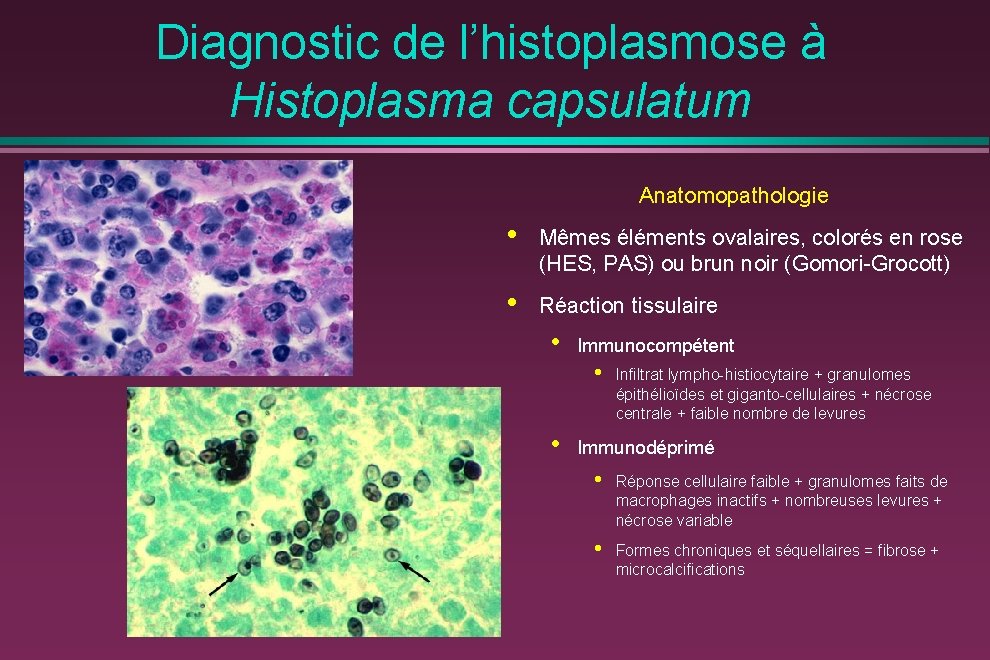
Diagnostic de l’histoplasmose à Histoplasma capsulatum Anatomopathologie • Mêmes éléments ovalaires, colorés en rose (HES, PAS) ou brun noir (Gomori-Grocott) • Réaction tissulaire • • Immunocompétent • Infiltrat lympho-histiocytaire + granulomes épithélioïdes et giganto-cellulaires + nécrose centrale + faible nombre de levures Immunodéprimé • Réponse cellulaire faible + granulomes faits de macrophages inactifs + nombreuses levures + nécrose variable • Formes chroniques et séquellaires = fibrose + microcalcifications

Diagnostic de l’histoplasmose à Histoplasma capsulatum Mise en culture des produits pathologiques • Manipulation des souches • Danger potentiel d'infestation par inhalation des spores (nombreux cas) hotte à flux laminaire

Diagnostic de l’histoplasmose à Histoplasma capsulatum Mise en culture des produits pathologiques • • Milieux riches : • • Sabouraud, gélose glucosée à la pomme de terre (PDA) • • • Gélose à l'extrait de levure + phosphate (YEP agar) Gélose coeur-cerveau (BHI agar additionné de 8 à 10 % de sang de cheval stérile ) Milieu de Kurung et Yegian Milieu synthétique de Pine et Drouhet + antibiotiques (chloramphénicol 50 mg / ml) + actidione (0, 5 mg / ml)

Diagnostic de l’histoplasmose à Histoplasma capsulatum Mise en culture des produits pathologiques • Meilleure technique d'hémoculture = lysecentrifugation (Isolator®) • Cultures en tubes (grand nombre) • Incubation à 37 °C, humidité = 100 % • Atmosphère enrichie en CO 2

Diagnostic de l’histoplasmose à Histoplasma capsulatum Mise en culture des produits pathologiques • Tubes gardés 1 mois : surveillance régulière des cultures • Développement : 10 à 30 jours d'une colonie duveteuse blanche, puis ocrée, à recto marron, plane puis à centre surélevé • Morphologie caractéristique du genre Histoplasma identique à celle de Histoplasma duboisii

Diagnostic de l’histoplasmose à Histoplasma capsulatum Mise en culture des produits pathologiques • Forme mycélienne de Histoplasma capsulatum obtenue par culture à température du laboratoire ou 30 °C
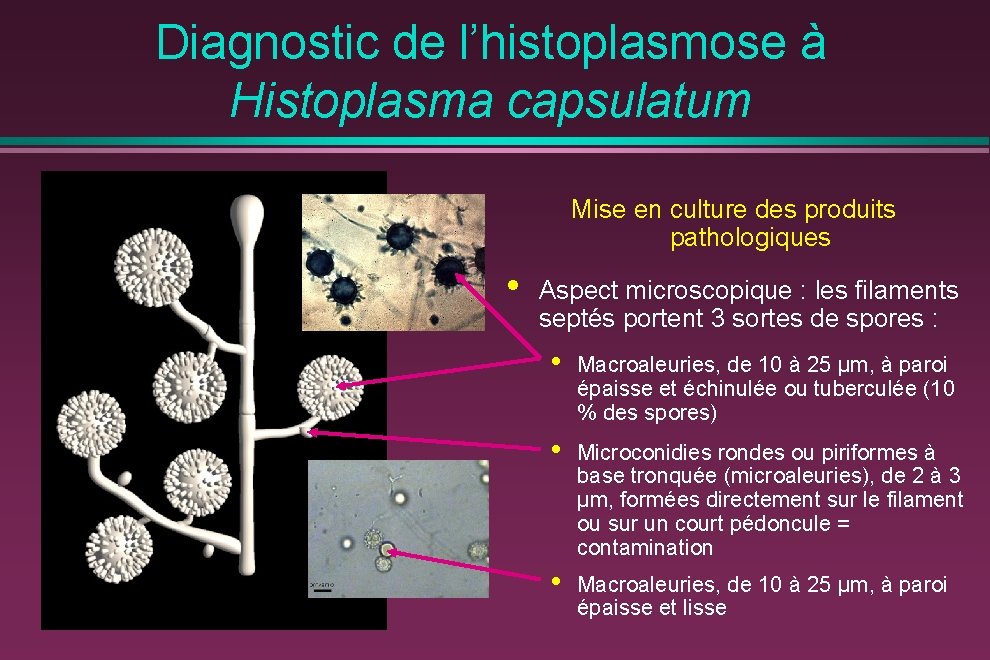
Diagnostic de l’histoplasmose à Histoplasma capsulatum Mise en culture des produits pathologiques • Aspect microscopique : les filaments septés portent 3 sortes de spores : • Macroaleuries, de 10 à 25 μm, à paroi épaisse et échinulée ou tuberculée (10 % des spores) • Microconidies rondes ou piriformes à base tronquée (microaleuries), de 2 à 3 μm, formées directement sur le filament ou sur un court pédoncule = contamination • Macroaleuries, de 10 à 25 μm, à paroi épaisse et lisse

Diagnostic de l’histoplasmose à Histoplasma capsulatum • Confirmation de l'identification de la souche recherchée par deux tests : • Test de l'uréase, réalisé sur milieu Urea-Agar Base (Difco) : fortement positif en 48 heures (différencie Histoplasma capsulatum d'Histoplasma duboisii, très faiblement positif ou négatif) • Identification des exo antigènes : réalisé par les laboratoires de référence • Formation en immuno-diffusion de lignes de précipitation spécifiques H et / ou M (entre un filtrat de culture concentré de souche et antisérum spécifique)

Diagnostic de l’histoplasmose à Histoplasma capsulatum Mise en culture des produits pathologiques • L'inoculation à l'animal = bon moyen d'obtention du champignon à partir de prélèvements très souillés • Intra-testiculaire au cobaye • Intra-péritonéal au hamster doré ou souris

Diagnostic de l’histoplasmose à Histoplasma capsulatum Biologie moléculaire • Difficulté + lenteur des moyens diagnostiques classiques développement des techniques PCR dans certains laboratoires de référence
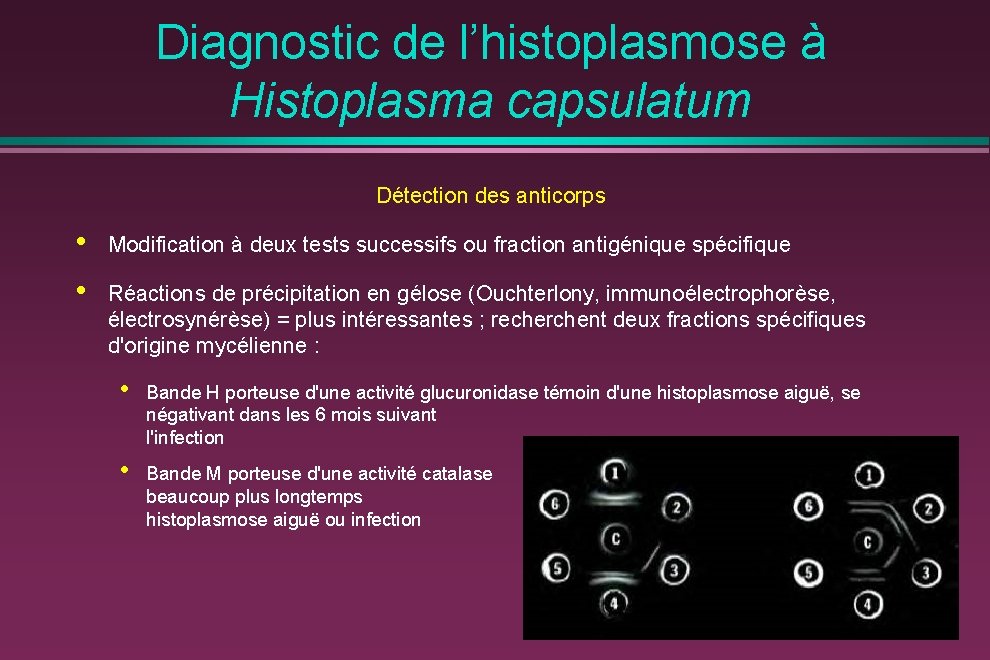
Diagnostic de l’histoplasmose à Histoplasma capsulatum Détection des anticorps • • Modification à deux tests successifs ou fraction antigénique spécifique Réactions de précipitation en gélose (Ouchterlony, immunoélectrophorèse, électrosynérèse) = plus intéressantes ; recherchent deux fractions spécifiques d'origine mycélienne : • Bande H porteuse d'une activité glucuronidase témoin d'une histoplasmose aiguë, se négativant dans les 6 mois suivant l'infection • Bande M porteuse d'une activité catalase beaucoup plus longtemps histoplasmose aiguë ou infection persiste chronique

Diagnostic de l’histoplasmose à Histoplasma capsulatum Détection des anticorps • • • Spécificité proche de 95 % Sensibilité = 80 % chez immunocompétents, 50 % chez immunodéprimés Réaction de fixation du complément avec l'antigène levure : • • • Significative si taux > 1/32 Sensibilité identique à sérologie classique (80 % à 50 %) et spécificité moindre Réactions sérologiques classiques croisées avec autres champignons dimorphiques : Histoplasma duboisii (même forme mycélienne même sérologie que Histoplasma capsulatum), Blastomyces dermatitidis, Paracoccidioides brasiliensis, Coccidioides immitis

Diagnostic de l’histoplasmose à Histoplasma capsulatum Détection des antigènes circulants • Positive même chez les sujets immunodéprimés et réalisable à partir de tous les liquides biologiques • Deux tests dans laboratoires de référence aux USA : • Détection d'un antigène polysaccharidique par technique radio-immunologique • • Sensibilité : urines > sérum, (> 90 % dans histoplasmose disséminée, moyenne (40 %) si histoplasmose chronique ou limitée Détection de fraction antigénique plus spécifique (70 k. Da) par ELISA et Western Blot • Spécificité meilleure, sensibilité = ; sérum > urines
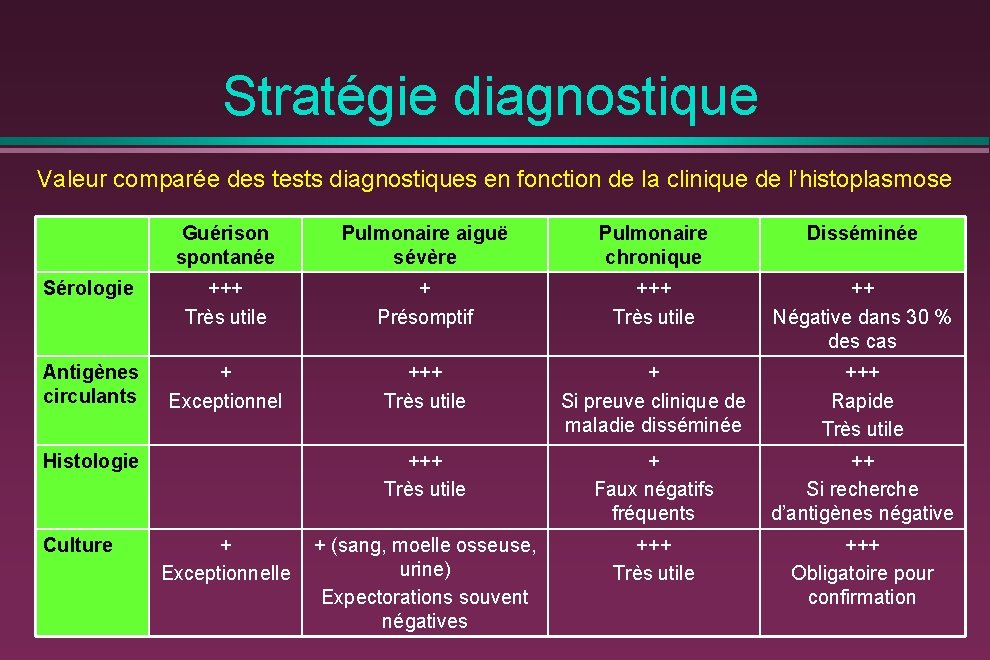
Stratégie diagnostique Valeur comparée des tests diagnostiques en fonction de la clinique de l’histoplasmose Guérison spontanée Pulmonaire aiguë sévère Pulmonaire chronique Disséminée Sérologie +++ Très utile + Présomptif +++ Très utile ++ Négative dans 30 % des cas Antigènes circulants + Exceptionnel +++ Très utile + Si preuve clinique de maladie disséminée +++ Rapide Très utile +++ Très utile + Faux négatifs fréquents ++ Si recherche d’antigènes négative + (sang, moelle osseuse, urine) Expectorations souvent négatives +++ Très utile +++ Obligatoire pour confirmation Histologie Culture + Exceptionnelle

Traitement de l’histoplasmose à Histoplasma capsulatum Patient immunocompétent • Primo-infection • Habituellement pas de traitement (kétoconazole / itraconazole / fluconazole utilisables) • Indications du traitement : • Formes pulmonaires chroniques • Formes disséminées ou endovasculaires • Formes méningées

Traitement de l’histoplasmose à Histoplasma capsulatum Patient immunocompétent • Histoplasmose pulmonaire chronique • Amphotéricine B • Efficacité : 75 % des cas • Durée du traitement : 6 semaines à 4 mois) • Kétoconazole • Efficacité : 84 % des cas • Posologie recommandée : 400 mg / jour • Durée de traitement : 6 à 12 mois

Traitement de l’histoplasmose à Histoplasma capsulatum Patient immunocompétent • Histoplasmose pulmonaire chronique • Itraconazole • • Efficacité : • • 65 % dans les formes cavitaires 100 % dans les formes parenchymateuses nodulaires Posologie recommandée : 200 à 400 mg / jour Durée médiane de traitement : 9 mois Fluconazole • • • Efficacité : 46 % des cas Posologie : 400 mg / jour Durée médiane de traitement : 7 mois

Traitement de l’histoplasmose à Histoplasma capsulatum Patient immunocompétent • Histoplasmose disséminée (atteintes endovasculaires) • Amphotéricine B • • Rechutes dans 5 à 23 % des cas Kétoconazole • • Réponse dans 55 à 100 % des cas • Durée de traitement : > 6 mois Posologie : 400 mg / jour (800 mg non recommandé toxicité et moindre efficacité)

Traitement de l’histoplasmose à Histoplasma capsulatum Patient immunocompétent • Histoplasmose disséminée (atteintes endovasculaires) • Itraconazole • 50 à 100 mg / jour, 6 mois : • • • 97 % d'amélioration 31 % de guérison 200 à 400 mg / jour, 9 mois : 100 % d'efficacité Enfant : 7, 2 mg kg / jour, ≥ 3 mois Fluconazole • • • Efficacité : 71 % des cas Posologie : 200 - 800 mg / jour Durée médiane de traitement : 11 mois

Traitement de l’histoplasmose à Histoplasma capsulatum Patient immunocompétent • Histoplasmose méningée • Rechutes dans 50 % (surveillance prolongée) • Inefficacité du kétoconazole (pas de pénétration dans le LCR) • Place de l'itraconazole et du fluconazole non précisée • Surveillance du LCR pendant 1 an après la guérison

Traitement de l’histoplasmose à Histoplasma capsulatum Patient VIH + • Le traitement comporte une phase d'attaque et une prophylaxie secondaire • L'amphotéricine B reste le traitement de référence des formes sévères (hypotension, hypoxie, troubles neuro-psychiatriques, myosite, CIVD) • L'itraconazole est le traitement de choix pour les formes non menaçantes et la prophylaxie secondaire

Traitement de l’histoplasmose à Histoplasma capsulatum Patient VIH + : traitement d’attaque • Amphotéricine B (ou dérivé liposomial) • 80 % de rémission obtenues rapidement • Posologie : 1 mg / kg / jour pendant 14 jours, puis relais par l'itraconazole • Kétoconazole • Non indiqué dans l'histoplasmose au cours du SIDA (réponse < 20 %)

Traitement de l’histoplasmose à Histoplasma capsulatum Patient VIH + : traitement d’attaque • Itraconazole • • • Réponses dans 84 % des cas à 600 mg / jour pendant 3 jours puis 400 mg / jour pendant 3 mois Rémission chez 7 / 12 patients Rapidité d'efficacité moindre qu'avec l‘amphotéricine B Surveillance des taux sériques et des interférences médicamenteuses Fluconazole • • • Administré chez 10 patients à des posologies allant de 100 à 800 mg / jour 4 succès 50 patients, 1600 mg J 1, puis 800 mg / jour pendant 12 semaines efficacité = 74 % Rechutes avec souches résistantes

Traitement de l’histoplasmose à Histoplasma capsulatum Patient VIH + : prophylaxie secondaire • Rechutes sans traitement = 35 à 80 % traitement à vie • Amphotéricine B • Toutes les semaines ou tous les 15 jours : efficacité de 80 à 95 % contre 50 % avec le kétoconazole • Contre-indiquée si atteinte neurologique initiale • Infections des voies veineuses centrales fréquentes

Traitement de l’histoplasmose à Histoplasma capsulatum Patient VIH + : prophylaxie secondaire • • Itraconazole • Efficacité : 95 % (200 mg ± x 2 / jour) après induction par amphotéricine B ; médiane de survie = 109 semaines • • Efficace dans l'endocardite et dans les formes neurologiques Prophylaxie secondaire de choix ; possibilité d’interruption si CD 4 > 150 / mm 3 Fluconazole • Rechutes dans 12 % des cas à la posologie de 100 - 400 mg / jour

Traitement de l’histoplasmose à Histoplasma capsulatum Patient VIH + : prophylaxie primaire • Efficacité de l’itraconazole (200 mg / jour) vs placebo • Pas de diminution de l'incidence sous fluconazole

Protection des personnes à risque Réduction de l’exposition des travailleurs à Histoplasma capsulatum • Dénicher les colonies de chauves-souris ou d’oiseaux

Protection des personnes à risque Chauves-souris • Dispositifs à ultra-sons et repellent chimiques inefficaces • Fermer TOUTES les ouvertures SAUF UNE avec une valve d’exclusion • Construction d’une zone de nidification contrôlée • (Hibernation)

Protection des personnes à risque Oiseaux • • Fermer toutes les ouvertures • Repellents chimiques non toxiques (liquide, aérosol, film, pâte) non permanents (ré application périodique) • Repellents semi-permanents : systèmes mécaniques anti-perchages (maintenance) • • Déplacement des oiseaux : peu efficace Temporairement : dissuasion visuelle ou sonore (Abattage)

Protection des personnes à risque • Signaler les zones à risques • Toutes les zones contaminées par Histoplasma capsulatum - ou susceptibles de l’être – doivent être signalées • L’avertissement doit fournir le nom et le numéro de téléphone d’une personne à contacter en cas de question à poser au sujet de cette zone • Dans certains cas, une clôture doit être construite autour de la propriété, ou des verrous posés sur les portes des greniers pour empêcher l’entrée d’individus non protégés

Protection des personnes à risque • Prévenir les travailleurs des risques encourus (par écrit)

Protection des personnes à risque • Contrôler la poussière mise en suspension lors d’activités de construction, d’excavation ou de démolition (mouillage, aspiration avec filtre haute efficacité) • Cabines à air conditionné (bulldozers, camions, …), nettoyage des camions

Protection des personnes à risque

Protection des personnes à risque • Désinfecter le matériel contaminé • Terre contaminée : saturation par le formol (peu écologique et toxique), eau de Javel, …

Protection des personnes à risque • Porter un équipement personnel de protection • Respirateur purificateur d’air équipé de filtre « High Efficiency Particulate Air » (HEPA) capable de filtrer des particules ≤ 2 m • Bleu de travail avec capuche et gants jetables

Le guano se ramasse à la pelle … … et l’histoplasmose aussi

Que faut-il retenir ? • Éviter les cavernes et les grottes, surtout pour une personne immunodéprimée • Consulter son médecin en cas d'apparition de toux ou de syndrome grippal au retour de vacances

Protegez les chauves –souris … … mais méfiez-vous de Batman

Histoplasmose à Histoplasma duboisii

Epidémiologie de l’histoplasmose à Histoplasma duboisii • Histoplasma duboisii : Afrique centrale et de l’ouest (Ouganda, Nigeria, RD Congo, Sénégal) • Principalement chez l’immunocompétent • Rarement décrite chez VIH+ • Champignon isolé chez homme et singe (babouins, cynocéphales), rarement dans sol • Infection contractée par voie respiratoire, voie cutanée ?
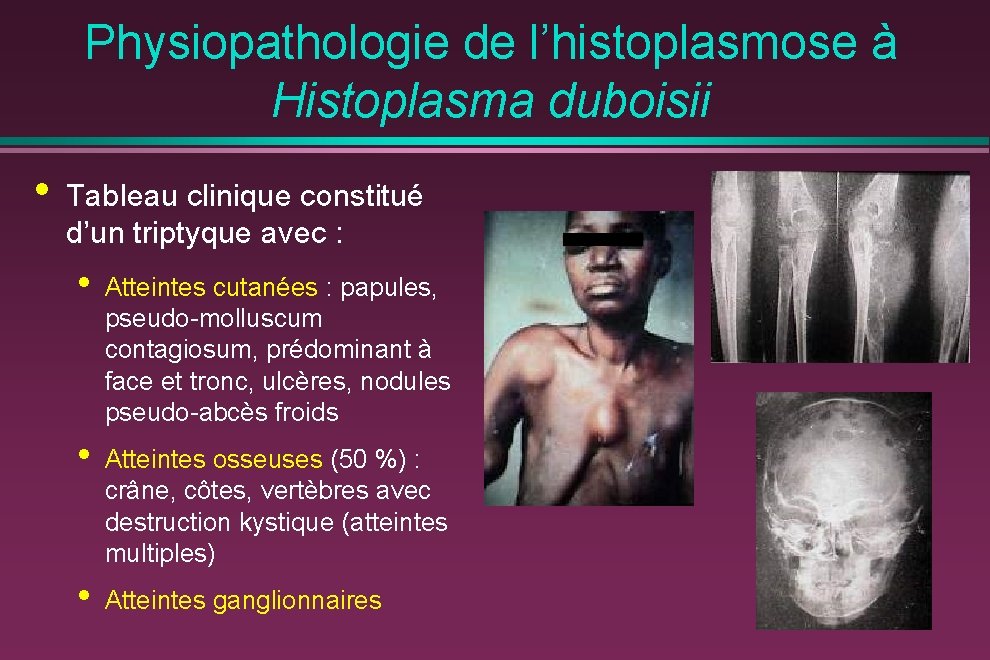
Physiopathologie de l’histoplasmose à Histoplasma duboisii • Tableau clinique constitué d’un triptyque avec : • Atteintes cutanées : papules, pseudo-molluscum contagiosum, prédominant à face et tronc, ulcères, nodules pseudo-abcès froids • Atteintes osseuses (50 %) : crâne, côtes, vertèbres avec destruction kystique (atteintes multiples) • Atteintes ganglionnaires

Physiopathologie de l’histoplasmose à Histoplasma duboisii • Atteintes pulmonaires et disséminées (multiviscérales) plus rares, de mauvais pronostic

Diagnostic de l’histoplasmose à Histoplasma duboisii Agent pathogène • Histoplasma duboisii est un champignon dimorphique Prélèvements • • • Frottis ou biopsie de lésions cutanées Biopsie ou ponction ganglionnaire Ponction d'abcès para-osseux ou biopsie osseuse Prélèvements pulmonaires Formes parasitaires levures de Histoplasma duboisii = grande abondance dans les tissus

Diagnostic de l’histoplasmose à Histoplasma duboisii Examen direct • Frottis sont examinés à frais, levures faiblement colorées par MGG • Coupes colorées au PAS ou Gomori-Grocott • Eléments de grande taille (8 - 15 μm / 4 - 6 μm), ovalaires (en citron) + paroi épaisse à double contour, souvent un ou deux globules graisseux intra-cellulaires + bourgeonnement polaire ou bipolaire en courtes chaînettes à base étroite • Levures dans granulomes inflammatoires, libres ou incluses dans le cytoplasme de plasmodes ou cellules géantes
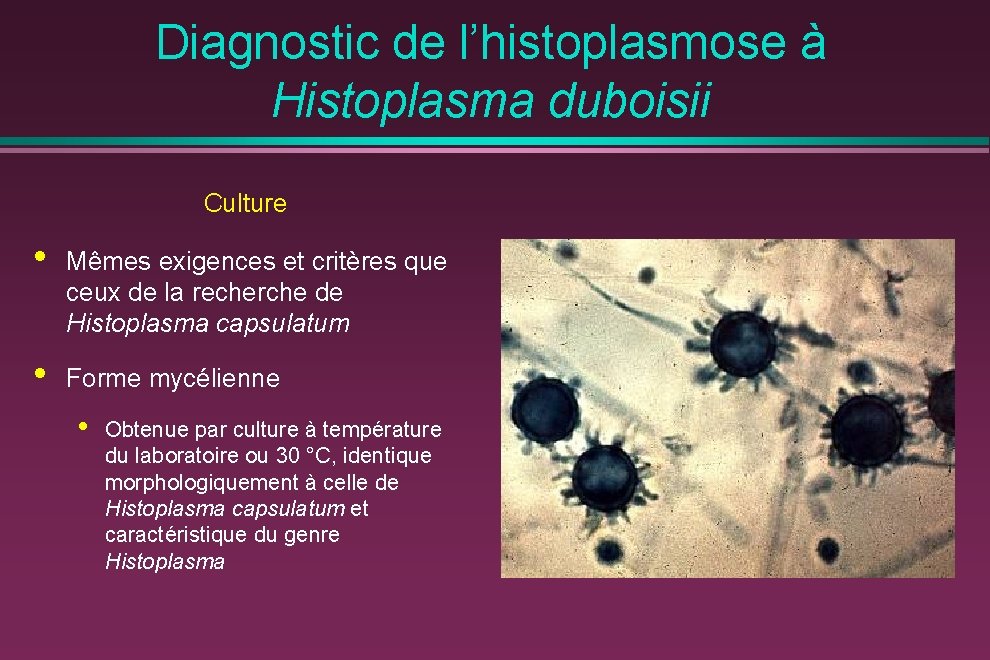
Diagnostic de l’histoplasmose à Histoplasma duboisii Culture • Mêmes exigences et critères que ceux de la recherche de Histoplasma capsulatum • Forme mycélienne • Obtenue par culture à température du laboratoire ou 30 °C, identique morphologiquement à celle de Histoplasma capsulatum et caractéristique du genre Histoplasma
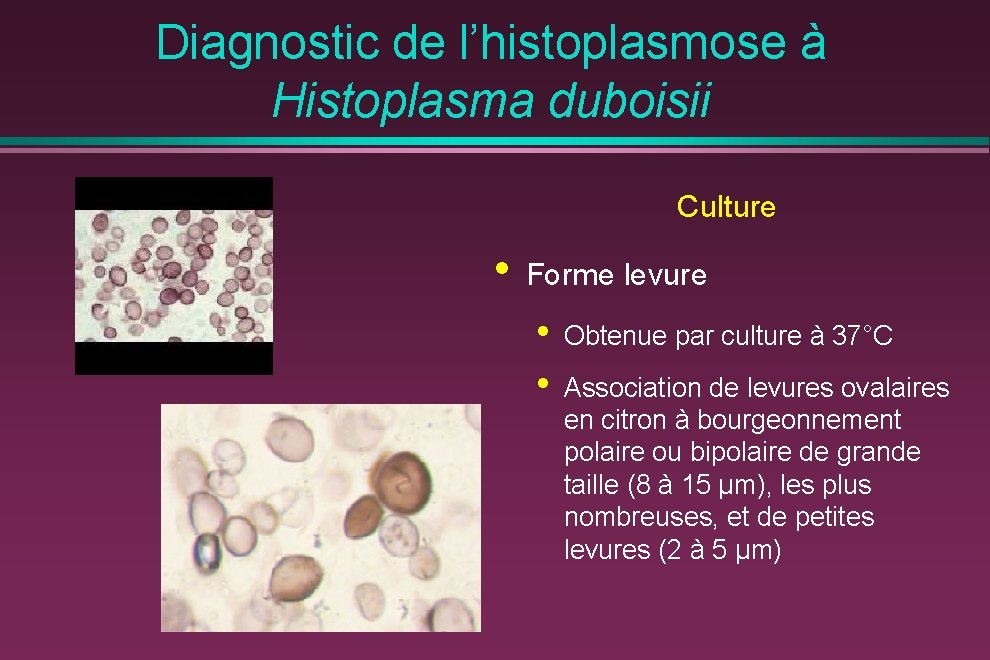
Diagnostic de l’histoplasmose à Histoplasma duboisii Culture • Forme levure • • Obtenue par culture à 37°C Association de levures ovalaires en citron à bourgeonnement polaire ou bipolaire de grande taille (8 à 15 μm), les plus nombreuses, et de petites levures (2 à 5 μm)

Diagnostic de l’histoplasmose à Histoplasma duboisii Inoculation à l’animal • Recherche des levures sur coupes histologiques (petites levures puis après 3 à 4 semaines, grandes levures) Diagnostic indirect • Techniques sérologiques classiques, utilisant mêmes réactifs que Histoplasma capsulatum = peu valables • Faible spécificité (réactions croisées avec autres champignons dimorphiques) • Faible sensibilité (30 à 50 % de faux négatifs)

Traitement de l’histoplasmose à Histoplasma duboisii • Médicaments • Amphotéricine B • • Kétoconazole • • 400 à 800 mg / jour pendant 3 mois puis posologie + faible pendant au moins 6 à 12 mois Itraconazole • • Dose cumulative de 2 g Efficacité dans quelques cas en 6 à 12 mois dans des formes résistantes évoluant depuis plusieurs années Fluconazole • Rares observations Chirurgie Rechutes parfois tardives (fausse rémission)
- Slides: 103