HIPERFUNCIN GLUCOCORTICOIDE SNDROME DE CUSHING Beln Gmez Vives
HIPERFUNCIÓN GLUCOCORTICOIDE: SÍNDROME DE CUSHING Belén Gómez Vives MIR-2 MFy. C. Tutor: Jesús Romero CS Rafalafena

DEFINICIÓN Ø Conjunto de alteraciones clínicas y metabólicas que se producen por el exceso crónico de GC. www. pituitarysociety. org

ETIOLOGÍA CUSHING ENDÓGENO 1. Dependiente de ACTH (80%): - Hiperproducción hipofisaria (enfermedad de Cushing): 70% (lo + frec. el microadenoma) - Secreción ectópica de ACTH y/o CRH 10 -15%: 50% Ca. Broncogénico micronodular, Ca de timo, páncreas, ovario, CMT, feocromocitoma… 2. Independiente de ACTH (20%): - Adenoma suprarrenal: 8 -15% - Carcinoma suprarrenal: 6% - Hiperplasia nodular suprarrenal: 3%

CUSHING EXÓGENO Causa más frecuente 1. Administración prolongada de GC. 2. Administración prolongada de ACTH. -
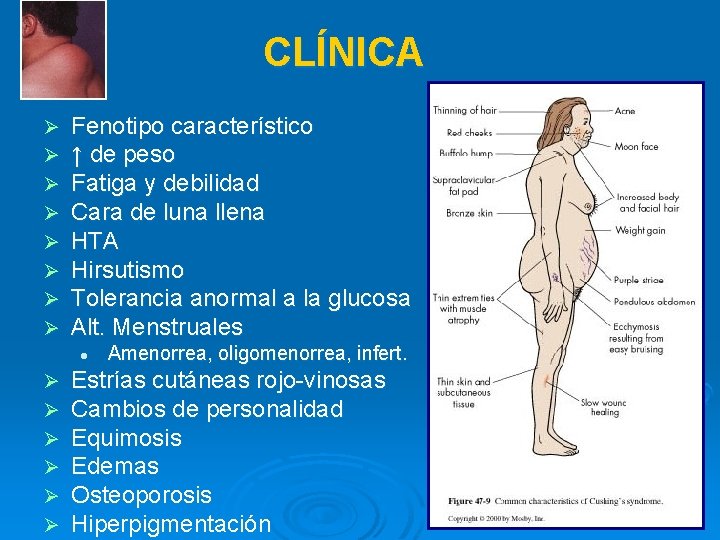
CLÍNICA Ø Ø Ø Ø Fenotipo característico ↑ de peso Fatiga y debilidad Cara de luna llena HTA Hirsutismo Tolerancia anormal a la glucosa Alt. Menstruales l Ø Ø Ø Amenorrea, oligomenorrea, infert. Estrías cutáneas rojo-vinosas Cambios de personalidad Equimosis Edemas Osteoporosis Hiperpigmentación
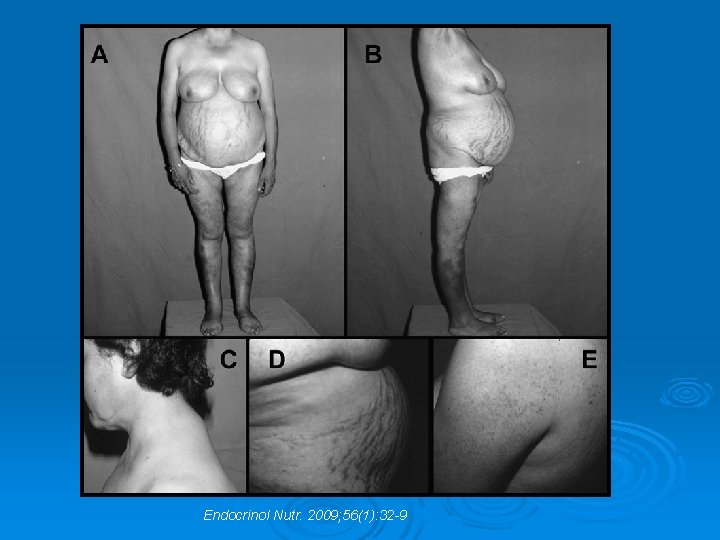
Endocrinol Nutr. 2009; 56(1): 32 -9

LABORATORIO: Ø Intolerancia HC en 50%. DM en 10 -15%. Ø Alcalosis hipopotasémica hipoclorémica en 20% (sdme ACTH ectópico o Ca suprarrenal). Ø Hipercalciuria en 40% Endocrinología, metabolismo y nutrición. Carmena, R. ; Ascaso, J. F. Ed. 2007
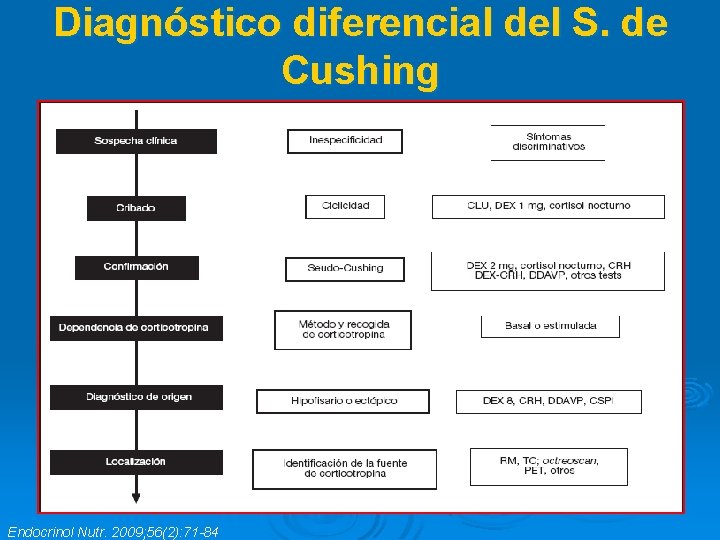
Diagnóstico diferencial del S. de Cushing Endocrinol Nutr. 2009; 56(2): 71 -84

FASES DEL DX DEL S. DE CUSHING 1. CRIBADO 2. CONFIRMACIÓN 3. EVALUACIÓN DE DEPENDENCIA A ACTH. 4. DIAGNÓSTICO DIFERENCIAL DEL SÍNDROME DE CUSHING 5. ESTUDIO MORFOLÓGICO

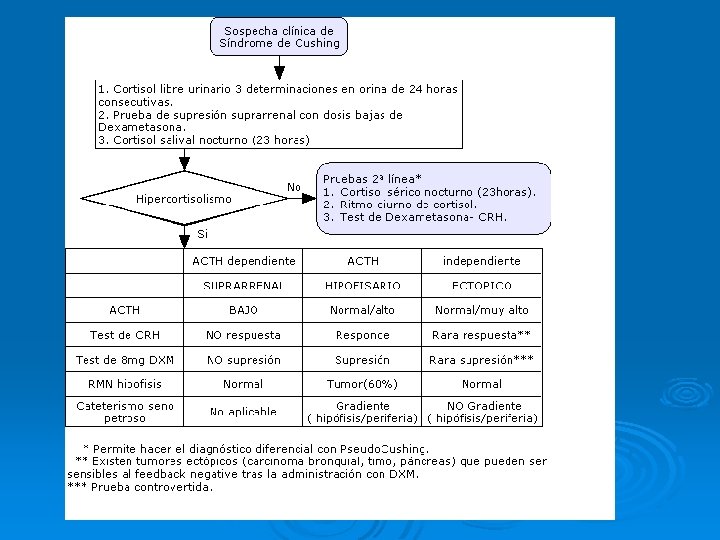
1. CRIBADO Seleccionar casos potenciales: AP, ↑S ↓E. Ø Pac con distribución central de la grasa, DM 2 de mal control, HTA, DL, alt. menstruales o hiperandrogenismo. Descartar adm. exógena de GC. Ø CLU: >100 -150μg/24 h (si >300 μg/24 h o + en 3 muestras = dx definitivo). Ø Test de Nugent: 1 mgr DXM a las 23: 00 h con medición de cortisol a las 8 h (nr<1, 8 ng/ml) o cortisol nocturno salival (70% del CLP). Ø Si alteración pasar a fase de confirmación. Ø

2. CONFIRMACIÓN Ø Repetición de CLU, CNP (entre 23 y 24 h >8 μg/ml), supresión tras 2 mg/día 2 días de DXM. Ø Pseudo-Cushing: si ↑mod de CLU o falta de supresión tras DXM 2 gr/día 2 días + cuadro clínico no suf signif).

3. EVALUACIÓN de ACTH DEPENDENCIA ACTH >20 pg/ml Ø ACTH <10 pg/ml Ø Ø ACTH-dependiente ACTH- independiente Si 10 -20= estimulación con CRH ↑[ACTH] =ACTH-depend. Origen suprarrenal Hipofisario Ectópico

4. Dx DIFERENCIAL DEL SD. DE CUSHING DEPENDIENTE DE ACTH Ø Objetivo: diferencia enf de Cushing de origen hipofisario de origen ectópico. Ø En algunos casos: agresividad, ♂, hipopotasemia, miopatía proximal e hiperpigmentación = origen ectópico. Ø DXM 8 mg: suprime en tumores hipofisarios y no en ectópicos secretores de ACTH. Ø CRH: origen hipofisario si ↑ACTH>50% del valor basal y/o de cortisol >20%.

5. ESTUDIO MORFOLÓGICO Ø Objetivo: confirmar con técnicas de imagen las alteraciones BQ. Ø Si sospecha suprarrenal: TC Ø Si sospecha hipofisaria: RM= adenomas >6 mm. Si no hay imagen o es <6 mm con pruebas q indican origen ectópico= CSPI Ø Si sospecha ectópico: Body-TC (st descartar tumor carcinoide bronquial) Octreo-scan PET
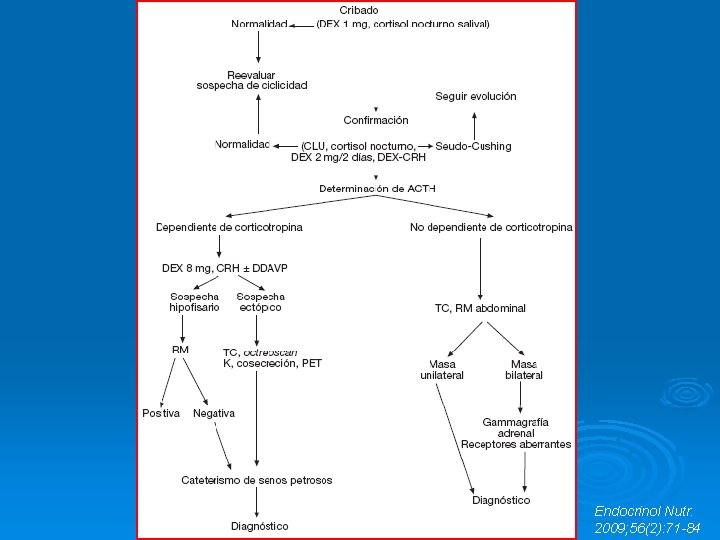
Endocrinol Nutr. 2009; 56(2): 71 -84

TRATAMIENTO TUMOR HIPOFISARIO PRODUCTOR DE ACTH: Ø 1. Cirugía transesfenoidal: de elección. En microadenomas curación del 95%. Ø 2. Suprarrenalectomía médica (fracaso, CI o negación de cirugía y en periodo previo a IQx): l Ketoconazol: 600 -1200 mg/día en 2 -3 dosis.

SÍNDROME DE ACTH ECTÓPICO Ø 1. Extirpación del tumor secretor de ACTH Ø 2. Inhibidores de enzimas adrenales: l Ketoconazol, Mitotano… Ø 3. Análogos de la l somatostatina: Ocreótide Ø 4. Antagonistas de los R de GC

GRACIAS!!!
- Slides: 19