HIDROLISIS GARAM Rudi Purwanto Tabung I Larutan Garam

HIDROLISIS GARAM Rudi Purwanto
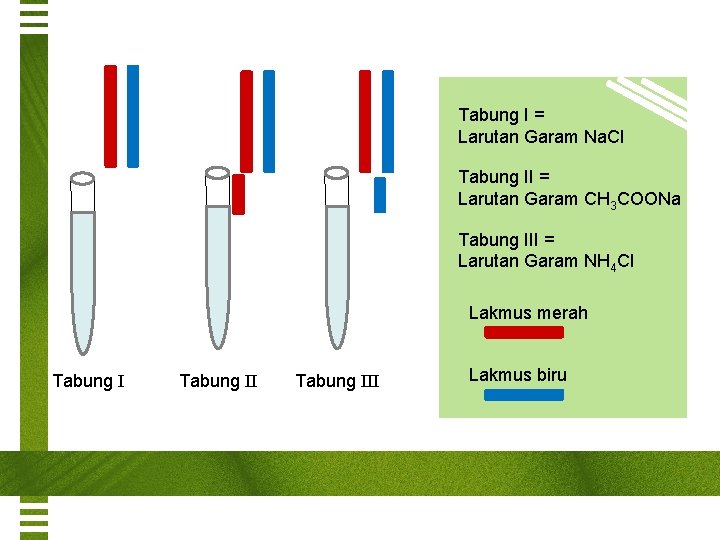
Tabung I = Larutan Garam Na. Cl Tabung II = Larutan Garam CH 3 COONa Tabung III = Larutan Garam NH 4 Cl Lakmus merah Tabung III Lakmus biru

Pengertian • Hidrolisis garam adalah “terurainya garam dalam air yang menghasilkan asam dan atau basa. ” Dapat terjadi ? Komponen penyusunnya : • Asam Lemah • Basa Lemah • Asam Lemah dan Basa Lemah

Jenis-Jenis Hidrolisis Parsial Kation atau Anionnya saja yang terhidrolisis Kation terhidrolisis = bersifat asam (Contoh : NH 4 Cl) Anion terhidrolisis = bersifat basa (Contoh : CH 3 COONa) Hidrolisis Total Kation maupun Anionnya terhidrolisis. Contoh : CH 3 COONH 4, Al 2 S 3

Asam dan Basa • Asam Kuat HCl, HNO 3, H 2 SO 4, HBr, HI, dan HCl. O 4 • Asam Lemah CH 3 COOH, HF, HCN, HNO 2 • Basa Kuat Na. OH, KOH, Ca(OH)2 dan Ba(OH)2 • Basa Lemah NH 3, CH 3 NH 2, C 5 H 5 N, NH 4 OH

Jenis-Jenis Garam 1 Garam dari asam kuat dan basa kuat Asam kuat + Basa kuat = Garam Sifat garamnya : • Tidak dapat dihidrolisis Karena kation dan anionya tidak bisa bereaksi dengan air (H 2 O) • Netral atau p. H=7 Contoh garam : K 2 SO 4 , KCl, Na. Cl

Jenis-Jenis Garam 2 Garam dari Asam Kuat dan Basa Lemah Asam kuat + Basa lemah = Garam Sifat garamnya : • Dapat dihidrolisis namun sebagian Karena kationya bisa bereaksi dengan air (H 2 O) • Bersifat Asam atau p. H<7 Contoh garam : NH 4 Cl dan (NH 4)2 SO 4

Penentuan p. H garam

Penentuan p. H garam Contoh Soal Hitunglah p. H dari larutan NH 4 Cl 0. 1 M dengan Kh = 10 -9! Jadi NH 4 Cl 0. 1 M memiliki p. H = 5

Jenis-Jenis Garam 3 Garam dari Basa Kuat dan Asam Lemah Basa kuat + Asam lemah = Garam Sifat garamnya : • Dapat dihidrolisis namun sebagian Karena anionnya bisa bereaksi dengan air (H 2 O) • Bersifat Basa atau p. H>7 Contoh garam : Ca(CH 3 COO) 2 dan Ba 3(PO 4)2

Penentuan p. H garam

Penentuan p. H garam Contoh Soal Jika diketahui Ka dari CH 3 COOH adalah 10 -5, maka hitunglah p. H dari larutan CH 3 COONa 0. 1 M!. . . Jadi CH 3 COONa 0. 1 M memiliki p. H = 5

Jenis-Jenis Garam 4 Garam dari Asam Lemah dan Basa Lemah Asam Lemah + Basa lemah = Garam Sifat garamnya : • Dapat terhidrolisis secara sempurna • Jika, Ka < Kb maka bersifat Basa Ka > Kb maka bersifat Asam Ka = Kb maka bersifat Netral Contoh garam : NH 4 CH 3 COO dan NH 4 F

Penentuan p. H garam

Penentuan p. H garam Contoh Soal • Hitunglah p. H larutan CH 3 COONH 4 0, 1 M, jika diketahui Ka = 10– 10 dan Kb NH 3 = 10– 5! Jadi CH 3 COONH 4 0, 1 M memiliki p. H = 10

Kesimpulan • Sifat larutan garam bergantung pada kekuatan relatif asam dan basa penyusunnya • Hidrolisis garam adalah reaksi antara komponen garam yang berasal dari asam atau basa lemah dengan air • Garam dari asam dan basa kuat tidak mengalami hidrolisis, larutannya bersifat netral

Kesimpulan • Garam dari asam lemah dan basa kuat mengalami hidrolisis anion, larutannya bersifat basa. • Garam dari asam kuat dan basa lemah mengalami hidrolisis kation, larutannya bersifat asam. • Garam dari asam dan basa lemah mangalami hidrolisis total, sifat larutannya bergantung pada harga Ka dan Kb penyusunnya

- Slides: 18