Hibridizacija s elektroni H 2 O O 1
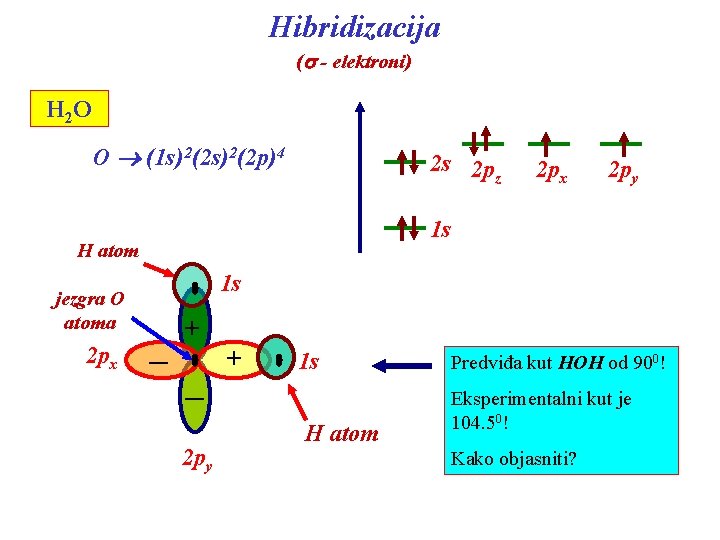
Hibridizacija (s - elektroni) H 2 O O (1 s)2(2 p)4 2 s 2 pz 2 px 2 py 1 s H atom jezgra O atoma 2 px 1 s _ + _ 2 py + 1 s H atom Predviđa kut HOH od 900! Eksperimentalni kut je 104. 50! Kako objasniti?
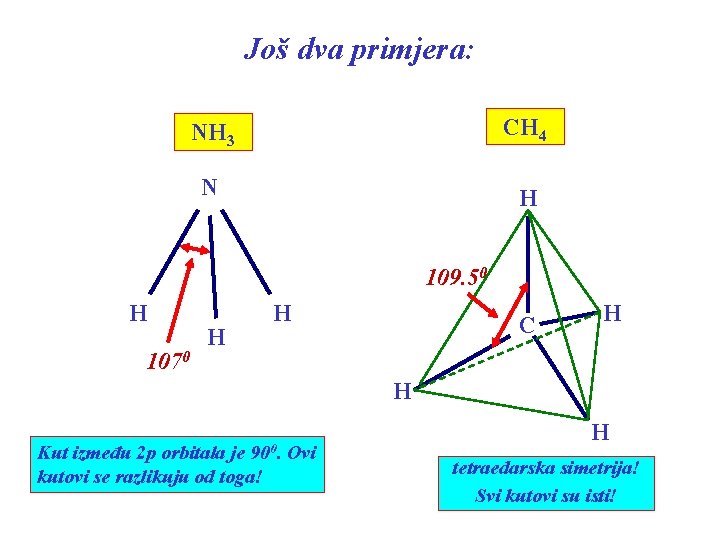
Još dva primjera: NH 3 CH 4 N H 109. 50 H 1070 H H C H H 900. Kut između 2 p orbitala je kutovi se razlikuju od toga! Ovi H tetraedarska simetrija! Svi kutovi su isti!
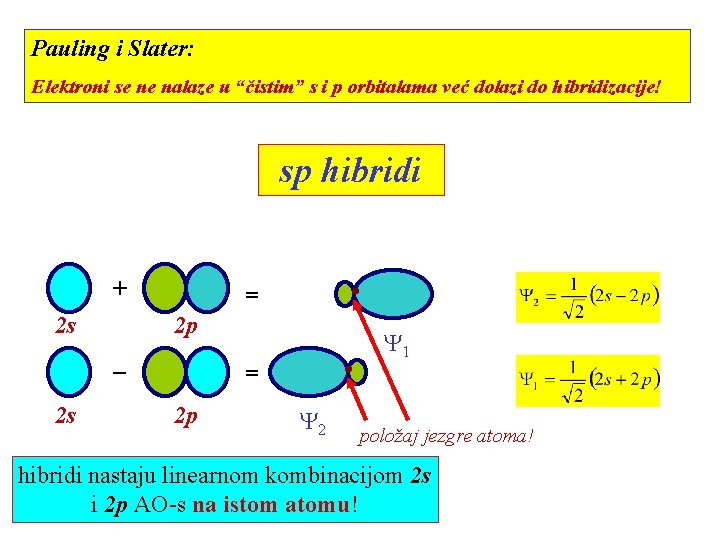
Pauling i Slater: Elektroni se ne nalaze u “čistim” s i p orbitalama već dolazi do hibridizacije! sp hibridi + 2 s = 2 p _ 2 s Y 1 = 2 p Y 2 položaj jezgre atoma! hibridi nastaju linearnom kombinacijom 2 s i 2 p AO-s na istom atomu!
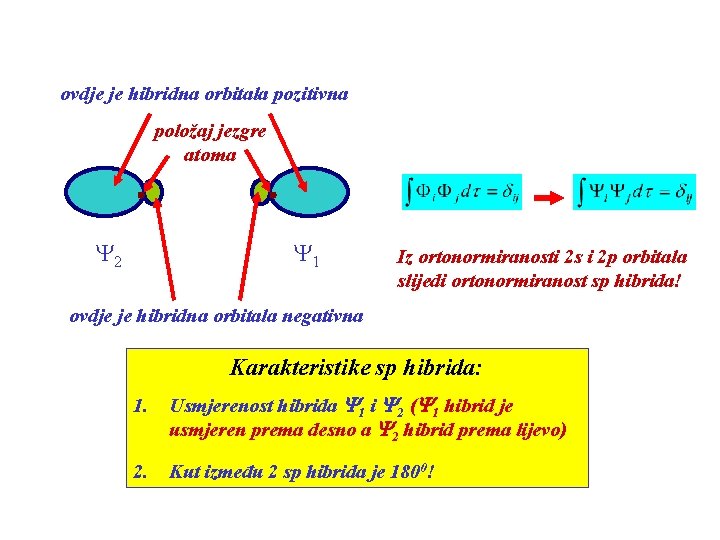
ovdje je hibridna orbitala pozitivna položaj jezgre atoma Y 2 Y 1 Iz ortonormiranosti 2 s i 2 p orbitala slijedi ortonormiranost sp hibrida! ovdje je hibridna orbitala negativna Karakteristike sp hibrida: 1. Usmjerenost hibrida Y 1 i Y 2 (Y 1 hibrid je usmjeren prema desno a Y 2 hibrid prema lijevo) 2. Kut između 2 sp hibrida je 1800!

Zašto dolazi do hibridizacije? • 2 p orbitala ima nešto višu energiju od 2 s orbitale. Stoga je potrebno potrošiti nešto energije da se elektron iz 2 s orbitale “promovira” u sp hibrid! To je negativan doprinos! • sp hibrid je puno više usmjeren od 2 s i od 2 p orbitale. Stoga, ako se u smjeru usmjerenja sp hibrida nalazi orbitala nekog drugog atoma, dolazi do puno jače kemijske veze nego li u slučaju 2 s ili 2 p orbitale. To je pozitivan doprinos! U konačnom balansu pozitivan doprinos je puno jači od negativnog i stoga je energetski povoljno formiranje hibrida! Glavni razlog nastajanja hibrida je mala razlika u energiji 2 s i 2 p orbitale. Da je ta razlika puno veća, do hibridizacije ne bi dolazilo!
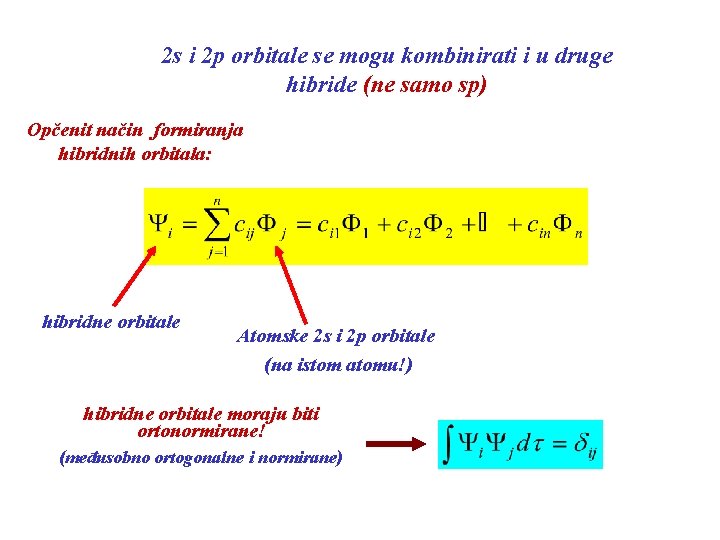
2 s i 2 p orbitale se mogu kombinirati i u druge hibride (ne samo sp) Opčenit način formiranja hibridnih orbitala: hibridne orbitale Atomske 2 s i 2 p orbitale (na istom atomu!) hibridne orbitale moraju biti ortonormirane! (međusobno ortogonalne i normirane)
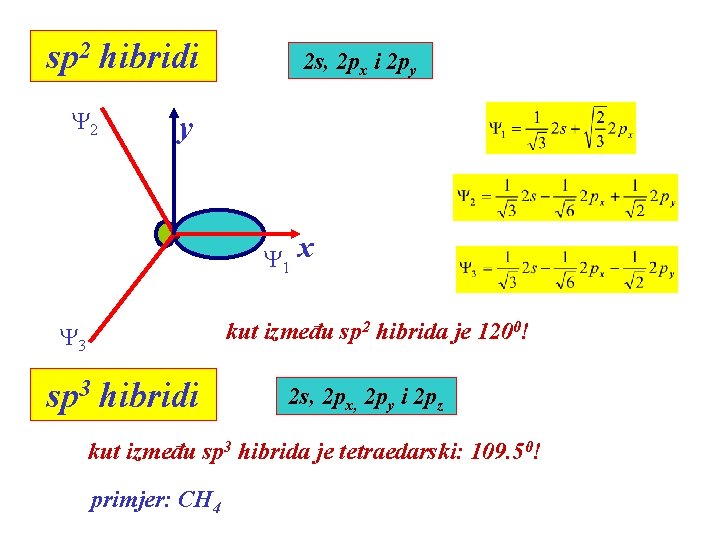
sp 2 hibridi Y 2 2 s, 2 px i 2 py y Y 1 x kut između sp 2 hibrida je 1200! Y 3 sp 3 hibridi 2 s, 2 px, 2 py i 2 pz kut između sp 3 hibrida je tetraedarski: 109. 50! primjer: CH 4
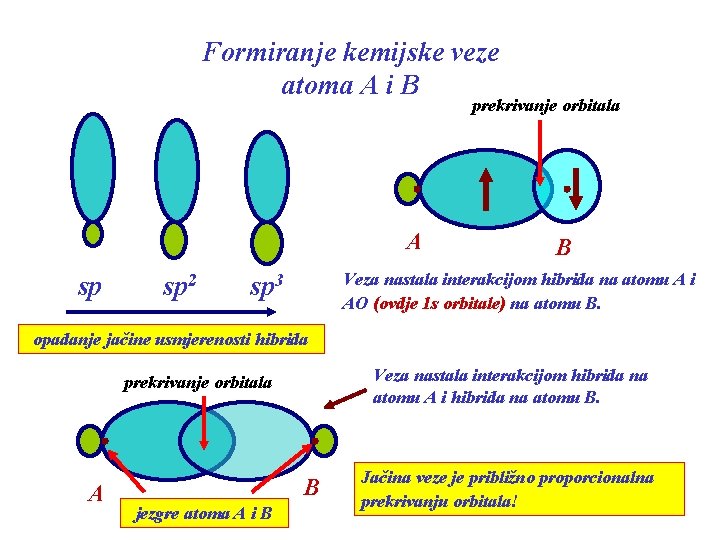
Formiranje kemijske veze atoma A i B prekrivanje orbitala A sp sp 2 B Veza nastala interakcijom hibrida na atomu A i AO (ovdje 1 s orbitale) na atomu B. sp 3 opadanje jačine usmjerenosti hibrida Veza nastala interakcijom hibrida na atomu A i hibrida na atomu B. prekrivanje orbitala A B jezgre atoma A i B Jačina veze je približno proporcionalna prekrivanju orbitala!
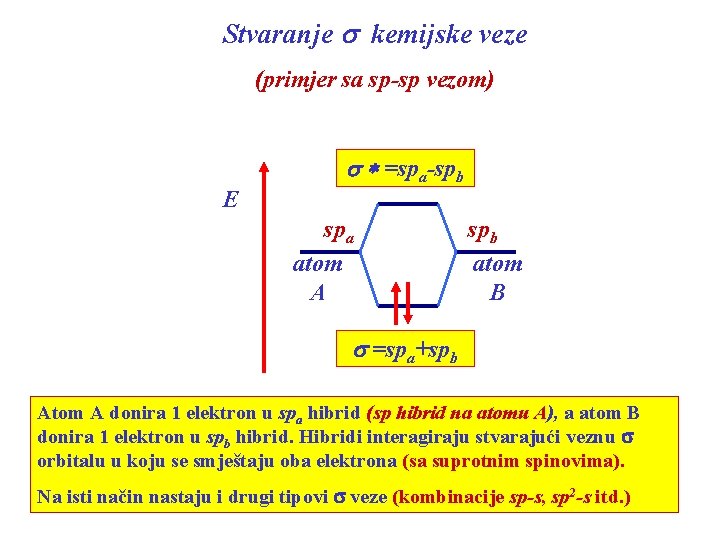
Stvaranje s kemijske veze (primjer sa sp-sp vezom) E s * =spa-spb spa atom A spb atom B s =spa+spb Atom A donira 1 elektron u spa hibrid (sp hibrid na atomu A), a atom B donira 1 elektron u spb hibrid. Hibridi interagiraju stvarajući veznu s orbitalu u koju se smještaju oba elektrona (sa suprotnim spinovima). Na isti način nastaju i drugi tipovi s veze (kombinacije sp-s, sp 2 -s itd. )
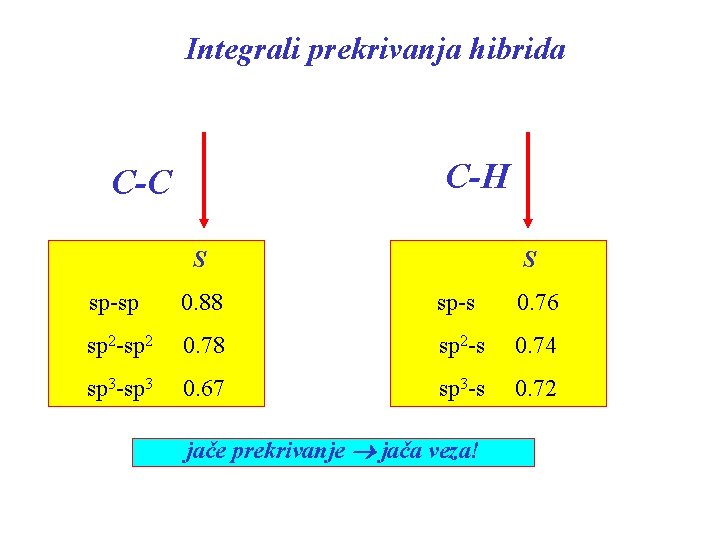
Integrali prekrivanja hibrida C-H C-C S S sp-sp 0. 88 sp-s 0. 76 sp 2 -sp 2 0. 78 sp 2 -s 0. 74 sp 3 -sp 3 0. 67 sp 3 -s 0. 72 jače prekrivanje jača veza!
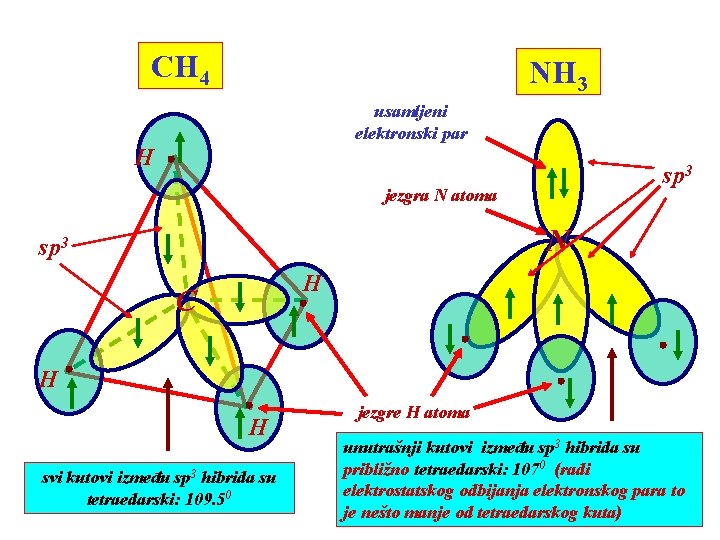
CH 4 NH 3 usamljeni elektronski par H sp 3 jezgra N atoma N sp 3 H C H H svi kutovi između sp 3 hibrida su tetraedarski: 109. 50 jezgre H atoma unutrašnji kutovi između sp 3 hibrida su približno tetraedarski: 1070 (radi elektrostatskog odbijanja elektronskog para to je nešto manje od tetraedarskog kuta)
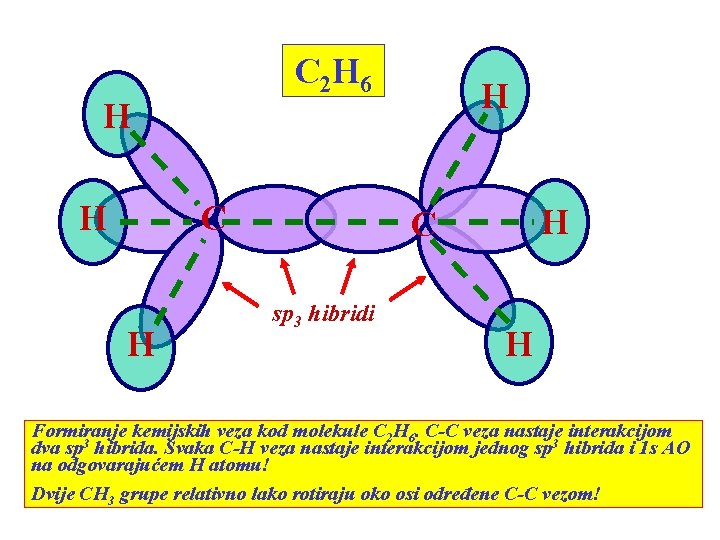
C 2 H 6 H H C H H H C sp 3 hibridi H Formiranje kemijskih veza kod molekule C 2 H 6. C-C veza nastaje interakcijom dva sp 3 hibrida. Svaka C-H veza nastaje interakcijom jednog sp 3 hibrida i 1 s AO na odgovarajućem H atomu! Dvije CH 3 grupe relativno lako rotiraju oko osi određene C-C vezom!
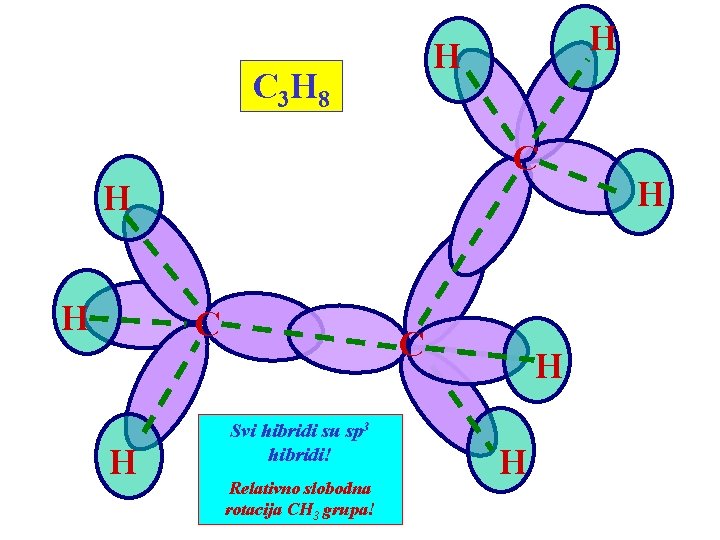
H C 3 H 8 C H H C Svi hibridi su sp 3 hibridi! Relativno slobodna rotacija CH 3 grupa! H H H
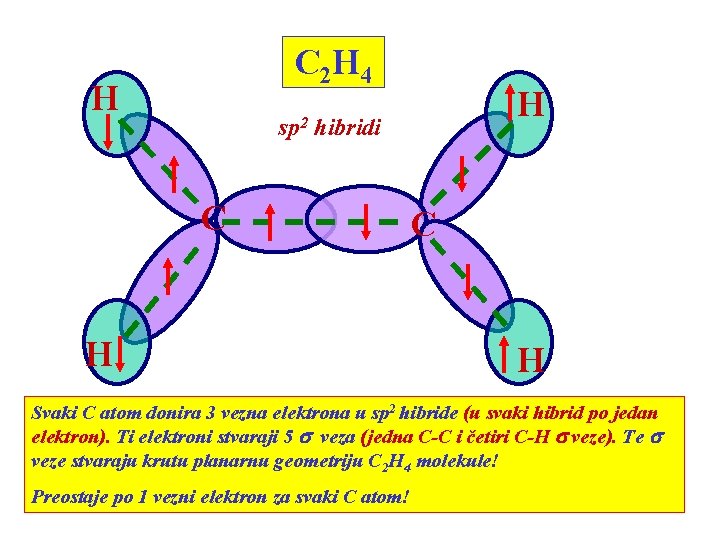
C 2 H 4 H sp 2 H hibridi C H Svaki C atom donira 3 vezna elektrona u sp 2 hibride (u svaki hibrid po jedan elektron). Ti elektroni stvaraji 5 s veza (jedna C-C i četiri C-H s veze). Te s veze stvaraju krutu planarnu geometriju C 2 H 4 molekule! Preostaje po 1 vezni elektron za svaki C atom!
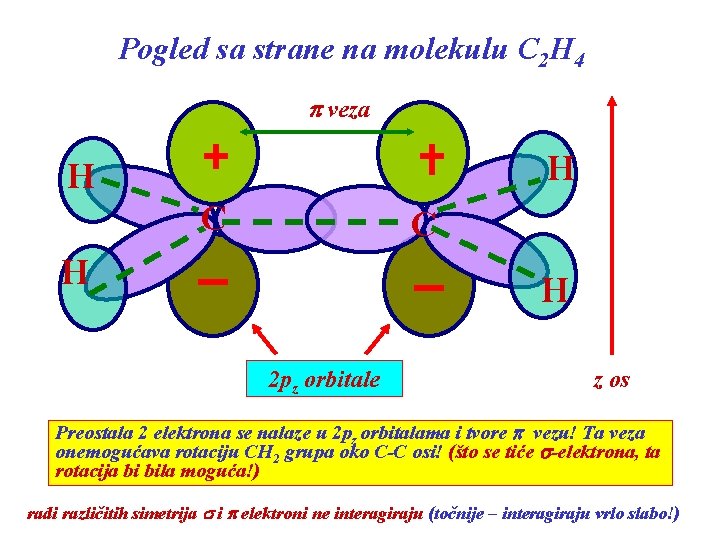
Pogled sa strane na molekulu C 2 H 4 p veza H H C C H H 2 pz orbitale z os Preostala 2 elektrona se nalaze u 2 pz orbitalama i tvore p vezu! Ta veza onemogućava rotaciju CH 2 grupa oko C-C osi! (što se tiće s-elektrona, ta rotacija bi bila moguća!) radi različitih simetrija s i p elektroni ne interagiraju (točnije – interagiraju vrlo slabo!)
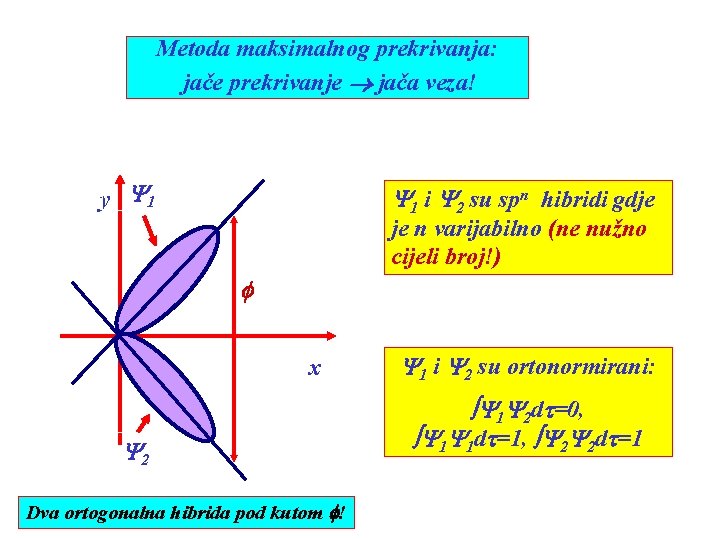
Metoda maksimalnog prekrivanja: jače prekrivanje jača veza! y Y 1 i Y 2 su spn hibridi gdje je n varijabilno (ne nužno cijeli broj!) f x Y 2 Dva ortogonalna hibrida pod kutom f! Y 1 i Y 2 su ortonormirani: Y 1 Y 2 dt=0, Y 1 Y 1 dt=1, Y 2 Y 2 dt=1
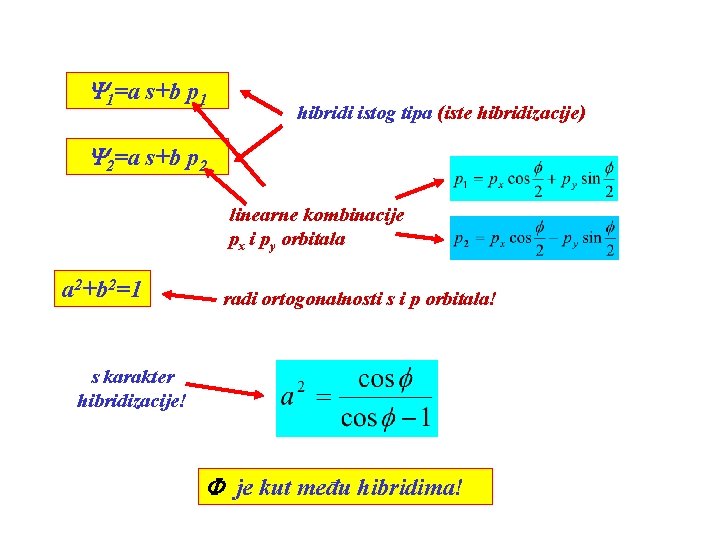
Y 1=a s+b p 1 hibridi istog tipa (iste hibridizacije) Y 2=a s+b p 2 linearne kombinacije px i py orbitala a 2+b 2=1 radi ortogonalnosti s i p orbitala! s karakter hibridizacije! F je kut među hibridima!
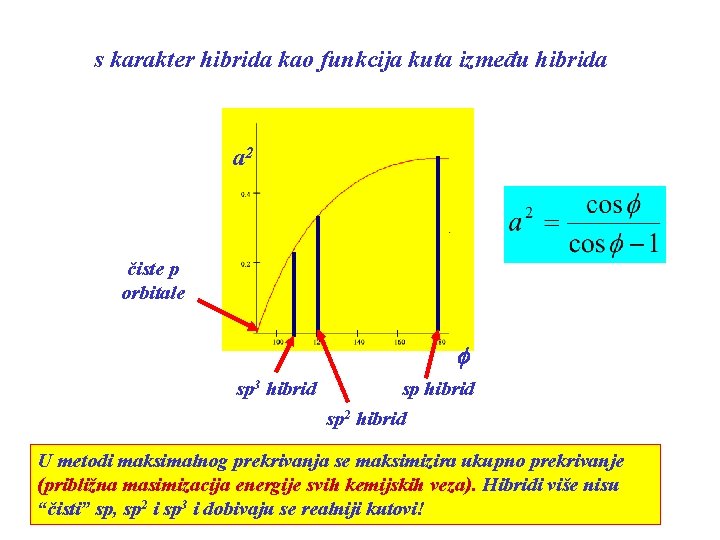
s karakter hibrida kao funkcija kuta između hibrida a 2 čiste p orbitale f sp 3 hibrid sp 2 hibrid U metodi maksimalnog prekrivanja se maksimizira ukupno prekrivanje (približna masimizacija energije svih kemijskih veza). Hibridi više nisu “čisti” sp, sp 2 i sp 3 i dobivaju se realniji kutovi!

Pitanja hibridizacija • Zašto je potrebna hibridizacija? Kako objašnjavamo kutove kod molekule vode, molekule amonijaka itd. ? • Objasnite pomoću hibridizacije geometriju CH 4 (NH 3) molekule! • Kako nastaje hibridizacija? Čime je ona omogučena? • Objasnite geometriju C 2 H 6 (C 3 H 8) molekule! • Objasnite svojstva sp (sp 2, sp 3) hibrida! • Što je to metoda maksimalnog prekrivanja? • Kako ovisi s karakter dva istovjetna hibrida o kutu između njih? • Kako ovisi jačina usmjerenosti hibrida o vrsti hibrida? • Objasnite geometriju C 2 H 4 molekule! • Zašto CH 3 grupe kod molekule C 2 H 6 relativno slobodno rotiraju oko C-C veze, a CH 2 grupe kod molekule C 2 H 4 ne rotiraju oko C-C veze? • Koja su svojstva hibridnih orbitala?
- Slides: 19