Herzinsuffizienz und Typ 2 Diabetes AT3449 052020 Diagnostik
Herzinsuffizienz und Typ 2 Diabetes AT-3449 05/2020

Diagnostik der Herzinsuffizienz
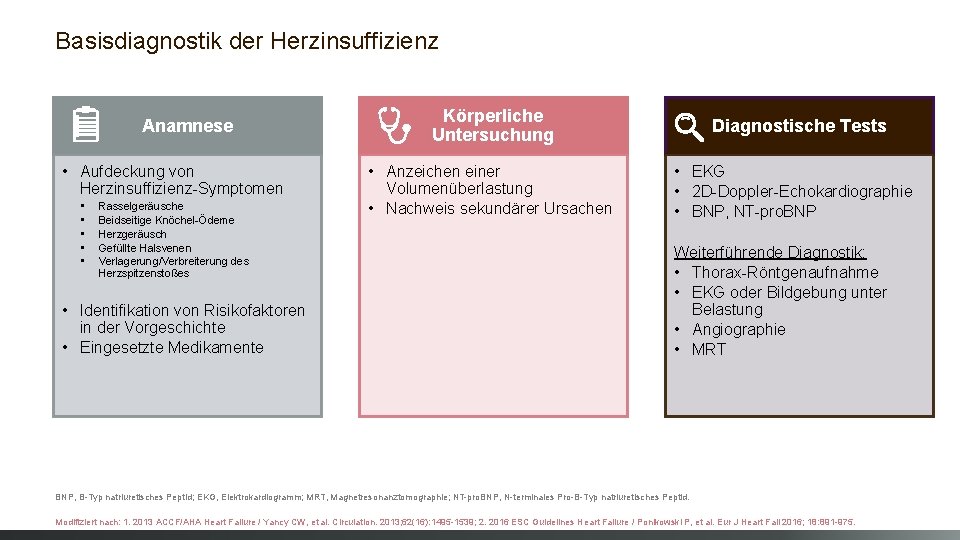
Basisdiagnostik der Herzinsuffizienz Anamnese • Aufdeckung von Herzinsuffizienz-Symptomen • • • Rasselgeräusche Beidseitige Knöchel-Ödeme Herzgeräusch Gefüllte Halsvenen Verlagerung/Verbreiterung des Herzspitzenstoßes • Identifikation von Risikofaktoren in der Vorgeschichte • Eingesetzte Medikamente Körperliche Untersuchung • Anzeichen einer Volumenüberlastung • Nachweis sekundärer Ursachen Diagnostische Tests • EKG • 2 D-Doppler-Echokardiographie • BNP, NT-pro. BNP Weiterführende Diagnostik: • Thorax-Röntgenaufnahme • EKG oder Bildgebung unter Belastung • Angiographie • MRT BNP, B-Typ natriuretisches Peptid; EKG, Elektrokardiogramm; MRT, Magnetresonanztomographie; NT-pro. BNP, N-terminales Pro-B-Typ natriuretisches Peptid. Modifiziert nach: 1. 2013 ACCF/AHA Heart Failure / Yancy CW, et al. Circulation. 2013; 62(16): 1495 -1539; 2. 2016 ESC Guidelines Heart Failure / Ponikowski P, et al. Eur J Heart Fail 2016; 18: 891 -975.
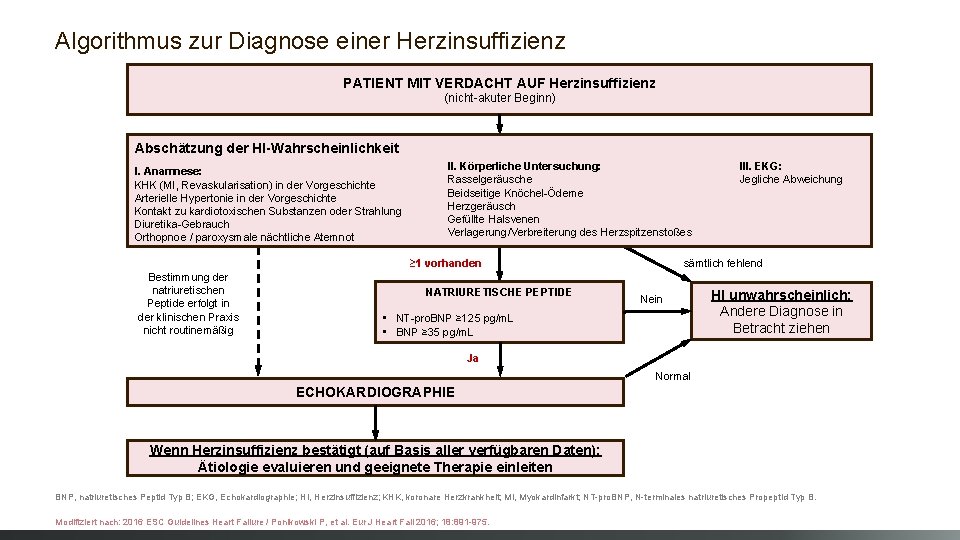
Algorithmus zur Diagnose einer Herzinsuffizienz PATIENT MIT VERDACHT AUF Herzinsuffizienz (nicht-akuter Beginn) Abschätzung der HI-Wahrscheinlichkeit I. Anamnese: KHK (MI, Revaskularisation) in der Vorgeschichte Arterielle Hypertonie in der Vorgeschichte Kontakt zu kardiotoxischen Substanzen oder Strahlung Diuretika-Gebrauch Orthopnoe / paroxysmale nächtliche Atemnot II. Körperliche Untersuchung: Rasselgeräusche Beidseitige Knöchel-Ödeme Herzgeräusch Gefüllte Halsvenen Verlagerung/Verbreiterung des Herzspitzenstoßes sämtlich fehlend ≥ 1 vorhanden Bestimmung der natriuretischen Peptide erfolgt in der klinischen Praxis nicht routinemäßig NATRIURETISCHE PEPTIDE III. EKG: Jegliche Abweichung Nein • NT-pro. BNP ≥ 125 pg/m. L • BNP ≥ 35 pg/m. L HI unwahrscheinlich: Andere Diagnose in Betracht ziehen Ja Normal ECHOKARDIOGRAPHIE Wenn Herzinsuffizienz bestätigt (auf Basis aller verfügbaren Daten): Ätiologie evaluieren und geeignete Therapie einleiten BNP, natriuretisches Peptid Typ B; EKG, Echokardiographie; HI, Herzinsuffizienz; KHK, koronare Herzkrankheit; MI, Myokardinfarkt; NT-pro. BNP, N-terminales natriuretisches Propeptid Typ B. Modifiziert nach: 2016 ESC Guidelines Heart Failure / Ponikowski P, et al. Eur J Heart Fail 2016; 18: 891 -975.
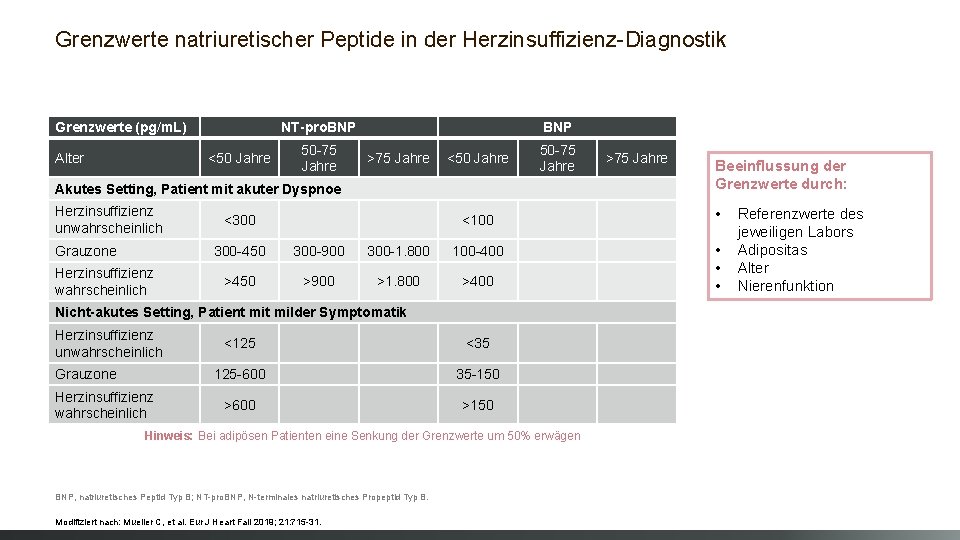
Grenzwerte natriuretischer Peptide in der Herzinsuffizienz-Diagnostik Grenzwerte (pg/m. L) Alter NT-pro. BNP <50 Jahre 50 -75 Jahre BNP >75 Jahre <50 Jahre 50 -75 Jahre Akutes Setting, Patient mit akuter Dyspnoe Herzinsuffizienz unwahrscheinlich Grauzone Herzinsuffizienz wahrscheinlich <300 <100 300 -450 300 -900 300 -1. 800 100 -400 >450 >900 >1. 800 >400 Nicht-akutes Setting, Patient milder Symptomatik Herzinsuffizienz unwahrscheinlich Grauzone Herzinsuffizienz wahrscheinlich <125 <35 125 -600 35 -150 >600 >150 Hinweis: Bei adipösen Patienten eine Senkung der Grenzwerte um 50% erwägen BNP, natriuretisches Peptid Typ B; NT-pro. BNP, N-terminales natriuretisches Propeptid Typ B. Modifiziert nach: Mueller C, et al. Eur J Heart Fail 2019; 21: 715 -31. >75 Jahre Beeinflussung der Grenzwerte durch: • • Referenzwerte des jeweiligen Labors Adipositas Alter Nierenfunktion

Herzinsuffizienz und Diabetes
Risikofaktoren für Herzinsuffizienz bei Diabetes mellitus Chronische Niereninsuffizienz (CKD) Koronare Herzkrankheit Herzinsuffizienz bei Patienten mit Diabetes Direkte myokardiale Effekte von Insulinresistenz/ Hyperglykämie Modifiziert nach: 2019 ESC/EASD Guidelines Diabetes, Pre-diabetes, Cardiovascular Diseases / Cosentino F, et al. Eur Heart J 2020; 41: 255 -323. Hypertonie
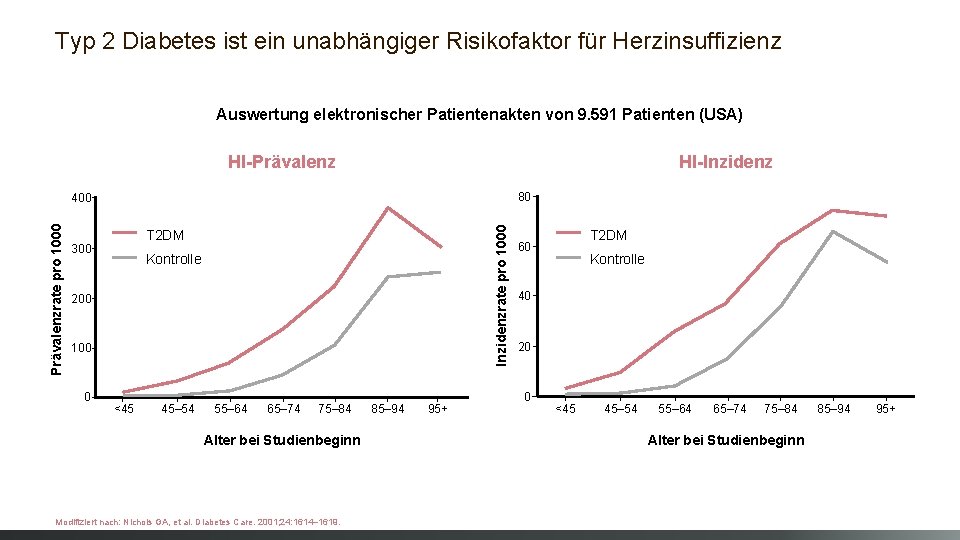
Typ 2 Diabetes ist ein unabhängiger Risikofaktor für Herzinsuffizienz Auswertung elektronischer Patientenakten von 9. 591 Patienten (USA) HI-Prävalenz HI-Inzidenz 80 Inzidenzrate pro 1000 Prävalenzrate pro 1000 400 T 2 DM 300 Kontrolle 200 100 0 <45 45– 54 55– 64 65– 74 75– 84 Alter bei Studienbeginn Modifiziert nach: Nichols GA, et al. Diabetes Care. 2001; 24: 1614– 1619. 85– 94 95+ T 2 DM 60 Kontrolle 40 20 0 <45 45– 54 55– 64 65– 74 75– 84 Alter bei Studienbeginn 85– 94 95+
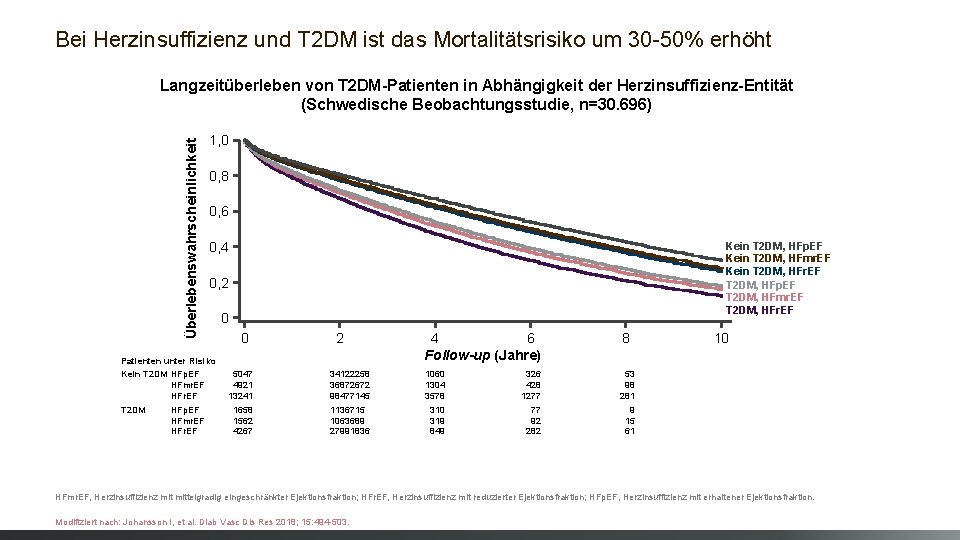
Bei Herzinsuffizienz und T 2 DM ist das Mortalitätsrisiko um 30 -50% erhöht Überlebenswahrscheinlichkeit Langzeitüberleben von T 2 DM-Patienten in Abhängigkeit der Herzinsuffizienz-Entität (Schwedische Beobachtungsstudie, n=30. 696) 1, 0 0, 8 0, 6 0, 4 Kein T 2 DM, HFp. EF Kein T 2 DM, HFmr. EF Kein T 2 DM, HFr. EF T 2 DM, HFp. EF T 2 DM, HFmr. EF T 2 DM, HFr. EF 0, 2 0 0 2 Patienten unter Risiko Kein T 2 DM HFp. EF HFmr. EF HFr. EF 4 6 Follow-up (Jahre) 8 5047 4921 13241 34122258 36872672 98477145 1060 1304 3578 326 428 1277 53 98 281 1658 1562 4267 1136715 1063689 27991836 310 319 849 77 92 282 9 15 61 10 HFmr. EF, Herzinsuffizienz mittelgradig eingeschränkter Ejektionsfraktion; HFr. EF, Herzinsuffizienz mit reduzierter Ejektionsfraktion; HFp. EF, Herzinsuffizienz mit erhaltener Ejektionsfraktion. Modifiziert nach: Johansson I, et al. Diab Vasc Dis Res 2018; 15: 494 -503.
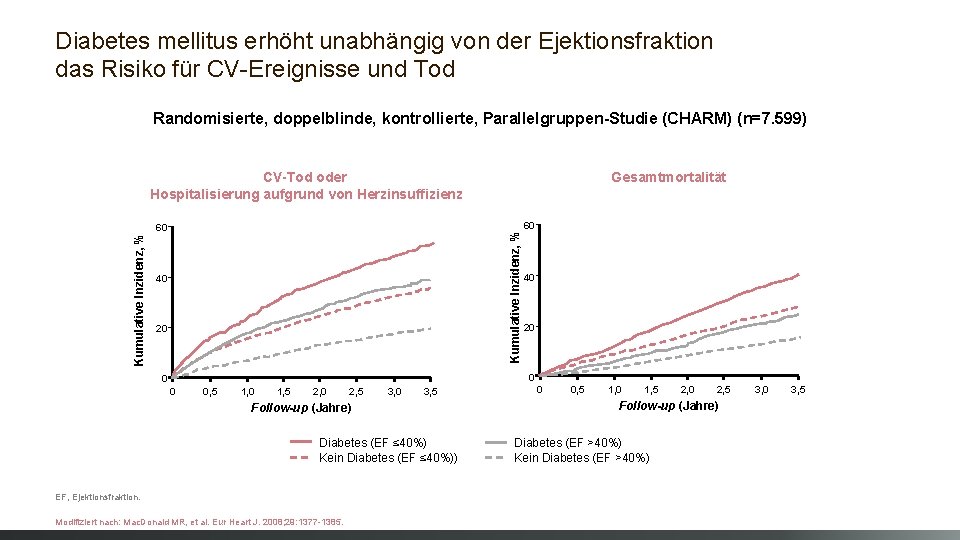
Diabetes mellitus erhöht unabhängig von der Ejektionsfraktion das Risiko für CV-Ereignisse und Tod Randomisierte, doppelblinde, kontrollierte, Parallelgruppen-Studie (CHARM) (n=7. 599) CV-Tod oder Hospitalisierung aufgrund von Herzinsuffizienz Kumulative Inzidenz, % 60 Gesamtmortalität 40 20 60 40 20 0 0, 5 1, 0 1, 5 2, 0 2, 5 3, 0 3, 5 Follow-up (Jahre) Diabetes (EF ≤ 40%) Kein Diabetes (EF ≤ 40%)) EF, Ejektionsfraktion. Modifiziert nach: Mac. Donald MR, et al. Eur Heart J. 2008; 29: 1377 -1385. 0 0, 5 1, 0 1, 5 2, 0 2, 5 Follow-up (Jahre) Diabetes (EF >40%) Kein Diabetes (EF >40%) 3, 0 3, 5
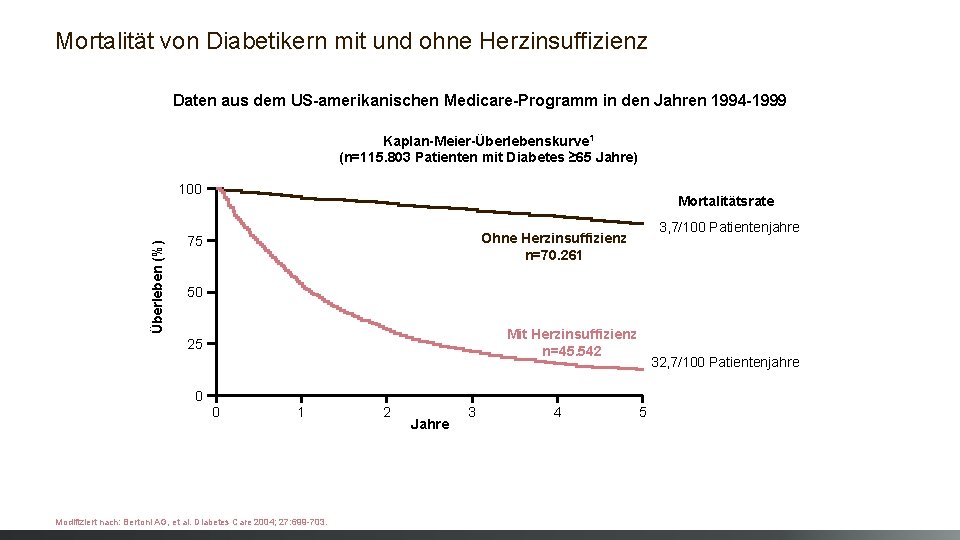
Mortalität von Diabetikern mit und ohne Herzinsuffizienz Daten aus dem US-amerikanischen Medicare-Programm in den Jahren 1994 -1999 Kaplan-Meier-Überlebenskurve 1 (n=115. 803 Patienten mit Diabetes ≥ 65 Jahre) Überleben (%) 100 Mortalitätsrate 3, 7/100 Patientenjahre Ohne Herzinsuffizienz n=70. 261 75 50 Mit Herzinsuffizienz n=45. 542 25 32, 7/100 Patientenjahre 0 0 1 Modifiziert nach: Bertoni AG, et al. Diabetes Care 2004; 27: 699 -703. 2 Jahre 3 4 5
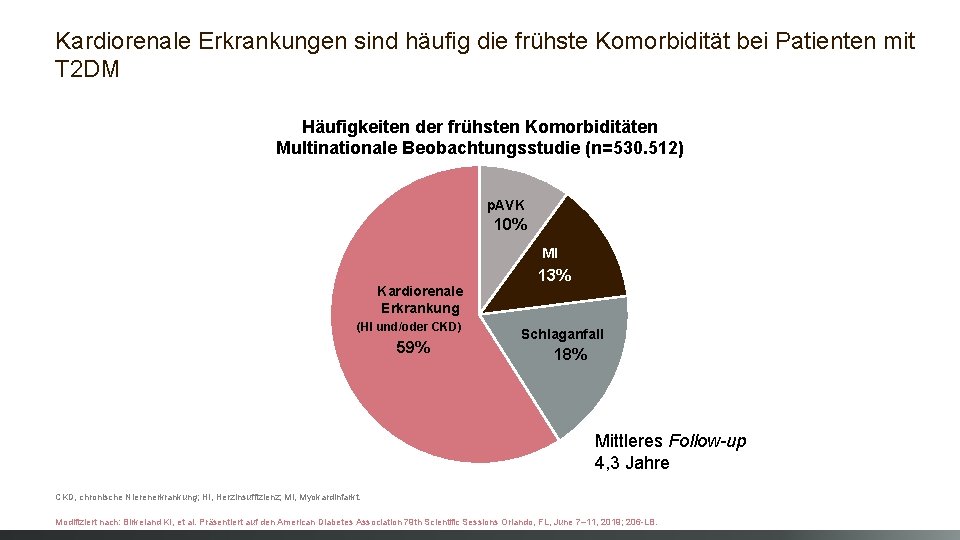
Kardiorenale Erkrankungen sind häufig die frühste Komorbidität bei Patienten mit T 2 DM Häufigkeiten der frühsten Komorbiditäten Multinationale Beobachtungsstudie (n=530. 512) p. AVK 10% MI Kardiorenale Erkrankung (HI und/oder CKD) 59% 13% Schlaganfall 18% Mittleres Follow-up 4, 3 Jahre CKD, chronische Nierenerkrankung; HI, Herzinsuffizienz; MI, Myokardinfarkt. Modifiziert nach: Birkeland KI, et al. Präsentiert auf den American Diabetes Association 79 th Scientific Sessions Orlando, FL, June 7– 11, 2019; 206 -LB.
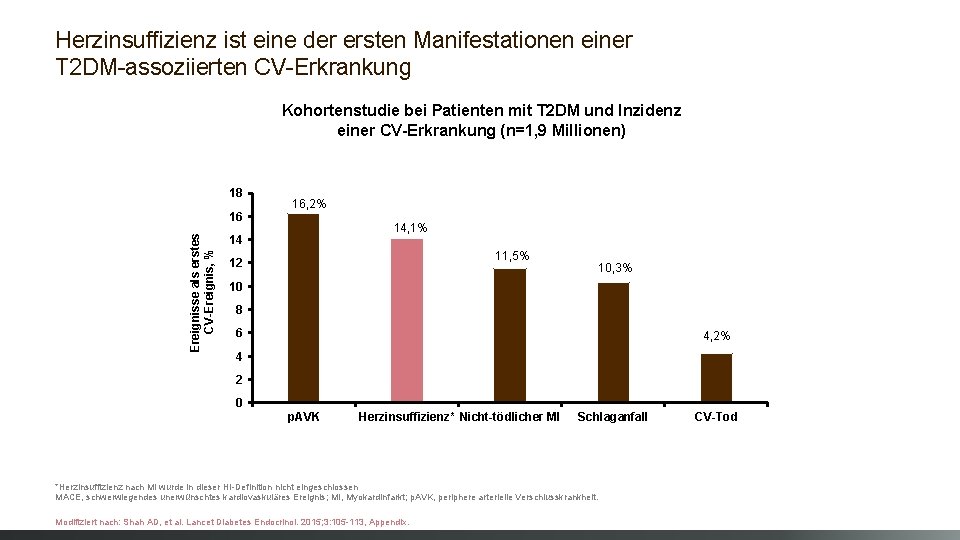
Herzinsuffizienz ist eine der ersten Manifestationen einer T 2 DM-assoziierten CV-Erkrankung Kohortenstudie bei Patienten mit T 2 DM und Inzidenz einer CV-Erkrankung (n=1, 9 Millionen) 18 Ereignisse als erstes CV-Ereignis, % 16 16, 2% 14, 1% 14 11, 5% 12 10, 3% 10 8 6 4, 2% 4 2 0 p. AVK Herzinsuffizienz* Nicht-tödlicher MI Schlaganfall *Herzinsuffizienz nach MI wurde in dieser HI-Definition nicht eingeschlossen MACE, schwerwiegendes unerwünschtes kardiovaskuläres Ereignis; MI, Myokardinfarkt; p. AVK, periphere arterielle Verschlusskrankheit. Modifiziert nach: Shah AD, et al. Lancet Diabetes Endocrinol. 2015; 3: 105 -113, Appendix. CV-Tod
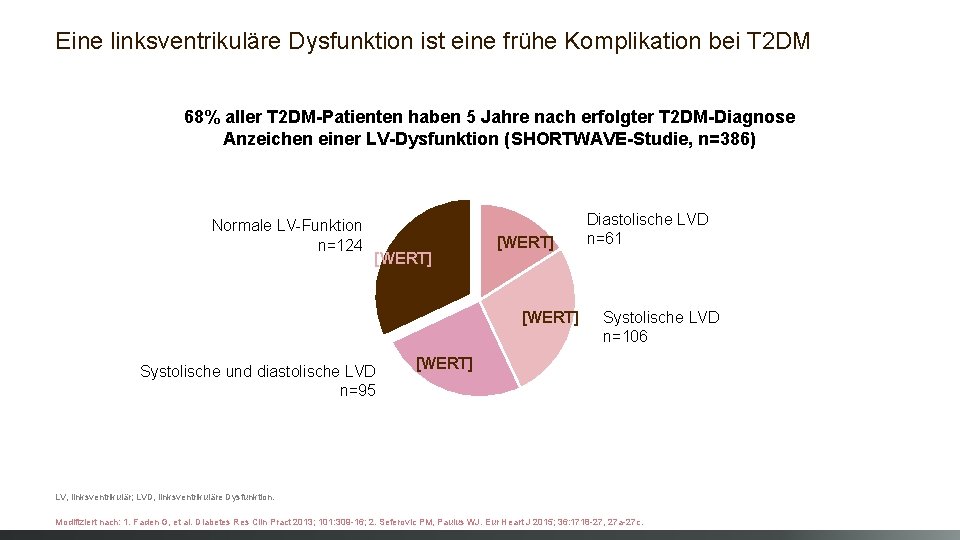
Eine linksventrikuläre Dysfunktion ist eine frühe Komplikation bei T 2 DM 68% aller T 2 DM-Patienten haben 5 Jahre nach erfolgter T 2 DM-Diagnose Anzeichen einer LV-Dysfunktion (SHORTWAVE-Studie, n=386) Normale LV-Funktion n=124 [WERT] Systolische und diastolische LVD n=95 Diastolische LVD n=61 Systolische LVD n=106 [WERT] LV, linksventrikulär; LVD, linksventrikuläre Dysfunktion. Modifiziert nach: 1. Faden G, et al. Diabetes Res Clin Pract 2013; 101: 309 -16; 2. Seferovic PM, Paulus WJ. Eur Heart J 2015; 36: 1718 -27, 27 a-27 c.
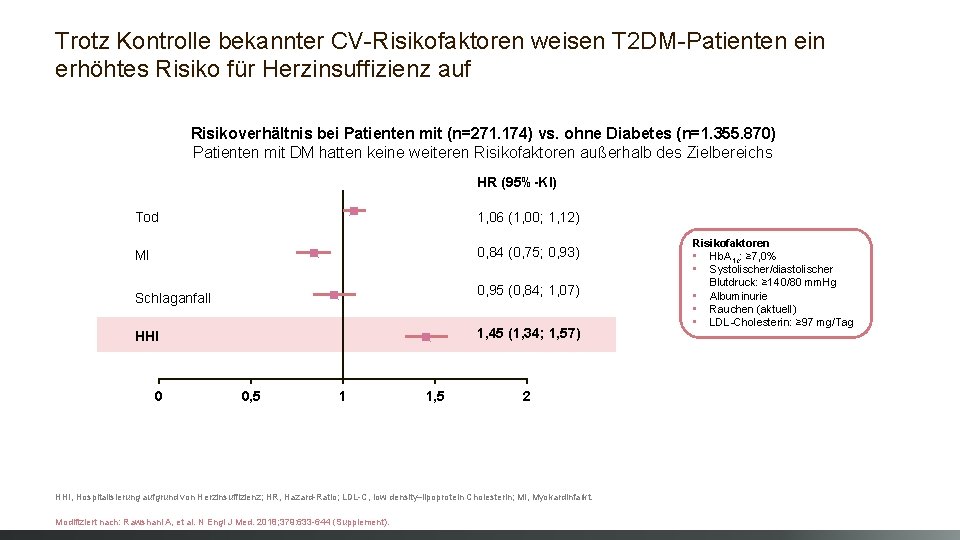
Trotz Kontrolle bekannter CV-Risikofaktoren weisen T 2 DM-Patienten ein erhöhtes Risiko für Herzinsuffizienz auf Risikoverhältnis bei Patienten mit (n=271. 174) vs. ohne Diabetes (n=1. 355. 870) Patienten mit DM hatten keine weiteren Risikofaktoren außerhalb des Zielbereichs HR (95%-KI) Tod 1, 06 (1, 00; 1, 12) MI 0, 84 (0, 75; 0, 93) 0, 95 (0, 84; 1, 07) Schlaganfall 1, 45 (1, 34; 1, 57) HHI 0 0, 5 1 1, 5 2 HHI, Hospitalisierung aufgrund von Herzinsuffizienz; HR, Hazard-Ratio; LDL-C, low density–lipoprotein Cholesterin; MI, Myokardinfarkt. Modifiziert nach: Rawshani A, et al. N Engl J Med. 2018; 379: 633 -644 (Supplement). Risikofaktoren • Hb. A 1 c: ≥ 7, 0% • Systolischer/diastolischer Blutdruck: ≥ 140/80 mm. Hg • Albuminurie • Rauchen (aktuell) • LDL-Cholesterin: ≥ 97 mg/Tag
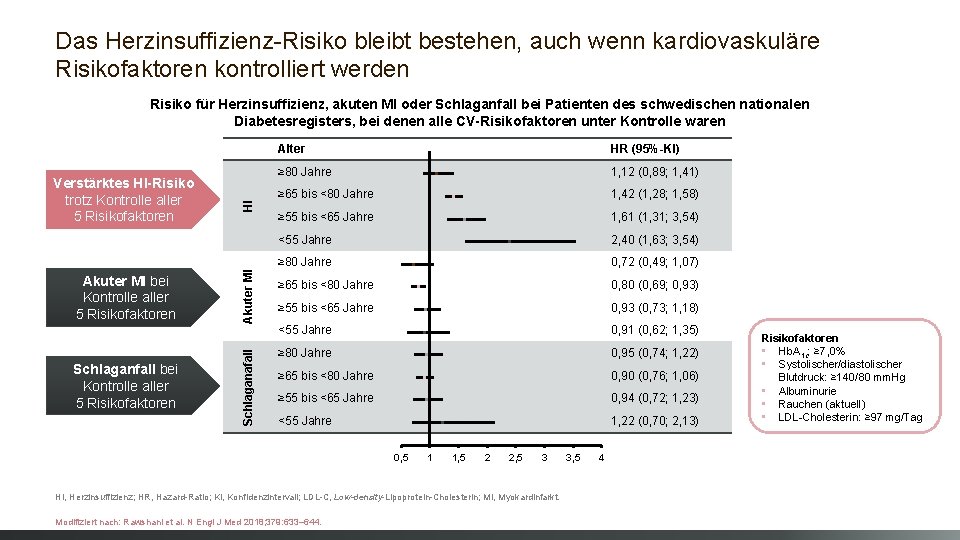
Das Herzinsuffizienz-Risiko bleibt bestehen, auch wenn kardiovaskuläre Risikofaktoren kontrolliert werden Schlaganfall bei Kontrolle aller 5 Risikofaktoren Akuter MI bei Kontrolle aller 5 Risikofaktoren Schlaganafall Verstärktes HI-Risiko trotz Kontrolle aller 5 Risikofaktoren HI Risiko für Herzinsuffizienz, akuten MI oder Schlaganfall bei Patienten des schwedischen nationalen Diabetesregisters, bei denen alle CV-Risikofaktoren unter Kontrolle waren Alter HR (95%-KI) ≥ 80 Jahre 1, 12 (0, 89; 1, 41) ≥ 65 bis <80 Jahre 1, 42 (1, 28; 1, 58) ≥ 55 bis <65 Jahre 1, 61 (1, 31; 3, 54) <55 Jahre 2, 40 (1, 63; 3, 54) ≥ 80 Jahre 0, 72 (0, 49; 1, 07) ≥ 65 bis <80 Jahre 0, 80 (0, 69; 0, 93) ≥ 55 bis <65 Jahre 0, 93 (0, 73; 1, 18) <55 Jahre 0, 91 (0, 62; 1, 35) ≥ 80 Jahre 0, 95 (0, 74; 1, 22) ≥ 65 bis <80 Jahre 0, 90 (0, 76; 1, 06) ≥ 55 bis <65 Jahre 0, 94 (0, 72; 1, 23) <55 Jahre 1, 22 (0, 70; 2, 13) 0, 5 1 1, 5 2 2, 5 3 HI, Herzinsuffizienz; HR, Hazard-Ratio; KI, Konfidenzintervall; LDL-C, Low-density-Lipoprotein-Cholesterin; MI, Myokardinfarkt. Modifiziert nach: Rawshani et al. N Engl J Med 2018; 379: 633– 644. 3, 5 4 Risikofaktoren • Hb. A 1 c: ≥ 7, 0% • Systolischer/diastolischer Blutdruck: ≥ 140/80 mm. Hg • Albuminurie • Rauchen (aktuell) • LDL-Cholesterin: ≥ 97 mg/Tag
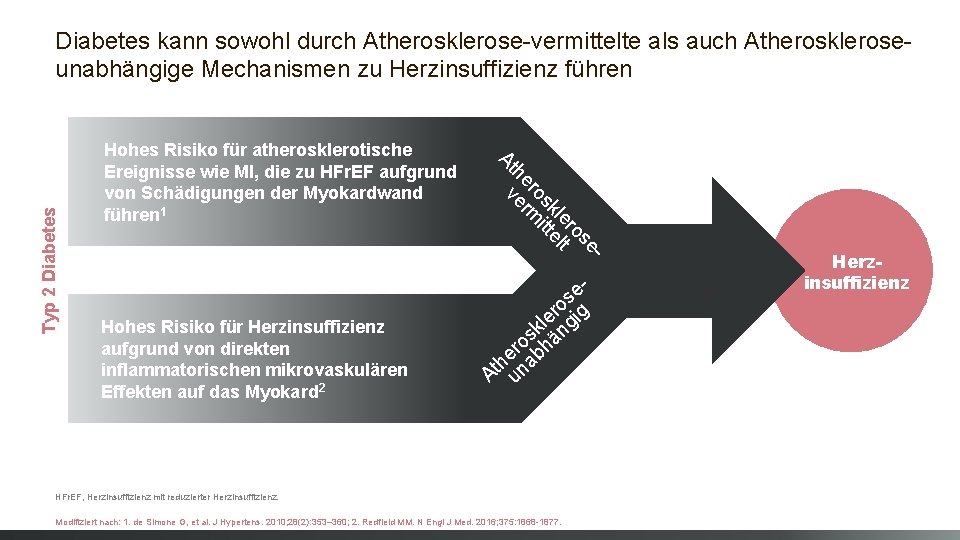
Typ 2 Diabetes kann sowohl durch Atherosklerose-vermittelte als auch Atheroskleroseunabhängige Mechanismen zu Herzinsuffizienz führen Hohes Risiko für atherosklerotische Ereignisse wie MI, die zu HFr. EF aufgrund von Schädigungen der Myokardwand führen 1 Hohes Risiko für Herzinsuffizienz aufgrund von direkten inflammatorischen mikrovaskulären Effekten auf das Myokard 2 At he ve ros rm kle itt ro el se t - e os ig r le ng k os hä r he nab t A u HFr. EF, Herzinsuffizienz mit reduzierter Herzinsuffizienz. Modifiziert nach: 1. de Simone G, et al. J Hypertens. 2010; 28(2): 353– 360; 2. Redfield MM. N Engl J Med. 2016; 375: 1868 -1877. Herzinsuffizienz
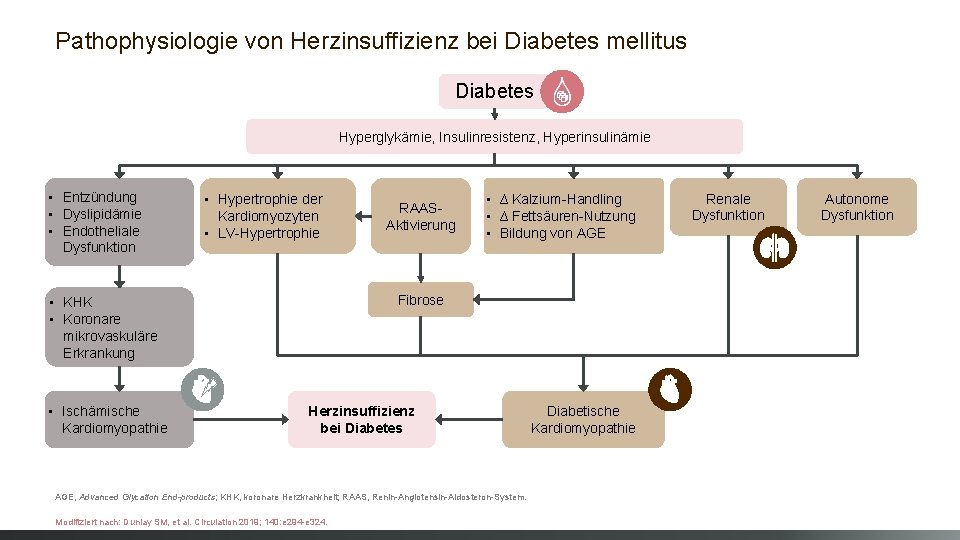
Pathophysiologie von Herzinsuffizienz bei Diabetes mellitus Diabetes Hyperglykämie, Insulinresistenz, Hyperinsulinämie • Entzündung • Dyslipidämie • Endotheliale Dysfunktion • Hypertrophie der Kardiomyozyten • LV-Hypertrophie • ∆ Kalzium-Handling • ∆ Fettsäuren-Nutzung • Bildung von AGE Fibrose • KHK • Koronare mikrovaskuläre Erkrankung • Ischämische Kardiomyopathie RAASAktivierung Herzinsuffizienz bei Diabetes AGE, Advanced Glycation End-products; KHK, koronare Herzkrankheit; RAAS, Renin-Angiotensin-Aldosteron-System. Modifiziert nach: Dunlay SM, et al. Circulation 2019; 140: e 294 -e 324. Diabetische Kardiomyopathie Renale Dysfunktion Autonome Dysfunktion
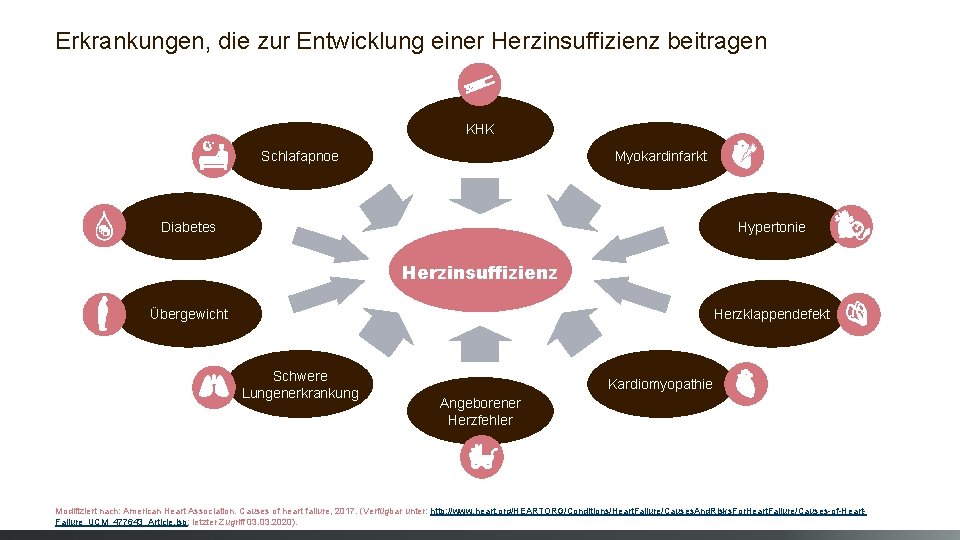
Erkrankungen, die zur Entwicklung einer Herzinsuffizienz beitragen KHK Schlafapnoe Myokardinfarkt Diabetes Hypertonie Herzinsuffizienz Übergewicht Herzklappendefekt Schwere Lungenerkrankung Kardiomyopathie Angeborener Herzfehler Modifiziert nach: American Heart Association. Causes of heart failure, 2017. (Verfügbar unter: http: //www. heart. org/HEARTORG/Conditions/Heart. Failure/Causes. And. Risks. For. Heart. Failure/Causes-of-Heart. Failure_UCM_477643_Article. jsp; letzter Zugriff 03. 2020).
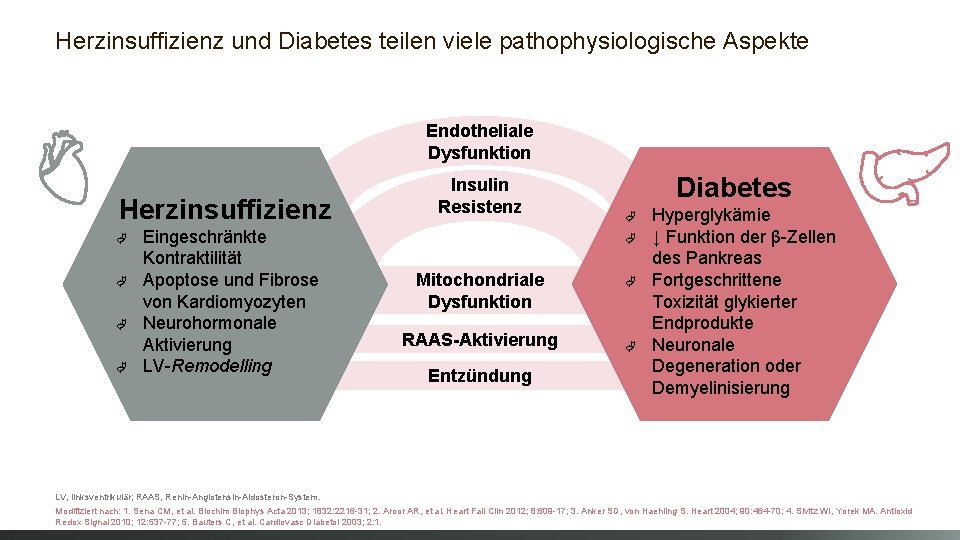
Herzinsuffizienz und Diabetes teilen viele pathophysiologische Aspekte Endotheliale Dysfunktion Herzinsuffizienz à à Eingeschränkte Kontraktilität Apoptose und Fibrose von Kardiomyozyten Neurohormonale Aktivierung LV-Remodelling Insulin Resistenz Diabetes à à Mitochondriale Dysfunktion RAAS-Aktivierung Entzündung à à Hyperglykämie ↓ Funktion der β-Zellen des Pankreas Fortgeschrittene Toxizität glykierter Endprodukte Neuronale Degeneration oder Demyelinisierung LV, linksventrikulär; RAAS, Renin-Angiotensin-Aldosteron-System. Modifiziert nach: 1. Sena CM, et al. Biochim Biophys Acta 2013; 1832: 2216 -31; 2. Aroor AR, et al. Heart Fail Clin 2012; 8: 609 -17; 3. Anker SD, von Haehling S. Heart 2004; 90: 464 -70; 4. Sivitz WI, Yorek MA. Antioxid Redox Signal 2010; 12: 537 -77; 5. Bauters C, et al. Cardiovasc Diabetol 2003; 2: 1.
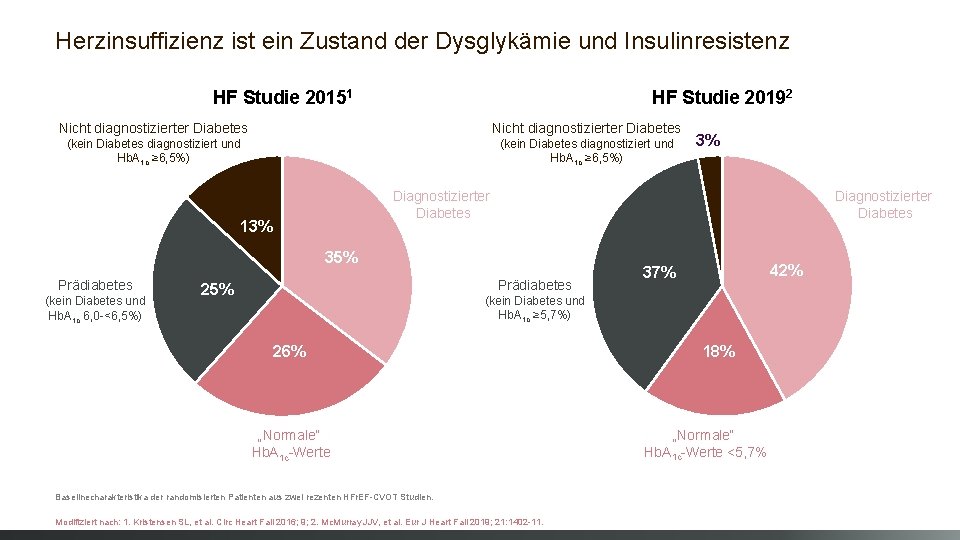
Herzinsuffizienz ist ein Zustand der Dysglykämie und Insulinresistenz HF Studie 20192 HF Studie 20151 Nicht diagnostizierter Diabetes (kein Diabetes diagnostiziert und Hb. A 1 c ≥ 6, 5%) Diagnostizierter Diabetes 13% Diagnostizierter Diabetes 35% Prädiabetes (kein Diabetes und Hb. A 1 c 6, 0 -<6, 5%) 3% Prädiabetes 25% 42% 37% (kein Diabetes und Hb. A 1 c ≥ 5, 7%) 26% „Normale“ Hb. A 1 c-Werte Baselinecharakteristika der randomisierten Patienten aus zwei rezenten HFr. EF-CVOT Studien. Modifiziert nach: 1. Kristensen SL, et al. Circ Heart Fail 2016; 9; 2. Mc. Murray JJV, et al. Eur J Heart Fail 2019; 21: 1402 -11. 18% „Normale“ Hb. A 1 c-Werte <5, 7%
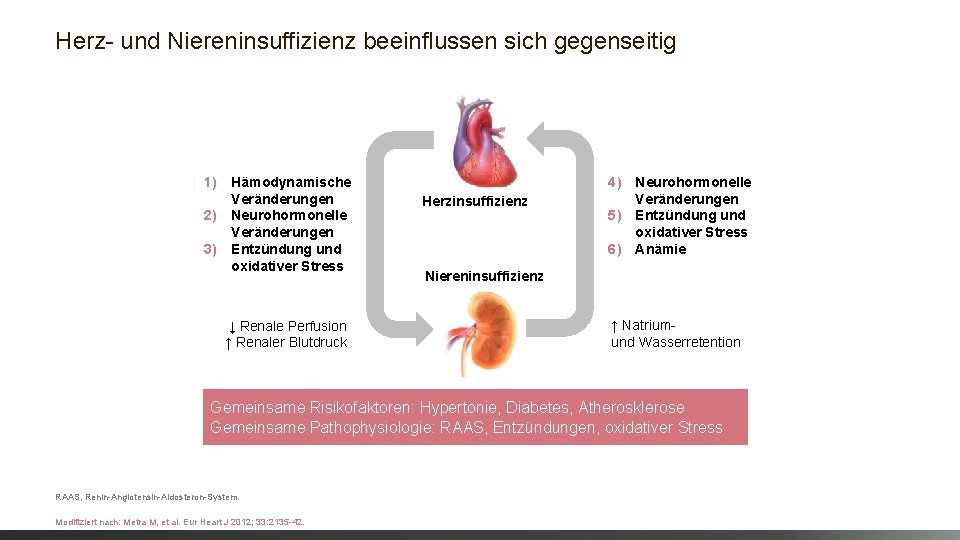
Herz- und Niereninsuffizienz beeinflussen sich gegenseitig 1) Hämodynamische Veränderungen 2) Neurohormonelle Veränderungen 3) Entzündung und oxidativer Stress ↓ Renale Perfusion ↑ Renaler Blutdruck Herzinsuffizienz 4) Neurohormonelle Veränderungen 5) Entzündung und oxidativer Stress 6) Anämie Niereninsuffizienz ↑ Natriumund Wasserretention Gemeinsame Risikofaktoren: Hypertonie, Diabetes, Atherosklerose Gemeinsame Pathophysiologie: RAAS, Entzündungen, oxidativer Stress RAAS, Renin-Angiotensin-Aldosteron-System. Modifiziert nach: Metra M, et al. Eur Heart J 2012; 33: 2135 -42.
Das kardiorenale Syndrom Akutes kardiorenales Syndrom – Typ 1 Eine akute Verschlechterung der Herzfunktion führt zu akutem Nierenversagen • • • Hypertensives Lungenödem Kardiogener Schock Akutes Rechtsherzversagen Chronisches kardiorenales Syndrom – Typ 2 Eine chronische Herzinsuffizienz führt zu einer chronischen Nierenerkrankung • • • Periphere Minderperfusion Makrovaskulopathie Mikrovaskulopathie Akutes renokardiales Syndrom – Typ 3 Ein akutes Nierenversagen führt zu kardialer Dysfunktion • • • Lungenödem Elektrolytentgleisung (Hyperkaliämie) – Arrhythmien/Herzstillstand Urämie – Perikarditis, reduzierte myokardiale Kontraktilität Chronisches renokardiales Syndrom – Typ 4 Eine chronische Verschlechterung der Nierenfunktion verschlechtert die Herzfunktion und führt zu kardiovaskulären Ereignissen • • • Kardiovaskuläres Remodelling (LVH, diastolische Dysfunktion) Erhöhte kardiovaskuläre Ereignisrate (z. B. Myokardinfarkt, Schlaganfall) Beschleunigte Atherosklerose Sekundäres kardiorenales Syndrom – Typ 5 Systemerkrankungen führen parallel zu Schädigungen von Herz und Nieren • • • Sepsis, septischer Schock Autoimmunerkrankungen Diabetes mellitus LVH, linksventrikuläre Hypertrophie. Modifiziert nach: Ronco C, et al. J Am Coll Cardiol 2008; 52: 1527 -39.
- Slides: 23