HendersonHasselbach ekvationen OBS Gller d syra och bas
![Henderson-Hasselbach ekvationen OBS! Gäller då [syra] och [bas] >> [OH-], [H 3 O+] [HA] Henderson-Hasselbach ekvationen OBS! Gäller då [syra] och [bas] >> [OH-], [H 3 O+] [HA]](https://slidetodoc.com/presentation_image_h/0cddb7187546543f1a96ecf32e1c80b8/image-1.jpg)
Henderson-Hasselbach ekvationen OBS! Gäller då [syra] och [bas] >> [OH-], [H 3 O+] [HA] p. H = p. Ka – log [A-] HÄRLEDNING: HA(aq) + H 2 O(l) A-(aq) + H 3 O+ (aq) [A-(aq) ][H 3 O+ (aq)] Ka = [HA(aq) ] [H 3 O+ [HA(aq) ] (aq)] = Ka [A (aq) ] -log [H 3 O+ (aq)] = -log Ka - log p. H KEMA 02/ © Sofi Elmroth 2010 p. Ka [HA(aq) ] [A-(aq) ]
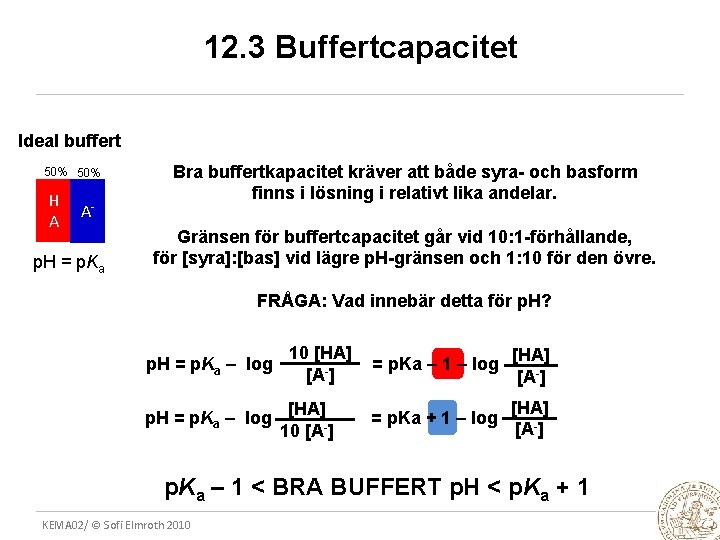
12. 3 Buffertcapacitet Ideal buffert 50% H A A- p. H = p. Ka Bra buffertkapacitet kräver att både syra- och basform finns i lösning i relativt lika andelar. Gränsen för buffertcapacitet går vid 10: 1 -förhållande, för [syra]: [bas] vid lägre p. H-gränsen och 1: 10 för den övre. FRÅGA: Vad innebär detta för p. H? p. H = p. Ka – log 10 [HA] [A-] p. H = p. Ka – log [HA]10 [A ] = p. Ka – 1 – log [HA] [A-] = p. Ka + 1 – log [HA] [A-] p. Ka – 1 < BRA BUFFERT p. H < p. Ka + 1 KEMA 02/ © Sofi Elmroth 2010
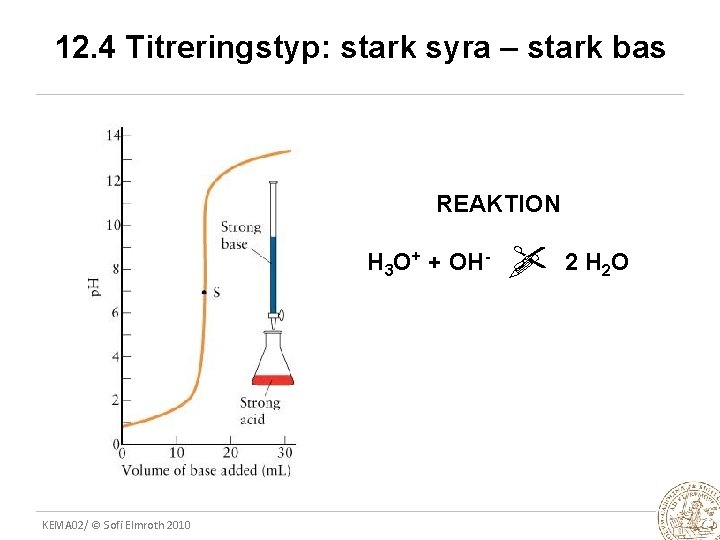
12. 4 Titreringstyp: stark syra – stark bas REAKTION H 3 O+ + OH- KEMA 02/ © Sofi Elmroth 2010 2 H 2 O
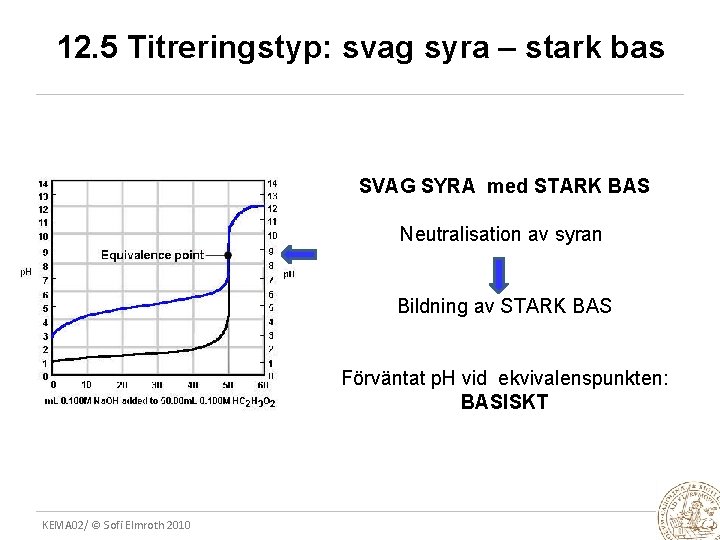
12. 5 Titreringstyp: svag syra – stark bas SVAG SYRA med STARK BAS Neutralisation av syran Bildning av STARK BAS Förväntat p. H vid ekvivalenspunkten: BASISKT KEMA 02/ © Sofi Elmroth 2010
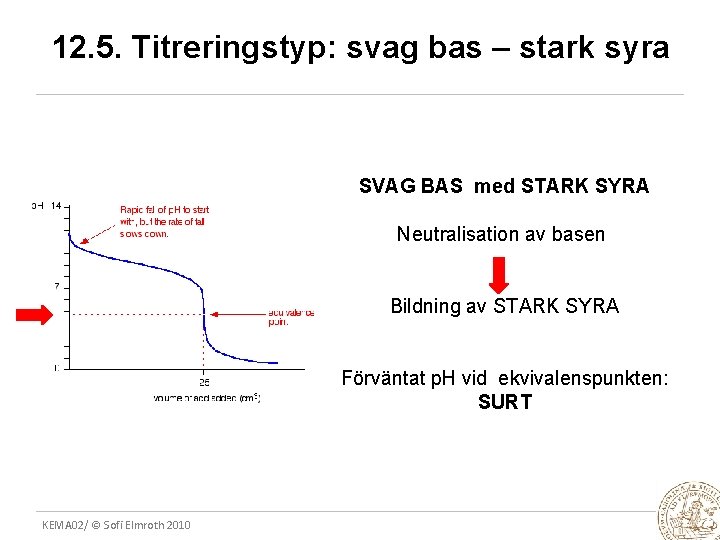
12. 5. Titreringstyp: svag bas – stark syra SVAG BAS med STARK SYRA Neutralisation av basen Bildning av STARK SYRA Förväntat p. H vid ekvivalenspunkten: SURT KEMA 02/ © Sofi Elmroth 2010

JV FLS 2(3) KEM A 02 Allmän- och oorganisk kemi JÄMVIKT i LÖSNING A: Kap 12 Föreläsning 2(3) mer p. H, indikatorer och löslighetsprodukt KEMA 02/ © Sofi Elmroth 2010
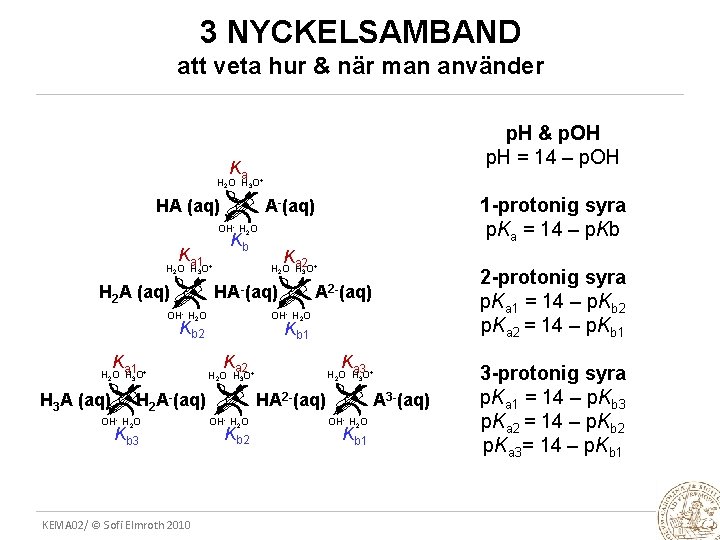
3 NYCKELSAMBAND att veta hur & när man använder p. H & p. OH p. H = 14 – p. OH Ka H 2 O H 3 O+ HA (aq) 1 -protonig syra p. Ka = 14 – p. Kb - OH- H 2 O Kb Ka 1 H 2 A (aq) OH- K H 2 O a 2 H 3 O+ H 2 O H 3 O+ HA-(aq) H 2 O OH- H 2 O Kb 2 Kb 1 Ka 2 Ka 1 H 2 O H 3 O+ Ka 3 H 2 O H 3 O+ H A (aq) HA H 3 A (aq) 2 - OH- H 2 O Kb 3 KEMA 02/ © Sofi Elmroth 2010 2 -protonig syra p. Ka 1 = 14 – p. Kb 2 p. Ka 2 = 14 – p. Kb 1 A 2 -(aq) OH- H 2 O Kb 2 2 -(aq) A OH- H 2 O Kb 1 3 -(aq) 3 -protonig syra p. Ka 1 = 14 – p. Kb 3 p. Ka 2 = 14 – p. Kb 2 p. Ka 3= 14 – p. Kb 1
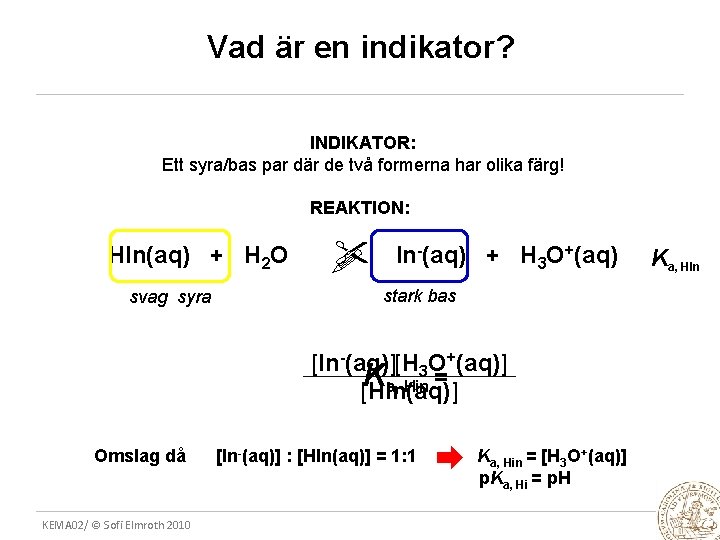
Vad är en indikator? INDIKATOR: Ett syra/bas par där de två formerna har olika färg! REAKTION: HIn(aq) + H 2 O svag syra In-(aq) + H 3 O+(aq) stark bas [In-(aq)][H 3 O+(aq)] Ka, Hin = [HIn(aq)] Omslag då KEMA 02/ © Sofi Elmroth 2010 [In-(aq)] : [HIn(aq)] = 1: 1 Ka, Hin = [H 3 O+(aq)] p. Ka, Hi = p. H Ka, HIn
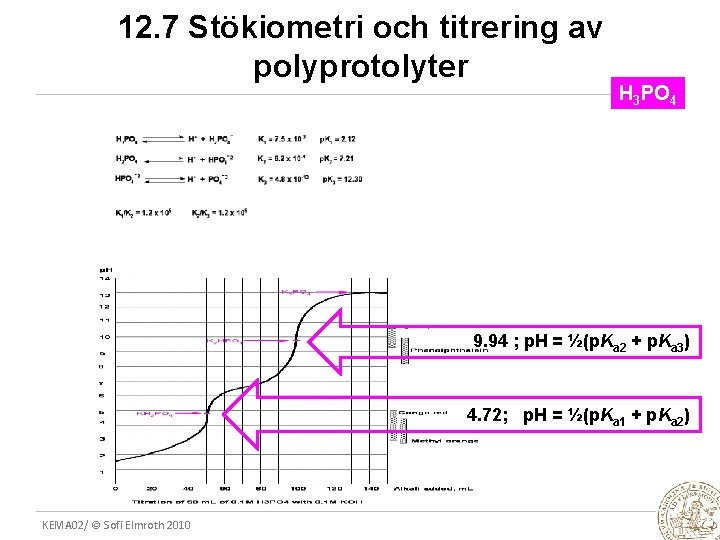
12. 7 Stökiometri och titrering av polyprotolyter H 3 PO 4 9. 94 ; p. H = ½(p. Ka 2 + p. Ka 3) 4. 72; p. H = ½(p. Ka 1 + p. Ka 2) KEMA 02/ © Sofi Elmroth 2010

LÖSLIGHETSJÄMVIKTER Salter – en kombination av katjoner och anjoner – kan vara mycket olika lösliga i vatten! “…. A barium sulphate suspension in water is the universal contrast medium used for examination of the upper gastrointestinal tract. ” KÄLLA: http: //www. e-radiography. net/ contrast_media/contrast_ media_introduction. htm Na. Cl – ”salt” mkt lättlösligt KEMA 02/ © Sofi Elmroth 2010

Löslighetsjämvikter & biorelevans TYPISKA OMRÅDEN & FRÅGESTÄLLNINGAR: några exempel. . . det finns mycket mer! Vattenkvalitet Fe(II/III), Cr(III-VII), Pb(II), Al(III) ”Bioavailability” av spårmetaller Cu(II), Ni(II), Mn(II) Läckage av metalljoner från gruvmiljö/deponier Metallothioniner är svavel-innehållande protein som används för att transportera tex Cu(II) och Hg(II). Fe(II/III), Ni(II/III), Pb(II/IV), Hg(I/II), Ag(I), Au(III/I) Toxicitet Fe(II/III), Ni(II/III), Pb(II/IV), Hg(I/II), Ag(I), Cd(II) Ksp (Cu. S) = 1. 3 E-36* Ksp (Hg. S) = 1 E-53* Sofi Elmroth 2010 *dvs. KEMA 02/ mkt liten©tendens till frisläppning av M(II) – mer om detta senare! Funktion Na(I), K(I)

12. 8 Löslighetsprodukt BEGREPP: Löslighetsprodukt – ett mått på lösligheten en jämvikt som alla andra! EXEMPEL: Upplösning av Bi 2 S 3(s) 2 Bi 3+(aq) + 3 S 2 -(aq) Ksp = a(Bi 3+(aq))2 a(S 2 -(aq))3 Ksp = [Bi 3+(aq)]2 [S 2 -(aq)]3 Ksp litet för svårlösliga salter; Ksp (Bi 2 S 3(s)) = 1. 0 E-97 M 4 KEMA 02/ © Sofi Elmroth 2010 Ksp

JV FLS 3(3) KEM A 02 Allmän- och oorganisk kemi JÄMVIKT i LÖSNING A: Kap 12 Föreläsning 3(3) mer löslighetsprodukt! KEMA 02/ © Sofi Elmroth 2010

Repetition Henderson-Hasselbach ekvationen för beräkning av p. H i ”buffert” - OK att använda - viktigast att förstå när den är applicerbar - egentligen helt onödig! Buffertkapacitet -bra p. H område ca ; p. Ka – 1 < p. H < p. Ka + 1 Utseende titrerkurva - Stark syra + stark bas; ekvivalenspunkt vid p. H = 7 - Svag syra + stark bas; ekvivalenspunkt vid p. H > 7 (stark bas genereras) - Svag bas + stark syra; ekvivalenspunkt vid p. H < 7 (stark syra genereras) - Titrerkurva polyprotolyter; H 2 SO 4, H 2 SO 3, H 2 CO 3, H 3 PO 4 + stark bas (OH-) Indikatorer - Funktion och använding (varför fungerar de? Matchning av indikator titrering) Löslighetsprodukt – mer om detta idag! KEMA 02/ © Sofi Elmroth 2010

12. 9 ”The common ion effect” vad heter detta på svenska? BAKGRUND Många metalljoner bildar hydroxider vid p. H 7 som faller ut. Den fria metalljonhalten bestäms av löslighetsprodukten, Ksp REAKTION – exempel Al 3+ ETT RIKTIGT EXEMPEL (oktober 2010) Al 3+(aq) + H 2 O Al(OH)3(s) + 3 H+ (HR bara i sur miljö!) ÖVER p. H ca 7. 5 beskrivs detta bäst av reaktionen: Al(OH)3(s) a=1 Al 3+(aq) + 3 OH-(aq) s 3 s Uppskattning av ca halt Al 3+ över Al(OH)3(s): s(3 s)3 = Ksp s = 2. 5 E-9 M (OBS! Ej HR heller. . . ) FRÅGA: Kan man sänka halten Al 3+(aq) ytterligare? KEMA 02/ © Sofi Elmroth 2010 Ksp= 1. 0 E-33 Tabell 12. 4

Strategi för sänkning av metalljonhalt TILLSATS AV MER OH- SKJUTER JÄMVIKTEN ÅT VÄNSTER (reaktanter) BERÄKNING för olika [OH-] Al(OH)3(s) a=1 Al 3+(aq) + 3 OH-(aq) s Ksp= 1. 0 E-33 Tabell 12. 4 [OH-] Generellt uttryck för Ksp: Ksp = s[OH-]3 [OH-] Ksp s = [Al 3+(aq)] 1 E-7 0. 1 1. 0 4. 0 s(1 E-7)3 s(0. 1)3 s(1. 0)3 s(4. 0)3 1. 0 E-12 1. 0 E-30 1. 0 E-33 1. 5 E-35 KEMA 02/ © Sofi Elmroth 2010 SLUTSATS: Förvaring i basisk miljö minimerar Al 3+(aq) MEN! Det blir problem då det läcker ut och p. H stiger!

Vad finns mer i rödslam? bildas vid framställing av Al(s) Bauxiten består av aluminiumoxid och aluminiumhydroxid, men även järnmineral*, titanoxider** och aluminiumsilikater***. [1] *Sannolikt Fe(OH)3(s) dvs rost! ** Tex Ti. O, – vitt pigment som används i färg *** Silikater Si. O 2 – vanlig sand VAD ÄR FARLIGT? ! OH-(aq) pga det höga koncentrationen Na. OH/KOH täcker sannolikt torra partiklar - Tungmetaller kan inte uteslutas; ex) Hg, Cr, As - Partiklar KEMA 02/ © Sofi Elmroth 2010 [1] KÄLLA: Jernkontorets forskning; Rapport nr D 182, 2004 -08 -16 U Lindunger & E Stark

Beräkna effekten av ”utsaltning” EXEMPEL 12. 9 Beräkna lösligheten av Ag. Cl(s) i Na. Cl(aq) VAD VÄNTAR VI OSS? ! KEMA 02/ © Sofi Elmroth 2010
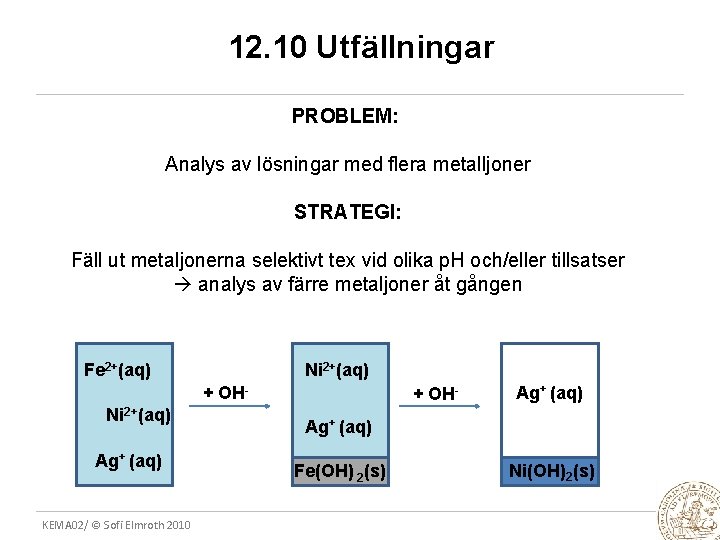
12. 10 Utfällningar PROBLEM: Analys av lösningar med flera metalljoner STRATEGI: Fäll ut metaljonerna selektivt tex vid olika p. H och/eller tillsatser analys av färre metaljoner åt gången Fe 2+(aq) Ni 2+(aq) + OH- Ni 2+(aq) Ag+ (aq) KEMA 02/ © Sofi Elmroth 2010 + OH- Ag+ (aq) Fe(OH) 2(s) Ni(OH)2(s)
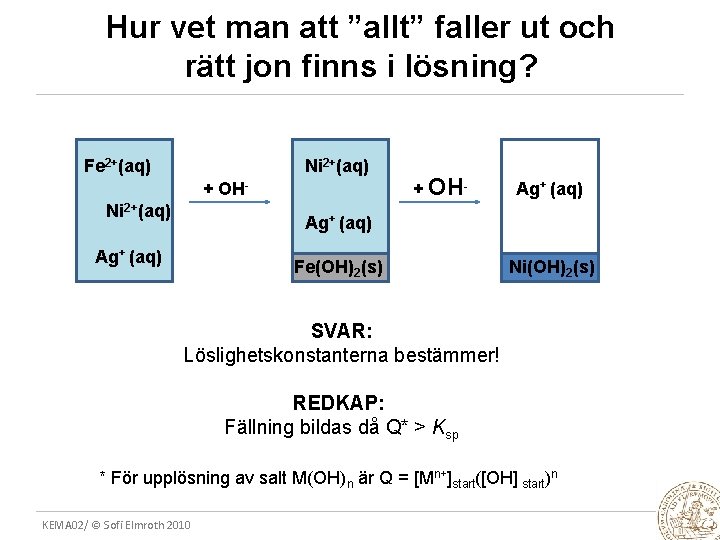
Hur vet man att ”allt” faller ut och rätt jon finns i lösning? Fe 2+(aq) Ni 2+(aq) + OH- Ag+ (aq) Fe(OH)2(s) Ni(OH)2(s) SVAR: Löslighetskonstanterna bestämmer! REDKAP: Fällning bildas då Q* > Ksp * För upplösning av salt M(OH)n är Q = [Mn+]start([OH] start)n KEMA 02/ © Sofi Elmroth 2010

Blandning av 2 lösningar – vad faller ut? EXEMPEL 12. 10 Faller något ut om lika volymer 0. 2 M Pb(NO 3)2(aq) och KI(aq) blandas? KEMA 02/ © Sofi Elmroth 2010

12. 11 Selektiv utfällning Användning av Ksp för att förutsäga i vilken ordning salter faller ut EXEMPEL 12. 11 Utfällning av Mg 2+ och Ca 2+ ur havsvatten m. hj. a. fast Na. OH(s) KEMA 02/ © Sofi Elmroth 2010
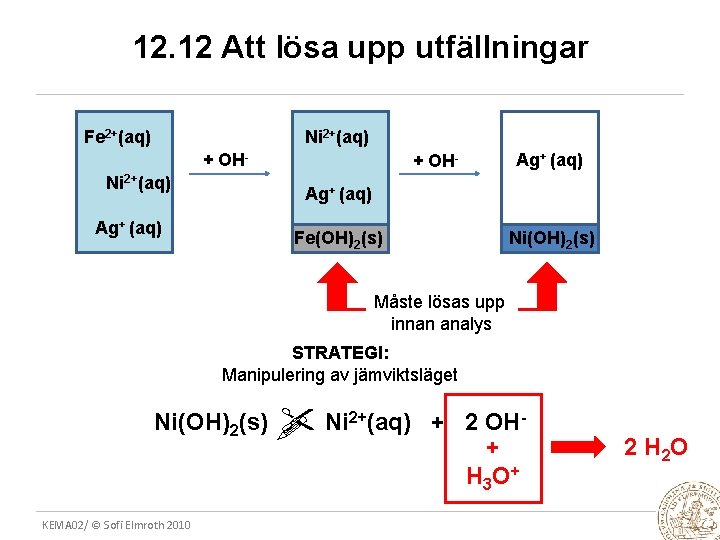
12. 12 Att lösa upp utfällningar Fe 2+(aq) Ni 2+(aq) + OH- Ag+ (aq) Ni(OH)2(s) Fe(OH)2(s) Måste lösas upp innan analys STRATEGI: Manipulering av jämviktsläget Ni(OH)2(s) KEMA 02/ © Sofi Elmroth 2010 2+(aq) Ni + 2 OH+ H 3 O + 2 H 2 O

Strategier exempel olika salter HYDROXIDER – tillsats av syra Ex) Ni(OH)2(s) Ni (aq) 2 H O 2+ OH- + H 3 O+ + 2 OH- (aq) 2 KARBONATER – tillsats av syra Ex) Zn (aq) 2 H O H CO Zn. CO 3(s) CO 32 - + 2+ 3 + 2 + CO 32 - (aq) 3 SULFIDER – tillsats av oxiderande syra Ex) 3 S 2 KEMA 02/ © Sofi Elmroth 2010 Cu (aq) + S (aq) + 8 HNO 2 S(s) + 2 NO(g) + 4 H O(l) + 6 NO Cu. S(s) 2+ 3 2 - 2 3 -

12. 13 Komplexbildning Ytterligare en strategi för upplösning av svårlösliga salter SPECIELLT LÄMPLIG FÖR ÖVERGÅNGSMETALLERNA! Fenomen: ”Maskering av metalljoner” Ag+ Ag. Cl(s) Ag+(aq) + Cl- (aq) Ag+(aq) + 2 NH 3 (aq) Ag(NH 3)2+(aq) EXEMPEL 12. 12: Hur mycket Ag. Cl(s) löses i 0. 1 M NH 3 ? KEMA 02/ © Sofi Elmroth 2010
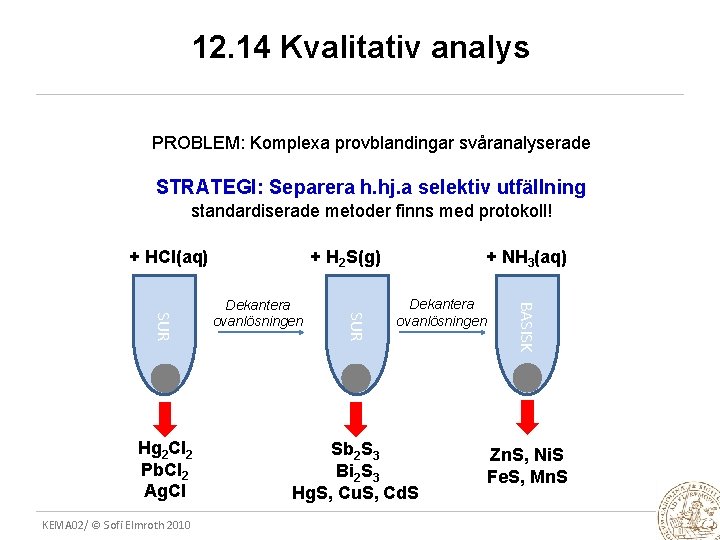
12. 14 Kvalitativ analys PROBLEM: Komplexa provblandingar svåranalyserade STRATEGI: Separera h. hj. a selektiv utfällning standardiserade metoder finns med protokoll! + HCl(aq) + NH 3(aq) Dekantera ovanlösningen Sb 2 S 3 Bi 2 S 3 Hg. S, Cu. S, Cd. S BASISK KEMA 02/ © Sofi Elmroth 2010 Dekantera ovanlösningen SUR Hg 2 Cl 2 Pb. Cl 2 Ag. Cl + H 2 S(g) Zn. S, Ni. S Fe. S, Mn. S
- Slides: 26