HEMOGLOBN VE HEMOGLOBNPATLER Porfirinler porfirin halka sistemi ieren

HEMOGLOBİN VE HEMOGLOBİNPATİLER
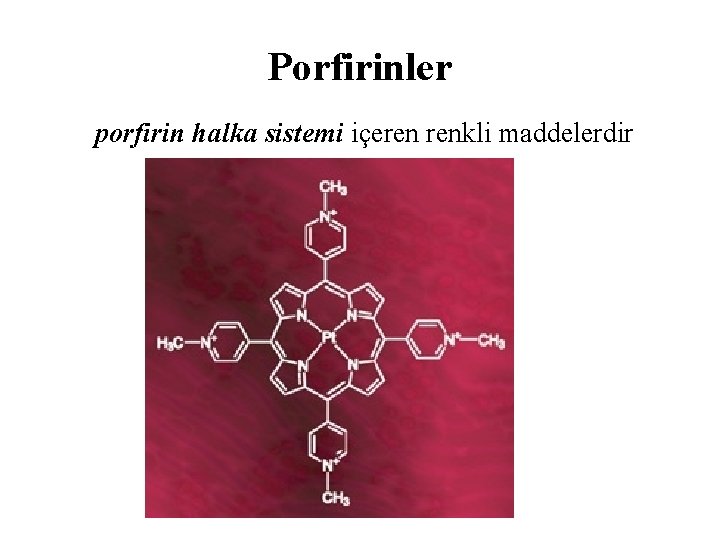
Porfirinler porfirin halka sistemi içeren renkli maddelerdir
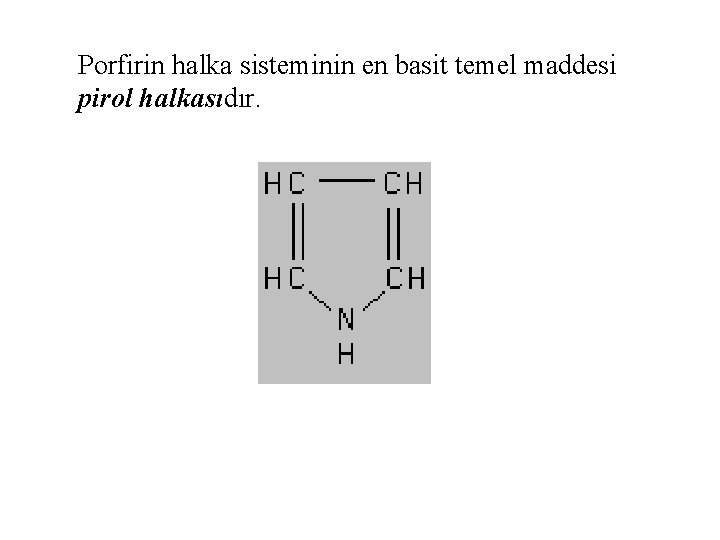
Porfirin halka sisteminin en basit temel maddesi pirol halkasıdır.
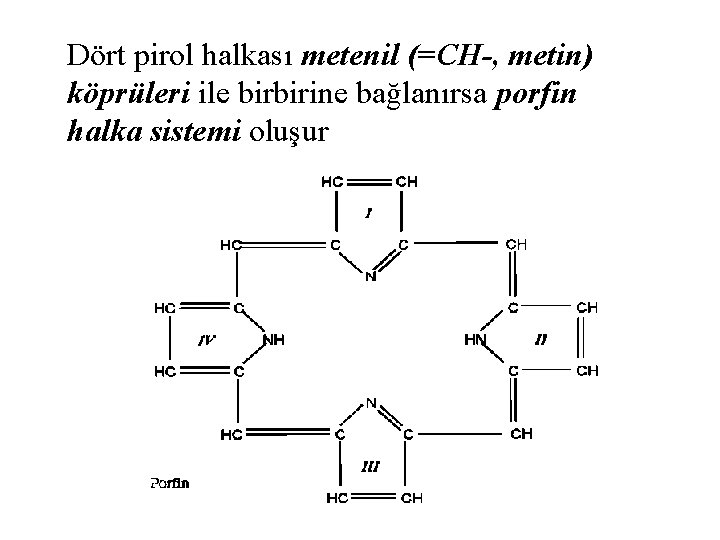
Dört pirol halkası metenil (=CH-, metin) köprüleri ile birbirine bağlanırsa porfin halka sistemi oluşur

Porfin halka sistemindeki pirol halkalarına çeşitli yan zincirlerin eklenmesiyle porfirin halka sistemi oluşur. Asetil (A) ve metil (M) küçük takılardır; propiyonil (P), vinil (V), etil (E) ve oksietil (EOH) büyük takılardır.

Doğada en çok tip. I ve tip III izomer şekiller bulunur

Eritrositlerde bulunan ve kana kırmızı rengini veren hemoglobinin yapısında bulunan hem, önemli bir demir-porfirin bileşiğidir.

Hem, hemoglobin, kasların kırmızı rengini veren miyoglobin, sitokromlar, sitokrom oksidaz, katalaz ve peroksidaz gibi enzimlerin yapısında bulunur. Bitkilerin yeşil rengini veren klorofil, magnezyum-porfirin bileşiğidir.

Hem biyosentezi için temel prekürsör, glisin amino asididir. Hem sentezinde ilk reaksiyon ve son üç reaksiyon mitokondride, diğerleri sitoplazmada gerçekleşir
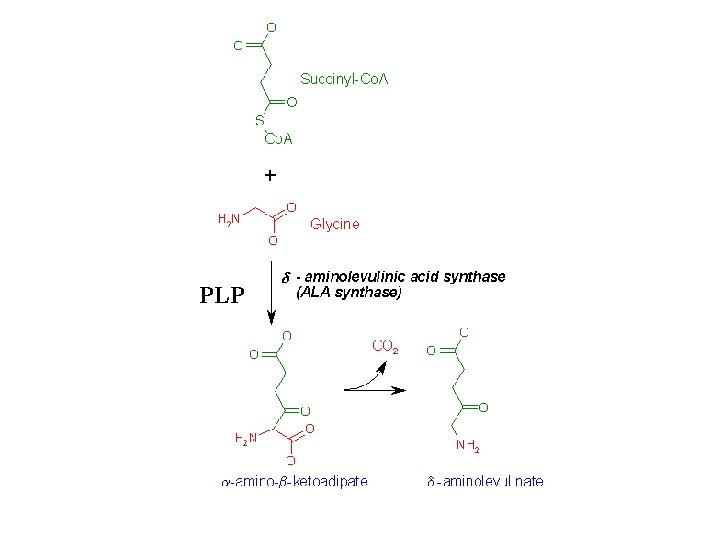
PLP
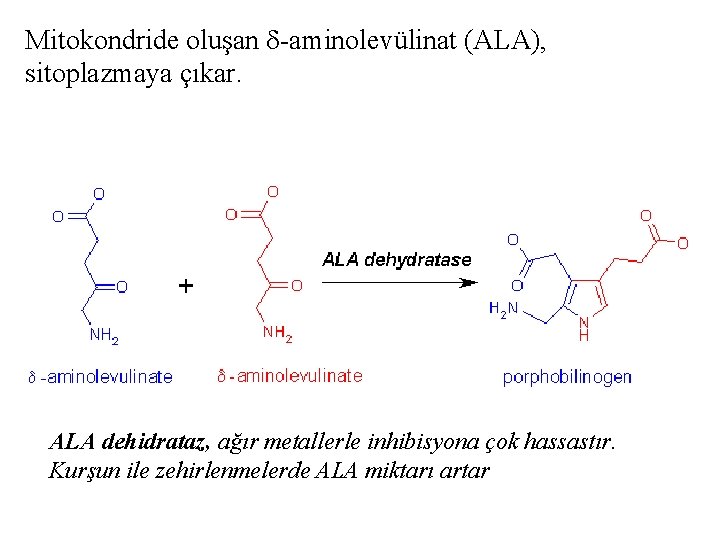
Mitokondride oluşan -aminolevülinat (ALA), sitoplazmaya çıkar. ALA dehidrataz, ağır metallerle inhibisyona çok hassastır. Kurşun ile zehirlenmelerde ALA miktarı artar


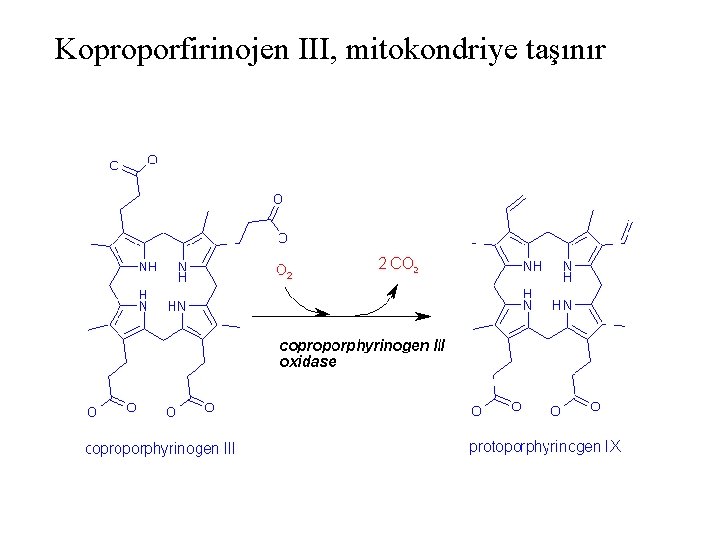
Koproporfirinojen III, mitokondriye taşınır

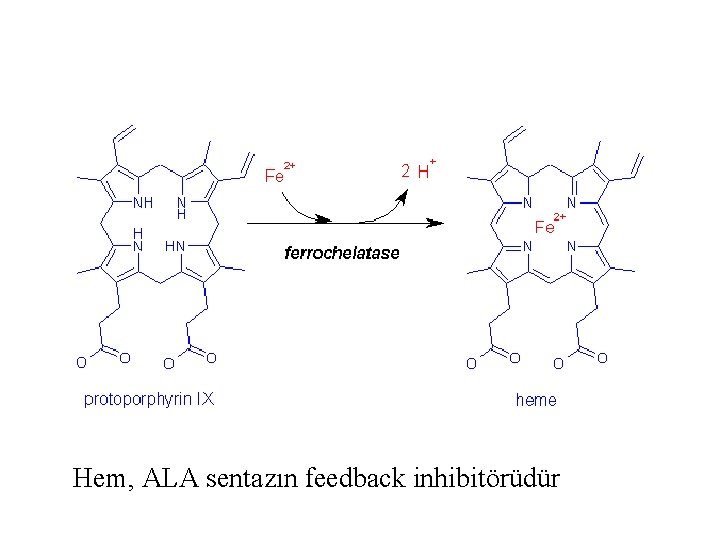
Hem, ALA sentazın feedback inhibitörüdür
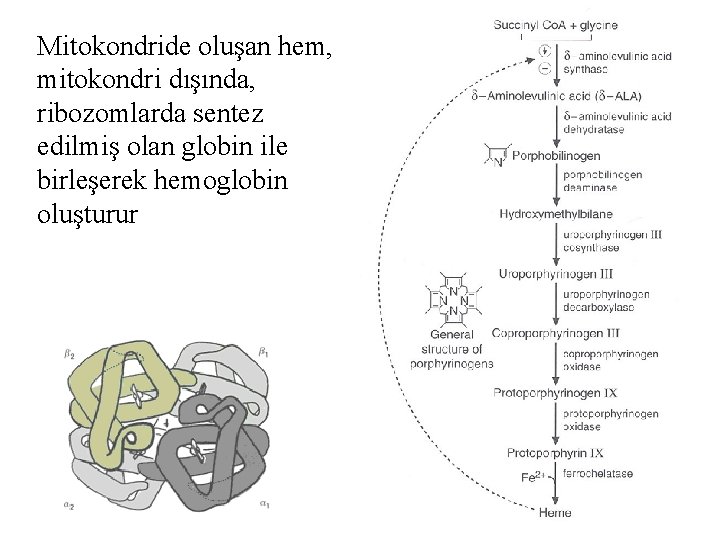
Mitokondride oluşan hem, mitokondri dışında, ribozomlarda sentez edilmiş olan globin ile birleşerek hemoglobin oluşturur
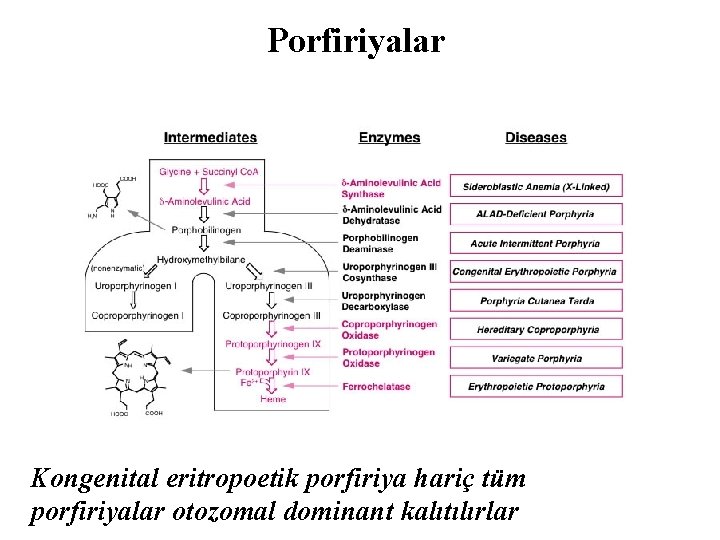
Porfiriyalar Kongenital eritropoetik porfiriya hariç tüm porfiriyalar otozomal dominant kalıtılırlar


Hemoglobin, kanda eritrositlerde bulunan, kana kırmızı rengini veren, demir-porfirinli bir bileşik proteindir yetişkin erkek için %14 -18 g yetişkin kadın için %12 -15 g çocuk için %12 -13 g yeni doğan için % 21 g kadardır
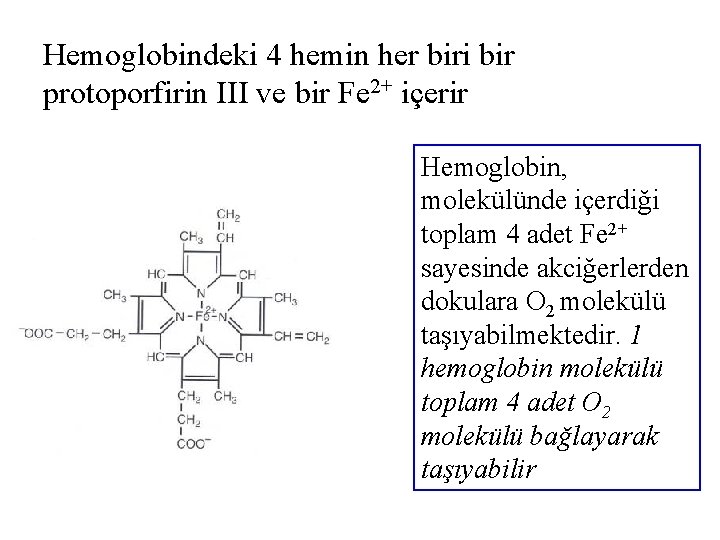
Hemoglobindeki 4 hemin her biri bir protoporfirin III ve bir Fe 2+ içerir Hemoglobin, molekülünde içerdiği toplam 4 adet Fe 2+ sayesinde akciğerlerden dokulara O 2 molekülü taşıyabilmektedir. 1 hemoglobin molekülü toplam 4 adet O 2 molekülü bağlayarak taşıyabilir
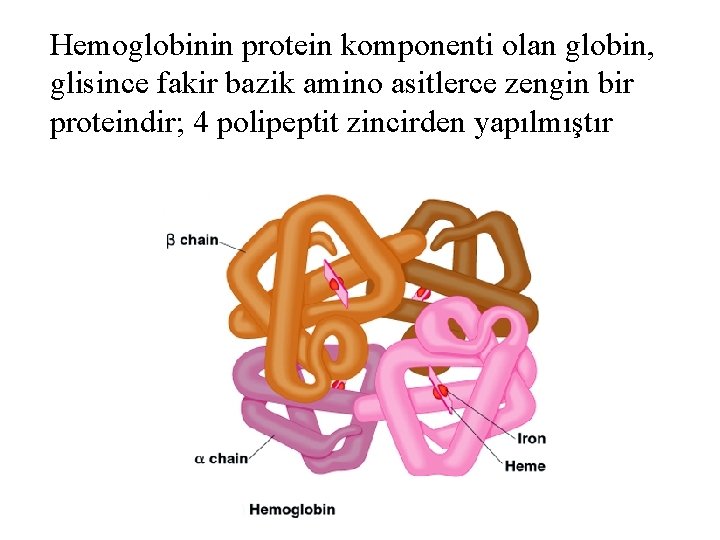
Hemoglobinin protein komponenti olan globin, glisince fakir bazik amino asitlerce zengin bir proteindir; 4 polipeptit zincirden yapılmıştır

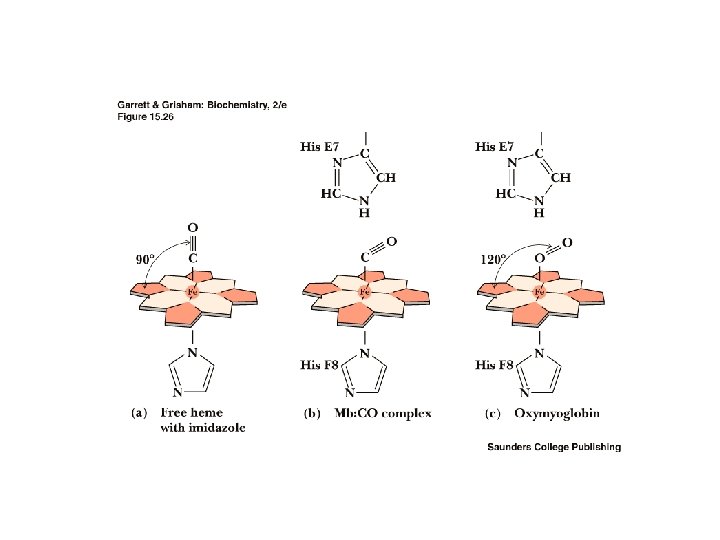
Oksihemoglobin (Hb. O 2) Oksihemoglobin, hemoglobin molekülündeki 4 Fe 2+’e akciğerlerde birer O 2 molekülü bağlanması sonucu oluşan hemoglobin bileşiğidir Hemoglobin molekülüne akciğerlerde O 2 moleküllerinin bağlanması olayı, hemoglobinin oksijenasyonu olarak tanımlanır Bir hemoglobin molekülü, oksijenasyon olayı sonucunda 4 O 2 molekülü bağlayabilmektedir

Hemoglobinin oksijene affinitesi, oksijenin kısmi basıncına bağlıdır p. O 2 değişimine karşı hemoglobinin oksijenle % satürasyonunu gösteren grafiklere hemoglobinin satürasyon eğrisi veya oksihemoglobinin dissosiasyon eğrisi denir
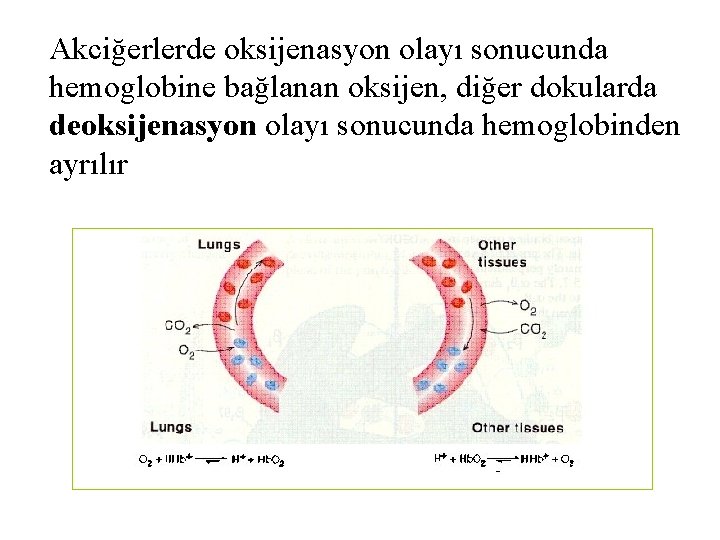
Akciğerlerde oksijenasyon olayı sonucunda hemoglobine bağlanan oksijen, diğer dokularda deoksijenasyon olayı sonucunda hemoglobinden ayrılır
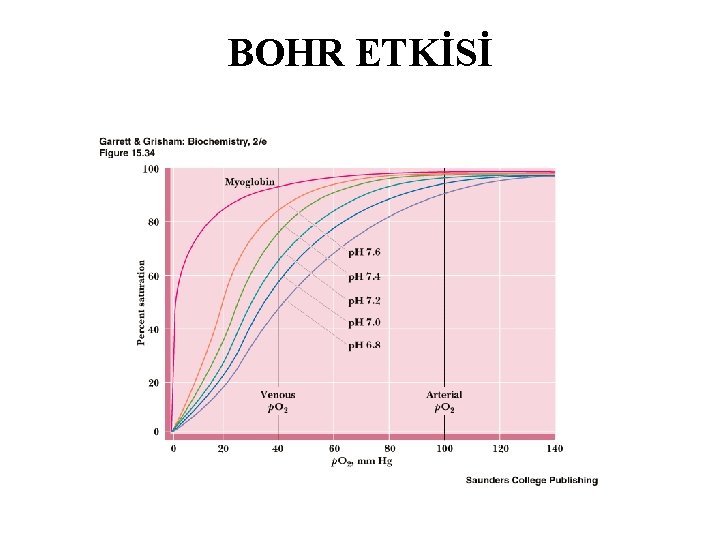
BOHR ETKİSİ

2, 3 -Bifosfogliserat • Hemoglobinin allosterik efektörüdür. • Glikolizde yer alan 1, 3 bifosfogliserattan sentez edilir. • Düşük oksijen basıncında hemolobinin oksijene olan ilgisini azaltarak dokulara bırakılmasını sağlar.

Oksijenize hemoglobin (oksihemoglobin) parlak kırmızı, deoksijenize hemoglobin (deoksihemoglobin) koyu kırmızıdır kanın oksijenlenmesinde bir azalma ve bunun sonucu olarak deoksijenize olmuş hemoglobinde artış, deri ve mukozalara karakteristik mavimtrak bir renk verir ki bu durum siyanoz olarak tanımlanır

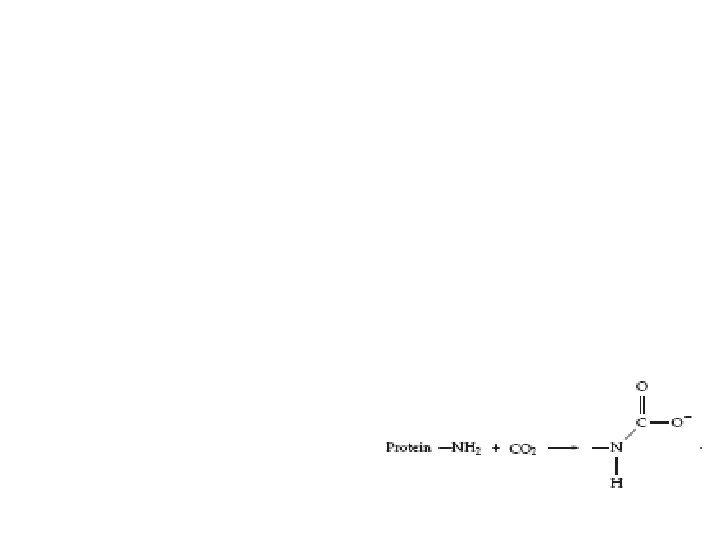
Karbaminohemoglobin Hemoglobindeki globinin serbest -amino gruplarına reversibl olarak CO 2 bağlanmasıyla oluşan hemoglobin bileşiğidir Karbamino grubu, hemoglobinin oksijene olan ilgisini azaltır ki bu etki, p. H düşüşünden bağımsızdır CO 2, deoksijenize hemoglobine oksihemoglobinden daha çok bağlanır ve böylece dokulardan akciğerlere hemoglobin ile taşınabilir

Karboksihemoglobin (Hb CO) Oksihemoglobindeki O 2 yerine karbonmonoksit (CO) geçmesi suretiyle oluşan hemoglobin bileşiğidir Hemoglobinin CO’e affinitesi O 2’e affinitesinden 200 misli fazladır; ortamda oksijen ve karbonmonoksit eşit miktarlarda bulunduğunda hemoglobine tercihli olarak CO bağlanır ve anemik hipoksiye neden olur

CO ile zehirlenmenin belirtileri, bilinç kaybı, tırnak dipleri ve mukoz membranların kiraz kırmızısı renk almasıdır CO ile zehirlenmenin tanısı için kan Na. OH ile karıştırılır; normalde koyu kahverengi renk gözlendiği halde CO ile zehirlenme durumunda kiraz kırmızısı renk gözlenir
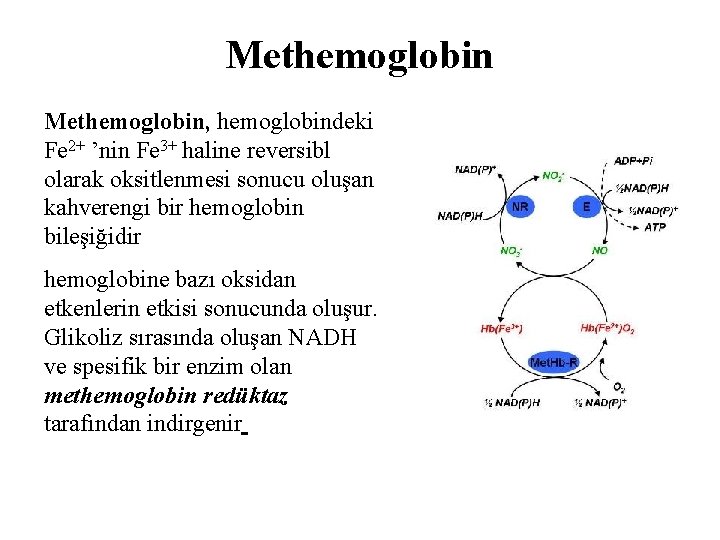
Methemoglobin, hemoglobindeki Fe 2+ ’nin Fe 3+ haline reversibl olarak oksitlenmesi sonucu oluşan kahverengi bir hemoglobin bileşiğidir hemoglobine bazı oksidan etkenlerin etkisi sonucunda oluşur. Glikoliz sırasında oluşan NADH ve spesifik bir enzim olan methemoglobin redüktaz tarafından indirgenir

Çeşitli hemoglobin tiplerinde bulunabilen polipeptit zincirleri -zincir, -zincir olmak üzere dört tiptir. Bir hemoglobin molekülünde bu zincirlerden iki tür bulunur

Fizyolojik hemoglobinler • Hb. A 1: Globininde 2 ve 2 polipeptit zinciri içeren fizyolojik hemoglobindir. Hb. A 1, erişkin bir şahsın eritrositlerinde bulunan hemoglobinin %97 -98’ini oluşturur • Hb. A 2: Globininde 2 ve 2 polipeptit zinciri içeren fizyolojik hemoglobindir. Erişkin sağlıklı bir şahsın eritrositlerinde bulunan hemoglobinin %0, 5 -2, 5’ini oluşturur • Hb. F: Globininde 2 ve 2 polipeptit zinciri içeren, primitif hemoglobin (Hb. P) diye de bilinir. yeni doğanda total hemoglobinin %70 -90’ını oluşturur

Hb. A 1’in globininin -polipeptit zincirindeki -amino grubuna enzimatik olmayan bir reaksiyonla kovalent bir şekilde karbonhidrat bağlanması sonucu glikozile hemoglobinler oluşur Glikozile hemoglobin oluşumu, yaş ve açlık kan şekeri artışıyla birlikte artar. Hb. A 1 a (Hb. A 3), Hb. A 1 b, Hb. A 1 c, Hb. A 1 d, Hb. A 1 e bilinen glikozile hemoglobinlerdir. Bu hemoglobinler normalde çok az bulunurlar ve hiçbiri toksik değildir Glikozile hemoglobinlerden en sık rastlananı, Hb. A 1 c’dir

Hb. A 1 c, erişkin sağlıklı bir insanda total hemoglobinin %5 -8’ini oluşturur; diyabetli kişilerde glikozile hemoglobin düzeyi total hemoglobinlerin %8’inin üzerine çıkarak normalin 2 -3 misli olabilir Kan Hb. A 1 c düzeyi, diyabetin takibinde ve kan glukoz düzeyinin regülasyonunda önemli bir kimyasal parametredir

Hb. F, yeni doğanda total hemoglobinin %7090’ını oluşturur Doğumda total hemoglobinin %70 -90’ını oluşturan Hb. F, 1. ayın sonunda %50 -70, 2. ayın sonunda %25 -30, 3. ayın sonunda %10 -30, 3 yaşında %1, erişkinde %0, 4’tür. Hb. F’in oksijene affinitesi fazladır.

Anormal hemoglobinler, oksijen taşıma kapasitesi azalmış olan hemoglobinlerdir 1) Hemoglobinin polipeptit zincirine bir veya daha fazla amino asit eklenebilir, zincirden amino asit çıkabilir veya zincirdeki amino asitler yer değiştirebilir 2) Globin zinciri üretiminde defekt olabilir; belli bir globin zinciri türü üretilmez 3) Tip 1 ve tip 2’nin kombinasyonu olabilir

• Hb S: Hb. A 1’in -zincirlerindeki 6. amino asit glutamik asit değil de valin olan hemoglobindir • Hb C: Hb. A 1’in -zincirlerindeki 6. amino asit glutamik asit değil de lizin olan hemoglobindir • Hb Gun Hill: Globini 4 hem değil de 2 hem içeren anormal hemoglobindir • Hb H ve Hb Bart: Hb H, globini -zinciri içermeyen 4 zinciri içeren hemoglobindir. Hb Bart ise globini -zinciri içermeyen, 4 -zinciri içeren hemoglobindir anormal hemoglobinlerin üretilmesiyle karakterize hastalıklar hemoglobinopatiler olarak tanımlanır

Hb S: Oksijensiz ortamda çözünürlüğü azalır; çubuk benzeri lifler ve fibröz agregatlar oluşturur. Hb S içeren eritrositler orak şeklinde görüntü oluştururlar ve kolayca parçalanırlar oraklaşmış eritrositlerin ince kapillerlerde dolaşımı yavaşlatmasıyla tromboz ve emboliler gelişebilir Hb S, orak hücreli anemi ( Hb S hastalığı) olarak tanımlanan hemoglobinopatinin ortaya çıkmasına neden olur

Orak hücreli anemi ( Hb S hastalığı), otozomal resesif kalıtılır; homozigotlarda hemolitik anemi ortaya çıkar. Heterozigot taşıyıcılarda asemptomatiktir Heterozigot orak hücreli anemi hastaları, sıtma paraziti olan plasmodyum falsiparuma karşı dirençlidirler; sıtmaya karşı hassasiyetleri azdır. Bu kişilerde eritrositlerin yaşam süresi normalden kısadır; parazit, eritrosit içindeki gelişimini tamamlayamaz.

Hb C: Hemoglobin C hastalığı olarak bilinen hemoglobinopatinin ortaya çıkmasına neden olur Homozigot hemoglobin C hastalarında, orta derecede kronik hemolitik anemi gözlenir

TALASEMİLER • Globin üretimini kontrol eden genlerde mutasyon ya da delesyon meydana gelir. • Herediter hemolitik hastalıklardır; insanlarda tek gen defektinin görüldüğü en sık rastlanan hastalık grubunu oluştururlar. Talassemilerde, normalde uyum içinde sentezlenen ve zincirlerinden biri sentezlenmez veya azalmış olarak sentezlenir. 0 veya 0, + veya + gibi, defektli globin zinciriyle anılan çeşitli talassemiler tanımlanmıştır • Akdeniz bölgesinde sıktır.

Alfa-TALASEMİ • Alfa globin zincirinin yapılmasından sorumlu olan gen ise 16. Kromozomda bulunur. • Bu gen üzerinde 2 zeta geni, 2 psödoalfa geni ve 2 alfa geni bulunur. • Homolog kromozomların herbirinde iki alfa geni olmak üzere toplam 4 fonksiyonel alfa geni bulunmaktadır. • Alfa talasemilerde tanımlanan moleküler defektler genelde gen delesyonlarıdır.

Alfa-TALASEMİ • Alfa talasemilerde 4 klinik sendrom tanımlanmıştır; • a. Sessiz alfa talasemi taşıyıcılığı (alfa talasemi 2); dört alfa geninden birinde parsiyel veya tama yakın delesyon vardır. Klinik veya hematolojik olarak tamamen normaldirler. • b. Alfa talasemi taşıyıcılığı (alfa talasemi 1); Aynı kromozom üzerinde iki veya farklı kromozom üzerinde birer alfa geninde parsiyel veya tama yakın delesyon vardır. • c. Hb. H Hastalığı; 4 alfa geninden üçünde parsiyel veya tam fonksiyonel bozukluk vardır. Klinik seyirleri genelde hafifitir ve hafif veya orta düzeyde hemolitik anemi ile kendini gösterir. • d. Hidrops fetalis; Dört alfa geninin dördünün de delesyonu sonucu bebekler ya ölü doğar veya doğumdan birkaç saat için kaybedilir.

Beta-TALASEMİ (Akdeniz Anemisi) • Beta globin zincir yapımından sorumlu olan beta gen kümesi 11 no’lu kromozomun kısa kolu üzerindedir. • Beta talasemilerde moleküler defektler beta globin gen ekspresyonundaki basamaklarda olan defektler ve gen delesyonlardır. • Beta talaseminin ağır(major), orta, ve hafif (minor) çeşitleri vardır.

Beta-TALASEMİ • • β 0 talasemi (Talasemi MAJOR) Zincir sentezi hiç yok ağır klinik tablo Tedavi edilemeyen vakalarda , kalp, dalak, karaciğerde büyüme görülür. İleri dönemlerde kemikler kırılgan hale gelir. • Sık aralarla , genç kan hücreleri içeren kan nakilleri yapılması ve hastalığın ciddi formlarında kemik iliği değişimi, tedavi uygulamaları arasında yer almaktadır.

Beta-TALASEMİ • Talasemi Minor (β+ talasemi): Zincir sentezi kısmen var (β++ talasemi): Zincir sentezi hafif azalmış Beta-talaseminin daha hafif bir şekli olan talasemi minör oldukça yaygındır. Bu hastalık demir eksikliği anemisindekine benzeyen kan hücrelerini meydana getirir, fakat hiçbir belirti yoktur.
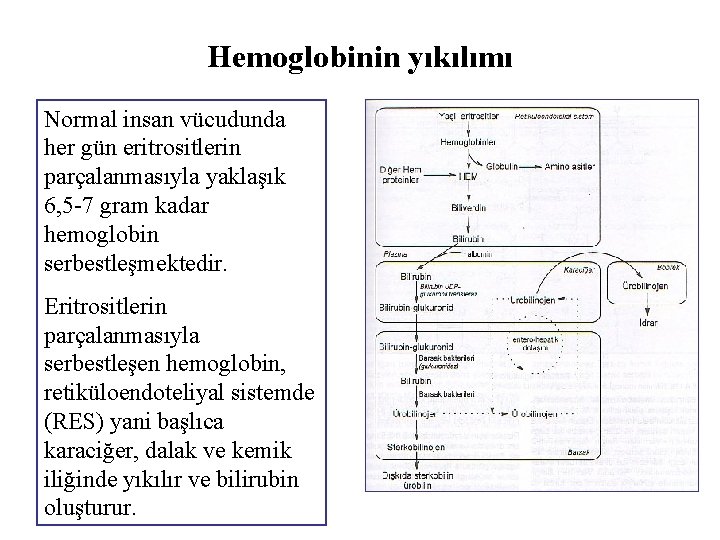
Hemoglobinin yıkılımı Normal insan vücudunda her gün eritrositlerin parçalanmasıyla yaklaşık 6, 5 -7 gram kadar hemoglobin serbestleşmektedir. Eritrositlerin parçalanmasıyla serbestleşen hemoglobin, retiküloendoteliyal sistemde (RES) yani başlıca karaciğer, dalak ve kemik iliğinde yıkılır ve bilirubin oluşturur.
- Slides: 51